Если попадет инфекция при раке
Инфекции — главные причины смерти при раке. Они не только часто встречаются, но нередко имеют более тяжелое течение, чем у других пациентов, менее подверженных действию терапии, и иногда вызываются организмами, которые не патогенны для здоровых людей. Такая восприимчивость является следствием подавления защитных механизмов больного, вызванного опухолью и ее лечением.
Кожа и слизистые оболочки служат барьером для инфекции. Опухолевая инфильтрация и местная лучевая радиотерапия могут привести к повреждению лимфатических или венозных сосудов, что приводит к увеличению восприимчивости к локальной инфекции. Воспроизводство эпителиальных клеток в желудочно-кишечном тракте подавляется химиотерапией, из-за чего повреждается и изъязвляется слизистая, что позволяет организмам из кишечника попасть в систему воротной вены.
Кожа повреждается внутривенными иглами и канюлями, особенно туннельными подкожными каналами. Это частые источники инфекции, которые вызываются такими кожными организмами, как Staphylococcus epidermidis. В носоглоточной полости возникают инфекции, вызванные Candida albicans.
Рак при запущенной стадии иногда связан с ухудшением функций и нейтрофилов, и моноцитов. Было описано подавление хемотаксической, фагоцитарной и бактерицидной активностей.
Ослабленная замедленная гиперчувствительность довольно распространена при запущенной болезни Ходжкина, но менее часта в других случаях злокачественных опухолей. Лимфопения неизменно вызывается действием алкилирующих агентов и массивной радиотерапией. Клеточный иммунитет особенно важен при защите организма хозяина от грибов, вирусов, туберкулеза и простейших.
Интенсивная цитотоксическая химиотерапия ведет к ухудшению образования антител к бактериальным и вирусным антигенам.
Циркулирующие бактерии удаляются фагоцитарными клетками, находящимися в синусах ретикулоэндотелиальной системы, особенно в печени и селезенке. Для этой чистки важны антитела и белки системы комплемента. Спленэкто-мия увеличивает риск серьезной бактериальной инфекции, особенно пневмококковый сепсис в детском возрасте и в меньшей степени во взрослом.
Бактериемия и септицемия у больных раком
Инфекции кровяного русла довольно часты у пациентов с гранулоцитопенией. Патогенами часто являются грамотрицательные бактерии (Escherichia coli, Pseudomonas aeruginosa), стафилококки и стрептококки. Увеличивается частота инфекций, вызванных грамположительными бактериями, особенно Staphylococcus epidermidis. Пациенты с тунельными подкожными каналами особенно подвержены поражениям этим организмом.
Жар у пациента с нейтропенией при раке — показатель присутствия бактерий в крови и под кожей. Если существует очевидный источник инфекции, например инфицированный порт для инфузий, следует взять культуру бактерий и удалить канюлю. Лечение не следует откладываеть для пациента с нейтропенией. Пациенты с лихорадочной нейтропенией с относительно низким риском развития серьезных осложнений относятся к тем, кого лечат короткими циклами химиотерапии для солидных опухолей.
Эти пациенты должны быть госпитализированы. Недавние исследования показали, что пероральный прием амоксициллина-клавуланата комбинированный с пероральным приемом ципрофлоксацина так же эффективен, как и внутривенная химиотерапия в этой группе (70% пациентов). Пациенты с высоким риском (с неконтролируемым раком или на стационарном лечении интенсивной терапией) лечатся внутривенными антибиотиками, в том числе b-лактамом и аминогликозидом или цефтазидимом.
Респираторные инфекции у больных раком
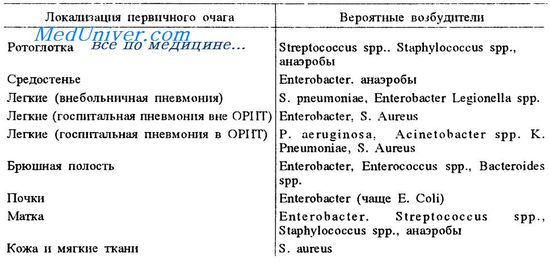
У пациента с серьезным подавлением иммунитета довольно часто возникает жар с легочным инфильтратом. Главные причины этого даны в таблице.
Осложнения в постановке диагноза могут быть значительны, поскольку тесты слюнных и кровеносных культур иногда отрицательны, а более инвазивные процедуры, такие как трансбронхиальная биопсия, невозможны из-за тромбоцитопении или общего состояния пациента.
Существуют некоторые клинические особенности, которые помогают при постановке диагноза. Кавитация наиболее часто сопровождает поражения анаэробными бактериями, стафилококками и микобактериями. Инфекции Pneumocystis вызывают заметную одышку, а на рентгенограмме грудной клетки видны билатеральные инфильтраты, обычно состоящие из хилуса. Болезнь, однако, может протекать вяло и вызвать долевое уплотнение. Цитомегаловирусные инфекции встречаются главным образом у пациентов с серьезным подавлением иммунитета, в частности в течение аллогенной ВМТ. Болезнь может также вызывать миокардит, невропатию или офтальмию.
Легочные инфильтраты обычно билатеральны. Инфекции Candida вызывают широкое разнообразие изменений в рентгенограмме. Инфекции Aspergillus обычно быстро прогрессируют. Тесты культур крови обычно отрицательны, а инфильтраты возможны в одном или двух легких.
При затруднениях в постановке диагноза можно следовать следующей схеме.
У пациентов без нейтропении или тромбоцитопении исследовать посевы крови, слюны, бронхоскопические промывания и трансбронхиальную биопсию там, где это возможно. Если кровяные и слюнные культуры отрицательны, лечить антибиотиками широкого антибактериального спектра действия (обычно в комбинации с аминогликозидом, пенициллином и метронидазолом или аналогичными соединениями). Если возможной причиной инфекции является Pneumocystis, следует давать высокие дозы котримоксазола. Если ответа нет, рассмотрите ацикловир для вируса простого герпеса и противогрибковую терапию с амфотерицином или кетоконазолом. Ацикловир не эффективен против цитомегаловирусов.
Если кровяные или слюнные тесты положительны, лечите соответствующе, но если ответа нет, рассмотрите смешанные инфекции.
Пациентам с нейтропенией или тромбоцитопенией проводят бронхоскопию, но биопсия не всегда возможна, и лечение продолжают без дальнейшего диагностического исследования. До и после бронхоскопии иногда необходимы антибиотики и переливание тромбоцитов.

Инфекции мочевыводящих путей у больных раком
Инфекции часты у пациентов с затрудненным мочеиспусканием. Затруднения могут быть вызваны опухолью или ослаблением мочевого пузыря у пациентов с компрессией спинного мозга и его корешков. Диагноз ставится после исследования уринокультуры, и лечение осуществляется антибиотиками и снятием осложнений, если это возможно.
Желудочно-кишечные инфекции у больных раком
Молочница ротовой полости (инфекция, вызываемая Candida albicans) — частое осложнение химиотерапии. Она особенно распространена у пациентов с подавленным иммунитетом, у пациентов, принимающих стероиды и тех, кого лечат антибиотиками с широким спектром действия. Рот и глотка становятся очень болезненными, а белые пятна грибков видны на эри-темной основе. У плохо питающихся пациентов инфекция может проникать глубже и распространяться по пищеводу, желудку и кишечнику. Обычно эффективен пероральный прием нистатина, амфотерицина или миконазола.
Проявление вируса простого герпеса на губах часто проблематично для пациентов с лейкопенией, и повреждения могут быть довольно обширными. В данном случае необходимо местное применение ацикловира для пациентов с подавленным иммунитетом или систематический прием ацикловира при более серьезных инфекциях.
Инфекции, вызванные Candida в пищеводе, необходимо лечить пероральным приемом суспензии нистатина, но если такое лечение неэффективно, то необходимо применение кетоко-назола или короткий курс амфотерицина. Кишечные инфекции, возникающие при поражении Candida, должны лечиться амфотерицином.
Перианальные инфекции распространены среди пациентов с нейтропенией. Всегда необходимо применять профилактические меры совместно с тщательной гигиеной промежности и смягчителями стула для предотвращения запора и анальных трещин. Распространяющиеся перинеальные (паховые) инфекции могут угрожать жизни пациента, и требуется срочное лечение внутривенными антибиотиками, действующими против грамотрицательных и анаэробных бацилл.
Менингит у больных раком
Инфекции центральной нервной системы (ЦНС) довольно редки, но у пациентов с лимфомой или лейкемией иногда развивается менингит из-за Cryptococcus neoformans. Начало заболевания индивидуально у каждого и сопровождается головной болью. Микроорганизм обнаруживают при окрашивании India ink спинномозговой жидкости (CSF).
Выявление антигенов Cryptococcus в крови и CSF возможно у большинства пациентов. Состояние многих пациентов улучшается при приеме амфотерицина, некоторые вылечиваются.
Кожные инфекции у больных раком
В отличие от инфекции, представленной на портах для вливания, наиболее частое кожное заболевание — опоясывающий лишай (varicella zoster). Возникает из-за реактивации вируса varicella zoster в ганглии дорсального корешка, вызывает кожную пузырчатую сыпь, которая особенно серьезна у людей с подорванным иммунитетом, может распространяться как ветряная оспа и вызывать фатальную пневмонию. Пациентов следует лечить ацикловиром как можно быстрее.

Следует иметь в виду, что инфекции при раке могут играть исключительно отрицательную роль. Заражение происходит, когда вредные бактерии, вирусы, или грибки (такие как дрожжи) вторгаются в организм и иммунная система не в состоянии уничтожить их достаточно быстро. Люди с раком более склонны к развитию инфекций, потому как рак и лечение рака может ослабить вашу иммунную систему.
Иммунная система
Лейкоциты, которые разрушают вредные бактерии, называются нейтрофилы. Состояние организма, при котором фиксируется низкий уровень нейтрофилов, называется нейтропения. Это состояние способствует увеличению риска развития опасных бактериальных инфекций.
Причины ослабления иммунной системы
Сама болезнь рак и лечение рака может вмешиваться в работу иммунной системы несколькими способами:
- Поскольку иммунная система занята борьбой с раком, она становится менее способной одновременно защищать и от других инфекций.
- Недостаток сна, стресс, плохое питание, и другие побочные эффекты рака и лечения рака ослабляют иммунную систему.
- Некоторые химиотерапевтические препараты могут вызвать сбои в работе костного мозга и других частей иммунной системы, снижая выработку белых кровяных телец.
- Лучевая терапия также может повлиять на костный мозг, особенно если облучению подлежат обширные участки тела или же будут облучаться кости в области таза, ног, груди или живота.
- Типы рака, которые влияют непосредственно на костный мозг (в том числе лейкемия или лимфома) или рак, который метастазировал в кости (например, рак молочной железы или рак легких) могут вытеснить нормальные клетки костного мозга и снизить производство белых кровяных телец.
Признаки и симптомы инфицирования
- Лихорадка (температура 38.6С или выше)
- Озноб или потливость
- Боль в горле или язвы во рту
- Боль в животе
- Боль или жжение при мочеиспускании или частое мочеиспускание
- Диарея или язвы вокруг ануса
- Кашель или одышка
- Любое покраснение, отек или боль, особенно вокруг пореза или раны
- Необычные выделения из влагалища и зуд
Лечение инфекций
Если присутствует нейтропения или низкий общий уровень лейкоцитов, врач может принять решение лечить инфекцию лекарствами, такими как филграстим (Neupogen), Pegfilgrastim (Neulasta), или Sargramostim (Leukine или Prokine) для стимуляции организма производить больше нейтрофилов или других видов белых кровяных телец, чтобы уменьшить риск разрастания инфекции. Если все же инфекция возникает, пациенты могут лечиться антибиотиками или противогрибковыми препаратами.
Если развились нейтропения и лихорадка (называется нейтропеническая лихорадка), пациенты могут нуждаться в госпитализации, чтобы получить внутривенно (ВВ) антибиотики. Пациенты с высоким риском развития инфекции из-за наличия нейтропении или потому, что ожидают лечение химиотерапией или лучевой терапией, могут быть обработаны в профилактических целях (превентивных) антибиотиками или противогрибковыми препаратами.

Советы по профилактике инфекций
- Больше отдыхайте и придерживайтесь хорошо сбалансированной диеты.
- Старайтесь избегать людных мест и связей с людьми, которые больны.
- Не делитесь пищей, питьевыми чашками, посудой или другими личными вещами, как, например, зубные щетки. В этом поведении нет ничего зазорного.
- Чаще мойте руки, особенно после посещения туалета или перед едой.
- Душ или ванну принимайте ежедневно, и используйте лосьоны для защиты вашей кожи от сухости и трещин.
- Будьте осторожны при использовании острых предметов, таких как ножницы или нож.
- Не ешьте сырые продукты, в том числе мясо, моллюсков и яйца, и избегайте или тщательно мойте сырые фрукты и овощи.
- Не изменяйте кошачьи туалеты и не выбрасывайте вручную отходы от домашних животных.
- Используйте перчатки для садоводства и по дому, особенно во время уборки.
- Чистите зубы и десны мягкой зубной щеткой и используйте жидкость для полоскания рта, чтобы предотвратить инфекции.
У онкологических пациентов риск сепсиса повышен. Его развитию способствует снижение иммунитета, серьезные хирургические вмешательства. В Европейской клинике есть всё необходимое, чтобы вовремя выявить это осложнение и провести эффективное лечение.
Не совсем так. Между обычной инфекцией и сепсисом есть принципиальная разница.
Инфекция развивается, когда болезнетворные агенты – например, бактерии или вирусы – попадают в организм, повреждают органы. Естественно, наш иммунитет пытается дать чужакам отпор. У человека возникают определенные симптомы. Некоторые инфекции протекают легко, некоторые смертельны. Онкологические больные находятся в группе повышенного риска. Инфекция, которая не опасна для здорового человека, может стать для них фатальной из-за снижения защитных сил организма.
Сепсис – это когда иммунитет реагирует на попавшие в тело микроорганизмы слишком бурно. Он начинает повреждать собственные ткани по всему организму, из-за этого нарушается функция органов, и это опасно для жизни. То есть, помимо инфекции есть еще синдром системного воспалительного ответа. И здесь онкологические больные тоже находятся в группе повышенного риска.
Бактериемия и септицемия у больных раком
Бактериемией называют состояние, когда в крови человека присутствуют бактерии. Ее выявляют с помощью посева крови. Считается, что в норме кровь должна быть стерильна. Впрочем, некоторые исследования показали, что даже в крови здоровых людей могут находиться бактерии, но в целом это не доказано.
Бактериемия может возникать при некоторых инфекциях, например, при брюшном тифе, туляремии, сибирской язве. При пневмонии (воспалении легких) и менингите она уже считается тяжелым осложнением. Если бактерии попали в кровь, и иммунитет слишком бурно начал на них реагировать, развивается септицемия – это синоним сепсиса.
Самая тяжелая форма сепсиса – септический шок. Его диагностируют, когда сильно нарушается работа сердечно-сосудистой системы, ухудшается кровоснабжение всех органов, они перестают получать нужное количество кислорода и справляться со своими функциями. Такие пациенты часто погибают.
Причины возникновения сепсиса у больных раком
Существует несколько причин, из-за которых риск сепсиса у онкологических больных повышен:
- Эти пациенты часто и подолгу находятся в клиниках. Существует такое понятие, как внутрибольничная инфекция: как бы строго персонал больницы ни придерживался правил асептики и антисептики, как бы тщательно ни проводили уборки и ни включали ультрафиолетовые лампы – стопроцентной стерильности достичь невозможно, в медицинском учреждении всегда будут циркулировать микробы. Некоторые из них становятся особенно опасными, потому что постоянно существуют бок о бок с антибиотиками и успевают выработать к ним устойчивость.
- Химиопрепараты атакуют все быстро размножающиеся клетки без разбору: и раковые, и здоровые. Из-за этого могут развиваться осложнения, одно из них – снижение иммунитета.
- Организм многих онкологических больных ослаблен: из-за возраста, злокачественной опухоли и сопутствующих заболеваний, проблем с питанием. Естественно, в такой ситуации снижаются защитные силы организма.
- Для лечения в онкологии часто прибегают к инвазивным процедурам, хирургическим вмешательствам. Когда организм готов неправильно реагировать на инфекцию, сепсис может возникнуть даже из-за укола иглой, не говоря уже, например, о серьезных полостных операциях в брюшной полости.
Вывод: врачи в онкологической клинике должны внимательно наблюдать за состоянием пациентов, знать первые симптомы сепсиса, уметь его диагностировать и своевременно проводить эффективное лечение. Именно так работают в Европейской клинике. У нас есть современные методы диагностики. Например, мы одна из немногих клиник в Москве, где проводится анализ крови на бактериальный эндотоксин.
Причиной сепсиса могут стать самые разные микроорганизмы, как в результате внутрибольничной инфекции, так и заражения вне стен клиники. Согласно некоторым данным, более чем в половине случаев (52,9%) виновниками септицемии становятся грамположительные бактерии, в частности, стафилококки, стрептококки и энтерококки.
На втором месте (41,6%) – грамотрицательные бактерии: кишечные палочки, синегнойные палочки, протеи, клебсиеллы.
Реже встречается сепсис, вызванный грибками (4,1%), обычно кандидами – возбудителями молочницы.
Зачастую анализы показывают, что микроорганизмы, которые поселились в теле пациента, устойчивы ко многим антибиотикам. Поэтому подбор эффективного антибактериального лечения может стать непростой задачей.
Симптомы сепсиса при раке
Сепсис может проявляться разными симптомами, и они бывают выражены в различной степени. Иногда его сложно распознать из-за незначительных проявлений, легко спутать с другими состояниями, такими как инсульт, инфаркт, тромбоэмболия легочной артерии, анафилактический шок. Существуют специальные критерии, которые помогают врачам выявить начинающуюся септицемию и понять, что пациенту требуется обследование, лечение.
Например, если обнаружены два симптома из этого списка, диагностируют синдром системного воспалительного ответа:
- Температура тела менее 36° C или более 38° C.
- Частота сердечных сокращений более 90 ударов в минуту.
- Частота дыхания более 20 в минуту.
- Парциальное давление углекислого газа в крови более 32 мм рт. ст.
- Количество лейкоцитов в крови менее 4 000 или более 12 000 на литр.
Существуют критерии сепсиса по “быстрой” шкале qSOFA. Если есть все три из списка, скорее всего, это сепсис, нужно провести обследование:
- Частота дыхания более 22 в минуту.
- Систолическое (“верхнее”) артериальное давление 100 мм рт. ст. или менее.
- Изменение мышления.
Есть более точная шкала SOFA, она учитывает симптомы и результаты обследования.
В целом, наиболее распространенные симптомы сепсиса: повышение температуры тела, увеличение частоты сердечных сокращений, повышенная потливость, учащенное дыхание. При септическом шоке состояние резко ухудшается, падает артериальное давление, возникает спутанность сознания, ноги, руки и губы становятся холодными, синюшными. Возникают симптомы нарушений функций различных органов. Например, при поражении почек уменьшается суточный объем мочи, легких - развивается одышка, дыхательная недостаточность.
Методы лечения сепсиса при раке
Лечение при сепсисе носит комплексный характер. Основные направления:
- Если есть очаг инфекции - его нужно ликвидировать, например, вскрыть и обработать гнойник.
- Лечение антибиотиками, к которым чувствителен возбудитель (в случае с грибками - противогрибковые препараты).
- Препараты, которые помогают стабилизировать кровообращение: вазопрессоры (сосудосуживающие), инотропные (увеличивающие силу сердечных сокращений).
- Инфузионная терапия - внутривенные вливания растворов через капельницу.
- При необходимости - искусственная вентиляция легких, плазмаферез, переливание компонентов крови.
В Европейской клинике применяется инновационная методика лечения сепсиса - селективная сорбция на картриджах для экстракорпоральной гемоперфузии Toramyxin PMX-20R. Во время этой процедуры, напоминающей плазмаферез, кровь пациента пропускают через специальный фильтр, который очищает ее от эндотоксина. Этот метод помогает эффективно бороться с сепсисом, вызванным грамотрицательной и смешанной флорой.
Прогнозы на выздоровление
Смертность при септицемии составляет от 10 до 40%. Среди пациентов, у которых развился септический шок, она выше. Прогноз главным образом зависит от трех факторов:
- Разновидности и характеристик инфекционного агента.
- Особенностей, физиологии организма пациента.
- От того, насколько правильно и своевременно был установлен диагноз, начато лечение.
В Европейской клинике работает отделение интенсивной терапии, оснащенное всем необходимым оборудованием. У нас есть все возможности для того, чтобы быстро и в полном объеме оказать помощь пациенту в состоянии любой степени тяжести.
Главная > Консультации > Детский врач > Существуют ли инфекции, способные спровоцировать рак? Онкогенные инфекции
В настоящее время доказано, что от 15 до 20% новообразований человека имеют вирусное происхождение.
Вирусами называют мельчайшие организмы, большую часть из которых нереально разглядеть, даже используя обыкновенный микроскоп. Они состоят из небольшого количества ДНК и РНК генов, которые находятся в белковой капсуле. Эти вирусы проникают в живые клетки, где впоследствии начинают размножаться. Бывают также вирусы вызывающие рак, которые могут помещать свою ДНК в клетки, в скором времени спровоцировав появление онкологических заболеваний. Характерной чертой онкогенных вирусов является то, что они могут стимулировать клетки размножаться с необычно высокой скоростью, что может привести к повреждению генетического материала в этих клетках. Дополнительные факторы, такие как курение или воздействие определенных канцерогенов, могут вызывать окончательное превращение нормальных клеток в раковые. Эти воздействия (дополнительные факторы), наряду с индивидуальными генетическими особенностями каждого человека, могут объяснить, почему у некоторых людей с онкогенными инфекциями развивается рак, а у других нет.
К онковирусам относятся инфекции, которые провоцируют появление раковых заболеваний, а также вирусы, которые способствуют развитию воспалительных процессов, носящих хронический характер.
По заключению экспертов Международного Агентства по Изучению Рака (МАИР) прямым канцерогенным действием на человека обладают следующие вирусы:
- вирусы гепатита В и С, вызывающие рак печени;
- определенные типы папилломавирусов человека, являющиеся причинным агентом рака шейки матки, некоторых опухолей ано-генитальной области и других локализаций;
- вирус Эпштейна-Барр, принимающий участие в возникновении целого ряда злокачественных новообразований;
- герпесвирус человека 8-го типа, играющий важную роль в возникновении саркомы Капоши, первичной выпотной лимфомы, болезни Кастлемана и некоторых других патологических состояний;
- вирус Т-клеточного лейкоза человека, являющийся этиологическим агентом Т-клеточного лейкоза взрослых, перHIVной выпотной лимфомы (Primary Effusion Lymphoma, PEL), а также тропического спастического парапареза (TSP) и ряда других неонкологических заболеваний;
- вирус иммунодефицита человека (ВИЧ), не обладающий трансформирующими генами, но создающего необходимые условия (иммунодефицит) для возникновения рака.
Все они включены в санитарные правила и нуждаются в кратких комментариях.
В настоящее время существует глобальная эпидемия вируса гепатита В (HBV): на планете инфицировано этим вирусом более 350 млн. человек. Каждый год от инфекции HВV умирает 2 млн. человек, из них более 300 тыс. от рака печени. Вирусом гепатита С в мире инфицировано более 170 млн. человек, и их число ежегодно увеличивается на 3–4 млн. По данным экспертов, вирус гепатита С ежегодно становится причиной смерти 250–350 тыс. человек от цирроза, печеночной недостаточности и гепатоцеллюлярной карциномы. Из общего числа случаев рака печени (гепатокарцином) более половины связано с инфицированием HBV, четверть — с инфицированием HCV и 22% случаев — с другими причинами.
Инфицированность населения HBV колеблется от низкой, не превышающей 2% в США и странах Западной Европы, до высокой в странах Африки и Юго-Восточной Азии, приближающейся к 10%. Россия по уровню инфицированности населения HBV занимает промежуточное положение. В окружающих Россию странах (Средняя Азия, Закавказье, Молдавия) инфицированность населения по данным ВОЗ достигает 8%.
Пути заражения вирусом гепатита В (HBV): перинатальный (от матери к плоду), парентеральный (главным образом с кровью или другими биологическим жидкостями больного человека, попадающими непосредственно в кровь инфицируемого, особенно при употреблении инъекционных наркотиков) и половым путем. Заразиться можно в местах, где собираются лица, употребляющие инъекционные наркотики, в салонах пирсинга и татуажа, парикмахерских (маникюр, педикюр — при совместном пользовании общими бритвами и маникюрными принадлежностями). Половой контакт с партнером носителем инфекции в 30% случаев заканчивается инфицированием партнера. Велика вероятность заразиться вирусом, если человек имеет много половых партнеров. У инфицированной HBV матери может родиться инфицированный ребенок. Заражение происходит при родах или нарушении целостности плаценты в ходе беременности. Вирус гепатита B обнаруживается в слюне, слезах, моче и кале инфицированных лиц. Риск заражения, хотя и незначительный, существует при попадании их на поврежденную кожу и слизистые оболочки другого человека. С пищей, при разговоре, т. е. контактно-бытовым путем гепатит В не передается.
Пути заражения вируса гепатита С (HCV): в основном такие же как при HBV. Половой путь передачи гепатита С мало актуален (не более 3–5%), однако значение его возрастает при наличии большого количества партнеров, случайных связей. От инфицированной матери плоду вирус гепатита С передается редко, не более, чем в 5% случаев и только в процессе родов при прохождении родовых путей. Не отмечена передача вируса с молоком матери и контактно-бытовым путем.
Профилактика. Исходя из вирусной природы указанных заболеваний, вакцинация является наиболее эффективным способом предотвращения распространения инфекции, возникновения острого и хронического гепатита, а, следовательно, и рака печени. В 1980 г. приготовлена вакцина против вируса гепатита В. Согласно рекомендациям, принятым в 1999 г. в США и практикуемым в России, вакцина рекомендована для лиц от 0 до 19 лет. В настоящее время во многих странах мира, включая Россию, введена обязательная вакцинация против гепатита В (HBV) среди новорожденных, детей раннего возраста, подростков и лиц из групп риска. С целью профилактики распространения HBV и рака печени проводится тестирование всех беременных и доноров крови на поверхностный антиген вируса (HbsAg) и антитела к нему (HBs).
Вирусы папилломы человека (HPV) принадлежат к группе Papillomavirus и являются вирусами, которые поражают клетки эпителия эктодермального происхождения (кожа, слизистые половых органов, ротовой полости).
В настоящее время известно более 100 типов HPV, которые могут вызывать бородавки на различных частях тела, но лишь немногие из них связывают с различными злокачественными новообразованиями. Некоторые штаммы вируса папилломы распространяются половым путем и вызывают остроконечные бородавки. Передаваемые половым путем вирусы папилломы связаны с развитием рака шейки матки, полового члена и анального прохода (последние встречаются не так часто). К группе высокого онкогенного риска относят наиболее распространенные в Европе и в России 16-й и 18-й типы вируса (HPV 16 и HPV 18), а также менее распространенные 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типы, ответственные, соответственно, за возникновение 65–75% и 18–20% случаев рака шейки матки (РШМ). Раннее обнаружение и лечение может уменьшить риск рака шейки матки, поэтому врачи советуют женщинам с выявленными вирусами папиломы периодически проводить тест мазок Папаниколау. Вирус папилломы человека является довольно распространенными венерическим заболеваниям с несколькими миллионами новых случаев инфицирования, диагностируемых каждый год.
Пути заражения. Передача инфекции осуществляется половым путем, возможны перинатальный (от матери к плоду) и оральный пути заражения. Большинство лиц обоего пола инфицируется вирусом в первые годы половой жизни. В последние 20–30 лет уровень инфицированности существенно возрос. У 90% женщин HPV инфекция протекает без явных клинических проявлений и вирус исчезает самостоятельно через год после инфицирования под влиянием иммунной системы организма. В трети случаев вирусную ДНК можно выявить более чем через год и в 10% — более чем через два года. Инфекция данным вирусом очень распространена среди здоровых женщин. К 50-летнему возрасту ею переболевает 8 женщин из 10.
Факторами риска для развития рака шейки матки служат раннее начало половой жизни, частая смена партнеров, сопутствующие урогенитальные инфекции (например, хламидийная или герпетическая), снижение клеточного иммунитета, гормональные воздействия (аборт, беременность, прием гормональных контрацептивов и др.), курение, неправильное питание (дефицит фолиевой кислоты), а также индивидуальные генетические особенности.
Вирус Эпштейн-Барра широко известен как вирус, который вызывает инфекционный мононуклеоз. Вирусом Эпштейн-Барра инфицировано практически всё население планеты. В развивающихся странах почти у каждого ребенка к пятилетнему возрасту выявляются антитела к этому вирусу. В развитых странах инфицированность несколько меньше: в США антитела выявляются у 50% выпускников средних школ, к сорока годам антитела к этому вирусу появляются у 90% населения. 15–25% взрослых являются выделителями вируса.
Данный вирус передается через контакт с жидкостью полости рта и носа инфицированного человека. Дети редко имеют выраженные симптомы вируса Эпштейн-Барра, но даже если они есть, симптомы, как правило, являются такими же, как при широко распространенных вирусных инфекциях. Вирус Эпштейн-Барра после заражения остается в организме, главным образом в лимфоцитах, всю остальную части жизни человека. Он находится в состоянии покоя в течение большей части времени, иногда проявляя себя, но не причиняя никакого реального вреда. При ослаблении организма и снижении защитных сил иммунной системы — вирус может активироваться и вызывать более агрессивные воздействия. Вирус Эпштейн-Барра ассоциируется, в первую очередь с развитием лимфобластомы, болезни Ходжкина, лимфомы носоглотки и лимфомы Беркитта, редкой формой рака, возникающего в лимфатических узлах. Кроме лимфобластомы, следует назвать такие вызываемые вирусом доброкачественные и злокачественные новообразования, как волосатоклеточная лейкоплакия полости рта, рак носоглотки и др., возникающие на фоне иммунодефицита организма различного происхождения.
Пути заражения. Основной путь передачи вируса — воздушно-капельный, но наиболее часто передача вируса происходит при непосредственных контактах слизистой рта (поцелуях). Заражение возможно и через содержащие вирус пищевые продукты, а также бытовым путём через руки и предметы обихода, при переливании крови и других парентеральных вмешательствах. Зафиксирован также половой путь передачи.
Ко-факторы. Поскольку у большинства лиц, инфицированных EBV, какой-либо патологии не возникает, то для ее появления, включая злокачественные новообразования, очевидно, необходимо воздействие на организм дополнительных факторов. Среди известных следует назвать паразитарные инфекции типа малярии; массивную инфекцию EBV в. раннем детском возрасте; ослабление иммунной системы; хроническое недоедание, а также использование в пищу продуктов, обладающих коканцерогенным действием; влияние любых факторов, вызывающих хромосомные мутации. Таким образом, можно сделать вывод, что инфицирование EBV является важным, но недостаточным условием для возникновения ассоциированных с ним онкологических заболеваний, чтобы возникла опухоль, необходимо действие ряда дополнительных факторов.
Открытый в 1994 г. герпесвирус саркомы Капоши в семействе герпесвирусов обозначен под номером 8 (HHV-8). В настоящее время считается доказанной его этиологическая роль в возникновении довольно редко встречающихся заболеваний, а именно саркомы Капоши (СК), выпотной В-клеточной лимфомы полостей тела (PEL) и болезни Кастлемана.
Распространенность HHV-8. Инфицированность населения HHV-8 в различных географических регионах существенно отличается и варьирует от долей процента в США и большинстве стран Западной Европы до 8–10% в странах Средиземноморья (Греция, Италия). Самый высокий процент серопозитивных лиц обнаружен в странах Восточной, Центральной и Западной Африки — странах, эндемичных для СК, где уровень инфицированности населения этим вирусом достигал 50–70%. В России уровень инфицированности HHV-8 среди доноров крови находится в пределах 4%.
Пути заражения. Основной путь передачи HHV-8 — половой, но также со слюной (при поцелуе), и с кровью (редко).
Профилактика. Учитывая половой путь передачи вируса основной профилактической мерой является практика безопасного секса, лечение хронического уропростатита у больных с выявленным HHV-8 в эякуляте и/или секрете предстательной железы, применение противовирусных препаратов в группах риска (больные, нуждающиеся в трансплантации органов и ВИЧ-инфицированные).
Профилактическая анти-вирусная (противоопухолевая) вакцина не создана, над ее изготовлением ведется работа.
Вирус Т-клеточного лейкоза человека (HTLV-1) — это онкогенный ретровирус, являющийся этиологическим фактором Т-клеточного лейкоза/лимфомы взрослых, протекающей чрезвычайно агрессивно со средней продолжительностью жизни около 6 месяцев, и нейро-дегенеративного заболевания под названием HTLV-1-ассоциированная миелопатия или тропического спастического парапареза. В регионах с высокой инфицированностью данным вирусом диагностируются также ассоциированные с вирусом увеиты, артриты, базедова болезнь, инсулинзависимый диабет, синдром Цезаря и др.
Распространенность. Спорадические случаи HTLV-1 инфекции встречаются во многих странах мира, включая Россию. Эндемичными же для этой инфекции являются некоторые регионы Японии, Южной Америки, Африки и часть стран Карибского бассейна.
Пути заражения. Существуют 3 основных пути передачи инфекции от инфицированных лиц: а) с молоком матери; б) при половом контакте главным образом через сперму; и в) с переливаемой кровью при гемотрансфузиях.
Ко-факторы. У большинства лиц, инфицированных HTLV-1, какой-либо патологии не возникает. После заражения вирусом ATL регистрируют не более чем у 1–5% вирусоносителей даже в эндемических для этого заболевания регионах и после длительного латентного периода, длящегося порой десятилетиями. Факторами, способствующими развитию ATL, являются паразитарные инфекции типа эписторхоза, использование иммунодепрессантов любого происхождения, ВИЧ-инфекция и др.
Профилактика. Для профилактики инфекции рекомендованы: отмена кормления грудным молоком младенцев инфицированными матерями; предохраняемый секс и контроль на присутствие HTLV-1 донорской крови не только в регионах с высоким уровнем распространения HTLV-1 среди населения, но и в других, т. к. переливание инфицированной вирусом крови, может способствовать его распространению и появлению заболеваний, связанных с HTLV-1 там, где они сейчас отсутствуют.
Этот вирус был открыт в 1983 г. и его ассоциация с синдромом приобретенного иммунодефицита (СПИД) доказана в 1984 г. Как уже упоминалось ранее, ВИЧ не обладает трансформирующим геном (онкогеном). Инфицированные им клетки (главным образом СD4+ Т-клетки и макрофаги) не подвергаются усиленной пролиферации (делению), а разрушаются, вызывая у инфицированного лица нарастающую степень иммунодефицита, и создавая тем самым условия, необходимые для возникновения опухоли. Доказано, что у больных СПИД`ом примерно 50% новообразований ассоциировано с Эпштейн-Барр вирусом или герпес вирусом саркомы Капоши (HHV-8). Чаще всего у таких больных диагностируют саркому Капоши либо одну из разновидностей не-ходжкинских лимфом. Характеристика этих новообразований, механизмы канцерогенеза, а также методы профилактики и лечения даны в предыдущих разделах, их можно найти также в многочисленных отечественных и зарубежных публикациях.
Несмотря на различную организацию онкогенных вирусов человека, неодинаковый спектр их клеток-мишеней, они обладают рядом общих биологических свойств, а именно:
- вирусы лишь инициируют патологический процесс, усиливая пролиферацию (разрастание ткани организма путём размножения клеток делением) и генетическую нестабильность инфицированных ими клеток;
- у инфицированных онкогенными вирусами лиц возникновение опухоли, как правило, событие нечастое: один случай новообразования возникает среди сотен, иногда тысяч инфицированных;
- продолжительность латентного периода от инфицирования до возникновения опухоли составляет иногда десятилетия;
- у большинства инфицированных лиц возникновение опухоли не является обязательным, но они могут составить группу риска, с более высокой возможностью ее возникновения;
- для злокачественной трансформации инфицированных клеток в организме человека необходимы дополнительные факторы и условия, приводящие к возникновению опухоли.
Профилактика активации вирусов и развития рака
- отказ от курения;
- коррекция питания и образа жизни;
- сокращение воздействия канцерогенных веществ;
- повышение защитной функции организма;
- определение и терапия заболеваний, находящихся в предраковой стадии;
- наблюдение групп высокого риска появления онкологий;
- диагностика рака на ранних стадиях.
Можно ли заразиться раком от больного человека, либо от носителя вируса?
То, что окружающие в безопасности рядом с онкобольными людьми, уже неоднократно доказано и подтверждено проведенными опытами. В 19 веке французским хирургом был выделен экстракт рака молочной железы. Затем он ввел его себе, и еще нескольким людям, участвовавшим в опыте добровольно, этот экстракт под кожу. В месте, куда была проведена инъекция, начались острые воспалительные процессы, которые прошли спустя несколько дней. Опыт в скором времени был проведен еще раз и результаты оказались те же.
Современные ученые также проводили исследования, которые подтвердили, что заразиться раком от другого человека невозможно. Медицинские работники провели анализ 350 тысяч процедур переливания крови, проводимые в течение 35 лет. У трех процентов доноров был обнаружен рак, однако ни один из людей, которым переливали кровь онкобольных, не был заражен.
Еще один важный вывод после проведенных медицинских исследований — генетика на появление раковых образований влияет гораздо больше, чем вирусы и другие факторы. Это значит, что попавший в организм онковирус имеет в развитии рака практически нулевую значимость, тогда как сбой в генетическом коде — ключевую.
Выводы
Вирусы, вызывающие рак — очень опасны для жизни и здоровья человека. Их профилактика и своевременная диагностика поможет максимально снизить риск появления серьезных последствий. При появлении каких-либо признаков вирусной инфекции необходимо срочно обратиться к компетентному специалисту и сдать анализы, которые помогут их выявить и вовремя принять необходимые меры.
Читайте также:

