Эндометрия матки при раке молочной железы

Красильников Сергей Эдуардович, доктор медицинских наук, профессор ГБУЗ НСО Новосибирский областной клинический онкологический диспансер
Гуляева Людмила Федоровна, доктор биологических наук, профессор Заведующая лабораторией ММК ГУ НИИ Молекулярной биологии и биофизики СО РАМН
Бабаянц Екатерина Владимировна, кандидат медицинских наук ГБУЗ НСО Новосибирский областной клинический онкологический диспансер Лаборатория ММК ГУ НИИ Молекулярной биологии и биофизики СО РАМН
Кедрова Анна Генриховна, доктор медицинских наук, профессор ФГБОУ ДПО Институт повышения квалификации Федерального медико-биологического агентства России, кафедра акушерства и гинекологии
Первое место в структуре онкологической заболеваемости и смертности женщин России в последние десятилетия занимает рак молочной железы (РМЖ), имеющий тенденцию к росту заболеваемости и смертности [7].
Число новых случаев рака молочной железы, ежегодно выявляемых в разных странах мира, в настоящее время превысило 1 млн. и составляет 10% от всех злокачественных опухолей различных локализаций.
В России в 2012 г. зарегистрировано 45 000 новых случаев и 22 000 женщин умерло от этого заболевания. При этом заболеваемость увеличивается ежегодно на 1-2% [7].
Рак молочной железы - одна из самых частых причин смерти женщин по сравнению с другими злокачественными опухолями. Каждый год во всех странах от РМЖ умирает 0,37 млн. женщин [7].
В Новосибирской области в 2013 году впервые выявлено 1324 больных раком молочной железы (11,7% от всех злокачественных новообразований в НСО). В Новосибирской области отмечается следующее распределение рака молочной железы по стадиям онкологического процесса: I стадия – 26%, II стадия – 46,5%, III стадия – 20,8 %, IV стадия – 6,7% пациенток. Свыше 5 лет на учете с диагнозом РМЖ состоят 7051 пациенток (59,7%). Умерло в 2013 году – 383 женщины, что составляет 8,4% от всех умерших от ЗНО в НСО.
В плане комплексного лечения больных раком молочной железы применяется тамоксифен. В литературе нет однозначных данных о так называемой тамоксифен-индуцированной гиперплазии эндометрия. Поэтому целью нашего исследования было: 1) Изучить встречаемость гиперпластических процессов эндометрия у больных раком молочной железы. 2) Оценить методы лечения гиперплазии эндометрия у больных раком молочной железы.
Гиперплазию эндометрия по-прежнему считают основой для формирования злокачественной трансформации слизистой тела матки [8]. Однако наиболее высокая онкологическая настороженность отмечается при атипической гиперплазии (АГ) слизистой. По данным разных авторов, частота перехода этой гиперплазии в рак эндометрия варьирует в пределах 10–40% и определяется ее морфологическими особенностями, длительностью рецидивирования заболевания, возрастом пациенток и наличием сопутствующих эндокринопатий [19].
В настоящее время отмечается рост гиперпластических процессов эндометрия после комплексного лечения рака молочной железы, в частности за счет применения антиэстрогенов и ингибиторов ароматазы. Гиперпластические процессы эндометрия составляют разнообразную группу, в большинстве связанную с гормональными нарушениями [2,6]. Цель лечения ГПЭ ― профилактика рака эндометрия и купирование клинических проявлений патологических изменений эндометрия (менометроррагий у пациенток репродуктивного и пременопаузального возраста) [5].
Лечение гиперпластических процессов эндометрия остаётся одной из важных проблем гинекологии. Лечебная тактика при ГПЭ зависит от патоморфологической характеристики эндометрия, возраста пациентки, этиологии и патогенеза заболевания, сопутствующей гинекологической и экстрагенитальной патологии. Терапия в различные возрастные периоды складывается из остановки кровотечения, восстановления менструальной функции в репродуктивном периоде или стойкой постменопаузы в более старшем возрасте и профилактики рецидива гиперпластического процесса [4].
Традиционно развитие гиперпластических процессов эндометрия ассоциировано с гиперэстрогенемией. Одной из функций поступающих из крови и синтезированных in situ (при участии ароматазы и стероидсульфатазы) эстрогенов является стимуляция пролиферации эндометрия. Этот эффект зависит от наличия ER. Кроме того, эстрогены могут метаболизироваться непосредственно в эндометрии при участии 2- и 4-эстрогенгидроксилаз, превращаясь в катехолэстрогены. Эстрогены ткаже могут подвергаться гидроксилированию в 16-м положении. Дальнейший метаболизм катехолэстрогенов протекает с участием КОМТ и ГТ с образованием неактивных и немутагенных производных. При недостаточной активности этих трансфераз возможны 2 варианта событий. Первый заключается в том, что пролиферативный эффект эстрогенов усиливается катехолэстрогенами и 16-гидроксиметаболитами. Во втором варианте под действием пероксидаз катехолэстрогены првращаются в орто-хиноны, которые обладают генотоксическим эффектом и могут вызывать онкогенные мутации [1,3,9,13].
Материал и методика:
В онкологическом отделении №4 ГБУЗ НСО Новосибирский областной клинический онкологический диспансер за период 2011-2014 г. пролечено 237 женщин с гиперпластическими процессами эндометрия. Из них с диагнозом рак молочной железы и гиперплазия эндометрия – 36 пациенток (15,1%). Средний возраст пациенток в этой группе составил 51,6 лет (от 36 до 68 лет). Всем пациенткам предварительно назначено УЗИ органов малого таза и для исключения РЭ (согласно рекомендациям ВОЗ) выполнена гистероскопия с раздельным диагностическим выскабливанием цервикального канала и стенок полости матки. Диагноз гиперплазии эндометрия установлен гистологическим исследованием.
При сочетании рака молочной железы и гиперплазии эндометрия выявлены следующие гистологические типы: простая железисто-кистозная гиперплазия эндометрия – у 24 (66,3%), сложная железисто-кистозная гиперплазия эндометрия – у 8 (22,6%), атипическая железисто-кистозная гиперплазия
Согласно международным стандартам использовались следующие схемы (приведены ниже) лечения гиперпластических процессов эндометрия
и атипической гиперплазии эндометрия (в репродуктивном, пред -, и климактерическом периодах):
При сочетании рака молочной железы, сложной и атипической железисто-кистозной гиперплазии эндометрия (33%) нами выполнено хирургическое лечение в объеме экстирпации матки с придатками.
1. Берштейн Л.М., Ковалевский А.Ю., Ларионов А.А. Ароматаза в нормальном и малигнизированном эндометрии // Акушерство и гинекология. 2001. №4. С.9–11.
2. Вейн А.М., Воскресенская Т.Г. Гипоталамический синдром // Врач. 2000. №4. С. 12-14.
3. Коломиец Л.А., Чернышева А.Л., Крицкая Н.Г., Бочкарева Н.В. Клинико-морфо-биохимические аспекты гиперпластических процессов и рака эндометрия // Томск: Изд-во НТЛ, 2003. 116 с.
4. Кулаков В.И., Савельева Г.М., Манухин И.Б. Гинекология. Национальное руководство // М.: 2010. С. 1088.
5. Моцкобили Т.А. Возможности сонографии и гистероскопии в диагностике патологических процессов эндометрия у больных раком молочной железы на фоне длительной антиэстрогенной терапии: автореф. дисс. … к.м.н. Москва, 2003.
6. Чепик О.Ф. Морфогенез гиперпластических процессов эндометрия // Практическая онкология. 2004. Т. 5. №1.С.9–15.
8. Шахламова М.Н., Бахтияров К.Р. Вопросы гинекологии, акушерства и перинатологии. 2005, Т.4, С. 2-11.
9. Cavalieri E.L., Rogan E.C., Chakravarti D. Initiation of cancer and other diseases by catechol orthoquinones: a unifying mechanism // Cell. Mol. Life Sci. 2002. Vol. 59. P. 665-681.
13. Hu R, Hilakivi-Clarke L, Clarke R. Molecular mechanisms of tamoxifen-associated endometrial cancer. // Oncol Lett. 2015. Apr; 9(4). Р.1495-1501.
15. Love CDB, Muir BB, Scrimgeour JB: Investigation of endometrial abnormalities in asymptomatic women treated with tamoxifen and an evaluation of the role of endometrial screening // Journal of Clinical Oncology. 1999. №17. Р. 2050-2054.
16. McGonigl KF, Marx HF, Morgan RJ : Uterine effects of tamoxifen: a prospective study. // Gynecological Oncology .1999.74. Р. 324(abstract 33)
17. Neyen P., De Muylder X., Van Belle Y., Campo R., Vanderick G: Tamoxifen and the uterus // BMJ 1994. 309. Р. 1313-4.
19. Sivridis E., Giatromanolaki A: Endometrial adenocarcinoma: an apostasy from early views. // Gynecol Oncol 2004. 95(3). Р. 772–3.
Чекалова М.А., Махова Е.Е., Шабанов М.А.,
Брюзгин В.В., Колпакова М.Н.,
ГУ РОНЦ им.Н.Н.Блохина РАМН, г.Москва
Материалы и методы:
За период с 2001 по 2006 гг. в поликлинике РОНЦ им. Н.Н.Блохина РАМН обследовано 4000 больных РМЖ. Из них 49% - первично обратившихся, 51% находящихся под наблюдением длительностью от 6 месяцев до 10 лет. Средний возраст пациенток составил 52,8 ± 1,7 года, практически половина из них была в возрасте от 40 до 63 лет, в состоянии постменопаузы находились более 50% женщин.
У большинства пациенток установлена I-II стадия заболевания (17,8% и 53%соответственно), в 28,5% наблюдений III-IVстадия.
Морфологическая верификация диагноза РМЖ получена в 100% наблюдений. В числе гистологических вариантов преобладал инфильтративный протоковый РМЖ (62,5%); на долю инфильтративного долькового рака пришлось 25%; в 4,1% диагностирован тубулярный рак; в 4,1 % - крупноальвеолярный и медуллярный. 44% опухолей молочной железы содержали рецепторы прогестерона, а 56%-рецепторы эстрогенов.
Первично-множественные новообразования были диагностированы у 21,9% женщин, при этом: метахронные у 5,6%, синхронные у 1,8%. В 10,7% - опухоли гениталий (рак шейки матки, маточной трубы, яичников, эндометрия), в 11,2% наблюдений помимо РМЖ были выявлены злокачественные опухоли других локализаций и лимфопролиферативные заболевания.
83 % пациенток получали первичное лечение в РОНЦ, 17% - по месту жительства. Комплексное лечение проведено 23% больным, комбинированное – 42,3%, оперативное –34,6%. 54,5% больных получали лечение антиэстрогенными препаратами (тамоксифен) или ингибиторами ароматазы (аримидекс, фемара).
В 23% наблюдений была произведена надвлагалищная ампутация матки с придатками, в 14,1% - экстирпация матки с придатками; у 11% - овариэктомия, 17% имели в анамнезе операцию по поводу заболеваний гениталий.
В обследование женщин, как правило, было включено несколько органов: щитовидная железа, молочные железы с регионарными областями, область послеоперационного рубца, печень, внутренние гениталии. В настоящей работе нами проанализированы данные ультразвуковой томографии (УЗТ) внутренних гениталий, которые были сопоставлены с результатами цитологического исследования эндометриальных аспиратов, гистологического исследования материала, полученного при выскабливании полости матки или другой операции.
Результаты:
Наибольшую часть наших наблюдений составили пациентки, находящиеся под мониторингом после первичного лечения в РОНЦ. Самой распространенной патологией среди них были доброкачественные процессы внутренних гениталий:
- множественная миома матки (24,6%),
- аденомиоз (15%)
- сочетание миомы матки и аденомиоза (20,4%)
- киста яичника (9,7%)
- хронический сальпингоофорит (19,3%)
- гиперплазия эндометрия (16,5%)
- полип эндометрия (6,3%).
Вместе с тем, у 10,7% больных комплексное обследование позволило выявить злокачественную патологию:
- Рак яичников(3,1%)
- Рак шейки матки(2,3%)
- Рак маточной трубы(1,2%)
- Рак эндометрия(2,8%)
- Саркома матки(1,3%)
В большинстве наблюдений это были метахронные опухоли, при этом интервал от лечения РМЖ до диагностики второй опухоли составил от двух до девяти лет. Приоритетное значение на первом этапе выявления этих новообразований, за исключением рака шейки матки, имела эхография. Нами была отмечена некая особенность: немалую долю составили неоплазии I –II стадии заболевания. Объяснением этому, возможно, могут служить лишь субъективные факторы, такие как: повышенная онкологическая настороженность пациенток после перенесенного ранее лечения, а также проводимый врачами активный мониторинг. Приведем клиническое наблюдение.
Больная Ю., 53 лет. Из анамнеза: за два года до обращения в онкоцентр получила комбинированное лечение по поводу РМЖ по месту жительства. Там же была обследована в связи с появившимися кровянистыми выделениями на фоне постменопаузы. При ультразвуковом исследовании внутренних гениталий было обнаружено утолщение срединных маточных структур до 12мм, что указывало на наличие гиперпластических изменений в эндометрии (рис.1).
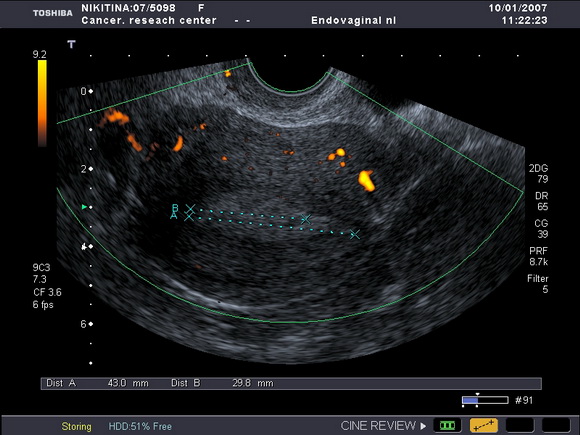
Рис.1
Ультразвуковая томограмма матки, выполненная в поперечной плоскости.
Определяется утолщение эндометрия (рак эндометрия-с учетом гистологического заключения)
В результате гистологического исследования материала, полученного при выскабливании полости матки, выявили умереннодиференцированную аденокарциному. При обследовании в РОНЦ (после раздельного диагностического выскабливания (РДВ)) по данным ультразвуковой томографии: матка не увеличена, с единичным интерстициальным миоматозным узлом диаметром 10мм, типичной структуры, эндометрий не утолщен – 2мм, контур полости матки не деформирован; структура левого яичника изменена – кистозно-солидное образование размерами 56х45мм, правый яичник не изменен, структура его соответствует возрастным нормам. Заключение: подозрение на опухоль яичника (нельзя исключить метастатическое поражение) (рис.2).
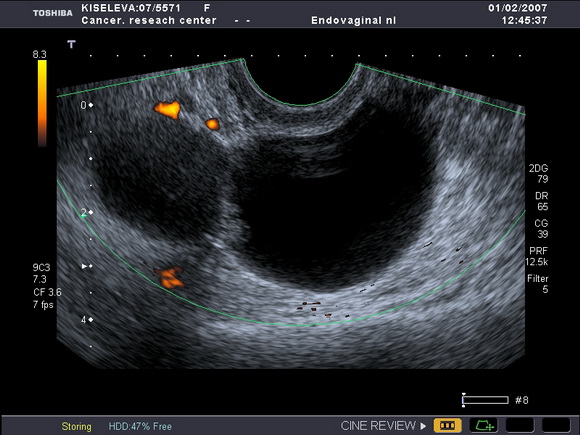
Рис.2
Ультразвуковая томограмма яичника, выполненная в продольной плоскости. Определяется опухоль яичника
В отделении онкогинекологии РОНЦ больной произведена экстирпация матки с придатками, резекция большого сальника.
Диагноз при выписке из РОНЦ: рак молочной железы T 1 N 0 M 0 ; рак эндометрия T 1а N 0 M 0 ; рак яичников T 1а N 0 M 0 .
Приведенный клинический пример убедительно показывает важность активного наблюдения за больными РМЖ с использованием вполне доступных широкому кругу населения диагностических тестов. Подобного рода мониторинг позволяет выявить злокачественную опухоль на ранней стадии, когда прогноз заболевания значительно лучше.
Особого внимания заслуживают вопросы, касающиеся диагностики рака эндометрия.
Применение клинического, цитологического и эхографического исследования позволило нам в 2,8% наблюдений выявить РЭ, причем диагностирован он был через два – три года после РМЖ. Короткий интервал между клиническим проявлением РМЖ (первая опухоль) и РЭ позволяет предположить, что ко времени обнаружения первой опухоли нередко синхронно существует вторая, уже доступная для углубленной диагностики.
Такой короткий интервал между проявлением двух гормонозависимых опухолей вполне может служить подтверждением общности их патогенеза [2] . УЗ – томография не выявила каких – либо индивидуальных особенностей в указанной группе больных, за исключением ранних стадий, для которых характерно диффузное равномерное увеличение толщины эндометрия (ТЭ) до 1,2 – 2,2см (особенно на фоне постменопаузы) (рис.3).
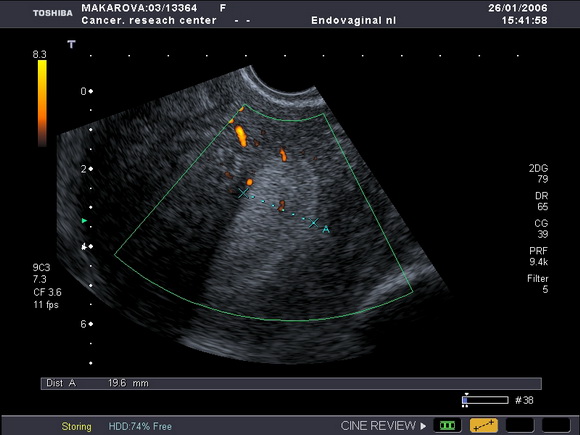
Рис.3
Ультразвуковая томограмма матки, выполненная в продольной плоскости.
Определяется диффузное равномерное увеличение толщины эндометрия
В одном наблюдении визуализировался полип (рис.4) в полости матки на фоне атрофичного эндометрия, а при гистологическом исследовании его были обнаружены фокусы аденокарциномы.
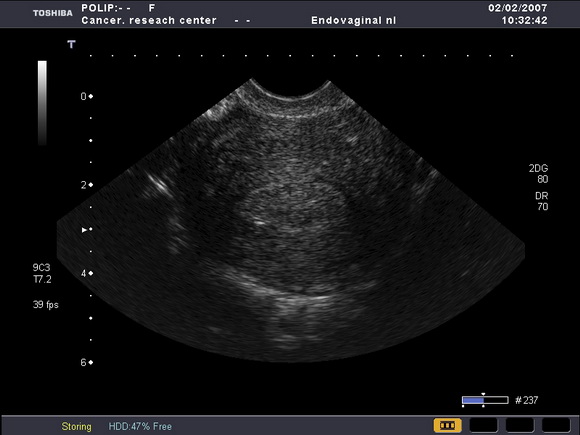
Рис.4
УЗ-томогамма матки, выполненная в поперечной плоскости.
Определяется полип эндометрия чение толщины эндометрия
На имевшемся в нашем распоряжении материале не обнаружено достоверного повышения частоты РЭ под влиянием тамоксифена у больных РМЖ. В то же время выявлено пролиферативное влияние на эндометрий у больных РМЖ.
Трудности, возникающие при интерпретации ультразвуковых данных, полученных при обследовании женщин, принимающих тамоксифен, до сих пор нередко являются предметом дискуссий специалистов.
Дешевым, доступным методом скрининга патологии эндометрия в данном случае является ультразвуковое исследование (УЗИ) органов малого таза влагалищным датчиком.
Среди изменений со стороны эндометрия под влиянием тамоксифена чаще всего встречается гиперплазия эндометрия, диагностируемая только по данным УЗТ, при этом никакой патологии со стороны эндометрия при гистологическом исследовании не обнаруживается.
В нашем исследовании признаки гиперплазии эндометрия визуализировались в 56% наблюдений, при этом большая часть из их пришлась на долю ложноположительных заключений. Так называемая ложноположительная гиперплазия эндометрия встречалась почти у каждой третьей женщины (31,3%), находящейся в периоде постменопаузы.
Ультразвуковая картина изменений эпителия матки при длительном приеме тамоксифена имеет ряд особенностей: гетерогенность структуры; множественные анэхогенные кистозные включения разного диаметра; срединные маточные структуры утолщены в сравнении с нормой в постменопаузе.
Нами было отмечено, что на фоне приема тамоксифена ТЭ может возрастать от атрофичного (1 – 2мм) (рис.5) до 8 – 10 – 15 мм (рис.6).
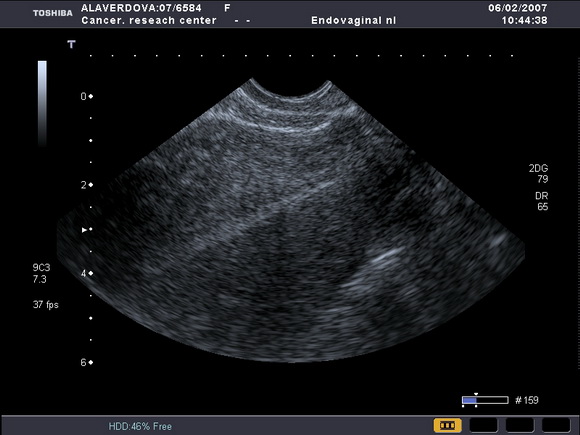
Рис.5
УЗ-томограмма матки, выполненная в продольной плоскости. Определяется атрофичный эндометрий
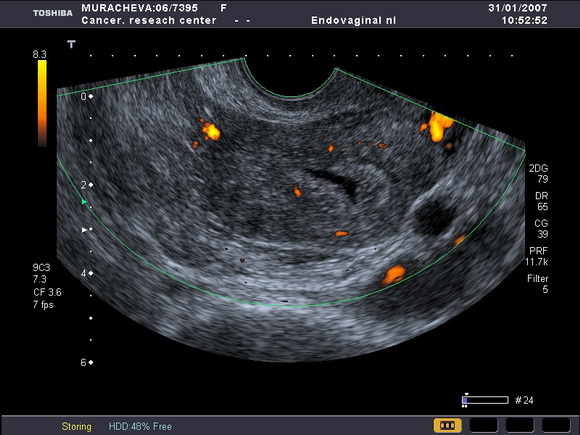
Рис.6
УЗ-томограмма матки. Определяется диффузное утолщение эндометрия
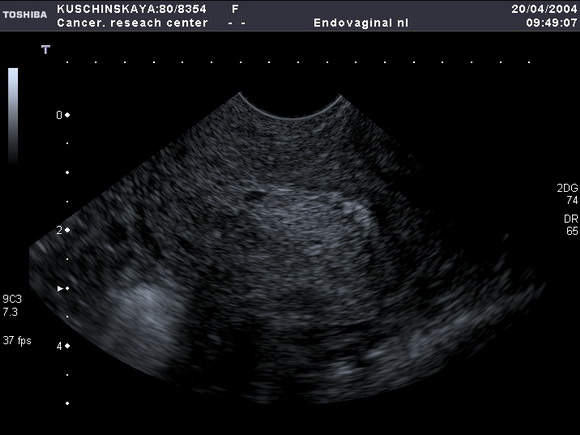
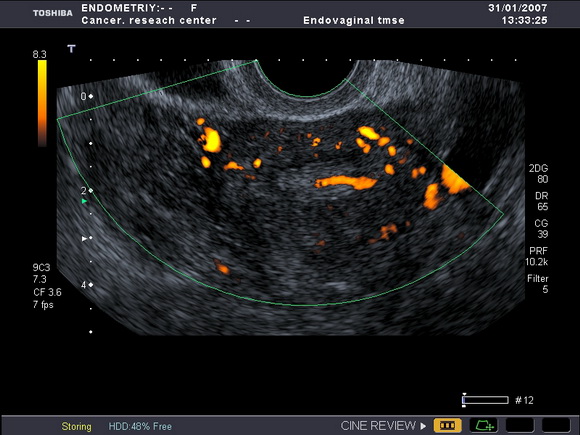
Рис.7 а,б
УЗ-томограммы матки, выполненные в продольной и поперечной плоскостях.
На фоне атрофичного эндометрия определяется полип лючения)
Микроскопически, полип характеризуется фрагментарной перигландулярной конденсацией стромальных клеток, пролиферативной активностью эпителиальных и стромальных клеток и смешанной эпителиальной метаплазией, включая сквамозную, трубную и муцинозную метаплазию (рис.7 в, г).
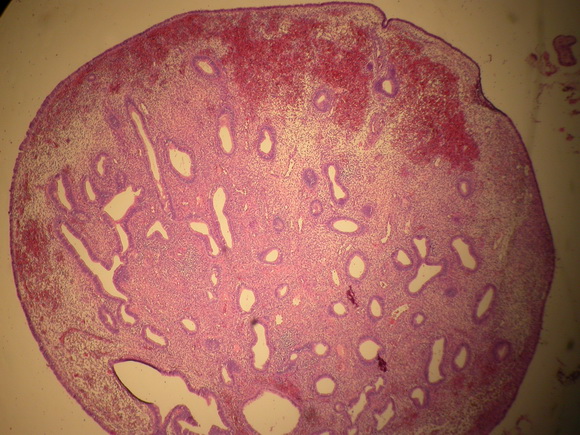
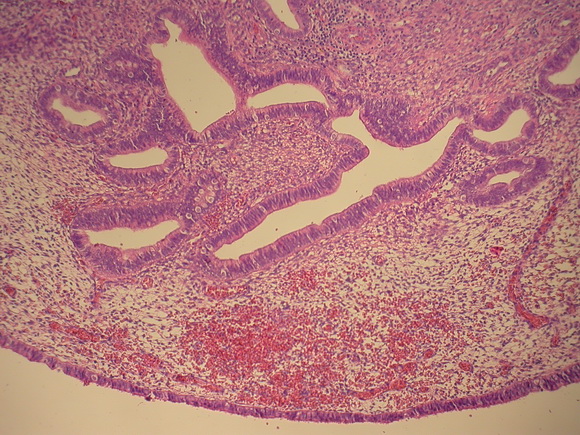
Рис.7 в,г
Железисто-фиброзный полип эндометрия на фоне приема тамоксифена.
Железы кистозно-расширены или неправильной формы железы, располагаются среди фиброзной стромы
с выраженными сосудами. Характерно расположение длинника желез параллельно поверхностной выстилки полипа.
Окраска гематоксилином и эозином, А. х 60 и В. Х200
Нехарактерно, чтобы эти три микроскопических признака сосуществовали в одном полипе у женщин, не принимающих тамоксифен.
Как было уже сказано, в большинстве наблюдений ультразвуковые заключения оказались ложнополжительными, при этом гистологическое исследование материала, полученного при выскабливании полости матки, выявило у этих пациенток следующую патологию (см. табл. 1).
Таблица 1
Состояние эндометрия по данным цитологического и гистологического исследования аспиратов и соскобов

- Как возникает рак матки?
- Факторы риска рака эндометрия
- Онкология матки: симптомы по стадиям
- Диагностика рака эндометрия
- Степень дифференциации опухоли
- Стадии рака эндометрия
- Прогноз выживаемости при раке тела матки
- Цены в Европейской клинике на лечение рака матки
Как возникает рак матки?
Рак всегда начинается с клеток — основы для формирования тканей. Из тканей состоят все органы тела человека, в том числе и матка. Здоровые клетки растут и делятся, чтобы появились новые клетки. Когда здоровые клетки стареют или повреждаются, они умирают, а их место занимают новые клетки. Но иногда этот процесс нарушается. Новые клетки начинают расти даже когда организм в них не нуждается, или же например старые и поврежденные клетки перестают умирать. Когда новых лишних клеток становится слишком много, формируется образование из ткани, которое и называется опухолью.
Доброкачественные опухоли матки, например, миомы, полипы, эндометриоз:
- не представляют угрозу для жизни;
- обычно могут быть удалены и не вырастают снова;
- не врастают в соседние органы и ткани;
- не распространяются в другие части тела
Злокачественные опухоли матки:
- представляют угрозу для жизни;
- обычно могут быть удалены и не вырастают снова;
- могут врастать и повреждать соседние ткани и органы, например, влагалище;
- могут распространяться в другие части тела.
Факторы риска рака эндометрия
Если у вас или ваших близких диагностирован рак эндометрия, совершенно естественно интересоваться и беспокоиться: что могло вызвать такое заболевание? Очень часто врачи просто не могут объяснить, почему у одной женщины появляется рак эндометрия, а у другой нет.

Но врачи знают, что существуют определенные факторы риска, которые могут с большей вероятностью привести к развитию рака матки. Среди них:
- Чрезмерный рост ткани эндометрия (гиперплазия эндометрия: патологическое увеличение числа клеток, которыми выстлана поверхность матки является фактором риска развития рака эндометрия. Гиперплазия сама по себе не является раком, но иногда может перерождаться в злокачественную опухоль. Частыми симптомами этого состояния являются: тяжелые и обильные менструации, кровянистые выделения между менструациями и кровотечения после менопаузы. Гиперплазия эндометрия — нередкое состояние у женщин старше 40 лет.
- Ожирение: Женщины с увеличенной массой тела больше подвержены риску развития рака эндометрия.
- Репродуктивный и менструальный анамнез: женщины, у которых никогда не было детей, женщины, у которых менструации начались до 12 лет, женщины, у которых менструации продолжались после 55 лет.
- Прием ТОЛЬКО эстрогена в анамнезе: риск рака эндометрия выше у женщин, которые принимали только эстроген (без прогестерона) много лет в качестве гормональной заместительной терапии при менопаузе.
- Прием тамоксифена в анамнезе: женщины, которые принимали тамоксифен для лечения или профилактики рака молочное железы.
- Лучевая терапия органов малого таза в анамнезе.
- Семейный анамнез: женщины, у которых у матери, сестры или дочери были случаи рака эндометрия находятся в зоне риска по возникновению этого заболевания, а также женщины с наследственной формой рака толстой кишки (синдром Линча).
Нужно помнить, что не у всех женщин с раком эндометрия присутствуют вышеперечисленные факторы риска. Совершенно не у всех женщин, у которых имеются эти факторы риска, возникнет рак эндометрия.
Онкология матки: симптомы по стадиям
- Первая стадия. Как правило, симптомов нет, либо могут иметься незначительные патологическое отделяемое из влагалища, например, коричневатые выделения, наличие прожилок крови на белье или общее увеличение объема влагалищных выделений.
- Вторая стадия. Симптомы более выражены. У женщин фертильного возраста это может быть увеличение продолжительности менструации, увеличение объема теряемой крови, ациклические кровотечения. У пациенток в менопаузе могут возникать скудные или обильные маточные кровотечения. Также может быть лейкорея — обильные водянистые выделения. Таким образом, распознать рак матки на ранней стадии по симптомам сложно, поскольку признаки сходны с другими заболеваниями, например, с менструальной дисфункцией.
- На третьей стадии, когда в процесс вовлекаются окружающие ткани, может наблюдаться болевой синдром (боли могут носить как постоянный, так и схваткообразный характер), выделения могут быть гнилостные (цвет мясных помоев) с неприятным запахом. При сдавлении опухолевыми массами мочеточников может развиваться гидронефроз, который характеризуется болью в пояснице и развитием азотемии — отравлением организма азотистыми продуктами обмена веществ, которые в норме должны выводиться почками.
- На четвертой стадии усиливается боль. В процесс может вовлекаться толстая кишка, что сопровождается развитием симптомов кишечной непроходимости (запоры, вздутие живота). Если опухоль проросла в стенку мочевого пузыря, в моче могут быть примеси крови. Довольно часто возникает асцит — скопление свободной жидкости в брюшной полости. При наличии отдаленных метастазов симптоматика будет определяться пораженным органом. Чаще всего рак тела матки метастазирует в печень и легкие. Также на 4 стадии отмечается общее воздействие опухоли на организм — кахексия, общая слабость и др.
Диагностика рака эндометрия
Для диагностики рака эндометрия используют следующие методики:
- Физикальное обследование органов малого таза: ваш врач будет исследовать вашу матку, влагалище и близлежащие органы, чтобы исключить наличие образований или изменений в форме и размере.
- Ультразвуковое исследование: аппарат для ультразвукового исследования использует звуковые волны, которые не слышны человеку. Эти волны отражаются от участков разной плотности. Таким образом создается изображение матки и близко расположенных органов. Такая картинка может показать опухоль эндометрия. Для получения более четкого изображения, ультразвуковое исследование может проводиться и трансвагинально (когда ультразвуковой датчик помещается во влагалище).
- Гистероскопия: использование тонкой, гибкой трубки, которая помещается во влагалище. На конце этой трубки располагается камера, которая выводит на экран изображение матки. Таким образом врач может детально рассмотреть состояние матки и эндометрия.
- Биопсия: это удаление ткани и ее дальнейшее исследование в поисках раковых клеток. Обычно используется тонкая трубка, которая помещается в матку через влагалище. Тонкий слой ткани соскабливается со стенки матки, а затем врач-патолог исследует эту ткань под микроскопом. Часто биопсия это единственный способ точной диагностики злокачественной опухоли матки.

Степень дифференциации опухоли
Если обнаружена опухоль, врач исследует образец ткани под микроскопом, чтобы определить тип и степень дифференциации опухоли. Эта степень говорит о том, насколько тип раковых клеток отличается от нормальных клеток эндометрия. По степени дифференциации опухоли можно определить как быстро она будет расти. Высоко дифференцированные опухоли часто растут быстрее и чаще распространяются. Степень дифференциации также помогает определить дальнейший протокол лечения.
При диагностике рака эндометрия очень важно определить стадию заболевания. Это самая важная информация для определения тактики лечения. Стадии заболевания определяются на основании того вросла ли опухоль в соседние органы или распространилась в другие части тела.
Когда опухоль распространяется в другие органы, то она состоит из точно таких же патологических клеток как и первичная опухоль и называется точно также. Например, рак эндометрия может распространяться в легкие; при этом в легком будут присутствовать клетки опухоли эндометрия. Это называется метастатический рак эндометрия, а не рак легкого. Лечится такое осложнение по протоколам лечения рака эндометрия, а не рака легкого.
Чтобы определить распространилась ли опухоль, врач может назначить один из следующих видов исследований:
- Лабораторные анализы. Pap-тест может показать распространился ли опухолевый процесс на шейку матки, а анализы крови могут выявить нарушения функции печени и почек. Также ваш врач может назначить анализ на субстанцию CA-125, которая часто повышается при различных видах рака.
- Рентген грудной клетки: рентген грудной клетки может помочь выявить опухоль в легком.
- Компьютерная томография: Компьютерная томография делает много последовательных рентгеновских снимков-срезов, охватывая большое количество органов, и позволяет получить высоко точную картину, найти опухоль в отдаленных участках тела: лимфоузлах, легких и др. Иногда компьютерная томография проводится с введением контрастного вещества.
- МРТ работает как большой магнит, который подключен к компьютеру и помогает получить очень точные изображения матки, других внутренних органов и лимфоузлов. Иногда МРТ также проводится с введением контрастного вещества.

Часто, чтобы точно определить стадию заболевания, необходима операция. Хирург удаляет матку и берет образцы ткани из органов малого таза и живота. Когда матка удалена, препарат исследуют и оценивают, насколько глубоко вросла опухоль. Хирург также проверяет повреждены ли соседние органы и лимфоузлы.
Стадии рака эндометрия
Стадия 0 — Патологические раковые клетки найдены ТОЛЬКО на слизистой оболочки внутреннего слоя матки такая опухоль называется карцинома матки in situ.
Стадия I — Опухоль проросла через слизистую в эндометрий. Иногда опухоль прорастает и в миометрий.
Стадия II — Опухоль проросла в шейку матки.
Стадия III — Опухоль проросла через все слои матки и внедрилась в соседние органы: влагалище и лимфоузлы.
Стадия IV — Опухоль проросла в мочевой пузырь или кишечник. Или клетки опухоли распространились в отдаленные части тела: печень, легкие или кости.
В лечении рака матки используют хирургию, химиотерапию и гормональную терапию. Часто используют комбинацию этих методов.
Прогноз выживаемости при раке тела матки
Прогноз выживаемости будет определяться стадией заболевания, возрастом пациентки и патогенетическими особенностями опухоли. Наиболее благоприятно протекают гормонально зависимые опухоли без метастазов у пациенток младше 50 лет. У них удается добиться 5-летней выживаемости у 90% пациенток. Наиболее неблагоприятный прогноз у женщин старше 70 лет с автономным типом опухоли. При отсутствии отдаленных метастазов у них удается добиться пятилетней выживаемости в 60% случаев.
Читайте также:

