Е и моисеенко онкология
– Завершается 2019 год. Чем он запомнится, если говорить о Вашем учреждении?
В 2019 году мы решили чисто технические проблемы, которые преследовали центр год из года. Благодаря внедрению информационных систем мы полностью решили вопрос с очередями.
2019 год для Петербургского онкоцентра был еще и годом науки. Мы продолжили сотрудничество с Санкт-Петербургским политехническим университетом в рамках программы разработки искусственного интеллекта. В этом году осуществилась наша мечта – мы открыли лабораторию клеточных технологий.
– Можете ли Вы сказать, что выделенные в этом году дополнительные средства на лекарственное обеспечение онкологических пациентов существенно изменили ситуацию? Если оценивать средние показатели, сколько процентов больных имели возможность получить таргетную и иммунотерапию?
В середине года Петербургскому онкоцентру неожиданно увеличили плановое задание. Это существенно изменило ситуацию с лекарственным обеспечением пациентов центра. 80% пациентов с раком легкого получают современную иммунотерапию. Дополнительное финансирование никак не сказалось на обеспечении пациентов таргетной терапией. Поскольку мы считаем таргетную терапию приоритетным направлением, и в 2018, и в 2019 году ее получили 100% пациентов, которым она была показана.
– Как Вы считаете, сколько денег в год необходимо Вашему учреждению, чтобы 100% больных получили новые опции терапии согласно рекомендациям RUSSCO?
Сложно однозначно ответить на этот вопрос. Перед нами стоит задача эффективно применять имеющиеся в нашем арсенале методы диагностики и лечения. Из года в год ситуация меняется. Меняется картина заболеваемости, меняется ландшафт лекарственных препаратов. Сейчас российские онкологи ждут появления российских аналогов дорогих импортных препаратов. Это существенно отразится на стоимости лечения. Но не будем забывать – ни одна страна мира не в состоянии на 100% обеспечить потребность.
– На Ваш взгляд, что нужно сейчас сделать в первую очередь, чтобы повлиять на увеличение продолжительности жизни больных в России?
На уровне Правительства в России делается очень много. В 2017 году введен новый порядок оказания помощи онкологическим больным, который четко определяет сроки проведения консультаций и обследований пациентов. В борьбе со злокачественными новообразованиями главное – не упустить время. На мой взгляд, ранняя диагностика – главный инструмент в борьбе с раком. А это уже зависит от отношения человека к своему здоровью. Как часто он проходит и проходит ли в принципе профилактические осмотры? Сегодня в среднем по России на начальных стадиях рак выявляется у 55,6% больных. Это очень низкий показатель. Как известно, продолжительность жизни онкологического больного определяет стадия заболевания и использование эффективных методов лечения. С увеличением финансирования появляются новые возможности в выборе этих методов.
Недавно в наш центр приезжала делегация хирургов-онкологов из Йельского университета. Американские специалисты фактически учились у российских оперировать пациентов с запущенным раком. Благодаря регулярному проведению скрининга онкозаболевания в Америке выявляются чаще на ранних стадиях.
– Какие законы затрудняют работу, что бы Вы изменили?
Основой для составления перечня схем терапии являются клинические рекомендации. В настоящее время таблетированные пероральные формы препаратов в рамках системы ОМС пациенты получают только в рамках КСГ (клинико-статистические группы). Согласно требованиям территориальной программы эта группа препаратов отпускается только в условиях стационара. Это значит, что пациент ежедневно вынужден приезжать в клинику за таблетками, врачи ежедневно ведут историю болезни. Отклонение от этой схемы является грубым административным нарушением. На прошедшем на днях итоговом собрании Ассоциации онкологов Северо-Запада обсуждался этот вопрос и было принято решение обратиться от имени Ассоциации в Министерство здравоохранения для выработки оптимальной схемы.
– Существуют ли проблемы с кадрами в Петербурге? Есть ли ощущение, что увеличивающееся количество онкологических больных может привести к значимому недостатку медицинского персонала? Случится ли это в ближайшие годы?
Борьба с онкологическими заболеваниями является приоритетной для государства. Правительство разрабатывает действенные меры по борьбе с онкологией, открывая ЦАОПы, модернизируя оснащение онкоцентров, выделяя средства на лекарственную и лучевую терапию. Однако уже давно в отрасли остро ощущается нехватка кадров. Практически во всех онкологических учреждениях укомплектованность колеблется на уроне 89%. По данным Минздрава, в России не хватает около 4 тысяч онкологов. Дефицит квалифицированных кадров испытывает и Петербургский онкоцентр. В настоящий момент у нас вакантны 24 ставки врача и 20 – среднего и младшего медицинского персонала. Мы активно сотрудничаем с медицинскими ВУЗами. Благодаря большой практической работе, хорошей оснащенности и поддержанию высокого уровня оплаты труда центр является прекрасной базой для молодых, ищущих реализации в профессии специалистов-онкологов.
– Говоря о мировых достижениях и успехах в онкологии, что Вас больше всего впечатлило за последнее время?
Как известно, в 2018 году Нобелевскую премию по физиологии и медицине получили иммунологи с разных концов света: профессор Техасского университета в Остине (США) Джеймс Эллисон и профессор Киотского университета (Япония) Тасуку Хондзё. Ученые десятилетиями пытались найти ответ на вопрос, почему иммунная система не может справиться с раковыми клетками. Поэтому наибольшим достижением последнего времени я считаю появление эффективных иммунотерапевтических препаратов, в частности, ингибиторов контрольных точек. Первая волна препаратов, представленная ингибиторами CTLA-4, двумя поколениями PD-1 и PD-L1, позволила значительно изменить подход к лечению и прогноз больных, например, немелкоклеточным раком легкого, меланомой. Сейчас мы с нетерпением ожидаем следующей волны препаратов этого класса, блокирующих другие мишени, опосредующие взаимодействие опухолевых, иммунокомпетентных клеток и структур микроокружения.
– В этом году исполнилось 20 лет Отечественной школе онкологов. Как Вы оцениваете этот проект, планируете ли его продолжение, есть ли план мероприятий на будущий год?
Отечественная школа онкологов создавалась с целью реализации образовательных программ для практикующих онкологов Санкт-Петербурга. Мы пытались восполнить информационный вакуум, когда не было ни интернета, ни возможности международного обмена опытом, не было представлений о стандартах. За 20 лет ситуация существенно изменилась. Сейчас мы испытываем избыток информации. Врачам сложно ориентироваться в ангажированном фармкомпаниями информационном поле. Мы стараемся дистанцироваться от коммерческих проектов. В течение года Школа проводит различные мероприятия прикладного характера – лекции, мастер-классы, круглые столы. За одни столом мы объединяем практиков и специалистов с мировым именем.

Прививка от рака – насколько это реально?
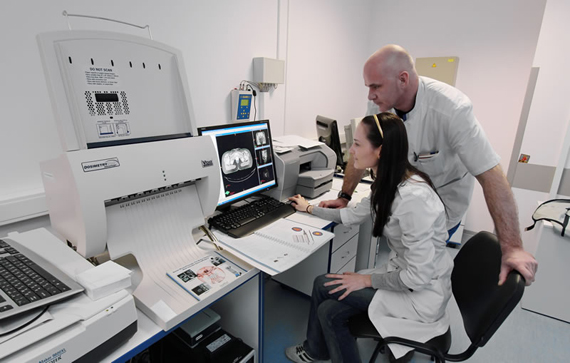
В структуре методов лечения пациентов со злокачественными новообразованиями, кроме хирургии и химиотерапия, не менее важным является и радиологическое лечение
— Технический прогресс, который мы наблюдаем каждый день, касается не только бытовых или, наоборот, космических технологий, но и здравоохранения. Сейчас онкология считается одной из самых наукоемких и самых быстроразвивающихся областей науки.
Это касается и молекулярной онкологии, это касается и иммунологической онкологии, и новых лекарственных форм, которые заставляют более эффективно доставлять старые, хорошо известные цитастатики (препараты, вызывающие некроз раковых клеток) к опухоли, повышая их эффективность, но при этом уменьшая токсичность лечения.
— Иммунотерапия, на самом деле, это второй после хирургии по возрасту метод лечения. Если хирургический метод лечения появился ещё за две–три тысячи лет до нашей эры и уже тогда использовался для лечения опухолей, то иммунотерапия появилась в середине XIX века.
И для некоторых опухолей это, действительно, оказалось справедливым. На сегодняшний день мы вакцинируем против рака шейки матки, например. Вакцинируем девочек до начала половой жизни, до инфицирования вирусом папилломы человека.
Вакцинируют и против гепатита, который является основной причиной рака печени.
И в некоторых странах, где высока частота опухоли печени (а это преимущественно азиатские страны), от вакцинации ожидается, что она значительно снизит заболеваемость. Понимаете, не только смертность, но именно заболеваемость этой патологией.
И это потому, что появились препараты, которые позволили решить очень многие проблемы, позволили сделать многие опухоли вероятно излечимыми.
Конечно, пока опыт их применения во всем мире небольшой. Так как они только начали клинически использоваться 10 лет назад, то и срок прослеживания больных, соответственно, не более десяти лет.
Отечественными фармацевтическими компаниями подобные препараты тоже разрабатываются, но они пока находятся на этапе предклиническом. А препараты, которые созданы за рубежом, на сегодняшний день уже регистрируются в нашей стране. Хотя, конечно, цена их астрономическая, и это не позволит пока использовать их широко. Но для двадцати (примерно) процентов больных, на которых использовались эти препараты, их применение приводит к полному излечению.
Например, меланома, дессиминированная, с метастазами, для которой вообще не было раньше никаких эффективных методов лечения, в современной медицине уже не считается не излечимой.
Или препараты для рака легкого у курильщиков. Еще недавно это был рак такой бесперспективной локализации.
Самое интересное, что эти новые препараты эффективны не при одной–двух опухолях, а на сегодняшний день известно 17 опухолей, при которых они дают в той или иной степени положительный эффект. То есть это очень серьезный прорыв.
Другое дело, что мы на сегодняшний день пока не знаем до начала лечения кому они могут помочь. Нет, так называемых предиктивных маркеров, и поэтому мы назначаем препараты всем подряд. И весь мир пока так назначает. Но! Идет активный поиск вот этих маркеров, которые позволили бы целенаправленно отбирать пациентов еще до введения этого дорогого препарата. А стоимость, повторюсь, у новых препаратов, к сожалению, пока астрономическая.
Охотники за мутациями
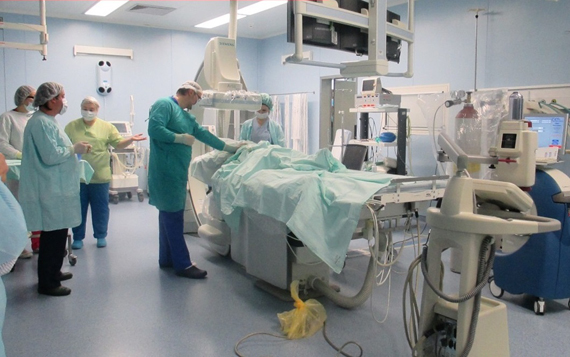
Отделение рентгенохирургии Центра является одним из самых оснащенных отделений подобного профиля не только в Российской Федерации, но и в Западной Европе
— А что такое молекулярная онкология, о которой вы упомянули?
— Это раздел онкологии, который занимается изучением изменений в генетическом аппарате опухоли. Потому что считается, что рак это генетическое заболевание.
Человеку через родителей передаются какие-то предрасположенности. И эти предрасположенности предполагают определенные генетические нарушения, в частности в клеточном аппарате, который отвечает за репарацию ДНК.
Мы рождаемся. А родители имели предполагающие к возникновению опухоли изменения. Присоединение предрасположенностей у отца и у матери могут привести к тому, что эта вероятность удвоится, утроится. И вопрос отдельный, что можно сделать в этой ситуации. Ведь примерно десять процентов опухолей связаны именно с наследственными генетическими нарушениями. Это прежде всего так называемая BRCA мутация.
И мы пытаемся этим заниматься, выявлять людей, у которых есть эти мутации. Их нужно по другому лечить, их нужно по другому наблюдать (это если мы говорим о здоровых). И может быть даже и делать то, что сделала Анджелина Джоли, когда удалила и молочные железы, и яичники. Потому что если бы она этого не сделала, то риск развития рака молочной железы и рака яичника, (а рак яичника практически невозможно выявить на ранних стадиях), у нее действительно соответствовал бы почти 100%.
Это я рассказал про одну группу больных. Другая проблема, которой занимается молекулярная онкология, изучение механизма развития опухоли и возможностей влиять на эти пути. И они позволяют определять потенциальные мишени для лекарственных препаратов.
Хотя тут тоже есть своя сложность, и на сегодняшний день она не решена. Редко бывают только одна-две-три мутации опухолевых клеток, чаще их десятки и сотни.
Допустим, делали полногеномное секвенирование у пациентов раком поджелудочной железы. И у них выявляется двести шестьдесят (!) мутаций. И какая из этих мутаций является так называемой драйверной, которая определяет развитие роста опухоли у конкретного больного? А какие мутации сопутствующие, не главные?
И теоретически есть коктейль препаратов, которые могут блокировать одну, вторую, третью, четвертую мутации. Есть. И вот мы заблокируем, допустим, часть этих мутаций и вылечим опухоль? Нет. Ничего подобного не получается. Потому что токсичность этих препаратов превышает тот эффект, который от них может быть получен.
Поэтому на сегодняшний день такая схема имеет очень ограниченное применение для рака легкого, например, когда есть мутация эпидермального фактора роста. Есть ингибиторы, которые блокируют рост опухоли, и рост прекращается, опухоль уменьшается.
Но спустя время опухоль находит коллатеральные пути, которые позволяют снова активизировать и возобновить рост. В зависимости от локализации это происходит через девять – двенадцать месяцев. И причем известно за счет чего новые мутации происходят. И соответственно известны и новые ингибиторы этих новых мутаций, и так далее. И это очень важно!
Очень важно! Так наличие таких ингибиторов позволяет все-таки перевести рак из категории неизлечимого заболевания с короткой выживаемостью в категорию неизлечимого заболевания с длительной выживаемостью. То есть рак, так же как и гипертоническая болезнь, как и сахарный диабет, становится в ряд просто хронических болезней.
Да, этот вид рака казалось бы неизлечим, но мы уже сегодня мы можем поддерживать тот критический уровень опухолевых клеток в организме, который не влияет на качество жизни больного. И делать так, чтобы они в дальнейшем не делились.
Нестоличная онкология

В Санкт-Петербургском клиническом научно-практическом центре специализированных видов медицинской помощи (онкологический) более 90% помощи оказывается бесплатно в рамках ОМС
— Насколько оправданы разговоры, что по настоящему рак лечат только в Петербурге и Москве? Не секрет, что очень многие больные из регионов едут лечиться именно в столицы.
— На самом деле в стране много хороших онкологических центров. Онкологическая хирургия всегда славилась, например, в Поволжье. Поволжская школа это Казань, Уфа, Нижний Новгород, Ульяновск и др. Там, действительно, традиционно очень сильная хирургия. Еще Оренбург, Екатеринбург, Ставрополь, Краснодар, Ростов-на-Дону. Томск уже многие годы является сильным центром в онкологии.
То есть сказать, что все сосредоточенно только в Москве и Санкт-Петербурге это неправильно. Тоже очень серьезные онкологические учреждения и очень хороший уровень оснащения. Нет, я не могу сказать, что сейчас как двадцать-тридцать лет назад есть центры только в Москве и Ленинграде. Сейчас уровень оснащения очень серьезный и квалификация специалистов достаточно высокая. И это во многих центрах в стране.
Это проблема общая. Из регионов едут в Петербург и Москву, а из Москвы едут в Израиль, в Германию. Едут в Париж. И я, кстати, ничего плохого в этом не вижу.
Я считаю, что, может быть, не лечиться надо ехать в другой город или другую страну, а например, услышать второе мнение. Это, конечно, если речь не идет о каких-либо эксклюзивных операциях, которые невыполнимы на месте.
Иногда советы второго врача бывают и очень интересными и полезными. И это нормальная практика во всем мире. А у нас в обществе это не принято. Считается, что если больной идет к другому доктору, то это воспринимается как некое предательство или неуважение.
А ведь это зачастую значит, что врач не уверен в себе, поэтому боится, что проявится его некомпетентность. А вообще речь идет о твоей судьбе, о жизни. И ты своей жизнью вправе распоряжаться сам.
Финансовая токсичность
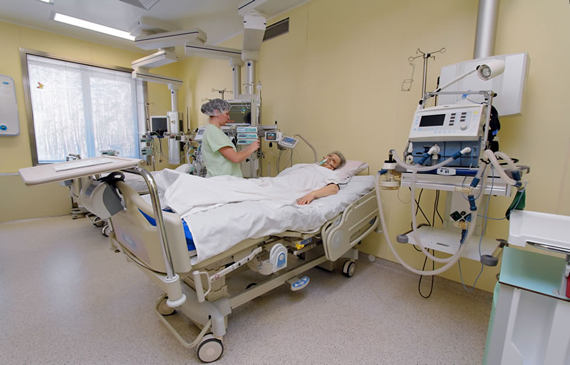
Сегодня и в России возможно оказание специализированной, в том числе высокотехнологичной, медицинской помощи больным с онкологическими и предопухолевыми заболеваниями
— Если смотреть на ситуацию в онкологии в целом, то денег не хватает нигде. Ни в Америке, ни в Японии, ни в Европе.
Это проблема общая, и сейчас даже появился термин такой за рубежом financial toxicity. Уже речь идет о токсичности не связанной с лекарственными препаратами, а именно о финансовой стороне вопроса, который не по силам даже, предположим американским страховым компаниям, хотя они несомненно богаты, и их возможности колоссальны.
И это связано, конечно, с ценой, безумной ценой препаратов. Каждый последующий препарат стоит дороже, чем предыдущий.
Если лечение, один цикл химиотерапии, в семидесятые годы стоил от десяти до ста долларов, то сейчас препараты стоят не меньше десяти тысяч долларов, это из числа тех, что самые современные. Десять тысяч долларов в месяц.
Так что это проблема общая. Просто она на разных уровнях. И решение у нас должно быть на государственном уровне. Нужно и ограничивать рост цен на лекарственные препараты на государственном уровне. И на государственном же уровне может быть увеличено финансирование лечения.
Ну и кроме того, необходима разработка отечественных препаратов. Но беда на сегодняшний день в том, что некоторые отечественные препараты на деле оказываются такой же стоимости как зарубежные, а иногда и дороже.
И к тому же, к нашим препаратам отношение скептическое. Да и к дженерикам вообще. Во всем мире доктора предпочитают назначать оригинальные препараты, а не дженерики или биосимиляры.
Я понимаю, что без развития отечественной фармацевтической промышленности у нас нет перспективы вообще никакой, нет будущего. Надо развивать собственное производство.
Но их (фармацевтические компании. – В.С.) надо и контролировать. Потому что это тоже бизнес, и у бизнеса основная задача заработать деньги. Это такая общественная серьезная проблема.
— Очень часто люди жалуются, что невозможно получить своевременную помощь бесплатно. Что же все-таки происходит в нашей медицине в плане коммерции?
— У нас в стране, медицина, в основе своей бесплатна. Просто говорят, что не бывает ничего совсем бесплатного. Кто-то должен платить. И, допустим, здесь, в нашем центре процентов 90-95 делается бесплатно.
Для пациентов бесплатно, но за счет страховых компаний и территориального фонда обязательного медицинского страхования. Деньги в клинику идут за выполненные работы и вроде бы все хорошо. Другое дело, что есть масса вопросов у докторов.
Тарифы низкие, и эти тарифы не всегда покрывают даже те расходы, которые несет клиника. Поэтому хотелось бы, чтобы тарифы были выше, но для пациента медицина при этом по прежнему оставалась бесплатной.
А что коммерческая медицина развивается параллельно, может это и хорошо? Потому что есть всегда возможность выбора, когда человек хочет чего-то необычного. Или дополнительных услуг, или использования технологий которых нет в государственных учреждениях. Почему бы нет?
В нашем центре мы также развиваем внебюджетную деятельность. Она ориентирована прежде всего на больных из других регионов и на иностранцев (жители Белоруссии, Украины, Казахстана – авт), а также на здоровых.
— И все же очень часто, несмотря на официальную бесплатную медицину, мы видим, что для излечения больных друзья и родственники объявляют сбор средств. Ваше личное отношение к такому социальному явлению?
— Я снова скажу, что я не вижу ничего плохого, если при невозможности лечения в нашей стране люди едут за новыми технологиями и новыми препаратами в другие страны. И насколько я знаю, зарубежные клиники переполнены русскими. Это и Швейцария, и Германия, и Франция. И это все, конечно, очень дорого.
И те люди, которые готовы помогать в критической ситуации незнакомым, заслуживают уважения. Помогают и детям, и взрослым, помогают искренне, помогают многим. И это, на мой взгляд, проявление настоящего милосердия. И я очень рад что в нашей стране так много отзывчивых людей.
Полный текст:
- Аннотация
- Об авторах
- Список литературы
- Cited By
Для понимания механизма эффективности локального применения 5 % геля 5-фторурацила (5-ФУ) с одновременным контактным ультразвуковым (УЗ) воздействием на опухоль у больных раком шейки матки в модельных условиях был изучен уровень поврежденности ДНК. Использована культура аденокарциномы шейки матки HeLa CC L-2, культивированная в стандартных условиях в среде RPMI-1640 с добавлением 10 % фетальной сыворотки теленка и 50 мкг/мл гентамицина. Воздействие ультразвуком осуществляли с помощью аппарата УЗТ-1.03У (Россия) в течение 10 мин с частотой 0,88 МГц и интенсивностью 0,2 Вт/см2. Доза 5-ФУ составила 0,7 мкМ, время воздействия 24 ч. Через 24 ч после начала воздействия уровень поврежденности ДНК клеток культуры исследовали методом ДНК-комет (Comet Assay) в щелочном варианте и оценивали по параметру % ДНК в хвосте кометы (% TDNA). Комбинированное воздействие УЗ/5-ФУ приводило к статистически значимому увеличению % TDNA – в 5,2 раза по сравнению с контрольной культурой, при этом % TDNA был в 1,9 раза выше показателя после воздействия только 5-ФУ и в 3,0 раза выше показателя после воздействия УЗ. Через 24 ч после комбинированного воздействия менее 50 % клеток культуры имели низкий уровень поврежденности ДНК ( 30 % TDNA) и, вероятно, находились в процессе апоптоза. Таким образом, комбинированное воздействие УЗ/5-ФУ на культуру HeLa способствовало преодолению резистентности к химиопрепарату, оказывая синергический эффект.
Франциянц Елена Михайловна, доктор биологических наук, профессор, заместитель генерального директора по науке, руководитель лаборатории изучения патогенеза злокачественных опухолей
344037, г. Ростов-на-Дону, ул. 14-я линия, 63
Сурикова Екатерина Игоревна, кандидат биологических наук, старший научный сотрудник лаборатории изучения патогенеза злокачественных опухолей
344037, г. Ростов-на-Дону, ул. 14-я линия, 63
AuthorID (РИНЦ): 301537. ORCID:
Горошинская Ирина Александровна, доктор биологических наук, профессор, главный научный сотрудник лаборатории изучения патогенеза злокачественных опухолей
344037, г. Ростов-на-Дону, ул. 14-я линия, 63
Моисеенко Татьяна Ивановна, доктор медицинских наук, профессор, главный научный сотрудник отделения гинекологии
344037, г. Ростов-на-Дону, ул. 14-я линия, 63
SPIN код: 6341-0549
Назаралиева Нелли Альбертовна, аспирант, отделение гинекологии
344037, г. Ростов-на-Дону, ул. 14-я линия, 63
Потемкин Дмитрий Сергеевич, младший научный сотрудник лаборатории молекулярной онкологии
344037, г. Ростов-на-Дону, ул. 14-я линия, 63
Васильченко Никита Геннадьевич, младший научный сотрудник лаборатории молекулярной онкологии
344037, г. Ростов-на-Дону, ул. 14-я линия, 63
1. Мерабишвили В.М., Бахидзе Е.В., Лалианци Э.И., Урманчеева А.Ф., Красильников И.А. Распространенность гинекологического рака и выживаемость больных. Вопросы онкологии. 2014; 60(3): 288–297.
3. Аксель Е.М., Виноградова Н.Н. Статистика злокачественных новообразований женских репродуктивных органов. Онкогинекология. 2018; 27(3): 64–78.
4. Меньшенина А.П., Моисеенко Т.И., Ушакова Н.Д. Возможности оптимизации предоперационной полихимиотерапии у больных инвазивным раком шейки матки. Злокачественные опухоли. 2014; (3): 30–36. doi: 10.18027/2224-5057-2014-3-30-36.
5. Меньшенина А.П., Моисеенко Т.И., Франциянц Е.М., Ушакова Н.Д., Назаралиева Н.А. Сравнительная оценка различных модификаций предоперационной полихимиотерапии у больных местно-распространенным раком шейки матки. Фундаментальные исследования. 2015; (1–8): 1629–1633.
7. Водолажский Д.И., Назаралиева Н.А., Моисеенко Т.И., Франциянц Е.М., Потемкин Д.С., Васильченко Н.Г., Меньшенина А.П. Усиление цитотоксического действия 5-фторурацила при сочетанном применении с ультразвуком. Известия вузов. Северо-Кавказский регион. Серия: Естественные науки. 2018; 198(2): 100–105. doi 10.23683/0321-3005-2018-2-100-105.
8. Оценка генотоксических свойств методом ДНК-комет in vitro. Методические рекомендации МР 4.2 0014-10. М., 2010. 15 с.
9. Тарнопольская О.В., Сурикова Е.И., Горошинская И.А., Тихановская Н.М. Способы оценки повреждения ДНК в лейкоцитах крови у пациенток раком молочной железы методом ДНК-комет. Клиническая и экспериментальная морфология. 2016; 18(2): 60–65.
10. Chemeris N.K., Gapeyev A.B., Sirota N.P., Gudkova O.Y., Kornienko N.V., Tankanag A.V., Konovalov I.V., Buzoverya M.E., Suvorov V.G., Logunov V.A. DNA damage in frog erythrocytes after in vitro exposure to a high peak-power pulsed electromagnetic field. Mutat Res. 2004; 558(1–2): 27–34. doi: 10.1016/j.mrgentox.2003.10.017.
11. Hu Z., Lv G., Li Y., Li E., Li H., Zhou Q., Yang B., Cao W. Enhancement of anti-tumor effects of 5-fluorouracil on hepatocellular carcinoma by low-intensity ultrasound. J Exp Clin Cancer Res. 2016 Apr 22; 35: 71. doi: 10.1186/s13046-016-0349-4.
12. Wang X., Wang Y., Wang P., Cheng X., Liu Q. Sonodynamically induced anti-tumor effect with protoporphyrin IX on hepatoma22 solid tumor. Ultrasonics. 2011 Jul; 51(5): 539–46. doi: 10.1016/j.ultras.2010.12.001.
13. Gao Z., Zheng J., Yang B., Wang Z., Fan H., Lv Y., Li H., Jia L., Cao W. Sonodynamic therapy inhibits angiogenesis and tumor growth in a xenograft mouse model. Cancer Lett. 2013 Jul 10; 335(1): 93–9. doi: 10.1016/j.canlet.2013.02.006.
14. Wood A.K.W., Sehgal C.M. A review of low-intensity ultrasound for cancer therapy. Ultrasound Med Biol. 2015 Apr; 41(4): 905–28. doi: 10.1016/j.ultrasmedbio.2014.11.019.
15. Sengupta S., Balla V.K. A review on the use of magnetic fields and ultrasound for non-invasive cancer treatment. J Adv Res. 2018 Jun 20; 14: 97–111. doi: 10.1016/j.jare.2018.06.003.
16. Yu T., Bai J., Hu K., Wang Z. Biological effects of ultrasound exposure on adriamycin-resistant and cisplatin-resistant human ovarian carcinoma cell lines in vitro. Ultrason Sonochem. 2004 Apr; 11(2): 89–94. doi: 10.1016/S1350-4177(03)00160-3.
17. Hassan M.A., Furusawa Y., Minemura M., Rapoport N., Sugiyama T., Kondo T. Ultrasound-induced new cellular mechanism involved in drug resistance. PLoS One. 2012; 7(12): e48291. doi: 10.1371/journal.pone.0048291.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Полный текст:
- Аннотация
- Об авторах
- Список литературы
- Cited By
Проценко Светлана Анатольевна - заведующий отделением химиотерапии и инновационных технологий, кандидат медицинских наук
Рудакова Алла Всеволодовна - доктор фармакологических наук, профессор кафедры медицинского и фармацевтического товароведения СПГХФА.
197022, Санкт-Петербург, ул. Профессора Попова, д. 14, тел. 8 (812) 234-18-01, е-mail: rudakova_a@mail.ru
Моисеенко Федор Владимирович - кандидат медицинских наук
Левченко Евгений Владимирович - заведующий отделением торакальной онкологии, доктор медицинских наук, профессор
Мацко Дмитрий Евгеньевич - руководитель отдела морфологии опухолей, доктор медицинских наук, профессор
Иванцов Александр Олегович - врач-патологоанатом отдела морфологии опухолей
Семенов Игорь Иванович - заведующий отделением лучевой диагностики, доктор медицинских наук, профессор
Иевлева Аглая Геннадъевна - научный сотрудник лаборатории молекулярной онкологии
Митюшкина Наталья Владимировна - врач лаборатории молекулярной онкологии
Того Александр Викторович - старший научный сотрудник лаборатории молекулярной онкологии, кандидат медицинских наук
Новик Алексей Викторович - научный сотрудник отделения химиотерапии и инновационных технологий, кандидат медицинских наук
Имянитов Евгений Наумович - руководитель лаборатории молекулярной онкологии, доктор медицинских наук, профессор.
197758, Россия, г. Санкт-Петербург, Песочный, ул. Ленинградская, д. 68, НИИ онкологии им. Н.Н. Петрова, тел. 8 (812) 596-65-11, e-mail: s.protsenko@list.ru
Моисеенко Владимир Михайлович - руководитель онкологического центра ЛДЦ МИБС им. С.М. Березина, доктор медицинских наук, профессор.
197758, Россия, г. Санкт-Петербург, Песочный, ул. Карла Маркса, д. 43, Тел. 8 (812) 596-80-85, e-mail: moiseyenkov@gmail.com
1. Государственный реестр цен на лекарственные средства, относящиеся к перечню жизненно необходимых и важнейших лекарственных средств (ЖНВЛС), по состоянию на 26 июля 2011 года || htpp: //www.ROS-MED.INFO.
2. Моисеенко В.М., Проценко С.А., Семенов И.И., Моисеенко Ф.В., Левченко Е.В., Мацко Д.E., Иванцов А.О., Иевлева А.Г., Митюшкина Н.В., Того А.В., Имянитов Е.Н. Эффективность гефитиниба в первой линии терапии неоперабельных аденокарцином лёгкого, содержащих мутацию в гене EGFR: исследование II фазы // Вопросы онкологии. – 2010. – Т. 56. – № 1. – С. 20-23.
6. Brock D. Ethical and value issues in insurance coverage for cancer treatment // The Oncologist. 2010. Vol. 15. Suppl. 1. P. 36–42.
7. Fukuoka M. Biomarker analyses and final overall survival results from a phase III, randomized, open-label, first-line study of gefitinib versus carboplatin/paclitaxel in clinically selected patients with advanced non–small-cell lung cancer in Asia (IPASS) / Fukuoka M., Wu Y.-L., Thongprasert S. et al. // J. Clin. Oncol. 2011. Vol. 29. P. 2866-2874.
8. Gridelli С. Gefitinib as first-line treatment for patients with advanced non-small-cell lung cancer with activating epidermal growth factor receptor mutation: Review of the evidence / С. Gridelli, F. De Marinis, M. Di Maio et al. // Lung Cancer. 2011. Vol.71. P. 249-257.
9. Horgan A. An economic analysis of the INTEREST trial, a randomized trial of docetaxel versus gefitinib as second-/third-line therapy in advanced non-small-cell lung cancer / A. Horgan, P. Bradbury, E. Amir et al. // Ann. Onc. 2011. Vol. 22. P. 1805–1811.
10. Malin J. Wrestling with the high price of cancer care: should we control costs by Individuals’ ability to pay or society’s willingness to pay? // J. Clin. Oncol. - 2010. Vol. 28. P. 3212-3214.
11. Moiseyenko V. M., Procenko S. A., Levchenko E. V., Barchuk A.S., Moiseyenko F.V., Iyevleva A.G., Mitiushkina N.V., Togo A.V., Semionov I.I., Ivantsov A.O., Matsko D.E., Imyanitov E.N. High efficacy of first-line gefitinib in non-Asian patients with EGFR-mutated lung adenocarcinoma // Onkologie. 2010. Vol. 33. №5. Р. 231-238.
12. Nadler E. S. Do oncologists believe new cancer drugs offer good value? / E.S. Nadler, B. Eckert, P. Neumann // J. Clin. Oncol. 2005. Vol. 23. Р. 6011.
13. Neumann P. Cancer therapy costs influence treatment: a national survey of oncologists/ P. Neumann, J. Palmer, E. Nadler et al. // Health Aff. 2010. Vol. 29. P. 196-202.
14. Petrelli N. Clinical Cancer Advances 2009: Major Research Advances in Cancer Treatment, Prevention, and Screening—A Report From the American Society of Clinical Oncology / N. Petrelli, E. Winer, J. Brahmer, et al. // J. Clin. Oncol. 2009. Vol. 27. P. 6052-6069.
15. Rocchi A. The role of economic evidence in Canadian oncology reimbursement decision-making: to lambda and beyond / A. Rocchi, D. Menon, S. Verma, E. Miller // Value Health. 2008. Vol. 11. P. 771–783.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Читайте также:

