Что значат баллы при онкологии
На основе гистологического заключения. Злокачественность опухоли напрямую влияет на исход болезни: чем выше степень, тем агрессивнее рак, и тем хуже прогноз для выздоровления.
Врач-гистолог оценит степень злокачественности
Злокачественность опухоли
Морфологическое исследование удаленных раковых тканей, как обязательный этап диагностики, помогает определить злокачественность опухоли. В организме человека триллионы клеточных структур, основой которых являются около 100 различных типов клеток: каждая из них может переродиться в раковую. При этом результат перерождения-трансформации может быть морфологически очень близок к исходно нормальной клетке. Или настолько сильно отличаться, что, кажется, и сравнивать не с чем.
Злокачественность опухоли – это степень клеточных изменений, указывающая на агрессивность Карциномы: чем выше цифра после буквы G, тем сильнее отличается злокачественное новообразование от исходной ткани в месте возникновения рака.
Степени злокачественности
Гистологический диагноз – это морфологический вариант опухоли и степень злокачественности. Выделяют 3 степени:
- Высокая степень дифференцировки опухолевой ткани (G1) – клетки первичного очага отличаются от нормальных клеточных структур удаленного органа или ткани, но морфологически похожи: у врача-гистолога нет никаких сомнений в том, что основой злокачественного перерождения стали клетки именно из этого органа или ткани;
- Средняя степень дифференцировки (G2) – схожие черты исходной ткани сохраняются, но различий больше: гистологически опухоль сильно отличается от нормы, но отошла еще не так далеко;
- Низкая степень (G3) – раковые клетки имеют крайне мало сходства с органом или тканью в первичном очаге: гистолог сразу понимает, что это чужеродный и агрессивный зверь.
Необходимо обращать внимание на цифровое значение критерия G в диагнозе: низкодифференцированные опухоли всегда прогностически хуже, при G1 шансы на выздоровление значительно выше.
Значимость клеточных изменений опухоли
Важно понимать: злокачественность опухоли – это одно из значений диагноза, необходимое для реального понимания силы Карциномы. Это вовсе не означает, что при G3 нет никаких шансов для выживания, а при G1 можно радостно подбрасывать чепчики – типа, мы уже почти победили врага.
Высокодифференцированные опухоли – это:
- Сравнительно медленная скорость прогрессирования;
- Низкий риск быстрого и раннего метастазирования;
- Высокая чувствительность к лекарственной терапии;
- Высокие шансы на длительную ремиссию.
Низкодифференцированные раки – это:
- Быстрый рост первичного опухолевого очага;
- Ранние метастазы в лимфоузлы и отдаленные органы;
- Отсутствие положительного ответа на химиотерапию;
- Низкие шансы на выживаемость.
Казалось бы, все просто: G1 – это благоприятно, G3 – это плохо. Но в жизни все значительно сложнее, потому что на прогноз при онкологии влияют масса факторов. Злокачественность опухоли – это важный элемент диагностики, на который надо обращать внимание: низкая степень дифференцировки раковых клеток указывает на то, что враг силен, зол, беспринципен и агрессивен. Война будет изнурительно-длительной, не каждая битва будет успешной, после каждого боя будет казаться, что Карцинома становится сильнее, но, тем не менее, шансы на победу есть всегда.

-
2 минут на чтение

Шкала Карновского в онкологии – это система, по которой происходит оценка общего состояния больных раком. Благодаря такому методу появляется возможность не только устанавливать, насколько эффективно прошла предоперационная подготовка, но и отслеживать в целом проведение терапевтических мероприятий. Чтобы оценить состояние пациента, может использоваться индекс Карновского по 100-бальной системе или шкала боли у онкобольных, предусматривающая 4-бальный критерий.
- Что такое
- Зачем нужна
- Методы оценки состояния онкологических пациентов
Что такое
Индекс Карновского, или шкала ECOG в онкологии, представляют собой широко востребованную систему, предназначенную для отслеживания функционального состояния людей с раковыми опухолями. Впервые введение понятия было отмечено в 1949 году.
Система позволяет описывать состояние пациентов благодаря использованию 11-бальной шкалы в соотношении с процентным значением, не превышающем 100% (отсутствуют признаки болезни) и 0% — летальный исход.
Зачем нужна
Качество жизни представляет собой ряд параметров, которые будут отражать состояние в период развития онкологического процесса и проведения терапевтических мероприятий. В результате специалист может оценить психологические, физические и функциональные особенности онкобольного.

- Общее
![]()
Наталья Геннадьевна Буцык- 6 декабря 2019 г.
Поскольку качество жизни представляет собой динамическое состояние, значения которого способны меняться во времени, то необходимо использовать систему в течение определенного периода как изменяющийся параметр, который будет зависеть от течения и разновидности злокачественного процесса, а также применяемых методов терапии.
Благодаря полученным данным специалист может более правильно подбирать тактику терапевтических мероприятий.
Методы оценки состояния онкологических пациентов
Определение состояния больного при помощи индекса Карновского выглядит следующим образом:
- 100% — жалобы у пациента отсутствуют, признаки патологии не были обнаружены;
- 90% – суточная активность сохраняется в нормальном состоянии, симптомы болезни имеют слабую степень проявления;
- 80% – поддержание активности проходит с затруднениями, симптоматика выражена умеренно;
- 70% – пациент может себя обслуживать, однако при выполнении активной работы возникают определенные сложности;
- 60% – способность самостоятельного обслуживания сохраняется, однако при определенных ситуациях требуется посторонняя помощь;
- 50% – больной может обслуживать себя не полностью, в большинстве случаев необходима помощь со стороны медицинского персонала;
- 40% – нужен специальный уход;
- 30% – у пациента отсутствует возможность к самостоятельному обслуживанию себя, назначается госпитализация, несмотря на то, что нет угрозы для жизни;
- 20% – болезнь протекает в тяжелой форме, больного госпитализируют, требуется проведение активного поддерживающего лечения;
- 10% – заболевание переходит в стадию термального периода, отмечается быстро прогрессирующее состояние;
- 0% – констатируется смертельный исход.

- Общее
![]()
Наталья Геннадьевна Буцык- 6 декабря 2019 г.
Если оценивать качество жизни онкологического больного по системе Еcog, то показатели будут иметь следующие значения:
- ECOG 0 — это означает полную активность пациента. Он может выполнять все те же функции, что и до начала развития злокачественной патологии. По шкале Карновского этот параметр будет расцениваться на 90-100 процентов.
- ECOG 1 — это указывает на отсутствие способности к выполнению тяжелого физического труда. Человек предрасположен к легкой или сидячей работе (70-80%).
- ECOG 2 – осуществляется амбулаторная терапия. Еще сохраняется способность к самостоятельному обслуживанию. Большую часть бодрствования больной проводит лежа (50-60% по индексу Карновского).
- ECOG 3 – отмечаются ограниченные возможности пациента. 50 процентов времени он находится в вертикальном положении (30-40%).
- ECOG 4 – присваивается инвалидность. Отсутствует способность самостоятельно себя обслуживать. По Карновскому этот параметр составляет 10-20%.
Описанная система позволяет оценивать не только качество жизни, но и уровень применяемого лечения. В настоящее время для определения подобных значений применяется комплекс методик.

В 2013 присвоена специальность онколог. Образование — МГМСУ на базе РОНЦ им. Н.Н. Блохина. В 2014 присвоена специальность гематолог. Обучение пройдено в ФГБУ НМИЦ гематологии Минздрава России. Стаж — 5 лет.
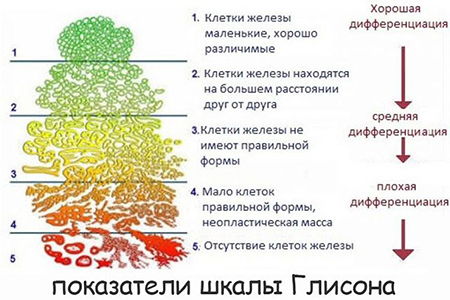
Шкала Глисона совместно с международной классификацией TNM активно используется для диагностики рака предстательной железы. В первом случае за основу берется дифференцировка клеток ПЖ – если она не просматривается, значит, опухоль запущена. Показатели по системе TNM указывают на размер новообразования, степень его агрессивности (метастазы), проникновение патологических молекул в лимфатические пути.

Перую градацию разработал американский гистолог Глисон в 1974 году, а вторым методом диагностики с 1943 по 1952 годы занимался французский ученый Пьер Денуа. При раке предстательной железы онкологи используют обе шкалы. Берется во внимание анализ крови на определение уровня простатспецифического антигена.
- Принцип оценки по Глисону
- 6 баллов
- 7 баллов
- 8 баллов
- 9 баллов
- 10 баллов
- Насколько точна оценка
Принцип оценки по Глисону
Сумма баллов обозначает, на какой стадии находится рак железы у мужчины.
Расшифровка индекса зависит от оценочной величины: если образцу ставится 1 балл, то это говорит о минимальных изменениях и невысокой агрессивности опухоли. Пять баллов – наихудший результат для отдельно взятого биоптата, свидетельствующий о максимальном онкологическом перерождении молекул железы.
Подробнее о значении G по шкале Глисона ниже:
- Один балл. Незначительные изменения в ядрах. Клеточные структуры однородны и не нарушены.
- Два балла. Новообразования разделяет соединительная ткань (строма). Дистанция между молекулами железы немного увеличивается.
- Три балла. Наблюдается неравномерность клеток. Строма между очагами опухоли исчезает.
- Уменьшается количество нормальных клеток, аномальные же, напротив, распространяются, в том числе и на окружающие ткани.
- Пять баллов. Простатических клеток в образце нет. Биоптат представляет собой недифференцированное скопление фиброзной материи.
Если сумма баллов в соответствии с радацией Дональда Глисона не превышает значения 2, это говорит о том, что клетки простаты практически здоровы. Если показатель составляет 3–4 единицы – рак находится на первой стадии. Разброс величин от 2 до 4 свидетельствует об очень медленном росте опухоли, отсутствии метастаз (индекс Mx по классификации TNM), незараженной лимфатической системе (Nx-N0).
Задайте вопрос врачу-урологу!

Показатель, не превышающий пяти, в результате прибавления оценок двух образцов по Глисону обозначает вторую стадию рака простаты. В этот период повышается уровень ПСА, отчетливо видны различия между здоровыми и раковыми клетками железы. Положительный момент: рост новообразования останавливается самостоятельно при активизации защитных сил организма.
Данная оценка говорит о медленно развивающемся раке ПЖ второй стадии. Строение железы неоднородное, распространение опухолевого процесса на другие органы отсутствует, иногда патологическое перерождение клеток затормаживается. Объективно симптомы заболевания практически никак не проявляются. При обнаружении рака с индексом 6 по Глисону прогнозы благоприятные – это местная незлокачественная опухоль, рост которой относительно продуктивно контролируется с помощью терапии.
Это агрессивная онкология простаты промежуточной стадии (между 2-й и 3-й). Хуже, если в примере первыми фигурируют 4 балла (4+3). Подобный показатель на таблице Глисона значит, что риск оккупации соседних тканей опухолевыми процессами крайне высок. Если при наличии семерки по Глисону наблюдается индекс M1 классификации TNM, это говорит о единичных метастазах. В обратном случае (3+4) прогноз более оптимистичный. Для лечения данного вида рака применяется химиотерапия. Также рекомендуют радикальное удаление простаты, если опухоль не вышла за границы органа.
Это быстро растущая опухоль 3–4-й стадии. Поставленные 8 баллов по шкале Глисона значат, что атипичные клетки пронизывают не только ткани простаты, но и органы малого таза. Аномальные молекулы поражают лимфоток (факт подтверждается показателем N1 согласно TNM-классификатору) и мгновенно разносятся по организму, попадая в мозг, легочную систему, позвоночный столб. ПСА в крови сильно увеличен, кости становятся хрупкими. Если метастазы не успели оккупировать организм полностью, то комплексная медикаментозная и гормональная терапия, облучение или радикальное иссечение железы приносят положительные результаты.
Терапия возможна, но зачастую малоэффективна. Лечение сводится к облучению, гормональному замещению. Карциному удаляют, если опухоль не вышла за пределы капсулы. Индекс TNM T3-Т4 говорит об инфильтрации раковых клеток в соседние ткани. Резекция на этом этапе не принесет результатов, поэтому в основном применяют паллиативные (поддерживающие) методы.
Наихудший индекс опухоли предстательной железы по Глисону – 10. Он означает, что клетки органа сильно укрупнились и переродились полностью. Простата прекратила выполнять свою функцию. В образцах не обнаруживаются нормальные молекулы. Более того, патологические клетки поражают весь организм.
Основные действия медицинских работников направлены на паллиативную помощь и торможение роста раковых новообразований. Операция при запущенной 4-й стадии (10 по Глисону) бессмысленна: резекция не помогает, а только ухудшает жизнь больного. Шансы на излечение – 5%, но если пациент попадет в этот счастливый промежуток, необходимо помнить, что риск рецидивов очень высок.

Насколько точна оценка
Достоверность результатов гистологического исследования зависит от правильности взятия материала. Если процедура проведена профессионально, то ее информативность высока: трактовка результатов с помощью таблицы Глисона подробно продемонстрирует характер клеточной трансформации. Важно, чтобы биоматериал был взят из наиболее видоизмененных областей простаты. Ошибочной считается пункция, когда один образец позаимствован с пораженного участка, а второй – со здорового. В результате диагностика будет неправильной и рак продолжит незаметно убивать организм больного.
Наиболее правильными называют пробы, взятые при проведении оперативного вмешательства. Метод определения агрессивности и характера атипичных клеток используется в крупных ведущих урологических центрах по всему миру. Лучше пройти раннюю диагностику, чем пытаться вылечить запущенную стадию рака. Берегите себя!
Если у вас остались вопросы, задайте их в комментариях (это абсолютно анонимно и бесплатно). По возможности, я или другие посетители сайта помогут вам.

ИГХ при раке молочной железы — необходимость современной онкологии. Его результаты позволяют подобрать максимально подходящее женщине противоопухолевое лечение.
Что такое иммуногистохимия при РМЖ?
Иммуногистохимический анализ или коротко ИГХ основан на способности иммунитета синтезировать вещества, нейтрализующие инородные агенты — бактерии, вирусы, грибы и выделяемые ими токсины. Инородные агенты — это антигены, в их присутствии иммунные клетки вырабатывают определённое антитело, на каждое антитело имеется свой антиген.
Рак молочной железы умело скрывается от санкций иммунитета, тем не менее раковые клетки и их структурные элементы — антитела, иммунитет их не видит, но ИГХ выявляет эти антитела.
При ИГХ кусочек опухоли обрабатывают реагентами с антигенами, которые находят своё антитело и соединяются с ним, изменяя окраску исследуемого кусочка злокачественной ткани.
Для чего проводят иммуногистохимию при РМЖ?
Иммуногистохимия нужна не для научной работы, а для практического использования:
- Обнаружение в клетках рецептора половых гормонов, чувствительного к эстрогену (ЭР) или прогестерону (ПР), прогнозирует чуть более плавное течение рака с меньшей вероятностью метастазирования, с преимущественной локализацией метастазов в костях, большую продолжительность жизни даже при генерализации процесса;
- Разная концентрация ЭР и ПР позволяет выбрать для конкретной женщины оптимальное лечение, так при высоком уровне ЭР в сочетании с ПР и даже без них можно рассчитывать на хороший результат гормональной терапии, без рецепторов обязательна химиотерапия;
- Наличие в клетке НЕR2 в высокой концентрации указывает на агрессивность рака, что требует химиотерапии и специфического нейтрализатора НЕR2;
- Сочетание позитивного гормонального статуса с НЕR2 вызывает сомнения в результативности гормонотерапии, поэтому в программу лечения включается химиотерапия;
- Высокая концентрация Ki-67 — свидетельство высокой степени злокачественности и, опять-таки, не позволяет избежать химиотерапии.
Показания к иммуногистохимии при РМЖ
При раке молочной железы для ИГХ только одно показания — определение степени агрессивности рака по его структурным компонентам для подбора оптимальной программы лечения.
Обычный морфологический анализ — гистология показывает степень злокачественности опухоли и её клеточный состав, часто неоднородный, но не позволяет определить белковые структуры:
- Чувствительность каждой клетки к лекарствам определяется наличием у нее рецепторов половых гормонов;
- Активность клеточного размножение и скорость роста ракового узла контролирует белок НЕR2, если его слишком много, то рак будет расти быстрее и формировать защиту клетки от лекарств вплоть до полной устойчивости;
- Способность быстро воспроизводить замену погибшим клеткам, захватывая при этом новые территории, определяет маркер пролиферации Ki-67.
Концентрацию всех этих клеточный субстанций и определяет ИГХ.
Подготовка к исследованию
ИГХ при раке молочной железы проводится вне организма больной, но с кусочком её опухоли. Сегодня всем женщинам с впервые обнаруженным новообразованием в железе на этапе диагностики специальной иглой выполняется биопсия — кор-биопсия.
Взятый небольшой столбик раковой ткани подвергается гистологическому исследованию и ИГХ, что позволяет верифицировать, то есть доказать наличие рака, и планировать первичное лечение. Удалённую во время операции на молочной железе опухоль тоже подвергают гистологическому и ИГХ исследованиям для уточнения плана лечения.
Женщине перед биопсией надо только успокоиться, никакой определенной подготовки от неё не требуется.
Проведение исследования
Взятый при биопсии или из удалённых при операции тканей молочной железы кусочек рака в пробирке с формалином (для консервации) отправляется в патоморфологическую лабораторию. Кусочек разрезается на тончайшие пластинки, которые консервируются на очень длительный срок — несколько десятилетий, чтобы при необходимости имелся материал для анализа. Пластинки также подвергают иммуногистохимии.
ИГХ делается двумя способами: внесённые с реактивом антигены напрямую контактируют с антителами или через антиген-посредник, который сначала ищет свое антителом, а затем этот дуэт находится вторым антигеном, концентрация которого и измеряется.
О чем говорят результаты?
Обнаружение в раке молочной железы рецепторов ЭР и ПР предсказывает относительно доброкачественное течение при эффективности гормональных препаратов, но в реальной жизни опухоль может не среагировать на эндокринную терапию, правда процент устойчивости невысок.
Обнаружение Ki-67 прогнозирует неспокойную жизнь и интенсивное лечение с использованием максимальных возможностей химиотерапии для изменения негативного прогноза болезни.
Рецептор НЕR2 — прогностический фактор, предлагающий сосредоточение на химиотерапии без особых надежд на антигормональное воздействие, но с другой стороны, предсказывает необходимость использование таргетного препарата, связывающего патологический белок.
Расшифровка исследования
Формально считается, что 1% ЭР уже положительно, но до 10% ЭР сомнительна надежда на значимый результат эндокринной терапии. Иммуногистохимический анализ рецепторного статуса рака молочной железы предполагает следующие ответы:
- от 0 до 2 баллов — нет гормональной зависимости;
- при 3 — 8 баллах — возможна зависимость от эндокринного воздействия, чем больше баллов, тем выше уровень рецепторов, тогда как при 3 баллах только десятая часть раковых клеток имеет рецептор.
Градации ответов при определении НЕR2:
Белок Ki-67 констатирует:
- меньше 15% — невысокая активность пролиферации;
- 16% — 30% — умеренная агрессивность;
- выше 30% — высокая агрессия.
Определяемые при иммуногистохимии структурные элементы не гарантируют исполнения предначертанного — в процессе лечения рак изменяет свои характеристики. В нашей клинике определяют реальные характеристики злокачественного процесса в конкретный момент времени и подбирают оптимальное лечение по панели из множества генов.
Лечение болевого синдрома в онкологии
Несмотря на выдающиеся достижения современной онкологии, проблема терапии боли у пациентов с онкозаболеваниями остается актуальной и у нас, и за рубежом. Общеизвестно, что практически каждый третий пациент, впервые пришедший на прием к онкологу, испытывает боль разной степени интенсивности.
Подбор и назначение эффективной противоболевой терапии – сложная задача, требующая многокомпонентного подхода. Для правильного и адекватного обезболивания при раке врачу-онкологу необходимо собрать анамнез боли: причина, давность, интенсивность, локализация, тип, факторы, усиливающие или уменьшающие боль; время возникновения боли в течение дня, применявшиеся ранее анальгетики, их дозы и эффективность.


Осмотр и клинико-лабораторные исследования важны для выбора наиболее безопасного для конкретного пациента комплекса анальгетиков и адъювантных средств.
Причиной боли при онкологическом заболевании является:
-
Боль, вызванная самой опухолью (поражение костей, мягких тканей, кожи, внутренних органов, органов пищеварительного тракта);
Боль при осложнениях опухолевого процесса (патологический перелом, некроз, изъязвление, воспаление, инфицирование тканей и органов, тромбозы);
Боль при паранеопластическом синдроме;
Боль при последствиях астенизации (пролежни);
- при осложнениях хирургического лечения (например, фантомная боль),
- при осложнениях химиотерапии (стоматит, полинейропатия и др.),
- при осложнениях лучевой терапии (поражение кожи, костей, фиброз и др).
Классификация болевого синдрома:
Специалистами разработана классификация болевых синдромов при онкологии, каждый из которых требует особенного подхода в терапии.
По локализации источника боли
По временным параметрам
По степени выраженности боли
Оценка интенсивности хронического болевого синдрома
0 баллов – боли нет, 1 балл – слабая боль, 2 балла – боль умеренная, 3 балла – боль сильная, 4 балла – нестерпимая, самая сильная боль.
Нередко онкологи применяют визуально-аналоговую шкалу интенсивности боли от 0 до 10, на которой предлагают пациенту отметить степень своих болевых ощущений. Эти шкалы позволяют количественно оценить динамику хронического болевого синдрома в процессе лечения.

На основании данных диагностики врач-онколог устанавливает причину, тип, интенсивность хронического болевого синдрома, локализацию боли, сопутствующие осложнения и возможные психические нарушения.


Пример "болевого" опросника, который заполняет врач-онколог при первичном осмотре пациента
На последующих этапах наблюдения и терапии лечащий врач проводит повторную оценку эффективности обезболивания, выраженности побочных эффектов фармакотерапии. Этим достигается максимальная индивидуализация терапии болевого синдрома, отслеживаются возможные побочные эффекты применяемых анальгетиков и динамика состояния пациента.
Основные принципы назначения фармакотерапии боли у онкологических пациентов:
- Прием обезболивающих препаратов по часам, а не по требованию. Соблюдение этого принципа позволяет достичь наибольшего эффекта с минимальной суточной дозой обезболивающего препарата.
Адекватная доза и режим приема анальгетиков должны соблюдаться как основа противоболевого действия;
Лечение по восходящей - означает, что лечение боли у онкологических больных следует начинать с ненаркотических препаратов, постепенно переходя к более сильным препаратам.
Трехступенчатая схема обезболивания при раке

- На первом этапе лечения боли слабой и средней интенсивности применяются ненаркотические препараты (неопиды). Основными препаратами этой группы являютсяаспирин, парацетамол, анальгин, седальгин, пентальгин, диклофенак и пр.
Необходимо понимать, что использование ненаркотических анальгетиков в лечении более сильной боли ограничено их способностью к обезболиванию. Обезболивающий эффект имеет свои пределы и не усиливается бесконечно с увеличением дозы препарата. При этом возрастает только опасность побочных реакций и проявлений токсичности.
- Поэтому когда боль у онкологических пациентов усиливается, несмотря на увеличение дозы обезболивающих препаратов, наступает второй этап лечения боли – добавление мягких опиоидных анальгетиков. Это трамал, трамадол, кодеин, дионин.
Обращаем ваше внимание, что подбор и дозировку анальгетиков проводит только врач-онколог!
- Когда применение ненаркотических препаратов не дает нужного эффекта, лечащий врач переходит к использованию препаратов третьего этапа - сильных опиатов (просидол, норфин, морфин, дюрогезик, MST-Continus, фендивия).
Дюрогезик – трансдермальный пластырь - содержит фентанил в дозе 25, 50. 75 и 100 мкг/час и выпускается в виде пластыря, содержащего резервуар с обезболивающим препаратом. Доза зависит от размера пластыря. Длительность действия препарата составляет 72 часа.

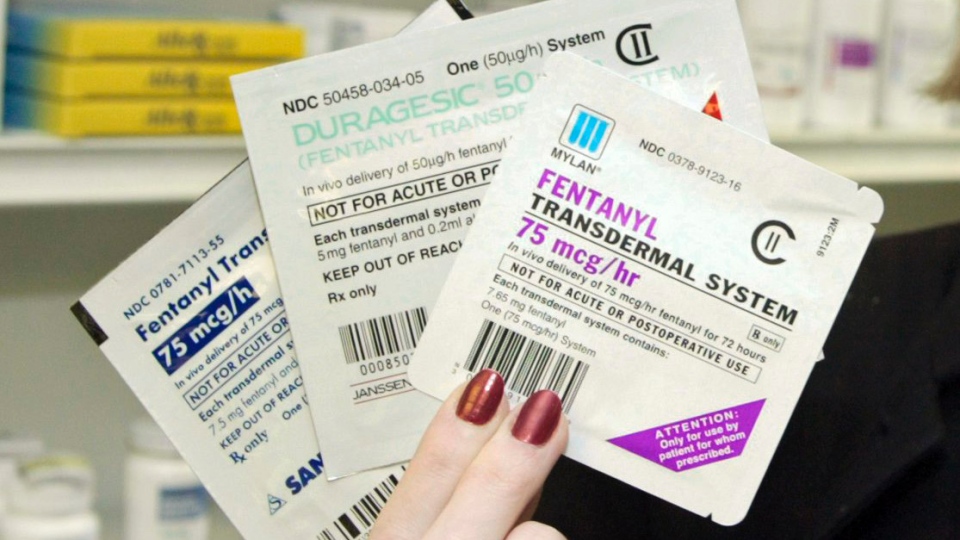
Наряду с основными анальгетиками (опиаты и неопиаты) большое значение имеют адъювантные, то есть вспомогательные препараты – кортикостероиды (дексаметазон), антидепрессанты (амитриптилин), противосудорожные (карбамазепин), антигистаминные, транквилизаторы.
Эти препараты используются в основном при лечении отдельных симптомов и осложнений у онкологических больных.
Лечение нейропатической боли
Лечение нейропатической (жгучей) боли представляет собой значительно более сложную задачу вследствие недостаточной эффективности большинства анальгетиков.
По статистике более 50% пациентов, имеющих нейропатическую боль, продолжают испытывать ее на фоне назначенного лечения опиоидами, что свидетельствует о низкой эффективности традиционных обезболивающих препаратов.
В Европейских рекомендациях по лечению нейропатической боли препаратами первой линии названы антиконвульсанты, антидепрессанты и местные анестетики – это амитриптилин, габапентин и прегабалин.
Прегабалин – препарат последнего поколения, обладающий меньшими побочными эффектами, полной безопасностью, эффективностью начальной дозы и быстрым началом действия.
Важной особенностью прегабалина является его способность уменьшать и полностью нивелировать остроту болевых ощущений, что подтверждается значительным снижением (в 2-5 раз) числа жалоб на жгучие, простреливающие и режущие боли. Это способствует улучшению качества жизни онкологических больных с хроническими болевыми синдромами.


Подводя итоги, мы хотим еще раз подчеркнуть, что один из важнейших принципов лечения болевого синдрома в онкологии – принцип индивидуальности. Выбор препарата для обезболивания при раке, а также подбор дозировки в каждом конкретном случае зависит от причины, вызывающей боль, общего состояния пациента, от наличия и выраженности имеющихся расстройств отдельных органов и систем.
Важно прогнозировать возможные или уже имеющиеся на момент осмотра побочные эффекты предшествующей противоопухолевой или обезболивающей терапии. Следует осуществлять направленный выбор основного препарата для терапии, в зависимости от патогенеза боли (ноцицептивная, нейропатическая, психогенная).
В современной онкологии врачи обладают широким арсеналом препаратов для борьбы с болью онкологического генеза, поэтому почти во всех случаях (>90%) удается полностью купировать болевой синдром или же значительно уменьшить его интенсивность.
Читайте также:


