Что такое симуляция в онкологии

Лучевая терапия — это один из ведущих методов противоопухолевого лечения, основанный на использовании ионизирующего излучения. Может применяться как самостоятельный вид терапии, так и в рамках комбинированного/комплексного лечения (совместно с другими методами), в качестве радикальной, нео- и адъювантной, консолидирующей, профилактической и паллиативной терапии.
- Виды лучевой терапии
- Этапы лучевой терапии
- Побочные эффекты лучевой терапии
- Химиолучевая терапия

Виды лучевой терапии
Уже несколько десятилетий человечество изучает воздействие ионизирующего излучение на организм человека. При этом акцентируется внимание как на положительном, так и отрицательном эффекте, возникающем при его применении. Разрабатываются новые методы, которые позволяют добиваться максимального лечебного эффекта при снижении отрицательного действия на организм. Улучшается оборудование для проведения лучевой терапии, появляются новые технологии облучения.
Сейчас классификация методов лучевой терапии довольно обширна. Мы остановимся только на самых распространенных методиках.
При контактной лучевой терапии источник излучения вводится непосредственно в опухоль или прилегает к ее поверхности. Это позволяет прицельно облучать новообразование с минимумом воздействия на окружающие его ткани.
К контактным видам лучевой терапии относятся:
- Аппликационная лучевая терапия. Применяется при лечении поверхностно расположенных опухолей, например, новообразований кожи, слизистых оболочек гениталий. В этом случае используются индивидуально изготовленные аппликаторы, которые накладываются непосредственно на поверхность новообразования.
- Внутриполостная лучевая терапия. Источник ионизирующего излучения вводится в просвет полого органа, например, в пищевод, мочевой пузырь, прямую кишку, полость матки или влагалища. Для облучения используются специальные аппликаторы (их называют эндостатами), которые заполняются радионуклидами.
- Внутритканевое облучение. Источник ионизирующего излучения вводится непосредственно в ткань опухоли. Для этого используются интростаты, которые могут иметь вид игл, шариков, трубочек, заполненных источником излучения.
Кроме того, существует такой вид лечения, как радионуклидная терапия. В этом случае используются открытые источники излучения в виде растворов радионуклидов (радиофармацевтический препарат — РФП), которые при попадании в организм прицельно накапливаются в опухолевых очагах и уничтожают их. Чаще всего РФП вводится внутривенно. Наибольшее распространение получили следующие виды радионуклидной терапии:
- Терапия радиоактивным йодом. Используется для лечения ряда видов рака щитовидной железы, поскольку йод избирательно накапливается в тиреоидной ткани.
- Применение остеотропных РФП используется для лечения метастазов в костях или костных опухолей.
- Радиоиммунотерапия — радионуклиды присоединяют на моноклональные антитела, чтобы добиться прицельного воздействия на опухолевую ткань.
При дистанционной лучевой терапии источник излучения находится на расстоянии от тела пациента, при этом на пути его прохождения могут лежать здоровые ткани, которые в процессе проведения терапии также подвергаются облучению, что приводит к развитию осложнений разной степени выраженности. Чтобы их минимизировать, разрабатываются различные технологии, позволяющие сконцентрировать максимальную дозу ионизирующего излучения непосредственно на в мишени (опухоли). С данной целью используются:
- Короткофокусная рентгенотерапия. При облучении используется рентгеновское излучение малой и средней мощности, которое способно проникать в ткани на глубину до 12 мм. Метод назван так из-за того, что источник располагается на коротком расстоянии от облучаемой поверхности. Таким способом лечат неглубокие опухоли кожи, вульвы, конъюнктивы и век, ротовой полости.
- Гамма-терапия. Этот вид излучения имеет большую проникающую способность, поэтому может использоваться для лечения более глубоко расположенных опухолей, нежели рентген-терапия. Однако сохраняющаяся большая нагрузка на окружающие органы и ткани приводят к ограничению возможности использования данного метода в современной онкологии.
- Фотонная терапия. Именно этим видом излучения проводится лучевое лечение большинства онкологических пациентов в современном мире. Достаточно высокая проникающая способность в сочетании с высокотехнологичными способами подведения дозы (IMRT и VMAT), достаточно совершенные системы планирования позволяют очень эффективно использовать этот вид излучения для лечения пациентов с приемлемыми показателями токсичности.
- Применение корпускулярного излучения (электроны, протоны, нейтроны). Эти элементарные ядерные частицы получают на циклотронах или линейных ускорителях. Электронное излучение используют для лечения неглубоких опухолей. Большие надежды возлагаются на протонную терапию, с помощью которой можно максимально прицельно подводить высокие дозы излучения к глубоко расположенным опухолям при минимальном повреждении здоровых тканей за счет выделения радиационной дозы на определённом отрезке пробега частиц, однако пока эти виды излучения играют сравнительно небольшую роль в лечении онкологических заболевания из-за своей высокой стоимости и ряда не до конца решённых технологических аспектов реализации метода.
Этапы лучевой терапии
Весь процесс проведения лучевой терапии делят на три этапа:
- Предлучевая подготовка (КТ-симуляция), этап выбора объёмов облучения и критических структур, этап дозиметрического планирования, верификации плана лучевой терапии.
- Этап облучения.
- Постлучевой этап.
Как правило, этап планирования занимает несколько дней. В это время проводятся дополнительные исследования, которые призваны дать возможность врачу более точно оценить границы опухоли, а также состояние окружающих ее тканей. Это может повлиять на выбор вида лучевой терапии, режима фракционирования, разовой и суммарной очаговых доз. Основой же данного этапа является выполнение так называемой КТ-симуляции, то есть компьютерной томографии необходимого объёма с определёнными параметрами и в определённом положении тела пациента. Во время КТ-симуляции на кожу пациента и/или его индивидуальные фиксирующие устройства наносятся специальные метки, призванные помочь правильно укладывать пациента в дальнейшем, а также облегчить задачу навигации по время проведения сеансов облучения.
Затем врач-радиотерапевт рисует объёмы облучения и критических структур (тех, на которые будет предписано ограничение дозы) на полученных срезах КТ с учётом данных других диагностических модальностей (МРТ, ПЭТ). Далее формируется задача для медицинского физика, включающая определение доз, которые должны быть подведены к мишени, мишеням или отдельным её частям, а также тех, которые не должны быть превышены в объёмах здоровых органов и тканей. Медицинский физик разрабатывает дозиметрический план в соответствии с заданными параметрами, при соблюдении которых и успешной верификации данного плана на фантоме, можно считать пациента готовым к лучевой терапии.
На этапе подготовки к лучевой терапии пациенту рекомендуется придерживаться нескольких правил:
- Отказаться от средств, раздражающих кожу.
- Если на коже в месте воздействия имеются повреждения или элементы сыпи, следует проконсультироваться с врачом.
- Если предполагается лучевая терапия в челюстно-лицевой области, требуется санация полости рта.
- Воздержаться от загара.
- Главное правило на любом этапе: обсудить все нюансы предстоящих подготовки и лечения с лечащим врачом-радиотерапевтом и строго придерживаться полученных рекомендаций!
Проведение этапа облучения будет зависеть от выбранного метода лучевой терапии.
Проведение дистанционной лучевой терапии
Продолжительность курса дистанционной лучевой терапии зависит от выбранного режима фракционирования, а также цели лечения. Паллиативные курсы, как правило, короче неоадъювантных и адъювантных, а те, в свою очередь, менее продолжительны, чем радикальные. Однако подведение радикальной дозы возможно и за один-несколько сеансов в зависимости от клинической ситуации. В таком случае курс дистанционной лучевой терапии называется стереотаксической радиотерапией или радиохирургией. Варьирует и кратность сеансов в день и в неделю: чаще всего используются схемы с пятью сеансами в неделю, однако могут быть предложены и 2-3 сеанса в день (гиперфракционирование) и схемы с 1-4 и 6 сеансами в неделю.
Во время облучения пациент в подавляющем большинстве случаев располагается лежа на столе специальной установки. Крайне необходимо соблюдать полную неподвижность во время сеанса облучения. Для достижения этого могут использоваться специальные фиксирующие устройства и системы иммобилизации.
Перед тем как включить установку, медперсонал покидает помещение, и дальнейшее наблюдение осуществляется через мониторы или окно. Общение с пациентом осуществляется по громкой связи. Во время выполнения сеанса, части аппарата и стол с пациентом совершают движения по заданной траектории. Это может создавать шум и беспокойство у больного. Однако бояться этого не стоит, поскольку вся процедура контролируется.
Сам сеанс лучевой терапии может длиться как 5-10, так и 60-120 минут, чаще — 15-30 минут. Само воздействие ионизирующего излучения не вызывает никаких физических ощущений. Однако в случае ухудшения самочувствия пациента во время сеанса (выраженной боли, судороги, приступа тошноты, паники), следует позвать медицинский персонал заранее оговоренным способом; установку сразу отключат и окажут необходимую помощь.
Контактная лучевая терапия (брахитерапия)
Брахитерапия проводится в несколько этапов:
- Введение в облучаемую зону неактивных проводников — устройств, в которые затем имплантируют источник ионизирующего излучения. При внутриполостной лучевой терапии используются приспособления, называемые эндостатами. Их устанавливают непосредственно в полость облучаемого органа и рядом с ним. При внутритканевой лучевой терапии используются интростаты, которые устанавливаются непосредственно в ткань опухоли по заранее просчитанной схеме. Для контроля их установки, как правило, используются рентгенологические снимки.
- Перемещение источника излучения из хранилища в интро- и эндостаты, которые будут облучать опухолевую ткань. Время облучения и особенности поведения пациента будут зависеть от вида брахитерапии и используемого оборудования. Например, при внутритканевой терапии, после установки источника ионизирующего излучения пациент может покинуть клинику и прийти на повторную процедуру через рекомендуемый промежуток времени. Весь этот период в его организме будет находиться интростат с радионуклидами, которые будут облучать опухоль.
Проведение внутриполостной брахитерапии будет зависеть от используемых установок, которые бывают двух типов:
- Установки низкой мощности дозы. В этом случае один сеанс облучения длится около 2-х суток. Под наркозом имплантируются эндостаты. После контроля правильности их установки и введения радионуклидов, пациент переводится в специальное помещение, где должен будет находиться все время, пока длится процедура, соблюдая строгий постельный режим. Разрешается только немного поворачиваться на бок. Вставать категорически запрещено.
- Установки высокой мощности дозы. Время облучения составляет несколько минут. Для установки эндостатов наркоза не требуется. Но во время процедуры все равно необходимо лежать абсолютно неподвижно. Внутриполостная лучевая терапия установкой высокой мощности проводится несколькими сеансами с интервалами от одного дня до одной недели.
При радионуклидной терапии пациент принимает радиофармпрепараты внутрь в виде жидкого раствора, капсул или инъекций. После этого он помещается в специальную палату, имеющую изолированную канализацию и вентиляцию. По истечении определенного срока, когда мощность дозы снизится до приемлемого уровня, проводится радиологический контроль, пациент принимает душ и переодевается в чистую одежду. Для контроля результатов лечения проводится сцинтиграфия, после чего можно покинуть клинику.
Лучевая терапия является серьезным стрессом для организма. У многих пациентов в этот период ухудшается самочувствие. Чтобы его минимизировать рекомендуется придерживаться следующих правил:
- Больше отдыхать. Минимизируйте физическую и интеллектуальную нагрузку. Ложитесь спать, когда почувствуете в этом необходимость, даже если она возникла в течение дня.
- Постарайтесь сбалансировано и полноценно питаться.
- Откажитесь на время проведения терапии от вредных привычек.
- Избегайте плотной обтягивающей одежды, которая бы могла травмировать кожу.
- Следите за состоянием кожи в месте облучения. Не трите и не расчесывайте ее, используйте средства гигиены, которые вам порекомендует врач.
- Защищайте кожу от воздействия солнечных лучей — используйте одежду и головные уборы с широкими полями.

Побочные эффекты лучевой терапии
Лучевая терапия, как и другие методы противоопухолевого лечения, вызывает ряд осложнений. Они могут быть общими или местными, острыми или хроническими.
Острые (ранние) побочные эффекты развиваются во время проведения радиотерапии и в ближайшие недели после неё, а поздние (хронические) лучевые повреждения — через несколько месяцев и даже лет после ее окончания.
Угнетенное эмоциональное состояние
Подавляющее большинство пациентов, проходящих лечение по поводу злокачественного новообразования, испытывают тревожность, страх, эмоциональное напряжение, тоску и даже депрессию. По мере улучшения общего состояния, эти симптомы стихают. Чтобы облегчить их, рекомендуется чаще общаться с близкими людьми, принимать участие в жизни окружающих. При необходимости рекомендуется обратиться к психологу.
Чувство усталости
Чувство усталости начинает нарастать через 2-3 недели от начала терапии. На это время рекомендуется оптимизировать свой режим дня, чтобы не подвергаться ненужным нагрузкам. В то же время нельзя полностью отстраняться от дел, чтобы не впасть в депрессию.
Изменение крови
При необходимости облучения больших зон, под воздействие радиации попадает костный мозг. Это в свою очередь приводит к снижению уровня форменных элементов крови и развитию анемии, повышению риска кровотечения и развития инфекций. Если изменения выражены сильно, может потребоваться перерыв в облучении. В ряде случаев могут назначать препараты, стимулирующие гемопоэз (кроветворение).
Снижение аппетита
Обычно лучевая терапия не приводит к развитию тошноты или рвоты, но снижение аппетита наблюдается довольно часто. Вместе с тем, для скорейшего выздоровления требуется полноценное высококалорийное питание с высоким содержанием белка.
Побочные реакции со стороны кожи
Вероятность развития кожных реакций и их интенсивность зависят от индивидуальных особенностей пациента. В большинстве случаев через 2-3 недели в области воздействия возникает покраснение. После окончания лечения оно сменяется пигментированием, напоминающим загар. Чтобы предотвратить чрезмерные реакции, могут назначаться специальные кремы и мази, которые наносятся после окончания сеанса. Перед началом следующего их необходимо смыть теплой водой. Если реакция выражена сильно, делают перерыв в лечении.
Реакции со стороны полости рта и горла
Если облучают область головы и шеи, могут развиться лучевой стоматит, который сопровождается болью, сухостью во рту, воспалением слизистых, а также ксеростомия вследствие нарушения функции слюнных желез. В норме эти реакции проходят самостоятельно в течение месяца после окончания лучевой терапии. Ксеростомия может беспокоить пациента в течение года и более.
Осложнения со стороны молочной железы
При прохождении лучевой терапии по поводу рака молочной железы могут возникать следующие реакции и осложнения:
- Покраснение кожи груди.
- Отек груди.
- Боль.
- Изменение размера и формы железы из-за фиброза (в некоторых случаях эти изменения остаются на всю жизнь).
- Уменьшение объема движения в плечевом суставе.
- Отек руки на стороне поражения (лимфедема).
Побочное действие на органы грудной клетки
- Воспаление слизистой пищевода, которое приводит к нарушению глотания.
- Кашель.
- Образование мокроты.
- Одышка.
Последние симптомы могут свидетельствовать о развитии лучевого пневмонита, поэтому при их возникновении следует немедленно обратиться к вашему врачу.
Побочные реакции со стороны прямой кишки/петель кишечника
- Расстройство стула — диарея или наоборот, запоры.
- Боли.
- Кровянистые выделения из заднего прохода.
Побочные действия со стороны мочевого пузыря
- Учащенное болезненное мочеиспускание.
- Наличие примеси крови в моче иногда может быть настолько выраженным, что моча приобретает кроваво-красный цвет.
- Наличие патологических примесей в моче — кристаллы, хлопья, гнойное отделяемое, слизь.
- Уменьшение емкости мочевого пузыря.
- Недержание мочи.
- Развитие везиковагинальных или везикоректальных свищей.
Побочные эффекты при облучении опухолей забрюшинного пространства, печени, поджелудочной железы
- Тошнота и рвота.
- Ознобы после сеансов.
- Боли в эпигастрии.
Химиолучевая терапия
Лучевая терапия довольно редко проводится в качестве самостоятельного лечения. Чаще всего она сочетается с каким-либо другим видом лечения: хирургическим, а чаще всего — с лекарственным. Это может быть как вариант одновременной химиолучевой терапии, так и последовательной, а также варианты сочетания лучевой терапии с иммунотерапией, таргетной и гормональной терапии. Такие виды лечения могут иметь ощутимо более высокую противоопухолевую эффективность, однако необходимо тщательно оценить риски совместных побочных эффектов, поэтому принятие решения о любом объёме лечения с онкологической патологией должен принимать мультидисциплинарный онкологический консилиум.
Лучевая терапия в EMC
Уважаемые пациенты!
Мы работаем в обычном режиме. Во всех наших клиниках усилены меры инфекционной безопасности, уменьшен интервал дезинфекции всех контактных поверхностей, усилена дезинфекция воздуха в помещениях. На ресепшн клиник размещены медицинские маски и дополнительные дезинфекторы для рук. Мы действуем в строгом соответствии с нормативными документами по выстраиванию системы противодействия вирусу в медицинских организациях г. Москвы.

В ЕМС используются самые передовые технологии в лучевой терапии, что позволяет применять широкий спектр современных методов для лечения онкологических заболеваний. Наши специалисты имеют возможность подобрать оптимальный вариант лечения для каждого пациента.
Благодаря лучевой терапии на оборудовании последнего поколения мы можем облучать опухоль с точностью до долей миллиметра, избегая воздействия на здоровые ткани. Таким образом достигается максимально возможная эффективность лечения и существенное снижение побочных эффектов.
По сравнению с некоторыми альтернативными методиками, при которых пациент вынужден в процессе лечения неподвижно лежать в течение длительного времени (1 час и более), мы имеем возможность провести лечение пациентов с такой же точностью и эффективностью за кратковременные сеансы (3-5 мин) в течение нескольких недель.

Лучевая терапия используется:
для лечения рака и предотвращения его рецидива;
до операции, чтобы уменьшить опухоль;
после операции для уничтожения оставшихся раковых клеток;
в сочетании с химиотерапией;
в качестве паллиативного лечения, когда удаление опухоли невозможно (паллиативная лучевая терапия предназначена для облегчения боли и других симптомов за счет уменьшения размеров опухоли).
Лучевая терапия применяется для лечения следующих видов рака:
опухолевые образования в головном мозге;
опухолевые образования головы и шеи;
рак молочной железы;
рак предстательной железы;
рак спинного мозга.
Как проводится лучевая терапия
Лучевая терапия состоит из четырех крайне важных для эффективности лечения этапов:
Сеанс лучевой терапии
Перед началом лечения необходима консультация врача, онколога-радиолога (его также называют лучевым или радиотерапевтом). Основываясь на конкретном случае, онколог-радиолог порекомендует определенный вид лучевой терапии, обсудит с вами необходимость сочетания с другими методами лечения, определит конкретные цели терапии и предупредит о возможных побочных эффектах.
КТ симуляция

Чтобы онколог-радиолог мог разработать план лечения, сначала должны быть определены точный размер и расположение опухоли. Обычно это делается путем создания детального 3D-изображения опухоли посредством компьютерной томографии (КТ).
Пациента укладывают на стол КТ-сканера в положение, в котором он будет находиться во время облучения, зафиксировав это положение с помощью специальных устройств. Все полученные изображения передаются в систему планирования, где уже на основе трехмерного изображения тела и отмеченной опухоли по данным КТ, создается план лечения.
В конце КТ симуляции на коже пациента рисуют смывающуюся специальную маркировку в точке центра облучения (изоцентра), которые помогут выбрать правильное положение в процессе лечения.
Планирование лучевой терапии
На основе КТ симуляции медицинские физики в команде с лучевым терапевтом создают индивидуальный план лечения пациента. При разработке плана лечения принимаются во внимание многие факторы, в том числе тип рака, расположение и размер опухоли, анамнез, а также результаты лабораторных анализов. План лечения, сформированный на основе этих факторов, определяет дозу излучения, углы, под которыми должно проводиться облучение, и количество сеансов, необходимое для выполнения назначенного лечения.
Сеанс лучевой терапии

Радиотерпевт помогает пациенту занять правильное положение на столе линейного ускорителя, как на КТ симуляции.
Процедура лечения безболезненна, излучение невидимо для глаз и не ощущается пациентом.
Первые две процедуры могут продолжаться 15 минут или больше, так как радиотерапевт помогает пациенту занять нужное положение и делает снимки, чтобы убедиться, что положение в установке то же, что предусмотрено планом лечения. Последующие процедуры часто бывают менее продолжительными. Некоторые процедуры – с момента входа в комнату ожидания до выхода из клиники – могут занимать всего от 12 до 30 минут.
Как правило, лучевая терапия проводится один раз в день, 5 раз в неделю. Курс лечения может длиться от 1 до 8 недель.
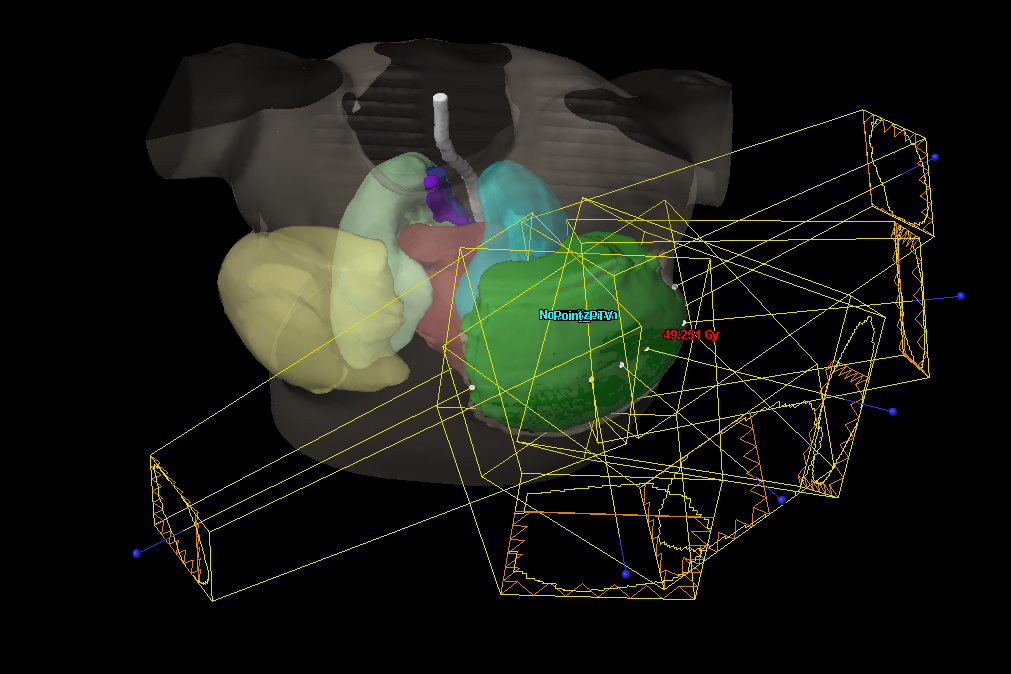
Технология IMRT (лучевая терапия с модулированной интенсивностью) использует пространственное 3D-сканирование тела для направления к опухоли пучков излучения под разными углами. При каждом из этих углов интенсивность излучения варьируется (модулируется), и форма пучка изменяется для соответствия форме опухоли.
Лучевая терапия останавливает деление и рост раковых клеток, тем самым замедляя или прекращая рост опухоли. Во многих случаях лучевая терапия способна уничтожить все раковые клетки, в результате чего происходит сокращение объема или исчезновение опухоли.
Лучевая терапия с модулированной интенсивностью (IMRT) – это технология высокоточной лучевой терапии, при которой используются линейные ускорители, обеспечивающие возможность дозировать излучение на различные области злокачественной опухоли и прилежащие к ней ткани. IMRT создает условия для более точного формирования пучка излучения для трехмерной (3-D) формы опухоли за счет модулирования, или контроля интенсивности в нескольких небольших объемах пределах самого пучка излучения. IMRT позволяет еще больше сфокусировать высокие дозы излучения на области в пределах опухоли, сводя при этом к минимуму дозу, действующую на окружающие здоровые структуры.
Лечение тщательно планируется с помощью 3-D компьютерной томографии (КТ) или магнитно-резонансной томографии (МРТ) в сочетании с компьютеризированным расчетом дозы, чтобы создать такое распределение интенсивности дозы, которое будет лучшим образом соответствовать форме опухоли. Комбинации нескольких полей с модулированной интенсивностью, с различных направлений, позволяют получить индивидуально подобранную форму излучения, в результате чего на опухоль действует максимальная доза, а на прилежащие здоровые ткани - минимальная.
Поскольку при использовании IMRT доза, действующая на здоровую ткань, снижена до минимума, более высокие и эффективные дозы излучения могут быть безопасно доставлены к опухолям с минимальными побочными эффектами, по сравнению с традиционными техниками лучевой терапии. По сравнению с традиционной лучевой терапией, IMRT, за счет своей сложности, требует несколько более длительных периодов ежедневного лечения и дополнительного планирования, а также оценки показателей безопасности, прежде чем пациент сможет начать лечение.
В настоящее время IMRT более активно используется для лечения рака предстательной железы, опухолей головы и шеи, а также опухолей центральной нервной системы. IMRT также применяется в отдельных случаях для лечения рака молочной железы, щитовидной железы, легкого, а также опухолей желудочно-кишечного тракта, гинекологических злокачественных новообразований и некоторых определенных видов сарком. IMRT также может быть методом выбора при лечении злокачественных новообразований у детей.
IGRT - это методика лучевого лечения, при которой увеличивается точность облучения за счет контроля положения опухоли с помощью изображений, полученных во время сеанса лечения. Снимки, полученные во время процедуры сравнивают с КТ, которое было выполнено при проведении симуляции, таким образом, радиолог настраивает форму пучка и изменяет положение пациента, увеличивая точность лечения и защищая здоровые ткани.
Когда применяется IGRT?
Методика IGRT применяется при лечении опухолей в органах, которые изменяют свое положение в процессе дыхания, например, опухолей легких, печени и предстательной железы, а также при опухолях, соседствующих с жизненно-важными структурами.
Кто осуществляет лечение?
Для осуществления IGRT требуется подбор необходимой дозы облучения и наиболее подходящих параметров проведения лучевой терапии – эти функции, как правило, выполняет радиотерапевт совместно с физиком-дозиметристом. Непосредственно сеанс лучевой терапии на аппаратах осуществляется радиотерапевтом и рентгенолаборантом.
Требуется ли от пациента специальная подготовка к проведению радиотерапии под визуальным контролем?
Перед началом лечения необходимо предупредить радиотерапевта о возможной беременности, а также о проведении грудного вскармливания. Следует сообщить врачу о наличии в организме металлических медицинских изделий, например протезов, искусственных водителей ритма, так как эти предметы могут повлиять на составление плана лучевой терапии, а также на возможность применения МРТ для планирования лучевой терапии. При симуляции лучевой терапии на кожу пациента наносятся маркером метки, с помощью которых при лечении воспроизводится идентичность укладки.
Как проводится IGRT?
Перед началом каждого сеанса пациент с помощью рентгенолаборанта укладывается на кушетку и принимает положение идентичное тому, в котором он находился при проведении симуляции лечения. Иногда для обеспечения идентичности укладки применяются различные фиксирующие устройства (маска, матрац и др.). Далее проводится контроль положения пациента с помощью снимка и сопоставление его положения с данными полученными при КТ симуляции. В случае неполной идентичности укладки врач просит пациента немного поменять положение и повторяет снимок. При полном совпадении положения пациента и физико-дозиметрических параметров начинается сеанс лучевой терапии.
RapidArc®
Новаторская технология RapidArc была разработана Varian Medical Systems с целью улучшения результатов лечения за счет более высокой точности, вариабельности лечения и укорочения сеанса лечения.
RapidArc позволяет использовать варианты положений и параметров установки, создающие большое количество модификаций воздействия на опухоль. В отличие от других вариантов лечения техническое оснащение RapidArc предоставляет 360 регулируемых позиций, в каждой из которых возможна настройка скорости вращения головки линейного ускорителя, формы многолепесткового коллиматора, который формирует направленный пучок лучей, а также регуляция мощности и дозы ионизирующего излучения.
Использование RapidArc позволяет охватить весь объем опухоли, что позволяет создать идеальный план лечения, именно для конкретного пациента с учетом конфигурации опухоли, обеспечивая точность воздействия на патологический очаг и максимально щадящее действие на здоровые ткани.
Объемное модулированное облучение увеличивает интенсивность лечения, уменьшая дозовую нагрузку на окружающие ткани. Данная методика также позволяет значительно сократить сроки лечения.
RapidArc, или VMAT, сочетает в себе прецезионность радиотерапии с необходимой мощностью, но при этом меньше воздействует на окружающие ткани.
Применение RapidArc лечение проводится в полном круговом диапазоне в трехмерном объеме, что позволяет создать план лечения любой сложности, что в свою очередь уменьшает побочные эффекты и позволяет значительно меньше воздействовать на здоровые ткани.
Кто выполняет лечение при применении RapidArc ?
Для осуществления этой технологии, как и при других методиках лучевой терапии, требуется подбор необходимой дозы облучения и наиболее подходящих параметров проведения лучевой терапии – эти функции, как правило, выполняют радиотерапевт совместно с физиком-дозиметристом. Лучевая терапия на аппаратах осуществляется радиотерапевтом и рентген-лаборантом.
При этой технологии сеанс лечения сокращается до 2 минут, но укладка пациента несколько сложнее за счет настройки аппарата под конкретного больного, форму и локализацию его опухоли.
Преимущества методики:
сокращение времени лечения в несколько раз по сравнению с другими методиками;
уменьшение смещения опухоли за счет сокращения времени сеанса лечения, уменьшение дозовой нагрузки на другие органы;
точность определения локализации опухоли обеспечивает максимально быстрое и точное проведение лучевой терапии.
Gated RapidArc позволяет использовать высокоточные методы лечения для многих видов опухолей, в том числе для опухолей легких, молочной железы, опухолей верхних отделов желудочно-кишечного тракта и др. локализаций с учетом их движения во время дыхания пациента.
Читайте также:

