Что такое радиочастотная абляция опухоли почек
Что такое абляция опухоли почки? Насколько абляция опухоли почки эффективна и безопасна? В каких случаях рекомендуется применять именно абляцию опухоли почки? В каких случаях противопоказана абляция опухоли почки? Каковы преимущества выполнения абляции опухоли почки в НКЦ Онкоурологии?
— Известно, что для лечения опухолей почек успешно применяются резекция опухоли почки или удаление почки. Что собой представляет абляция опухоли почки, какие у нее преимущества и недостатки?
— Давайте для начала определим цель той или иной операции. По сути, и удаление опухоли почки, и радикальное удаление самой почки вместе с новообразованием преследуют одну цель — избавить пациента от опухоли. А теперь давайте представим ситуацию, когда у человека выявлен рак почки, но, в силу разных причин, мы не можем его оперировать. Например, из–за сопутствующих заболеваний, не позволяющих дать наркоз. Или, скажем, у пациента опухоль единственной почки — ясно, что удалять эту почку нельзя. Всего несколько лет назад хирургу оставалось либо брать пациента на крайне рискованную операцию, либо развести руками — ничего сделать было нельзя. Сейчас нам в таких случаях приходит на помощь абляция опухоли почки.
Абляция опухоли почки — это разрушение ткани опухоли при помощи разных видов энергии: холодовой (криоабляция), тепловой (радиочастотная абляция) или ультразвуковой (HIFU).
Мы в НКЦ Онкоурологии применяем радиочастотную абляцию.
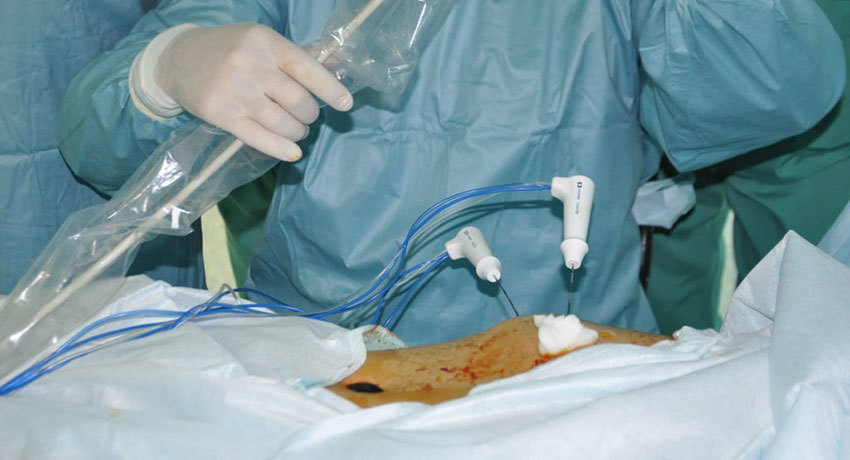
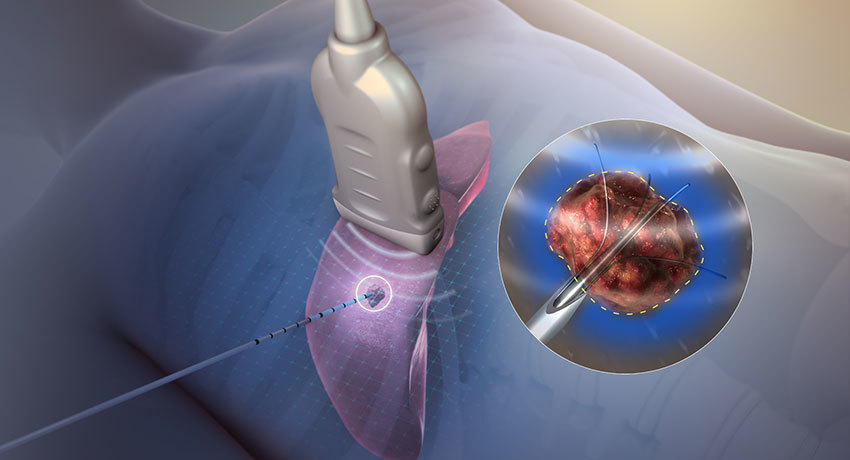
Данная методика предполагает введение специальной иглы–электрода (аблятора) в центр опухоли почки и нагревание до 90 градусов. Это позволяет, по сути, убивать опухоль вокруг электрода на расстоянии до см, не повреждая здоровую ткань почки. Для введения иглы–электрода мы применяем УЗИ аппарат экспертного класса BK–Medical, позволяющий очень точно позиционировать зону поражения опухоли. Тем самым, мы решаем задачу уничтожения новообразования почки без разреза и без большой хирургической агрессии.
Таким образом, среди преимуществ абляции почки мы можем выделить минимальную травму, возможность ее применения у пациентов с противопоказаниями к стандартным операциям, у пациентов с единственной почкой.
— А насколько абляция опухоли почки эффективна? Ведь если нет противопоказаний, то предпочтение отдается стандартной операции.
— Абляция опухоли почки — сравнительно новая методика лечения. На сегодняшний день Европейская Ассоциация Урологии рекомендует применять абляцию лишь в случаях, когда радикальная операция невозможна: в силу возраста, сопутствующих заболеваний, наличия опухолей обеих почек, наличие опухоли единственной почки. Важно понимать, что абляция опухоли почки является менее радикальным способом, чем операция. Между тем, согласно опять же данным европейских исследователей, этот способ довольно часто позволяет добиться безрецидивной выживаемости, иначе говоря, позволяет победить опухоль. Безопасность абляции опухоли почки, отсутствие травмы доступа, короткое время наркоза или вовсе — отсутствие последнего — вот преимущества, позволяющие нам предлагать данную методику для лечения рака почки.
— В каких случаях противопоказана абляция опухоли почки?
— Существуют два противопоказания к проведению абляции почки: во–первых, это крайне тяжелое состояние пациента, например, сепсис, во–вторых — это тяжелые нарушения свертывающей системы крови (коагулопатии).
— Каковы преимущества выполнения абляции опухоли почки в НКЦ Онкоурологии?
— Создавая Научно–клинический центр Онкоурологии, мы ставили перед собой задачу междисциплинарного подхода к лечению любого пациента. По поводу каждого пациента мы собираем консилиум ведущих специалистов, где обсуждаем возможности как хирургического или терапевтического лечения, так и вопросы дальнейшего активного наблюдения за пациентом. Думаю, нелишне отметить опыт абляционной хирургии (как опухолей почек, так и метастазов печени), накопленный в НКЦ Онкоурологии, оборудование последнего поколения, возможность провести как пункционную, так и лапароскопическую абляцию опухоли почки.
- English
- Русский







































Главное меню
- Редакционная коллегия
- Редакционный совет журнала
- Архив
- База авторов
- Порядок рецензирования статей
- Информация для авторов
- Информация для рекламодателей
- Издательский дом
- Политика редакции
- Обратная связь
Главное меню
- Редакционная коллегия
- Редакционный совет журнала
- Архив
- База авторов
- Порядок рецензирования статей
- Информация для авторов
- Информация для рекламодателей
- Издательский дом
- Политика редакции
- Обратная связь
В мире рак почки (РП) составляет 2-3% в структуре всех злокачественных новообразований. Ежегодный прирост этого заболевания составляет до 6%. В странах Европейского союза в 2006 г. было выявлено больше 63 тыс. новых случаев рака почки, умерло 26 тыс. пациентов.
В структуре заболеваемости злокачественными новообразованиями населения России РП составляет 3,6%. Абсолютное число впервые в жизни диагностированного РП в России с 1998 по 2008 гг. выросло с 7 до 9 тыс. случаев. Прирост больных РП на 100 тыс. населения также с 1998 по 2008 гг. составил: среднегодовой – 3,5%, общий прирост – 41%. Сейчас РП занимает первое место среди всех злокачественных заболеваний (И. Чиссов, 2008).
Место малоинвазивных методов при опухолях почек
Методика выполнения РЧА опухолей почки
Абляция – это методика прямого направленного разрушения тканей, которая достигается путем термического либо химического/ электрохимического воздействия. К термической абляции относятся: лазерная, микроволновая, радиочастотная, ультразвуковая и криодеструкция. Химическая (электрохимическая) абляция ассоциирована с инъекциями этанола, уксусной кислоты, электрохимическим лизисом.
Преимуществами абляции является малая инвазивность, сравнительно недорогое оборудование, хороший объективный терапевтический эффект, малый койко-день
и практически отсутствие противопоказаний.
Показаниями к проведению данной методики являются небольшой размер опухоли до 5 см, рак единственной почки при невозможности ее резекции, билатеральный рак и сопутствующая патология, которая является противопоказанием к проведению радикального лечения.
Опухоли почек могут располагаться по отношению к органу экзофитно, центрально и иметь смешанное расположение. Лучшие результаты РЧА получены при экзофитном расположении опухоли, когда более 25% диаметра опухоли находится в паранефральной клетчатке. Радиочастотная абляция выполняется чрескожным, лапароскопическим и лапаротомным доступами. Методика представляет собой введение атравматического электрода в опухоль и воздействие на последнюю током частотой 450-500 КГц. В результате опухолевая ткань разогревается до температуры 90оС, при которой происходят необратимые изменения в клетках, и ткань некротизируется.
Результаты РЧА
Безрецидивная выживаемость пациентов после абляции зависит от размеров опухоли. Чем меньше размеры опухоли, тем выше безрецидивная выживаемость.
Частота осложнений при чрескожной радиочастотной абляции почек, по литературным данным, составляет до 10%. Основными осложнениями являются: повреждение верхних мочевых путей с образованием урином, проксимальные стриктуры мочеточников; паранефральная или субкапсулярная гематома и травмы органов брюшной полости (Gervais D.A., 2005, Farrell M.A., 2005, Matsumoto E.D., 2005).
Опыт выполнения РЧА в РНЦРР Минздравсоцразвития РФ
В РНЦРР Минздравсоцразвития РФ в 2010 г. был создан внутренний протокол по лечению рака почки. При наличии противопоказаний к проведению хирургического лечения в объеме резекции почки или нефрэктомии, рекомендовано проведение минимально-инвазивного альтернативного лечения – радиочастотной абляции опухоли почки.
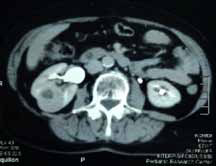
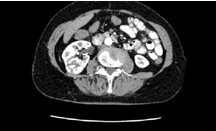
Рисунок 1. Результаты РЧА опухолей почек
По данным компьютерной томографии уменьшение размеров опухоли на 30% было отмечено у 55% больных и стабилизация размеров опухоли у 45% больных. При проведении нефросцинтиграфии объем функционирующей паренхимы почек у всех пациентов после проведения абляции уменьшался, а индекс интегрального захвата остался прежним у 16 больных и значительно уменьшился только у 4 больных, и, в среднем, составлял 78-89 единиц при норме от 92 до 140 единиц (рисунок 2).
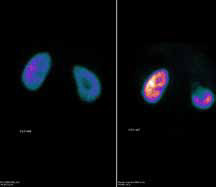
Рисунок 2. Результаты статической сцинтиграфии (данные РНЦРР)
В нашем центре были зафиксированы осложнения в виде ожога первой степени у 15 пациентов в месте введения датчиков, подкапсульная гематома была у 3 больных, однако, серьезных осложнений, потребовавших дополнительного лечения, не было. Время наблюдения за этими пациентами составляет не больше года, поэтому безрецидивная выживаемость пока у всех 100%, отдаленных результатов пока также нет.
Клинический пример
Пациент 1947 года рождения (рисунок 3).
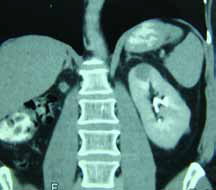
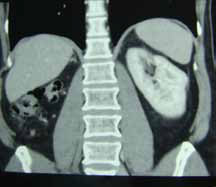
Рисунок 3. Клинический пример
Диагноз: Первично-множественный синхронный рак: 1. Рак правой почки T1NoMo, 2. Рак левой почки T1NoMo.
Опухоль правой почки занимала практически 2/3 всго органа, а в левой почке было два очага: один – 3 см, другой – 2 см. Первый очаг располагался в верхнем сегменте, второй в среднем сегменте левой почки.
Пациенту было проведено комплексное лечение: нефроэктомия справа – июнь 2010 г., РЧА – июль 2010 г. опухоли верхнего сегмента левой почки, РЧА – сентябрь 2010г опухоли среднего сегмента левой почки. В настоящее время данных
за рецидив и продолженный рост не выявлено.
Выводы
Данное наблюдение убедительно показывает, что эффективность метода радиочастотной абляции при лечении опухолей почек может быть достоверно высокой (Gervais D.A., 2005, Mahnken A.H., 2005). На частоту некрозов опухолей почек при радиочастотной абляции влияет локализация и размеры опухолевых узлов, способ навигации, количество аппликаций и личный опыт хирурга.
Ключевые слова: рак почки, радиочастотная термоабляция.
Keywords: kidney cancer, RFA.
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК - 2016
Общая информация
Приложение 1
к типовой структуре
Клинического протокола диагностики и лечения
Название оперативного и диагностического вмешательства: Радиочастотная абляция опухолей почек.
Лечение
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Цель проведения процедуры/вмешательства: целью радиочастотной абляции (РЧА) является полный некроз злокачественного новообразования почки (первичного и метастатического) с возможность длительной безрецидивной выживаемостью.
Радиочастотная абляция – это метод разрушения опухолевой ткани с помощью высокоэнергетических радиоволн, в процессе которого происходит нагревание клеток опухоли до высоких температур и, как следствие, их гибель. В настоящее время метод является достаточно эффективным и широко применяется в лечении рака почек. Радиочастотная абляция способствует как частичному, так и полному удалению опухоли.
Показания и противопоказания для проведения процедуры/ вмешательства:
Показания к проведению РЧА злокачественных опухолей почек:
Абсолютные:
· наличие противопоказаний к хирургической резекции, отказ в хирургическом лечении;
· наличие у больного единственной почки и высокий риск полной потери функции почки вследствие хирургического удаления почки;
· генетическая предрасположеность больных к развитию множественных опухолей (BHD,VHL);
· опухоль визуализируется при РКТ, УЗКТ;
· согласие больного на проведение РЧА.
Относительные:
· отсутствие внепочечных проявлений заболевания;
· размеры опухолевого узла меньше 5 см в диаметре.
Противопоказания к РЧА опухолей почек:
Абсолютные:
· некоррегируемая коагулопатия;
· сепсис;
· сосудистая инвазия.
Относительные:
· ожидаемая продолжительность жизни больше года;
· центральная локализация опухоли.
Перечень основных и дополнительных диагностических мероприятий (отдельно перечислить основные/обязательные и дополнительные обследования, консультации специалистов с указанием цели и показаний):
Основные (обязательные) диагностические обследования:
· ОАК с тромбоцитами;
· ОАМ;
· группа крови и резус-фактор;
· биохимический анализ крови: общий белок с фракциями, АЛТ, АСТ, общий/прямой билирубин, ЩФ, ГГТП, ЛДГ, креатинин, мочевина, амилаза, глюкоза;
· электролиты: калий, натрий;
· микрореакция;
· коагулограмма: протромбиновое время, МНО, АЧТВ, фибриноген;
· маркеры вирусных гепатитов: HBsAg, anti-HCV, ВИЧ;
· альфа-фетопротеин, специфические маркеры;
· УЗИ органов брюшной полости, почек;
· рентгенография органов грудной клетки;
· КТ/МРТ торако-абдоминального сегмента с контрастированием;
· биопсия до РЧА: морфологическое подтверждение злокачественного характера опухоли легкого является обязательным до ее термодеструкции. Биопсия может выполняться непосредственно перед РЧА, однако предпочтительнее проводить ее заранее, чтобы избежать возможных связанных с ней осложнений и сдвинуть сроки проведения РЧА. Кроме того, могут быть выявлены особенности при морфологическом исследовании, способные повлиять на тактику лечения.
Дополнительные диагностические обследования:
· anti-HAV, anti-HEV, anti-HDV IgG;
· у мужчин - РЭА, ПСА 19-9, у женщин - ХГЧ, СА-125;
· УЗИ периферических лимфатических узлов, ЭХОКГ,
· Сцинтиграфия/ ПЭТ/КТ для исключения отдаленных метастазов.
Требования к техническому оснащению:
· наличие всех инструментов/оборудования, необходимых для радиочастотной абляции -генератора, системы охлаждения.
· помещение должно быть оснащено системой вентиляции, обеспечивающей оптимальные условия для профилактики хирургической инфекции и работы с газами, используемыми при анестезии;
· наличие инструментов, расходных материалов и оборудования для проведения анестезиологического пособия. Инструменты и оборудование должны находиться непосредственно в операционной или смежных помещениях и быть доступны в любое время.
Требования к оснащению, расходным материалам, медикаментам:
· любая сертифицированная система для РЧА опухолей: одноигольчатые электроды с максимальным диаметром воздействия 3 см, выдвигающиеся электроды с максимальным диаметром воздействия 5см и др.;
· система лучевой навигации: РКТ, УЗИ, МРТ;
· анестезиологическое оборудование (аппарат для искусственной вентиляции легких, монитор для контроля сердечной деятельности, артериального давления, сатурации и др.);
· динамический контроль: КТ с внутривенным контрастным усилением, ПЭТ/КТ, МРТ с внутривенным контрастным усилением. Критерии оценки результатов: mRECIST, EASL.
Основные расходные материалы:
· набор белья для чреспочечных процедур;
· комплект кластерных или 1-3 одиночных электродов для РЧА;
· генератор;
· насос и система охлаждения;
· емкость для воды;
· ножной выключатель;
· ультразвуковой аппарат.
Дополнительные расходные материалы:
· система одноразовая для инфузий;
· скальпель одноразовый;
· марля медицинская;
· шприцы 20 мл;
· шприцы 10 мл;
· перчатки стерильные;
· перчатки нестерильные;
· шапочки одноразовые;
· маски хирургические;
· бахилы одноразовые;
· одноразовые электроды для ЭКГ.
Требования к подготовке пациента:
· вечером накануне операции легкий ужин до 20.00;
· в день операции – голод;
· побрить операционное поле накануне операции;
· провести перед операцией все гигиенические процедуры: прополоскать полость рта, почистить зубы, снять съемные зубные протезы, очистить полость носа, мужчинам побриться;
· обработка операционного поля препаратами бактерицидного действия;
Индикаторы эффективности процедуры/вмешательства:
· отсутствие/уменьшение;
· отсутствие послеоперационных осложнений (осложнений, связанных с доступом и процедурой);
· послеоперационной летальности;
отсутствие в послеоперационный период выявляемого всеми доступными визуализационными методами роста резидуальных опухолевых очагов в зоне выполненной абляции.
Информация
Указание на отсутствие конфликта интересов: нет.
Указание условий пересмотра протокола: пересмотр протокола через 3 года и/или при появлении новых методов диагностики/лечения с более высоким уровнем доказательности.
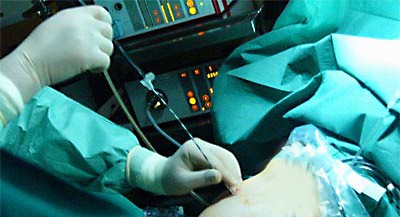
Не для кого не секрет, что в настоящее время малоивазивные методы хирургического лечения представляют немалый интерес как для специалистов так и для пациентов. К одному из множества подобных методов малоинвазиных вмешательств относится и радиочастотная термоаблация (РЧА). В мире эту методику аблации для лечения новообразований применяют уже в течении двадцати лет. Первооткрывателем этого метода является французский ученый Де. Арсонваль, который в конце ХIХ века впервые открыл явление нагревания живых тканей радиочастотной энергией.
Уже около 30 лет метод РЧА с успехом применяется в хирургии и кардиологии.
В этой статье мы постараемся подробнее остановится на применение радиочастотной термоаблации в урологии, при опухолях почки. Механизме воздействия РЧА заключается в распространении электродом колеблющихся движений ионов на расстояние 5 см, в результате чего температура на этом участке поднимается до 100 градусов, что в конечном итоге приводит к биологическому разрушению опухолевых тканей.
Во время операции непосредственно в опухоль устанавливают электрод. Разрушение ткани опухоли происходит благодаря работе генератора, который в свою очередь производит высокочастотный переменный ток. Под действием высокой температуры достигающей 70-100 градусов опухолевые клетки погибают в течении нескольких минут, а на их месте образуется соединительнотканный рубец.
Вместе с коагуляцией ткани новообразования, при термоалации происходит тромбоз микроциркуляторного русла в зоне воздействия. Глубина коагуляции ограничивается неравномерным нагревом ткани. Размер зоны некроза зависит от процесса теплоотдачи на периферии очага, которая происходит за счет циркуляции крови. В свою очередь крупные сосуды диаметром более 3 мм будут препятствовать полному некрозу ткани, так как в электрод будет омываться током крови при этом не набирая необходимой для коагуляции температуры. При необходимости во время манипуляции всегда овзможно увеличение зоны коагуляционного некроза, что достигается путем использования многозубцовых электродов, использованием прерывистого режима работы генератора, внутренним охлаждением электрода и временным прекращением почечного кровотока.
Радиочастотная аблация при опухолях почки может выполняться тремя доступами чрескожным, открытым и лапароскопическим.
Метод радиочастотной термоабляции в РНПЦ онкологии и медрадиологии применяют уже около 6 лет, использовали этот метод в первую очередь для лечения больных раком печени и легкого. Исследование длилось около 5 лет, за время этого исследования пролечено более 50 человек. Метод оказался эффективным при опухолях указанных выше органов, в результате начат теперь уже новой эксперимент, но уже с другим видом опухоли и органом.
Метод РЧА безусловно очень перспективный, применяющийся в настоящее время не в одном направлении медицины. В онкоурологии, в частности при опухолях почки происходит зарождение революционно нового метода борьбы с опухолями почки, являющегося многообещающей альтернативой открытым операциям в частности резекции почки. Одно в настоящее время можно сказать точно, необходимо накопления большей базы пролеченных радичастотной термоаблацией пациентов, для достижения более достоверных результатов и заключений. Мы в свою очередь постараемся отслеживать все последние новости связанные с этим напралением лечения в онкоурологии.
Резюме. Радиочастотная абляция небольших опухолей почки у пациентов с сопутствующей патологией. Польский опыт

Радиочастотная абляция (РЧА) — минимально инвазивный метод, использующий чрескожную пункционную технику, ставший наиболее эффективным для лечения рака почки на начальных стадиях. Развитие визуализирующих технологий в последние годы позволило выявлять опухоли почки на ранних стадиях, в том числе у пациентов пожилого и преклонного возраста и групп высокого риска. В такой ситуации частичная нефрэктомия (нефронщадящая хирургия) рассматривается как стандарт лечения при опухолях T1a, N0. Традиционное хирургическое вмешательство в данной ситуации имеет относительные противопоказания, обусловленные высоким риском периоперационных осложнений на фоне сопутствующей патологии. Развитие малоинвазивных технологий позволяет по-иному решать хирургические проблемы, которые недавно являлись неразрешимыми. Целью настоящего сообщения было представить опыт лечения больных раком почки на начальных стадиях с использованием РЧА у пациентов группы повышенного риска и с сопутствующей патологией.
В 2006–2012 гг. в Онкологическом центре Быдгоща проведено 103 чрескожных РЧА под ультразвуковым контролем у пациентов с нераспространенным раком почки T1a, N0. Средний возраст пациентов составил 68,6 года (51–89 лет). При этом у всех наблюдалась высокая коморбидность, что исключало выполнение обычного оперативного вмешательства. Все они относились к группе операционного риска ASA ≥3 (29 пациентов с оценкой ASA 4 и 74 — с ASA 3). Размер опухоли составлял ≤4 см (в среднем 27,2±12,7 мм). Диагноз подтвержден при комп’ютерной томографии брюшной полости с одномоментной биопсией. Явление клеточной карциномы было доминирующей патологией — 98 случаев, 3 случая хромофобного и 2 — сосочкового рака. Среднее время наблюдения составляло 46 мес.
Как сообщается в статье, общая выживаемость на протяжении 1 года, 3 и 5 лет составила соответственно 97; 90 и 75%. Семнадцать пациентов умерли в течение 5 лет после процедуры. При этом пролонгации заболевания как причины смерти не установлено. Причинами летального исхода были: респираторная недостаточность — 7, инфаркт миокарда — 2, инсульт — 2, другое новообразование (не почки) — 2, иные причины — 4. Ранней послеоперационной летальности и развития госпитальных осложнений по классификации Clavien — Dindo ≥3 не отмечалось. Длительность госпитализации в связи с минимальной травматичностью оперативного лечения составила в среднем 2 дня. При этом рецидива опухоли и смертности от прогрессирования онкопроцесса не наблюдалось, и специфическая выживаемость в отношении рака составляла 100%.
В заключение статьи авторы подчеркивают, что РЧА, выполняемая чрескожно, является минимально инвазивным методом лечения и может применяться у пациентов, имеющих высокий риск оперативного вмешательства из-за сопутствующей патологии.
РЧА может быть рекомендована для удаления опухолей почки небольших размеров при высоком прогнозируемом риске неблагоприятного исхода от прочих (не онкологических) событий с гарантированной эффективностью.
Александр Осадчий
- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
Применение радиочастотной абляции для лечения нарушений ритма сердца началось только в годах. Первые же публикации относительно объема коагулируемой ткани в печени относятся к началу годов ХХ века.
В годах опубликованы и другие экспериментальные данные о применении радиочастотной абляции печени. В середине годов ХХ века появились первые сообщения о паллиативном лечении метастатического поражения печени с использованием радиочастотной абляции. А вскоре и лечения опухолей легких и почек.
В настоящее время в России не более 10 центров, занимающихся проблемой лечения метастатического рака печени. В основном они располагаются в крупных городах, областных центрах с сильной медицинской школой — Москве, , Новосибирске, Томске. Таким образом, потребность в данной высокотехнологичной медицинской помощи удовлетворяется не более чем на 15%. Другой проблемой, сдерживающей развитие данной методики, является дороговизна аппаратного обеспечения. Так, стоимость одноразового набора для радиочастотной абляции составляет до 1000 долларов США, стоимость одного сеанса криоабляции может составлять до 5000 долларов США.
Методика термоабляции новообразований (физические основы абляции тканей)
Основным элементом электрохирургической системы является электрогенератор. Высокочастотный ток передается на электроды. Аппарат нагревает прилегающие к электроду мягкие ткани высокочастотным током специальной формы. В процессе разогрева с периодичностью 2 мс контролируется импеданс тканей. Высокочастотный ток может подаваться однократно или циклически в течение заданного времени. При однократной подаче высокочастотный ток разогревает прилегающие к электроду ткани до температуры (95–110 С) и в момент полного высушивания тканей подача тока автоматически прекращается. При циклической подаче аппарат в течение установленного времени повторяет следующие циклы: подача высокочастотного тока до разогрева (95–110 С) и полного высушивания тканей, выдержка паузы для увлажнения (уменьшения импеданса), возобновление подачи высокочастотного тока. Циклический процесс подачи тока, разогрева и высушивания, повторяющийся многократно, позволяет поддерживать высокую температуру в зоне абляции длительное время и достигать большого объёма коагулированной ткани.
Форма и объём зоны абляции зависят от выбранного электрода и режима работы. Зона абляции делится на три области по степени поражения ткани:
- ближе к электроду расположена область высушивания (дессикации) мягких тканей;
- далее располагается область коагуляции мягких тканей;
- область девитализации располагается вокруг зоны коагуляции.
При увеличении длительности (экспозиции) процедуры абляции общая зона абляции растёт незначительно, однако область дессикации увеличивается.
Показания и противопоказания
Абляцию опухолей применяют в тех случаях, когда невозможно выполнить радикальное оперативное лечение. Это может быть неоперабельность первичной опухоли или сопутствующая патология, которая делает невозможным выполнение радикальной операции в силу её объема и тяжести, но не препятствует выполнению абляции.
Согласно национальным рекомендациям, имеются следующие показания и противопоказания к радиочастотной абляции опухолей печени:
При чрескожном доступе:
- Предшествующее радикальное хирургическое лечение первичной опухоли;
- Отсутствие внепеченочных проявлений заболевания (при колоректальных метастазах);
- Наличие в печени 5 и менее опухолевых узлов (при метастазах нейроэндокринного рака допускается большее количество узлов);
- Диаметр узлов не более 5 см каждый (допустимо подвергать воздействию узлы исходно большего диаметра, но регрессировавшие в объеме под воздействием химиотерапии и других методов лечения);
- Остаточная опухоль после ранее проведенной РЧА либо другого метода лечения;
- Местный рецидив после ранее проведенной РЧА, резекции печени либо другого метода лечения;
- Метахронные метастазы после ранее проведенной РЧА, резекции печени либо другого метода лечения.
Показания к проведению РЧА лапароскопическим доступом:
- Отсутствие выраженных сращений;
- Отсутствие стандартных противопоказаний для всех лапароскопических вмешательств;
- Расположение очага в зонах, доступных лапароскопии;
- Подкапсульное расположение с возможным прилежанием к органам, которые в ходе вмешательства возможно отведением обезопасить от термического воздействия;
- При билобарном поражении печени наличие единичных небольших (до 5 см) узлов в правой доле, в то время как образование левой доли может быть удалено лапароскопически.
Показания к проведению РЧА в ходе открытого вмешательства:
- Билобарное поражение, при котором возможно удалить большую часть пораженной печени и подвергнуть РЧА остающиеся очаги;
- Прилежание к органам брюшной полости и забрюшинного пространства, магистральным сосудам и диафрагме, когда возможно отделение (резекция) этих участков;
- Заранее планируемое сочетанное вмешательство;
- Выраженные сращения, процесс в брюшной полости, особенно после ранее произведенных операциях на печени, когда патологический очаг расположен непосредственно по краю резекции;
- Наличие кроме внутрипеченочного еще и экстраорганного, но удалимого опухолевого узла; общее операбельное состояние пациента; согласие больного на выполнение данного вида лечения.
Противопоказания к проведению РЧА:
Показания к проведению радиочастотной абляции опухолей легких (по Herrera L.J. et al.):
- Больные НМКРЛст., не подлежащие хирургическому лечению по следующим причинам: сопутствующие заболевания, отказ пациента от хирургического лечения.
- Больные, имеющие несколько метастазов в разных долях легких.
- Рецидив опухоли менее чем через 6 месяцев после резекции легкого.
- Диаметр опухоли до 4 см.
- Согласие больного на проведение лечения.
Противопоказания к проведению гипертермической абляции опухолей печени (по et al.):
- Расположение опухоли ближе 3 см от прикорневых структур.
- Первичная опухоль не удалена.
- Более 3 метастазов в каждом легком.
- Общее количество метастазов более 5.
- Имеется метастатический плеврит.
Показания к абляции первичного рака почки:
- Пациентов с тяжелой сопутствующей патологией, либо отказавшихся от хирургического лечения.
- Наличие опухолевого узла до 5 см в диаметре (лучшие результаты при РЧА экзофитно расположенных опухолей до 3 см в диаметре).
- Опухоль единственной почки.
Выполнение РЧА чрескожным или лапароскопическим доступом требует соблюдения ряда условий:
При чрескожном доступе:
- Четкая визуализация патологических очагов при УЗИ и КТ/МРТ (в зависимости от способа навигации);
- Возможность достаточно безопасного доступа к опухолевому узлу (достаточная отдаленность от магистральных печеночных сосудов и желчных протоков);
- Отсутствие прорастания (тесного контакта) диафрагмы, почки, желудка, кишки, желчного пузыря;
- Невозможность выполнения оперативного вмешательства в силу соматического состояния;
- Полная обеспеченность возможности экстренной лапаротомии и адекватности традиционного вмешательства;
- Согласие больного на выполнение данного вида лечения;
При лапароскопическом доступе:
- возможность обеспечения достаточно полноценного со стороны брюшной полости;
- полная обеспеченность возможности экстренной лапаротомии и адекватности традиционного вмешательства;
- согласие больного на выполнение данного вида лечения.
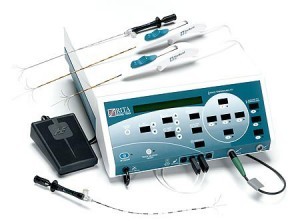
Используемое оборудование и инструментарий
В настоящее время на рынке имеется множество приспособлений для выполнения радиочастотной абляции тканей. Пожалуй, наиболее известным является аппарат Radionics ® Ablation System и набор водоохлаждаемых электродов RITA ® Medical Systems (Angiodynamics, США).
Эта система комплектуется тремя моделями многозубцовых электродов:
Доступы для проведения процедуры абляции
На сегодняшний день нет единого мнения о выборе доступа для проведения абляции. Для позиционирования электрода используется чреcкожный доступ под УЗИ, КТ- или . И интраоперационные доступы при лапаротомии под УЗИ наведением и чреcкожный доступ под контролем лапароскопии.
Методики РЧА
Наиболее часто прибегают к чреcкожным методам позиционирования электрода. В качестве метода контроля над движением электрода наиболее часто используется ультразвуковая навигация.
Преимущества ультразвуковых методов заключаются в простоте проведения процедуры, отсутствии вредных воздействий на пациента в виде лучевой нагрузки, контроль над происходящими процессами в реальном времени, возможность визуализации сосудистых структур органа, а также наличие направляющих адаптеров на рукоятке ультразвукового датчика.
При выборе направления движения электрода необходимо учитывать расстояние от кожи до места проведения абляции, наличие на пути электрода полых органов, таких как кишка, желудок, желчный пузырь, крупных сосудов, синусов плевры.
Также необходимо учесть угол, под которым будет осуществляться ультразвуковой контроль, дыхательную экскурсию, что особенно важно при поддиафрагмальном расположении опухолевых узлов. Немаловажным является и расположение опухолевых узлов относительно правой или левой долей печени. Так, при расположении опухоли в левой доли печени наиболее целесообразным будет выбор эпигастральной области в качестве места проведения электрода.
При локализации опухолевого узла в правых сегментах печени более целесообразным представляется установка электродов в межреберьях. В этих случаях необходима четкая визуализация расположения плеврального синуса.
В целом выбор области для проведения чрескожной абляции аналогичен таковому при проведении пункционных биопсий очаговых образований печени.
В ряде случаев выполнение абляции под ультразвуковым наведением может оказаться затруднительным или даже невозможным. Это может быть связано с изоэхогенной структурой опухоли, когда выполнить её четкую визуализацию не представляется возможным, наличием выраженной гиперэхогенной зоны при неоднократном проведении процедуры абляции, а также наличием костей или заполненных газами полых органов на предполагаемом пути установки электрода. В таких случаях для позиционирования электрода можно воспользоваться компьютерной томографией.
Выделяются 5 этапов абляции:
- Планирование;
- Прицеливание;
- Мониторинг;
- Контроль эффективности;
- Оценка эффективности.
Сначала определяют точку введения электрода путем размещения пациента на столе в наиболее удобном для доступа к опухоли положении, установки стола на уровне среза, выбранного для доступа, и маркировки точки введения электрода.
После установки электрода и его продвижения производят контроль его положения путем последовательного сканирования, при этом дистальная тень позволяет контролировать положение кончика электрода.
В тех случаях, когда опухоль не визуализируется ни при УЗИ, ни при КТ без контрастного усиления, можно выполнить предварительную жировую эмболизацию.
Преимуществом МРТ перед КТ является отсутствие ионизирующего излучения, хорошая контрастность мягких тканей, возможность мультипланарной реконструкции, возможность отображать функциональность и температуру ткани.
Лапаротомия или торакотомия, которые выполняют для проведения абляции, имеют ряд преимуществ по сравнению с чрескожными методами. К ним относятся возможность интраоперационной ревизии органов, выполнение ИОУЗИ печени, уточнение распространения опухоли, стадии онкологического процесса, выявления необнаруженных на дооперационном этапе отсевов опухоли.
Кроме того, возможно выполнить освобождение предполагаемой области вмешательства от прилегающих петель кишки, выполнить абляцию на участках, прилегающих к желчному пузырю, куполу диафрагмы, сосудам.
Читайте также:





