Что такое бф в онкологии
Онкологические заболевания в современном мире встречаются все чаще. Это связано с особенностями экологии, множеством новых вирусов, а также с большим количеством канцерогенов. Ежегодно ученые вводят новые методы борьбы с раком. Однако прежние способы лечения применяются до сих пор. Одним из них является ПХТ. Расшифровка этой аббревиатуры – полихимиотерапия. Системное введение цитостатических препаратов помогает устранить атипичные клетки, из которых состоит опухоль. Несмотря на то что данный вид лечения нелегко переносится пациентами, он является одним из самых эффективных методов.
ПХТ в онкологии: расшифровка аббревиатуры
В медицинской документации людей, страдающих от раковых заболеваний, часто встречается такое понятие, как химиотерапия. Сокращенно ее называют ПХТ. В онкологии расшифровка данной аббревиатуры - полихимиотерапия, что означает сочетанное воздействие сразу нескольких цитостатических средств. Данный вид лечения направлен на полное устранение опухоли или ее уменьшение.
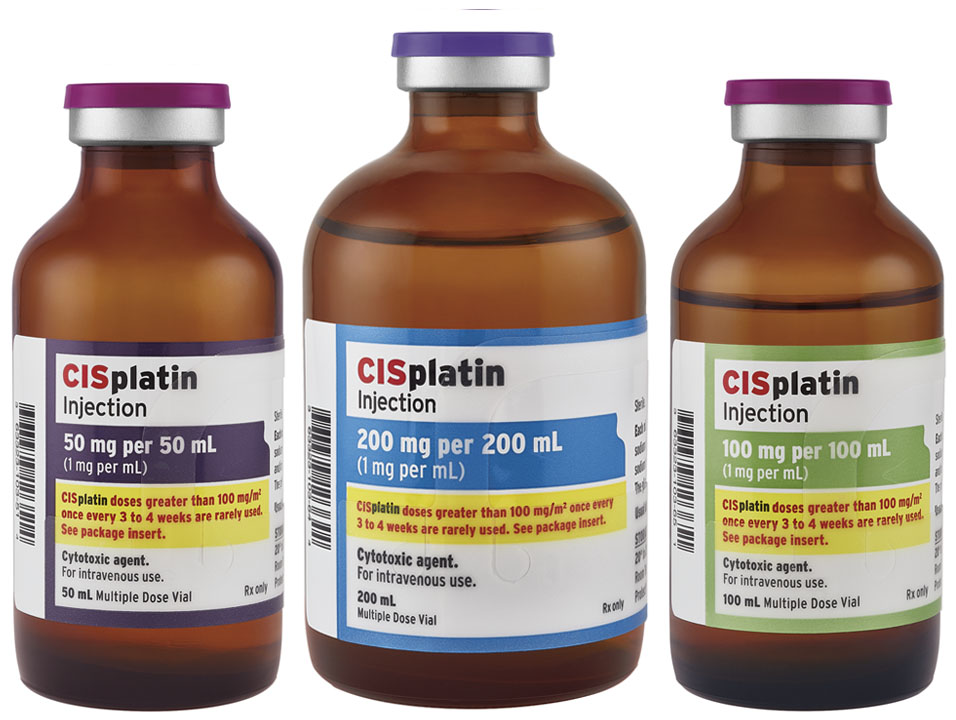
В большинстве случаев ПХТ сочетают с другими методами лечения. Среди них – хирургическое удаление патологического образования и лучевая терапия. Иногда полихимиотерапия является самостоятельным методом лечения. Выбор ПХТ зависит от расположения и стадии рака, а также от состояния больного. Назначать цитостатические препараты может только врач-онколог.
Виды химиотерапии в онкологии

Противоположным понятием является адъювантная ПХТ в онкологии. Расшифровка аббревиатуры проста. АПХТ – это профилактическое лечение рака после операции. Имеется в виду, что саму опухоль полностью удалили, однако для предотвращения рецидива требуется цитостатическая терапия. Перечисленные виды ПХТ относятся к комбинированному или комплексному лечению злокачественных опухолей. То есть, помимо назначения препаратов, пациенту проводится операция, а иногда – и облучение.
Отдельным видом терапии является самостоятельный (лечебный) курс ПХТ в онкологии. Расшифровка подобного медицинского термина понятна не каждому врачу. Зачастую отличить лечебный курс от профилактической терапии может только онколог. Самостоятельная ПХТ проводится в тех случаях, когда другие методы оздоровления не показаны. Например, при мелкоклеточном раке легкого или наличии метастазов в отдаленные органы.
Показания к проведению терапии
Стоит отметить, что каждая злокачественная опухоль лечится по-разному. Иногда достаточно только оперативного лечения или облучения, в других случаях – требуется химиотерапия. ПХТ назначают лишь по специальным медицинским показаниям, когда это необходимо. Если подобное лечение не было предложено после операции врачом, значит злокачественный процесс был ограничен небольшим участком и не поразил глубокие слои органа. Кроме того, некоторые типы опухолей не поддаются химиотерапии. Выделяют следующие показания для ПХТ в онкологии:
- Злокачественные образования лимфоидной ткани.
- Рак крови.
- Опухоли пищеварительного тракта.
- Мелко- и крупноклеточный рак легкого.
- Новообразования головы и шеи.
Следует отметить, что эффективность химиотерапии зависит от гистологического типа опухоли. К примеру, железистый рак поддается цитостатическому лечению лучше, чем плоскоклеточная карцинома или саркома. Зачастую ПХТ не назначают на первых стадиях болезни, если опухоль можно удалить оперативным путем. Адъювантная терапия показана пациентам, у которых после хирургического лечения была обнаружена 2 или 3 стадия рака. Если опухоль имеет большой размер и проросла в соседние органы, назначают самостоятельный курс ПХТ. Иногда данный вид лечения применяется на поздней стадии рака, когда другие методы бессильны.
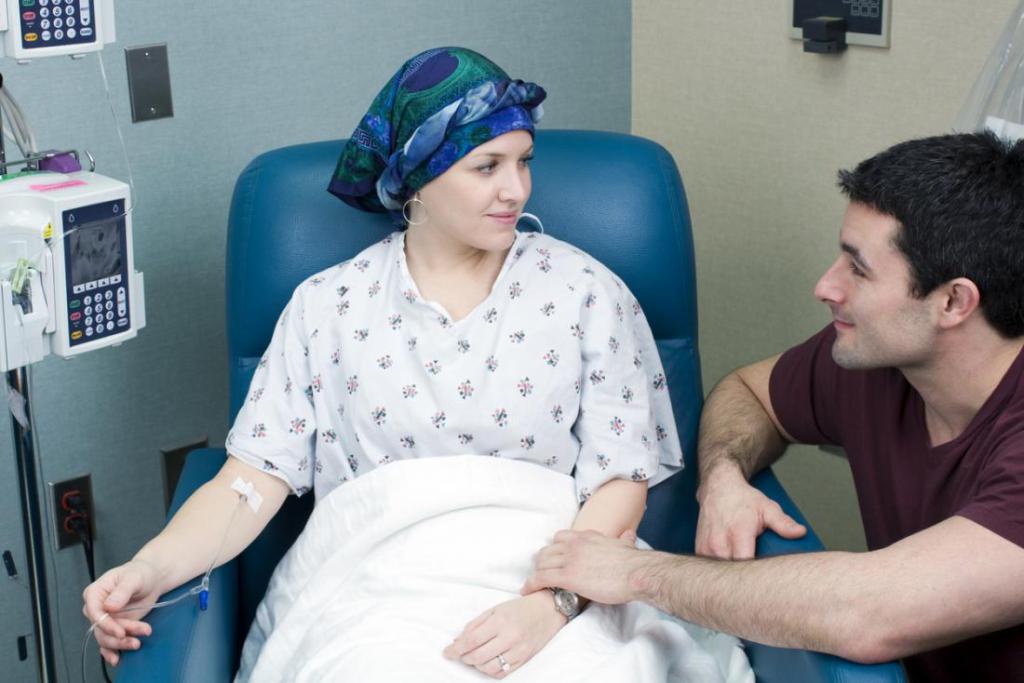
Что такое курс химиотерапии?
Большинство людей знает, что химиотерапию принято назначать курсами. Это означает, что цитостатические средства вводятся в организм неоднократно, а на протяжении длительного времени - с определенными промежутками. Подобная схема лечения необходима, потому что препараты разрушают не только саму опухоль, но и другие клетки организма. Введение большой дозы единовременно невозможно, так как цитостатики обладают кардио-, нефро- и гепатотоксичным действием. Чтобы организм восстановился после курса ПХТ, требуется время. В среднем это занимает 2-4 недели. За этот период клетки крови успевают обновиться, и общее самочувствие пациента приходит в норму.
Количество курсов ПХТ в онкологии может быть различным. Оно зависит от переносимости препаратов, состояния больного и эффективности лечения. После 3 курсов проводится обследование, благодаря которому врач делает соответствующее заключение. Если опухоль полностью исчезла или частично уменьшилась, химиотерапию продолжают. В случаях, когда имеется прогрессирование злокачественного процесса, схему ПХТ меняют. При этом отсчет курсов начинается заново.
Подготовка и сопроводительная терапия
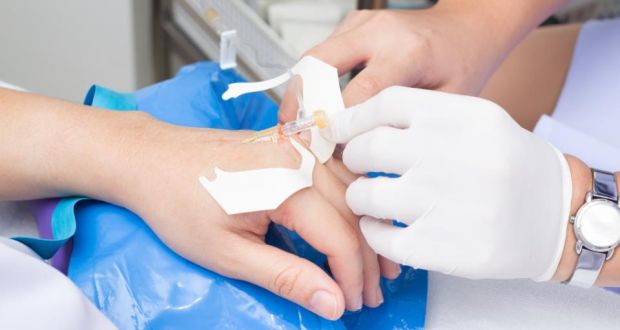
Противопоказания к назначению химиотерапии
Несмотря на то что химиотерапия относится к одним из самых эффективных методов лечения рака, ее проведение не всегда необходимо. В некоторых случаях цитостатические средства приносят больше вреда, чем пользы. Проведение ПХТ противопоказано в следующих случаях:
- Старческий возраст (от 70 лет).
- Непереносимость цитостатических средств.
- Наличие тяжелых патологий со стороны сердца.
- Почечная и печеночная недостаточность.
- Прогрессирование заболевания, несмотря на проводимую терапию.
- Наличие множественных метастазов.
- Кахексия.
Перед тем как назначить ПХТ, проводится комплекс обследований. К ним относятся: общий и биохимический анализ крови, ЭКГ, ОАМ, коагулограмма, УЗИ сердца. При выявлении декомпенсированных заболеваний лечение цитостатиками нецелесообразно.
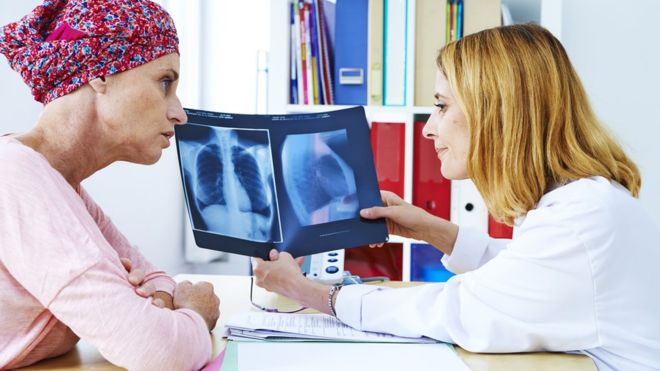
Возможные результаты химиотерапии
Для контроля эффективности ПХТ проводится повторное обследование. Благодаря этому оценивается результат терапии. К благоприятным исходам лечения относятся: полный и частичный регресс опухоли, а также стабилизация. В первом случае новообразование исчезает или уменьшается в размере в 2 раза и более. Стабилизация процесса означает, что опухоль осталась прежней. Однако это расценивается как положительный результат, ведь без лечения рак быстро прогрессирует.
Если при обследовании выявлено, что злокачественное образование растет, или появились метастазы, схему лечения меняют. При удовлетворительном состоянии пациента количество курсов химиотерапии неограниченно. Однако постоянное прогрессирование служит показателем того, что лечение не приносит результата, а только вредит организму. Это служит противопоказанием для назначения ПХТ.

Список лекарственных средств
Злокачественные опухоли часто приводят к поражению костей. Как правило, речь идет о метастазах — отсеве опухолевых клеток из места первичной локализации и распространении их по всему организму с возникновением новых очагов.
- Бисфосфонаты при поражении костей
- Классификация бисфосфонатов
- Применение бисфосфонатов при костных метастазах
- Применение бисфосфонатов при остеопорозе
- Гиперкальциемия и бисфосфонаты
- Побочные эффекты от применения бисфосфонатов
Чаще всего в кости метастазирует рак молочной железы и простаты. Также костные метастазы могут быть при раке почки, щитовидной железы и злокачественных новообразованиях легкого. Наибольшее разрушение наблюдается при миеломной болезни. Для того чтобы понять, как метастазы действую на кости, сначала поговорим о здоровой костной ткани.
Костная ткань — это разновидность соединительной ткани. В течение всей жизни она подвергается циклическим изменениям — костеобразование сменяется резорбцией (разрушением костной ткани). Такой процесс называется ремоделированием. Оно проходит в несколько этапов:
Основным моментом при образовании костных метастазов служит нарушение процесса ремоделирования. Раковые клетки выделяют вещества, стимулирующие как остеокласты, так и остеобласты. Таким образом, происходит резорбция и одновременно с ней аномальный рост костной ткани.
Основными проявлениями метастазов в костях являются:
- Боль.
- Патологические переломы, которые возникают без серьезных механических нагрузок.
- Компрессия спинного мозга, которая может быть вызвана сдавлением нервных корешков опухолевыми массами или костными отломками, образовавшимися в результате патологического перелома.
- Гиперкальциемия — повышение уровня кальция в крови, при которой развивается комплекс патологических симптомов, например, интоксикация или нарушение системы свертывания крови. В ряде случаев гиперкальциемия может привести к летальному исходу.
Для лечения костных метастазов используется комплексный подход, включающий противоопухолевые методы воздействия, например, химиотерапию, таргетную терапию, облучение, паллиативные операции. В рамках патогенетического лечения применяются бисфосфонаты.
Бисфосфонаты при поражении костей
Бисфосфонаты — это препараты, влияющие на костный метаболизм. По химической структуре они сходны с природными неорганическими фосфатами. Обладают высоким сродством к ионам кальция, благодаря чему проникают вглубь костной ткани.
В основе механизма их действия лежит угнетение развития и жизнедеятельности остеокластов, которое реализуется сразу несколькими путями:
- Непосредственное влияние на остеокласты, благодаря чему те утрачивают свою способность резорбировать костную ткань, или даже погибают.
- Действуют на клетки-предшественницы остеокластов, препятствуя их развитию и дифференцировке.
- Оказывают влияние на остеобласты, из-за чего снижается продукция остеокласт-стимулирующего фактора.
Помимо этого, есть данные о том, что бисфосфонаты снижают объем опухоли. Почему так происходит, до конца не ясно. Предполагается, что за-за снижения резорбции, опухоль не получает достаточного количество факторов роста и цитокинов, которые содержатся в костной ткани.
Классификация бисфосфонатов
В лечебной практике применяется 8 бисфосфонатных соединений, которые в зависимости от химического строения делят на три группы:
- Безазотные бисфосфонаты. Это препараты первого поколения. Сюда относят клодронат, тилудронат и этидронат.
- Азотсодержащие бисфосфонаты. Это препараты второго поколения. Сюда входят памидронат, ризедронат и алендронат.
- И, наконец, препараты последнего, третьего поколения. Они являются аминосодержащими бисфосфонатами. К ним относятся золедроновая кислота и ибандронат.
Клодронат относится к бисфосфонатам первой генерации. Он выпускается в форме для перорального употребления, а также для внутривенных инфузий. Недостатком перорального приема является плохая абсорбция из желудка.
Памидронат — это препарат второго поколения бисфосфонатов. Отличается от первого тем, что имеет в формуле один атом азота. Благодаря этому, он может подавлять процесс перестройки белков в остеокластах, что в конечном итоге приводит к их гибели путем апоптоза. Этот препарат используется для лечения остеолитических метастазов, которые характерны для множественной миеломы и рака молочной железы.
Проблема его использования заключается в том, что максимальная эффективность в лечении гиперкальциемии требует назначения высоких доз препарата. Однако это сопровождается высокими рисками токсических эффектов со стороны пищеварительной системы. Кроме того, эффективность паминдроната снижается у больных с циркуляцией в крови PTHrP (белок, который образуется при остеолизисе)
Памидронат вводится путем внутривенных инфузий. Разовая доза составляет 60-90 мг. Продолжительность инфузии — 4 часа. Препарат применяют раз в три недели.
Ибандронат относится к третьему поколению бисфосфонатов и содержит уже 2 молекулы азота. Он обладает большей эффективностью у больных с повышенным содержанием PTHrP, вызывает меньше осложнений, на обладает нефротоксичностью. Применяется он 1 раз в 4 недели в виде 15-минутных внутривенных инфузий.
Золедроновая кислота относится к препаратам третьего поколения. Она содержит 2 атома азота, располагающихся в противоположных позициях. Такая особенность строения позволяет ей оказывать не только антиостеолитический эффект, но и негативно влиять на саму злокачественную опухоль. В частности, золедроновая кислота обладает антиангиогенным эффектом, препятствуя росту клеток эндотелия, тем самым нарушается кровоснабжение новообразования, что приводит к сдерживанию его роста.
Препарат назначается внутривенно, в дозе 4 мг. Инфузия длится 15 минут. Кратность применения — раз в 3-4 недели. На период лечения необходимо принимать витамин Д и кальций, ввиду риска транзиторной гипокальциемии.
Применение бисфосфонатов при костных метастазах
Применение бисфосфонатов при метастазах в костях стало золотым стандартом лечения. Такие препараты эффективны около 2-3 лет, и после развития резистентности их меняют на таргетную терапию деносумабом.
К лечению приступают после определения метастазов в костях с помощью рентгенологических исследований. Сцинтиграфия для выявления остеолитических метастазов не подходит.
Применение бисфосфонатов при остеопорозе
Остеопороз — это хроническое заболевание, для которого характерно снижение костной массы. В результате снижается плотность кости, повышаются риски патологических переломов. Такая патология больше характерна для женщин в период менопаузы, но встречаются и у пожилых мужчин.
Для лечения заболевания применяется комплексный подход, включающий специальную диету, лечебную физкультуру. Также применяется фармакотерапия у лиц с высокими рисками развития патологических переломов. Препараты предотвращают потерю костной массы, что было в клинических испытаниях. Наиболее эффективны в этом плане алендронат, золедроновая кислота и ризедроновая кислота.
Гиперкальциемия и бисфосфонаты
Еще относительно недавно гиперкальциемия (повышение уровня кальция в крови) было одним из наиболее часто встречающихся жизнеугрожающих осложнений костных метастазов. В конце ХХ века около 20% больных с метастатическим раком молочной железы походили через это состояние. Однако благодаря применению бисфосфонатов, частота таких осложнений существенно снизилась.
Выделяют два механизма развития гиперкальциемии:
- Первый основан на том, что костные метастазы приводят к остеолизису, при котором кальций из разрушенной костной ткани поступает в кровь. Этот путь реализуется при миеломной болезни и метастазах рака молочной железы.
- Второй механизм не связан с костными метастазами, а реализуется он за счет стимуляции резорбции кальция под действием паратгормон-подобных белков, которые могут секретироваться внекостными очагами опухоли.
Гиперкальциемия приводит к нарушению работы почек, из-за чего с мочой выделяется много жидкости. В результате возникает обезвоживание, еще больше ухудшается работа почек, кальций не выводится, и ситуация замыкается в порочный круг.
В клинической картине отмечаются следующие симптомы:
- Нарушения со стороны сердечно-сосудистой системы — снижение давления, аритмии и другие нарушения работы сердца.
- Нарушение со стороны ЖКТ — тошнота и рвота, потея аппетита, панкреатиты.
- Нарушение сознания, заторможенность, сопор и даже кома.
Основными моментами при лечении гиперкальциемии является восполнение жидкости, усиление выведение кальция и блокирование резорбции костной ткани под действием опухоли. Именно на последний момент направлено действие бисфосфонатов. В настоящее время их рекомендуют назначать всем пациентам с выявленными костными метастазами.
Побочные эффекты от применения бисфосфонатов
При лечении бисфосфонатами могут отмечаться следующие побочные реакции:
- Диспепсические явления — тошнота, боли в животе, метеоризм.
- Повышение температуры тела, сопровождающееся ломотой в мышцах.
- Транзиторная гипокальциемия — снижение уровня кальция в крови.
- Головные боли.
- Зуд кожи.
- Сыпь.
- Появление крови в моче.
Довольно редким, но вместе с тем тяжелым осложнением, является асептический остеонекроз челюсти. Чаще всего он возникает после стоматологических манипуляций. В этой связи рекомендуется отсрочка начала лечения бисфосфонатами до санации полости рта и заживления ее слизистой.
Паллиативная химиотерапия (ПХТ)

Радикальные методы лечения поздней стадии онкологического заболевания не всегда бывают доступны. В этом случае врачи часто назначают медикаментозную терапию в виде паллиативной химиотерапии (ПХТ). Такое лечение не устраняет причину заболевания, но позволяет значительно облегчить состояние пациента. Разработаны различные схемы ПХТ, необходимые для терапии определенных форм злокачественных новообразований. Консультация онколога может пациенту получить больше информации о таком лечении.
Химиотерапией называют основной медикаментозный метод лечения злокачественных новообразований, основанный на применении противоопухолевых препаратов. Введение специальных медикаментов позволяет уменьшить размер опухоли и остановить распространение болезни в организме, однако химиотерапия редко помогает полностью избавиться от патологии. Как и лучевая терапия, противоопухолевое лечение обычно назначается после оперативного вмешательства. При терминальных стадиях, когда опухоль распространяется на другие органы, онкологи чаще назначают паллиативное лечение (ПХТ) в качестве основного метода.
Механизм действия любой формы химиотерапии, включая ПХТ, зависит от назначаемых препаратов. Одни лекарственные средства непосредственно разрушают аномальные клетки, а другие способны лишь остановить рост опухоли. Существенным недостатком такого лечения является отсутствие абсолютной селективности: лекарственные вещества также воздействуют и на здоровые ткани, что становится причиной осложнений. Тем не менее особенности деления и метаболизма злокачественных клеток делают их более легкой мишенью для противоопухолевых средств. Кроме того, ученые постоянно разрабатывают новые высокоселективные медикаменты.
Особым преимуществом ПХТ в онкологии является высокая доступность. Хирургическое лечение может быть нецелесообразным из-за неоперабельного расположения опухоли, наличия метастазов и высокого риска осложнений, однако химиотерапия почти всегда доступна даже на поздних стадиях болезни. В отличие от хирургии, медикаментозное лечение не требует полного удаления поврежденного органа и не вызывает обширную травматизацию тканей.
Как уже было сказано, ПХТ может иметь разные формы влияния на заболевание. Подбор медикаментов зависит от цели терапии, формы онкологического заболевания и состояния пациента. Обычно онкологи назначают несколько препаратов для улучшения терапевтического эффекта.
Основные виды препаратов:
- Цитотоксические лекарственные средства, нарушающие внутриклеточные процессы. Главным представителем этой группы являются антиметаболиты, по своей химической структуре напоминающие внутриклеточные протеины. Проникновение таких химических соединений в опухолевую ткань обуславливает разрушение клеток.
- Цитостатические лекарственные средства, необходимы для предотвращения дальнейшего роста злокачественного очага. Это алкилирующие препараты, растительные алкалоиды и противоопухолевые антибиотики, поражающие внутриклеточную ДНК. Такие медикаменты нарушают процесс деления клеток.
Различные схемы ПХТ предусматривают назначение комбинированной терапии, в которой представлены цитостатические и цитотоксические лекарства. Также в схемах учитывается количество циклов лечения, порядок и кратность приема лекарственных средств. Использование сразу нескольких видов химиотерапии показывает большую эффективность, чем назначение одного препарата в качестве монотерапии.
Онкологические заболевания характеризуются прогрессирующим течением. Изначально опухоль формируется из аномальных клеток определенной ткани и растет в пределах определенной области. Постепенно рост патологии затрагивает все более глубокие ткани, что приводит к распространению опухоли на соседние структуры. Проникновение злокачественных клеток в лимфатическую ткань и кровоток постепенно приводит к формированию вторичных опухолей (метастазов) в отдаленных органах. На этой стадии радикальное лечение, как правило, недоступно, поэтому главной формой терапии является облегчение состояние пациента.
Медикаментозная терапия в виде ПХТ также необходима для улучшения качества жизни онкологического больного. Введение противоопухолевых препаратов помогает устранить некоторые осложнения заболевания, включая отеки, воспалительные процессы и болевой синдром. При этом врачу необходимо учитывать влияние побочных эффектов химиотерапии, поскольку такое лечение само по себе может значительно ухудшить состояние больного. Таким образом, курс ПХТ на поздней стадии онкологии назначается только в том случае, если позитивный эффект химиотерапии перекрывает ее побочные эффекты. Часто такой метод паллиативного лечения позволяет увеличить срок жизни пациента.
Другие виды паллиативной помощи:
- Назначение обезболивающих препаратов для устранения болевого синдрома.
- Проведение психотерапии с назначением антидепрессантов и анксиолитиков.
- Терапевтическое и хирургическое лечение осложнений онкологии.
Грамотное совмещение паллиативной химиотерапии с другими видами медицинской помощи позволяет значительно облегчить тягостные симптомы болезни.

Любая форма терапии злокачественного новообразования может быть назначена только после проведения тщательной диагностики, что также касается и ПХТ. Химиотерапия является сложной медицинской процедурой, характеризующейся высоким риском возникновения побочных эффектов, поэтому врачу необходимо сразу исключить наличие противопоказаний. Перед проведением лечения проводится консультация с целью уточнения состояния больного. Онколог спрашивает пациента о жалобах, изучает анамнестические данные и проводит физикальное обследование. Для подтверждения диагноза требуются результаты инструментальных и лабораторных исследований.
- Рентгенография, компьютерная и магнитно-резонансная томография – высокоточные методы визуального обследования внутренних органов, с помощью которых врач может установить область локализации патологии и определить стадию болезни.
- Ультразвуковое обследования – способ визуализации внутренних органов, подразумевающий использование высокочастотных звуковых волн. Во время обследования врач может видеть структуру пораженного органа на экране.
- Эндоскопическое исследование полостных органов с помощью гастроскопии, колоноскопии, бронхоскопии и других процедур.
- Биопсия – забор небольшого участка злокачественного новообразования с последующим гистологическим исследованием материала. Микроскопирование клеток позволяет уточнить форму патологии и стадию болезни, что очень важно для назначения ПХТ.
- Анализ крови для обнаружения онкологических маркеров, свидетельствующих о наличии патологического процесса в том или ином органе.
- Лабораторные тесты печени, почек и других органов для оценки общего состояния организма.
После получения всех необходимых результатов врач назначает определенную схему противоопухолевой терапии.
Несмотря на то, что химиотерапия подчас является менее агрессивным методом лечения онкологии, чем оперативное вмешательство, нельзя не учитывать степень негативного влияния противоопухолевых препаратов на здоровые клетки. Даже самые высокоселективные препараты могут нарушать функции внутренних органов. Степень проявления побочных эффектов зависит от индивидуальной восприимчивости организма пациента. Для уточнения возможных рисков врачи ориентируются на противопоказания.
Абсолютные и относительные противопоказания к медикаментозному лечению:
- Тяжелая степень почечной или печеночной недостаточности.
- Непроходимость желчных путей.
- Аллергическая реакция на лекарственные средства.
- Выраженные патологии сердца и сосудов.
- Тяжелая онкологическая кахексия.
- Острый дефицит эритроцитов и гемоглобина в крови (анемия).
- Невосприимчивость опухолевых клеток к химиотерапии.
- Острая стадия системных воспалительных и инфекционных заболеваний.
Назначение противоопухолевой терапии при наличии перечисленных противопоказаний может вызвать жизнеугрожающее осложнение, в то время как основной целью паллиативного лечения является облегчение состояния пациента.
Состояние после ПХТ обычно отягощается возникновением негативной симптоматики, обусловленной влиянием цитостатических и цитотоксических препаратов на здоровые клетки. К самым распространенным побочным эффектам химиотерапии относят:
- Выпадение волос и ломкость ногтей.
- Тошноту и рвоту.
- Дефицит тромбоцитов и лейкоцитов в крови.
- Слабость и усталость.
- Потерю аппетита.
- Подавление функций иммунитета.
Таким образом, паллиативное лечение (ПХТ) онкологических заболеваний подходит далеко не всем пациентам. Для уточнения всех необходимых деталей и прохождения обследования необходимо обратиться к онкологу.
- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
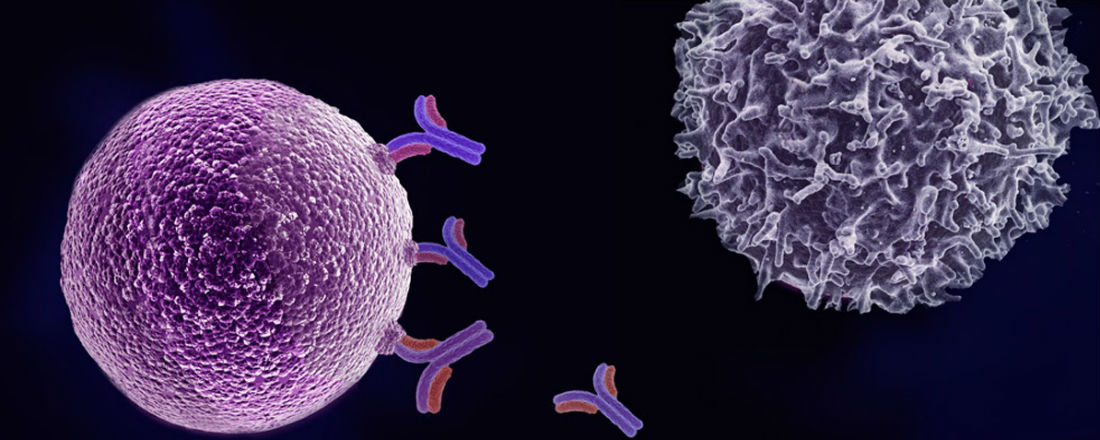
Что такое иммунотерапия?
Объясните, как это работает?
Откуда вообще взялся этот метод лечения?
Первые попытки вылечить пациентов, больных раком, с помощью иммунотерапии были предприняты более ста лет назад. Одним из родоначальников метода считается хирург Уильям Коли. Он заметил, что у некоторых пациентов с рожистым воспалением (бактериальной кожной инфекцией) онкологическое заболевание полностью регрессировало. Коли предположил, что инфекция стимулирует иммунитет на уничтожение опухолевых клеток, и решил подтвердить свои догадки экспериментально. В 1891 году он ввел стрептококковые бактерии пациенту с саркомой кости и смог добиться сокращения злокачественной опухоли.
Тогда его исследования подверглись активной критике, так как не имели внятного теоретического обоснования. Постепенно накапливались знания о физиологии иммунитета, вместе с этим предпринимались новые попытки активировать собственные защитные силы организма для борьбы со злокачественными опухолями — иммунотерапия получила развитие.
Если иммунотерапия существует так давно, почему о ней активно заговорили только сейчас?
Потому что настоящие прорывы произошли лишь в последние годы. Так, в 2018-м Нобелевскую премию по медицине вручили ученым Джеймсу Эллисону из США и Тасуку Хондзё из Японии за открытие контрольных точек — благодаря этому было создано несколько иммунотерапевтических препаратов. Короткий промежуток между теоретическим открытием и внедрением его результатов в медицинскую практику — еще одна причина того, что о новой методике активно говорят. Иммунотерапия открыла новые возможности для борьбы с онкологическими заболеваниями, которые лечатся с большим трудом, например с меланомой и раком легких. Теперь некоторые такие пациенты могут жить на несколько лет дольше без прогрессирования болезни.
Любой ли рак можно вылечить с помощью иммунотерапии?
Это зависит от препарата и особенностей опухоли. Так, препарат пембролизумаб стал первым, который можно назначать вне зависимости от места возникновения рака, если опухоль имеет специфический биомаркер — микросателлитную нестабильность, или PDL-экспрессию. Иммунотерапию применяют для лечения меланомы, рака легких, почки, желудка, мочевого пузыря, простаты, поджелудочной железы, глиобластомы, лимфомы Ходжкина и еще нескольких видов опухолей. Но пока лучшие результаты терапия показала в лечении меланомы и рака легких. Определить, какое лечение подойдет в конкретном случае, может только лечащий врач.
А побочные эффекты есть?
Есть. Так же как и у других эффективных методов лечения онкологических заболеваний — но они отличаются от нежелательных явлений при химиотерапии: причина их возникновения не токсическое действие самих препаратов, а сильный иммунный ответ. Нередко пациенты на иммунотерапии могут сталкиваться с усталостью, кашлем и тошнотой, теряют аппетит, а на коже может появиться сыпь. Реже эти лекарства могут вызывать более серьезные проблемы в легких, кишечнике, печени, почках и других органах. Обычно так бывает, если иммунитет начинает атаковать не только опухолевые клетки, но и здоровые. Пациенты, которые проходят лучевую терапию, также нередко испытывают усталость, у них могут быть проблемы с кожей, а люди, которые получают химиотерапию, сталкиваются с потерей волос, анемией, тошнотой и рядом других проблем.
Объясните, как проходит лечение. Обязательно ложиться в больницу?
В России этот метод лечения популярен?
Нет. Некоторые препараты, например пембролизумаб, ниволумаб, ипилимумаб и атезолизумаб, зарегистрированы в России. Но о широком доступе к терапии говорить не приходится. Препараты зарегистрированы не по всем показаниям, и во многих ситуациях назначить их можно только офлейбл (не по инструкции), но тогда лечение нельзя будет получить бесплатно по полису ОМС.
Читайте также:





