Чем отличается рак ин ситу от дисплазии
Дисплазия многослойного плоского эпителия шейки матки — патология строения, дифференцировки и созревания клеток, морфологически проявляющаяся гипер- и паракератозом, акантозом, нарушением слоя эпителиального пласта и полярности расположения клеток. Характеризуется изменением размеров и формы ядра, увеличением ядерно-цитоплазматического индекса, возникновением митозов преимущественно в базально-парабазальных слоях. Это отличает дисплазию эпителия от фоновых процессов, при которых атипии клеток нет. Таким образом, дисплазия — понятие чисто морфологическое.
Для определения степени выраженности дисплазии в клинической практике используется классификация Richart (1968), согласно которой слабая дисплазия обозначается как CIN I (цервикальная интраэпителиальная неоплазия), умеренная — CIN II, тяжелая — CIN III. В категорию CIN III входит и преинвазивный рак, что объединяет их в общий биологический процесс.
По классификации ВОЗ (1982 г.), в зависимости от степени атипии клеток и глубины поражения эпителиального пласта различают 3 степени дисплазии: слабую (I), умеренную (II) и выраженную (III).
Слабая характеризуется небольшими нарушениями дифференцировки эпителия с незначительной пролиферацией клеток базального слоя. Изменения захватывают лишь 1/3 толщи эпителиального пласта, строение остального эпителия сохраняется.
При умеренной дисплазии отмечается более значительная атипичность клеток до 1/2 толщи эпителиального пласта.
Резко выраженная, или тяжелая, дисплазия характеризуется поражением 2/3 его. При этом нарушается взаиморасположение клеток, значительно увеличиваются размеры ядра, изменяется ядерно-цитоплазматическое соотношение, появляются патологические митозы — несмотря на то, что структура верхнего слоя эпителия сохранена.
Дальнейшее прогрессирование процесса с полным поражением всей толщи многослойного плоского эпителия, нарастанием ядерной и клеточной атипии рассматривается как внутриэпителиальный рак, что свидетельствует о патогенетическом единстве этих патологических состояний.
По литературным данным, вероятность развития интраэпителиального рака у больных с дисплазией шейки матки в 20 раз, а инвазивного — в 8 раз выше, чем у женщин с нормальной шейкой.
Эпителиальные дисплазии I и II степени могут не прогрессировать длительное время, а в ряде случаев — подвергаться обратному развитию. Это, как правило, бывает после излечения сопутствующего воспалительного процесса. Однако чаще всего дисплазия со временем прогрессирует и переходит в рак шейки матки. В среднем сроки развития внутриэпителиального рака из слабой дисплазии составляют 5 лет, из умеренной — 3 года, из выраженной — 1 год.
Среди факторов риска возникновения эпителиальных дисплазий важное значение имеют:
- раннее начало половой жизни, частая смена половых партнеров;
- травмы шейки матки во время родов и абортов;
- воспалительные заболевания половых органов;
- инфицирование вирусом простого герпеса 2-го типа и вирусом папилломы человека;
- абсолютная или относительная гиперэстрогения;
- инфекции, передаваемые половым путем.
Учет факторов риска необходим для диспансеризации указанного контингента женщин, своевременного выявления и лечения у них фоновых и предопухолевой патологий шейки матки.
Возрастной пик умеренной формы приходится на 31–40 лет, выраженной — на 40–50 лет.
У молодых женщин дисплазия поражает преимущественно влагалищную часть, а с увеличением возраста — цервикальный канал, что связано с особенностями строения шейки матки при старении.
В отношении эпителиальных дисплазий недопустима выжидательная тактика. Выбор метода лечения осуществляется индивидуально в зависимости от выраженности патологического процесса, его локализации, распространенности в пределах шейки матки и возраста больных.
Слабая дисплазия эпителия (CIN I), морфологически сохраняющаяся после противовоспалительной терапии, у женщин детородного возраста подлежит диатермоэлектрокоагуляции (ДЭК). Последняя возможна при условии, что вся зона трансформации четко визуализируется кольпоскопически. При невидимой зоне трансформации, наличии сопутствующих дисплазий эктропионов, деформаций шейки матки, а также в возрасте свыше 40 лет показано хирургическое лечение.
При умеренной дисплазии (CIN II) у женщин в возрасте до 40 лет допустима ДЭК шейки матки. Эффективность ДЭК при этой форме зависит от тщательного цитологического, эндоскопического и гистологического обследований больной, предшествующих лечению, а также ограничения зоны трансформации только эктоцервиксом, что устанавливается кольпоскопически. При наличии дисплазии II степени на шейке с невизуализуемой зоной трансформации в сочетании с обширным эктропионом, деформацией шейки матки, а также пациенткам старше 45 лет выполняется операция — гистерэктомия.
Основным методом лечения выраженной дисплазии (CIN III) шейки матки является конизация, осуществляемая ножевым способом. Эффективность ее в возможности полного удаления патологически измененных тканей шейки в пределах 2/3 слизистой эндоцервикса, что соответствует принципам онкологического радикализма, а также доступности гистологического исследования.
При сглаживании влагалищных сводов у больных с дисплазией III степени, атрофических изменениях, у женщин старше 48–50 лет органосохраняющее вмешательство затруднено, объем операций расширяется до простой гистерэктомии.
Несмотря на наличие множества программ, касающихся диагностики и лечения фоновых и предопухолевых заболеваний шейки матки, у части пролеченных все же развивается инвазивный рак.
Для изучения частоты фоновой и предраковой патологии, предшествующей развитию рака шейки матки (РШМ), а также оценки эффективности применяемых методов лечения проанализированы данные амбулаторных карт и историй болезни 120 больных в НИИ (ныне — РНПЦ) онкологии и медрадиологии им. Н. Н. Александрова.
РШМ возник у 86 (71,7%) пациенток, отметивших в анамнезе фоновые или предраковые заболевания шейки матки, пролеченные консервативно либо методом ДЭК.
Появление РШМ у ранее подвергшихся электрохирургическим либо консервативным методам лечения предраковых заболеваний шейки матки позволяет сделать вывод, что в ряде случаев его развитие произошло изза ошибок, допущенных на этапе обследования, или при выборе лечения, либо при немотивированном воздержании от оптимальных методов. Есть и беспечные женщины, уклоняющиеся от лечения, а врачи не придают должного значения риску трансформации заболевания в рак.
Случай из практики . Больная М., 60 лет. Поступила в онкогинекологическое отделение института по поводу дисплазии шейки матки.
Жалоб не предъявляла. Цитологически при профосмотре у нее выявили дисплазию. На дообследование в женскую консультацию пришла через 10 месяцев, когда появились кровянистые выделения из влагалища.
В соскобе из слизистой цервикального канала диагностирована дисплазия III степени, интраэпителиальный рак. Направлена в НИИ онкологии. М. пришла с этим направлением через… 7 месяцев.
При гинекологическом исследовании в зеркалах — шейка на уровне сводов, чистая, пальпаторно плотная, выделения слизисто-гнойные, есть инфильтрация парацервикальной клетчатки. Тело матки, придатки и параметральные отделы клетчатки не изменены.
В пересмотренных микропрепаратах биоптата — дисплазия III степени, местами интраэпителиальный рак. В соскобе из цервикального канала — пласты многослойного плоского эпителия с картиной рака. Окончательное морфологическое заключение — плоскоклеточный рак Gr II. Клинический диагноз — рак шейки матки IB стадии, эндоцервикальная форма.
Случай из практики. Больная П., 43 года. Поступила в онкогинекологическое отделение для обследования в связи с клинической картиной менометроррагии.
Более 2 лет назад подвергалась ДЭК по поводу эрозии шейки матки. Со слов больной, эрозию коагулировали при первом обращении к гинекологу без осуществления биопсии и выскабливания цервикального канала. На диспансерном учете не состояла. Спустя полгода после повторной ДЭК у пациентки появились контактные мажущие выделения, которые перешли в кровотечение со сгустками, что и заставило ее снова обратиться к врачу. После выскабливания цервикального канала и слизистой полости матки диагностирован РШМ. Направлена в институт для лечения.
При осмотре в зеркалах шейка матки бочкообразно раздута, опухолево изменена, увеличена. Передняя губа изъязвлена, кровоточит при дотрагивании, с обеих сторон в малом тазу определяются параметральные инфильтраты, не достигающие стенок таза. Гистологически — плоскоклеточный рак. Диагноз: РШМ IIB стадии (T2N0M0) — эндоцервикальная локализация, параметральный вариант.
Случай из практики. Больная М., 60 лет. Поступила для обследования в НИИ онкологии и медрадиологии по поводу дисплазии шейки матки.
Заболевание цитологически выявлено при профилактическом осмотре. Клинически определены разрыв шейки матки в родах и кольпит. На 1-м этапе проведено противовоспалительное лечение без типирования патогенной влагалищной микрофлоры. Затем без дополнительных обследований выполнена ДЭК шейки матки. Спустя год появились контактные кровянистые выделения. Осуществлено
раздельное диагностическое выскабливание цервикального канала и слизистой полости матки. Морфологически обнаружены фрагменты железистого полипа, бактериоскопически — трихомонады, в связи с чем провели курс специального лечения. Повторно обследована; цитологически выявлена дисплазия III степени. Направлена в НИИ с результатами всех ранее проведенных исследований. Морфологически диагностирован рак шейки матки IA стадии. Больная оперирована в объеме простой гистерэктомии с придатками.
Случай из практики. Больная Н., 45 лет. Поступила в онкологическое отделение с жалобами на беспорядочные кровянистые выделения, появившиеся более 3 месяцев назад. К врачу обратилась из-за опасения РШМ: ее мать умерла от этой патологии. Из перенесенных заболеваний отмечает эрозию шейки матки, которая была излечена методом ДЭК. На диспансерном учете не состояла. До возникновения у нее менометроррагии считала себя здоровой. При осмотре в зеркалах шейка укорочена, на уровне сводов деформирована, с обширной язвой, переходящей в цервикальный канал. Пальпаторно представлена плотным бугристым образованием с инфильтрацией параметральных отделов клетчатки, доходящих до стенок таза. Гистологически в соскобе из цервикального канала и биоптате из шейки матки — плоскоклеточный рак Gr II.
Клинический диагноз: РШМ III ст., язвенно-инфильтративная форма, влагалищно-параметральный вариант.
Здесь электрокоагуляция на деформированной шейке не достигла ни косметического эффекта, ни исчезновения дисплазии. Вероятно, в глубоких слоях эпителия после вмешательства оставался неизлеченный процесс предопухолевого заболевания, который подвергся малигнизации, не распознанной на ранней стадии. Можно предположить и то, что при электроэксцизии участок дисплазии на деформированной шейке не попал в иссеченный конус, остался в ней, либо имеющаяся патология не оказалась в срезе при микроскопическом исследовании. Поэтому больные, подвергшиеся такой сохранной лечебной процедуре по поводу дисплазии цервикального канала, как электроэксцизия, должны состоять на диспансерном учете и входить в группу риска по развитию РШМ.
За женщинами, ранее лечившимися по поводу дисплазии, важно вести надлежащий диспансерный контроль. При этом следует строго придерживаться утвержденного диагностического алгоритма, включающего клинический осмотр шейки матки, кольпоскопию, взятие под контролем мазков на атипические клетки из экзо- и эндоцервикса и биопсию из патологического очага, а в случае дисплазии — произвести выскабливание цервикального канала. Надо помнить, что деформированная и с разрывами шейка матки является противопоказанием к использованию ДЭК.
Больные, пролеченные в прошлом по поводу фоновой или предраковой патологии шейки матки методом ДЭК либо консервативными средствами, должны состоять на диспансерном учете не менее 3 лет и входить в группу риска по возможному возникновению у них РШМ.
Улучшить выявление РШМ на ранних стадиях помогут совершенствование онкологических знаний врачами-акушерами-гинекологами, просвещение ими широких слоев населения и осуществление скрининга.
Снять больных с дисплазией шейки матки I–III степени с учета можно лишь при условии отрицательных кольпоскопических и цитологических данных через 2 года после лечения. Перед этим необходимо провести углубленное обследование, включающее контрольную расширенную кольпоскопию, взятие мазков из влагалищной и цервикальной частей шейки матки на цитологию, а также выскабливание
цервикального канала с последующим морфологическим исследованием соскоба. При этом каждую из больных следует вызывать к гинекологу два раза в год даже при полном благополучии.
Оценка клинических наблюдений РШМ у больных, ранее пролеченных по поводу фоновых и предопухолевых заболеваний шейки матки, позволяет сделать вывод, что в целях совершенствования профилактики РШМ и ранней его диагностики необходимо внедрить в практику системный патогенетический скрининг и наладить диагностику среди женщин группы риска:
- имеющих несколько половых партнеров;
- рано начавших половую жизнь;
- страдающих ИППП;
- ранее получавших лечение по поводу дисплазии и фоновых заболеваний шейки матки.
Не вызывает сомнений, что выраженность дисплазии тесно коррелирует с риском возникновения карциномы, а тяжелая дисплазия эпителия является стадией, непосредственно предшествующей развитию рака.
При этом в результате дальнейших изменений возникает трансформированная клетка, которая формирует скопление себе подобных, питающихся за счет диффузии веществ из окружающей тканевой жидкости.
На этой стадии в опухоли еще отсутствуют достаточные генные перестройки и поэтому ей несвойственны инвазивный рост и метастазирование.
Стадия неинвазивной опухоли
И все же в последние годы большинство онкологов признает, что carcinoma in situ является пограничным этапом малигнизации и представляет собой рак со всеми атрибутами цитологической злокачественности, за исключением сформированного опухолевого узла, инвазивного роста в подлежащие ткани и метастазирования.
Морфологически эпителиальный пласт, пораженный карциномой in situ, представлен анаплазированными опухолевыми клетками и имеет все черты полиморфизма, характерные для рака (нарушение вертикальной направленности расположения клеток в пласте, полиморфизм ядер, ядерно-цитоплазматическое соотношение в пользу ядра, повышенная митотическая активность, патологические митозы) (рис. 7.2. и 7.3).

Рис. 7.2. Морфологическая характеристика дисплазии различной степени развития и карциномы in situ. БМ — базальная мембрана. [Ганцев Ш.Х., Хуснутдинов Ш.М., 2003]

Рис. 7.3. Морфологический континуум. Схематически показаны изменения от нормального эпителия до инвазивного и метастатического рака.
Хотя инвазивный рост еще отсутствует, но процесс уже сопровождается лимфогистиоцитарной инфильтрацией в подлежащей субэпителиальной основе.
Carcinoma in situ чаще диагностируется в матке, мочевом пузыре, легких, молочной железе и в слизистой оболочке ротовой полости, но, вероятно, может существовать во всех органах и тканях.
Однако, в клинической онкологии прочно утвердилось положение, что carcinoma in situ, в отличие от предопухолевых заболеваний, — это необратимый канцерогенный процесс, который неминуемо рано или поздно превращается в классический рак.
В этот период рак еще не имеет признаков инвазивного роста, но прорыв базальной мембраны и метастазирование могут наступить в любой момент. Гарантии доброкачественности поражения нет. Поэтому при сложившихся стандартах лечения трактовка подобных изменений как предрака (а не рака) может привести к печальным последствиям.
Прединвазивный рак
Прединвазивный рак может быть выявлен клиническими методами исследования (осмотр, пальпация при наружных локализациях) и различными методами визуализации. Но окончательное подтверждение диагноза можно получить только при гистологическом исследовании пораженной ткани, нередко с использованием серийных срезов.
Диагностика этой стадии рака — трудная и ответственная задача и требует высокой квалификации патологоанатома. Это связано с необходимостью проведения радикального лечения, нередко с неоправданной потерей органа в случае гипердиагностики или нерадикапьности воздействия при нераспознанном микроинвазивном раке.
Современный подход к ранней онкологической патологии требует широких контактов и консультаций морфологов с клиницистами и эндоскопистами.
Практический врач должен четко представлять себе различие между инвазивным и неинвазивным раком. Подход к лечению должен быть дифференцированным с учетом локализации.
Так, у некоторой части больных рак in situ может быть излечен консервативно (прогестинами при поражении эндометрия), могут применяться органосохраняющие методы печения (при неинвазивном раке шейки матки, молочной железы) или радикальные операции. Результаты лечения carcinoma in situ учитываются отдельно. Как правило, 5-летняя выживаемость составляет 100%.
Угляница К.Н., Луд Н.Г., Угляница Н.К.
Онкологические заболевания шейки матки занимают второе место среди всех опухолей у женщин по распространенности. Их отличием является тот факт, что причина развития таких новообразований точно известна – вирус папилломы человека (ВПЧ). Своевременная диагностика рака шейки матки играет решающую роль выборе адекватной тактики лечения и в общем прогнозе по заболеванию.
Развитие опухоли происходит в несколько стадий, и ключевым моментом является наличие фазы длительных предраковых состояний, так называемых дисплазий. Итак, рассмотрим, чем отличается дисплазия от рака шейки матки по симптомам и как она диагностируется и классифицируется.
Причины и факторы риска
Как уже было указано, основной причиной развития рака шейки матки является ВПЧ. Однако, этот вирус присутствует у 90% здоровых женщин в виде бессимптомного носительства. Почему же он может быть неопасным, а иногда может приводить к развитию грозных опухолей?
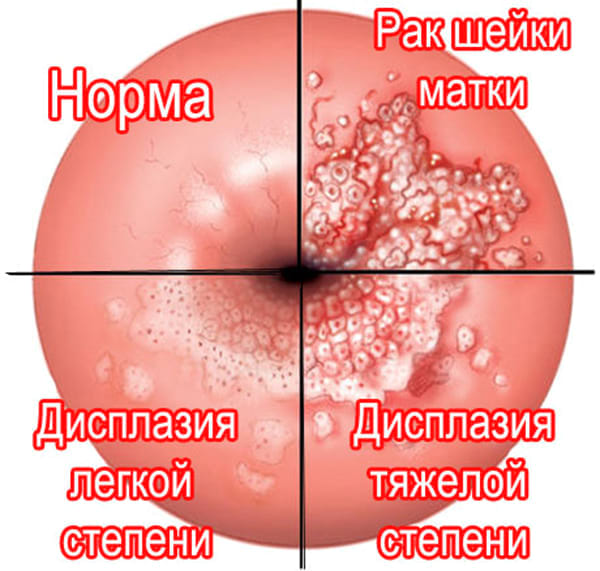
Дело в том, что существует десятки штаммов ВПЧ и лишь некоторые из них обладают высокоонкогенным статусом – например, 16, 18, 31 штаммы. Кроме этого, Наличие даже опасной разновидности вируса в организме не гарантирует развитие рака или диспластических процессов. Но, если есть провоцирующие факторы риска, вероятность заболеть растет. К ним относятся:
- большое количество половых партнеров;
- инфекционные процессы в мочеполовой системе;
- травмы шейки матки в анамнезе;
- гиперэстрогения разного генеза.
Все эти факторы могут с высокой долей вероятности приводить к развитию дисплазии шейки матки, а затем и раку.
Морфология и патофизиология
Дисплазия представляет собой нарушение строения, деления и функционирования эпителиальных клеток шейки матки. Морфологически это чаще всего проявляется утратой нормальной формы и строения клетки. Она может удлинняться или деформироваться, у клетки появляется несколько ядер, а делиться она начинает с нарушениями.
Это еще не раковые клетки, когда происходит полное перерождение. При превращении в злокачественные, клетки полностью теряют свою естественную функцию, и начинают бесконтрольно делиться.
Однако, наличие дисплазии тканей, особенно запущенных степеней практически со 100% вероятностью свидетельствует о том, что рано или поздно клетки начнут превращаться в атипические.
Классификация и стадирование
У дисплазии есть несколько стадий и разновидностей, которые меняются по мере развития патологических процессов в эпителиальном слое шейки матки. Так, по старой классификации 1968 года Richart выделялось 3 степени дисплазии клеток – CIN 1, CIN 2 и CIN 3.
По новой пересмотренной классификации ВОЗ 1982 года выделяют также 3 стадии:
- легкую,
- умеренную,
- тяжелую
Тяжелая степень дисплазии и стадия CIN 3 соответствуют облигатном предраку или даже, как иногда его принято называть “рак in situ”. Предраковые состояния характеризуются тем, что со 100% вероятностью развиваются в злокачественную опухоль.
Диагностика патологий шейки матки
Диагностические меры для выявления дисплазии или рака сводятся к двум основным методам – определение наличия ВПЧ с помощью ДНК-теста и так называемый мазок на цитологию по Папаниколау. Правда, следует отметить, что оба эти теста далеки от идеала в плане информативности и достоверности.
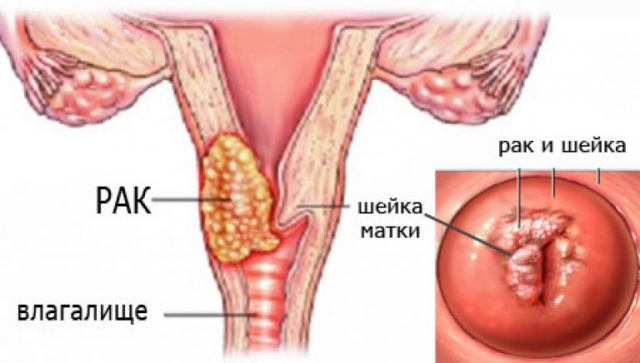
Например, при выявлении ВПЧ, даже онкогенного типа, речь не идет о наличии диспластических процессов или рака в шейке матки. Тем не менее, наличие вируса дает много дополнительной информации.
Мазок по Папаниколау является золотым стандартом в мире онкогинекологии. Принцип метода состоит в том, что у женщины на гинекологическом осмотре берется материал из шейки с помощью специальной щеточки. После этого мазок направляется на цитологический анализ в лабораторию.
В мазке по морфологии клеток определяется стадия дисплазии, предрак или рак. Однако, и здесь в 15-25% возможна ошибка при постановке диагноза. В случае дисплазии 1 или 2 степени врач рекомендует лечение.
На данный момент разрабатываются специфические исследования, которые лишены недостатков ДНК-теста и мазка Папаниколау. Речь идет о новых эпигенетических тестах, которые будут со 100% точность определять степень клеточной дисплазии или атипии.
Профилактика
На сегодняшний день в развитых государствах (например, Израиль, Австралия) проводится тотальная вакцинация женщин от вируса папилломы человека. Это является 100% эффективным способом профилактики дисплазии и рака шейки матки. Так, Австралия прогнозируемо станет первым в мире государством, где рак шейки матки удастся полностью побороть.
Второстепенными методами профилактики являются:
- соблюдение культуры половой жизни,
- грамотная гормональная контрацепция,
- регулярные гинекологические скрининги и осмотры,
- отказ от вредных привычек.
Из группы рака шейки матки выделяют так называемую преинвазивную форму, или рак in situ.
Рак in situ (преинвазивный рак, рак нулевой стадии, поверхностный рак, начальный рак, латентный рак, потенциальный рак, внутриэпителиальная покровная эпителиома и др.) возникает чаще всего в области стыка многослойного плоского и призматического эпителия, который получил название трансформационной зоны. В этой зоне отмечают повышенную митотическую активность клеток эпителия и чувствительность к различным канцерогенным факторам. Средний возраст больных раком in situ по сравнению с возрастом больных инвазивным раком меньше на 8—10 лет.
Рак in situ нередко развивается мультицентрично, захватывая экто- и эндоцервикс. По краю очагов рака in situ обнаруживают зоны с разной степенью выраженности диспластических изменений эпителия. Протяженность очагов дисплазии и рака in situ у разных больных неодинакова. При наличии рака in situ в эндоцервиксе дисплазия может отмечаться во влагалищной части и наоборот. В связи с этим необходимо гистологическое исследование не только материала, взятого из эктоцервикса, но и соскоба из канала шейки матки. В канале шейки матки рак in situ может захватывать только покровный эпителий или сочетаться с одновременным поражением желез слизистой оболочки. В более редких случаях очаги рака обнаруживают только в области желез.
Различают плоскоклеточный и резервногенный рак in situ. В литературе описаны также отдельные случаи железистого рака in situ.
Плоскоклеточный рак in situ в основном обнаруживают во влагалищной части шейки матки, источником его является многослойный плоский эпителий. При этом нарушена вертикальная анизоморфность многослойного плоского эпителия, но степень нарушения неодинакова. В некоторых случаях отмечают тенденцию к ороговению отдельных клеток или группы клеток. Поэтому делают попытку выделить плоскоклеточный рак in situ со склонностью к ороговению, неороговевающие и низкодифференцированные его варианты. Однако независимо от варианта для рака in situ характерны выраженный клеточный и ядерный полиморфизм и атипия, появление митотически делящихся клеток на разных уровнях пласта, значительное число патологических митозов.
Резервногенный рак in situ, источником которого являются резервные клетки призматического эпителия, развивается в эндоцервиксе и в очагах эндоцервикоза эктоцервикса. По структуре он неоднороден. Часто такой рак in situ не отличается от плоскоклеточных форм, так как возникает в метаплазированном многослойном плоском эпителии. Вместе с тем он имеет и свои особенности. Часто состоит из мелких веретенообразных клеток. последние нередко складываются в пучки, образуя завитки, что говорит о нарушении ориентации клетки по отношению к базальной мембране. Ядра клеток вытянутые, палочковидные, гиперхромные. Так же как и в плоскоклеточных формах, имеются митозы, в том числе и патологические. Иногда в цитоплазме клеток можно обнаружить слизь.
Железистый рак in situ возникает чрезвычайно редко, преимущественно в эндоцервиксе, иногда на фоне аденоматоза. Характеризуется появлением в одной или группе желез атипического призматического эпителия. Последний располагается в 1 —2 ряда, образуя многоядерные и криброзные структуры. Границы клеток четкие, форма их округлая, вытянутая. Ядра крупные, гиперхромные, иногда уродливые. Имеются митотически делящиеся клетки. В цитоплазме некоторых клеток выявляют слизь.
Независимо от формы рака in situ базальная мембрана всегда сохранена. В подлежащей соединительной ткани отмечают лимфогистиоцитарные инфильтраты с примесью плазматических и тучных клеток, деструкция коллагеновых и эластических волокон.
Различают III степени выраженности CIN. При CIN I—недифференцированные клетки занимают 1/3 толщи эпителиального пласта, что соответствует слабо выраженной дисплазии; при CIN II- изменения захватывают 2/з эпителиального пласта, что соответствует умеренно выраженной дисплазии; при CIN III — весь или почти весь эпителиальный пласт представлен незрелыми клетками с явлениями атипии, что соответствует тяжелой дисплазии и раку in situ. Таким образом, под рубрикой CIN III объединяют и тяжелую форму дисплазии и рак in situ, так как провести дифференциальный диагноз между этими процессами очень сложно. Вместе с тем такое объединение многими оспаривается, так как лечебная тактика при них различна.
Изменения при CIN могут пройти весь цикл развития от слабой дисплазии до формирования очагов инвазивного рака, но могут регрессировать на любом этапе.
После того как диагноз дисплазии или рака in situ по биоптату из эктоцервикса установлен, клиницисты обычно проводят диагностическое выскабливание канала шейки матки с тем, чтобы исключить его опухолевое поражение. При гистологическом исследовании соскоба нередко в нем обнаруживают лить пласты атипично измененного эпителия без подлежащей ткани, что затрудняет диагностику. В таких случаях часто ограничиваются формальным описанием пласта, хотя отторжение атипичных пластов характерно для тяжелых форм дисплазии и рака in situ. Оно обусловлено выраженным отеком, разрыхлением и лимфогистиоцитарной инфильтрацией подлежащей ткани. Атипичные пласты отторгаются вместе с базальной мембраной и ею ограничены. В этих случаях даже при отсутствии подлежащей соединительной ткани может быть поставлен гистологический диагноз рака in situ.
Из группы рака шейки матки выделяют так называемую преинвазивную форму, или рак in situ.
Рак in situ (преинвазивный рак, рак нулевой стадии, поверхностный рак, начальный рак, латентный рак, потенциальный рак, внутриэпителиальная покровная эпителиома и др.) возникает чаще всего в области стыка многослойного плоского и призматического эпителия, который получил название трансформационной зоны. В этой зоне отмечают повышенную митотическую активность клеток эпителия и чувствительность к различным канцерогенным факторам. Средний возраст больных раком in situ по сравнению с возрастом больных инвазивным раком меньше на 8—10 лет.
Рак in situ нередко развивается мультицентрично, захватывая экто- и эндоцервикс. По краю очагов рака in situ обнаруживают зоны с разной степенью выраженности диспластических изменений эпителия. Протяженность очагов дисплазии и рака in situ у разных больных неодинакова. При наличии рака in situ в эндоцервиксе дисплазия может отмечаться во влагалищной части и наоборот. В связи с этим необходимо гистологическое исследование не только материала, взятого из эктоцервикса, но и соскоба из канала шейки матки. В канале шейки матки рак in situ может захватывать только покровный эпителий или сочетаться с одновременным поражением желез слизистой оболочки. В более редких случаях очаги рака обнаруживают только в области желез.
Различают плоскоклеточный и резервногенный рак in situ. В литературе описаны также отдельные случаи железистого рака in situ.
Плоскоклеточный рак in situ в основном обнаруживают во влагалищной части шейки матки, источником его является многослойный плоский эпителий. При этом нарушена вертикальная анизоморфность многослойного плоского эпителия, но степень нарушения неодинакова. В некоторых случаях отмечают тенденцию к ороговению отдельных клеток или группы клеток. Поэтому делают попытку выделить плоскоклеточный рак in situ со склонностью к ороговению, неороговевающие и низкодифференцированные его варианты. Однако независимо от варианта для рака in situ характерны выраженный клеточный и ядерный полиморфизм и атипия, появление митотически делящихся клеток на разных уровнях пласта, значительное число патологических митозов.
Резервногенный рак in situ, источником которого являются резервные клетки призматического эпителия, развивается в эндоцервиксе и в очагах эндоцервикоза эктоцервикса. По структуре он неоднороден. Часто такой рак in situ не отличается от плоскоклеточных форм, так как возникает в метаплазированном многослойном плоском эпителии. Вместе с тем он имеет и свои особенности. Часто состоит из мелких веретенообразных клеток. последние нередко складываются в пучки, образуя завитки, что говорит о нарушении ориентации клетки по отношению к базальной мембране. Ядра клеток вытянутые, палочковидные, гиперхромные. Так же как и в плоскоклеточных формах, имеются митозы, в том числе и патологические. Иногда в цитоплазме клеток можно обнаружить слизь.

Железистый рак in situ возникает чрезвычайно редко, преимущественно в эндоцервиксе, иногда на фоне аденоматоза. Характеризуется появлением в одной или группе желез атипического призматического эпителия. Последний располагается в 1 —2 ряда, образуя многоядерные и криброзные структуры. Границы клеток четкие, форма их округлая, вытянутая. Ядра крупные, гиперхромные, иногда уродливые. Имеются митотически делящиеся клетки. В цитоплазме некоторых клеток выявляют слизь.
Независимо от формы рака in situ базальная мембрана всегда сохранена. В подлежащей соединительной ткани отмечают лимфогистиоцитарные инфильтраты с примесью плазматических и тучных клеток, деструкция коллагеновых и эластических волокон.
Различают III степени выраженности CIN. При CIN I—недифференцированные клетки занимают 1/3 толщи эпителиального пласта, что соответствует слабо выраженной дисплазии; при CIN II- изменения захватывают 2/з эпителиального пласта, что соответствует умеренно выраженной дисплазии; при CIN III — весь или почти весь эпителиальный пласт представлен незрелыми клетками с явлениями атипии, что соответствует тяжелой дисплазии и раку in situ. Таким образом, под рубрикой CIN III объединяют и тяжелую форму дисплазии и рак in situ, так как провести дифференциальный диагноз между этими процессами очень сложно. Вместе с тем такое объединение многими оспаривается, так как лечебная тактика при них различна.
Изменения при CIN могут пройти весь цикл развития от слабой дисплазии до формирования очагов инвазивного рака, но могут регрессировать на любом этапе.
После того как диагноз дисплазии или рака in situ по биоптату из эктоцервикса установлен, клиницисты обычно проводят диагностическое выскабливание канала шейки матки с тем, чтобы исключить его опухолевое поражение. При гистологическом исследовании соскоба нередко в нем обнаруживают лить пласты атипично измененного эпителия без подлежащей ткани, что затрудняет диагностику. В таких случаях часто ограничиваются формальным описанием пласта, хотя отторжение атипичных пластов характерно для тяжелых форм дисплазии и рака in situ. Оно обусловлено выраженным отеком, разрыхлением и лимфогистиоцитарной инфильтрацией подлежащей ткани. Атипичные пласты отторгаются вместе с базальной мембраной и ею ограничены. В этих случаях даже при отсутствии подлежащей соединительной ткани может быть поставлен гистологический диагноз рака in situ.
Читайте также:

