Чем отличается первичная опухоль от метастазов
В последние десятилетия усилия многих онкологов были направлены на установление детальных механизмов зарождения раковой опухоли, регуляции ее активного роста и процессов формирования благоприятного для нее микроокружения из клеток стромы, соединительнотканного каркаса органа. Со временем стало понятно, что основная угроза рака заключена в его способности к распространению по организму.
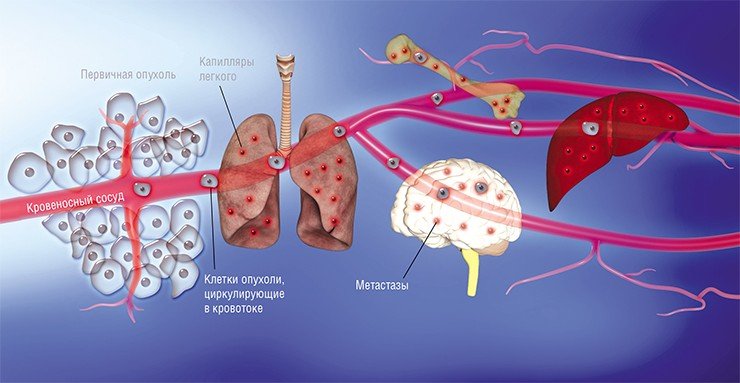
Наконец в 1970-е гг. благодаря экспериментам на лабораторных мышах, которым делались инъекции раковых клеток, меченных радиоактивными изотопами, американский исследователь И. Фидлер смог доказать, что на результат метастазирования влияет природа раковых клеток: клетки меланомы метастазировали в легкие, но не в печень, в сосудах которой они не выживали. Позднее были установлены и другие факты, подтверждающие, что раковые клетки разной природы метастазируют преимущественно в определенные органы, иногда даже и в определенной последовательности. Например, клетки рака молочной железы формируют метастазы сначала в костях, печени, лимфатических узлах и легких, и лишь потом уже – в мозге. Явление специфичного распределения метастазов по организму назвали органотропией метастазирования.
И сегодня в онкологии все еще остается много вопросов без ответов. Например, отличаются ли метастазные раковые клетки от других клеток первичной опухоли? Что лежит в основе органотропии? И главное: как метастазам удается выжить после удаления первичной опухоли и проведения химиотерапии?
Метастазы: от генетики до эпигенетики
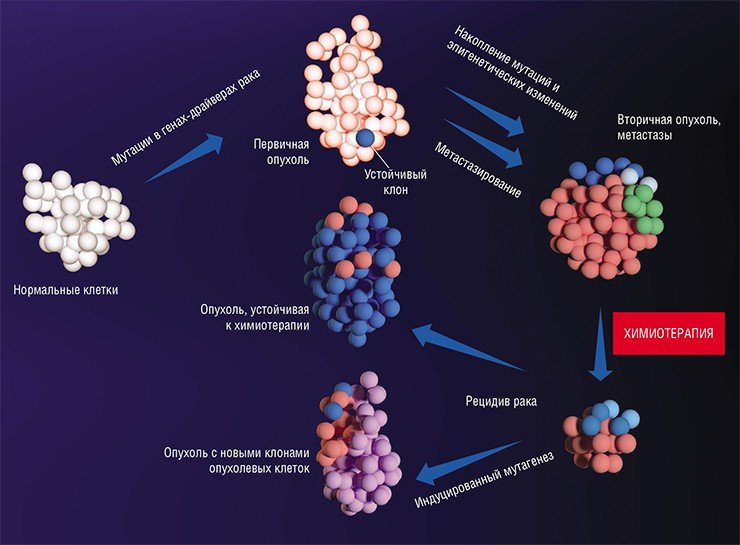
Интересно, что был обнаружен как минимум один ген – FBXW7, мутации в котором противодействуют метастазированию (Mlecnik et al., 2016). Происходит это за счет усиления провоспалительной реакции, увеличения численности и роста активности T-лимфоцитов, что стимулирует формирование иммунных реакций по отношению к опухолевым клеткам. Таким образом, появление мутаций в гене FBXW7 раковых клеток предотвращает развитие характерной для опухолей иммуносупрессии.
После формирования преметастазных ниш с благоприятным клеточным окружением некоторые раковые клетки покидают первичную опухоль и формируют микрометастазы в других тканях и органах. Финальный этап формирования вторичного очага может занимать от нескольких месяцев до нескольких лет
До сих пор мы говорили о непосредственных изменениях в самой структуре ДНК. Следующая ступень в регуляции экспрессии генов – эпигенетические изменения, связанные с метилированием ДНК и гистонов (ДНК-связывающих белков). По своей природе такие изменения более пластичны по сравнению с генетическими: они подвержены влиянию клеточных каскадов передачи сигнала, подстраивающихся под действие внешних факторов.
На развилке метаболических путей
Эпигенетическая регуляция – один из важнейших механизмов программирования клеточного метаболизма. С ростом опухоли внутри нее образуются области, куда не доходят кровеносные сосуды и где возникает кислородная недостаточность (гипоксия). В результате деметилирования ДНК в раковых клетках начинает активно работать ген, кодирующий белок HIF‑1-альфа, который так и называется – фактор, индуцируемый гипоксией. Усиленное образование этого белка, в свою очередь, влияет на уровень экспрессии генов множества метаболических ферментов и белков-транспортеров, что приводит к комплексным изменениям метаболизма раковых клеток.
Как известно, клеточный метаболизм включает процессы расщепления соединений с выделением энергии (катаболизм) и их образования с использованием энергии (анаболизм). Энергетический обмен клетки обеспечивается благодаря клеточному дыханию, в котором выделяют гликолиз (ферментативный распад глюкозы), цикл трикарбоновых кислот (окислительные превращения промежуточных продуктов распада и синтеза белков, жиров и углеводов) и окислительное фосфорилирование (запасание энергии в результате окисления молекул органических веществ).
Раковые клетки по-своему приспосабливают энергетический обмен к условиям недостатка кислорода. В первичной опухоли они в основном используют анаэробный гликолиз, а не окислительное фосфорилирование, как в нормальных клетках. Это усиленное поглощение и расщепление глюкозы до молочной кислоты, которая выделяется раковыми клетками, названо эффектом Варбурга. Такая адаптация позволяет раковым клеткам успешно выживать и активно размножаться при недостатке кислорода.
Но все это относится к первичной опухоли, для клеток же метастазов особенности генерирования энергии до сих пор мало изучены. Тем не менее, используя клетки рака молочной железы, обладающие широкой органотропией при метастазировании, ученые обнаружили различия в метаболизме первичной опухоли и метастазов. Раковые клетки, колонизировавшие кости и легкие, более активно использовали окислительное фосфорилирование, а колонизировавшие печень – гликолиз. Когда раковые клетки колонизировали все возможные органы-мишени, в них активировались оба метаболических пути (Rosen, Jordan, 2009). Похоже, что такая метаболическая пластичность помогает раковым клеткам осваивать новые ниши.
Почему же метастазам в одном случае выгоднее использовать преимущественно один вид метаболизма, а в другом – другой? Ответ на этот вопрос, как и на вопрос о роли различных факторов в регуляции метаболической пластичности раковых клеток, еще только предстоит узнать.
Несмотря на всю свою адаптационную пластичность, метастазные раковые клетки не могут в одиночку справиться со столь непростой задачей – освоением совершенно незнакомого места обитания.
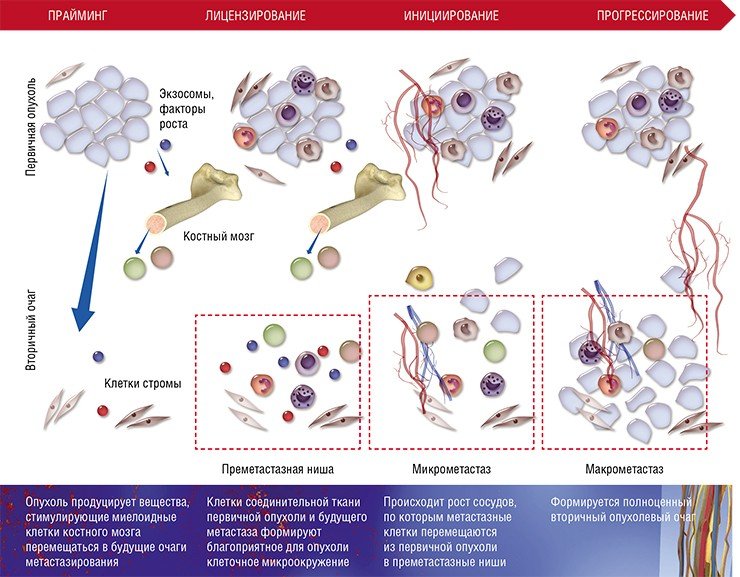
Хотя описанная выше схема характерна для большинства органов, у нее имеются особенности в зависимости от места (органа), где формируются метастазы. Например, в печени и легких в процессе создания преметастазной ниши активно участвуют еще одни клетки крови – нейтрофильные гранулоциты. Известно, что лейкоциты этого вида помогают раковым клеткам интегрироваться в новую нишу, секретируя протеазы и цитокины и непосредственно контактируя с раковыми клетками при выходе из капилляров.
Основная же функция лизилоксидазы заключается в формировании поперечных связей между коллагеновыми волокнами соединительной ткани. При развитии гипоксии раковые клетки молочной железы увеличивают синтез этого фермента, что способствует ремоделированию внеклеточного матрикса при подготовке уже другой преметастазной ниши – в легких.
При некоторых типах рака (например, меланоме) для успешного метастазирования в лимфатические узлы и органы необходимо, чтобы в их преметастазной нише сформировались новые лимфатические сосуды. Недавно было установлено, что такой лимфангиогенез начинается на ранних стадиях роста первичной опухоли, а медиатором его запуска является белковый фактор роста мидкин, секретируемый клетками меланомы (Olmeda et al., 2017).
Ученые провели интересный эксперимент: выделив экзосомы от раковых клеток разного происхождения (рака груди, поджелудочной железы и др.), они ввели их в кровоток лабораторных мышей, которым были привиты опухоли другого типа (Hoshino et al., 2015). Оказалось, что с помощью экзосом можно перепрограммировать распределение метастазов по органам.
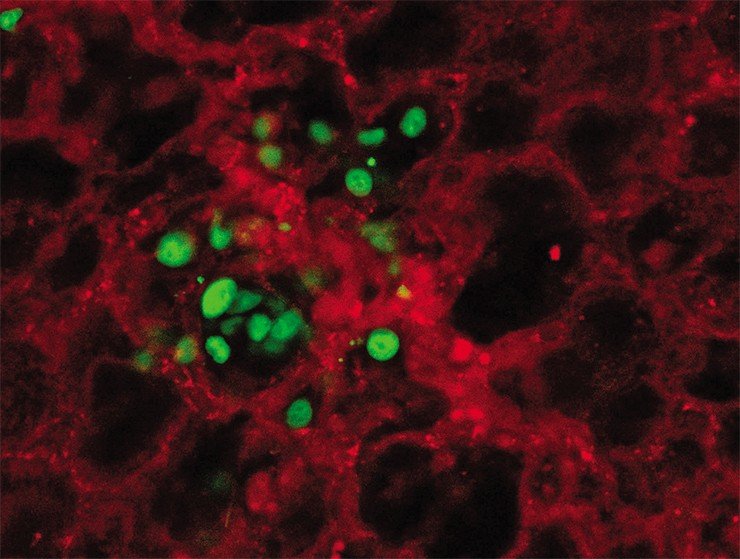
Подведем итог. Все описанные механизмы метастазирования, безусловно, усложняют картину течения онкозаболеваний и тактики их лечения. Особого внимания требует гетерогенность первичной опухоли и метастазов по ряду самых разных признаков, из чего следует необходимость использовать комбинированное и таргетное (направленное) лечение на разных стадиях течения болезни. Подтверждение этому – результаты одного из последних исследований, базирующихся на лечении онкологического пациента с рецидивами между курсами длительной иммунотерапии (Jiménez-Sánchez et al., 2017). Сравнение популяций T-лимфоцитов из микроокружения разных метастазов показало, что они гетерогенны. Следовательно, первичная, вторичные и последующие опухоли по-разному отвечают на лечение.
Alderton G. K. Tumour evolution: epigenetic and genetic heterogeneity in metastasis // Nat Rev Cancer. 2017. V. 17. N. 2. P. 141.
Cox T. R., Rumney R. M. H., Schoof E. M., et al. The hypoxic cancer secretome induces premetastatic bone lesions through lysyl oxidase // Nature. 2015. V. 522. N. 7554. P. 106—110.
Jiménez-Sánchez A., Memon D., Pourpe S., et al. Heterogeneous Tumor-Immune Microenvironments among Differentially Growing Metastases in an Ovarian Cancer Patient // Cell. 2017. V. 170. N. 5. P. 927—938.e20.
Hoshino A., Costa-Silva B., Shen T.-L., et al. Tumour exosome integrins determine organotropic metastasis // Nature. 2015. V. 527 N. 7578. P. 329—335.
Mlecnik B., Bindea G., Kirilovsky A., et al. The tumor microenvironment and Immunoscore are critical determinants of dissemination to distant metastasis // Sci Transl Med. 2016. V. 8. N. 327. P. 327ra26-327ra26.
Olmeda D., Cerezo-Wallis D., Riveiro-Falkenbach E., et al. Whole-body imaging of lymphovascular niches identifies pre-metastatic roles of midkine // Nature. 2017. V. 546 N. 7660. P. 676—680.
Rosen J. M., Jordan C. T. The increasing complexity of the cancer stem cell paradigm // Science. 2009. V. 324. N. 5935. P. 1670–1673.
Yates L. R., Knappskog S., Wedge D., et al. Genomic Evolution of Breast Cancer Metastasis and Relapse // Cancer Cell. 2017. V. 32. N. 2. P. 169—184.e7

- Что такое метастазы?
- Из-за чего возникают метастазы?
- С какой вероятностью возникают метастазы?
- От чего зависит скорость распространения метастазов по организму?
- Как метастазируют различные виды рака?
- Как проявляются метастазы?
- Как диагностируются метастазы?
- Можно ли вылечить метастазы, и что это дает?
- Где лучше лечить рак с метастазами — в Москве, в Израиле или в Германии?
Что такое метастазы?
Современные концепции развития метастазов основаны на том, что метастазы развиваются практически сразу, как только появляется сама злокачественная опухоль. Отдельные оторвавшиеся от нее клетки сначала проникают в просвет кровеносного (гематогенный путь диссеминирования) или лимфатического (лимфогенный путь диссеминирования) сосуда, а затем переносятся с током крови или лимфы, останавливаются на новом месте, выходят из сосуда и растут, образуя метастазы. Вначале этот процесс идет медленно и незаметно, поскольку раковые клетки из материнского очага подавляют активность вторичных очагов.
С момента, когда возникают вторичные очаги, рак называют метастатическим. Процесс распространения раковых клеток называют метастазированием.
Способность к метастазированию — один из ключевых признаков злокачественных опухолей, который отличает их от доброкачественных новообразований.
Из-за чего возникают метастазы?
Будут ли отдельные клетки отрываться от материнской опухоли и формировать метастазы? Опухолевые клетки отрываются и будут отрываться всегда. Местные факторы иммунной системы очень долгое время защищают организм от быстрого роста опухолевых клеток. Вопрос лишь в вероятности возникновения метастазов, а она зависит от типа опухоли, скорости ее роста, степени дифференцировки клеток (насколько они отличаются от нормальных), стадии, на которой был диагностирован рак, и других факторов.
Распространившись, опухолевые клетки долго, на протяжении ряда лет, могут оставаться неактивными или расти очень медленно. Точные механизмы запуска быстрого роста метастазов в организме не изучены.
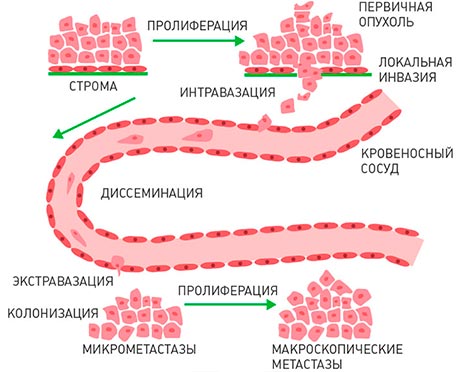
Важен другой факт: по мере увеличения числа клеток в метастазе, они начинают выделять особые вещества - факторы роста. Эти факторы роста стимулируют образование капиллярной сети, что обеспечивает клетки раковой опухоли всеми питательными веществами в ущерб остальным тканям организма.
Можно выделить несколько стадий распространения рака по организму:
- Проникновение опухолевых клеток в ближайший кровеносный или лимфатический сосуд;
- Распространение с током крови или лимфы по различным частям тела;
- Затем раковая клетка останавливается в одном из мелких сосудов и проникает через его стенку в ткани;
- Какое-то время она неактивна или размножается, но очень медленно;
- Бурный рост, разрастание капиллярной сети.
Многие опухолевые клетки погибают на одной из этих стадий. Те, которым удалось выжить, дают начало метастазам.
С какой вероятностью возникают метастазы?

От чего зависит скорость распространения метастазов по организму?
Время, необходимое для клинического проявления первых метастазов, во многом определяется видом опухоли и степенью дифференцировки её тканей.
- Высокодифференцированные опухоли, как правило, метастазируют гораздо реже и позднее, чем низкодифференцированные опухоли.
- В низкодифференцированных опухолях клетки практически утрачивают черты нормальной ткани. Такой рак ведет себя агрессивнее.
Вероятность метастазирования можно снизить при помощи разных методов лечения:
- Химиотерапия. Например, адъювантная химиотерапия проводится после операции и помогает уничтожить раковые клетки, которые, возможно, остались в организме.
- Лучевая терапия.
Существует такое заблуждение, что метастазы возникают из-за проведенных процедуры. Однако, удаление части опухоли или ее биопсия (взятие ткани опухоли на исследование) не повышают частоту развития метастазов.
Как метастазируют различные виды рака?
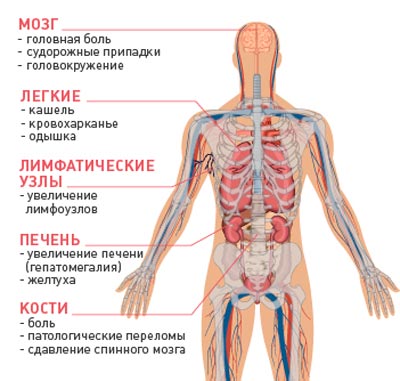
Наиболее часто метастазы обнаруживаются в лимфатических узлах, печени, легких, существенно реже — в мышце сердца, скелетных мышцах, коже, селезенке, поджелудочной железе. Промежуточное место по частоте обнаружения метастазов при различных видах рака занимают центральная нервная система, костная система, почки, надпочечники.
- Метастаз Крукенберга — в яичники;
- Метастаз сестры Марии Джозеф — в пупок;
- Метастаз Вирхова — в лимфоузлы над левой ключицей.
- Рак молочной железы: легкие, печень, кости.
- Рак яичников: брюшина, печень, легкие.
- Рак желудка: печень, брюшина, легкие.
- Рак кишечника (толстой кишки): печень, брюшина, легкие.
- Рак прямой кишки: печень, легкие, надпочечники.
- Рак предстательной железы: кости, легкие, печень.
- Рак матки: печень, легкие, брюшина.
- Рак почек: легкие, печень, кости.
- Рак легкого: надпочечники, печень, второе легкое.
- Меланома: легкие, кожа/мышечные ткани, печень.
- Рак поджелудочной железы: печень, легкие, брюшина.
- Рак щитовидной железы: легкие, печень, кости.
Метастазирование, как правило, происходит в случаях, когда исчерпаны резервы организма в борьбе с опухолью. Метастазы существенно нарушают функционирование всех жизненно важных органов и систем. В подавляющем большинстве смерть онкологических пациентов обусловлена именно метастазами.
Кроме того, метастазы существенно ухудшают общее состояние, нередко сопровождаясь нестерпимыми болями, требующими постоянного обезболивания.
Как проявляются метастазы?
Клиническая картина метастатического рака определяется местом расположения метастазов:
- Поражение брюшины (канцероматоз брюшины) приводит к возникновению асцита, что требует проведения лапароцентеза;
- Поражение плевры (канцероматоз плевры) вызывает развитие экссудативного плеврита, который требует выполнения торакоцентеза;
- Поражение костей и позвоночника ведет к болям в разных частях тела, переломам;
- Поражение легких проявляется в виде одышки;
- Метастазы головного мозга приводят к головным болям, головокружениям, судорогам, нарушению сознания;
- Поражение печени приводит к механической желтухе.
Кроме того, высвобождающиеся в ходе постоянной гибели опухолевых клеток токсины вызывают раковую интоксикацию организма.
Как диагностируются метастазы?
Обзорная рентгенография, ультразвуковое исследование, радиоизотопное исследование, компьютерная томография, магнитно - резонансная томография, позитронно - эмиссионная томография, — все эти методики имеют существенное значение в распознавании метастазов. Эти методики дают возможность уточнить величину, распространенность и характер роста метастазов, их распад, нагноение, прорастание в соседние органы и ткани. Кроме того, эти же методики диагностики позволяют контролировать эффективность лечения по степени регресса метастазов.
Условно можно выделить два этапа диагностики метастазов:
- Первичное обследование, когда только диагностирована основная опухоль;
- Наблюдение у онколога после пройденного лечения. Если изначально метастазы обнаружены не были, а лечение прошло успешно, в будущей все равно придется периодически проходить обследования - есть риск рецидива.
Можно ли вылечить метастазы, и что это дает?
Основной целью активной химиотерапии и лучевой терапии является профилактика возникновения метастазов рака на максимально ранней стадии. Лечение основано на общих принципах лечения опухолей, включая химиотерапию, лучевую терапию, оперативное лечение (при одиночных метастазах).
Лечение метастазов рака имеет определенные сложности. Поэтому в ряде случаев мы проводим лечение метастазов с целью облегчения симптомов и продления жизни. Мы используем системную терапию (химиотерапия, гормонотерапия, таргетная терапия), и местные виды лечения (хирургия, радиотерапия). Лечение тормозит рост опухоли, уменьшает ее размеры, замедляет процесс метастазирования. Это помогает подарить пациенту лишние месяцы, а иногда и годы.
Параллельно проводят поддерживающую терапию, которая помогает справиться с симптомами и побочными эффектами химиотерапии. При болях назначают сильные обезболивающие средства.
За рубежом при метастатических очагах в печени часто используют чрескожную чреспеченочную радиочастотную аблацию. Данная методика доступна нашим пациентам в Европейской клинике.
Как говорилось выше, лечение в таких случаях является средством облегчения состояния пациента. Вероятность достижения ремиссии очень мала.
Мы в Европейской клинике также используем такую методику как эмболизация артерий, питающих крупные метастазы в различных органах.
Узнайте о современных методах лечения метастазов рака в печени, которые применяют врачи Европейской клиники, а также о результатах лечения - историях пациентов Европейской клиники.
Где лучше лечить рак с метастазами — в Москве, в Израиле или в Германии?
Для того чтобы получить наиболее современное и эффективное лечение при раке с метастазами, российскому пациенту не обязательно ехать за границу. В Европейской клинике применяются те же препараты и технологии, что и в ведущих онкологических центрах мира.
Даже если вероятность ремиссии мала, лечение нужно продолжать. Врачи-онкологи Европейской клиники знают, как облегчить страдания пациента, продлить жизнь. Для этого мы используем наиболее современные методики и препараты. Если вы проходите курс лечения в другой клинике, у нас всегда можно получить второе врачебное мнение: иногда подходы разных врачей к лечению метастатического рака сильно различаются.
Выберите врача и запишитесь на приём:

Главный врач Европейской клиники, онколог, к.м.н.
Все опухоли делятся на доброкачественные и злокачественные.
Название доброкачественных опухолей состоит из названия ткани и суффикса –ома. Например:
- Фиброма – доброкачественная опухоль соединительной ткани.
- Липома – доброкачественная опухоль из жировой ткани.
- Аденома – доброкачественная опухоль из железистой ткани.
- Миома – доброкачественная опухоль из мышечной ткани. Если это поперечно-полосатая мышечная ткань (например, мышцы рук и ног), то доброкачественная опухоль называется рабдомиома. Если же гладкая мускулатура (в стенках артерий, кишечника) - опухоль называется лейомиома.
Если в доброкачественной опухоли имеется сочетание клеток разных тканей, то названия звучат соответствующим образом: фибромиома, фиброаденома, фибролипома и т.д.
О классификации злокачественных опухолей будет рассказано в третьей части цикла.
В прошлый раз я уже писал о свойствах опухолевых клеток. Давайте повторим и углубим наши знания.
-
Атипия (необычность) и полиморфизм (разнообразие) клеток.
Клетки доброкачественной опухоли похожи по структуре и функции на клетки нормальных тканей организма. Отличия от здоровых клеток минимальны, хотя они есть. Степень развития клеток называется дифференцировкой. Клетки доброкачественных опухолей являются высокодифференцированными.
Клетки злокачественных опухолей значительно отличаются по строению и функции от нормальных, являясь средне- или низкодифференцированными. Иногда изменения настолько большие, что под микроскопом трудно или даже невозможно разобраться, из какой ткани или органа развилась опухоль (подобные клетки называют недифференцированными). Недифференцированные клетки очень часто делятся, поэтому по внешнему виду не успевают превратиться в обычные. Внешне они похожи на стволовые клетки. Стволовые клетки являются нормальными (материнскими) клетками, из которых, пройдя несколько этапов деления, развиваются обычные клетки.

Benign - доброкачественная: клетки похожи друг на друга и на нормальную ткань.
Malignant - злокачественная.
Клетки злокачественной опухоли всегда выглядят уродливо и разнообразно.
Для идентификации недифференцированных клеток при необходимости используют биохимические, цитогенетические методы определения вида ткани. Характер роста.
Доброкачественные опухоли имеют экспансивный рост: опухоль медленно увеличивается и раздвигает окружающие ткани и органы.

Известная картинка, где видно, почему опухоль называют "раком".
Итак, доброкачественные опухоли при своем росте РАЗДВИГАЮТ здоровые ткани, а злокачественные – ПРОРАСТАЮТ свозь них. Метастазирование.
Метастазы – это очаги отсева опухоли, метастазирование - сам процесс образования метастазов. В результате роста опухоли ее отдельные клетки могут отрываться, попадать в кровь, лимфу и переноситься в другие ткани. Там они вызывают рост вторичной (дочерней) опухоли. По структуре метастазы обычно не отличаются от родительской опухоли.
Метастазируют только злокачественные опухоли. Доброкачественные опухоли метастазов не дают.
Основные пути метастазирования:
-
Лимфогенный (с лимфой по лимфатическим сосудам). Самый частый способ. Лимфоузлы являются барьером для всего чужеродного организму: инфекции, опухолевых (измененных) клеток, инородных частиц. Попадая в местные (регионарные) лимфоузлы, большинство опухолевых клеток там задерживается и постепенно уничтожается макрофагами (это разновидность лейкоцитов). Если же клеток очень много, лимфоузлы не справляются.

Злокачественная опухоль прорастает в окружающие ткани.
Лимфатические сосуды забиты конгломератами опухолевых клеток
(показаны красными стрелками).
Кликните по рисунку, чтобы его увеличить.
Если же опухоль была удалена не полностью, ее повторный рост не считается рецидивом. Это проявление прогрессирования патологическогог процесса. Общее влияние на больного.
Доброкачественные опухоли проявляются местно: причиняют неудобство, сдавливают нервы, сосуды и окружающие органы. От доброкачественных опухолей умирают в исключительных случаях:
- Медленное сдавление головного мозга с жизненно важными центрами
- Опухоли эндокринных органов бывают опасными: например, феохромоцитома (доброкачественная опухоль из мозгового слоя надпочечников) обнаруживается у 1 из 250 больных артериальной гипертензией. Она вырабатывает и временами выбрасывает в кровь адреналин и норадреналин, что вызывает резкое повышение артериального давления, сердцебиение, потливость, головную боль. Особенно опасна феохромоцитома для роженицы и плода (для справки: беременная во время родов до рождения плода называется роженицей, после рождения – родильницей)
Злокачественные опухоли вызывают раковую интоксикацию (интоксикация – отравление, от слова токсин – яд), вплоть до раковой кахексии (кахексия - истощение). С чем это связано?
- Клетки злокачественного новообразования быстро делятся и растут, они расходуют много питательных веществ (глюкоза, аминокислоты). Естественно, что нормальным тканям не хватает. Больной чувствует слабость, вялость, недомогание, он худеет.
- Кроме этого, при быстром росте опухоли кровеносные сосуды в ней не успевают образовываться в нужном количестве. Поэтому из-за недостатка кислорода центр опухоли погибает (это называется некроз, или омертвение). Продукты распада клеток всасываются в кровь и отравляют организм (раковая интоксикация), происходит потеря аппетита, интереса к жизни, больной становится бледным.

Кахексия бывает разного происхождения (опухоли, заболевания кишечника и др.)
Кроме этого, любое (!) повреждение и гибель (некроз) клеток вызывает воспалительную реакцию. Вокруг места некроза развивается воспаление. Из-за этого у тяжелых раковых больных может повышаться температура. C другой стороны, проводимое лечение угнетает иммунную систему, из-за чего онкобольные больше подвержены разным инфекциям.
Из-за чего у некоторых онкологических больных бывают сильнейшие боли, которые снимаются только наркотиками?
- Прорастание и разрушение опухолью других тканей и органов, мелких нервов и крупных нервных стволов.
- Сдавление окружающих тканей, что вызывает в них ишемию (недостаток кислорода) и боли.
- Некроз (омертвение) в центре опухоли вызывает сильнейшие боли. По своему механизму возникновения и силе эти боли похожи на боли при инфаркте миокарда, которые также купируются (снимаются) наркотиками.
Еще раз вспомним, что мы сегодня усвоили.
Отличия доброкачественных и злокачественных опухолей кратко сформулированы в таблице:
В настоящее время врачи ведущих клиник мира применяют инновационные методы лечения рака, которые повышают выживаемость пациентов с метастазами. Успехов в лечении метастатического рака достигли онкологи Юсуповской больницы. В больнице применяются современные методики терапии и диагностики, благодаря чему количество больных, которым удалось продлить жизнь и повысить её качество, за последние годы увеличилось. Врачи Юсуповской больницы применяют комплексное лечение, учитывая общее состояние пациента, локализацию опухоли и активность ее метастазирования.
Проблема метастатического рака
Что собой представляют метастазы рака
Рак бывает первичным, когда опухоль образуется в органе, и метастатическим (Metastasis по гречески означает перемещение), когда опухолевые клетки поражают другие органы. Независимо от размеров первичной опухоли, наличие отдаленных метастазов говорит о IV стадии рака.
Довольно часто врачи впервые определяют метастазы, не диагностировав первичную опухоль. Это случается в случае таких видов онкологической патологии:
- рак молочной железы;
- меланома кожи;
- рак шейки матки;
- рак простаты
- рак желудка
- рак предстательной железы
- рак поджелудочной железы
Как атипичные клетки, из которых состоит раковая опухоль, попадают из одного органа в другой? Известны 3 пути метастазирования рака: лимфогенный, с током лимфы, гематогенный, с кровью и имплантационный.
Попадая в кровь или лимфу, раковые клетки разносятся по всему организму, оседая в различных органах. Там они начинают быстро делиться и образуют метастазы. Эпителиальный рак преимущественно метастазирует по лимфатическим сосудам. Для меланомы и различного вида сарком характерный гематогенный путь метастазирования. Метастазы при раке желудка выявляют по путям оттока лимфы.
На процесс распространения метастаз влияют иммунные и биологические процессы. Одни из них способствуют распространению атипичных клеток, а другие блокируют их. В связи с этим процесс метастазирования может быть или активным, или замедленным. Это во многом зависит от степени злокачественности опухолевых клеток.
Скорость распространения метастаз зависит от многих факторов:
- кровоснабжения органа;
- путей лимфооттока;
- степени злокачественности атипичных клеток;
- состояние иммунной системы.
- Возраст пациента
На интенсивность метастазирования также влияют вирусные инфекции, интоксикация, употребление алкоголя, неправильное питание. Противораковый иммунитет ослабляет хронический нервный стресс и нарушение кровоснабжения (облитерация периферических сосудов).
Метастазируют опухоли независимо от локализации в любой орган. Наиболее часто поражаются метастазами:
- печень;
- почки;
- лёгкие;
- центральная нервная система;
- костная система (позвоночник, рёбра, кости черепа, таза и конечностей, грудина);
- яичники
Симптомы метастатического рака
При наличии метастаз речь идёт о запущенной стадии заболевания. Она проявляется такими общими признаками:
- нарушение сна;
- снижение массы тела;
- ухудшение аппетита;
- головные боли;
- выраженная или общая слабость;
- анемия;
- повышение температуры тела.
- Лихорадка, озноб
- диарея, запоры
- тошнота, рвота
Как выглядят метастазы? Местные симптомы зависят от локализации метастаз. При наличии метастатических очагов в лёгких пациентов беспокоит кашель, боль в грудной клетке и одышка. Метастазы в мягких тканях выявляют при меланоме. Когда диагностированы метастазы в печени, симптомы будут следующие:
- боль в правом подреберье;
- увеличение живота в объеме;
- желтушность кожных покровов и сслизистых
- горечь во рту
- зуд кожи
Могут быть метастазы в поджелудочной железе. Когда имеется рак почки, метастазы выявляют в печени, лёгких, головном мозге. Головные боли, головокружение, периодическая рвота, приступы судорог, расстройства чувствительности, памяти, речи, слуха и зрения – это признаки метастазов в головной мозг.
Особо коварные метастазы в позвоночник. Сначала они имеют симптомы, сходные с признаками остеохондроза, не вызывая у больного опасения. Люди не знают, как отличить остеохондроз от метастазов. И только после того, как появляется слабость мышц конечностей, возникают парезы и параличи, врачи обнаруживают значительные изменения в позвонках и признаки сдавления спинного мозга.
Метастазы. Диагностика
В Юсуповской больнице врачи диагностируют метастатический рак, применяя современные методы исследования:
- томографические (МРТ, КТ, ПЭТ-КТ);
- сцинтиграфию костей скелета;
- Ультразвуковое исследование;
- различные диагностические пункции под визуальным контролем томографа;
- полное лабораторное исследование, в том числе определение уровня онкомаркеров в биологических жидкостях, иммунологическое и молекулярно-генетическое;
- эндоскопическую (гастроскопию, бронхоскопию, колоноскопию) диагностику с биопсией;
Лечение метастаз
При лечении метастазов сегодня применяются новейшие достижения молекулярной биологии. Созданы медикаменты, замедляющие рост и уничтожающие клетки метастаз. Врачи Юсуповской больницы применяют комплексное лечение, учитывающее общее состояние здоровья пациента, локализацию основной, вторичной опухоли и их активность метастазирования.
Онкологи Юсуповской больницы применяют индивидуальный подход в лечении пациентов: разрабатывают схему лечения, подбирают максимально подходящие препараты, в зависимости от стадии развития патологического процесса и места расположения злокачественных образований, а также степени поражения здоровых тканей и органов.
Читайте также:

