Андрогенпродуцирующие опухоли у женщин признаки
Гормонально активные опухоли коры надпочечников могут вырабатывать в избыточном количестве кортизол или альдостерон, или андрогены. В первом случае развивается синдром Иценко - Кушинга, во втором - первичный альдостеронизм (синдром Конна). К андрогено-продуцирующим опухолям коры надпочечников относятся те опухоли, которые секретируют в повышенном количестве главным образом или исключительно стероиды, обладающие андрогенным действием.
Патологическая анатомия
Андростеромы - опухоли, вырабатывающие андрогены, бывают доброкачественными и злокачественными. Доброкачественные андростеромы построены в основном из темных клеток, иногда образующих тяжистые структуры, напоминающие сетчатую зону коры надпочечников. Клетки и их ядра отличаются большим полиморфизмом. Большинство ядер гиперхромны, но встречаются и крупные светлые ядра. Липоидов в ткани опухоли мало, встречаются глыбки извести.
Злокачественные андростеромы построены из клеточных элементов, близких тем, из которых состоят соответствующие доброкачественные опухоли, но отличаются большим полиморфизмом ядер, большим количеством многоядерных гигантских клеток, наличием некрозов и кровоизлияний, инфильтрирующим ростом. Митозы встречаются редко, часто встречаются фигуры амитотического деления клеток. Злокачественные опухоли заключены в соединительнотканную капсулу, но местами наблюдается прорастание капсулы опухолевыми клетками и врастание их в окружающие органы, чаще всего в почки; наблюдается также прорастание нижней полой вены. Злокачественные опухоли метастазируют в печень, почки, легкие, кости, лимфатические узлы, второй надпочечник, брюшину, мозг и другие органы.
Клиническая картина
При вирилизирующих опухолях коры надпочечников определяется специфическим гормональным действием стероидов, обладающих гормональной активностью, которые в избыточном количестве вырабатываются клетками опухоли.
При развитии опухоли в детском возрасте у девочек отмечается быстрый рост и ускоренное созревание скелета, развитие мускулатуры, появление acne, растительности на теле, огрубение голоса, гипертрофия клитора. У мальчиков наблюдается картина преждевременного полового созревания по изосексуальному типу, однако яички остаются атрофичными. Как у мальчиков, так и у девочек ускоряется физическое развитие и созревание скелета. Психическое развитие ребенка обычно соответствует его истинному возрасту.
У женщин при развитии андрогено-продуцирующей опухоли коры надпочечников наблюдается дефеминизация - менструации делаются редкими и скудными, а затем наступает аменорея, молочные железы атрофируются. Размеры матки уменьшаются, клитор гипертрофируется. Наряду с этим появляются мужские вторичные половые признаки - растительность на лице и на теле, угри на лице; может иметь место облысение головы по мужскому типу. Голос делается низким. Мышцы гипертрофируются, мышечная сила повышается. Черты лица грубеют, омужествляются. Вследствие развития мускулатуры и перераспределения отложения жира в подкожной клетчатке, а также в связи с атрофией молочных желез изменяются контуры тела - телосложение приближается к мужскому.
У взрослых мужчин клинические признаки андрогено-продуцирующей опухоли коры надпочечников трудно улавливаются. В отдельных случаях эти опухоли у мужчин проходят под видом гормонально неактивных опухолей надпочечников и, возможно, даже под видом неправильно трактуемых опухолей почки.
Ввиду того, что при опухолях коры надпочечников, продуцирующих преимущественно андрогены, нередко имеет место в большей или меньшей степени повышение продукции других гормонов коры надпочечников, у некоторых больных, наряду с вирилизацией, наблюдаются и другие признаки гиперкортицизма.
Гормональные исследования
При гормональном исследовании наиболее характерным признаком андрогено-продуцирующей опухоли коры надпочечников является повышенное выделение мочой 17-кетостероидов, иногда умеренное - до 50-60 мг/24 ч, иногда - очень значительное - до нескольких сотен и даже до 1000 мг/24 ч. При фракционировании 17-кетостероидов можно отметить изолированное повышение выделения бета-фракции, имеющей надпочечниковое происхождение. Особое значение имеет повышение продукции одного из кетостероидов - дегидроэпиандростерона, которое особенно свойственно андрогено-продуцирующим опухолям коры надпочечников.
Наряду с этим, в случаях, когда клетки опухоли вырабатывают в избыточном количестве не только стероиды, обладающие андрогенной активностью, а в той или иной степени и другие кортикостероиды, может иметь место повышенное содержание в крови и выделение мочой 17-гидроксикортикостероидов и в частности кортизола.
У некоторых больных наблюдается повышенное выделение мочой эстрогенов. Учитывая, что эстрогены вырабатываются в надпочечниках теми же клетками, что и 17-кетостероиды и продукция их надпочечниками повышается при стимуляции надпочечников адренокортикотропным гормоном, можно предполагать, что повышенное выделение эстрогенов у этих больных связано с повышенной их выработкой клетками опухоли.
В ряде случаев значительно повышается выделение мочой прегнандиола.
Диагноз и дифференциальный диагноз
Диагноз андрогено-продуцирующих опухолей коры надпочечников основывается в первую очередь на характерной клинической картине - появлении признаков вирилизации у девочек и женщин, не имевших до начала заболевания нарушений со стороны половой системы, и преждевременном половом развитии у мальчиков, сопровождающемся атрофией тестикул. Наиболее существенным лабораторным признаком андрогено-продуцирующей опухоли коры надпочечников является повышение выделения мочой 17-кетостероидов и специально дегидроэпиандростерона.
При дифференциальной диагностике опухолей коры надпочечников может быть использована и проба с введением АКТГ. У больных с опухолями после введения АКТГ выделение 17-кетостероидов не изменяется, в то время как у больных с гиперплазией коры надпочечников увеличивается.
Важным диагностическим методом, позволяющим не только установить наличие опухоли коры надпочечников, но и уточнить ее локализацию, является рентгеновское исследование. Рентгеновские снимки области почек и надпочечников производятся после введения газа в клетчатку, окружающую эти органы. Газ можно вводить как непосредственно в околопочечную клетчатку, так и в забрюшинную клетчатку пресакральным проколом. Последний метод введения газа предпочтительнее, так как при нем газ попадает в область обеих почек. На фоне введенного газа контурируются почки и надпочечники и может быть обнаружена опухоль.

На рисунке: Оксисупраренорентгенограмма гормонально активной опухоли левого надпочечника. Левая почка оттеснена кнаружи и вниз.
Эффективность метода повышается при использовании помимо обычных обзорных снимков томограмм.
Это исследование целесообразно сочетать с экскреторной урографией или ретроградной пиелографией, позволяющими выявить некоторые косвенные признаки опухоли надпочечников, в частности смещение или деформацию почек.
Этот метод исследования безопасен. При использовании в качестве контурирующего газа не воздуха, а кислорода или углекислого газа и введении его через пресакральный прокол опасность воздушной эмболии практически отсутствует.
Однако с помощью рентгеновского исследования удается достоверно установить наличие только относительно крупных опухолей, и, по данным некоторых авторов, частота выявления опухоли с помощью оксисупрарентгенографии не превышает 50%. Косвенные данные о наличии опухоли, если она не контурируется, можно получить на основании обнаружения смещения почек.
Приведенные методы исследования направлены в основном на дифференциальную диагностику опухолей коры надпочечников и других вирильных синдромов, связанных с патологией надпочечников, в частности врожденной вирилизирующей гиперплазии коры надпочечников. Наряду с этим, вирилизирующие опухоли коры надпочечников необходимо дифференцировать с вирилизацией, связанной с заболеванием половых желез.
У больных с андрогено-продуцирующими опухолями яичников - арренобластомами (или андробластомами), липидоклеточными опухолями может развиваться вирильный синдром, клинически трудно отличимый от адрено-генитального синдрома, в частности от синдрома, развивающегося у больных вирилизирующими опухолями коры надпочечников. Дифференциальный диагноз этих заболеваний основывается на данных физикального исследования - обнаружения опухоли яичника при гинекологическом обследовании или опухоли надпочечника при оксисупрарентгенографии, а также на данных гормонального исследования. При аренобластомах яичников выделение 17-кетостероидов может быть нормальным или умеренно повышенным; повышение выделения 17-кетостероидов при этом не соответствует степени вирилизации. Возможно, это связано с тем, что вирилизация у больных аренобластомой связана не столько с выработкой клетками опухоли 17-кетостероидов, сколько с выработкой тестостерона, обнаруживаемого в ткани опухоли. Повышение же количества тестостерона мало влияет на выделение 17-кетостероидов.
Статьи по теме:
- Физиология коры надпочечников
- Хроническая недостаточность коры надпочечников. Аддисонова болезнь
- Кровоснабжение и иннервация надпочечников
- Клиническая оценка лабораторных методов исследования функционального состояния коры надпочечников
- Определение кортикостероидов и их метаболитов в моче
- Диагноз и дифференциальный диагноз врожденной гиперплазии коры надпочечников
- Лечение хронической недостаточности надпочечников
- Апоплексия коры надпочечников. Синдром Уотерхауза–Фридериксена (waterhouse- friderichsen)
- Врожденная вирилизирующая гиперплазия коры надпочечников
- Лечение врожденной гиперплазии коры надпочечников
- Острая недостаточность коры надпочечников
Определенное значение может иметь фракционирование 17-кетостероидов. Если при опухолях коры надпочечников обычно отмечается значительное повышение выделения дегидроэпиандростерона, то при аренобластомах повышается преимущественно выделение андростерона и в меньшей степени этиохоланолона.
У больных липидоклеточными вирилизирующими опухолями яичников выделение 17-кетостероидов может быть как нормальным, так и значительно повышенным и такое исследование не может служить целям дифференциальной диагностики этого редкого заболевания и вирилизирующих опухолей коры надпочечников.
При склерокистозных яичниках вирилизация редко бывает настолько выраженной, чтобы возникла необходимость в дифференциальном диагнозе между этим заболеванием и вирилизирующей опухолью коры надпочечников.
Необходимо иметь в виду, что склерокистозные яичники могут развиваться у больных вирилизмом надпочечникового происхождения. Суммарное выделение 17-кетостероидов у больных склерокистозными яичниками обычно бывает нормальным или незначительно выше нормы (в отличие от больных с опухолями коры надпочечников). При фракционном разделении 17-кетостероидов у больных склерокистозными яичниками отмечается повышение выделения андростерона и этиохоланолона, а не дегидроэпиандростерона, как у больных с вирилизирующими опухолями коры надпочечников.
Дифференциальный диагноз преждевременного полового созревания в связи с опухолью яичек основывается на обнаружении в последнем случае пальпируемой опухоли. Повышение выделения 17-кетостероидов при опухоли яичек меньше, чем при опухоли надпочечников.
Лечение
Лечение вирилизирующих опухолей коры надпочечников хирургическое. В случае, когда клетки опухоли избирательно вырабатывают в избыточном количестве только стероиды, обладающие андрогенным действием, а продукция гликокортикоидов нормальная, торможения адренокортикотропной функции гипофиза и связанной с этим атрофии второго надпочечника не наступает. При этом отсутствует опасность гипокортицизма в послеоперационном периоде. Однако как клинически, так и при гормональном обследовании далеко не всегда можно исключить у больных вирилизирующими опухолями коры надпочечников известную степень повышения продукции кортизола. Поэтому более безопасно оперативное вмешательство по поводу вирилизирующих опухолей коры надпочечников проводить на фоне лечения кортизолом, так как это рекомендуется при операциях по поводу опухолей коры надпочечников, протекающих с синдромом Иценко- Кушинга. Дозы стероидных препаратов при этом могут быть несколько меньшими. После операции дозы кортикостероидов постепенно снижаются. Скорость отмены препаратов определяется наличием или отсутствием симптомов недостаточности коры надпочечников.
Нарушение репродуктивной функции женщины может явиться следствием повышения уровня мужских половых гормонов в крови (андрогенов), избыток которых в организме женщины связан с нарушением работы яичников или надпочечников, которые ответственны за выработку этих гормонов.
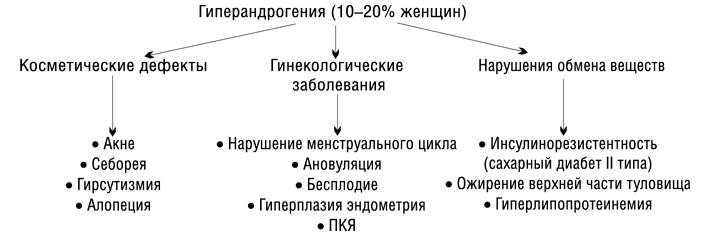
Остановимся коротко на основных терминах, которые используются при данной патологии.
Гиперандрогенемия — повышенная концентрация андрогенов в сыворотке крови, которая проявляется, в большинстве случаев, андрогенизацией (гирсутизм, алопеция, угревая сыпь). Так, частота гирсутизма при гиперандрогении составляет около 80%.
Андрогенизация — проявление симптомов, типичных для высокого уровня андрогенов (гирсутизм, алопеция, угревая сыпь и вирилизация).
Гирсутизм – заболевание, при котором у женщин рост и распределение терминальных волос происходит по мужскому типу.
Алопеция — видимое на глаз разрежение волос на голове с появлением проплешин. Наиболее частая форма – андрогенетическая алопеция (распространенность составляет 30-40%), чаще наблюдается у женщин в перименопаузе (за счёт физиологического повышения уровня андрогенов).
Угри (акне) — заболевание сальных желез волосяных фолликулов. Распространенность обыкновенных угрей среди подростков составляет 35-90% . У юношей акне наблюдается чаще, чем у девушек, а в более позднем возрасте соотношение мужчин и женщин с угревой сыпью обратное –у женщин больше, чем мужчин. С возрастом частота акне уменьшается: у женщин 20-29 лет она составляет 51%, старше 50 лет – 15%.
Вирилизация — появление у женщин мужских черт телосложения и мужских вторичных половых признаков (низкий тембр голоса, увеличение гортани, мужские пропорции тела, увеличение клитора гирсутизм).
Гиперадрогения – андрогенизация без повышения уровня андрогенов в крови (гиперандрогенемии).
Гипертрихоз — рост волос на участках тела, не характерный для данного пола, и появление терминальных волос на участках, где в норме растут пушковые волосы.
Симптомы андрогенизации – одна из причин обращения к гинекологу за консультацией. Данные симптомы могут встречаться при следующих заболеваниях:
- синдром поликистозных яичников (СПКЯ) (см. раздел СПКЯ);
- врожденный адреногенитальный синдром (АГС);
- андрогенпродуцирующия опухоль яичника (редкая опухоль – 1% от всех опухолей яичника);
- синдром Кушинга.
При симптомах андрогенизации необходимо сдать следующие анализы на гормоны: общий тестостерон, ДГЭАС, 17 – ОНР, эстрадиол, ЛГ, ФСГ, ТТГ, пролактин, кортизол. При необходимости на втором этапе проводят пробы с дексаметазоном, пробу с гормоном АКТГ.
Внизу остановимся коротко на каждом из этих заболеваний.
Врожденный АГС, или врожденная гиперплазия надпочечников — общее название нескольких наследуемых дефектов ферментов, участвующих в биосинтезе кортизола в надпочечниках. Наиболее частым из них является недостаточность фермента 21 – гидроксилазы (в 95% случаев). В зависимости от степени недостаточности дефектного фермента различают тяжелую (классическую) и легкую (неклассическую, или позднею) формы АГС.
- минералокортикоиды синтезируются в клубочковой зоне,
- глюкокортикоиды – в пучковой,
- половые гормоны — в сетчатой зоне.
Главными источниками половых гормонов являются половые железы. Продукции половых гормонов корой надпочечников придают функ-циональное значение только в необычных условиях, когда на путях биосинтеза в надпочечных железах появляются дефекты ферментов.
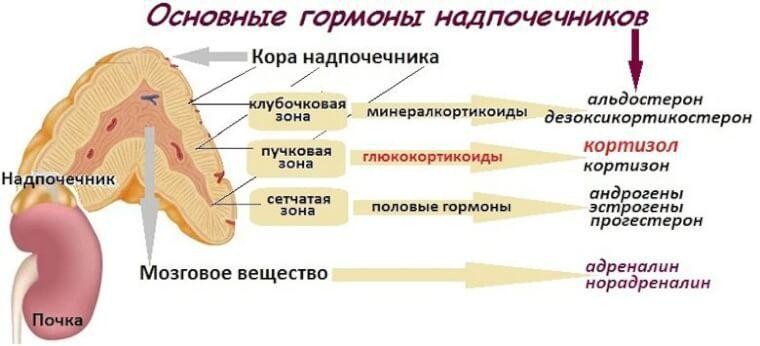
При АГС, в зависимости от дефектного фермента, отмечаются различные типы нарушения биосинтеза стероидных гормонов.
Внизу представлена схема образования гормонов с участием различных ферментов.
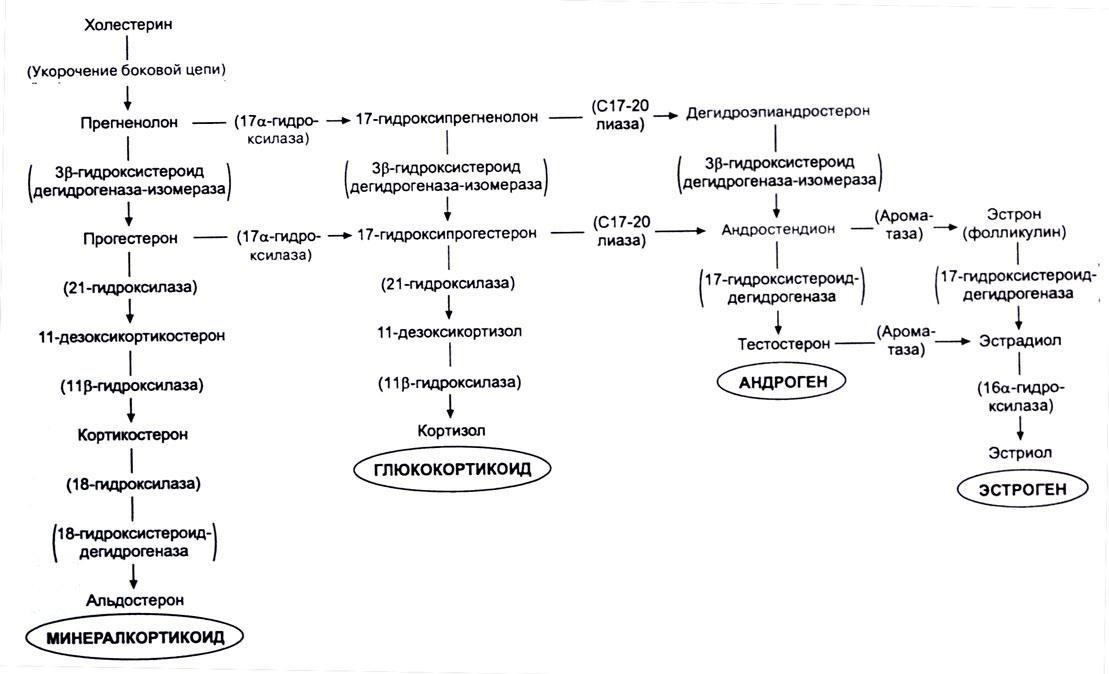
Например, при недостаточности фермента 21 – гидроксилазы, нарушается превращение 17 – ОНР (17 – гидроксипрогестерона) в 11 – дезоксикортизол, в результате снижается синтез кортизола в надпочечниках, в ответ повышается секреция АКТГ гипофизом. АКТГ стимулирует кору надпочечников, в результате чего, из 17 – ОНР синтезирируются андрогены, уровень которых повышается.
Лабораторная диагностика непосредственно гиперандрогенемии основывается на определении общего тестостерона, ДГЭАС и 17 – ОНР.
При определении концентрации андрогенов в сыворотке крови, говорить о принадлежности этих гормонов к тому или иному секретирующему органу — надпочечникам или половым железам, можно лишь условно.
Так, 50% ДГЭАС образуется в коре надпочечников, 25% в яичниках и 25% в периферических тканях. 50% тестостерона синтезируется в периферических тканях, остальное количество – в яичниках 25% и коре надпочечников 25%.
Классическая форма АГС обычно диагностируется в детстве, и поэтому рассматривать ее мы не будем.
Неклассическая (поздняя, или легкая) форма АГС проявляется только клиническими признаками избыточной выработки андрогенов, усиливающимися с возрастом. Клинические признаки избытка андрогенов у подростков и взрослых: угри – 30% случаев, гирсутизм – 60-90% случаев, алопеция – меньше 10% случае, нарушение менструального цикла, например олигоменорея – 55% случаев или аменорея – 5% случаев, бесплодие – 15% случаев.
Следует обратить внимание, что для уменьшения проявлений андрогенизации, глюкокортикоиды не являются препаратами выбора. При бесплодии, для стимуляции овуляции кортикостероиды применяются только в случае АГС с поздним началом. Обычно назначают гидрокортизон в дозе 10-20 мг 2 раза в сутки или дексаметазон в дозе 0,25- 0,5 мг 1 раз в сутки.
Андрогенпродуцирующие опухоли проявляются быстрым проявлением симптомов андрогенизации. В том случае, если уровень андрогенов невысокий, но гирсутизм или вирилизация прогрессируют, то в первую очередь, следует исключить андрогенпродуцирующую опухоль. Опухоли поражают в основном яичники и реже выявляются в надпочечниках.
Диагностика: УЗИ яичников, МРТ надпочечников.
Синдром Кушинга
Синдром гиперкортицизма или синдром Иценко — Кушинга объединяет группу заболеваний, при которых происходит длительное хроническое воздействие на организм избыточного количества гормонов коры надпочечников, независимо от причины, которая вызвала повышение количества этих гормонов в крови. В основе патологических изменений со стороны большинства органов и систем, при синдроме Кушинга, в первую очередь, лежит гиперпродукция кортизола.
Синдром Кушинга также может возникать при первичном поражении коры надпочечников (при доброкачественных или злокачественных опухолях коры надпочечников, при гиперплазии коры надпочечников).
Гормонально-активная опухоль коры надпочечника называется кортикостеромой. Она продуцирует в кровь избыточное количество глюкокортикоидов. При этом, из-за избыточного количества глюкокортикоидов, по механизму обратной связи, снижается количество адренокортикотропного гормона гипофиза, а оставшаяся ткань надпочечников подвергается атрофическим изменениям.
Синдром гиперкортицизма может возникнуть при лечении различных заболеваний гормонами коры надпочечников — глюкокортикоидами, в случае, если происходит передозировка этих препаратов. Это является частым вариантом, с которым сталкиваются врачи большинства специальностей. Болеют в основном лица в возрасте 20—40 лет.
Помимо синдрома, отдельно выделяют болезнь Иценко — Кушинга — это нейроэндокринное заболевание, характеризующееся повышенной продукцией гормонов коры надпочечников, которая обусловлена избыточной секрецией АКТГ клетками гиперплазированной или опухолевой ткани гипофиза (в 90% это микроаденома).
При подозрении на синдром Иценко — Кушинга (повышение уровня общего кортизола в сыворотке крови) выполняются различные пробы с дексаметазоном и выполняется двух- или трехкратное определение свободного кортизола в суточной моче.
Лечение заболевания зависит от результатов обследования, т. е. от того, в какой именно области выявлен патологический процесс, приведший к возникновению гиперкортицизма.
На сегодняшний день единственным, действительно эффективным методом лечения болезни Иценко–Кушинга, возникшей в результате аденомы гипофиза, является хирургический, при котором проводится селективная транссфеноидальная аденомэктомия. Эта нейрохирургическая операция показана при выявлении аденомы гипофиза, локализация которой чётко была установлена при обследовании. У подавляющего числа больных, эта операция дает положительные результаты. Достаточно быстро происходит восстановление нормального функционирования гипоталамо-гипофизарной системы, в 70–80 % случаев наступает стойкая ремиссия заболевания. Однако у 10–20 % пациентов может возникнуть рецидив.
Хирургическое лечение болезни Иценко–Кушинга обычно сочетается с лучевой терапией, а также методом деструкции гиперплазированных надпочечников (т. к. масса желез увеличивается в результате длительного гормонального сбоя).
При наличии противопоказаний к хирургическому лечению аденомы гипофиза (тяжелое состояние пациентки, наличие тяжелых сопутствующих заболеваний и др.), проводится медикаментозное лечение.
Применяются препараты, которые подавляют секрецию адренокортикотропного гормона (АКТГ), повышение уровня которого и приводит к гиперкортицизму. На фоне такого лечения, при необходимости, обязательно проводится и симптоматическая терапия гипотензивными, сахароснижающими препаратами, антидепрессантами, лечение и профилактика остеопороза и др.
Если причиной возникновения гиперкортицизма стали опухоли надпочечников или других органов, то необходимо их удаление. При удалении пораженной надпочечниковой железы, с целью профилактики гипокортицизма в дальнейшем, больным будет необходима длительная заместительная гормональная терапия под постоянным контролем врача.
Адреналэктомия (удаление одного или двух надпочечников) в последнее время используется редко, только в случае невозможности лечения гиперкортицизма другими способами. Эта манипуляция приводит к хронической надпочечниковой недостаточности, требующей пожизненной заместительной гормональной терапии.
Все пациенты, которым было проведено или проводится лечение этого заболевания, нуждаются в постоянном наблюдении эндокринолога, а при необходимости, и других специалистов.
Рост количества новообразований наблюдается уже достаточно длительное время. Яичник – это орган женской половой системы. Частота новообразований в яичниках и их разновидностей особо многочисленна. Все опухоли яичника принято разделять на доброкачественные, злокачественные и пограничные опухоли яичника.
Гормонально-активные опухоли — новообразования, которые развиваются из желёз внутренней секреции и характеризуются чрезмерным выделением гормонов или продуктов их образования.
Гормонпродуцирующие опухоли могут быть диагностированы во всех железах человеческого организма. Опухоль выделяет большое количество гормонов, что приводит к возникновению симптомов и признаков гиперфункции. Гормонпродуцирующие опухоли могут иметь как доброкачественное, так и злокачественное течение.
Гормонпродуцирующие опухоли яичников – новообразования, которые принято разделять в зависимости от гормона, который она выделяет. Гормоноактивная опухоль яичников усиленно выделяет либо эстрогены, либо андрогены.
К гормоноактивным опухолям яичников, выделяющим эстрогены, относятся гранулезоклеточная опухоль, тека-клеточные опухоли, фолликулома, и опухоли, которые комбинируют несколько видов. Клиническая картина гормонально-активных опухолей, вызванная гиперэстрогенемией, проявляется нарушениями менструального цикла и местными симптомами.
Гормоно-активные опухоли яичников, выделяющие андрогены, включают арренобластому, опухоли хилуса, маскулиновобластомы и комбинированные опухоли. В клинической картине превалируют явления вирилизма.
Юсуповская больница круглосуточно стоит на страже здоровья населения. Широко профильность и разносторонность Юсуповской больницы позволяет оказывать экстренную помощь, заниматься диагностикой и лечением огромного количества заболеваний. Не боятся специалисты браться за сложные случаи, вести пациентов от начала диагностики до полного восстановления, продолжая вести динамическое наблюдение во избежание рецидива.
Диагностические процедуру в Юсуповской больнице проходят быстро, без очередей и ожиданий, и качественно, потому что все оборудование современное, ведущих производителей. Лечение заболеваний, в том числе гормонпродуцирующих опухолей яичника, проводится в условиях абсолютного доверия и консенсуса между пациентом и докторами Юсуповской больницы. Применяются современные протоколы, стандарты, подходы индивидуальные и эффективные. Знания в каждой отрасли пополняются. Медицинские препараты подбираются для каждого, чтобы получить максимальный эффект от терапии. Специалисты работают в команде, дополняя работу друг друга.
Палаты Юсуповской больницы рассчитаны на количество пациентов от одного (палата повышенной комфортности), до четырех. Есть палаты интенсивной терапии, оборудованы по всем стандартам. Питание пациентов подбирается также индивидуально, поскольку пациенты с раковыми новообразованиями и так страдают плохим, или вовсе отсутствующим аппетитом, диспепсическими явлениями и нарушениями стула.
В Юсуповской больнице охотно ведутся и пациенты после специфического лечения для как можно быстрого и качественного восстановления. Запись на консультацию поможет уладить некоторые вопросы, получить необходимую информацию и т.д. записаться можно по телефону и онлайн.
Причины гормонпродуцирующих опухолей яичников
Этиология развития любого вида новообразований до конца не изучена. Исследования ведутся и в настоящее время, но пока достижения ограничатся только определением возможных причин:
- Гормональные нарушения. Большое значение имеет гормональный фон женщины, наличие в анамнезе беременностей и родов. Из-за овуляции ткани яичника повреждаются, что сопровождается последующей регенерацией. Но иногда такое повышенное деление клеток переходит в патологическое. Овуляция отсутствует во время беременности и грудном вскармливании, поэтому в это время риск возникновения новообразования существенно снижается. Такие факты как ранее начало менструации, поздняя менопауза, отсутствие родов и отказ от кормления грудью риски повышают.
- Отягощенный анамнез и генетическая предрасположенность. С этим фактором связаны двух процентов новообразований. При неблагополучном семейном анамнезе и диагностике рака у близких родственников, пациентки имеют высокий риск возникновения и ракового перерождения яичников. В этом случае необходимо проходить обследование, наблюдаться у гинеколога.
- Употребление большого количества продуктов с высоким содержанием канцерогенов и животных жиров. Статистические данные свидетельствуют в пользу данного утверждения из-за исследования пищевых привычек у определенных странах мира и сопоставлением их с уровнем заболеваемости на рак.
Причины, по которым одни опухоли гормоны продуцируют, а другие – нет, на данный момент остаются неизвестными.
Клиника гормонпродуцирующих опухолей яичников
Эстрогенпродуцирующие опухоли яичника могут быть диагностированы в любом возрасте: у детей и молодых девушек наиболее распространенная гранулезоклеточная, теко-клеточная – менопаузном периоде. Гранулезоклеточная опухоль развивается из гранулезной ткани, текома по строению напоминает клетки фолликулов. Клинические симптомы и признаки у девочек:
В старшем возрасте при эстрогенпродуцирующей опухоли яичника на первый план выходят симптомы нарушения менструации в виде дисфункциональных кровотечений из матки. У девушек наблюдается бесплодие. В женщин за пятьдесят появлению геморрагические выделений из половых путей, развивается железистая гиперплазия.
Андробластома – маскулинизирующая гормонопродуцирующая опухоль, которая тормозит функцию гипофиза и вследствие этого уменьшается уровень эстрогенов. Клинические признаки:
- Отсутствие менструации;
- Нарушение репродукции в виде бесплодия;
- Молочная железа уменьшается в размере;
- Голос становится грубым и низким;
- Оволосение изменяет на мужской тип;
- Страдает либидо;
- Увеличивается клитор;
- Формы тела приобретают мужские черты и др.
Наиболее часто пациентки обращаются с жалобами на отсутствие менструации и нарушение репродукции, иногда беспокоят боли внизу живота.
Диагностика гормонпродуцирующих опухолей яичников:
- Консультация у специалиста со сбором жалоб, анамнеза болезни и жизни.
- Бимануальное исследование.
- Биохимические и клинические анализы крови и мочи.
- Определение в сыворотке крови уровня СА-125,
- Определение уровня половых гормонов.
- Ультразвуковое исследование.
- Компьютерная и магнитно-резонансная томография.
- При необходимости проводятся другие дополнительные методы исследования.
- Окончательное заключение и установление диагноза дает гистологическое и цитологическое исследование биоптата, взятого путем оперативного вмешательства.
Лечение гормонпродуцирующих опухолей яичников
При некоторых видах достаточно резецировать образование в пределах здоровых тканей яичника, или одностороннее удаление придатков. При злокачественном поражении необходимо проводить удаление матки с придатками и сальником.
После удаления гормоноактивной опухоли большинство признаков и симптомов будут ликвидированы - наладятся менструальная и репродуктивная функции.
Обязательным пунктом является дальнейшее динамическое наблюдение, регулярные осмотры и обследования.
Юсуповская больница работает с пациентами с любыми видами новообразований яичников. Диагностика, лечение и восстановление в Юсуповской больнице проводятся качественно и эффективно. Записаться на консультацию можно по телефону и онлайн.
Читайте также:

