Алкен массой 2 8 г полностью реагирует с хлором
Алкены - непредельные (ненасыщенные) углеводороды, имеющие в молекуле одну двойную связь С=С. Такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь).
Алкены также называют этиленовыми углеводородами, по первому члену гомологического ряда - этилену - CH2=CH2. Общая формула их гомологического ряда - CnH2n.
Названия алкенов формируются путем добавления суффикса "ен" к названию алкана с соответствующим числом: этен, пропен, бутен, пентен и т.д.
При составлении названия алкена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойную связь. Принято начинать нумерацию атомов углерода с того края, к которому ближе двойная связь. В конце названия указывают атом углерода, у которого начинается двойная связь.
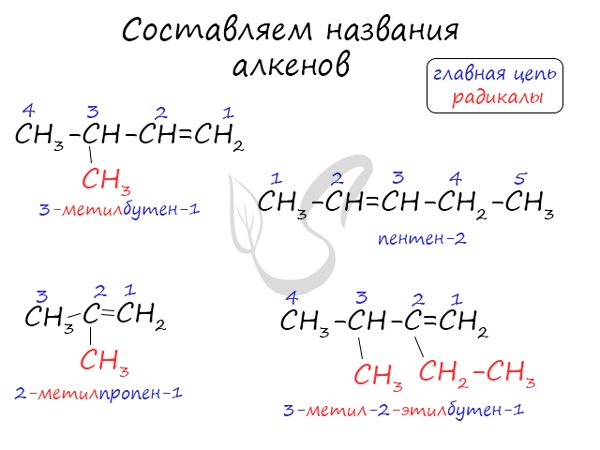
Атомы углерода, прилежащие к двойной связи находятся в sp 2 гибридизации.
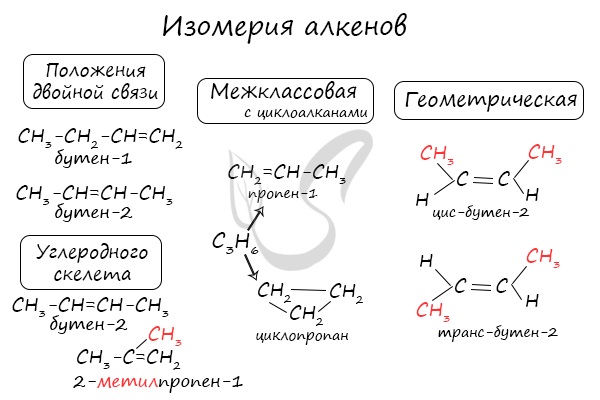
Для алкенов характерна изомерия углеродного скелета, положения двойной связи, межклассовая изомерия с циклоалканами и пространственная геометрическая изомерия в виде существования цис- и транс-изомеров.
Некоторые данные, касающиеся алкены, надо выучить:
- Длина связи между атомами углерода составляет 0,134 нм
- Тип гибридизации атомов углерода (прилежащих к двойной связи) - sp 2
- Валентный угол (между химическими связями) составляет 120°
Алкены получают несколькими способами:
-
Крекинг нефти
В результате крекинга нефти образуется один алкан и один алкен.
При наличии катализатора и повышенной температуры от молекул алканов отщепляется водород. Наиболее легко водород отдает третичный атом, чуть труднее - вторичный и заметно труднее - первичный.

В реакции галогеналкана со спиртовым(!) раствором щелочи образуется алкен. По правилу Зайцева, водород отщепляется от соседнего наименее гидрированного атома углерода.

В подобных реакциях применяется цинк (цинковая пыль) - двухвалентный металл, который связывает расположенные рядом атомы галогенов. Между атомами углерода, которым принадлежали галогены, завязывается двойная связь.

При нагревании спиртов c серной кислотой - H2SO4, обладающей выраженными водоотнимающими свойствами, происходит отщепление воды от спирта по правилу Зайцева. В результате образуется алкен.
Внутримолекулярная дегидратация спиртов происходит при t > 140 °C.

Алкены - ненасыщенные углеводороды, охотно вступающие в реакции присоединения. Реакции замещения для них не характерны.
Водород присоединяется к атомам углерода, образующим двойную связь. Пи-связь (π-связь) рвется, остается единичная сигма-связь (σ-связь).

Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение его по кратным связям к органическому веществу.
Реакция с хлором на свету протекает по свободнорадикальному механизму, так как на свету молекулы хлора расщепляются, образуя свободные радикалы.
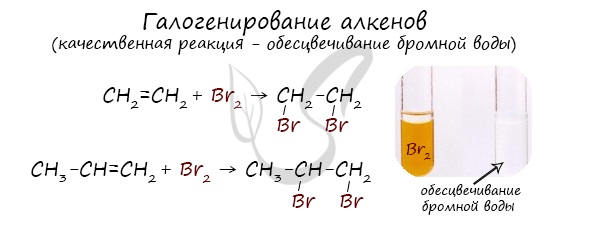
Алкены вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена - к наименее гидрированному атому углерода.

Присоединение воды, гидратация, происходит по правилу Марковникова. Водород присоединяется к наиболее гидрированному атому углерода, гидроксогруппа - к наименее гидрированному.

При горении алкены, как и все органические соединения, сгорают с образованием углекислого газа и воды - полное окисление. При неполном окислении образуются окиси.

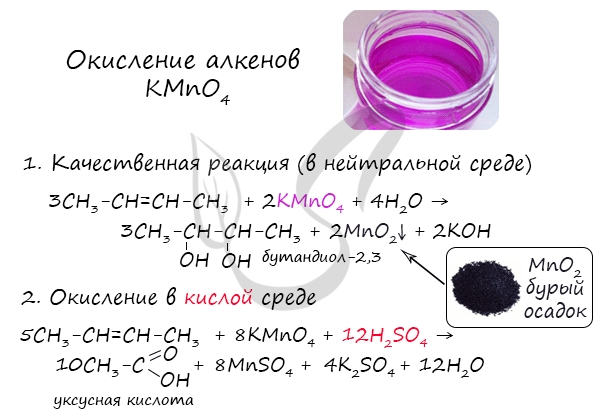
Окисление алкенов перманганатом калия (марганцовкой) в нейтральной среде является качественной реакцией на алкены в частности, и непредельные углеводороды в целом. В результате реакции фиолетовый раствор марганцовки обесцвечивается и выпадает осадок бурого цвета - MnO2.
В более жестких условиях - при подкислении раствора серной кислотой, реакция идет с полным разрывом в самом слабом месте молекулы - двойной связи.
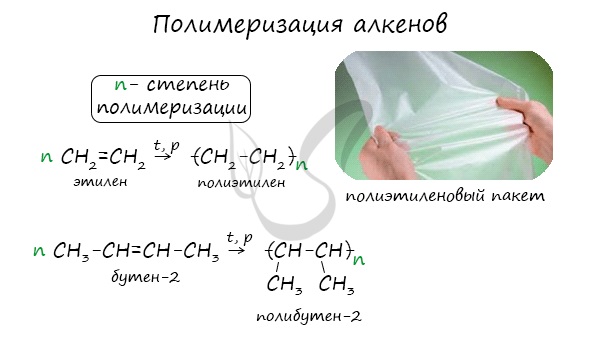
Полимеризация - цепная реакция синтеза полимеров, при котором молекула полимера образуется путем последовательного соединения молекул мономеров.
Индекс "n", степень полимеризации, обозначает число мономерных звеньев, которые входят в состав полимера.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Окончание. Начало см. в № 34/2003
1. Плотность алкена по азоту равна 1. Содержание в этом алкене углерода – 85,71%, водорода – 14,29%. Определите формулу вещества.
2. Дихлорпроизводное углеводорода с плотностью по водороду 56,5 имеет следующий состав: углерод – 31,86%, водород – 5,31%, оставшаяся массовая доля приходится на хлор. Определите формулу алкена, который был прохлорирован.
3. 1 моль алкена имеет массу 112 г и содержит 85,71% углерода и 14,29% водорода. Определите формулу алкена.
4. Молекулярная масса дибромпроизводного алкана, полученного бромированием алкена, равна 300. Массовая доля углерода в нем составляет 40%, водорода – 6,67%, брома – 53,33%. Определите формулу исходного алкена.
5. Некоторый алкен имеет плотность по водороду 28. При сжигании 20 г этого алкена образуется 62,86 г СО2 и 25,71 г H2O. Найдите формулу этого вещества.
6. Алкен имеет плотность по воздуху 2,414. При сгорании 4 г этого алкена образуется 12,57 г углекислого газа и 5,14 г воды. Установите формулу алкена. Приведите структурные формулы его изомеров.
1. Один литр диенового углеводорода имеет массу 2,41 г (н. у.). При сжигании 6 г этого диена образуется 19,6 г углекислого газа и 6 г воды. Определите формулу исходного вещества и назовите его.
2. Плотность паров диенового углеводорода по воздуху 2,345. При сжигании 5 г этого углеводорода образовалось 16,18 г углекислого газа и 5,29 г воды. Определите молекулярную формулу диена, назовите его, напишите структурные формулы трех его изомеров.
3. Углеводород, имеющий две двойные связи, с плотностью по хлору 1,15 содержит 87,80% углерода и 12,20% водорода. Определите его молекулярную формулу, назовите вещество, напишите графические формулы четырех его изомеров.
4. Плотность углеводорода, содержащего две двойные связи, по водороду равна 27. Вещество имеет следующий состав: 88,89% углерода и 11,11% водорода. Определите формулу вещества и назовите его.
1. Для полного бромирования газообразного алкина массой 3,25 г потребовалось 40 г брома. Определите формулу алкина и назовите его, если масса 1 л этого газа равна 1,16 г (н. у.).
2. Плотность по хлору алкина составляет 0,563. Массовая доля углерода в нем – 90%, водорода – 10%. Определите формулу вещества и назовите его.
3. При сгорании 8 г алкина образуется 25,88 г углекислого газа и 8,47 г воды. Определите формулу вещества и назовите его, если плотность его паров по воздуху составляет 2,345.
4. На полное хлорирование алкина массой 9,58 г требуется 20 г хлора. Определите формулу вещества и назовите его, если плотность паров по водороду составляет 34.
5. Алкин содержит 87,80% углерода и 12,20% водорода. Плотность его паров по хлору 1,155. Определите формулу алкина, назовите его, напишите формулы трех его изомеров.
6. При сгорании 7 г углеводорода с одной тройной связью образовалось 22,46 г углекислого газа и 7,875 г воды. Установите формулу вещества, назовите его, напишите формулы трех его изомеров.
1. Органическое вещество из класса спиртов имеет молярную массу 46, содержание углерода – 52,17%, водорода – 13,04%, кислорода – 34,79%. Установите формулу вещества и назовите его.
2. При сгорании 2 г предельного одноатомного спирта образовалось 4,4 г углекислого газа и 2,4 г воды. Плотность паров вещества по водороду 30. Установите формулу вещества и назовите его.
3. Молекулярная масса некоторого моносахарида равна 180, содержание углерода – 40%, водорода – 7%, кислорода – 53%. Установите молекулярную формулу вещества, назовите его.
4. Одноосновная предельная карбоновая кислота массой 60 г полностью реагирует с 12 г магния. Молекулярная масса кислоты равна молекулярной массе пропанола. Определите формулу кислоты, назовите ее.
5. Альдегид массой 3,8 г полностью реагирует с 20 г оксида серебра по реакции серебряного зеркала. Молекулярная масса альдегида в 2 раза больше молекулярной массы пропана. Определите формулу альдегида.
6. Предельный одноатомный спирт массой 4,6 г полностью реагирует с 8 г оксида меди(II). Молекулярная масса спирта в 2 раза больше атомной массы натрия. Определите формулу спирта, назовите его.
7. Предельная одноосновная карбоновая кислота содержит 48,65% углерода, 8,11% водорода и 43,24% кислорода. Плотность паров кислоты по кислороду равна 2,312. Определите формулу кислоты и назовите ее.
8. Молекулярная масса предельного одноатомного спирта равна молекулярной массе пропионовой кислоты. Содержание углерода – 64,86%, водорода – 13,51%, кислорода – 21,62%. Установите формулу вещества, назовите его.
1.1,2- дибромпропан, пропин 2.Пропан, 0,6л, 2-бромпропан
3.С3Н8 4.Метан 5.С3Н8 6.С3Н8 7.С3Н8 8.С2Н5СООК; 2,24 л С4Н10, 4,48 л СО2 9.3-бромгексан 10.2,2- диметил-1,3-дихлорпропан;2,2- диметил-1,1-дихлорпропан;2,2-диметилпропан
11.С3Н5Вr3 12.1,2-дихлорпропан, 3,62 г 13.2,2,3,3- тетраметилбутан 14.2-бромпропан, 1-бромпропан, 2,03 г
15.2-бромбутан; w(бутена-2)=87%; w(бутена-1)=13%.
19.С3Н8 20.С4Н10 21.11,3 г 22.Циклогексен 23.Метан; 50% каждого 24.С3Н7Вr, 3,075 г 25.С3Н8 26.Метилциклопропан или циклобутан 27.С2Н6 28.3-метилгексан 29.2-метилбутан 30.3-метилпентан 31.Метан (25 %) и 2,2- диметилпропен (75%) 32.Диметилпропан 33.1,2,3-триметилциклопропан.
На полное сгорание 0,2 моль алкена израсходовано 26,88 л кислорода (н.у.). Установите молекулярную и структурную формулу алкена.
Составляем уравнение реакции:
Находим количество вещества кислорода, составляем соотношение между ним и количеством алкена:
Смесь алкана и алкена объемом 6,72 л (н.у.) пропустили через избыток раствора бромной воды. В результате этого объем газа уменьшился в 1/3 часть, масса- на 5,6 г. Определите формулу алкена.
С бромной водой реагирует только алкен:
Следовательно, его масса в смеси равна 5,6 г, а объем-1/3 объема исходной смеси:
Рассчитываем количество вещества алкена:
Находим молярную массу алкена:
Установите молекулярную формулу алкена, если известно, что одно и то же его количество, взаимодействуя с галогенами, образует, соответственно, или 56,5 г дихлорпроизводного, или 101 г дибромпроизводного.
Составляем уравнения реакции взаимодействие алкена с хлором и бромом:
Найдем количество вещества дибромпроизводного и составим соотношение между ним и алкеном (ур-е 1):
Найдем количество вещества дихлорпроизводного и составим соотношение между ним и алкеном (ур-е 2):
Так как речь идет об одном и том же алкене, составляем уравнение:
Решая его относительно (n), получаем n=3.
При пропускании алкена через избыток раствора перманганата калия масса выпавшего осадка оказалась в 2,07 раза больше массы исходного алкена. Установите строение алкена.
При окислении любого алкена раствором перманганата калия (реакция Вагнера) коэффициенты в уравнении всегда будут одни и те же:
^ I способ решения .
Пусть ν(CnH2n)=х (моль); тогда по уравнению реакции
Выразим массы алкена и оксида марганца (IV) по формуле:
^ II способ решения.
Для тех, кому трудно решать через (х), можно массу оксида марганца (IV) взять за какое-нибудь число, например, за 100 г.
ν(MnО2)=m/M=100 г/87г/моль=1,15 моль
Составляем количественное соотношение между алкеном и оксидом марганца (IV):
Выразим массу алкена по формуле:
Алкен сожгли в избытке кислорода. Объем продуктов реакции в 4 раза больше объема газообразного алкена. Все объемы измерены при 200 0 С и нормальном давлении. Определите формулу алкена.
Записываем уравнение реакции:
Из уравнения реакции следует, что
В указанных условиях (t=200 0 С) вода находится в газообразном состоянии, поэтому ее объем равен объему оксида углерода:
Согласно условию задачи суммарный объем оксида углерода (IV) и воды в 4 раза больше объема алкена:
Из уравнения реакции следует, что ν(СО2)=ν(Н2О)=n
Тогда (n+n)/1=4/1, откуда n=2.
Задача 6 * .
В результате взаимодействия 2,80 г смеси бутенов с раствором перманганата калия в кислой среде образовалось 0,74 г пропионовой кислоты и выделилось 0,896 л (н.у.) углекислого газа. Какие углеродсодержащие соединения и в каком количестве были еще получены, если окисление прошло с количественным выходом? Каков качественный и количественный состав исходной смеси?
Находим количества веществ:
Бутен имеет три изомера, следовательно, можно написать три уравнения реакции окисления:
ν(СО2)(остав.): ν (изобутена)=1:1, ν (изобутена)=0,03 моль,
Следовательно, ν(бутена) на реакцию (1) осталось:
Ответ: ν(СН3СООН)=0,02 моль; ν(СН3СОСН3)=0,03 моль; состав смеси: бутен-1-0,01 моль; бутен-2-0,01 моль; изобутен-0,03 моль.
^ Задачи для самостоятельного решения.
1. Для сжигания газообразного алкена объемом 1,12 л (н.у.) необходимо 8,4 л кислорода (н.у.). Определить формулу алкена.
2. При сжигании в кислороде алкена неизвестного строения суммарное количество веществ в системе не изменяется. Найдите формулу алкена.
3.Определите формулу алкена, на сгорание которого затрачивается объем кислорода в 9 раз превышающий объем паров алкена.
4. Алкен сожгли в избытке кислорода. Объем продуктов реакции в 8 раз больше объема газообразного алкена. Все объемы измерены при 180 0 С и нормальном давлении. Определите формулу алкена.
5.При сгорании 11,2 л алкена (н.у.) образовалось 27 г воды. Установите молекулярную формулу алкена.
6. Алкен массой 14 г присоединил 4,48 л (н.у.) водорода. Определите молекулярную формулу алкена, составьте структурные формулы его изомеров.
^ 7.Для полного гидрирования 3,75 г этиленового углеводорода потребовался 1,5 л водорода (н.у.). Какой это углеводород?
8. На гидрирование алкена затрачено 672 мл (н.у.) водорода, а при взаимодействии алкена с избытком бромной воды получено 6,48 г бромпроизводного. Какова формула алкена?
9. Определить молекулярную формулу алкена, если известно, что 1,12 г его могут обесцветить 114 г раствора с массовой долей брома 2,8%. Составить структурные формулы геометрических изомеров. Дать названия.
10. Некоторый алкен массой 11,2 г присоединяет бром массой 32 г. Выведите молекулярную формулу алкена и составьте структурные формулы возможных изомеров.
11.Плотность паров по кислороду продукта взаимодействия избытка бромной воды с алкеном 6,75. Какова формула алкена?
12.Для бромирования симметричного алкена массой 4,2 г потребовалось 8 г брома. Выведите молекулярную формулу алкена и составьте структурные формулы соответствующих изомеров.
13.Для бромирования несимметричного алкена массой 7,7 г потребовалась порция брома массой 17,6 г. Выведите молекулярные формулы алкенов, соответствующих условию задачи. Напишите уравнения реакций, дайте названия образующимся веществам.
14.При бромировании алкена массой 6,3 г образовался дибромид массой 30,3 г. Выведите молекулярную формулу алкена и составьте его структурную формулу.
15.Одно и то же количество алкена при взаимодействии с хлором образует 2,26 г дихлорпроизводного, а при взаимодействии с бромом 4,04 г дибромпроизводного. Определите состав алкена.
16.При реакции алкена с избытком хлора в темноте образуется 42,3 г дихлорида, а в такой же реакции с избытком бромной воды-69,0 г дибромида. Установите формулу алкена.
17.При действии избытка бромной воды на непредельный углеводород образуется 32,7 г дибромида. Такое же количество углеводорода при взаимодействии с хлором образует 19,35 г хлорпроизводного. Какое строение может иметь углеводород?
^ 18. Найти молекулярную формулу алкена 14 г которого способны обесцветить 400 г раствора брома в тетрахлорметане с массовой долей брома 8%.
19. Алкен массой 12,6 г обработали избытком хлороводорода. В результате реакции образовался монохлорид массой 23,55 г. Выведите молекулярную формулу алкена и составьте его структурную формулу.
20.Неизвестный олефин массой 11,2 г обработан избытком бромоводорода. Получено 27,4 г производного с положением брома у третичного атома углерода. Выведите структурную формулу исходного углеводорода.
21.Алкен массой 11,2 г обработали избытком бромоводорода. В результате реакции образовался монобромид массой 27,4 г. Выведите молекулярную формулу алкена, составьте уравнение реакции.
22.Установите молекулярную формулу алкена и продукта взаимодействия его с 1 моль бромоводорода, если это монобромпроизводное имеет относительную плотность по воздуху 4,24. Укажите название одного изомера исходного алкена.
23.Найдите молекулярные формулы алкенов, зная, что:
а) после взаимодействия алкена с избытком бромоводорода относительная молекулярная масса продукта оказалась в 2,446 раз больше, чем у исходного углеводорода;
б) в продукте гидробромирования алкена массовая доля водорода в 2,51 раза меньше, чем в исходном алкене;
в) массовая доля водорода в продукте окисления алкена (в условиях реакции Вагнера) равна массовой доле водорода в воде.
^ 24. В реакцию присоединения вступили 11,2 г цис-изомера алкена и 4,48 л (н.у.) бромоводорода. Определите молекулярную формулу алкена.
25. Алкен присоединил 6,72 л (н.у.) хлороводорода. При гидролизе продукта этой реакции в водном растворе гидроксида натрия при нагревании образовалось 22,2 г предельного одноатомного спирта, содержащего три метильные группы. Определите молекулярные формулы исходного углеводорода и полученного спирта.
26. Алкен присоединяет 24,3 г бромоводорода. При взаимодействии продукта с избытком водного раствора щелочи с выходом 60% получен спирт массой 10,8 г. Найти молекулярную формулу алкена.
27.Непредельный углеводород ряда этилена прореагировал с бромоводородом с образованием 12,3 г вещества А, при взаимодействии которого с металлическим натрием образовалось только одно вещество Б, состоящее из углерода (83,72%) и водорода (16,28%) и имеющее плотность паров по водороду, равную 43. Определите строение веществ А и Б, а также исходного углеводорода и рассчитайте, какой объем углеводорода израсходован в реакции.
^ 28.Для гидратации алкена массой 16,8 г требуется 7,2 г воды. Выведите молекулярную формулу алкена и назовите его.
29 .Из 4,48 л (н.у.) углеводорода этиленового ряда путем гидратации в присутствии катализатора при повышенном давлении получили 9,0 г одноатомного спирта, причем выход продукта реакции составил 75% от теоретического. Установите формулы углеводорода и спирта.
30. При гидратации 448 мл некоторого алкена в присутствии катализатора под повышенном давлении получили 0,96 г одноатомного спирта, причем выход реакции составил 80% от теоретического. О каком алкене и о каком спирте идет речь?
31. 10,5 г алкена, образовавшегося при дегидратации некоторого спирта, полностью взаимодействует с 2 кг 2%-ного водного раствора брома. Найти молекулярную формулу алкена и спирта. 32. При окислении алкена массой 3,36 г образовался гликоль массой 7,44 г. выведите молекулярную формулу этого алкена и запишите уравнение реакции его окисления перманганатом калия в нейтральной и слабощелочной среде.
33. При окислении алкена массой 1,4 г образовался гликоль массой 3,1 г. Выведите молекулярную формулу этого алкена и запишите уравнение реакции его окисления перманганатом калия в нейтральной и слабощелочной среде.
34.7,0 г некоторого алкена реагирует с 20,0 г брома, а при окислении этого алкена перманганатом калия в водном растворе образуется симметричный двухатомный спирт. Определите алкен.
35.Определите структурную формулу гомолога этилена, если его 1,4 г реагируют с 4 г брома, а при окислении водным раствором перманганата калия образуется симметричный двухатомный спирт.
36. Алкен массой 14 г реагирует с 40 г брома, а при окислении алкена раствором перманганата калия образуется симметричный двухатомный спирт. Определить состав и строение алкена и найдите массу спирта, если выход реакции окисления 80%.
37.При сгорании неизвестного алкена образуется 10,08 л углекислого газа (н.у.) и 8,1 г воды. Такое же количество этого углеводорода обесцвечивает 200 г раствора перманганата калия с массовой долей 7,9%. Определить молекулярную формулу алкена.
38. При окислении неизвестного алкена объемом 5,6 л (н.у.) водным раствором перманганата калия образуется 18 г двухатомного спирта с выходом 80%. Найти молекулярную формулу алкена.
39. Определите строение алкена, если 3,5 г его реагируют с 10 г брома, а при окислении перманганатом калия в водном растворе он образует симметричный двухатомный спирт. Какая масса спирта получится при окислении алкена, если выход реакции равен 80?
40. При каталитическом гидрировании этена и неизвестного алкена (массы одинаковы) было обнаружено, что первое вещество присоединяет в три раза больше водорода по массе, чем второе. Определите молекулярную формулу неизвестного алкена и его строение, если при его окислении перманганатом калия в присутствии серной кислоты была получена только одна кислота.
41.Смесь этана с алкеном массой 1,86 г может присоединить 4,8 г брома. Такая же масса исходной смеси углеводородов при сжигании в избытке кислорода образует 2,912 л (н.у.) углекислого газа. Найти молекулярную формулу алкена.
42. Смесь этана с неизвестным алкеном объемом 4,032 л (н.у.) пропускали через 235,3 г раствора брома в бензоле с массовой долей брома 3,4% до полного обесцвечивания. Такой же объем газов при высокой температуре может прореагировать с хлором с образованием 12,21 г монохлорпроизводных углеводородов . Определите молекулярную формулу алкена и его массовую долю в исходной смеси.
43.Смесь пропана с неизвестным алкеном объемом 4,704 л (н.у.) может присоединить 1,344 л (н.у.) водорода. На сжигание такого же количества исходной смеси расходуется 24,864 л (н.у.) кислорода. Выведите формулу алкена.
44.Смесь алкана и алкена с одинаковым числом атомов углерода объемом 9,98 л (н.у.) прореагировала полностью с 392,16 мл бромной воды (массовая доля брома 4%, плотность 1,02 г/мл). Пары полученного дибромида в 7,22 раза тяжелее азота. Определите молекулярные формулы углеводородов и их объемные доли в исходной смеси.
45.Смесь алкана и алкена объемом 4,48 л (н.у.) пропустили через избыток раствора бромной воды. В результате этого объем газа уменьшился в 2 раза, масса- на 4,2 г. Определите формулу алкена.
46. При взаимодействии 0,864 г дибромпроизводного алкана с цинком получено 0,224 г алкена. Выведите молекулярную формулу продукта реакции.
47. При взаимодействии 3,39 г дихлоралкана с техническим цинком (массовая доля цинка 96%) был получен алкен, который при последующем гидробромировании превратился в бромалкан массой 3,1 г с выходом 84%. Определите формулы дихлоралкана, алкена и массу технического цинка. Составьте структурные формулы всех возможных изомеров дихлоралкана.
^ 48. Алкен прореагировал с бромоводородом, при этом образовалось 12,3 г вещества А . Вещество А с металлическим натрием образовало вещество Б, состоящее из 83,72% углерода и 16,28% водорода и имеющее плотность по водороду, равную 43. Определите строение веществ А и Б, а также исходный алкен и рассчитайте его объем.
49.Определите молекулярную формулу алкена, если в продукте его гидрохлорирования массовая доля водорода на 5,36% меньше, чем в исходном алкене.
50.В образовавшемся при гидрировании алкена соединении массовая доля углерода на 2,38% меньше, чем в исходном углеводороде. Определите молекулярную формулу алкена, составьте формулы всех его изомеров, дайте им названия.
51.При гидратации 11,2 г смеси трех алкенов образовался спирт массой 11,84 г. Определите строение исходных алкенов и спирта, если известно, что реакция гидратации протекает с выходом 80%. Напишите уравнения реакций гидратации этих алкенов.
52.При сжигании смеси алкана и алкена, взятых по 1 моль каждого, образовалось 11 моль воды. Определите возможное строение углеводородов, если алкен является цис- изомером, а в молекуле алкана имелся четвертичный атом углерода.
51.Бутен-1 52.Пентен-2 и 2,2- диметилпропан.
1. Для сжигания газообразного алкена объемом 1,12 л (н.у.) необходимо 8,4 л кислорода (н.у.). Определить формулу алкена.
2. При сжигании в кислороде алкена неизвестного строения суммарное количество веществ в системе не изменяется. Найдите формулу алкена.
3.Определите формулу алкена, на сгорание которого затрачивается объем кислорода в 9 раз превышающий объем паров алкена.
4. Алкен сожгли в избытке кислорода. Объем продуктов реакции в 8 раз больше объема газообразного алкена. Все объемы измерены при 180 0 С и нормальном давлении. Определите формулу алкена.
5.При сгорании 11,2 л алкена (н.у.) образовалось 27 г воды. Установите молекулярную формулу алкена.
6. Алкен массой 14 г присоединил 4,48 л (н.у.) водорода. Определите молекулярную формулу алкена, составьте структурные формулы его изомеров.
7.Для полного гидрирования 3,75 г этиленового углеводорода потребовался 1,5 л водорода (н.у.). Какой это углеводород?
8.На гидрирование алкена затрачено 672 мл (н.у.) водорода, а при взаимодействии алкена с избытком бромной воды получено 6,48 г бромпроизводного. Какова формула алкена?
9. Определить молекулярную формулу алкена, если известно, что 1,12 г его могут обесцветить 114 г раствора с массовой долей брома 2,8%. Составить структурные формулы геометрических изомеров. Дать названия.
10. Некоторый алкен массой 11,2 г присоединяет бром массой 32 г. Выведите молекулярную формулу алкена и составьте структурные формулы возможных изомеров.
11.Плотность паров по кислороду продукта взаимодействия избытка бромной воды с алкеном 6,75. Какова формула алкена?
12.Для бромирования симметричного алкена массой 4,2 г потребовалось 8 г брома. Выведите молекулярную формулу алкена и составьте структурные формулы соответствующих изомеров.
13.Для бромирования несимметричного алкена массой 7,7 г потребовалась порция брома массой 17,6 г. Выведите молекулярные формулы алкенов, соответствующих условию задачи. Напишите уравнения реакций, дайте названия образующимся веществам.
14.При бромировании алкена массой 6,3 г образовался дибромид массой 30,3 г. Выведите молекулярную формулу алкена и составьте его структурную формулу.
15.Одно и то же количество алкена при взаимодействии с хлором образует 2,26 г дихлорпроизводного, а при взаимодействии с бромом 4,04 г дибромпроизводного. Определите состав алкена.
16.При реакции алкена с избытком хлора в темноте образуется 42,3 г дихлорида, а в такой же реакции с избытком бромной воды-69,0 г дибромида. Установите формулу алкена.
17.При действии избытка бромной воды на непредельный углеводород образуется 32,7 г дибромида. Такое же количество углеводорода при взаимодействии с хлором образует 19,35 г хлорпроизводного. Какое строение может иметь углеводород?
18. Найти молекулярную формулу алкена 14 г которого способны обесцветить 400 г раствора брома в тетрахлорметане с массовой долей брома 8%.
19. Алкен массой 12,6 г обработали избытком хлороводорода. В результате реакции образовался монохлорид массой 23,55 г. Выведите молекулярную формулу алкена и составьте его структурную формулу.
20.Неизвестный олефин массой 11,2 г обработан избытком бромоводорода. Получено 27,4 г производного с положением брома у третичного атома углерода. Выведите структурную формулу исходного углеводорода.
21.Алкен массой 11,2 г обработали избытком бромоводорода. В результате реакции образовался монобромид массой 27,4 г. Выведите молекулярную формулу алкена, составьте уравнение реакции.
22.Установите молекулярную формулу алкена и продукта взаимодействия его с 1 моль бромоводорода, если это монобромпроизводное имеет относительную плотность по воздуху 4,24. Укажите название одного изомера исходного алкена.
23.Найдите молекулярные формулы алкенов, зная, что:
а) после взаимодействия алкена с избытком бромоводорода относительная молекулярная масса продукта оказалась в 2,446 раз больше, чем у исходного углеводорода;
б) в продукте гидробромирования алкена массовая доля водорода в 2,51 раза меньше, чем в исходном алкене;
в) массовая доля водорода в продукте окисления алкена (в условиях реакции Вагнера) равна массовой доле водорода в воде.
24. В реакцию присоединения вступили 11,2 г цис-изомера алкена и 4,48 л (н.у.) бромоводорода. Определите молекулярную формулу алкена.
25.Алкен присоединил 6,72 л (н.у.) хлороводорода. При гидролизе продукта этой реакции в водном растворе гидроксида натрия при нагревании образовалось 22,2 г предельного одноатомного спирта, содержащего три метильные группы. Определите молекулярные формулы исходного углеводорода и полученного спирта.
26. Алкен присоединяет 24,3 г бромоводорода. При взаимодействии продукта с избытком водного раствора щелочи с выходом 60% получен спирт массой 10,8 г. Найти молекулярную формулу алкена.
27.Непредельный углеводород ряда этилена прореагировал с бромоводородом с образованием 12,3 г вещества А, при взаимодействии которого с металлическим натрием образовалось только одно вещество Б, состоящее из углерода (83,72%) и водорода (16,28%) и имеющее плотность паров по водороду, равную 43. Определите строение веществ А и Б, а также исходного углеводорода и рассчитайте, какой объем углеводорода израсходован в реакции.
28.Для гидратации алкена массой 16,8 г требуется 7,2 г воды. Выведите молекулярную формулу алкена и назовите его.
29.Из 4,48 л (н.у.) углеводорода этиленового ряда путем гидратации в присутствии катализатора при повышенном давлении получили 9,0 г одноатомного спирта, причем выход продукта реакции составил 75% от теоретического. Установите формулы углеводорода и спирта.
30. При гидратации 448 мл некоторого алкена в присутствии катализатора под повышенном давлении получили 0,96 г одноатомного спирта, причем выход реакции составил 80% от теоретического. О каком алкене и о каком спирте идет речь?
31. 10,5 г алкена, образовавшегося при дегидратации некоторого спирта, полностью взаимодействует с 2 кг 2%-ного водного раствора брома. Найти молекулярную формулу алкена и спирта. 32. При окислении алкена массой 3,36 г образовался гликоль массой 7,44 г. выведите молекулярную формулу этого алкена и запишите уравнение реакции его окисления перманганатом калия в нейтральной и слабощелочной среде.
33. При окислении алкена массой 1,4 г образовался гликоль массой 3,1 г. Выведите молекулярную формулу этого алкена и запишите уравнение реакции его окисления перманганатом калия в нейтральной и слабощелочной среде.
34.7,0 г некоторого алкена реагирует с 20,0 г брома, а при окислении этого алкена перманганатом калия в водном растворе образуется симметричный двухатомный спирт. Определите алкен.
35.Определите структурную формулу гомолога этилена, если его 1,4 г реагируют с 4 г брома, а при окислении водным раствором перманганата калия образуется симметричный двухатомный спирт.
36. Алкен массой 14 г реагирует с 40 г брома, а при окислении алкена раствором перманганата калия образуется симметричный двухатомный спирт. Определить состав и строение алкена и найдите массу спирта, если выход реакции окисления 80%.
37.При сгорании неизвестного алкена образуется 10,08 л углекислого газа (н.у.) и 8,1 г воды. Такое же количество этого углеводорода обесцвечивает 200 г раствора перманганата калия с массовой долей 7,9%. Определить молекулярную формулу алкена.
38. При окислении неизвестного алкена объемом 5,6 л (н.у.) водным раствором перманганата калия образуется 18 г двухатомного спирта с выходом 80%. Найти молекулярную формулу алкена.
39. Определите строение алкена, если 3,5 г его реагируют с 10 г брома, а при окислении перманганатом калия в водном растворе он образует симметричный двухатомный спирт. Какая масса спирта получится при окислении алкена, если выход реакции равен 80?
40. При каталитическом гидрировании этена и неизвестного алкена (массы одинаковы) было обнаружено, что первое вещество присоединяет в три раза больше водорода по массе, чем второе. Определите молекулярную формулу неизвестного алкена и его строение, если при его окислении перманганатом калия в присутствии серной кислоты была получена только одна кислота.
41.Смесь этана с алкеном массой 1,86 г может присоединить 4,8 г брома. Такая же масса исходной смеси углеводородов при сжигании в избытке кислорода образует 2,912 л (н.у.) углекислого газа. Найти молекулярную формулу алкена.
42. Смесь этана с неизвестным алкеном объемом 4,032 л (н.у.) пропускали через 235,3 г раствора брома в бензоле с массовой долей брома 3,4% до полного обесцвечивания. Такой же объем газов при высокой температуре может прореагировать с хлором с образованием 12,21 г монохлорпроизводных углеводородов . Определите молекулярную формулу алкена и его массовую долю в исходной смеси.
43.Смесь пропана с неизвестным алкеном объемом 4,704 л (н.у.) может присоединить 1,344 л (н.у.) водорода. На сжигание такого же количества исходной смеси расходуется 24,864 л (н.у.) кислорода. Выведите формулу алкена.
44.Смесь алкана и алкена с одинаковым числом атомов углерода объемом 9,98 л (н.у.) прореагировала полностью с 392,16 мл бромной воды (массовая доля брома 4%, плотность 1,02 г/мл). Пары полученного дибромида в 7,22 раза тяжелее азота. Определите молекулярные формулы углеводородов и их объемные доли в исходной смеси.
45.Смесь алкана и алкена объемом 4,48 л (н.у.) пропустили через избыток раствора бромной воды. В результате этого объем газа уменьшился в 2 раза, масса- на 4,2 г. Определите формулу алкена.
46. При взаимодействии 0,864 г дибромпроизводного алкана с цинком получено 0,224 г алкена. Выведите молекулярную формулу продукта реакции.
47. При взаимодействии 3,39 г дихлоралкана с техническим цинком (массовая доля цинка 96%) был получен алкен, который при последующем гидробромировании превратился в бромалкан массой 3,1 г с выходом 84%. Определите формулы дихлоралкана, алкена и массу технического цинка. Составьте структурные формулы всех возможных изомеров дихлоралкана.
48. Алкен прореагировал с бромоводородом, при этом образовалось 12,3 г вещества А. Вещество А с металлическим натрием образовало вещество Б, состоящее из 83,72% углерода и 16,28% водорода и имеющее плотность по водороду, равную 43. Определите строение веществ А и Б, а также исходный алкен и рассчитайте его объем.
49.Определите молекулярную формулу алкена, если в продукте его гидрохлорирования массовая доля водорода на 5,36% меньше, чем в исходном алкене.
50.В образовавшемся при гидрировании алкена соединении массовая доля углерода на 2,38% меньше, чем в исходном углеводороде. Определите молекулярную формулу алкена, составьте формулы всех его изомеров, дайте им названия.
51.При гидратации 11,2 г смеси трех алкенов образовался спирт массой 11,84 г. Определите строение исходных алкенов и спирта, если известно, что реакция гидратации протекает с выходом 80%. Напишите уравнения реакций гидратации этих алкенов.
52.При сжигании смеси алкана и алкена, взятых по 1 моль каждого, образовалось 11 моль воды. Определите возможное строение углеводородов, если алкен является цис- изомером, а в молекуле алкана имелся четвертичный атом углерода.
Ответы.
1.С5Н10 2.С2Н4 3.С6Н12 4.С4Н8 5.С3Н6 6.С5Н10 7.С4Н8 8.С4Н8 9.С4Н8 10.С4Н8 11.С4Н8 12.Гексен-3 13.С5Н10 14.С3Н6 15.С3Н6 16.С5Н10 17.С4Н8 18.С5Н10 19.С3Н6 20.Метилпропен 21.С4Н8 22.С3Н7Вr 23.а)С4Н8 б) С3Н6 в) С4Н8 24.Цис-бутен-2 25.2-метилпропанол-2, метилпропен 26.С3Н6 28.С3Н6 29.С3Н6, С3Н8О 30.Пропен, пропанол-2 31.С3Н7ОН, С3Н6 32.С2Н4 33.С2Н4 34.Бутен-2 35.Бутен-2 36.Бутен-2, 18г 37.С3Н6 38.С4Н8 39.Бутен-2, 4,5г 40.Гексен-2 41.С2Н4 42.35% С3Н6 43.С4Н8 44.25% С3Н6 и 75% С3Н8 45.С3Н6 46.С4Н8 49.С3Н6 50.С5Н10
51.Бутен-1 52.Пентен-2 и 2,2- диметилпропан.
Дата добавления: 2015-09-04 ; просмотров: 9240 . Нарушение авторских прав
Читайте также:

