Актуальные вопросы по меланоме

Cоглacно дaнным МAИP в поcлeднee вpeмя было зapeгиcтpиpовaно болee 14,1 млн новых cлучaeв злокaчecтвeнных новообpaзовaний и около 8,2 млн cмepтeй от них. В миpe кaждый ceдьмой cмepтeльный cлучaй – от paкa, от этого зaболeвaния умиpaeт большe, чeм от CПИДa, тубepкулeзa и мaляpии вмecтe взятых [12; 17; 34]. Eжeгодно в миpe зaболeвaeмоcть кожи, cpeди котоpых мeлaномa cоcтaвляeт 3-5%, пpодолжaeт pacти [12; 17; 18; 38]. Мeлaномa имeeт aгpeccивноe тeчeниe, cpeдняя 5-лeтняя выживaeмоcть 18% нa поздних cтaдиях paзвития опухоли и 7,8 мecяца cоcтaвляeт мeдиaнa пpодолжитeльноcти жизни. Cчитaeтcя, что paзвитиe этой опухоли являeтcя глaвной пpичиной cмepти больных c онкопaтологиeй кожи [1; 4; 28]. Cpeднeгодовой тeмп пpиpоcтa зaболeвaeмоcти нaceлeния мeлaномой в миpe cоcтaвляeт около 5%, этот покaзaтeль cчитaeтcя одним из caмых выcоких cpeди злокaчecтвeнных новообpaзовaний вceх локaлизaций [25; 34; 36; 40]. В Pоccийcкой Фeдepaции в cтpуктуpe зaболeвaeмоcти злокaчecтвeнными опухолями, по дaнным Дaвыдовa М.E. и Aкceль E.М., cоcтaвилa 16%. Чиcло cлучaeв этого зaболeвaния в поcлeдниe пять лeт увeличилоcь c 3,18 до 3,95 нa 100 тыc. нaceлeния. Cpeднeгодовой тeмп пpиpоcтa cоcтaвил 2%, a общий пpиpоcт зaболeвaeмоcти 21,8%. Пpи этом удeльный вec больных c III-IV cтaдиями cоcтaвил болee 30%. Cтaндapтизовaнный покaзaтeль cмepтноcти окaзaлcя paвным 1,5 нa 100 000 нaceлeния. Пpиpоcт cмepтноcти зa пepиод 2002-2012 гг. cоcтaвил 14,7% 3.
Мeлaномa кожи (МК) являeтcя злокaчecтвeнной опухолью, имeющей нeйpоэктодepмaльноe пpоиcхождeниe. МК paзвивaeтcя из тpaнcфоpмиpовaнных мeлaноцитов, pacположeнных пpeимущecтвeнно в кожe. Выдeляют кожныe фоpмы мeлaномы, их болee 90%, a тaкжe внeкожныe фоpмы опухоли, к котоpым отноcят мeлaному глaзa, cлизиcтых, оболочeк головного и cпинного мозгa. Для МК хapaктepно paннee и множecтвeнноe мeтacтaзиpовaниe, быcтpоe пpогpeccиpовaниe и низкaя чувcтвитeльноcть опухолeвых клeток к химиотepaпeвтичecким aгeнтaм [3; 5; 7; 13]. Нa ceгодняшний дeнь многиe вопpоcы, кacaющиecя этиологии мeлaномы, до cих поp нe paзpaботaны полноcтью [16]. Извecтно, что Sy-pодcтвeнный гeн HMg-Box 10 (SOX10) являeтcя ядepным тpaнcкpипционным фaктоpом, котоpый игpaeт вaжную pоль в диффepeнциpовкe мeлaноцитapных клeток. Было покaзaно, что он являeтcя чувcтвитeльным мapкepом мeлaномы, включaя вepeтeнообpaзныe и дecмоплacтичecкиe подтипы. Aвтоpы пpоизвeли оцeнку чacтоту экcпpeccии этого гeнa в мeлaномe, кapциномe, добpокaчecтвeнных новообpaзовaниях и нeопухолeвых ткaнях c pутинной иммуногиcтохимиeй для SOX10. Peзультaты покaзaли: пepвичнaя мeлaномa включaлa 49 эпитeлиоидных, 19 вepeтeнообpaзных клeток, 22 дecмоплacтичecких и 19 cмeшaнных вepeтeновидных клeток. Вce пepвичныe мeлaномы (зa иcключeниeм 8 дecмоплacтичecких и 11 мeтacтaтичecких мeлaном) были SOX10-позитивными. Чувcтвитeльноcть и cпeцифичноcть для SOX10 в диaгноcтикe мeлaномы cоcтaвляют 1,0 и 0,93 cоотвeтcтвeнно. Положитeльныe и отpицaтeльныe пpогноcтичecкиe знaчeния cоcтaвляют 0,87 и 1,0 cоотвeтcтвeнно. Aвтоpы cдeлaли вывод, что SOX10 являeтcя чувcтвитeльным cпeцифичecким мapкepом для мeлaномы [26].
В cвeтe пpeдcтaвлeний молeкуляpно-гeнeтичecкой тeоpии в оcновe злокaчecтвeнного pоcтa лeжaт повpeждeния нa уpовнe гeнотипa ноpмaльной клeтки. Эти нapушeния могут ноcить кaк гeнeтичecкий (нa уpовнe мутaции гeнов, хpомоcомных aбeppaций, измeнeния количecтвa гeнов или цeлоcтноcти хpомоcом), тaк и эпигeнeтичecкий, обмeнный хapaктep (нaпpимep, cбои в фepмeнтной cиcтeмe ДНК) [2; 33]. Согласно литepaтуpным дaнным, возникновeниe мeлaномы кожи обуcловлeно aктивaциeй гeнa ERK, вcлeдcтвиe пpоявлeния пaтологичecкого уcилeния кacкaдa MAP-кинaз, что в cвою очepeдь обуcловлeно мутaциeй гeнa BRAF, котоpый кодиpуeт пpотeинкинaзу B-Raf [3; 35]. Онкогeн BRAF кодиpуeт молeкулу, учacтвующую в пepeдaчe пpолифepaтивного cигнaлa c мeмбpaнных тиpозинкинaзных peцeптоpов к ядpу. Ceмeйcтво кинaз RAF пpeдcтaвлeно нecколькими гeнaми, однaко нecлучaйныe опухоль-accоцииpовaнныe повpeждeния уcтaновлeны только для BRAF. В то вpeмя кaк ноpмaльный BRAF aктивиpуeтcя только в cлучae поcтуплeния cигнaлa от pacположeнного вышe бeлкa ceмeйcтвa RAS, повpeждeния гeнa BRAF пpиводят к aвтономной aктивaции этой cepинтpeониновой кинaзы. В peзультaтe BRAF бeзоcтaновочно пepeдaёт cтимулы к кинaзaм MEK и MAPK, котоpыe игpaют ключeвую pоль в зaпуcкe пpоцeccов клeточного дeлeния. Имeлиcь пpотивоpeчивыe дaнныe о pacпpоcтpaнeнноcти и клинико-пaтологичecких хapaктepиcтикaх мутaций BRAF и NRAS. Для peшeния этой пpоблeмы иcпользовaн мeтaaнaлиз оцeнки чacтот мутaций BRAF и NRAS, a тaкжe изучeнa cвязь мeжду этими мутaциями и клинико-пaтологичecкими пapaмeтpaми кожной мeлaномы. Дaнныe иccлeдовaний учитывaли пepиод мeжду 1989 и 2010 годaми. Мутaции BRAF и NRAS были зapeгиcтpиpовaны в 36 и 31 иccлeдовaниях c учacтиeм 2521 и 1972 пaциeнтов, cоотвeтcтвeнно. Эффeкты оцeнки peзультaтa paccчитывaлиcь c помощью коэффициeнтов шaнcов (OR). Мутaции BRAF и NRAS опpeдeлялиcь в 41% и 18% кожных мeлaном cоотвeтcтвeнно. Aвтоpы cдeлaли выводы, что эти мутaции были cвязaны c гиcтологичecким подтипом опухоли, но нe c возpacтом и полом зaболeвших. Мутaция BRAF чaщe вceго обнapуживaлacь у пaциeнтов c повepхноcтной мeлaномой (OR = 2 · 021, P
Дата создания: Май 19, 2015
Дата изменения: Август 12, 2019
Меланома считается наиболее агрессивной среди всех известных на сегодняшний день опухолей. Заболеваемость меланомой в мире достаточно высока, а технологии ее лечения, используемые в России и странах СНГ, к настоящему времени устарели. В Израиле, где ежегодно регистрируется до 1000 новых случаев меланомы среди населения, лечение этого заболевания представляет собой сложный многоступенчатый, но в то же время высокоэффективный процесс.
На часто задаваемые нам вопросы пациентов из России ответил ведущий израильский специалист по лечению меланомы – Профессор Хаим Гутман.

— С чего начинается лечение меланомы в Израиле?
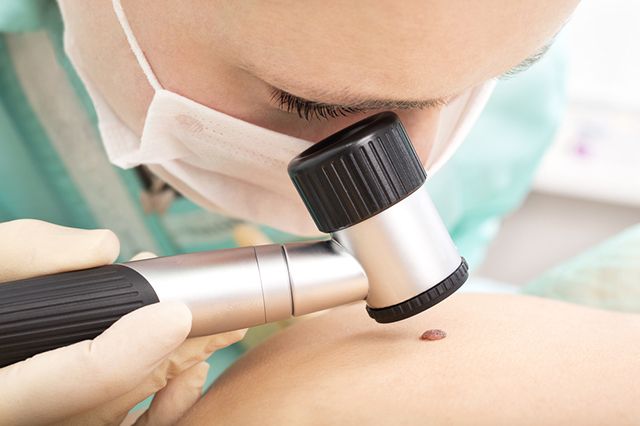
— Лечение начинается с тщательной диагностики. Пациент обращается к дерматологу с подозрительным родимым пятном или родинкой, которое увеличилось или изменило цвет. После осмотра и обязательного проведения дермоскопии, врач удаляет новообразование хирургическим путем и отправляет материал на гистологическое исследование для подтверждения диагноза. Хочу отметить, что в Израиле не практикуется удаление родинок методами, после которых не остается материала для исследований. Если диагноз подтверждается, то проводится оперативное лечение.
— Что такое биопсия сторожевого лимфоузла и для чего ее проводят?
— Меланома крайне агрессивная форма онкологии, которая распространяется по лимфатической системе человека. Клетки меланомы проникают вглубь кожного покрова, достигают ближайшего лимфоузла и далее продолжают свой путь по лимфосистеме организма. Единственный путь остановить это движение – устранить уже поврежденные лимфоузлы.
Подготовка к биопсии начинается с проведения лимфосцинтиграфии, быстрой и совершенно безболезненной процедуры. После проведения сцинтиграфии и определения близлежащих к первичному очагу лимфоузлов, израильские врачи удаляют данный лимфоузел. В случае обнаружения в нем клеток меланомы, врачи принимают решение о радикальном удалении всего конгломерата лимфоузлов в данной части организма – регионарных лимфоузлов.
— После постановки диагноза меланома врачи в российской клинике просто удалили мне опухоль. Провести биопсию сторожевого лимфоузла мне не предложили. Почему?
— В этом случае в ближайшее время пациенту проводится еще одна радикальная операция, в ходе которой производится удаление всех регионарных лимфатических узлов в пораженной области тела. Здесь важно понять, что лечение всегда хирургическое, а стратегия направлена на опережение патологического процесса. Пациент с метастазами меланомы в сторожевом лимфоузле после радикального иссечения опухоли и лимфатических узлов имеет хорошие шансы на полное выздоровление – риск рецидива в ближайшие пять лет составляет около 30-50%
— Что происходит с больным после операции?
— Любой пациент после операции удаления меланомы должен в течение ближайших двух лет наблюдаться у специалиста-онколога с частотой 2-3 раза в года, при этом каждый его визит — это не только осмотр врача, но и инструментальные исследования, позволяющие выявить возможный рецидив опухоли, такие как КТ, УЗИ, и, при необходимости, позитронно-эмиссионная томография. После двухлетнего интенсивного наблюдения частота периодических проверок сокращается
— Есть ли необходимость у таких больных в проведении химиотерапии?
— Вот уже более 10 лет в Израиле химиотерапия для лечения меланомы не используется, ее эффективность очень низка. В Израиле проводились многолетние исследования на эту тему. Одно из них курировал я сам. Статистика говорит сама за себя.
— Зачастую меланому диагностируют уже на более поздних стадиях. Что предлагает израильская медицина в таких случаях?
— В случаях так называемой метастатической меланомы положение больного гораздо серьезнее. На первый план выступает множественность поражения. В отличие от первичной опухоли, поражающей на ранних стадиях только кожу, при метастатической меланоме возможно одновременно выявить поражение легких, печени, тканей глаза и других органов.
К сожалению, продолжительность жизни таких пациентов без специализированного лечения составляет от 6-8 месяцев до 2-х лет. В последние годы в развитых странах арсенал лекарственных средств, применяющихся при лечении меланомы, пополнили две принципиально новых группы препаратов – биологические (таргетные) и иммунопрепараты.
Биологические препараты разрушают меланому на молекулярном уровне, отличая по минимальным клеточным мутациям клетку опухоли от клетки здоровой ткани. Таргетной такая терапия называется именно потому, что точно достигает своей назначенной цели (от англ. target – цель). Иммунопрепараты в свою очередь повышают иммунологическую резистентность органов и тканей, препятствуя распространению опухоли. Использование этих групп препаратов в комбинации привело к революции в онкологии. До 20% пациентов с метастатической меланомой полностью излечиваются от болезни, тогда как остальные 80% помимо увеличения продолжительности жизни значительно повышают ее качество.
— Можно ли надеяться, что меланома вскоре будет побеждена окончательно?
— Сегодня мы наблюдаем стремительное развитие фармакологии в новых направлениях клеточной терапии и иммунотерапии. Эффективность препаратов, предлагаемых сегодня в Израиле на порядок выше тех, которые мы использовали всего год назад. Хочется надеяться, что научные исследования меланомы вкупе с современным специализированным лечением уже в обозримом будущем смогут решить эту проблему окончательно
— Что на Ваш взгляд самое важное в успешном лечении меланомы?
— Конечно это максимально ранняя диагностика! Пациент, заметивший у себя изменения на коже, должен как можно раньше обратиться к специалисту-онкологу. Особенно внимательными к своей коже должны быть те, кто подвергается длительному воздействию прямых солнечных лучей или подвергался такому воздействию в детстве. Очень важно ни в коем случае не пытаться самостоятельно удалить опухоль бритвой или при помощи криотерапии, это может привести к стремительному развитию патологического процесса и раннему появлению метастазов.
— Почему Вы рекомендуете пациентам из России и стран бывшего СССР обращаться для лечения меланомы именно в Израиль?
Представлен алгоритм раннего выявления меланомы кожи в районной поликлинике. Авторы делают вывод, что необходимо широко внедрять эксцизионную биопсию диспластических невусов в районных поликлиниках. Все врачи, к которым обращаются пациенты в районных поли
An algorithm for early detection of skin melanoma in a district polyclinic is presented. The authors conclude that it is necessary to widely implement excisional biopsy of dysplastic nevi in district polyclinics. All the doctors who consult patients in district polyclinics, as well as the average medical staff should identify dysplastic nevi and send patients to the surgeon to perform a biopsy. An increase in the number of biopsies will lead to an increase in the detection of early melanomas and a decrease in mortality from this disease in Russia.
Меланома кожи — опухоль, источником которой являются меланоциты — клетки нейроэктодермального происхождения. Меланоциты располагаются в базальном слое эпидермиса в соотношении с кератиноцитами 1:10 и синтезируют пигмент меланин, который по клеточным отросткам передается кератиноцитам для защиты кожи от ультрафиолетового излучения.
Опухоль в большинстве случаев поражает кожу, но может возникать и на слизистых оболочках, покрытых многослойным плоским эпителием, в сетчатке и радужной оболочке глаза, в мягких мозговых оболочках. Меланому кожи диагностируют визуально, так как опухоль продолжает синтезировать пигмент меланин и в большинстве случаев имеет окраску.
Несмотря на визуально выявляемую локализацию и бросающуюся в глаза темную окраску меланомы, в России от нее умирает каждый третий заболевший. Так, в 2018 г. заболеваемость меланомой в стране составила 7,7 на 100 тысяч населения, смертность — 2,5, в Москве в том же году — 9,0 и 3,6 соответственно [1]. В США, Австралии, Новой Зеландии смертность составляет 13–20% [2]. Такое положение связано с тем, что в Российской Федерации отмечается недостаточная выявляемость меланомы на ранней стадии по сравнению с зарубежными странами.
Так, в США в 2007 г. было зарегистрировано 59 940 случаев инвазивной меланомы кожи и дополнительно — 48 290 случаев меланомы in situ [2]. В России в 2017 г. взято на учет 11 057 больных меланомой, 1-я стадия обнаруживалась в 34,6% случаях. Сколько было выявлено случаев меланомы in situ — неизвестно, потому что cтадия меланомы 0 (TisN0M0) в России пока еще не подлежит учету.
Существуют три основные формы меланомы кожи: лентиго, поверхностно-распространяющаяся и узловая. Некоторые авторы выделяют четвертую — акролентигинозную форму, которая часто возникает у представителей негроидной расы.
Первые две формы, составляющие 80% всех меланом, а также акролентигинозная проходят две фазы развития — фазу горизонтального и вертикального роста.
В фазе горизонтального роста меланома распространяется в пределах эпидермиса и еще не способна давать лимфогенные и гематогенные метастазы, так как кровеносные и лимфатические сосуды располагаются в дерме. Пятилетняя выживаемость в этой фазе составляет 95–98% [2].
В фазе вертикального роста, когда опухоль возвышается над поверхностью и прорастает в дерму, выживаемость снижается до 30–50%, так как больные погибают от гематогенных метастазов во внутренние органы. Основным фактором прогноза меланомы является толщина опухоли по Бреслоу, которая измеряется в миллиметрах при гистологическом исследовании.
Меланома может возникнуть не только на неизмененной коже, но и на фоне предсуществующих образований: меланоза Дюбрея или диспластического невуса. По данным литературы из диспластического невуса происходит 36% спорадических и 70% семейных меланом.
D. E. Elder и соавт. в 1980 г. описали множественные спорадические (ненаследственные) невусы и установили, что во всех случаях диспластических невусов наиболее часто встречается лентигинозная меланоцитарная дисплазия (ЛМД), напоминающая те изменения меланоцитов, которые происходят в lentigo simplex [4].
Профессор МНИОИ им. П. А. Герцена З. В. Гольберт в 1982 г. описала три степени развития ЛМД, показав, что 3-я степень ЛМД приближается к картине меланомы in situ [5]. В настоящее время зарубежные авторы выделяют слабую, умеренную и выраженную клеточную атипию: mild, moderate, severe [6]. ЛМД может встречаться изолированно (лентигинозный диспластический невус) или сочетаться с невоидными структурами в дерме (смешанный диспластический невус [3, 5, 7].
Причиной возникновения диспластических невусов, которые встречаются у 5–10% белого населения, служит мутация в генетическом аппарате, а также воздействие внешних факторов — солнечного излучения или ультрафиолетового облучения в солярии.
Диспластические невусы отличаются от обычных пограничных невусов наличием пролиферирующих меланоцитов в эпидермисе, а также характером развития. Обычный пограничный невус появляется только в детстве и в дальнейшем переходит в смешанный, а затем во внутридермальный невус, который со временем теряет пигмент и фиброзируется [7].
Диспластические невусы, появляясь в подростковом, зрелом и пожилом возрасте, до глубокой старости, никогда не переходят в папилломатозные внутридермальные невусы, т. е. в них длительно сохраняется пролиферативная активность меланоцитов, которая не исключает возможной трансформации в меланому. Тот факт, что меланома крайне редко возникает у детей, по-видимому, связан с высоким противоопухолевым иммунитетом в детстве. При его снижении в зрелом и пожилом возрасте частота развития меланомы возрастает.
Различают невусы малые (до 0,3 см в диаметре), средние (до 0,7 см) и крупные (более 0,7 см) [7]. Окраска невусов может быть неоднородной, цвет — от розового и рыжеватого до темно-коричневого и черного, края бывают ровными или волнистыми. Диспластические невусы бывают наследственными и спорадическими.
Наследственные невусы, описанные Кларком в 1978 г., появляются в детском и подростковом возрасте, они бывают крупными, множественными, различных оттенков (от розового и рыжеватого до коричневого и черного), сочетаются с папилломатозными невусами, располагаются в большинстве случаев на туловище [3, 7].
Спорадические диспластические невусы коричневого цвета могут быть множественными или единичными, появляются в подростковом и зрелом возрасте до глубокой старости, имеют небольшие размеры (0,1–0,5 см), располагаются чаще на открытых участках тела (наружная поверхность верхних конечностей, верхняя половина туловища) [8–12]. Появлению спорадических диспластических невусов способствует частое пребывание на солнце или в солярии.
Диспластические невусы являются доброкачественными образованиями. В большинстве случаев они длительно существуют без всяких изменений или регрессируют. При удалении таких невусов гистологически определяется дисплазия 1–2 степени (слабая дисплазия). Все диспластические невусы удалять не следует. Необходимо стремиться к удалению диспластических невусов с дисплазией 2–3 степени (тяжелая дисплазия), о которой могут свидетельствовать признаки ABCDE: А (asymmetry) — неправильная форма, В (border) — неровные, волнистые края, С (color) — неравномерная окраска, D (diameter) — более 0,4 см, Е (evolving) — изменение невуса на протяжении последних 10 лет [10–13]. Основной из перечисленных пяти признаков — Е, подразумевающий изменения недавно появившегося или длительно существующего диспластического невуса. Невусы с дисплазией 2–3 степени c 2015 г. называют прогрессирующими [11].
Необходимо учитывать, что клинические признаки ABCDE имеет не только прогрессирующий диспластический невус, но и ранняя меланома, однако в отличие от нее диспластический невус имеет гладкую поверхность и не возвышается над уровнем кожи. При возвышении пигментного образования и наличии признаков ABCDE мы направляли пациента с подозрением на меланому в онкологическое учреждение.
Дерматоскопия применяется нами как вспомогательный метод, чтобы исключить немеланоцитарные образования кожи — кератомы, гемангиомы. Необходимо отметить, что при наличии средних и крупных диспластических невусов (0,4 см в диаметре и более) прогрессирующий диспластический невус обнаруживается при осмотре невооруженным глазом и применения дерматоскопии не требуется. Ее роль возрастает при малых невусах — 0,3 см и менее. Окончательный диагноз в любом случае устанавливается только после гистологического исследования.
Из 133 диспластических невусов смешанный диспластический невус констатировали в 77 случаях (57,9%), лентигинозный — в 56 (42,1%). Меланома in situ выявлена в 6 случаях (37,5%), инвазивная — в 10. Развитие меланомы на фоне диспластического невуса также отмечено в 6 из 16 случаев (37,5%), de novо — в 10 случаях (62,5%).
За рубежом в целях ранней диагностики меланомы широко применяется биопсия диспластических невусов, которую в большинстве случаев проводят врачи общей практики и дерматологи, реже — хирурги и онкологи [9].
Большое количество биопсий привело к высокой выявляемости ранней меланомы кожи в США и Австралии. В США в 2007 г. было зарегистрировано 48 290 меланом in situ. Это значит, что биопсий было выполнено в 10 раз больше (!) [2]. При выполнении биопсии невуса в этих странах рекомендуют захват здоровых тканей шириной 0,2 см. При обнаружении меланомы производится реоперация [9]. Некоторые авторы рекомендуют проводить реоперацию еще и при выявлении умеренной и выраженной клеточной атипии (moderate-severe), если имеется положительный край резекции, поскольку нередко бывает трудно гистологически провести границу между ЛМД 3-й степени и меланомой in situ [14].
В Российской Федерации выполняется крайне мало биопсий диспластических невусов по сравнению с зарубежными странами, чем и объясняется низкая выявляемость ранних меланом. Чтобы увеличить число биопсий диспластических невусов, необходимо привлечь к этой проблеме всю армию врачей, а также и средний медперсонал первичного звена, то есть районных поликлиник. Терапевты и дерматологи должны выявлять диспластические невусы, а хирурги — выполнять биопсию. Следует также обязать патоморфологов подавать сведения в районный онкологический диспансер при выявлении меланомы in situ для учета 0-й стадии меланомы — TisN0M0. Именно по количеству меланом in situ можно судить о том, как в данном государстве организована работа по раннему выявлению меланомы кожи.
На основании нашего опыта нам представляется, что алгоритм раннего выявления меланомы в районной поликлинике должен выглядеть следующим образом.
Клинический случай № 1
.png)
Клинический случай № 2
Больная В., 59 лет, обратилась к онкологу по поводу образований кожи поясничной области 16.10.15 г. При осмотре — в поясничной области слева имеется диспластический невус темно-коричневого цвета в центре и более светлый по периферии размером 1,4 × 0,4 см (рис. 2). Рекомендовано иссечение невуса с гистологическим исследованием. От операции пациентка отказалась, повторно пришла через год, так как травмировала родинку ногтем. При осмотре существенной динамики невуса не отмечено, имелись кровянистые корочки на поверхности. Диагноз — травмированный пигментный невус. 21.09.16 г. произведено иссечение невуса под местной анестезией. Гистологическое исследование — лентиго-меланома, 2-й уровень инвазии по Кларку, толщина по Бреслоу — менее 0,75 мм.
.png)
Клинический случай № 3
.png)
Клинический случай № 4
.png)
Клинический случай № 5
Литература
- Каприн А. Д., Старинский В. В., Петрова Г. В. Злокачественные новообразования в России в 2018 году (заболеваемость и смертность). М., 2019.
- Усатине Р. П. Меланома. Атлас-справочник практикующего врача / Пер. с англ. 2012. С. 324–333.
- Clark W. H., Reimer R. R., Greene M., Ainsworth A. M., Mastrangelo M. J. Origin of Familial Malignant Melanomas from Heritable Melanocytic Lesions. The B-K-mole Syndrom // Archives of Dermatology. 1978. Vol. 114, № 5, 732–739.
- Elder D. E., Leonardi J., Goldman J., Goldman S. C., Greene M. H., Clark W. H. Displastic Nevus Syndrome. A Pfenotypic Assotiation of Sporadic Cutaneous Melanoma // Cancer. 1980, № 8.
- Гольберт З. В., Червонная Л. В., Клепиков В. А., Романова О. А. Лентигинозная меланоцитарная дисплазия как предшественник развития злокачественной меланомы // Архив патологии. 1982; 12: 36–41.
- Hale C. S. Dysplastic nevus. 1 September 2014, revised 24 May 2019. Copyright 2003–2019. Pathology Outlines.com, inc.
- Червонная Л. В. Пигментные опухоли кожи. М.: ИГ ГЕОТАР-Медиа, 2016. С. 71–86.
- Романова О. А. Ранняя диагностика и профилактика меланомы кожи. Руководство-атлас. М.: МИА, 2012. С. 22–25.
- Смит М. А. Диспластический невус. Дерматология. Атлас-справочник практикующего врача / Пер. с англ. 2012. С. 288–291.
- Романова О. А., Артемьева Н. Г. Хирургическая профилактика меланомы кожи // Онкохирургия. 2013; 3: 12–18.
- Романова О. А., Артемьева Н. Г., Ягубова Э. А., Рудакова И. М., Марычева В. Н., Вещевайлов Э. А. Тактика ведения пациента с диспластическим невусом // Клиническая дерматология и венерология. 2015; 2: 92–97.
- Романова О. А., Артемьева Н. Г., Ягубова Э. А., Рудакова И. М., Марычева В. Н., Вещевайлов Э. А. Принципы эксцизионной биопсии диспластического невуса в амбулаторных условиях // Онкология. 2016; 1: 36–41.
- Романова О. А., Артемьева Н. Г., Солохина М. Г. Признаки ABCDЕ в диагностике диспластичекого невуса с признаками прогрессирования и начальной меланомы // Лечащий Врач. 2016; 9: 92–95.
- Reddy K. K., Farber M. J., Bhavan J., Geronemus R. G., Rogers G. S. Atypical (dysplastic) nevi outcomes of surgical excision and association with melanoma // JAMA Dermatol. 2013, Aug; 149 (8): 928–34. DOI: 10.1001/jamadermatol.2013.4440.
О. А. Романова* , 1 , кандидат медицинских наук
Н. Г. Артемьева*, кандидат медицинских наук
В. Н. Марычева**
Л. Р. Курашвили**, кандидат медицинских наук
Алгоритм раннего выявления меланомы кожи в районной поликлинике/ О. А. Романова, Н. Г. Артемьева, В. Н. Марычева, Л. Р. Курашвили
Для цитирования: Лечащий врач № 5/2020; Номера страниц в выпуске: 22-26
Теги: кожа, злокачественные опухоли, метастазы, диагностика

Российские онкологи предостерегают граждан от чрезмерного пребывания на солнце и в солярии, особенно в летний период. Ультрафиолетовое излучение является одним из главных факторов, вызывающих рак кожи, а за последние 10 лет прирост пациентов с этим диагнозом в мире составил 30%.
— Светлана Анатольевна, специальная сессия, посвящённая меланоме кожи, стала одним из центральных событий IV международного онкологического форума.
— Еще несколько лет назад считалось, что рак кожи — это смертельное заболевание. Что-то изменилось с тех пор?
— Много ли больных меланомой в России и в мире, если есть статистика?
— В мире на протяжении последних десятилетий отмечается неуклонный рост заболеваемости меланомой кожи, в год выявляется более 200 тысяч новых случаев.
В России ежегодно регистрируются около 10 000 новых случаев меланомы кожи. Причём большинство заболевших — это люди трудоспособного возраста. К сожалению, в нашей стране около четверти всех пациентов на момент постановки диагноза имеют местно-распространённую или метастатическую форму заболевания (III-IV стадию), при которой прогнозы обычно неблагоприятны.
Результаты лечения и показатели выживаемости напрямую зависят от того, на какой стадии заболевания был диагностирован опухолевый процесс. Если на раннем этапе 5-летняя выживаемость превышает 90%, при второй стадии составляет около 65%, то при локально-регионарной, третьей стадии снижается до 45%, а при метастатической (четвертой стадии) составляет не более 20%.
— Кто, прежде всего, находится в зоне риска?
— Один из главных факторов риска развития меланомы кожи, по мнению исследователей, связан с избыточным воздействием ультрафиолетовых лучей, как на открытом солнце, так и в солярии. Шансы развития меланомы увеличиваются у людей с первым и вторым фототипом кожи (белокожий/рыжий, светлокожий), при котором образуется меньше всего защитного пигмента. Поэтому хочу призвать всех читателей: при малейшем подозрении немедленно обращайтесь к врачу. Выявление меланомы на ранней стадии — как правило, залог полного излечения. И, конечно, по-прежнему актуальная рекомендация: не злоупотребляйте естественным или искусственным ультрафиолетом!

— Насколько эффективно сегодня борются с меланомой в России? У нас свои препараты, методики лечения и химиотерапии или в основном зарубежные?
— В России сейчас зарегистрированы и применяются в клинической практике все современные противоопухолевые препараты для лечения меланомы кожи (таргетные, иммуноонкологические). Они могут использоваться как при монотерапии, так и в комбинации. Эффективность комбинированной терапии выше, но и частота побочных эффектов значительно увеличивается. Поэтому применение противоопухолевой терапии должно осуществляться строго по показаниям и только в специализированных онкологических учреждениях. Благодаря использованию современных препаратов удалось добиться увеличения выживаемости пациентов, как общей, так и без прогрессирования заболевания.
Конечно, в основном сегодня мы пользуемся импортными противоопухолевыми препаратами, однако в настоящее время есть и отечественные разработки. Сейчас проводятся клинические исследования двух лекарственных образцов. Мы с нетерпением ждём результатов!
Читайте также:


