Возможности методов визуализации в диагностике и мониторинге опухоли почки
Никольский Ю.Е., Попков В.М., Чехонацкая М.Л., Понукалин А.Н., Захарова Н.Б., Хмара Т.Г., Зуев В.В.
Резюме
На основе анализа данных отечественной и зарубежной литературы, освещены возможности лучевых методов визуализации в диагностике рака почечной паренхимы. Рассмотрены особенности применения различных методов для верификации доброкачественных и злокачественных новообразований почки.
Ключевые слова
Обзор
В России в структуре заболеваемости онкологическими заболеваниями мужского населения рак почки (РП) занимает 9-е место, женского населения – 12-е место. В 2009 г. в нашей стране диагностировано 18328 новых случаев РП. В структуре смертности населения России от злокачественных новообразований почечно-клеточный рак занимает 16-е место. Заболеваемость РП в большинстве стран мира растет, ежегодно увеличиваясь на 2–4,5 % [1]. По абсолютному приросту впервые выявленных онкоурологических заболеваний почечная карцинома занимает второе место, уступая раку предстательной железы [2].
Почечная карцинома – агрессивная опухоль. При первичном обращении к урологу метастазы наблюдаются у каждого третьего больного [3]. Из них порог 5-летней выживаемости достигнут только 5 % [4].
Главной проблемой в диагностике РП стоит выбор алгоритма диагностических методов, которые должны быть неинвазивными и обладать высокой информативностью [7]. При своевременной диагностике РП на ранних стадиях 5-летняя выживаемость больных после выполнения радикальной нефрэктомии достигает 80 % и более. В современной литературе представлены достоинства и недостатки рентгенологических, ультразвуковых и томографических методов визуализации РП и алгоритмы их применения в практической медицине.
Традиционными методами в диагностике объемных образований почек, в том числе и злокачественных опухолей, являются обзорная рентгенография мочевыводящих путей и экскреторная урография. Дешевизна и доступность – достоинства рентгенологических методов исследования почек и мочевыводящих путей.
Рентгенологические признаки характерны для всех объемных образований почек, поэтому дифференциацию между доброкачественными и злокачественными образованиями почек после выделительной урографии и обзорного рентгенологического исследования провести невозможно. По мнению Ю.А. Пытеля и соавт [9], при экскреторной урографии лишь в 67 % наблюдений был выявлен объемный процесс в почке, оказавшийся при дополнительном исследовании опухолью. Урография неэффективна вдобавок при определении стадии опухолевого процесса. Возможность оценки заинтересованности околопочечного пространства отсутствует [7].
Не стоит забывать про вероятность возникновения аллергической или токсической реакции на введение внутривенно йодсодержащего контрастного препарата при выполнении выделительной урографии и лучевую нагрузку на пациента.
Существует мнение, что от выполнения экскреторной урографии можно отказаться, припегнув к помощи ультразвукового исследования (УЗИ), а затем мультиспиральной компьютерной томографии (МСКТ) [10].
Выполнение УЗИ для первичного обнаружения опухоли почки в большинстве случаев вполне достаточно. Эхографический метод считается методом первичной диагностики РП. Благодаря ему удается выявить до 80 % бессимптомных опухолей почки. При этом количество больных с малыми опухолями паренхимы почки ежегодно увеличивается. Точность ультразвукового метода (УЗ метод) в диагностике опухолей почек составляет 96 – 97,3 % [11]. Информативность экскреторной урографии и эхографии в диагностике злокачественных опухолей почки размером до 3 см. составляет 67 % и 79 % соответственно [12]. Эффективность ультразвуковой диагностики в обнаружении опухолей почки менее 1,5 см. низка. Проблему для визуализации представляют также интрапаренхиматозные опухоли без деформации контура почки. Выявление опухолей размерами более 3 см. в клинической практике для УЗИ не представляет сложности.
При выполнении эхографии возможно проведение цветового доплеровского картирования (ЦДК), которое дает информацию о типе васкуляризации опухолевого узла [15]. В настоящее время широко применяется энергетическое доплеровское картирование (ЭДК), данные которого сопоставимы с результатами рентгеновской ангиографии [7].
УЗИ на амбулаторном этапе при РП должно включать в себя обязательный осмотр почечных сосудов и нижней полой вены [16]. Сканирование почечных вен, нижней полой вены и правого предсердия необходимо для определения протяженности венозной инвазии РП [8], выявляемость которой эхографическим методом колеблется от 50 до 95 %. Информацию об опухолевом поражении нижней полой вены дополняют ангиография, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ).
Чувствительность УЗИ в определении увеличенных лимфатических узлов составляет от 50 до 90 %. Среди достоинств эхографии важно отметить возможность выявления метастатического поражения печени [1] и оценку вовлеченности в патологический процесс лимфатических узлов.
Под контролем УЗ метода выполняется интраоперационная оценка локализации и размеров опухоли при резекции почки, проводится тонкоигольная аспирационная биопсия и последующий мониторинг подвергнутых оперативному вмешательству больных [1, 17]. Несмотря на высокую ценность и информативность УЗИ, необходимо выполнение компьютерной или магнитно-резонансной томографии [18].
КТ обладает высокой способностью оценивать структуру опухоли. Например, присутствие кальцинатов в капсуле и солидного мягкотканного компонента в составе кистозного образования почки будет в пользу злокачественного процесса [1]. КТ помогает дифференцировать карциному почки и ангиомиолипому. Присутствие жировых компонентов в составе опухоли является патогномоничным признаком ангиомиолипомы [22]. Иногда жировые элементы входит в состав почечно-клеточной карциномы, и тогда отличить ее от ангиомиолипомы крайне затруднительно. На РП будут указывать участки кальцинации в составе опухолевого узла.
Чувствительность КТ без использования контрастного усиления в выявлении опухолей почки составляет 85,2 %, специфичность – 94,8 % [23]. КТ, выполненная с контрастным усилением, информативнее нативного исследования, особенно в верификации опухолей до 4 см. с частичной деформацией контуров почки или расположенных внутри паренхимы почки. Благодаря контрастной КТ определяют принадлежность опухоли почки к паренхиме или чашечно-лоханочной системе, измеряют ее точные размеры опухоли и изучают топографическое отношение к почечным сосудам, околопочечным тканям и прилежащим органам [24].
КТ высоко информативна в диагностике опухолевого тромбоза почечной вены и нижней полой вен и позволяет оценивать протяженность опухолевого тромба [26]. Общая точность метода в идентификации венной инвазии при РП варьирует от 68 до 96 %. Ограничением в визуализации венной инвазии является одновременное контрастирование опухоли и крови в нижней полой вене [1].
КТ значительно эффективнее УЗ метода в определении заинтересованности периренальной клетчатки. Считается, что КТ со 100 % достоверностью позволяет оценивать вовлечение в процесс рядом расположенных структур [7].
КТ-ангиография информирует о сосудистой архитектонике пораженной раковым узлом почки, позволяя сканировать кровеносные сосуды, диаметром которых не превышает 1 – 2 мм. в объемной трехмерной реконструкции, и определять локализацию метастазов в печеночной паренхиме в соответствии с ее сегментарным строением. При выполнении КТ-ангиографии возможна оценка протяженности и границы опухолевого тромба почечной вены и нижней полой вены. Чувствительность метода составляет 88 %, специфичность – 94 %.
Выполнение трехмерных реконструкций при КТ сканировании почек дает возможность исследовать пространственную локализацию, распространенность, сосудистую архитектонику опухоли, наличие и степень венозной инвазии, вовлечение в процесс регионарных лимфатических узлов, а также оценить состояние мочевыводящих путей. Полученные данные помогают в планировании резекции почки [10,28].
При проведении КТ почек лучевая нагрузка на больного, в среднем, составляет 3–6 мЗв. Это в несколько раз превышает дозу излучения при рентгенографии грудной клетки и должно учитываться при обследовании детей и женщин детородного возраста. При УЗИ и МРТ радиационная нагрузка на обследуемого отсутствует.
Рентгеноконтрастные йодсодержащие препараты, используемые для контрастного усиления при КТ, могут вызывать аллергические и нефротоксические реакции. Их не следует вводить пациентам с почечной недостаточностью. В таких случаях МРТ должна заменять КТ [29].
Возможность выполнения исследования без подготовки пациента, получение изображения в трех взаимно перпендикулярных плоскостях на разных уровнях без перемещения больного, отсутствие артефактов от костных структур, изменение импульсных последовательностей, высокая разрешающая способность – все это делает МРТ высокоинформативным методом визуализации опухолей почки, результаты которого не зависят от телосложения пациента, от наличия газов в кишечнике [30].
Одним из недостатков МРТ диагностики является визуализация отложений кальция. В свою очередь, наличие кальцинатов в стенке кистозного образования может быть признаком кистозной формы почечно-клеточного рака. Проведение МРТ рекомендуется при сомнительных данных КТ. Особенно для дифференциации сложных кист почки от кистоподобных форм РП.
Использование контрастного усиления позволяет МРТ обнаруживать опухоли почек размером менее 1см. В целом, МРТ сравнима с КТ в выявлении объемных образований почки: чувствительность метода равна 93,5 % против 93,8 % у КТ. Но полная точность МРТ в дифференицальном диагнозе почечных образований превосходил таковую КТ. Импульсные последовательности с подавлением сигнала от жира помогают отличать жиросодержащие опухоли почки, такие как липома, ангиомиолипома и фибросаркома, от почечной карциномы, обнаруживать кисты и опухоли диаметром менее 1 см. [29].
Данные о распространенности опухоли почки, полученные при МРТ, информативнее аналогичных данных КТ, что помогает более достоверно определить Т– и N–стадии РП. Т–стадия достоверно определяется КТ в 78,4 %, по МРТ – в 84 % случаев, а стадия N в 81,8 % и 79,5 % соответственно. Еще одним преимуществом МРТ перед КТ является более высокая информативность в обнаружении псевдокапсулы опухоли почки, которую чаще имеют высоко- или умереннодифференцированные почечные карциномы размерами до 4 см. [29]. Наличие псевдокапсулы является показанием к выполнению органосохраняющей операции. Дефекты псевдокапсулы служат признаками инвазивного роста РП, позволяя точнее определить стадии T1 и Т3a [10]. МРТ эффективна в диагностике экстраренальной инвазии опухоли, инфильтрации окружающих органов и тканей [29].
По некоторым данным, МРТ проигрывает КТ в оценке поражения лимфатических узлов. Так, по данным А.С. Переверзева и соавт. [31] точность МРТ в диагностике забрюшинной лимфаденопатии при РП, считая метастатически пораженными лимфатические узлы размерами более 1 см., составила 93,5 %, чувствительность – 90,6 %, специфичность – 94,7 %. Согласно другим источникам, чувствительность МРТ в диагностике лимфаденопатии составляет более 95 % [14].
Точность МРТ в выявлении опухолевой инвазии РП почечной вены и нижней полой вены составляет 98 % и 100 % соответственно, чувствительность – 95 %, специфичность – 100 % [7,29]. МРТ позволяет дифференцировать опухолевый и кровяной тромб, четко определять верхнюю границу опухолевой инвазии нижней полой вены и ее протяженность, что дает возможность не проведить больному нижнюю венокавографию [8]. Однако МР сканирование почечной вены и нижней полой вены ограничено артефактами от дыхания и сердечной деятельности.
МРТ обладает преимуществом перед КТ и УЗ методом в оценке вторичных изменений при РП в печени, костях, головном мозге. Например, при КТ есть вероятность пропустить маленькие очаги метастатического поражения, локализованные в задней черепной ямке. Всем страдающим РП со спинальными и радикулярными симптомами рекомендуется МРТ всего позвоночника и спинного мозга [32].
Если сравнивать КТ и МРТ между собой, то оба метода позволяют выявить новообразование почки и помочь в оценке стадии процесса [29], а также обеспечить мониторинг пациентов в послеоперационном периоде.
Противопоказаниями к проведению МР-исследования являются наличие у больного клаустрофобии (боязни замкнутого пространства), металлических имплантатов и протезов, водителей сердечного ритма.
В последнее время ангиография используется все реже в связи с широким применением ультразвуковой допплерографии, позволяющая без предварительной подготовки больного и без инвазии получать информацию о характеристиках почечного кровотока [33].
Нижняя кавография в недалеком прошлом выполнялась всем больным РП с венной инвазией. Верхняя кавография применялась при полном блоке нижней полой вены и при плохой визуализации верхней границы опухолевого тромба [1]. Селективная почечная венография определяет сдавление, прорастание, тромбоз и деформацию ветвей почечной вены. При наличии блока на нижней кавограмме обязательным считается проведение атриовентрикулярной кавографии [7]. В настоящее время кавография проводится больным РП при недостаточной информативности или наличии противопоказаний к выполнению других методов визуализации [1].
Авторы: Tim J. van Oostenbrugge, Jurgen J. Fütterer, Peter F.A. Muldersa
Вступление
Увеличение использования изображений брюшной полости привело к увеличению числа мелких почечных инциденталом в последние десятилетия. Поскольку до 20% твердых небольших почечных новообразований
Из злокачественных опухолей почек 90% составляют почечно-клеточные карциномы (ПКК). Остальные 10% опухолей почки состоят из метанефрических, нефробластических и мезенхимальных опухолей. Группа мезенхимальных опухолей включает в себя широкий спектр сарком. Также встречаются более редкие опухоли, такие как нейроэндокринные, гемопоэтические, лимфоидные, половых клеток и другие.
В этой статье обсуждаются возможности обнаружения и дифференциации опухолей с помощью ультразвука (УЗИ), компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ).
УЗИ
Когда УЗИ стало доступным для обнаружения почечных новообразований, другие методы визуализации, такие как внутривенная пиелография, постепенно устарели. В настоящее время УЗИ считается возможным вариантом первичной визуализации для скрининга опухолей почек.
Для обычного трансабдоминального серошкольного B-режима УЗИ используется датчик с частотой 3–6 МГц. Пациент находится на спине или в положении на боку, а почки сканируются в продольной и поперечной плоскостях. Когда изображение затеняется кишечным воздухом, можно рассмотреть возможность изменения положения пациента. Задержка дыхания после вдоха может улучшить визуализацию почек.
Почечные новообразования распознаются на УЗИ по искажению нормальной структуры тканей. Помимо технических аспектов и состояния организма пациента, эффективность УЗИ при обнаружении опухолей почек зависит от эхогенности, размера и локализации опухоли.
Солидные опухоли почки могут быть категоризированы как полностью солидные, мультифокальные или частично кистозные опухоли. Последние в основном связаны с некрозом. Появление солидных почечных опухолей при УЗИ может варьировать между изоэхогенным, гипоэхогенным и гиперэхогенным по сравнению с нормальной паренхимой почки.
До 77% ПКК ≤30 мм описываются как гиперэхогенные, а остальные являются изоэхогенными или гипоэхогенными по сравнению с нормальной почечной паренхимой и являются более сложными для выявления. До 18% опухолей ≤20 мм и 21% опухолей между 20 и 25 мм не выявляются с помощью УЗИ. В заключение, наиболее сложными опухолями для выявления с использованием УЗИ являются небольшие изоэхогенные опухоли почек, особенно с эндофитным паттерном роста.
В нескольких исследованиях изучалась дифференциация подтипов опухолей почек с использованием УЗИ. Несмотря на то, что большинство ПКК
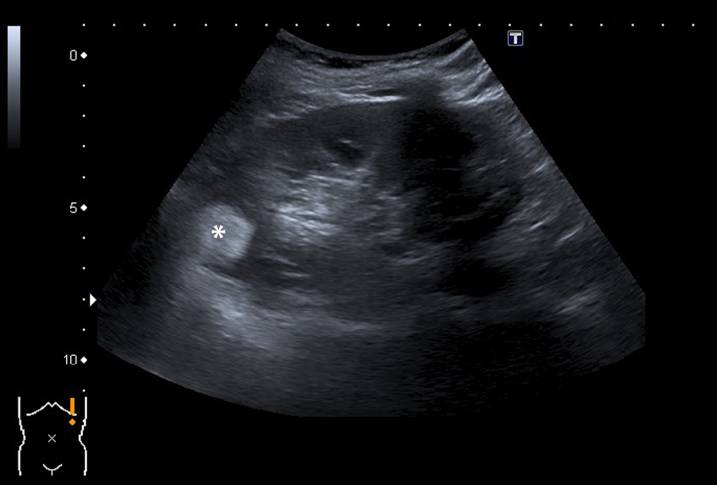
Рисунок 1 : 63-летняя женщина была направлена для наблюдения за ангиомиолипомой, ранее диагностированной на компьютерной томографии. Ультразвук во время наблюдения действительно выявил сильную гиперэхогенную опухоль размером 25 мм (отмеченную звездочкой) в верхнем полюсе левой почки в соответствии с ангиомиолипомой.

Рисунок 2 : 78-летний мужчина прошел УЗИ почек из-за прогрессирующего нарушения функции почек. При ультразвуковом исследовании в среднем / нижнем полюсе левой почки была обнаружена опухоль размером 65 мм (отмечена звездочкой). Опухоль была неоднородной на УЗИ со смешанными изоэхогенными и гиперэхогенными участками.
Сегодня используются дополнительные методы визуализации, чтобы улучшить обнаружение опухолей почки. Цветная допплерография – это метод, в котором эффект допплера используется для визуализации движения жидкостей. Это движение может быть объединено с обычным B-режимом для визуализации кровотока относительно окружающих анатомических структур. Этот метод показал дополнительную ценность в случае изоэхогенных эндофитных опухолей, которые трудно обнаружить при использовании только серошкальных УЗИ. Допплерография может показать сосуды с высокой скоростью кровотока из-за неоваскуляризации.
Было описано, что при опухолях ≤30 мм дополнительное использование допплерографии помогает дифференцировать подтипы на основе паттерна сосудистого распределения, особенно в случае ангиомиолипомы.
CEUS – еще один метод для определения новообразований почек. Этот метод предоставляет информацию о микроциркуляции, в отличие от допплерографии, которая касается макроциркуляции.
Контрастные агенты, используемые для CEUS, не являются нефротоксичными. CEUS более чувствителен при обнаружении гиповаскулярных солидных поражений, не различимых при допплерографии и КТ.
КТ
КТ считается золотым стандартом для характеристики опухолей почек. Из-за своего превосходства над УЗИ и меньшей степенью доступности МРТ КТ часто является первым выбором визуализации для оценки опухоли почки.
Большим преимуществом по сравнению с МРТ является быстрое время сбора данных. Основными ограничениями КТ являются использование ионизирующего излучения и нефротоксичных йодоконтрастных агентов.
Для оптимального выявления и характеристики опухолей почечной коры следует провести КТ с контрастным усилением, состоящую из нерасширенной кортикомедуллярной фазы (25–40 секунд после инъекции) и нефрогенной фазы (100–200 секунд после инъекции).
Минимальная толщина среза для адекватного сканирования составляет 3 мм в сочетании с многоплоскостными реконструкциями.
Посредством 3-фазной КТ можно выявить большинство опухолей почки, и можно охарактеризовать несколько гистологических подтипов на основе исследований, сравнивающих диагноз КТ с окончательным отчетом по гистопатологии после операции / биопсии.
Ангиомиолипома . Ослабление –10 HU или менее является патогномоничным для ангиомиолипомы; однако кальцификации должны вызывать подозрения на ПКК (рис. 3).
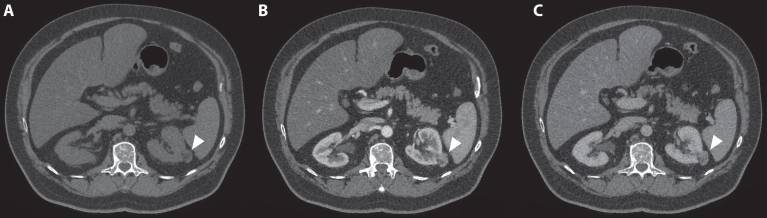
Рисунок 3 : ( A ) В кортикомедуллярной фазе наблюдается усиление опухоли ( B ) с умеренным эффектом вымывания в нефрогенной фазе ( C ).
Кисты. Гомогенное поражение с гладкой стенкой, без перегородок, без кальцификации и затуханием от –10 до +20 HU на не усиленной КТ соответствует простой кисте. Ослабление> 70 HU указывает на геморрагическую кисту. После введения контраста увеличение> 20 HU отмечает опухоль как неопределенную и подозрительную для ПКК.
ПКК. Светлоклеточная ПКК демонстрирует сильное усиление в кортико-медуллярной фазе (в среднем 114 ± 44 HU) из-за гиперваскуляризации и оказывает эффект вымывания во время нефрогенной фазы (в среднем 66 ± 24 HU) (рис. 4).
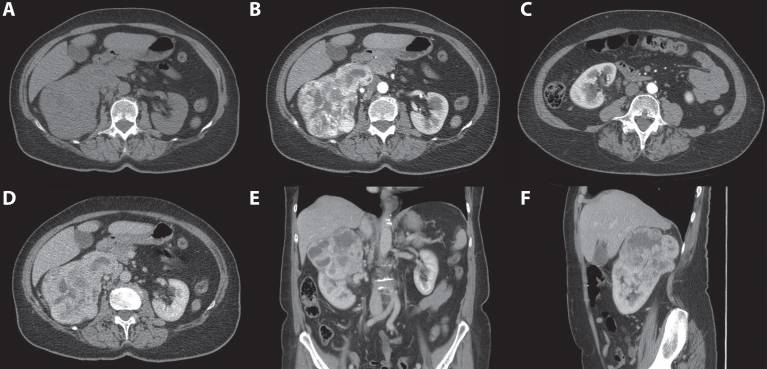
Рисунок 4 : 70-летняя женщина. При скрининговом УЗИ выявлена гиперваскулярная и гиперэхогенная почечная масса правой почки. 3-фазная компьютерная томография показала опухоль, выходящую из верхнего полюса правой почки. ( A ) Сильное усиление твердых частей наблюдается в кортикомедуллярной фазе. ( B ) Нижний полюс правой почки не был затронут. ( C ) В нефрогенной фазе наблюдается явный эффект вымывания.
Папиллярный ПКК . Папиллярный ПКК может иметь гетерогенный вид, опухоли обычно однородны и гиповаскулярные. Поэтому усиление контраста обычно более тонкое по сравнению с светлоклеточным ПКК и измеряется до 20 HU в кортико-медуллярной фазе (рис. 5).
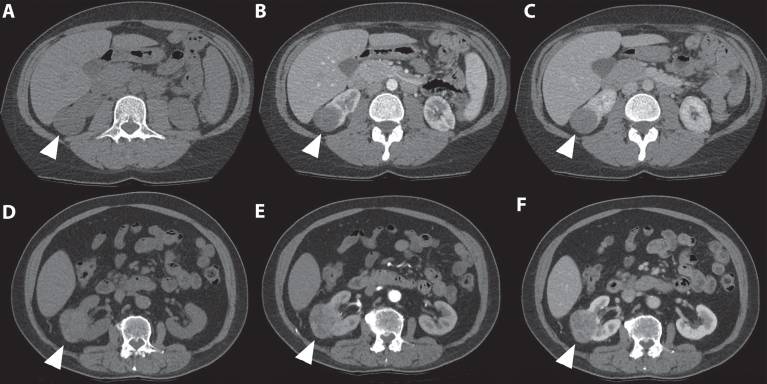
Рисунок 5 : На этом снимке показано различие во внешнем виде и усилении структуры светлоклеточного и папиллярного почечно-клеточного рака. Первый случай ( A-C ) касается 41-летней женщины, направленной на анализ инциденталомы правой почки, обнаруженной при УЗИ. 3-фазная компьютерная томография показала, что опухоль нижнего полюса правой почки размером 36 мм имеет типичное постепенное усиление. Второй случай ( D-F ) касается 67-летнего мужчины, у которого при МРТ позвоночного канала была обнаружена инциденталома в правой почке. Опухоль оценивали с помощью компьютерной томографии, которая показала межполярную опухоль правой почки размером 67 мм.
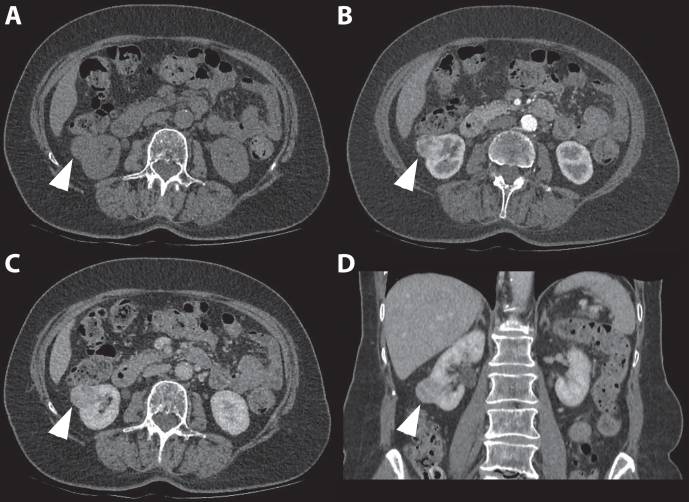
Рисунок 6 : 80-летняя женщина была направлена со случаем инциденталомы правой почки, обнаруженной при УЗИ. Трехфазная компьютерная томография показала изоаттенуирующую экзофитную опухоль почки правого нижнего полюса в неконтрастной фазе. ( A ) Неоднородный характер усиления наблюдается в кортикомедуллярной фазе ( B ) с последующим вымыванием во время нефрогенной фазы ( C и D ).
МРТ
МРТ часто используется в качестве инструмента для определения неоднозначных результатов при УЗИ и КТ. МРТ также часто используется у пациентов, которым противопоказана контрастная КТ из-за нарушения функции почек Ограничениями в использовании МРТ являются длительное время приобретения и несовместимость с металлическими имплантатами, такими как кардиостимуляторы.
Протоколы многопараметрической МРТ для визуализации почек включают динамические последовательности с контрастом и диффузионно-взвешенные последовательности в качестве дополнения к анатомическим изображениям, взвешенным по T1 и T2. Протокол МРТ состоит из анатомической, взвешенной по T1 и по T2 последовательности.
Папиллярный ПКК . По сравнению с светлоклеточным ПКК, папилярный хорошо очерчен и выглядит более однородным, хотя более крупные опухоли могут быть гетерогенными из-за кровоизлияния или некроза. Опухоли демонстрируют низкую интенсивность сигнала при T2-взвешенной визуализации, что соответствует преобладающей папиллярной архитектуры при патологии. По сравнению с сПКК наблюдается менее выраженная и медленная картина усиления.
ПРАВИЛЬНО ЛИ ВЫ УХАЖИВАЕТЕ ЗА УЗ-АППАРАТОМ?
Скачайте руководство по уходу прямо сейчас

Светлоклеточный ПКК . При T1-взвешенной МРТ сПКК является изоинтенсивным по сравнению с окружающей почечной паренхимой. При T2-взвешенной визуализации он является гиперинтенсивным, но гетерогенная интенсивность сигнала может присутствовать в крупных опухолях с некрозом и кровоизлиянием. Некроз кажется гомогенным гипоинтенсивным при T1-взвешенной визуализации и от умеренной до гиперинтенсивной при T2-взвешенной визуализации (рис. 7). Поскольку сПКК являются гиперваскулярными опухолями, после введения контраста наблюдается гетерогенное усиление, которое вызывает большее изменение интенсивности сигнала.
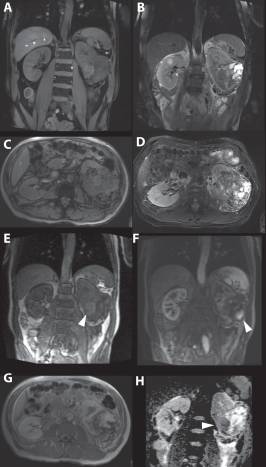
Рисунок 7 : 63-летняя женщина. Магнитно-резонансная томография показала в целом изоинтенсивную опухоль при T1-взвешенной визуализации ( A и C ) и гетерогенную, в основном, интенсивность гипертонического сигнала при T2-взвешенной визуализации ( B и D ), состоящую из смеси опухолевых и кистозных областей и областей с некрозом. Раннее усиление наблюдается в твердых частях опухоли, расположенных более в центре. ( E) В более поздней фазе твердые части периферической опухоли также сильно увеличились. ( F и G ).
Почки – жизненно важный орган, выполняющий фильтрационную и выделительную функции. Различные нарушения в работе могут приводить к тяжелым осложнениям, вплоть до смерти. Поэтому важно выявлять и лечить болезнь на начальной стадии. Для постановки диагноза используют визуальные методы исследования.
Визуальная диагностика почки что это
Под визуальной диагностикой почек понимают набор методов и процессов создания наглядного представления внутренних структур органа для анализа строения, функционирования и медицинского вмешательства.
Благодаря технике визуализации доктор может заглянуть во внутренние структуры, которые скрыты под кожей, жировой прослойкой, костями. Это значительно упрощает и ускоряет диагностику.
Медицинская визуализация позволяет создать базу данных нормальной физиологии и анатомии, чтобы потом индентифицировать аномалии. Визуализацию почки выполняют по определенным медицинским показаниям.
Виды и методы исследований
Сегодня для визуальной диагностики почки медики применяют большое количество инструментальных методов:
- Ультразвуковую диагностику (УЗИ)
- Рентген.
- Радиоизотопное сканирование с контрастным содержимым.
- Радионуклидное исследование.
- Урографию.
- Компьютерную томографию (КТ)
- Магнитно-резонансную томографию (МРТ).
На УЗИ видны размеры, структура, форма почек. Такой метод обследования позволяет выявить врожденные аномалии строения, кистозность, конгломераты, новообразования доброкачественного либо злокачественного характера, хронические патологии.
Ультразвуковое исследование абсолютно безопасно и не требует от пациента дополнительной подготовки. Но УЗИ не дает возможность выявить динамику болезни, скрытые аномалии. Поэтому на 100% верными результаты ультразвукового исследования считать нельзя.

Для уточнения диагноза доктор иногда назначает рентген. Без контрастного вещества изображение получается смазанным, но позволяет увидеть некоторые особенности протекания заболевания. Введение контраста делает клиническую картину максимально полной.
Специалист видит размеры, положение почек, наличие образований, изменений. Процедуру проводят натощак, после полного опорожнения кишечника и мочевика. Рентгенологические снимки не всегда выходят информативными. Поскольку изображения делаются в одной либо двух проекциях.
Во время диагностики человек получает определенную дозу излучения.

Радиоизотопная диагностика бывает таких видов:
- Реноангиография.
- Статическая сцинтиграфия.
- Динамическая сцинтиграфия.
Процедура дает доктору возможность быстро и легко определить функционирование почек, наличие опухолей и деструктивных очагов. Статическая сцинтиграфия показывает форму органа, его расположение, повреждение чашечек и лоханок.
Динамическая сцинтиграфия предполагает введение контраста. Она дополнительно показывает ток крови по сосудам. Перед обследованием пациенту вводят контрастное вещество, которое выводится из организма вместе с уриной. Результаты фиксируются на датчиках и служат основой для постановки верного диагноза.
Томография выявляет патологические изменения в лоханочной системе при кистозных поражениях почек, наличии конкрементов и опухолевых образований в органе. Бывает, что клиническая картина получается неявной. Тогда дополнительно выполняют биопсию.
Радионуклидная диагностика используется для выявления заболевания почек на ранней стадии. Применяется тогда, когда другие визуальные методы исследования не дают явной картины.
Преимуществами процедуры являются:
- Возможность повторного проведения без нанесения вреда здоровью больного,
- Простота.
- Определение суммарной работы почек и оценка функционирования органов по отдельности.
- Возможность применения в отношении пациентов, у которых имеется аллергия на контрастное содержимое.
Но для получения точного результата важна правильная установка датчика.
Урография применяется тогда, когда надо установить степень повреждения почечных артерий, оценить кровоснабжение в органах мочевыделительной сферы. Процедура предполагает введение в организм контрастного содержимого. Когда вещество распространяется по сосудам, венам и капиллярам, на мониторе визуализируются мельчайшие сосуды.

Самую полную и четкую картину состояния почек дают МРТ и КТ. Эти методы являются взаимодополняющими. Их обязательно используют при подозрении на почечную недостаточность. Обе процедуры безболезненные.
Единственное, у пациента может возникать дискомфорт из-за необходимости лежать без движения, шумового фона при работе оборудования.
КТ показывает доктору послойное строение почки. Томография применяется в том случае, если другие способы оказались неэффективными. Лучевая нагрузка при КТ в 40-50 раз выше, чем при рентгене. Поэтому часто делать такую диагностику запрещается.

МРТ считается более точным методом обследования, чем КТ. Процедура может проводиться с контрастным содержимым и без него. Она показывает размеры почек, состояние сосудов, все изменения в структуре тканей органа, выявляет новообразования, застойные процессы, степень функционирования органа, наличие почечной недостаточности, очаги воспаления и другие патологические изменения.
При этом МРТ не оказывает лучевую нагрузку на человеческий организм. Поэтому этот вариант обследования безопасный и универсальный. После процедуры результат с расшифровкой и подробным описанием выдают пациенту спустя 15-20 минут.

Какой выбрать метод визуальной диагностики почек, решает доктор, основываясь на предполагаемом диагнозе. Сначала используют УЗИ, а потом (при получении недостаточных данных) назначают другие исследования.
Читайте также:

