Рфп для диагностики в онкологии
Вопрос №2. Что такое радиофармпрепарат?
Радиофармпрепарат (РФП) – это соединение, состоящее из специального вещества и радионуклида (изотопа, радионуклидной метки). Специальное вещество отвечает за то, в каком органе накопится РФП, а радионуклидная метка позволяет врачу-диагносту увидеть это накопление на изображении.
В настоящее время для производства РФП используется очень широкий спектр как специальных веществ, так и радионуклидных меток. Во всем мире самым часто используемым у онкологических больных соединением специального вещества и радионуклидной метки является 18 F-фтордезоксиглюкоза ( 18 F-ФДГ). В данном соединении 18 F выполняет функцию радионуклидной метки, ФДГ – специального вещества.
Вопрос №3. Что такое физиологическое накопление РФП?
Физиологическое накопление (гиперфиксация) РФП – это повышенное накопление РФП, определяющееся в различных органах и системах в норме.
Физиологическое накопление наблюдается при исследованиях со всеми РФП: 18 F-ФДГ, 11 С-холином, 11 С-метионином, 68 Ga-ПСМА и т.д. В зависимости от типа РФП меняется лишь местоположение физиологической гиперфиксации. Например, при ПЭТ и ПЭТ/КТ с самой часто используемой 18 F-ФДГ физиологическое накопление РФП определяется в коре головного мозга, ротоглотке, носоглотке, мышцах гортаноглотки, миокарде левого желудочка, чашечно-лоханочных системах почек, фрагментарно по ходу петель толстой кишки, мочевом пузыре.
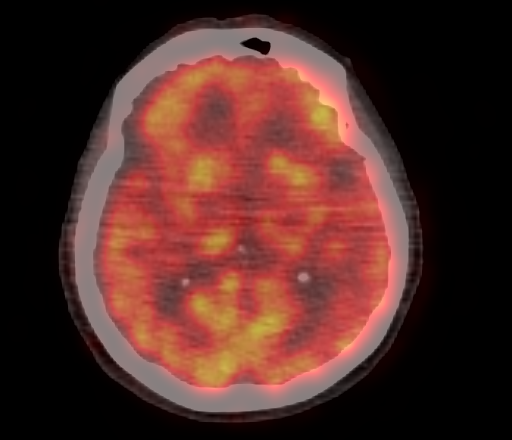 | 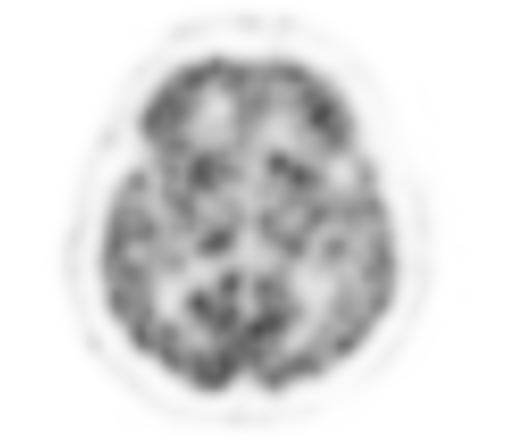 |
| Физиологическое накопление 18 F-ФДГ в коре головного мозга. | |
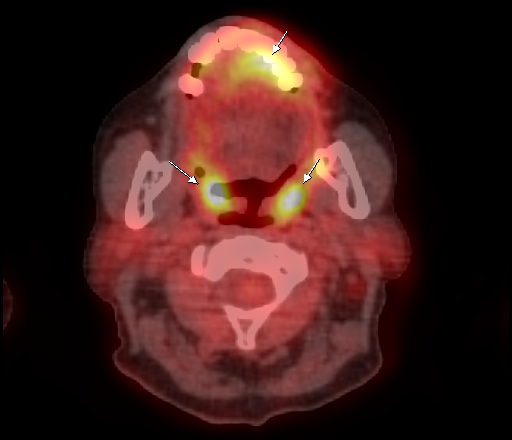 | 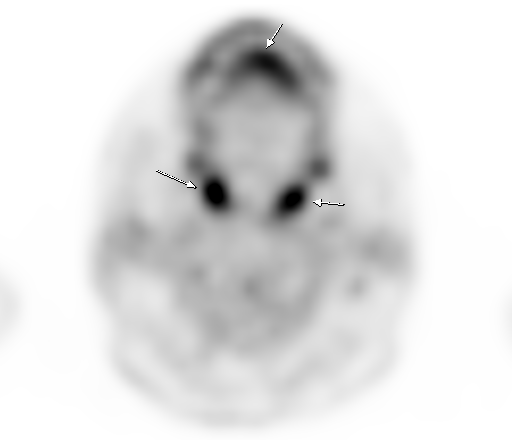 |
| Физиологическое накопление 18 F-ФДГ в ротоглотке. | |
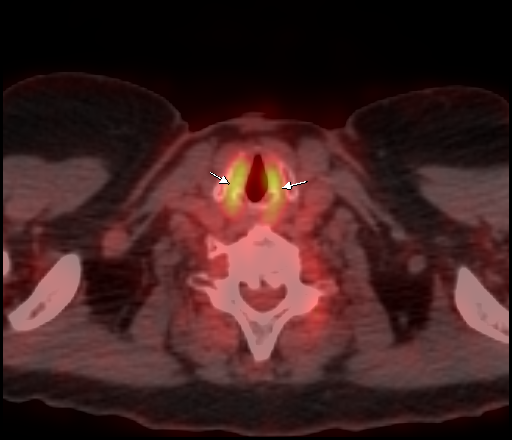 | 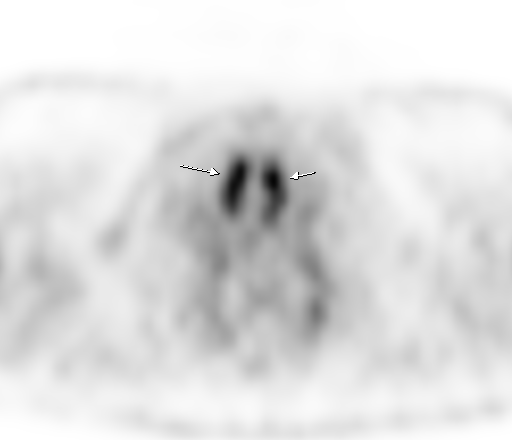 |
| Физиологическое накопление 18 F-ФДГ в мышцах гортаноглотки. | |
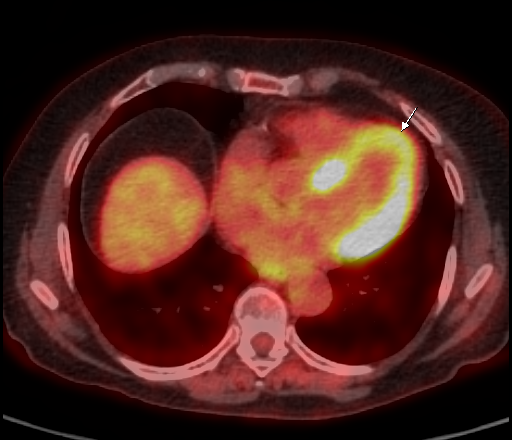 | 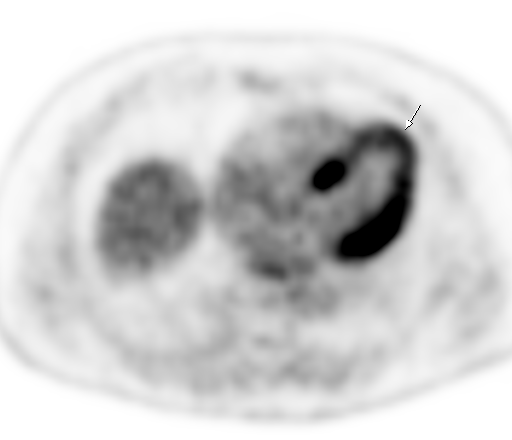 |
| Физиологическое накопление 18 F-ФДГ в миокарде левого желудочка. | |
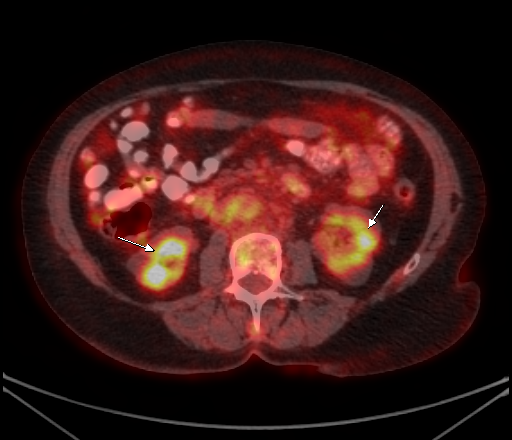 | 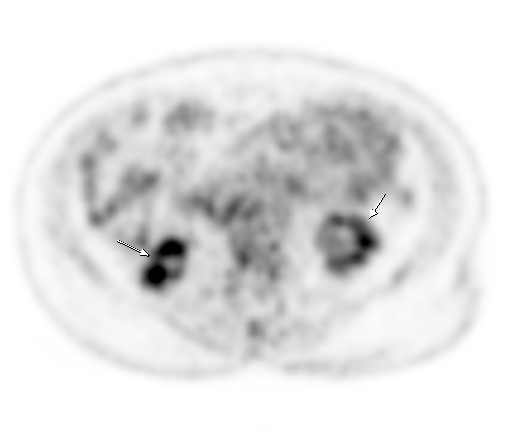 |
| Физиологическое накопление 18 F-ФДГ в чашечно-лоханочных системах почек. | |
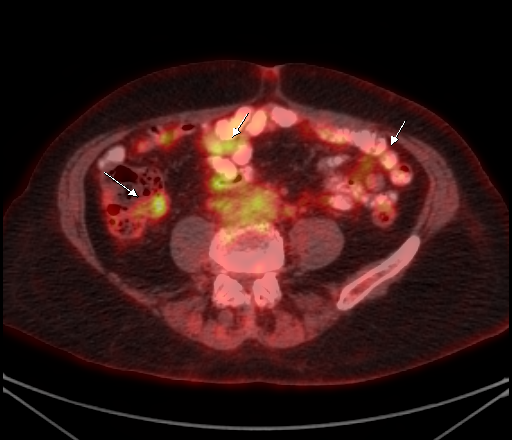 | 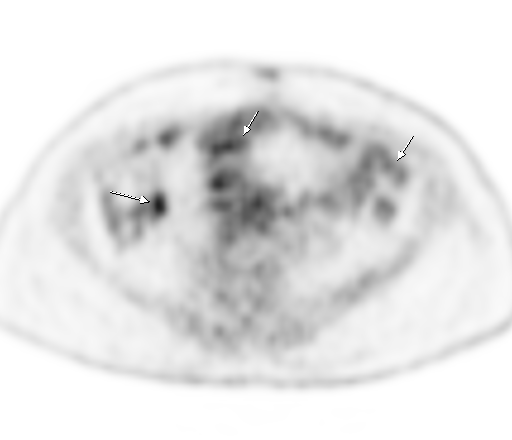 |
| Физиологическое накопление 18 F-ФДГ по ходу петель толстой кишки. | |
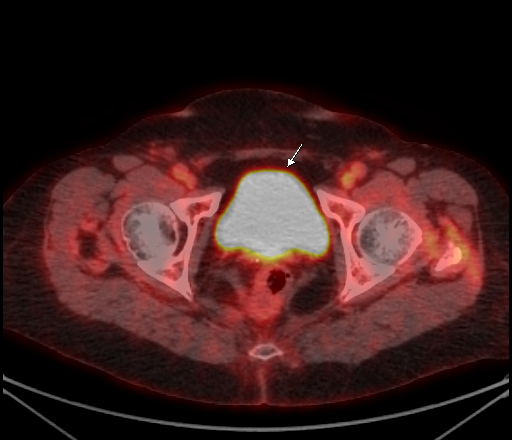 | 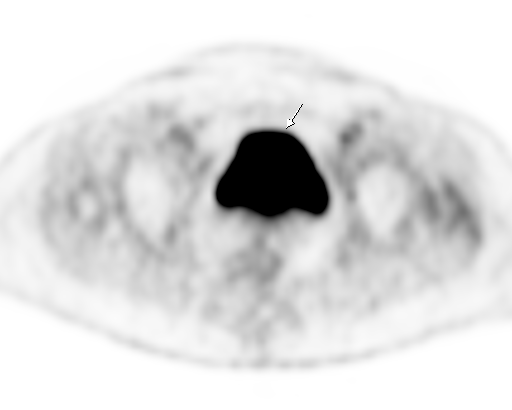 |
| Физиологическое накопление 18 F-ФДГ в мочевом пузыре. | |
Вопрос №4. Что такое патологическое накопление РФП?
Патологическое накопление РФП – это повышенное накопление РФП в органах и тканях, регистрирующееся при заболеваниях, чаще всего в злокачественных опухолях.
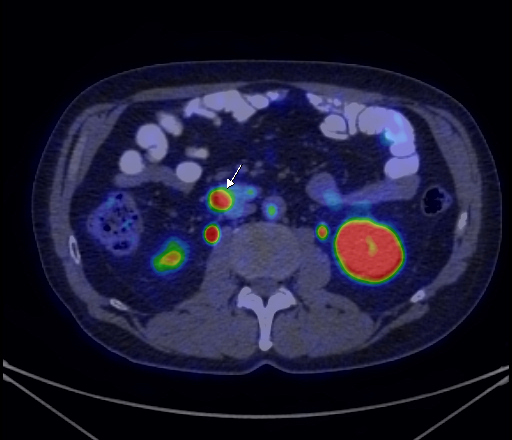 |
| Данные ПЭТ/КТ с 68 Ga-DOTA-TATE у пациента с нейроэндокринной опухолью тощей кишки. В проекции злокачественной опухоли, расположенной в тощей кишке, определяется очаг патологической гиперфиксации РФП. |
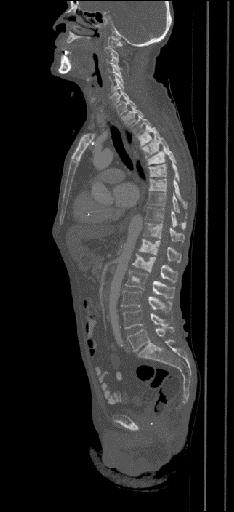 | 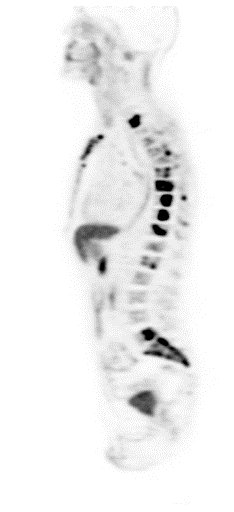 | 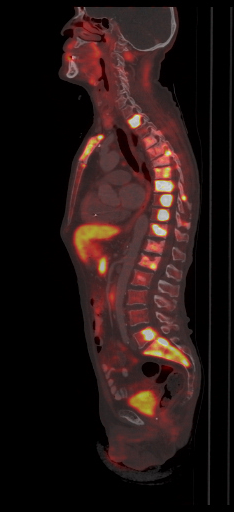 |
| Данные ПЭТ/КТ с 11 С-холином у пациента с раком предстательной железы. Состояние после простатэктомии. В костях скелета визуализируются множественные очаги патологического накопления РФП (метастазы). | ||
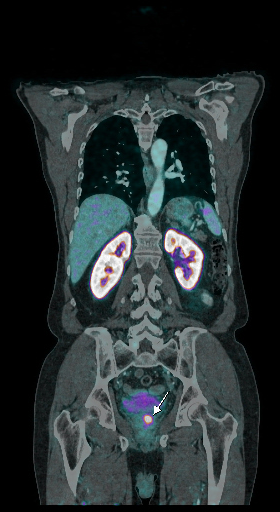 | 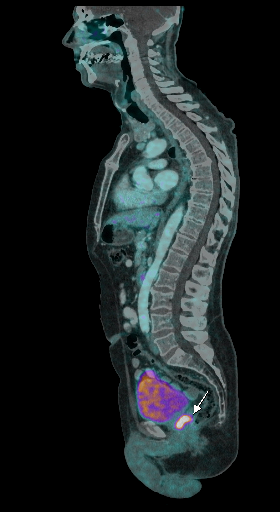 | 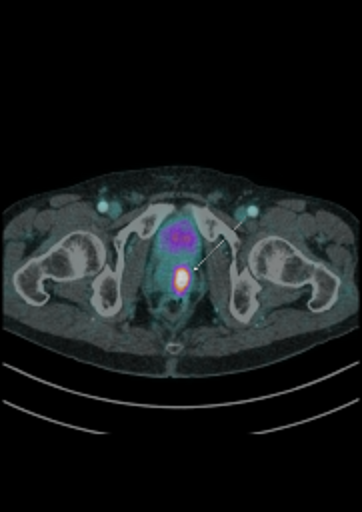 |
| Данные ПЭТ/КТ с 68 Ga-ПСМА у пациента с местным рецидивом рака предстательной железы. Состояние после лучевой терапии. В левых отделах предстательной железы определяется очаг патологического накопления РФП. | ||
Вопрос №5. Что такое метаболически активное и метаболически неактивное образование?
Метаболически неактивное образование – это образование, которое не накопило РФП. Чаще всего отсутствие повышенного накопления РФП в опухоли свидетельствует о ее доброкачественной природе.
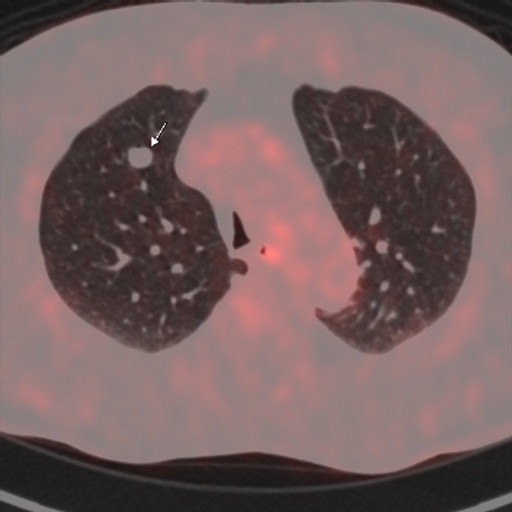 |
| Данные ПЭТ/КТ с 18 F-ФДГ у пациента с метаболически неактивным образованием правого легкого (доброкачественная опухоль - гамартома). |
Метаболически активное образование – это образование, в котором накопился РФП в повышенном количестве. Повышенное накопление РФП в опухоли чаще всего свидетельствует о ее злокачественном характере.
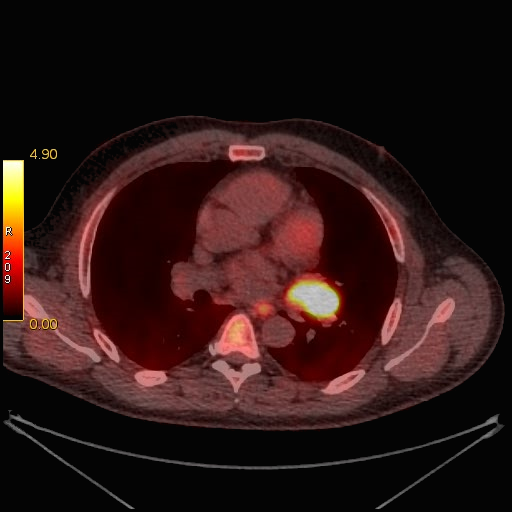 |
| Данные ПЭТ/КТ с 11 С-метионином у больного с метаболически активным образованием корня левого легкого (типичный карциноид). |
Вопрос №6. Что такое SUV?
SUV (Standardized Uptake Value, стандартизированный уровень захвата) – это величина, отражающая интенсивность накопления РФП в зоне интереса, например, в опухоли.
Показатель SUV рассчитывается программным комплексом автоматически и измеряется в различных единицах. В нашем Центре, как и в большинстве отечественных и зарубежных медицинских учреждений, где проводится позитронная эмиссионная томография, в качестве единиц измерения показателя SUV принято использовать г/мл (g/ml).
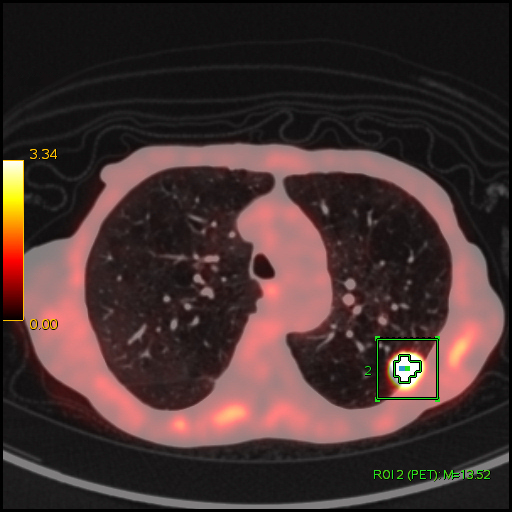 |
| Данные ПЭТ/КТ с 18 F-ФДГ. Оконтуривание метаболически активной злокачественной опухоли левого легкого для измерения показателя SUV. В данном случае величина SUV в опухоли определяется на уровне 13,52 g/ml. |
Вопрос №7. Для чего используется величина SUV?
Величина SUV в основном используется для оценки ответа злокачественной опухоли на проведенное лечение. Важно подчеркнуть, что в ряде клинических ситуаций показатель SUV в опухоли является единственным критерием, позволяющим оперативно получить информацию о чувствительности образования к только что начатой терапии.
Если опухоль чувствительна к лечению, то уровень SUV в ней при повторном ПЭТ-исследовании будет снижаться, если нечувствительна или малочувствительна (резистентна, устойчива) – значение SUV останется без изменений или увеличится. Следует помнить, что своевременная диагностика устойчивости опухоли к лечению позволит скорректировать план лечения, а в некоторых случаях и радикально его изменить.
Как уже было сказано выше, для оценки эффективности терапии врач-радиолог оценивает динамику показателя SUV до и после лечения.
Существует четыре варианта метаболического ответа опухоли на проведенное лечение:
- Частичный метаболический ответ – устанавливается при уменьшении значения SUV в опухоли на 25% и более;
- Полный метаболический ответ – заключается в отсутствии повышенного накопления РФП в опухоли;
- Метаболическое прогрессирование – устанавливается при увеличении SUV на 25% и более и/или при появлении новых очагов патологической гиперфиксации РФП;
- Метаболическая стабилизация – регистрируется при отсутствии достоверных (менее 25%) изменений показателя SUV в опухоли.
 |  |  |
| а | б | в |
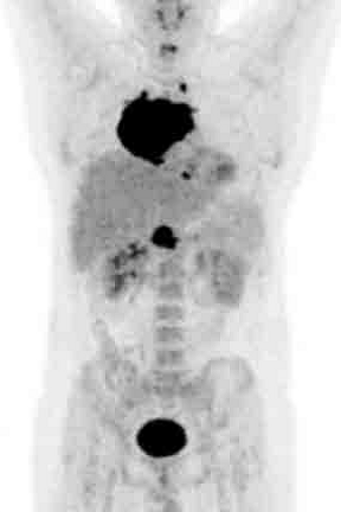
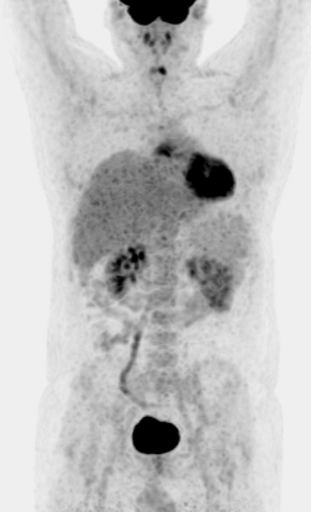
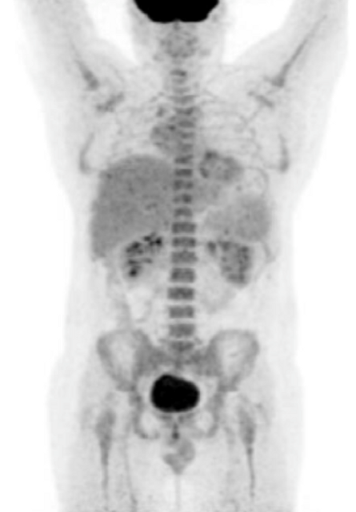
Результаты ПЭТ с 18 F-ФДГ у пациента с диффузной В-клеточной крупноклеточной лимфомой до лечения (а), после 2 курса ПХТ (б) и через 13 месяцев после окончания терапии (в).
а – до лечения в средостении визуализируется массивное метаболически активное образование с уровнем SUV=12,6;
б – после 4 курса ПХТ отмечается значительное уменьшение метаболического объема опухоли и снижение показателя SUV до 3,4 (достигнут частичный метаболический ответ, т.е. опухоль чувствительна к выбранной ПХТ);
в – через 13 месяцев после окончания ПХТ очагов патологической гиперфиксации РФП в проекции органов средостения не обнаружено (достигнут полный метаболический ответ).
В настоящее время как никогда актуальна стала ранняя диагностика заболеваний, когда еще нет симптомов заболевания, но уже есть изменения на уровне клеточного обмена веществ. Это неудивительно: чем раньше будет выявлена патология и начато лечение, тем выше вероятность выздоровления для пациента.
Что такое ПЭТ КТ обследование
ПЭТ (позитронно-эмиссионная томография) – ядерный метод обследования, который предусматривает введение в организм специальных радиоактивных веществ, испускающих позитроны (элементарные частицы с положительным зарядом). Определенные радионуклиды обычно тропны (обладают способностью избирательно накапливаться) к определенным тканям и органам. Благодаря этому можно провести прицельное обследование интересующей области человеческого тела.
КТ (компьютерная томография) благодаря использованию рентгеновских лучей позволяет получать послойные изображения исследуемой области человеческого тела. Изображение, получаемое при помощи КТ, представляет собой тени отдельных органов и анатомических образований. Интенсивность цвета области снимка, соответствующего определенному органу, зависит от способности этого органа поглощать рентгеновские лучи.
ПЭТ дает врачу информацию о состоянии обменных процессов в организме, но локализовать патологический очаг при помощи данного метода может быть затруднительно. В связи с этим в настоящее время используются комбинированные аппараты для проведения ПЭТ/КТ обследования. ПЭТ позволяет получить сведения о метаболизме тканей, а КТ применяется для локализации патологических изменений.
Что такое радиофармпрепараты (РФП)
ПЭТ КТ с холином применяется для диагностики рака предстательной железы и его метастазов. Для выявления опухолей мозга используется ПЭТ КТ с метионином, так как очень часто исследование, проведенное с использованием меченой фтордиоксидглюкозы, дает неоднозначные результаты из-за вариабельного поглощения глюкозы здоровыми клетками мозга.
До сих пор ПЭТ КТ с метионином многие специалисты рассматривают как экспериментальную методику, которая еще нуждается в исследовании и доработке, однако ряд клиник в крупных городах России уже активно применяет метод для обследования своих пациентов и определения тактики лечения выявленных заболеваний.
Изготавливаются радиофармпрепараты индивидуально для каждого пациента в специальных лабораториях, оснащенных циклотроном – прибором для получения радиоактивного изотопа. Период полураспада используемых изотопов колеблется от 2 до 109 минут. Это значит, что радиофармпрепараты не предназначены для длительного хранения, и они не могут причинить вред здоровью человека, так как быстро распадаются.
Что диагностирует ПЭТ КТ
Чаще всего метод используют для обследования пациентов с онкологическими заболеваниями. ПЭТ КТ позволяет:
- выявить первичный очаг опухоли;
- обнаружить метастазы даже в том случае, если найти первичный очаг не представляется возможным;
- определить стадию опухолевого процесса;
- оценить результаты проведенного лечения (хирургического удаления, радио- или лучевой терапии).
Также ПЭТ КТ диагностика применяется при эпилепсии, когда необходимо выявить эпилептический очаг, сосудистых заболеваниях и травмах головного мозга, деменции и заболеваниях сердца.
Подготовка к ПЭТ КТ всего тела
Для того чтобы подготовиться к исследованию, необходимо будет выполнить несколько простых рекомендаций:
- последний прием пищи вечером накануне обследования;
- в день накануне обследования необходимо исключить сладости, мучное, фрукты и овощи, оптимальные для подготовки продукты – это творог и кефир;
- пить можно чистую негазированную воду без ограничений;
- на процедуру необходимо явиться в теплой по сезону одежде без металлических застежек.
Как делают ПЭТ КТ
Следует быть готовым к тому, что основное время процедуры занимает подготовительный этап, на котором в организм пациента вводится радиофармпрепарат. Перед введением РФП пациенту предлагают занять удобное положение в кресле и выпить некоторое количество чистой воды. Желательно в это время сходить в туалет помочиться. РФП вводится внутривенно с небольшим количеством мочегонного препарата. В зависимости от вида РФП после его введения необходимо будет отдохнуть в течение 30-90 минут для того, чтобы препарат лучше распределился по тканям.
Спустя время пациента помещают на диагностическую кровать на 20-40 минут. Именно столько времени может понадобиться сканеру для того, чтобы собрать необходимую информацию.
После того, как сканирование будет закончено, пациенту разрешают встать с кушетки и отправляют его в комнату отдыха.
Расшифровка полученных результатов
ПЭТ КТ исследование позволяет получить снимки исследуемой области. Расшифровкой полученных данных занимается врач лучевой диагностики. По времени расшифровка может занять от 30 до 60 минут. По истечении этого времени пациент получает на руки снимки и заключение врача.
Первое применение радиоактивных индикаторов относят к 1911 году и связывают с именем Дьердя де Хевеши. Молодой ученый, живший в дешевом пансионе, начал подозревать, что остатки пищи, которые он не доел, подавали ему вновь на следующий день.
Первое применение радиоактивных индикаторов относят к 1911 году и связывают с именем Дьердя де Хевеши. Молодой ученый, живший в дешевом пансионе, начал подозревать, что остатки пищи, которые он не доел, подавали ему вновь на следующий день. Он добавил радиоизотопный индикатор к несъеденной порции и с помощью детектора излучения доказал своей хозяйке, что дело обстояло именно так. Хозяйка выгнала молодого ученого из пансиона. Он же продолжал начатую работу, результатом которой стала Нобелевская премия за использование радионуклидов в качестве индикаторов в биологии Радионуклидная (радиоизотопная) диагностика охватывает все виды применения открытых радиоактивных веществ в диагностических и лечебных целях.
Сканирование и сцинтиграфия — это различные методы радиоизотопной визуализации. Сцинтиграфия существенно превосходит сканирование по объему и точности диагностической информации. Современные сцинтилляционные камеры представляют собой компьютеро-сцинтиграфические комплексы, позволяющие получать, хранить и обрабатывать изображения отдельного органа и всего тела в широком диапазоне сцинтиграфических режимов: статическом и динамическом, планарном и томографическом. Независимо от типа получаемого изображения оно всегда отражает специфическую функцию исследуемого органа. По сути, это картирование функционирующей ткани. Именно в функциональном аспекте заключается принципиальная отличительная особенность сцинтиграфии от других методов визуализации. Попытка взглянуть на результаты сцинтиграфии с анатомических или морфологических позиций — еще один ложный стереотип, влияющий на предполагаемую результативность метода.
Диагностическая направленность радиоизотопного исследования определяется используемым радиофармацевтическим препаратом (РФП). Что же такое РФП? Радиофармацевтический препарат — это химическое соединение с известными фармакологическими и фармакокинетическими характеристиками. От обычных фармацевтических средств он отличается не только радиоактивностью, но и еще одной важной особенностью — количество основного вещества настолько мало, что при введении в организм не вызывает побочных фармакологических эффектов (например, аллергических). Специфичность РФП по отношению к определенным морфофункциональным структурам определяет его органотропность. Понимание механизмов локализации РФП служит основой для адекватной интерпретации радионуклидных исследований. Введение РФП связано с небольшой дозой облучения, неспособной вызвать какие-либо неблагоприятные специфические эффекты. В этом случае принято говорить об опасности переоблучения, однако при этом не учитываются темпы развития современной радиофармацевтики.
Визуализация костной системы (остеосцинтиграфия) — наиболее точный метод выявления участков нарушенного костного метаболизма. Остеотропные РФП (Тс-фосфонаты) обладают высоким сродством к кристаллам фосфата кальция, поэтому они связываются преимущественно с минеральным компонентом костной ткани. Уровень накопления РФП в различных типах костей и участках скелета обусловлен степенью остеобластической и метаболической активности, величиной кровотока, что необходимо учитывать при дифференциации нормального и патологического накопления РФП. В частности, повышенное накопление РФП наблюдается в метаэпифизарных отделах трубчатых костей, в областях с постоянной физической нагрузкой.
Заболевания костей сопровождаются патологической перестройкой костной ткани, реактивным или опухолевым костеобразованием — основными механизмами, обусловливающими изменение костного метаболизма и накопление остеотропных РФП в пораженных отделах. В зависимости от сочетания указанных процессов возрастает уровень накопления остеотропных РФП при опухолевых, воспалительных, дегенеративных, травматических заболеваниях.
Основная и наиболее ответственная задача остеосцинтиграфии — поиск метастатических и оценка распространенности опухолевых поражений скелета. Сцинтиграфическая манифестация патологии может проявиться на 3-12 месяцев раньше, чем появятся рентгенологические признаки. Связано это с тем, что локальное изменение обмена остеотропных РФП возникает на ранних фазах развития патологии, еще до появления не только рентгенологической, но и клинической симптоматики. По этой причине радионуклидное исследование обладает наибольшей эффективностью в до- и послеоперационном обследовании больных опухолями с высокой частотой метастазирования в кости (молочная железа, легкие, предстательная железа, почки).
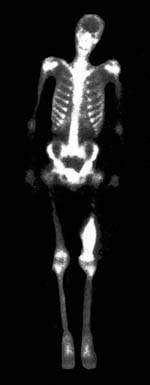 |
| Рисунок 1. Остеогенная саркома бедра. Обширная область высокого накопления РФП в дистальном отделе левого бедра |
При различных клинических ситуациях может меняться как форма кривых, так и их количественные характеристики. Следует, однако, подчеркнуть, что характер и величины изменений малоспецифичны для конкретной патологии и прежде всего отражают тяжесть патологического процесса. Наибольшая информативность реносцинтиграфии проявляется при дифференциации одно- или двустороннего поражения почек.
Ведущий признак, определяющий сторону поражения, — асимметрия амплитудно-временных характеристик ангионефросцинтиграмм. Асимметрия сосудистых параметров, и прежде всего выраженная разница времени поступления РФП в почечные артерии, — один из критериев стеноза почечной артерии. Симметричность изменений паренхиматозной функции более характерна, в частности, для гломерулонефрита; асимметрия — довольно постоянный признак пиелонефрита не только при одно-, но и при двустороннем процессе. Аналогичные изменения могут сопровождать различные варианты аномалий почек и верхних мочевых путей (нефроптоз, удвоение собирательной системы, гидронефроз).
В основе метода визуализации печени (гепатосцинтиграфии) лежит использование меченых коллоидов, которые после внутривенного введения фагоцитируются и распределяются в морфофункциональных структурах, содержащих клетки РЭС в соответствии с локальными значениями органного кровотока. В норме в печени локализуется более 90%, в селезенке — около 5%, а в костном мозге — менее 1% введенного радиоколлоида. В зависимости от характера и тяжести патологии эти соотношения меняются. Наиболее общим показанием к гепатосцинтиграфии является гепато- и/или спленомегалия неясного генеза. Основная задача исследования — дифференциация характера и уточнение тяжести поражения печени.
Диффузные заболевания печени манифестируются изменением размера и формы изображения, распределения радиоколлоида в печени и его внеорганного накопления, параметров фагоцитарной способности РЭС и печеночного кровотока. Следует подчеркнуть, что исследование не позволяет дифференцировать клинические или клинико-морфологические формы заболевания печени (например, хронический гепатит). Наибольшая информативность метода проявляется в возможности выявления синдрома портальной гипертензии (СПГ).
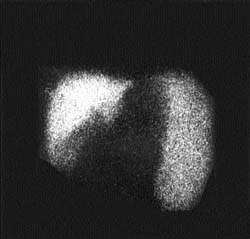 |
| Рисунок 2. Внепеченочная блокада портального кровообращения. Синдром портальной гипертензии манифестируется высоким захватом радиоколлоида увеличенной селезенкой |
Возможность выявления очаговой патологии зависит и от разрешающей способности гамма-камеры. Очаги менее 1 см, как правило, сцинтиграфически не манифестируются.
Визуализация желчевыделительной системы (гепатохолесцинтиграфия) основана на использовании серии гепатотропных РФП, аналогичных по своей фармакокинетике красителям (бромсульфалеин, вофавердин). После внутривенного введения они связываются с белками крови, поглощаются полигональными клетками печени и выводятся в составе желчи. Основным преимуществом гепатохолесцинтиграфии является непрерывность визуальной и количественной регистрации процесса кинетики РФП.
Визуальный анализ серии изображений позволяет выявить некоторые органические изменения желчных протоков (расширение), желчного пузыря (деформации), а также функциональные изменения двенадцатиперстной кишки.
Анализ кривых позволяет получить количественные критерии, характеризующие поглотительно-выделительную функцию печени, наполнение желчного пузыря, длительность латентного периода после желчегонного завтрака, скорость опорожнения желчного пузыря. Дискинезии желчного пузыря дифференцируются на основе изменения скорости его опорожнения (гипо- или гипермоторная дискинезия). Следует подчеркнуть, что точность радиологической оценки двигательной функции желчного пузыря превышает рентгенологическую или эхографическую. Это связано с тем, что при сравнении площадей изображения органа до и через фиксированное время после желчегонного завтрака практически невозможно учесть длительность латентного периода желчеотделения и выделить собственно фазу опорожнения желчного пузыря.
Визуализация щитовидной железы (тиреосцинтиграфия) проводится с использованием Тс-пертехнетата и основывается на сходстве в поведении ионов йода и пертехнетата. Однако это сходство прослеживается только на начальной неорганической фазе внутритиреоидного транспорта. Пертехнетат, в отличие от йода, не переходит в органическую фазу, то есть не включается в состав тиреоидных гормонов. Эта особенность исключает возможность его использования при послеоперационном поиске метастазов рака щитовидной железы (последнее проводится только с радиоактивным йодом).
ПЭТ/КТ (позитронно-эмиссионная томография — компьютерная томография) — это метод диагностики заболеваний, при котором совмещается исследование структуры и функциональных особенностей тканей. Наиболее востребована эта технология в онкологии для диагностики и определения степени распространения злокачественных новообразований.
- Описание технологии ПЭТ/КТ
- Преимущества и недостатки ПЭТ
- Виды препаратов для проведения ПЭТ
- Когда показано проведение ПЭТ/КТ
- Противопоказания к ПЭТ/КТ
- Подготовка к ПЭТ
- Прохождение диагностики ПЭТ/КТ
- Осложнения и побочные эффекты ПЭТ/КТ
- Лучевая нагрузка на пациента при ПЭТ-сканировании
Описание технологии ПЭТ/КТ
В основе технологии ПЭТ лежит исследование как структурных, так и функциональных особенностей тканей. Функция тканей оценивается благодаря обмену веществ. Например, выбирается универсальное вещество, которое необходимо всем клеткам организма. Его маркируют радиоактивной меткой, вводят в организм и наблюдают места его максимального накопления.
Одним из самых универсальных веществ в человеческом организме является глюкоза. Она необходима для питания практически всех клеток и тканей. Но наибольшее ее потребление идет в злокачественных новообразованиях, поскольку на рост и размножение опухоли тратится очень много энергии.
При проведении ПЭТ/КТ исследования глюкозу маркируют радиоактивными атомами с коротким периодом полураспада, например, фтором-18. И после введения в организм она в больших количествах накапливается в тканях с наиболее интенсивным метаболизмом, т. е. в злокачественных новообразованиях.
Радиоактивная метка подвергается распаду, излучая энергию в виде гамма-лучей. Излучение регистрируется прибором, и на основании полученных данных строится визуальная модель, которая показывает место локализации опухоли, ее размеры и метастазы.
Радиоактивные метки накапливаются только патологическими клетками, в то время, как здоровые ткани не визуализируются. Когда доктор хочет видеть и здоровые, и измененные структуры, выполняется компьютерная томография. Она позволяет получить детальное изображение с точностью до миллиметра.
После получения данных от обеих сканирующих систем, программное обеспечение накладывает их друг на друга, выстраивая изображение, которое дает врачу четкое представление о том, где локализуются патологические очаги.
Преимущества и недостатки ПЭТ
- Возможность совмещения в одном исследовании нескольких видов диагностики, что позволяет получить данные высокой точности.
- Исследование безболезненно, не вызывает дискомфорта.
- Возможность диагностики рака на ранней, досимптомной стадии.
- Возможность исследования сразу всех органов.
- Процедура проводится амбулаторно и не требует госпитализации в стационар.
К недостаткам метода относят необходимость применения радиоактивных препаратов. Чтобы уменьшить риски, исследование проводится в строгом соответствии с нормами радиационной безопасности.
В целом побочные эффекты от ПЭТ несоизмеримы с тем, какую ценную информацию дает такой метод исследования. В данном случае действуют три правила:
- Исследование должно быть обосновано. Польза от диагностики должна превышать вред от облучения.
- Оптимизация. Медперсонал обязан принимать все меры, которые позволят минимизировать лучевую нагрузку на организм.
- Нормирование. Должны жестко соблюдаться все нормы и правила радиационной безопасности.

Виды препаратов для проведения ПЭТ
Потенциал ПЭТ исследований определяется арсеналом используемых радиофармпрепаратов — фармацевтических препаратов, которые помечены нестабильными изотопами, делающими эти вещества радиоактивными.
В настоящее время в ПЭТ исследовании широко используются изотопы следующих элементов:
- углерод-11;
- азот-13;
- кислород-15;
- фтор-18.
В онкологической практике наибольшее распространение получил фтор, поскольку он имеет наибольший период полураспада при наименьшей энергии излучения. Это, во-первых, позволяет получить изображения высокого качества и пространственного разрешения. А во-вторых, относительно большой период полураспада (109,8 мин) дает возможность транспортировки препарата от места производства до центров сканирования.
Самым распространенным РФП в онкологии является фтордезоксиглюкоза ФДГ. Это аналог глюкозы, которая является универсальным веществом, поглощаемым всеми клетками организма. Раковые клетки поглощают его быстрее, поэтому накапливают препарат в большей дозировке, что хорошо видно при сканировании. Недостатком этого вещества является то, что он в несколько большем количестве накапливается в тканях мозга и нефронах, что может вызывать подсвечивание этих органов даже при нормальном состоянии. Поэтому встает вопрос о поиске других, более специфичных РФП.
Для головного мозга таким препаратом является 18F-FET. В его состав входит аминокислота тирозин, меченая изотопом фтора-18. Тирозин имеет очень высокую избирательную накопительность в мозговой ткани, что применяется для визуализации нейроопухолей. Помимо этого, 18F-FET используется для диагностики опухолей ротоглотки, при поисках метастазов и для диагностики поражения лимфоузлов шеи.
Кроме того, существует ряд специфичных радиофармпрепаратов для диагностики отдельных опухолей:
- 68GaPSMA — применяется при диагностике рака предстательной железы.
- 68Ga-DOTA-TATE, -NOC, TOC, -LAN и др. используются для диагностики нейроэндокринных опухолей.
- 18 FCH — используется для диагностики гепатоцеллюлярной карциномы.
Когда показано проведение ПЭТ/КТ
Противопоказания к ПЭТ/КТ
Выделяют абсолютные и относительные противопоказания к проведению ПЭТ/КТ. К абсолютным относят следующие состояния:
- Беременность. Исследование не проводится при установленном диагнозе, и в случае, когда женщина предполагает ее наличие.
- Кормление грудью. Рекомендуется прекратить кормление грудью за 6 часов до предполагаемого исследования. Сроки возобновления кормления определяются используемым трейсером.
Относительным противопоказанием к исследованию является декомпенсированный сахарный диабет при планировании использования в качестве радиофармпрепарата фтордезоксиглюкозы (ФДГ). В этом случае требуется консультация эндокринолога и стабилизация уровня глюкозы в крови ниже 7,7 ммоль/л.
С осторожностью исследование проводят при нарушении функции почек, поскольку здесь может быть искажение получаемых данных за счет задержки радиофармпрепарата в тканях.
Подготовка к ПЭТ
За день до назначенной даты исследования необходимо исключить физические нагрузки. Если предполагается применение ФДГ также нужно отказаться от продуктов, богатых углеводами. Сюда относят не только сладости и сладкие напитки, но и фрукты, овощи, хлебобулочные изделия, бобовые и пр. В день процедуры категорически запрещается есть. Пить можно только чистую воду.
Пациент должен прибыть в клинику в удобной одежде. Желательно, чтобы она не содержала металлической фурнитуры и украшений (молнии, кнопки, пуговицы, застежки и др.). Но при необходимости персонал может выдать одноразовый халат.
Если пациент страдает сахарным диабетом, перед исследованием следует измерить уровень глюкозы. Если он выше 7 ммоль/л, необходимо принять инсулин в половинной дозе. Минимальное время между инъекцией инсулина и введением РФП составляет 5 часов. Если пациент принимает таблетированные препараты для снижения уровня глюкозы, необходимо обсудить с эндокринологом возможность их отмены на день исследования.
Прохождение диагностики ПЭТ/КТ
Пациент должен явиться в клинику строго к назначенному времени. При этом необходимо взять все медицинские документы, которые представляют интерес в рамках заболевания — данные предыдущих КТ, данные гистологии, лабораторных анализов, выписка о проведенном лечении, а также данные о сопутствующей патологии, которая может повлиять на результаты диагностики (сахарный диабет, заболевания почек).
После оформления документов пациента проводят в процедурный кабинет. Там ему берут анализ крови на глюкозу и измеряют антропометрические данные. Если все в порядке, пациента проводят в комнату для релаксации. Там он удобно располагается, и ему устанавливают периферический внутривенный катетер, через который вводится РФП. Чтобы он равномерно распределился, необходимо каждые 15 минут выпивать стакан воды (либо контрастного препарата, который предложит медсестра). После введения РФП необходимо находиться в расслабленном состоянии и не разговаривать. Любая физическая активность может привести к неравномерному распределению трейсера и искажению результатов.
Через 60–90 минут пациента приглашают на сканирование. Сначала проводят компьютерную томографию, а потом ПЭТ. КТ длится считанные минуты, а ПЭТ-сканирование занимает до получаса. При этом важно лежать неподвижно, чтобы не спровоцировать образование на снимках артефактов, которые могут искажать изображение. Оба исследования проводятся в одном томографе и не вызывают болевых ощущений. После того как процедура завершится, пациент должен еще в течение часа находиться в клинике, поскольку может понадобиться повторное сканирование для уточнения данных.
После ПЭТ-исследования пациент в течение 24 часов не должен находиться в местах скопления людей, контактировать с детьми и беременными. В семейном кругу следует держаться на расстоянии не менее 1 м друг от друга. Такие ограничения действуют 24 часа после введения радиофармпрепарата.
Кроме того, в этот период необходимо принимать достаточное количество жидкости, не менее 2,5 л. Это поможет быстрее и безопаснее вывести контраст и радиофармпрепарат. Пить можно не только воду. Можно употреблять любые бескофеиновые продукты — соки, газированную воду, морсы, минеральную воду и др.
Осложнения и побочные эффекты ПЭТ/КТ
Осложнения при проведении ПЭТ/КТ в основном связаны с введением контраста для КТ. Как правило это аллергические реакции и осложнения, связанные с пунктированием вены — повреждение сосудов, гематома, боль, неврит и др. Крайне редко возникает нарушение функции почек. При пероральном употреблении контраста возможно чувство тошноты, рвота и диарея.
После ПЭТ может возникнуть головокружение и слабость из-за необходимости проведения исследования натощак. Поэтому рекомендуется захватить с собой перекус, который можно будет съесть после того, как все процедуры, связанные с исследованием, закончатся.
Лучевая нагрузка на пациента при ПЭТ-сканировании
Лучевая нагрузка при ПЭТ/КТ зависит от используемого радиофармпрепарата и объема исследования. Например, при сканировании головы облучение будет меньше, чем при исследовании всего тела. Чтобы максимально снизить вред от ПЭТ/КТ, используются следующие стандарты:
- Исследование выполняется с помощью ультракороткоживущих изотопов, время полураспада которых составляет несколько минут или часов.
- Используется индивидуальный расчет дозы для каждого пациента с учетом веса, роста и возраста.
- На сканерах используются специальные фильтры и программы, которые снижают дозы рентгеновского излучения.
- Применение необходимого количества жидкости не только улучшает качество получаемого изображения, но и помогает быстрее вывести радиофармпрепарат.
Читайте также:

