Лучевая диагностика при раке печени
Рак печени – это группа злокачественных опухолей, развивающихся из клеток или стромы органа. Наиболее частой разновидностью является гепатоцеллюлярная карцинома. По данным ВОЗ, это заболевание включено в число самых распространенных причин смертности. Рак развивается на фоне цирроза, вирусного гепатита, алкоголизма, токсического воздействия некоторых веществ. Мужчины страдают чаще женщин в четыре раза. Несмотря на высокотехнологичные методы лечения, пятилетняя выживаемость при гепатоцеллюлярной карциноме не превышает 30%.
Основные методы диагностики
Диагностика при раке печени складывается из объективного осмотра, характера развития заболевания, результатов инструментальных и лабораторных методов обследования.
Гепатоцеллюлярная карцинома развивается очень быстро. Поначалу она характеризуется неспецифическими проявлениями – боли в верхней половине живота, длительное повышение температуры, потеря аппетита, похудание. Типичные клинические признаки возникают позже.

Вскоре начинает увеличиваться печень, ее нижний край достигает пупка. Пальпаторно можно определить уплотнение на поверхности органа. Поздними симптомами рака являются пожелтение кожных покровов, вздутие живота, расширение вен на передней брюшной стенке. Лицо приобретает землистый оттенок, обращает на себя внимание выраженное похудание конечностей в сочетании с увеличенным животом. Часто возникают носовые кровотечения.
Выяснение динамики заболевания очень важно для постановки диагноза. При первом посещении клиники врач расспрашивает пациента о давности появления жалоб, характере их развития. Далее определяется очередность возникновения симптоматики, ее выраженность. Для обнаружения возможной причины онкозаболевания изучается наследственность, сопутствующие патологии, наличие производственных вредных факторов.
Лабораторная диагностика рака печени направлена на исследование крови, выявление специфических маркеров злокачественной опухоли.
Общий анализ крови при раке печени дает следующие отклонения от нормы:
- снижение уровня эритроцитов и/или гемоглобина – анемия разной степени выраженности;
- увеличение количества лейкоцитов, смещение лейкоцитарной формулы влево;
- зернистость эритроцитов, связанная с интоксикацией;
- значительный рост СОЭ – 50 и более мм/ч.
Данные показатели крови при раке печени неспецифичны, так как могут наблюдаться при других заболеваниях. На их основании диагноз выставить нельзя, но можно сделать вывод о наличии патологического процесса.
В общем анализе мочи изменения появляются редко, их можно наблюдать уже при далеко зашедшей онкологии:
- увеличение кетоновых тел в результате распада белка;
- появление уробилина;
- рост уровня мочевины.

Эти критерии показывают степень нарушения метаболизма из-за интоксикации.
Биохимические анализы при раке печени выявляют изменения следующих показателей:
- повышение уровня глобулинов;
- рост фибриногена;
- значительная активность щелочной фосфатазы.
Важно знать! Эти показатели также нельзя считать основными для постановки диагноза, так как они отражают только степень нарушения функции печени.
Онкомаркерами называют вещества, которые обнаруживаются в крови только при развитии злокачественных опухолей. Для гепатоцеллюлярной карциномы таковым является альфа-фетопротеин. Этот онкомаркер при раке печени представляет собой соединение белка с глюкозой, которое имеется только в организме эмбриона и плода. После рождения его количество резко снижается, практически достигая нуля.
Онкомаркеры на рак печени неспецифичны, они могут обнаруживаться и при других онкологических заболеваниях. Предположить гепатоцеллюлярную карциному можно, если уровень этого белка превышает 1000 нг/мл. Если же количество альфа-фетопротеина значительно больше этой цифры, его уже считают специфическим маркером рака печени.
Кровь для общего и биохимического анализ при раке печени забирают обычным образом. Процедура осуществляется в утренние часы, человеку рекомендуют не есть менее чем за 12 часов до исследования. За 2-3 дня до сдачи анализа придерживаются принципов здорового питания. Кровь забирается из локтевой вены, затем проводится ее лабораторное изучение.
Инструментальные методы позволяют визуально оценить внешний вид органа, определить расположение, количество и размеры новообразований. Расшифровку исследований дают врачи, проводящие их, но диагноз ставится на основании совокупности данных.
Это первичный метод, позволяющий диагностировать рак. Обнаруживается сама опухоль, ее расположение в органе, размеры. УЗИ дает оценку структурному состоянию печеночной ткани. Признаком новообразования является участок затемнения с неровными краями.
МРТ дает послойное изображение изучаемых тканей, благодаря чему можно выявить даже мельчайшую опухоль. Метод основан на способности магнитных лучей проникать в органы и отражаться от них с разной скоростью. Также используется для дифференциальной диагностики с другими заболеваниями. Позволяет отличить злокачественное новообразование от доброкачественного. С его помощью можно определить состояние сосудов внутри органа.
Показательна при достижении опухолью больших размеров. В данном случае лапароскопическая картина выглядит следующим образом:
- крупный одиночный узел, с неровной поверхностью, беловато-серого цвета, с плотной консистенцией;
- многоузловая форма рака – несколько образований разного диаметра, коричневого цвета;
![]()
- цирроз-рак – утолщенная капсула, множество мелких узелков на поверхности печени.
Также лапароскопия может выявить наличие свободной жидкости в брюшной полости – асцит.
Это метод изучения сосудов печени с помощью рентгеновского аппарата и вводимого контраста. Применяется для оценки состояния артерий, питающих новообразование, на основании чего делается вывод о возможности оперативного вмешательства.
Этот вид диагностики основан на микроскопическом изучении ткани печени. Забор кусочка органа осуществляется с помощью пункции. Берут длинную иглу с полым стержнем, прокалывают переднюю брюшную стенку, достигая печени. Процедура проводится под контролем УЗИ. Из новообразования забирают кусочек, затем готовят гистологический материал, который изучают под микроскопом.
Позитронно-эмиссионная томография относится к радионуклидным методам исследования. Анализ этот достаточно сложный и дорогой, требует специального оборудования. В вену вводится радиофармпрепарат, затем осуществляется сканирование тела на позитронном томографе. Опухолевая ткань поглощает намного больше контрастного вещества, чем здоровые гепатоциты. Поэтому при просвечивании она выглядит значительно ярче.
Для печени специфичным индикатором является только альфа-фетопротеин. Существует много других онкомаркеров, но они могут обнаруживаться при раке желудка, яичников, поджелудочной железы.
Плюсы ранней диагностики рака
Гепатоцеллюлярная карцинома – один из самых агрессивных видов рака. Срок жизни после установления диагноза исчисляется несколькими годами. Прогноз ухудшается еще и тем, что заболевание, как правило, обнаруживается на 3-4 стадии, когда уже началось распространение метастазов.
Внимание! Чем раньше обнаружена раковая опухоль, тем раньше будет начато лечение.
В данном случае возможно проведение комбинированного подхода, включая химиопрепараты, лучевую терапию, оперативное вмешательство. Ранняя помощь позволяет улучшить самочувствие пациента, максимально продлить срок его жизни.

Как правило, новообразование печени впервые обнаруживают при УЗИ, однако чувствительность метода не позволяет выявить все малые опухоли и все имеющиеся узлы. К примеру, для выявления мелких метастазов, которые могут быть наряду с первичной опухолью, разрешающих возможностей ультразвукового исследования недостаточно. В то же время УЗИ навигация помогает контролировать выполнение чрескожной биопсии, что неотъемлемо при интервенционных вмешательствах и полезно в наблюдении за течением процесса.
Для первичной диагностики рака печени УЗИ не пригодно.
Как ставят диагноз рака печени?
В стандарты диагностики рака печени включены компьютерная (КТ) и магнитно-резонансная томографии (МРТ) обязательно с контрастными веществами, выявляющие типичную для гепатоцеллюлярного рака (ГЦР) васкуляризацию (сосудистую структуру) опухоли. Кровоснабжение опухоли идёт из других сосудов, нежели остальная ткань печени. В большинстве случаев злокачественные опухоли печени возникают на фоне хронической патологии, что тоже вносит изменение в картину КТ и МРТ, но есть типичные для каждого состояния моменты выведения контрастного вещества, которые хорошо знают специалисты.
Международные рекомендации считают доказанным гепатоцеллюлярный рак при независимой фиксации изменённого кровоснабжения печени во время динамической КТ и МРТ.
В России выполнение сразу двух исследований обычно не проводят, бывает достаточно и одного, но с совершенно типичной для рака картиной васкуляризации, не оставляющей каких-либо сомнений. Это может быть на выбор КТ с контрастным усилением или МРТ, то есть любой доступный метод объективной лучевой визуализации. Исследования позволяют оценить распространение злокачественного процесса, установить его стадию, оценить состояние всей печени.
Позитронно-эмиссионная томография для первичной диагностики рака печени пока не рекомендуется.
Биопсия печени
Полученный при биопсии материал может быть малоинформативным совсем не по вине хирурга, а из-за особенностей строения и патологических изменений печени пациента, тем более при наличии цирроза или хронического гепатита.
Манипуляция малоприятна, но больше психологически, чем физически. В хороших хирургических руках осложнения довольно редки. Вероятность кровотечения из-за повреждения сосуда составляет едва ли 1-2%. Опасения распространения опухолевых клеток по пункционному каналу оправданы, но при среднем полуторагодичном наблюдении такое возможно максимально в 11% случаев.
Биопсию печени не проводят, если изменённой в результате цирроза печени во время мультифазной компьютерной томографии выявлена васкуляризация, характерная для гепатоцеллюлярного рака, и диагноз подтверждается на контрастной МРТ.
Биопсия опухоли обязательна, если:
- новообразование печени без признаков цирроза;
- опухоль больше 2 см и на КТ и МРТ нетипичная васкуляризация;
- опухоль менее 2 см с типичным для ГЦР кровотоком, выявленном любым методом объективной визуализации;
- неоднозначная трактовка исследований при отсутствии изменений альфа-фетопротеина (АФП).
Биопсия не показана:
- не предполагается лечение из-за тяжёлой сопутствующей патологии;
- не планируется лечение из-за декомпенсированного цирроза печени;
- планируется резекция печени.

Лабораторные тесты
Анализы показывают функциональные возможности печени, но не способны что-либо сообщить о наличии или отсутствии злокачественной опухоли. То есть расскажут о циррозе и гепатите, но рак на показателях не отражается.
Роль альфа-фетопротеина (АФП) в диагностике рака печени несколько преувеличена. Этот маркёр повышается при любой патологии печени (и не только печени). При выявлении небольшого гепатоцеллюлярного рака АФП повышается у пятой части больных. Но при высоких показателях в несколько сот единиц и нарушениях васкуляризации при КТ или МРТ опухоли более 2 см, конечно, сомнений в злокачественности быть не может.
Наряду с методами визуализации маркёр АФП используется для контроля эффективности лечения рака печени, поскольку увеличивается при формировании сосудов в растущей опухоли.
а) Терминология:
1. Синонимы:
• Гепатоцеллюлярная карцинома, гепатома, первичный рак печени
2. Определения:
• Злокачественное новообразование, развивающееся из гепатоцитов
б) Визуализация:
1. Общая характеристика:
• Ключевые диагностические признаки:
о Солидное, внутрипеченочное образование > 1 см у пациента с факторами риска, такими как хронический гепатит или цирроз
о Прорастание воротной вены или печеночной вены с большой долей вероятности предполагает печеночноклеточный рак
• Размер:
о От небольших до крупных: 5 см
о Диффузный или инфильтративный: от менее одного сантиметра и до > 5 см
• Основные положения:
о Наиболее распространенная первичная злокачественная опухоль внутренних органов:
- Составляет 80-90% всех первичных злокачественных опухолей у взрослых
- Обычно развивается на фоне цирроза печени, вызванного хроническим вирусным гепатитом (HBV, HCV) или алкоголизмом
о Вторая по частоте злокачественная опухоль печени после гепатобластомы у детей
о Различный рост печеночноклеточного рака: три основных типа:
- Одиночное, часто крупное образование
- Многоузловой или многоочаговый
- Диффузный или инфильтративный
о Метастазирует в легкие, кости, надпочечники, лимфатические узлы
2. УЗИ при печеночноклеточном раке:
• Серошкальное исследование:
о Гипоэхогенный: наиболее распространенный ультрасонографический вид:
- Солидная опухоль
- Может быть окружена тонким, гипоэхогенным ободком (капсула)
о Гиперэхогенный:
- Отражение жирового перерождения/гиперваскуляризации
- Имитирует гемангиомы/очаговый стеатоз:
Если присутствуют факторы риска и обнаружен гиперэхогенный очаг > 1 см, не следует предполагать гемангиому
о Смешанная эхогенность: чаще при крупном печеночноклеточном раке:
- Из-за некроза/фиброза опухоли
- Очаговые скопления жировой ткани в некоторых случаях
о Фоновый цирроз (за исключением фиброламеллярного печеночноклеточного рака и гепатита В)
о При отсутствии лечения кальцификация встречается редко
о Прорастание воротной вены и (реже) печеночной вены с большой долей вероятности указывает на печеночноклеточный рак
о Гемоперитонеум при разрыве субкапсулярного или экзофитного образования
о Ассоциирован с симптомами портальной гипертензии: асцитом, спленомегалией, портокавальными анастомозами
о Фиброламеллярный рак:
- Встречается редко, 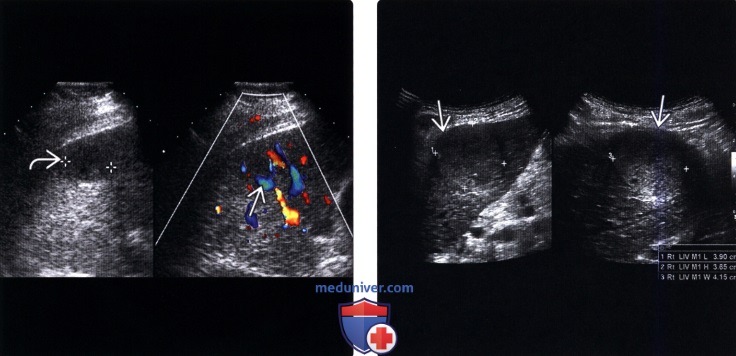
(Левый) На поперечном серошкальном ультразвуковом срезе и цветовой допплерографии печени визуализируется солидный гипоэхогенный узел печеночноклеточного рака с внутренней васкуляризацией.
(Правый) На продольном и поперечном ультразвуковом срезе левой доли печени визуализируется относительно гиперэхогенный солидный узел печеночноклеточного рака с гипоэхогенным ободком. Окружающая паренхима печени неоднородная, что указывает на цирроз. 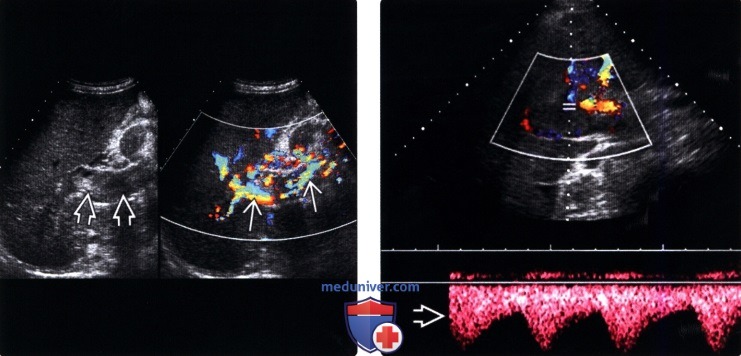
(Левый) На поперечном серошкальном ультразвуковом срезе и цветовой допплерографии воротной вены визуализируется солидный внутрипротоковый опухолевый тромб с выраженной внутренней васкуляризацией. Наличие опухолевого тромба почти всегда свидетельствует о наличии инфильтративного или распространенного печеночноклеточного рака.
(Правый) Спектрограмма сосудов в области опухолевого тромба. Отмечается артериальная форма волны, направленная от печени, отражающая артериальную неоваскуляризацию опухолевого тромба. 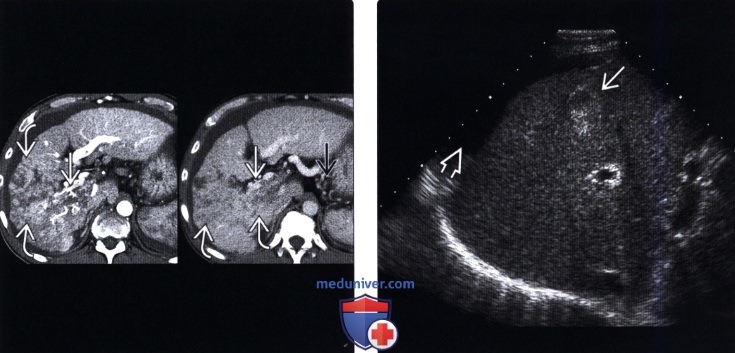
(Левый) КТ с контрастированием в позднюю артериальную фазу (слева) и отсроченную фазу (справа). Визуализируется узел инфильтративного печеночноклеточного рака в правой доле печени, отмечается опухолевый тромбоз воротной вены. Окружающая паренхима печени цирротична, также отмечается расширение вен желудка и умеренный асцит.
(Правый) Поперечный серошкальный УЗ срез печени. Визуализируется узел печеночноклеточного рака смешанной эхогенности. Окружающая паренхима печени умеренно цирротична, отмечается асцит .
6. Радионуклидная диагностика:
• Гепатобилиарное сканирование: поглощение до 50%
• Сканирование с галлием: поглощает галлий в 90% случаев
• ПЭТ/КТ с ФДГ: поглощение в 55% случаев
7. Рекомендации по визуализации:
• УЗИ: скрининг и наблюдение у пациентов с высоким риском (хронический гепатит или цирроз):
о Текущей рекомендацией Американской ассоциации по изучению заболеваний печени (AASLD) является ультразвуковой скрининг/наблюдение каждые шесть месяцев:
- При узелках 1 см выполняют КТ или МРТ с контрастированием для получения дополнительных данных
• КТ или МРТ с контрастированием: определение характера очага:
о Используйте критерии для изображений системы баз данных LI-RADS или сети OPTN
• УЗИ с контрастированием: при необходимости может использоваться для определения характера очага
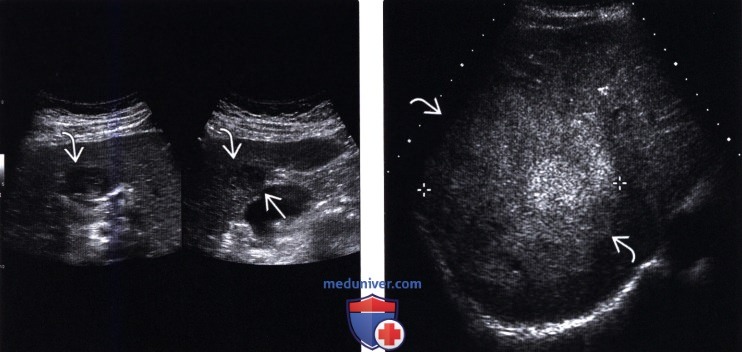
(Левый) На поперечном и продольном серошкальных ультразвуковых срезах печени визуализируется солидный неоднородный узел печеночноклеточного рака, слегка выступающий за контур печени.
(Правый) Поперечный серошкальный УЗ срез правой доли печени. Визуализируется крупный изоэхогенный солидный узел печеночноклеточного рака. 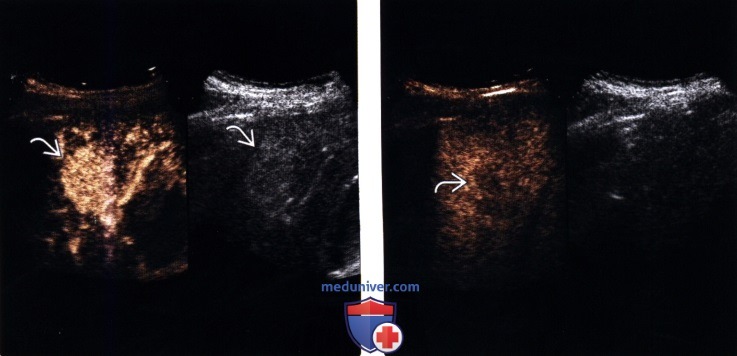
(Левый) Две ультрасонограммы исследования печени в артериальную фазу (слева - с контрастированием, справа — серошкальное). Визуализируется ги пер васкуляризированный узел печеночноклеточного рака, ярко контрастируемый на фоне окружающей паренхимы.
(Правый) УЗИ с контрастированием у этого же пациента, отсроченная фаза. В образовании отмечается повышенное вымывание контрастного вещества по сравнению с окружающей паренхимой печени, что характерно для печеночноклеточного рака. 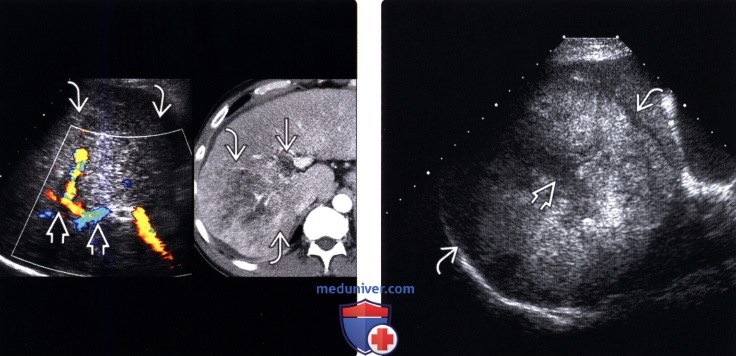
(Левый) УЗИ с цветовой допплерографией и КТ с контрастированием. Визуализируется крупный инфильтративный очаг печеночноклеточного рака. В некоторых случаях инфильтративную опухоль при УЗИ сложно обнаружить, но выраженное смещение печеночных сосудов кзади -полезный признак наличия новообразования. Опухолевый тромбоз часто наблюдается при крупных узлах инфильтративного печеночноклеточного рака.
(Правый) Поперечный серошкальный УЗ срез печени. Визуализируется крупное, преимущественно гиперэхогенное образование с толстым гипоэхогенным центральным рубцом. Установлено, что образование являлось фиброламеллярным раком.
в) Дифференциальная диагностика печеночноклеточного рака:
1. Узелки регенерации или дисплазии:
• Если 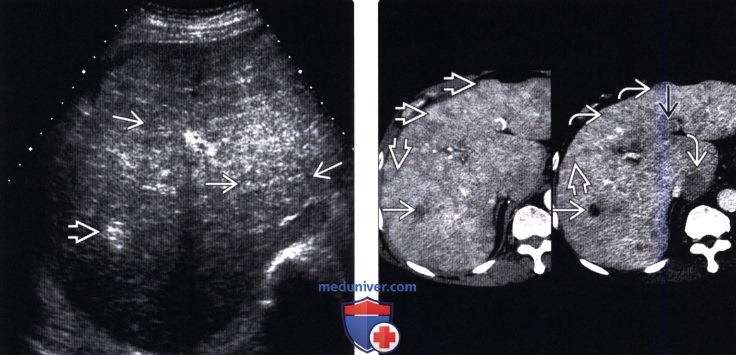
(Левый) Поперечный серошкальный УЗ срез печени. Отмечается выраженная неоднородность печени с множественными рефракционными тенями, образованными узлами диффузно-инфильтративного печеночноклеточного рака. Очаговое гиперэхогенное образование является жиросодержащим участком печеночноклеточного рака.
(Правый) КТ с контрастированием у того же пациента в артериальную фазу (слева) и в отсроченную фазу (справа), аксиллярная проекция. Визуализируются множественные очаги гиперваскуляризированного печеночноклеточного рака, вымывание очевидной. Жиросодержащий очаг печеночноклеточного рака визуализируется в правой доле печени. В левой ветви воротной вены отмечается опухолевый тромб. 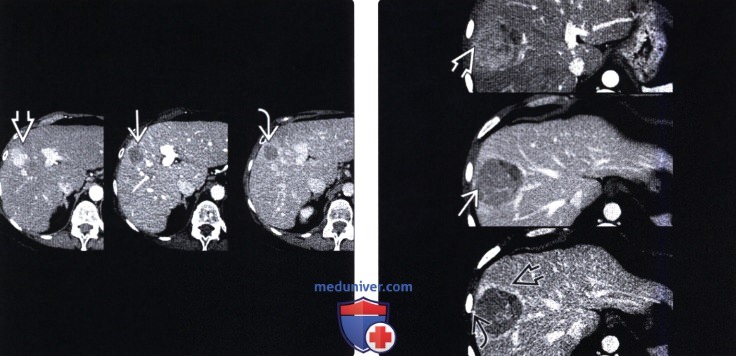
(Левый) Типичный вид узла печеночноклеточного рака при трехфазной КТ. Гиперваскуляризированный в артериальную фазу, узел печеночноклеточного рака подвержен вымыванию в портальную и отсроченную фазы контрастирования.
(Правый) КТ печени, аксиллярная проекция. Визуализируется типичный узел печеночноклеточного рака, гиперваскуляризированный в артериальную фазу и подверженный вымыванию в портальную и отсроченную фазы контрастирования. На периферии очага отмечается отсроченное контрастирование псевдокапсулы. 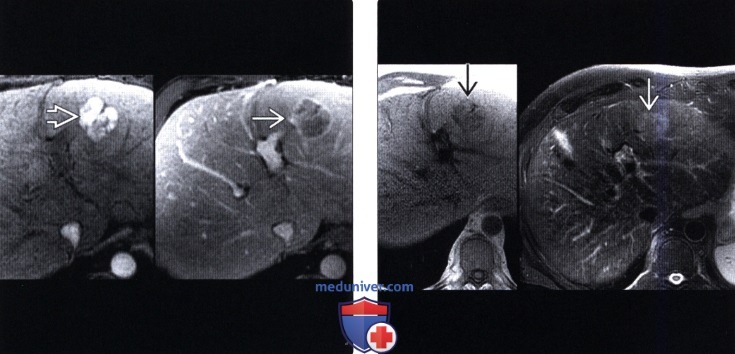
(Левый) Артериальная фаза МРТ с контрастированием, Т1 с FS; визуализируется гиперваскуляризированный узел печеночноклеточного рака, подверженный вымыванию в портальную фазу и имеющий контрастируемую псевдокапсулу.
(Справа) MPT, Т1-взвешенное изображение без контрастирования (левое изображение) у того же пациента. Отмечается типичный низкий внутренний Т1 сигнал и умеренно гиперинтенсивный Т2 сигнал (правое изображение).
г) Патология:
1. Общая характеристика:
• Этиология:
о Цирроз (60-90%): вызванный хроническими вирусными гепатитами (HBV, HCV), алкогольный, первичный билиарный:
- Пациенты с HCV как правило страдают от цирроза; у пациентов с HBV цирроз наблюдается редко
о Неалкогольный стеатогепатит (НАСГ) все чаще является причиной развития печеночноклеточного рака в Северной Америке
о Канцерогены: афлатоксины, сидероз, торотраст, андрогены
о Дефицит α-1-антитрипсина, гемохроматоз, болезнь Вильсона-Коновалова, наследственная тирозинемия
• Генетика:
о ДНК вируса гепатита В интегрируется в геном клетки-хозяина — геномная нестабильность
2. Макроскопические и хирургические особенности:
• Мягкая опухоль, образованная гепатоцитами; может содержать участки некроза, кальцификации, кровоизлияния, жировые включения, сосудистую инвазию
3. Микроскопия:
• Синусоидальные сосуды окружают клетки опухоли
• Виды архитектоники: трабекулярная (чаще всего), солидная, трубчатая (ацинарная, протоковидная, псевдожелезистая)
• Варианты печеночноклеточного рака: клеточный (может содержать жир или гликоген), фиброзный, саркомоподобный, склерозный, смешанный печеночноклеточный-холангиокарцинома
д) Клинические особенности:
1. Проявления:
• Пациент пожилого возраста с циррозом, асцитом, потерей веса, болями в правом верхнем квадранте живота и ↑ уровня α-фетопротеина (AFP) в анамнезе
• Лабораторные данные: ↑ уровня сывороточного AFP и функциональных тестов печени:
о Если при визуализации наблюдается характерная картина, диагноз может быть поставлен на основании КТ с контрастированием или МРТ; биопсию выполняют в сомнительных случаях
2. Демография:
• Возраст:
о Районы с низким уровнем заболеваемости: 6-7 декады
о Районы с высоким уровнем заболеваемости: 30-45 лет
• Пол:
о Районы с низким уровнем заболеваемости: (М:Ж = 2,5:1)
о Районы с высоким уровнем заболеваемости: (М:Ж = 8:1)
• Эпидемиология:
о Высокий уровень заболеваемости: Африка и Азия
о Печеночноклеточный рак при циррозе, вызванном вирусом гепатита С
о Печеночноклеточный рак может развиваться у 30% пациентов с HBV без цирротических изменений
3. Течение и прогноз:
• Осложнения: спонтанный разрыв и гемоперитонеум
• 30% пятилетняя выживаемость
4. Лечение печеночноклеточного рака:
• Хирургическая резекция у пациентов с адекватным резервом печеночной ткани
• Радиочастотная/алкогольная/микроволновая абляция в случае мелких, изолированных опухолей
• Трансплантация печени при наличии миланских критериев: одиночная опухоль 2-5 см или три опухоли каждая
Редактор: Искандер Милевски. Дата публикации: 2.11.2019
Среди первичных злокачественных новообразований печени наиболее часто встречается гепатоцеллюлярная карцинома, или печеночно-клеточный рак, который, как видно из названия, берет свой рост в гепатоцитах — клетках печени. Значительно реже регистрируют злокачественные опухоли, растущие из эпителия внутрипеченочных желчных протоков — холангиокарциномы, а также смешанные новообразования — гепатохолангиокарциномы.
Рак печени занимает третье место в структуре смертности от онкологических заболеваний в мире, и каждый год уносит жизни около миллиона человек. Наиболее часто патология регистрируется в возрасте 40-50 лет, при этом мужчины страдают от заболевания в 4-9 раз чаще, чем женщины.
Факторы риска
Менее 10% рака развивается в исходно здоровой печени. В остальных случаях ему предшествуют различные патологические состояния:
- цирроз печени;
- вирусные гепатиты В и С;
- алкогольная болезнь печени;
- аутоиммунное воспаление;
- токсическое повреждение, в частности афлатоксинами и винилхлоридом;
- наследственная патология, сопровождающаяся дефицитом α1- антитрипсина.
Показательно, что наиболее высока заболеваемость раком печени в регионах с высоким уровнем вирусных гепатитов. Установлено, что у носителей гепатита В гепатоцеллюлярная карцинома встречается почти в 100 раз чаще, чем у остальных пациентов.
Знание факторов риска позволяет определить группы риска для проведения скрининговых исследований. Пациентам с циррозом печени, носителям вируса гепатита В, людям с семейным анамнезом по раку печени рекомендовано регулярная ультразвуковая томография печени с определением уровня альфа-фетопротеина (АФП) в крови, повышенное содержание которого является основанием для более глубокого исследования.
Клиническая картина
Симптомы заболевания и жалобы пациента, как правило, не отличаются специфичностью, поэтому на ранних стадиях выявить рак печени можно практически исключительно в ходе скрининга. На более поздних стадиях у еще достаточно стабильных пациентов появляются:
- неопределенные боли в животе;
- потеря веса;
- ухудшение общего состояния;
- лихорадка (не всегда);
- пальпируемое образование в правом подреберье;
- асцит;
- перитонит (при кровотечении).
Следует заметить, что и в этом случае, симптомы рака практически не отличаются от симптомов тяжелого поражения печени, например, вследствие цирроза, поэтому также не могут служить основанием для постановки диагноза.
Помимо этого, у части пациентов могут развиваться различные метаболические нарушения, в частности: повышение уровня глюкозы, жиров и кальция в крови, что также иногда сопровождается соответствующими клиническими проявлениями.
Стадирование рака печени
Первичный гепатоцеллюлярный рак стадируется согласно международной системе ТNМ, где:
Т — размеры опухоли и степень ее инвазии;
N — метастазы в лимфоузлы;
М — отдаленные метастазы;
0 — отсутствие признака.
Т1 — новообразование до 2 см без инвазии в сосуды.
Т2 — опухоль менее 2 см с инвазией в сосуд, или множественные опухоли в одной доле менее 2 см без инвазии, или новообразование более 2 см без инвазии.
Т3 — более 2 см с инвазией, или множественные в одной доле менее 2 см с инвазией, или множественные одной доле размером более 2 см.
N1— метастазы в регионарных лимфоузлах.
Т4 — множественные новообразования в обеих долях, или опухоль, распространяющаяся на соседние органы или прорастающая в брюшину.
М1 — имеются отдаленные метастазы
Поскольку рак печени очень часто развивается на фоне ее цирроза, для объективной оценки состояния пациента и предполагаемой эффективности лечения применяется также BCLC, или Барселонская система стадирования, в которой присутствует 5 стадий от 0 (очень ранняя) до D (терминальная).
Диагностика рака печени
Диагностические процедуры при раке печени могут носить скрининговый и уточняющий характер. К их числу относятся:
- Исследование крови на АФП, который считается опухолевым маркером, хотя его уровень может быть повышен и при некоторых других заболеваниях печени, а также при опухолях другой локализации.
- Ультразвуковая КТ применяется как метод скрининга, а также в качестве средства навигации при проведении чрезкожной биопсии и некоторых интервенционных вмешательствах. При всех достоинствах, метод недостаточно чувствителен в отношении мелких новообразований.
- КТ и МРТ с контрастированием позволяют обнаружить типичные для гепатокарциномы изменения локального кровообращения.
Биопсия печени — надежный метод диагностики, требующий интервенционного вмешательства, которое, впрочем, при должном опыте врача достаточно безопасно. Биопсия просто необходима при небольших опухолях, в ситуациях, когда заключения, полученные иными методами, расходятся, а также при обнаружении любой опухоли в нецирротической печени. Вместе с тем биопсия может быть и не показана. Так, например, в следующих ситуациях проведение исследования нецелесообразно:
- декомпенсированный цирроз или другие тяжелые заболевания, которые делают лечение заведомо неэффективным;
- при запланированной резекции печени;
- наличие специфичной картины при проведении мультифазной КТ или МРТ.
С учетом того, что рак печени чаще всего появляется на фоне цирроза и другой патологии, требующей собственных диагностических мероприятий, в каждом случае необходима оценка выраженности фонового процесса.
Методы лечения
Лечение гепатоцеллюлярного рака — сложная задача, требующая индивидуального подхода, который учитывает наличие и степень цирроза, функциональные возможности печени, распространение опухоли. В разработке плана лечебных мероприятий принимает участие целая команда специалистов, в том числе онколога, радиолога, химиотерапевта, трансплантолога и других.
Удаление части печени
Резекция (удаление части) печени является методом выбора при раннем гепатоцеллюлярном раке. Операцию возможно провести при сохраненных функциях органа и в отсутствие портальной гипертензии. Наилучшие результаты лечения были получены у пациентов с новообразованием размерами менее 5 см.
Трансплантация
Пересадка печени показана в ситуациях, когда резекция не рекомендована, например, при множественных узлах или выраженном циррозе. При отборе пациентов для трансплантации печени используют так называемые “миланские” критерии, следуя которым удается обеспечить 5-летнюю выживаемость на уровне 70%.
Радиочастотная аблация
Метод термодеструкции, который предпочтительно применять на ранних стадиях новообразования, если невозможно выполнить резекцию и трансплантацию. Такой вариант лечения не оправдан при множественных опухолях, при большом размере узлов (более 3 см), а также у пациентов с декомпенсированным циррозом.
Трансартериальная химиоэмболизация
Введение цитостатиков в артерию, которая питает опухоль. Метод используется в паллиативном лечении неоперабельных пациентов, но не применяется при выраженном циррозе.
Лучевая терапия
Дистанционная лучевая терапия в классическом виде применяется редко, поскольку наносит существенный ущерб неповрежденным тканям печени. Хорошие перспективы имеет стереотаксическая лучевая терапия, которая позволяет минимизировать воздействие на интактные ткани.
Химиотерапия
Назначается с целью увеличить продолжительность жизни пациента. Показаниями к ней являются отдаленные метастазы и прогрессирование заболевания после лечения другими методами, а также наличие противопоказаний к другим вариантам терапии.
Какой бы способ лечения не применялся, прогноз жизни пациента зачастую определяется не только новообразованием, но и циррозом печени.
Томотерапия в лечении рака печени
В лечении рака печени, а также других опухолей, хирургическое лечение которых подчас затруднительно, а химиолучевая терапия недостаточно эффективна и безопасна, популярность приобретают стереотаксические радиологические методы, позволяющие обеспечить подачу высокой дозы радиации в границах новообразования.
Именно такой системой является TomoTherapy HD, которая представляет собой
КТ-сканер, совмещенный с устройством для облучения, что позволяет добиться точного позиционирования пациента во время каждого сеанса лечения. Основные преимущества томотерапии:
- лечение опухолей разных форм и размеров;
- одновременное лечение сразу нескольких новообразований;
- избирательное излучение, не затрагивающее здоровые ткани;
- минимум побочных эффектов;
- возможность повторного применения.
Использование TomoTherapy HD открывает новые возможности в лечении пациентов с неоперабельным раком печени, позволяя значительно улучшить их прогноз выживаемости.
Стоимость лечения рака печени лучевой терапией
| Наименование услуги | Цена, руб. | Ед. измерения |
|---|---|---|
| Консультация врача онколога радиотерапевта | 0 | шт. |
| Консультация врача детского онколога | 0 | шт. |
| Повторная консультация специалистов | 500 | шт. |
| Топометрия на специализированном компьютерном томографе первичная | 15 000 | процедура |
| Топометрия на специализированном компьютерном томографе повторная | 7 000 | процедура |
| Дозиметрическое планирование лучевой терапии (томотерапии) первичное | 20 000 | шт. |
| Дозиметрическое планирование лучевой терапии (томотерапии) повторное | 7 000 | шт. |
| Лучевая терапия (томотерапия), включая IMGRT (*) | 223 000 | курс |
| Лучевая терапия (томотерапия) стереотаксическая радиохирургия(*) | 250 000 | курс |
| Лекарственная сопроводительная терапия: внутривенные введение в процедурном кабинете (без учета стоимости лекарственных препаратов) | 1 000 | процедура |
| Лекарственная сопроводительная терапия: внутримышечное введение в процедурном кабинете (без учета стоимости лекарственных препаратов) | 200 | процедура |
| Топометрическая разметка | 750 | процедура |
Вид лучевой терапии и количество сеансов курса определяется врачебной комиссией индивидуально для каждого пациента исходя из локализации, нозологии опухоли и с учетом анамнеза.
Часто задаваемые вопросы
Сколько стоит курс лечения?
Курс лечения вместе с предлучевой подготовкой стоит 258 000 рублей. Есть возможность оформления рассрочки на весь период лечения.
Есть ли онлайн-консультация?
Для жителей других регионов, а также для тех, кому визит к врачу затруднителен, наш центр предоставляет возможность бесплатной онлайн - консультации.
Документы, которые необходимы для получения онлайн-консультации?
Для получения консультации о возможности получения томотерапии, вам необходимо направить нам все имеющиеся у вас медицинские выписки и обследования, включая гистологическое заключение. Направление на бесплатную консультацию не требуется.
Возможно ли лечение детей?
Томотерапия наиболее благоприятна для лечения детей, так как лучевая терапия проходит щадящим методом, не задевая здоровые органы и ткани развивающегося ребенка.
На какой стадии можно применять лучевую терапию?
В современной онкологии возможности лучевой терапии применяются очень широко на любой стадии. Однако каждому пациенту требуется индивидуальный подход, так как выбор тактики и плана лечения зависит от многих факторов: расположения опухоли, сопутствующих заболеваний, возраста и общего состояния пациента. Поэтому для получения информации о возможности лечения, необходимо получить консультацию врача-радиотерапевта.
Читайте также:


