Лучевая диагностика опухолей головного и спинного мозга
Наиболее точная информация о наличии и характере опухолевого процесса содержится в медицинских изображениях мозга, получаемых различными видами томографии. Направление на обследование дается после изучения симптомов, истории болезни пациента, проведения физического осмотра и специальных неврологических тестов.
Неврологические тесты позволяют проверить двигательные и сенсорные функции, слух и речь, рефлексы, зрение, координацию, психическое состояние и другие неврологические функции пациента, нарушения в которых могут свидетельствовать о наличие опухоли.
Методы томографии
Для постановки диагноза необходимы детальные изображения головного и спинного мозга, нервных волокон, костей и других органов. Медицинские изображения помогают не только определить наличие опухоли, но также позволяют оценить некоторые ее характеристики, обнаружить воспалительные процессы. Ниже приведен перечень основных методов томографии.
- Компьютерная томография (КТ) . Обработанные компьютером данные рентгенографии позволяют построить множество сечений тела или 3D модель органов, костей, различных тканей, в том числе опухолевых. Эффективна для обнаружения кальцинирования тканей, которое служит предпосылкой опухолевого роста.
- МРТ . Магнитно-резонансная томография позволяет построить более точные двумерные или трехмерные модели в сравнении с КТ.
- Контрастная МРТ или КТ . Как МРТ, так и КТ могут проводиться с контрастным агентом: внутривенно вводится специальный безвредный агент, выполняющий роль красителя. При такой технике опухоли выглядят отчетливее.
- Функциональная МРТ . Проводится для исследования областей мозга, отвечающих за определенные функции, например, двигательные или речевые. Позволяет оценить степень повреждения нервной структуры и расстояние от них до опухоли.
- МРС . Магнитно-резонансная спектроскопия позволяет дифференцировать ткани по химическому составу, который выявляется из реакции ткани на электромагнитное излучение.
- Позитрон-эмиссионная томография . Позволяет построить модели биохимических процессов и функции клеток. Оценивается потребление глюкозы, которая вводится в кровоток и имеет небольшую радиоактивность. Т.к. злокачественные образования, как правило, потребляют больше глюкозы – они становятся ярче на изображении.
- Однофотонная эмиссионная компьютерная томография (SPECT). Изучается кровоток к тканям. Некоторые опухоли создают дополнительные кровеносные сосуды для питания, которые и выявляются в ходе исследования. Радиоактивный изотоп вводится внутривенно, затем его движение по черепу отслеживается специальным устройством, по результатам работы которого воссоздается трехмерная картина кровотока головного мозга.
- Ангиография . Может применяться для выявления характерных для опухоли структур сосудов. При этом в кровоток вводится рентгеноконтрастный краситель. Во многих случаях ангиография заменятся неинвазивными методиками КТ или МРТ.
- Спондилография . Рентгенография позвоночника в двух проекция проводится при подозрении на опухоль спинного мозга. Может быть заменена на более точную КТ позвоночника.
Лабораторные исследования
- Анализ крови, мочи могут дать некоторые сведения об опухоли. Проводится гормональный анализ.
- Может потребоваться проведение электроэнцефалограммы (ЭЭГ), которая по записи биотоков мозга позволяет определить характер нарушений.
- Анализ цереброспинальной жидкости . В некоторых случаях с помощью специальной иглы берут пробу цереброспинальной жидкости, которая исследуется на наличие злокачественных клеток и отклонения в биохимическом составе.
- Магнитоэнцефалография позволяет отследить активность нервных клеток.
Результаты томографии и лабораторных исследований позволяют с высокой степенью достоверности установить диагноз опухоли головного или спинного мозга, а также получить информацию, характеризующую опухолевый процесс. Однако для некоторых видов опухолей с целью уточнения диагноза необходимо проведение биопсии (открытой, пункционной или стереотаксической).

Диагностика опухолей спинного мозга
Стандартные методы обследования, к которым прибегают при различных заболеваниях нервной системы, также относятся к диагностике опухолей спинного мозга на ранних стадиях. Это может быть физикальное и неврологическое обследование, а также особый метод исследования функций периферических нервов - электронейромиография.
ЭНМГ отличается от других нейрофизиологических исследований тем, что является многоступенчатым и довольно сложным процессом. Специалист, проводящий ЭНМГ, должен определять методику исследования для каждого пациента индивидуально. Только в этом случае можно получить информацию для постановки максимально точного диагноза.
Для проведения электронейромиографии необходимо наличие определенных сведений. К ним относится предварительный диагноз пациента, а также указание тех участков организма, которые должны быть исследованы.
К наиболее современным методам диагностики опухолей спинного мозга относятся КТ (компьютерная томография) и МРТ (магнитно-резонансная томография). Они позволяют определить точное расположение опухоли, ее форму, размер, а также ее отношение к соседним органам и тканям.
МРТ (магнитно-резонансная томография) является неинвазивным методом диагностики, который помогает специалистам довольно точно поставить тот или иной диагноз.
Принцип МРТ заключается в использовании мощных магнитных полей, высокочастотных импульсов и сложной компьютерной системы, которая позволяет получить детальное изображение позвоночника. Снимки, полученные в результате МРТ, можно изучать на мониторе компьютера, распечатывать или копировать на различные информационные носители. Рентгеновское излучение при МРТ не используется, следовательно, она является абсолютно безопасной.
Информация, полученная при помощи МРТ, позволяет специалистам точно оценить состояние опухоли, так как данный метод диагностики является наиболее чувствительным в обследовании позвоночника на предмет наличия опухоли.
КТ позвоночника проводится с помощью специального оборудования - компьютерного томографа. Он представляет собой аппарат, состоящий из кольца, оснащенного детекторами и двигающейся кушетки, на которой располагается пациент. Кушетка въезжает в кольцо, что дает возможность специальной установке сделать снимки позвоночника пациента в разных проекциях.
КТ одной зоны занимает 15-20 минут. В некоторых случаях для нее используется контрастное вещество, которое вводится пациенту с целью получения более четких снимков. Данное вещество совершенно безопасно и выводится из организма довольно быстро - в течение нескольких дней.
Если опухоль спинного мозга находится в области мягких тканей, то ее можно диагностировать при помощи УЗИ. Это – довольно
точный и безопасный метод диагностики опухолей спинного мозга, не требующий особых временных и финансовых затрат.
Существует еще один метод диагностики опухолей спинного мозга – биопсия. Она представляет собой забор биоптата - клеток или тканей из организма пациента для дальнейшего изучения на предмет признаков заболевания.
Биопсия может проводиться самыми разными способами. В некоторых случаях для нее используется полая игла, которая дает возможность взять небольшой кусочек ткани. Но в некоторых ситуациях необходимо хирургическое удаление всего образования целиком.
Существует несколько методов лечения опухолей спинного мозга, цена которых также различна. Это может быть:
- хирургическая операция,
- лучевая терапия,
- химиотерапия,
- радиохирургия,
- комплексное лечение.
Хирургическая операция заключается в удалении большей части опухоли. Этот метод лечения является инвазивным и может вызвать некоторые осложнения, например, кровотечение.
Лучевая терапия осуществляется при помощи мощного радиоактивного излучения, направленного на опухоль и полностью уничтожающего ее либо уменьшающего ее размеры.
Химиотерапия заключается в употреблении лекарственных препаратов, уничтожающих раковые клетки. Медикаменты распространяются по организму вместе с кровотоком, поражая не только раковые, но и некоторое количество здоровых клеток.
Комплексное лечение назначается тогда, когда опухоль спинного мозга отличается высокой степенью развития. Оно включает в себя хирургическое вмешательств, химиотерапию и лучевую терапию.
К радиохирургическому лечению относится система КиберНож. Это наиболее прогрессивный метод лечения опухолей спинного мозга, не требующий предоперационной подготовки, анестезии и длительного пребывания больного в стационаре.
| Стоимость лечения | |
| Опухоль спинного мозга (от 305 000) |
Точная стоимость лечения определяется только после консультации с врачом
- О центре
- Специалисты
- Новости
- Партнеры
- Отзывы
- Запись на приём
- Стоимость лечения
- Консультация
- Диагностика
- FAQ
- Статьи
- Аппарат Кибернож
- Уникальность системы
- Показания к лечению
- Противопоказания
- Как происходит лечение
- Сравнение методов
- Дистанционная
- Комбинированное лечение
- Лечение
- Опухоли головного мозга
- Рак легкого
- Рак печени
- Рак почки
- Рак предстательной железы
- Рак носоглотки
- Опухоль спинного мозга
- Опухоль ЦНС у детей
- Рак поджелудочной железы
- Опухолевое поражение костей
- Метастазы
- Невралгия тройничного нерва
- Пяточная шпора
Информация, получаемая с помощью стандартной рентгеновской краниографии при опухолях пинеальной области, весьма ограничена.
На краниограммах можно увидеть кальцифицированное шишковидное тело, отложение солей в капсуле опухоли или фрагменты костных структур, например, зубы, которые могут встречаться в структуре тератомы.
Общие сведения
Рентгеновская компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) в настоящее время являются основными диагностическими методами, позволяющими дать достаточно полную характеристику патологического процесса, расположенного в пинеальной области.
При этом, возможности МРТ более широки, чем у КТ. Этому способствует не только получение изображений в аксиальной, сагиттальной и фронтальной плоскостях, но и трехмерных изображений, а также большой спектр дополнительных возможностей, характерных для самого метода МРТ (МР-ангиография, МР-ликвородинамическое исследование, MP-спектроскопия и т.д.).
Метод магнитно-резонансной томографии позволяет детально изучить топографию и структуру опухоли, ее отношение к прилегащим структурам мозга, распространение опухоли по субэпендимарному слою, уточнить характер нарушения ликвороциркуляции. Большим преимуществом МРТ является возможность выявления метастазов в спинномозговом канале.
Перечисленные возможности помогают определить расположение опухоли по отношению к третьему желудочку и окружающим тканям, направление ее преимущественного роста (супра-субтенториально). Помимо этого, МРТ исследование опухоли в разных режимах дает представление о более тонкой структуре и химическом составе опухоли (рис.13).

Рис. 13. Стандартная МРТ больных с опухолями пинеальной области. Разные больные.
МРТ в режимах Т1 (а) и Т2 (б) выявляет диффузную опухоль пинеальной области с небольшой кистой в се толще. После внутривенного введения контрастного вещества отмечается его интенсивное накопление опухолью (в,г,д). Исследование в трех проекциях позволяет оценить объем, конфигурацию опухолевого узла и его взаимоотношение с окружающими структурами мозга. МРТ с контрастным усилением четко демонстрирует массивную субарахноидальную диссем и нацию опухоли в пределах всей центральной нервной системы (е,ж). Субарахноидальное метастазирование (з,стрелки) и единичный метастаз анапластической пипсоцитомы на уровне С4-С5.
Особо следует отметить роль неинвазивной МР-ангиографии, точнее — МР-венографии в обследовании больных с опухолями пинеальной области, которая определяет отношение опухоли к важным венозным коллекторам — галеновой вене и ее притокам (рис.14).

Рис.14. Магнитно-резонансная томография больных с опухолью пинеальной области:
а) сагиттальная МРТ в режиме Т1 с контрастным усилением у больного с герминомой пинеальной области и метастазами в инфундибулярной части третьего и четвертом желудочках (стрелки); б,в) MP-ангиография и г,д) трехмерная ангиография того же больного. На ангиограммах хорошо визуализируются как артериальные, так и венозные сосуды головного мозга.
Более того, MP-ангиография с контрастным усилением (Magnevist, Omniscan) позволяет выявить артериальные сосуды, кровоснабжающие опухоль, а в некоторых случаях (особенно при менингиомах) оценить степень васкуляризации опухоли. Можно так же подчеркнуть роль метода в решении дифференциально-диагностических проблем, в частности, для выявления сосудистых мальформаций, которые могут локализоваться в пинеальной области (в первую очередь речь идет об аневризмах галеновой вены).
В настоящее время изучаются возможности МРТ в визуализации ликворной системы и процесса ликворооттока — магнитно-резонансная миело- и цистернография (режимы PSIF, 2D FLASH). Эта неинвазивная методика позволяет получать высококонтрастные изображения ликворных пространств по отношению к веществу мозга. Данная технология хорошо зарекомендовала себя в диагностике состоятельности вентрикулостом, определении уровня и характера окклюзии ликворных путей головного мозга (рис. 15).

Рис.15. МРТ исследование ликвородинамики. Разные больные. Режим PSIF.
а) кистозное перерождение шишковидного тела. Потеря MP-сигнала (стрелки) указывает на проходимость водопровода мозга; б) больших размеров киста охватывающей цистерны, вызывающая полную окклюзию водопровода и гидроцефалию; в) МPT-феномен тока ликвора (потеря сигнала) по водопроводу мозга в режиме 2D FLASH (стрелка)
Несмотря на меньшую информативность КТ, сохраняются показания для ее применения, особенно при проведении исследования с контрастным усилением. Помимо таких характеристик, как размер и локализация опухоли пинеальной области, наличие в ее строме кист или геморрагических компонентов, степень расширения желудочков, КТ позволяет лучше выявлять петрифицированную часть опухоли (рис.16).

Рис.16. КТ в диагностике опухолей пинеальной области. Разные больные:
а) анапластическая пинеоцитома с обильным кальцифицированием: б) тератома третьего желудочка с участками пониженной плотности (холестатомные массы); в,г) трехмерная (3D) реконструкция опухоли, занимающей третий и четвертин желудочки: д) сагиттальная реконструкция больного с опухолями пинеальной и хиазмальной областей; е) обызвествление шишковидного тела; ж) тромбироваппая аневризма пинеальной области с выраженной окклюзионной гидроцефалией.
Необходимо отметить, что отложение солей кальция в шишковидном теле не свойственно здоровым детям до 6 лет. Поэтому, выявление петрификата в шишковидном теле у детей, особенно при его эксцентричном расположении, может указывать на наличие опухоли.
Рентгеновская КТ занимает ведущее место в оценке радикальности удаления опухоли и выявлении осложнений в раннем послеоперационном периоде. Это связано с тем, что данные МРТ, полученные в эти же сроки, часто сложно однозначно интерпретировать из-за наличия продуктов окисления гемоглобина. Однако, как показывает наш опыт, уже через 2-3 недели после операции выраженность артефактов уменьшается и метод МРТ позволяет адекватно оценить эффективность операции.
Одним из недостатков КТ по сравнению с МРТ является низкая чувствительность метода в случае малых размеров опухоли пинеальной области, например при небольших опухолях четверохолмия.
Современные высокоразрешающие рентгеновские и магнитно-резонансные компьютерные томографы дают высокодостоверную информацию о строении, предположительной гистоструктуре опухоли и, что очень важно для хирурга, с высокой точностью определяют ее отношение к окружающим структурам (край вырезки мозжечкового намета, средний мозг, третий желудочек и вена Галена с ее притоками).
Селективная церебральная ангиография при опухолях пинеальной области позволяет визуализировать тонкую ангиоархитектонику опухолей и получить информацию о состоянии крупных артериальных и глубинных венозных сосудов (рис.17). Уточнение их взаиморасположений с опухолевым узлом помогает хирургу в планировании доступа к опухоли.

Рис.17. Пункционная ангиография в диагностике опухолей пинеальной области. Варианты кровоснабжения опухоли пинеальной области. Разные больные.
# МРТ в сагиттальной (а) и аксиальной (б) проекциях больной с анапластической пинеотомой. Тотальная ангиография (в,г,д) выявляет кровоснабжение опухоли только ветвями задней мозговой артерии — задней медиальной и латеральной ворсинчатой артериями (стрелки). Дренирование венозной крови осуществляется через глубокие вены — внутреннюю (1) и базальную (2) — в вену Галена (3) и в прямой синус (4);
# МРТ в сагиттальной проекции больного с менингиомой пинеальной области (е). Источниками кровоснабжения опухоли являются ветви сонной (ж) и задней мозговой артерии (з).
Особенно важно ангиографическое исследование при подозрении на менингиому, которая по сравнению с другими опухолями пинеальной области имеет склонность к инвазии стенок сосудов и их окклюзии. Отсутствие контрастирования внутренних и галеновой вен указывает на их облитерацию.
Несмотря на все положительные стороны, роль прямой ангиографии в диагностике патологии пинеальной области переоценивать не следует. Топографию глубоких вен мозга легко определить с помощью МРТ в стандартных режимах, а современная МР-ангиография позволяет визуализировать сосудистую сеть опухоли и изучить интенсивность ее кровоснабжения. По этим причинам в настоящее время прямая ангиография, относящаяся к инвазивным методам диагностики, при опухолях пинеальной области применяется достаточно редко.
Дооперационное определение предположительной гистоструктуры опухоли пинеальной области нередко представляется сложной задачей, что в определенной степени обусловлено многообразием локализующихся в ней новообразований. Тем не менее, с большой долей вероятности можно распознавать такие опухоли как тератомы, эпидермоидные кисты, менингиомы, значительную часть термином. До настоящего времени нет абсолютно надежных патогномоничных КТ- и МРТ-признаков, способствующих определению гистологической принадлежности опухоли.
Несмотря на высокую информативность диагностических методов КТ и МРТ, в нашей практике встречались наблюдения, когда распознавание опухоли пинеальной области было сопряжено со значительными трудностями. Ниже приводим одно из таких наблюдений (рис. 18).

Рис.18. Возможности КТ и МРТ в диагностике опухолей пинеальной области. Ребенок 9 лет, с несахарным диабетом в анамнезе.
Стандартная МРТ (а,б,в) без внутривенного введения контрастного вещества не выявляет явные признаки патологического процесса головного мозга. Обращает внимание несколько увеличенное в размерах шишковидное тело. При КТ (г) с контрастным усилением отмечается усиленное накопление контраста в области шишковидного тела. Несмотря на это, основываясь только на данных МРТ. наличие опухолевого поражения головного мозга было исключено. Через 4 гола, в связи с ухудшением состояния, ребенок был обследован повторно. Проведенные КТ (д) и МРТ (е,ж) установили наличие опухоли в пинеальной области с метастазированием в инфундибулярную область третьего желудочка. МРТ после проведения лучевой и химиотерапии (з) показала значительное сокращение опухоли в пинеальной области и исчезновение метастаза.
КТ и МРТ топография опухолей пинеальной области
КТ и особенно МРТ, давая точное представление о расположении опухоли, позволяют выделить различные топографические варианты опухолей пинеальной области, что чрезвычайно важно для обоснования оптимальных хирургических доступов к ним.
Попытки такой топографической классификации были предприняты рядом авторов. C.Lapras (1984) выделил следующие группы:
а) опухоли с преимущественным расположением в задних отделах третьего желудочка и блокирующие вход в сильвиев водопровод без врастания в его просвет;
б) опухоли, преимущественно расположенные в области цистерны четверохолмия и сдавливающие четверохолмную пластинку;
в) опухоли задних отделов третьего желудочка, врастающие в водопровод мозга и оттесняющие четверохолмную пластинку кзади.
H.Satoch и соавторы (1995) в основу предложенной ими классификации взяли отношение опухоли к валику мозолистого тела.
Наш клинический опыт показал, что упомянутые выше классификации не охватывают все встречавшиеся в нашей серии наблюдений топографические варианты опухолей пинеальной области.
В основу принятой нами топографоанатомической группировки опухолей пинеальной области легли два основных признака — положение относительно окружающих ее мозговых структур (в первую очередь таких, как четверохолмие, водопрвод, задние отделы третьего желудочка) и размеры опухоли. Меньшее значение имело место исходного роста опухоли в связи с высокой частотой выраженного инвазивно-инфильтративного роста этих новообразований.

Рис.19. Различные топографоанатомическис варианты опухолей пинеальной области в зависимости от их размеров, локализации и преимущественного распространения: а) первая топографоанатомическая группа; б) вторая топографоанатомическая группа; в) третья топографоанатомическая группа.

Рис.20. Различные топографоанатомичсские варианты опухолей пинеальной области в зависимости от их размеров, локализации и преимущественного распространения: г) четвертая топографоанатомическая группа; д, е) пятая топографоанатомическая группа.
На основании сопоставления данных КТ, МРТ и интраоперационных находок мы выделили следующие группы опухолей пинеальной области (рис. 19,20):
1. Опухоли небольших размеров (диаметр опухолевого узла до 2,5 см) с преимущественной локализацией в четверохолмной цистерне (41 наблюдение);
2. Опухоли небольших размеров (диаметр опухолевого узла до 2,5 см) с преимущественным расположением в задних отделах третьего желудочка (46 наблюдений);
3. Опухоли средних размеров (диаметр опухолевого узла от 2,5 до 4 см), располагающиеся как в четверохолмной цистерне, так и в задних отделах третьего желудочка (103 наблюдения);
4. Опухоли больших размеров (диаметр опухоли от 4 до 6 см), полностью занимающие четверохолмную цистерну и задние отделы третьего желудочка, нередко врастающие в один из боковых желудочков (77 наблюдений);
5. Опухоли, диаметром более 6 см, которые обычно практически полностью занимали полость третьего, часть четвертого желудочков и врастали в оба боковых желудочка (20 наблюдений).
Варианты опухолей пинеальной области и частота их встречаемости представлены на основе предложенной нами классификации на рис.21.

Рис.21. Распределение опухолей пинеальной области по топографическим вариантам.
По нашему мнению, важным моментом, с точки зрения планирования операции, является уточнение взаиморасположения опухоли и четверохолмной пластинки. При этом, наиболее достоверная и полная информация может быть получена с помощью МРТ.

Рис.22. Варианты взаиморасположения опухоли пинеальной области и четверохолмной пластинки.

Рис.23. Варианты взаиморасположения опухоли пинеальной области и четверохолмной пластинки.
Поданным МРТ, нами были выделены следующие основные варианты (рис.22,23):
а) опухоль лежит на четверохолмной пластинке, придавливая ее к покрышке среднего мозга;
б) опухоль растет из четверохолмной пластинки и частично разрушает ее;
в) опухоль врастает в просвет сильвиева водопровода через его оральное отверстие и приподнимает только передние отделы четверохолмной пластинки. Диаметр каудального отверстия сильвиева водопровода практически не изменен;
г) опухоль располагается, в основном, в просвете сильвиева водопровода, смещая четверохолмную пластинку в сторону четверохолмной цистерны на всем ее протяжении. Каудальные отделы опухоли достигают четвертого желудочка;
д) опухоль располагается в задних отделах третьего желудочка, при этом задняя часть опухоли прилегает к оральным отделам сильвиева водопровода.
Такая, на первый взгляд, детальная группировка опухолей и уточнение отношения новообразования к пластинке четверохолмия, водопроводу мозга и задним отделам третьего желудочка, по нашему мнению, представляются оправданными, поскольку позволяют выбрать оптимальный доступ к опухоли и дают возможность хирургу более уверенно ориентироваться в отношении опухоли к окружающим структурам, которые могут быть смещены и инфильтрированы.
а) Вопросы лучевой диагностики с позиций анатомии. Новообразования, поражающие позвоночник, могут распространяться напрямую, по лимфатическим путям, гематогенным путем и стоком ликвора. Может также наблюдаться сочетание различных путей распространения опухоли, при этом наиболее типичным является гематогенная диссеминация опухоли в тела позвонков с последующим прямым проникновением ее в эпидуральное пространство.
Первичные опухоли паравертебральных мягких тканей также могут поражать позвоночный столб. Примером служит рак легких, прорастающий в грудную стенку, паравертебральные ткани и далее в позвоночник и эпидуральное пространство. Опухоли предстательной железы, мочевого пузыря или кишечника могут прорастать в пресакральное пространство и затем в позвоночник и эпидуральное пространство. Рак носоглотки может распространяться в область ската и основания черепа и далее следовать вдоль черепных нервов. В редких случаях может наблюдаться прямой рост опухоли ЦНС вдоль биопсийного тракта или операционной раны.
Также описаны редкие случаи роста опухоли ЦНС вдоль постоянного шунтирующего катетера с последующим системным метастазированием. Данные лучевой диагностики в случае прямого распространения опухоли и поражения позвоночника включают мягкотканное объемное образование с разрушением соседних костных структур и различной выраженности сдавлением нервных образований. Напрямую в эпидуральное пространство наиболее часто распространяются опухоли из тел позвонков, разрушающие заднюю продольную связку. Передняя продольная связка и межпозвонковый диск относительно резистентны к опухолевой инвазии. Передняя продольная связка более мощная по сравнению с задней и характеризуется меньшим числом перфорирующих ее сосудов. При проникновении в эпидуральное пространство опухоль встречается с достаточно толстой твердой мозговой оболочкой, которая является эффективным барьером для дальнейшего распространения опухоли.
Описанные барьеры позволяют на основании лучевых признаков достаточно четко разграничить инфекционное поражение диска с вовлечением смежных участков позвонков, при котором эпицентром является именно межпозвонковый диск, и опухолевое поражение, когда эпицентром являются тела позвонков, а межпозвонковые диски остаются относительно сохранными. Прямое распространение опухоли также может наблюдаться при первичных опухолях спинного мозга на шейном уровне, когда опухоль растет в инфратенториальное пространство. Изредка до верхнешейного уровня могут распространяться опухоли ствола мозга или мозжечка.
Лимфогенный путь распространения опухолей в лучевой диагностике поражений позвоночника имеет лишь ограниченное значение. Местно-распространенный рост опухолей таза с инвазией поясничного отдела позвоночника при отсутствии метастазов в легких позволяет предположить распространение опухоли по венозным или лимфатическим коллекторам.
Гематогенный путь является наиболее актуальным путем метастазирования злокачественных опухолей в позвоночник. Сплетение Батсона представляет собой продольно ориентированную сеть бесклапанных вен, расположенных вдоль позвоночного столба. Эти вены лежат вне плевральной и брюшной полости и имеют множество анастомозов с другими отделами венозной системы - полой веной, позвоночными венами, воротной веной, межреберными венами, легочными и почечными венами. Направление кровотока в сплетении Батсона вариабельно и зависит от внутригрудного и внутрибрюшного давления.
Опухоли самой различной анатомической локализации могут метастазировать по венам этого сплетения, минуя легкие или печень. Клетки рака простаты вместе с током крови по венам сплетения Батсона могут метастазировать в тела позвонков, минуя нижнюю полую вену. Рак молочной железы распространяется в тела позвонков через систему непарной вены и сплетение Батсона. В сплетение Батсона шунтируется не более 5-10% объема портального кровотока, что объясняет относительно невысокую частоту спинальных метастазов при первичных опухолях желудочно-кишечного тракта и мочеполовой системы. При подавляющем большинстве метастатических поражений позвоночника точно сказать, каким путем произошло метастазирование, невозможно. Органотропные характеристики опухолевых клеток и особенности зоны их имплантации могут иметь даже более важное значение, чем тот или иной путь их метастазирования.
Распространение по ликворопроводящим путям является важным путем метастазирования первичных интракраниальных опухолей. Опухолевые эмболы попадают в ликвор при фрагментации опухоли, а также при тех или иных хирургических манипуляциях. Распространение по ликворопроводящим путям описано для таких опухолей ЦНС, как медуллобластома, эпендимома, опухоли шишковидной железы, астроцитома и лейкемия, карцинома сосудистого сплетения и ретинобластома (неблагоприятный прогноз при амплификации гена MYCN). Метастазирование по ликворопроводящим путям может наблюдаться и после первичной гематогенной диссеминации опухоли. Например, подобная картина будет иметь место при метастатическом поражении спинного мозга и мягких мозговых оболочек после первичного гематогенного поражения позвоночника при раке легких и молочной железы.
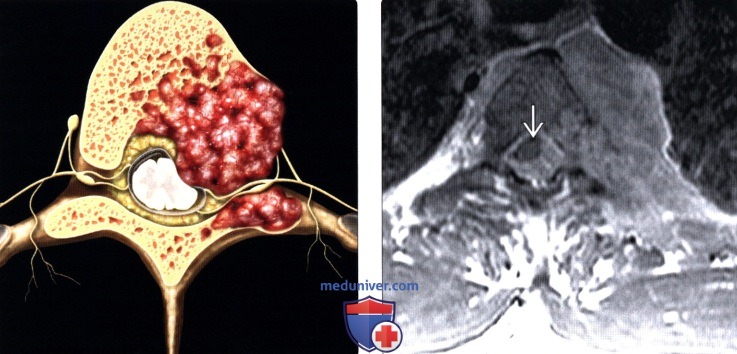
(Слева) На схеме сагиттального среза показано гематогенно-диссеминированное литическое метастатическое поражение тела и корня дуги грудного позвонка с последующим прямым эпидуральным распространением опухоли и сдавлением спинного мозга.
(Справа) Аксиальный срез, Т1-ВИ с КУ: гематогенный метастатический паравертебральный очаг, поражающий тело позвонка и распространяющийся на задние элементы, грудную стенку и эпидуральное пространство со сдавлением спинного мозга. 
(Слева) Сцинтиграмма скелета пациента с распространенным бластическим метастатическим поражением на фоне рака предстательной железы: множественные фокусы усиленного захвата изотопа, соответствующие диффузному метастатическому поражению скелета.
(Справа) Сагиттальный срез, Т1-ВИ с КУ, пациент с распространенным метастатическим поражением позвоночника на фоне рака предстательной железы: диффузное патологическое снижение интенсивности тел и задних элементов всех позвонков с множественными очагами распространения опухоли в вентральные отделы эпидурального пространства и незначительной компрессией спинного мозга на этих уровнях.
б) Вопросы патологической анатомии. Метастатическое поражение внутренних органов и костей скелета развивается у 40% больных раком. Позвоночник является наиболее типичным местом костного метастазирования. Метастатическое поражение позвонков несколько чаще наблюдается у мужчин (соотношение мужчин и женщин составляет 3:2). Большинство метастатических поражений тел позвонков составляют метастазы рака предстательной железы, легких и молочной железы. Локализация— грудной отдел (70%) > поясничный отдел (20%) > шейный отдел.
Первичные опухоли обычно образованы различными в биологическом отношении клетками, отличающимися различным метастатическим потенциалом. Клетки опухолей постоянно попадают в общий кровоток, но сохраняют жизнеспособность и достигают отдаленных органов-мишеней менее 0,01-0,1 % из них. Процесс метастазирования достаточно сложен и включает несколько этапов: отделение клетки от первичной опухоли, попадание в кровоток, ликвор или лимфатическую систему, сохранение жизнеспособности в транспортной системе, прикрепление к эндотелию сосудов отдаленных от первичного источника органов и тканей, а также выход из сосуда в интерстициальное пространство и, наконец, формирование локального кровоснабжения в зоне имплантации. Отдаленные от первичного источника органы и ткани отличаются своими анатомическими особенностями. Это касается в т.ч. и характера венозного и артериального кровоснабжения.
в) Механизмы туморогенеза. Туморогенез у человека является многоэтапным процессом. Его этапы являются отражением генетических нарушений, которые индуцируют прогрессирующую трансформацию нормальных клеток человеческого тела в высокозлокачественные их формы. Показано, что заболеваемость раком имеет четкую возрастную зависимость и связана с развитием 4-7 ограниченных во времени случайных событий. Развитие опухоли требует наличия определенных изменений генома клетки, каждое из которых характеризуется теми или иными изменениями роста и деления клеток, что в конечном итоге приводит к прогрессирующей трансформации нормальных клеток в опухолевые. Раковые клетки по определению характеризуются дефектами регуляторных механизмов, которые в норме отвечают за пролиферацию клеток и их гомеостаз. Дефекты эти подразделяют на шесть типов:
1) самодостаточность ростковых сигнальных систем;
2) нечувствительность к подавляющим эти сигнальные системы факторам;
3) обход механизмов запрограммированной гибели клеток (апоптоза);
4) неограниченный репликативный потенциал;
5) поддержание процессов ангиогенеза и
6) инвазия в другие ткани и метастазирование.
Каждое из этих шести изменений физиологии клетки является отражением нарушения механизмов противораковой защиты, присущих всем клеткам и тканям человеческого тела.
Нормальные клетки человеческого тела начинают активно пролиферировать только при получении соответствующих сигналов. Эти сигналы передаются клеткам через трансмембранные рецепторы, которые способны связываться с самыми различными сигнальными молекулами - диффундирующие факторы роста, компоненты внеклеточного матрикса и клеточные адгезивные молекулы (КАМ). Многие опухолевые клетки приобретают способность самостоятельно синтезировать необходимые им факторы роста, что формирует патологический замкнутый круг. Примерами являются продуцирование клетками глиобластомы тромбоцитарного фактора роста (TDGF) или клетками сарком фактора роста опухолей α (TGF-α). В опухолях мозга обнаруживается рецептор к эпидермальному фактору роста (EFR-R).
Нормальные ткани обладают различными механизмами, ограничивающими их пролиферацию. Это и ингибиторы факторов роста, и ингибиторы в составе внеклеточного матрикса на поверхности соседних клеток. Многие антипролиферативные факторы проникают в клетку через каналы, образованные различными вариантами белка, называемого супрессором роста ретинобластомы (pRb). Нарушение этого пути делает клетки нечувствительными к антипролиферативным факторам за счет репрессии факторов транскрипции, кодируемых геном E2F, и пролиферации клеток.
Обход механизма запрограммированной гибели клетки (апоптоза) обычно развивается за счет мутаций гена-супрессора опухолей р53. Инактивация белка, кодируемого этим геном, наблюдается более чем у 50% больных злокачественными опухолями.
Одним из наиболее изученных аспектов патофизиологии опухолевых клеток является, наверное, ангиогенез опухолей. В качестве классических индукторов ангиогенеза рассматриваются сосудистый эндотелиальный фактор роста (VEGF) и фактор роста фибробластов (FGF). Всего известно более двух дюжин ангиогенез-индуцирующих факторов и такое же количество их ингибиторов.
г) Метастазирование и движение клеток. Метастазы являются причиной 90% смертей от онкологических заболеваний. Инвазивный рост опухоли и метастазирование являются очень сложными процессами, в которых задействовано множество генетических и биохимических механизмов. Эти процессы можно описать такими терминами, как инвазия опухоли, гематогенная или лимфогенная диссеминация опухолевых клеток, колонизация отдаленных органов и развитие метастаза. В удержании клеток в присущем для них микроокружении участвует несколько классов белков. При инвазии и метастазировании эти механизмы меняются. Межклеточная регуляторная сигнальная система построена на КАМ и интегринах. Первым барьером на пути опухолевых клеток является базальная мембрана. Рецепторы на поверхности клеток распознают гликопротеины базальной мембраны, к которой прикрепляются клетки.
За этим следует протеолиз входящего в состав базальной мембраны коллагена IV типа опухолеспецифичными коллагеназами. Происходит лизис базальной мембраны и клетки получают доступ в интерстициальное пространство, лимфатические и кровеносные сосуды. Хемоаттрактанты путем активации специфических рецепторов и нисходящих внутриклеточных сигнальных путей могут активировать процесс миграции и инвазии клеток. Этот процесс коренным образом реорганизует актиновый цитоскелет клеток. Хорошо известными регуляторами организации цитоскелета являются Rho/Rac ГТФ-азы. Активация Rac приводит к формированию складок клеточных мембран, образованию адгезивных комплексов и развитию у клеток ламеллоподий.
Диссеминация и движение опухолевых клеток осуществляется тремя различными путями, включающими эпителиально-мезенхимальное перемещение (ЭМП), амебообразное движение и коллективную миграцию. При ЭМП клетка удлиняется, ферментативно разрушает расположенный вокруг себя матрикс и мигрирует, образуя на своей поверхности выросты, подобные псевдоподиям. При амебообразном движении клетка приобретает сферическую форму и проходит по пространствам во внеклеточном матриксе. При коллективной миграции клетки мигрируют целыми пластами или кластерами. ЭМП включает уменьшение числа эпителиальных маркеров в области плотных межклеточных контактов и цитокератиновой филаментной сети и увеличение числа мезенхимальных маркеров — N-кадерина, виментина, интегринов, тенасцина С, фибронектина и фибробласт-специфичного протеина 1.
N-кадерин, по-видимому, является наиболее важным из этой группы маркеров. Процессы ЭМП управляются внутриклеточными онкогенными факторами, например, мутацией K-Ras или гиперэкспрессией гена Нег2. При некоторых опухолях, например, раке легкого, роль центрального регулятора ЭМП принадлежит TGFβ. TGFP индуцирует процессы ЭМП путем влияния на гены, участвующие в процессах пролиферации клеток, апоптоза, дифференцировки, движения и миграции.
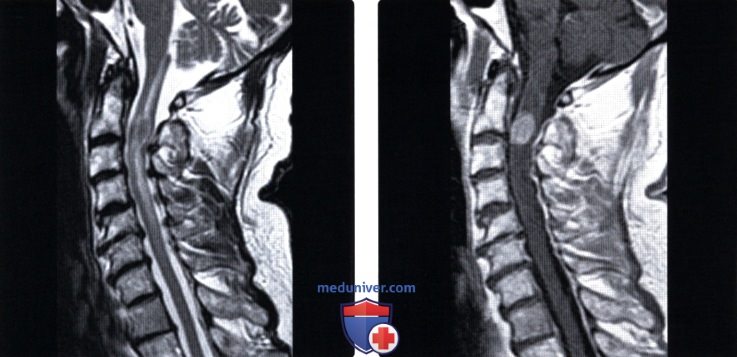
(Слева) Сагиттальный срез, Т2-ВИ, пациент с раком легкого и метастатическим поражением шейного отдела спинного мозга: определяются признаки диффузного отека спинного мозга, продолжающегося от цервикомедуллярного перехода до уровня С5. Более очаговые изменения сигнала отмечаются на уровне С2-С3.
(Справа) Сагиттальный срез, Т1-ВИ с КУ: у этого же пациента отмечается накопление контраста в области интрамедуллярного метастатического образования на уровне С2-С3. 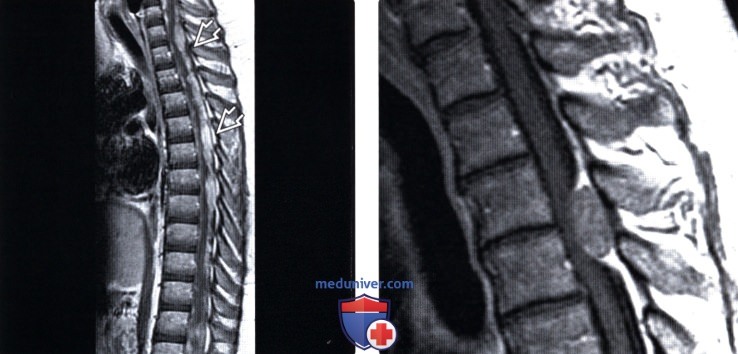
(Слева) Сагиттальный срез, Т1-ВИ с КУ, пациент с высокозлокачественной олигодендроглиомой головного мозга и распространенным метастатическим поражением мягких мозговых оболочек: отмечается массивное узелковое контрастное усиление сигнала опухолевых очагов в толще мягкой мозговой оболочки. Ребенок поступил с клиникой быстро развившейся вялой параплегии, что позволяет заподозрить инфаркт спинного мозга вследствие сдавления опухолью.
(Справа) Сагиттальный срез, Т1-ВИ с КУ: фокальное эпидуральное объемное образование, являющееся метастазом меланомы. Путь метастазирования в данном случае только гематогенный.
д) Клинические вопросы. Основным проявлением метастатического поражения позвоночника является постоянная боль в спине. При объективном исследовании чаще всего ничего не обнаруживается, либо обнаруживается только на поздней стадии заболевания (пальпируемое объемное образование или деформация позвоночника). Боль в спине и слабость нижних конечностей являются признаками эпидурального распространения опухолевого процесса. Ввиду наличия перекреста спиноталамических трактов уровень нарушения чувствительности может определяться на 1-2 сегмента ниже уровня компрессии. Чувствительные нарушения являются редким проявлением метастатического поражения позвоночника.
е) Список использованной литературы:
1. Balic М et al: Circulating tumor cells: from bench to bedside. Annu Rev Med. 64:31-44, 2013
2. Perlikos Fetal: Key molecular mechanisms in lung cancer invasion and metastasis: a comprehensive review. Crit Rev Oncol Hematol. 87(1):1 -11,2013
3. lanari A et al: Cell death or survival: The complex choice of the retinoblastoma tumor suppressor protein. Cell Cycle. 9(1):23-4, 2010
4. Chen HZ et al: Emerging roles of E2Fs in cancer: an exit from cell cycle control. Nat Rev Cancer. 9(11):785-97, 2009
5. Fiorentino FP et al: Senescence and p130/Rbl2: a new beginning to the end. Cell Res. 19(9): 1044-51, 2009
6. Mazel C et al: Cervical and thoracic spine tumor management: surgical indications, techniques, and outcomes. Orthop Clin North Am. 40(1):75-92, vi-vii, 2009
7. Sciubba DM et al: Solitary vertebral metastasis. Orthop Clin North Am. 40(1): 145-54, viii, 2009
8. Fokas E et al: Metastasis: the seed and soil theory gains identity. Cancer Metastasis Rev. 26(3-4):705-15, 2007
9. Guillevin R et al: Spine metastasis imaging: review of the literature. J Neuroradiol. 34(5):311—21, 2007
10. Christofori G: New signals from the invasive front. Nature. 441 (7092):444-50, 2006
11. Demopoulos A: Leptomeningeal metastases. Curr Neurol Neurosci Rep. 4(3):196-204, 2004
12. Batson OV: The function of the vertebral veins and their role in the spread of metastases. Ann Surg. 112(1):138-49, 1940
Редактор: Искандер Милевски. Дата публикации: 22.8.2019
Читайте также:

