Аденоматоидная опухоль надпочечника дифференциальная диагностика
- И. — это случайные находки в надпочечниках (н.).
- И. обнаружены ≈5% от всех исследований.
- Меньше 10% имеют эндокринные проявления и меньше 5% являются злокачественными.
- До сих пор однозначно не ясно что делать:
— признаки доброкачественности = не дообследовать;
— нет динамики за год = высокая вероятность доброкачественности
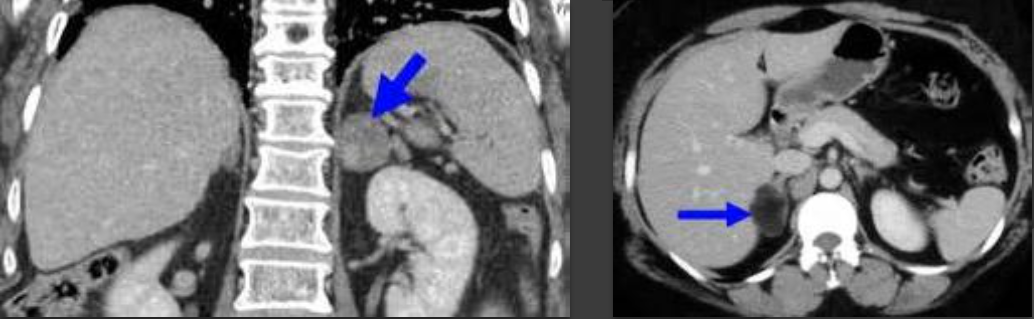
- чрезмерная продукция альдостерона клубочковой зоной коры н.
- ≈ 2% от всех И. ≈60% двусторонняя идиопатическая. гиперплазия коры н.
- ≈35% аденома коры н., продуцирующая альдостерон
- Стойкая АГ, снижение плазменной активности ренина, возможна гипокалиемия
- хроническое воздействие избытка гормонов коры н. ( кортизола) От 2-15% аденом коры н. производят кортизол. Размер часто до 2см.
- увеличение веса, увеличение жира, АГ, аменорея, гирсутизм, диабет, угри, слабость мышц.
- феохромацитомы ≈3-6% от всех И.
эпизодические головные боли, потоотделения и тахикардия, с или без АГ. - диагноз ставят после 24-часовое измерение мочи на катехоламины и метанефрины
- обычно связаны с опухолями с увеличением частотой злокачественности.
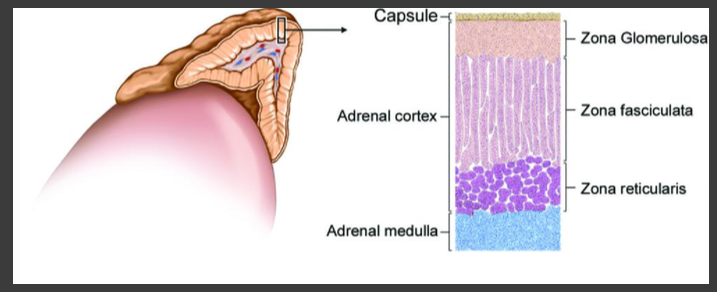
- клубочковая зона производит минералокортикоиды.
- пучковая зона производит глюкокортикоиы.
- сетчатая зона производит годнадокортикоиды.
- мозговое вещество надпочечника производит катехоламины.
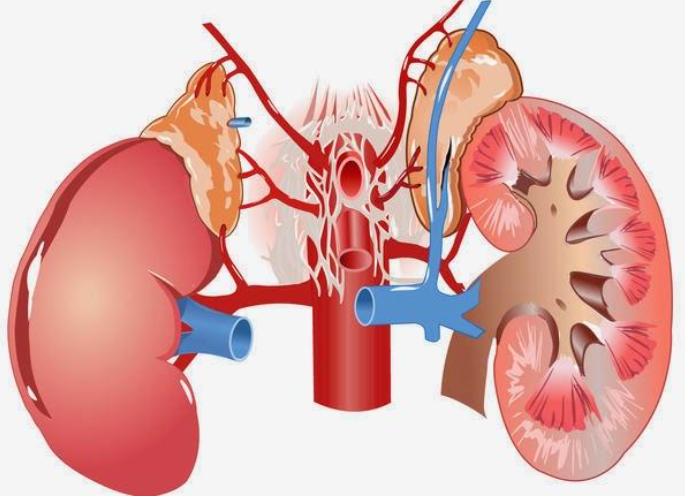
- Верхние – из диафрагмальных а.
- Средние – из брюшной аорты.
- Нижние – из почечных а.
- Слева
- в левую почечную в. или
- в низшую диафрагмальную в.
- Справа – в нижнюю полую вену.
- Аденома коры надпочечников.
- Гиперплазия коры надпочечников.
- Надпочечное кровотечение.
- Надпочечные кисты.
- Миелолипома.
- Феохромацитома.
- Гемангиома.
- Лимфангиома.
- Шваннома
- Гангионеврома.
- Аденоматоидные опухоли.
- Онкоцитома.
- Инфекционные поражения надпочечников.
- Аденомы – самые частые опухоли н. от 1,4- 8,9% всех вскрытий.
- Безконтрастная КТ: плотность до 10 HU имеет высокуючувствительность (79%) и специфичность (96%).
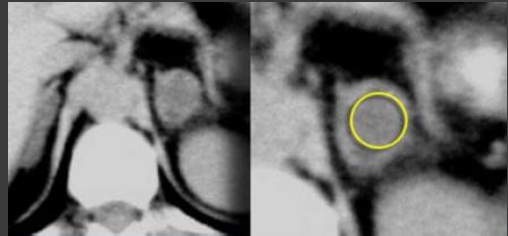
КТ. Аденомы изменение более 1⁄2.
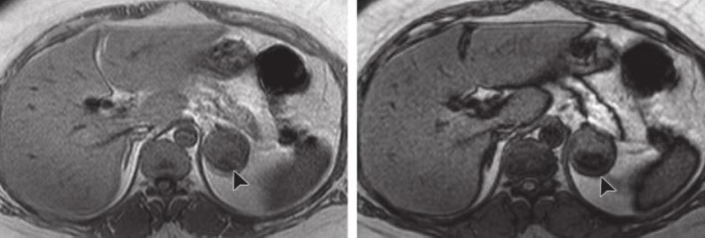
МРТ. Аденома. Т1ВИ. Интрацитоплазматический жир
МР химический сдвиг использует изменения различных прецессионных частот протонов в воде против протонов в жире в пределах того же вокселя и создает совпадающие по фазе и не совпадающие по фазе изображения, в которых сигналы протонов либо суммируются, либо вычитаются друг из друга. Эта последовательность оценивает интрацитоплазматический жир найденный в большинстве аденом. Большинство аденом показывают уменьшение в интенсивности сигнала на несовпадающих по фазе изображениях.
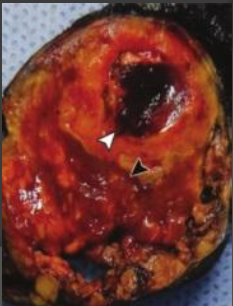
Наличие жира по КТ и МРТ может совпадать mts светлоклеточного почечноклеточного рака, феохромацитомой, раком надпочечника.
10%-40% имеют мало жира (≥10HU), такие аденомы называются “lipid-poor” и считаются неопределенными, необходимо контрастирование (через 1 мин и 15 мин).
Первичный гиперальдостеронизм
Первичный гиперальдостеронизм, требующий оперативного лечения, необходимо дифференцировать от вторичного. Основной тест, позволяющий проводить такой анализ, - оценка активности ренина плазмы. При вторичном гиперальдостеронизме активность ренина очень высокая, тогда как при первичном - очень низкая.
Дифференциальная лабораторная диагностика основных двух форм первичного гиперальдостеронизма сложна. В качестве оценочных тестов исследуют гипокалиемию, проводят маршевую (постуральную) пробу и изучают индекс альдостерон/активность ренина плазмы.
Установлено, что гипокалиемию при идиопатической гиперплазии обоих надпочечников отмечают реже, чем у больных альдостерон-секретирующей аденомой. В качестве ориентира на скрытую гипокалиемию следует использовать ЭКГ. Довольно постоянными, хотя и неспецифическими ЭКГ-признаками гипокалиемии служат частые желудочковые экстрасистолы, удлинение сегмента QRS, снижение интервала S-T, низкий и уплощённый зубец T, выраженный зубец U.
Маршевая проба. Измеряют динамику выработки альдостерона, вызванную четырёхчасовым нахождением в вертикальном положении (концентрацию альдостерона замеряют в 8 ч утра и днём в 12 ч). У здоровых людей и больных двусторонней гиперплазией уровни ренина и альдостерона повышаются, а у больных с односторонней альдостерон-секретирующей аденомой отмечают снижение уровня альдостерона.
В норме индекс альдостерон/активность ренина плазмы не превышает 20. У больных с идиопатической гиперплазией надпочечников индекс повышается в пределах 50, а при продуцирующей альдостерон-секретирующей аденоме он значительно выше 50.
Топические методы исследования дополняют лабораторные в плане дифференциальной диагностики формы первичного гиперальдостеронизма. При КТ альдостерон-секретирующие аденомы определяют в виде небольшой (в среднем от 0,6 до 3,0 см в диаметре) изогенной, реже гипоэхогенной по сравнению с окружающей надпочечниковой тканью округлой опухоли с чёткими контурами. Из-за невысокого содержания холестерина средняя плотность альдостером равна 10,8 ед. Хаунсфилда, которая существенно (на 10-12 ед. Хаунсфилда) отличается от плотности нормальных надпочечников. В дифференциальной диагностике могут возникать затруднения при небольших ( 131 I-19-холестеролом (NP-59) сопоставима с КТ и МРТ, составляя около 90%. Но специфичность этого метода, в том числе в диагностике односторонней микро- и макроузловой гиперплазии, практически абсолютна, приближаясь к 100%. Это очень важное преимущество перед КТ и МРТ, которые вполне закономерно обладают меньшей специфичностью для диагностики не только первичного гиперальдостеронизма, но любых других гормонально-активных опухолей надпочечников. Асимметричное накопление радионуклида в ткани обоих надпочечников позволяет идентифицировать альдостерон-секретирующую аденому. При идиопатической гиперплазии надпочечников после введения радиоизотопа NP-59 отмечают умеренное его поглощение обоими надпочечниками через 72-120 ч.
Радиоизотопная сцинтиграфия позволяет установить локализацию опухолей надпочечников диаметром от 0,5 мм при альдостерон-секретирующей аденоме, а также выявить диффузную, либо диффузно-узловую гиперплазию обоих надпочечников при их идиопатической гиперплазии. Нужно, однако, учесть, что для проведения радиоизотопной сцинтиграфии требуется 5-6 дней, а также обязательная предварительная блокада щитовидной железы, так как NP-59 содержит радиоактивный йод.
В затруднительных клинических случаях, когда не удаётся установить вариант первичного гиперальдостеронизма по клинико-лабораторным и МРТ-данным, целесообразна двусторонняя селективная надпочечниковая флебография с забором крови на альдостерон и ренин. Одностороннее повышение уровня альдостерона в 5-8 раз в сочетании со значительным снижением концентрации ренина на стороне поражённого надпочечника позволяет достоверно диагностировать альдостерон-секретирующую аденому. Выявляемые при двусторонней надпочечниковой гиперплазии симметричные высокие уровни альдостерона (менее чем трёхкратное увеличение) свидетельствуют об идиопатической гиперплазии надпочечников.
Синдром Иценко-Кушинга
С целью выбора оптимального варианта лечения необходим дифференцированный подход к определению формы синдрома Иценко-Кушинга (кортикостерома, болезнь Иценко-Кушинга, АКТГ-эктопический синдром). Клинических дифференциальных признаков, отличающих эти формы синдрома Иценко-Кушинга, нет. Дифференциальная лабораторная диагностика заключается в определении в крови фонового уровня АКТГ до и после проведения стимулирующих тестов, а также оценке уровня 17-оксиглюкокортикоидов в суточной моче после подавления большой дозой дексаметазона (8 мг).
Крайне низкое содержание АКТГ отмечают при кортикостероме, очень высокое - при АКТГ-эктопическом синдроме. При болезни Иценко-Кушинга уровень АКТГ нормальный или повышен. После применения кортикотропина уровень АКТГ повышается при болезни Иценко-Кушинга, что выражается в большей продукции гиперплазированными надпочечниками кортизола. У пациентов с кортикостеромой (адренокортикальной карциномой) и АКТГ-эктопическим синдромом уровень АКТГ и кортизола крови после введения кортикотропина не меняется.
Отсутствие подавления уровня экскреции 17-оксиглюкокортикоидов в суточном количестве мочи, собранной на третьи сутки приёма больным 8 мг дексаметазона, свидетельствует или о кортизол-продуцирующей опухоли надпочечника, или АКТГ-эктопическом синдроме. Снижение уровня 17-оксиглюкокортикоидов в моче на третьи сутки более чем на 50% по сравнению с исходным уровнем указывает на болезнь Иценко-Кушинга. Вместе с тем чувствительность большого дексаметазонового теста в выявлении кортизол-продуцирующей опухоли составила 85,0%, что свидетельствует о необходимости адекватной интерпретации результатов теста с другими гормональными показателями и данными методов топической лучевой диагностики.
Один из эффективных методов морфофункциональной оценки изменений в надпочечниках - сцинтиграфия с 131 I-19-холестеролом (NP-59). Её информативность, по мнению некоторых авторов, достигает 95%. Сцинтиграфию с использованием NP-59 выполняют без дексаметазонового теста на подавление. Изображения могут быть получены на 5-7-й день после введения радиоактивного индикатора. Двустороннее поглощение предполагает надпочечную гиперплазию, а одностороннее, вторичное к контралатеральному, указывает на аденому. Следует отметить, что отсутствие поглощения NP-59 при сцинтиграфии надпочечников связано со злокачественным характером поражения из-за недостатка поглощения радиоактивного вещества новообразованием. Нужно лишь помнить, что есть и другие факторы, приводящие к отсутствию двусторонней визуализации надпочечников (гиперхолестеринемия, лечение глюкокортикоидами). Из-за трудностей использования методики, её дороговизны и вышеназванных причин сцинтиграфия не приобрела популярности даже в зарубежных учреждениях.
В сомнительных случаях топических изменений в надпочечниках (кортикостерома, двусторонняя гиперплазия) показано проведение селективной надпочечниковой флебографии с забором проб крови на кортизол из правого и левого надпочечников. Односторонняя гиперсекреция кортизола, как правило, свидетельствует о кортикостероме, двусторонняя - о гиперплазии надпочечников вследствие их избыточной стимуляции АКТГ.
Отсутствие кортикостеромы в надпочечниках и подавление продукции 17-оксиглюкокортикоидов в моче на третьи сутки более чем на 50% у больного с синдромом Иценко-Кушинга требует исключения кортикотропиномы гипофиза. Оптимальный вариант топической диагностики в таких случаях - МРТ головного мозга (с внутривенным контрастированием гадодиамидом). Такой подход позволяет диагностировать микроаденому гипофиза в 90-95% случаев.
В тех случаях, когда кортикостерома надпочечников исключена и не обнаруживают при МРТ головы микроаденому гипофиза, показано проведение забора крови на АКТГ из нижних каменистых синусов и периферических вен. Путём катетеризации из нижних каменистых синусов твёрдой мозговой оболочки и из периферических вен забирают пробы крови. Соотношение уровня АКТГ в крови синуса к уровню АКТГ в периферических венах больше 2,0 наблюдают при микроаденоме гипофиза, тогда как соотношение менее 1,5 характерно для АКТГ-эктопического синдрома.
Вирильный синдром
Клинические проявления андростеромы могут характеризоваться клинической картиной, в одних случаях сходной с гермафродитизмом, врождённой вирилизирующей гиперплазией коры надпочечников, в других - синдромом и болезнью Иценко-Кушинга с вирильными проявлениями. Маскулинизирующие опухоли яичников также необходимо учитывать при дифференциальной диагностике.
Врождённую вирилизирующую гиперплазию коры надпочечников можно исключить на основании анализа клинических проявлений, отмечаемых сразу после рождения ребёнка. Показательна реакция при проведении большого дексаметазонового теста по Лиддлю: у больных с врождённой вирилизирующей гиперплазией коры надпочечников отмечают выраженное снижение экскреции 17-оксиглюкокортикоидов с мочой. Визуализация надпочечников при врождённой вирилизирующей гиперплазии коры надпочечников не выявляет их опухолевого роста.
При синдроме и болезни Иценко-Кушинга, несмотря на нередко имеющиеся вирильные проявления, доминирует картина гиперкортизолизма с характерными для него признаками. При андростероме, как правило, не бывает гипокалиемии, миастенического синдрома, стрий на животе и бёдрах, остеопороза, высокой артериальной гипертензии.
Маскулинизирующие опухоли половых желёз (арренобластома, лейдигома и др.) имеют клиническую картину, сходную с клинической картиной андростеромы. В крови и моче определяют повышение дегидроэпиандростерона, тестостерона, 17-оксиглюкокортикоидов. При УЗИ, КТ и МРТ выявляют опухоль яичников, что служит определяющим фактором при дифференциальной диагностике андростеромы.
Похожие темы научных работ по клинической медицине , автор научной работы — Шингареева Л.А., Байков Д.Э., Ряховский А.Е., Васкаева Г.Р.
Аспирант III года обучения кафедры общей хирургии БГМУ
Профессор кафедры общей хирургии БГМУ
Аспирант III года обучения кафедры патологической физиологии БГМУ
Студентка V курса лечебного факультета
Е-mail: gulnaz.vaskaeva@gmail. com АДЕНОМАТОИДНАЯ ОПУХОЛЬ НАДПОЧЕЧНИКОВ
Аденомы надпочечников обычно являются доброкачественными новообразованиями мезотелиального происхождения. Встречаются у мужского и женского пола в одинаковых соотношениях. Есть случаи, когда аденоматоидные опухоли встречаются в печени, кишечной брыжейки, поджелудочной железе и т.д. Первая аденоматоидная опухоль была описана в 1945 году Голденом. За последние годы объемные образования надпочечников стали диагностировать все чаще. Это связано с модернизацией диагностических технологий. На сегодняшний день, благодаря КТ, МРТ, ПЭТ исследованиям злокачественные образования своевременно обнаруживается на ранних стадиях. В настоящей статье рассматривается клинический случай образования надпочечника.
В Клинику поступила пациентка К. 30 лет. При УЗИ обследовании брюшной полости визуализировали образование надпочечника без клинических симптомов. Она была госпитализирована в клинику эндокринологии для дообследования.
При анализе лабораторных показателей было установлено: уровень натрия, калия в крови в пределах нормы, уровень кортизола с утра составлял 890 нмоль /л (нормальный 55-690 нмоль /л) и 39 нмоль /л после 1 мг дексаметазона, показывающий ответ на снижение кортизола.
При проведении компьютерной томографии установлено: в области латеральной ножки правого надпочечника, выходя на контур, визуализировалось образование изоденсивной плотности размерами не превышающее 20х15мм. представляла собой образование округлой формы, с четкими ровными контурами, неоднородной структуры. Увеличенных лимфоузлов не выявлено. При внутривенном усилении в артериальную фазу отмечалось быстрое накопление контрастного препарата, в венозную, отсроченную фазу быстрое вымывание контраста и повышением плотностью на 50% HU. Исходя из вышесказанного, был верифицировано заключение: гормононеакивная аденома надпочечника.
Было принято решение о хирургическом вмешательстве, как и лечение выбора, проводилось по размеру опухоли (>6см). Пациентка прошла лапароскопическую правостороннюю адреналэктомию без осложнений. На данный момент не наблюдается рецидива опухоли или метастатического заболевания, на ранних последующих наблюдениях.
Аденоматоидные опухоли надпочечников происходят из мезотелиальных остатков в надпочечниковой железе. Во время эмбриогенеза существует связь между надпочечниками и муллерианским трактом, поэтому мезотелиальные остатки могут присутствовать в надпочечниках. Возраст образований колеблется от 24 до
64 лет, с пиковым заболеванием в четвертые десятилетия. Эти опухоли в основном нефункциональные, бессимптомные и обнаруживаются случайно, во время лучевых обследований. Некоторые из них проявляют гормональную активность. Иногда пациенты могут проявлять клинические симптомы, такие как: увеличение массы тела, верилизация, повышение артериального давления. Для обнаружения этих образований используются различные радиологические методы, включая ультразвуковое исследование, компьютерное томографию, магнитно-резонанснную томографию, ПЭТ. Единственный способ подтвердить структуру образования - это гистологический метод. При необходимости проводится хирургическое лечение. Выводы
Адреноматоидная опухоль надпочечников - редкое доброкачественное новообразование, которое следует добавлять в дифференциальную диагностику любой надпочечниковой опухоли, возникающей в надпочечниковой железе. Гистологические и иммуногистохимические профили очень благоприятны для достижения диагноза этой доброкачественной опухоли происхождения мезотелиальных клеток, что помогает избежать инвазивного лечения.
Список использованной литературы
1. Wachter DL, Wunsch PH, Hartmann A, Agaimy A. Adenomatoid tumors of the female and male genital tract. A comparative clinicopathologic and immunohistochemical analysis of 47 cases emphasizing their site-specific morphologic diversity. Virchows Arch 2011;458:593-602. [PubMed]
2. Travis WD, Lack EE, Azumi N, et al. Adenomatoid tumor of the adrenal gland with ultrastructural and immunohistochemical demonstration of a mesothelial origin. Arch Pathol Lab Med 1990;114:722-724. [PubMed]
3. Golden A, Ash JE. Adenomatoid tumors of the genital tract. Am J Pathol 1945;21:63-79. [PMC free article][PubMed]
4. Evans CP, Vaccaro JA, Storrs BG, Christ PJ. Suprarenal occurrence of an adenomatoid tumor. J Urol1988;139:348-9. [PubMed]
5. Rodrigo Gasque C, Marti-Bonmati L, Dosda R, Gonzalez Martinez A. MR imaging of a case of adenomatoid tumor of the adrenal gland. Eur Radiol 1999;9:552-4. [PubMed]
6. Zhao M, Li C, Zheng J, et al. Cystic lymphangioma-like adenomatoid tumor of the adrenal gland: report of a rare case and review of the literature. Int J Clin Exp Pathol 2013;6:943-50. [PMC free article] [PubMed]
7. Krstevska B, Dimitrovski C, Pemovska G. Evaluation the methods in decision- making for surgery of adrenal incidentalomas. Maced Med J 2003.
8. Raaf HN, Grant LD, Santoscoy C, et al. Adenomatoid tumor of the adrenal gland: a report of four new cases and a review of the literature. Mod Patholan Off J United States Can AcadPathol Inc 1996;9:1046-51. [PubMed]
9. Chung-Park M, Yang JT, McHenry CR, Khiyami A. Adenomatoid tumor of the adrenal gland with micronodular adrenal cortical hyperplasia. Hum Pathol 2003;34:818-21. [PubMed]
10. Simpson PR. Adenomatoid tumor of the adrenal gland. Arch Pathol Lab Med 1990;114:725-7. [PubMed]
11. Denicol NT, Lemos FR, Koff WJ. Adenomatoid tumor of supra-renal gland. Int Braz J Urol 2004;30:313-5. [PubMed]
12. Hamamatsu A, Arai T, Iwamoto M, et al. Adenomatoid tumor of the adrenal gland: case report with immunohistochemical study. Pathol Int 2005;55:665-9. [PubMed]
ПРОФИЛАКТИКА ЗАБОЛЕВАНИЙ: УЧАСТИЕ ФАРМАЦЕВТИЧЕСКИХ РАБОТНИКОВ
В условиях снижающейся доступности медицинской помощи, особенно в сельской местности, и возрастающей хронизации заболеваний реализация Государственной программы Российской Федерации "Развитие здравоохранения" возможна только при объединении усилий медицинских и фармацевтических работников.
Провизор, профилактика заболеваний, санитарно-просветительная работа, информационно-консультационно-обучающие услуги
Профилактика - комплекс мероприятий, направленных на сохранение и укрепление здоровья и включающих в себя формирование здорового образа жизни, предупреждение возникновения и (или) распространения заболеваний, их раннее выявление, выявление причин и условий их возникновения и развития, а также направленных на устранение вредного влияния на здоровье человека факторов среды его обитания [4].
Профилактика является одним из основных принципов охраны здоровья в нашей стране [4, ст. 4 п.8]. При этом профилактика неинфекционных заболеваний предусматривается на популяционном, групповом и индивидуальном уровнях, а формирование здорового образа жизни у граждан (начиная с детского возраста) - с помощью мероприятий по информированию о факторах риска для здоровья, мотивации к ведению здорового образа жизни и т. д. [ 4, ст.30].
Общероссийский классификатор занятий свидетельствует, что к специалистам в области здравоохранения высшего уровня квалификации (код 22) относятся провизоры (код 2262), к среднему медицинскому персоналу здравоохранения (код 32) - фармацевты (код 3213). Таким образом, профессиональная деятельность фармацевтических работников осуществляется в единой системе с врачами, фельдшерами и т.д., курируемой Министерством здравоохранения Российской Федерации.
Министерство здравоохранения Российской Федерации (МЗ РФ), являясь федеральным органом исполнительной власти, осуществляет функции по выработке и реализации государственной политики и
- Что такое Гормонально-неактивные опухоли надпочечников (инциденталомы)
- Диагностика Гормонально-неактивных опухолей надпочечников (инциденталом)
- Лечение Гормонально-неактивных опухолей надпочечников (инциденталом)
Что такое Гормонально-неактивные опухоли надпочечников (инциденталомы)
Опухоли надпочечников, не приводящие к развитию характерных клинических признаков гиперкортицизма, первичного гиперальдостеронизма, феохромоцитомы, феминизирующей или вирилизирующей опухоли, долгое время считались сравнительно редкими образованиями. Они являются, как правило, случайной находкой при выполнении УЗИ, КТ или МРТ органов брюшной полости и забрюшинного пространства, предпринятых по поводу других заболеваний. Применяемый в таких случаях термин "инциденталома" или "адреналома" подчеркивает, что опухоль выявлена случайно и клинически асимптоматична. Частота обнаруженных таким образом опухолей надпочечников неуклонно возрастает и колеблется в пределах 1,5-10%. Обычно они встречаются в возрасте 30-60 лет, чаще у женщин и в 60% имеют левостороннюю локализацию. В 3-4% наблюдений опухоль выявляют в обоих надпочечниках. Среди всех больных, находящихся на обследовании по поводу различных заболеваний надпочечников, частота инциденталом достигает 18-20%. По данным секционных статистик, случайно выявленные опухоли надпочечников встречаются в 1,5-8,7% наблюдений.
При выявлении инциденталомы дальнейшую дифференциальную диагностику проводят среди следующих основных групп заболеваний:
- первичное поражение самих надпочечников (опухоли, гиперпластические изменения, кисты, гематомы и др.);
- вторичное, метастатическое поражение надпочечников (метастазы рака легких, молочной железы, щитовидной железы, толстой кишки, почки, меланомы и др.) - 8-13%;
- псевдонадпочечниковые поражения, имитирующие опухоль надпочечников (заболевания почек, тела и хвоста поджелудочной железы, селезенки, расположенных рядом крупных сосудов и др.).
Важно помнить о возможности патологических изменений в эктопированной надпочечниковой ткани.
Среди заболеваний надпочечников наиболее часто выявляют аденомы коркового вещества (около 30%), аденоматоз или диффузно-узелковую гиперплазию коры надпочечника, феохромоцитому (10%), намного реже встречаются кисты (ретенционные, паразитарные) и псевдокисты надпочечников (менее 0,08%), липомы, миелолипомы (менее 0,2%), лимфомы, сосудистые опухоли надпочечников и др. Ежегодная частота рака коры надпочечников обычно не превышает 2 наблюдений на 1 млн населения (0,02-0,04% всех злокачественных опухолей).
В топической диагностике наибольшее значение придают полипозиционному УЗИ (при необходимости в сочетании с тонкоигольной аспирационной биопсией), КТ, МРТ, селективной ангиографии (артериографии, флебографии). Реже используют радионуклидную сцинтиграфию ( 111 I либо 123 I-метайодбензилгуанидин, избирательно накапливающийся в хромаффинной ткани, радиофармпрепарат NP-59 или 131 I-19-йодхолестерол, накапливаемый гиперфункционирующей корковой тканью).
Комплексное применение методов топической диагностики (УЗИ, КТ, МРТ) позволяет выявить опухолевые изменения надпочечников размером 5 мм.
Для дифференциальной диагностики злокачественных кортикостером используют иммуногистохимические реакции: положительную реакцию с Р-53 и отсутствие моноклональных антител к кератинам. Одним из онкомаркеров считают дегидроэпиандростерона сульфат (ДГЭАС), уровень которого при раке коры надпочечников обычно повышен. Следует отметить, что в ряде случаев случайно выявленные гормонально-неактивные опухоли надпочечников на самом деле проявляют некоторую гормональную активность, которая, однако, не приводит к появлению заметных клинических симптомов (так называемый преклинический синдром Кушинга, альдостеромы, феохромоцитомы и др.). Для оценки функциональной активности выявленной опухоли определяют содержание свободного кортизола, катехоламинов, альдостерона, ванилилминдальной кислоты и гомованилиновой кислоты в суточной моче, применяют малую дексаметазоновую пробу. Даже при отсутствии клинических признаков эндогенного гиперкортицизма и нормальном уровне кортизола в суточной моче и крови, но отсутствии суточного ритма его секреции и подавлении секреции дексаметазоном следует предположить преклинический синдром Кушинга. В сложных диагностических случаях функциональную активность опухоли оценивают по результатам селективной надпочечниковой флебографии с определением уровня гормонов в оттекающей венозной крови (важно помнить о возможности развития криза при наличии феохромоцитомы и исключить ее до исследования).
Выявление гормональной активности опухоли является показанием к операции. Подлежат хирургическому удалению и образования, превышающие 3 см в диаметре при отсутствии гормональной активности. Опухоли меньшего размера, но имеющие признаки злокачественного роста (быстрый рост, неоднородность ткани, неровность и нечеткость контуров, наличие микрокальцинатов, обильная васкуляризация, атипичные клетки при тонкоигольной аспирационной биопсии и др.), также подлежат оперативному лечению в специализированном стационаре. Динамическое наблюдение за больным со случайно выявленными опухолями надпочечников оправдано при небольших размерах образований (менее 3 см), отсутствии признаков злокачественного роста и гормональной активности.
Таким образом, термины "инциденталома" или "адреналома" являются собирательными понятиями и указывают на то, что выявленная (чаще случайно) опухоль не привела к развитию типичной клинической картины эндогенного гиперкортицизма, первичного гиперальдостеронизма, феохромо-цитомы, феминизирующей или вирилизирующей опухоли. Этот диагноз должен рассматриваться лишь как предварительный (рабочий) и нацеливать врача на применение определенного алгоритма исследований с целью установления клинического диагноза и принятия оптимального решения о тактике ведения больного (операция, наблюдение).

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
- Код по МКБ-10
- Эпидемиология
- Причины
- Симптомы
- Стадии
- Формы
- Диагностика
- Что нужно обследовать?
- Как обследовать?
- Дифференциальная диагностика
- Лечение
- К кому обратиться?
- Прогноз
Опухоли надпочечника выявляют в 1-5% наблюдений при КТ живота, выполненной по другим показаниям. Однако только 1% опухолей имеет злокачественный характер.
Код по МКБ-10
Эпидемиология
Заболеваемость раком надпочечника составляет 0,6-1,67 на 10 6 человек в год. Соотношение женщин и мужчин - 2,5-3:1. Наибольшую заболеваемость раком надпочечника регистрируют в возрасте до 5 и в 40-50 лет.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Причины опухолей надпочечника
Опухоли надпочечника разделяют на спорадические и ассоциированные с наследственными синдромами [синдромы Gardner, Beckwith-Wiedemann, множественной эндокринной неоплазии 1-го типа, SBLA (саркома, рак молочной железы, лёгкого и надпочечника), Li-Fraument].
В зависимости от гистогенеза выделяют опухоли коры надпочечника (альдостерома, кортикостерома, андростерома, кортикоэстрома, смешанные опухоли надпочечника, аденома, рак) и мозгового вещества надпочечников (феохромоцитома), а также первичную надпочечниковую лимфому, саркому, вторичные (метастатические) опухоли надпочечника.
Для злокачественных опухолей надпочечника характерен местно-деструирующий рост с вовлечением в процесс соседних органов (почка, печень), а также инвазией венозной системы с формированием опухолевого венозного тромбоза (надпочечниковой и нижней полой вен). Диссеминация опухолей происходит лимфогенным и гематогенным путями. При этом поражаются забрюшинные лимфатические узлы, лёгкие, печень и кости.

[11], [12]
Симптомы опухолей надпочечника
Симптомы опухоли надпочечника складываются из проявлений первичной опухоли (пальпируемое образование, боль, лихорадка, снижение массы тела), её метастазов (симптомы опухоли надпочечника определяются локализацией отсевов опухоли) и эндокринных симптомов. Гормонально активный рак надпочечников составляет 60% всех наблюдений и может вызывать следующие эндокринные синдромы: синдром Кушинга (30%), вирилизация и преждевременное половое созревание (22%), феминизация (10%), первичный гиперальдостеронизм (2,5%), полицитемия (менее 1%), гиперкалиемия (менее 1%), гипогликемия (менее 1%), надпочечниковая недостаточность (характерно для лимфомы), резистентность к инсулину, не связанная с глюкокортикоидами, катехоламиновый криз (характерно для феохромоцитомы), кахексия.

[13], [14], [15]
Стадии
- Стадия 1 - T1N0M0.
- Стадия 2 - T2N0M0.
- Стадия 3 - Т1 или Т2. N1M0.
- Стадия 4 - любая Т, любая N+M1 или ТЗ, N1 или Т4.

[16], [17], [18], [19], [20]
Формы
На основании признака секреции гормонов коры надпочечников (глюкокортикоиды, минералокортикоиды, андрогены, эстрогены) выделяют функционально активные и неактивные опухоли надпочечника. Более чем в 50% случаев рак коры надпочечников функционально не активен, однако злокачественные опухоли надпочечника вызывают в 5-10% случаев синдром Кушинга.
Т - первичная опухоль:
- Т1 - опухоль 5 см в диаметре и менее, нет местной инвазии;
- Т2 - опухоль более 5 см в диаметре без локальной инвазии;
- Т3 - опухоль любого размера, есть локальная инвазия, нет прорастания соседних органов;
- Т4 - опухоль любого размера, есть локальная инвазия, есть прорастание соседних органов.
N - регионарные метастазы:
- N0 - нет регионарных метастазов;
- N1 - есть регионарные метастазы.
М - отдалённые метастазы:
- М0 - нет отдалённых метастазов;
- Ml - есть отдалённые метастазы.

[21], [22], [23]
Диагностика опухолей надпочечника
Обследование больных опухолями надпочечника, помимо рутинных лабораторных исследования (общий, биохимический анализы крови, коагулограмма, общий анализ мочи), должно включать тесты, направленные на выявление повышенной продукции гормонов. Для выявления синдрома Кушинга используют дексаметазоновую пробу (1 мг) и определение экскреции кортизола в моче (24 часа).
При гиперальдостеронизме оценивают концентрацию и соотношение альдостерона и ренина; при вирилизации - сывороточный уровень надпочечниковых андрогенов (андростендион, дигидроэпиандростерон сульфат) и тестостерона, а также экскрецию 17-кетостероидов в моче (24 часа); при феминизации - концентрация эстрадиола и эстрона в плазме. Для исключения феохромоцитомы необходима оценка суточной экскреции катехоламинов (эпинефрин, норэпинефрин, допамин) и их метаболитов в моче (особенно метанефрин и норметанефрин), а также уровня сывороточных метанефрина и катехоламинов.
Радиологическая диагностика опухолей надпочечника включает КТ или МРТ живота (оценка размеров и синтопии первичной опухоли, выявление метастазов), а также рентгенографию или КТ грудной полости (выявление метастазов). Радиологические признаки рака надпочечника - неправильная форма опухоли надпочечника, её размер более 4 см, высокая плотность при КТ, превышающая 20 HU, гетерогенная структура, обусловленная геморрагиями, некрозами и кальцинатами, а также инвазия окружающих структур.
Рутинное выполнение биопсии с целью верификации диагноза до начала лечения при опухолях надпочечников не рекомендуют.

[24], [25], [26], [27]
Что нужно обследовать?
Как обследовать?
Дифференциальная диагностика
Дифференциальная диагностика опухолей надпочечника проводится с нейробластомой и нефробластомой у детей и гамартомами, тератомами, нейрофиброматозом, амилоидозом и гранулёмами надпочечников у взрослых.
К кому обратиться?
Лечение опухолей надпочечника
Лечение опухолей надпочечника, а особенно гормонально активных опухолей заключается в их удалении. Исключить злокачественную природу гормонально неактивного локализованного новообразования до начала лечения сложно. У взрослых вероятность злокачественного характера опухолей менее 6 см низка. В подобных случаях возможно тщательное динамическое наблюдение. При новообразованиях большего диаметра. а также малых опухолях надпочечника у детей показано оперативное лечение. Стандартным объёмом операции является адреналэктомия, при маленьких гормонально неактивных опухолях может выполняться резекция надпочечника. Рутинно используют лапаротомный доступ, однако при небольших новообразованиях без признаков местной инвазии возможно выполнение лапароскопической адреналэктомии без ущерба онкологическим результатам.
Рак надпочечника - радиорезистентная опухоль, её чувствительность к химиотерапии низка. Единственный эффективное лечение данной категории больных - оперативный. Частота местных рецидивов после операции высока (80%). Оптимальный подход к лечению локальных рецидивных опухолей у больных, не имеющих отдалённых метастазов, - оперативный. Назначение адъювантной химиотерапии и облучения радикально оперированным больным не улучшает результатов лечения.
При диссеминированном раке надпочечника продемонстрирована умеренная эффективность митотана в дозе 10-20 г/сут, длительно (частота объективных ответов 20-25%, контроль гиперсекреции гормонов - 75%). Опубликованы данные, свидетельствующие о возможном увеличении безрецидивной выживаемости при использовании режима митотан (10-20 г/сут, длительно). В качестве второй линии химиотерапии у больных, не ответивших на лечение митотаном, используют режимы, основанные на цисплатине (цисплатин, циклофосфамид, 5-фторурацил). Немаловажную роль в лечении опухолей надпочечников играет симптоматическая терапия, направленная на ликвидацию эндокринных симптомов гормонально-активных опухолей. При синдроме Кушинга используют митотан, кетоконазол, мифепристон и этомидат в режиме монотерапии или различных комбинациях.
Гиперальдостеронизм служит показанием к назначению спиронолактона, амилорида, триамтерена и антигипертензивных препаратов (блокаторы кальциевых каналов). При гиперандрогении используют стероидные (ципротерон) и нестероидные (флутамид) антиандрогены. кетоконазол, спиронолактон и циметидин; при гиперэстрогении - антиэстрогены (кломифен, тамоксифен, даназол). Надпочечниковая недостаточность требует проведения гормонозаместительной терапии. При смешанных карциномах с феохромоцитомным компонентом возможно применение препаратов радиоактивного метайодобензилгуанидина. Повышение артериального давления, в том числе при феохромоцитоме, служит показанием к назначению альфа-адреноблокаторов с последующим применением бета-адреноблокаторов (пропранолол).
Прогноз
Доброкачественные опухоли надпочечника имеют благоприятный прогноз. Общая 5-летняя выживаемость при раке надпочечника составляет 20-35%. Прогноз больных гормонально-активными опухолями лучше, чем при эндокринно-неактивных формах заболевания, что связано с ранним выявлением и своевременным лечением новообразований, продуцирующих гормоны. Общая 5-летняя выживаемость радикально оперированных больных достигает 32-47%, неоперированных пациентов с местнораспространёнными опухолями - 10-30%; среди больных диссеминированным раком надпочечника ни один не переживает 12 мес.

[28], [29], [30], [31], [32], [33]
Читайте также:

