Удаление лимфомы хирургическим путем
У вас появился жировик (в медицине его называют липомой)? Тогда вам обязательно стоит показаться хирургу. Специалист, как правило, быстро диагностирует образование и даст совет, как действовать дальше. И если даже липома небольшая, она все равно представляет косметический дефект.
Хирургическое удаление
Специалист может предложить воспользоваться менее травматичной и более щадящей малоинвазивной хирургией. В этом случае разрез на коже будет до одного сантиметра в длину.
Где сделать операцию
От чего зависит стоимость
Цены зависят от ряда факторов, но в первую очередь от размера образования и его расположения, а также квалификации хирурга. Следует также помнить, что существуют так называемые множественные липомы, на удаление которых у хирурга уходит больше времени и сил.
Что еще надо знать
Обычно размер жировика не превышает трех сантиметров в диаметре, однако некоторые вырастают и в четыре раза больше.
Появляются образования на любой части тела и обычно располагаются под кожей, но некоторые вырастают на внутренних органах. Если образование мешает нормальному функционированию органа, его удаляют немедленно.
В ряде случаев, для того чтобы поставить исчерпывающий диагноз, пациенту делают УЗИ, рентген или компьютерную томографию. При удалении фрагмент обязательно отправляют на дополнительное исследование.
Считается, что липома не трансформируется в злокачественную опухоль, однако иногда такое перерождение все же происходит. В частности, очень внимательными надо быть женщинам. Например, липома молочной железы может трансформироваться в липосаркому. Такая ситуация требует постоянного наблюдения, и если хирург советует ее удалить, то лучше пойти на операцию, а не играть с огнем. Кстати, у женщин жировики встречаются чаще, чем у мужчин.
Но есть совет, который пригодится и женщинам, и мужчинам. Если обнаружили даже небольшую липому, не тяните с обращением к врачу, которому вы доверяете. Он обязательно покажет путь к здоровью.
Стоимость услуг
| Наименование услуги | Цена, руб. |
|---|---|
| Прием врача хирурга первичный, амбулаторный (сбор анамнеза и жалоб, осмотр, пальпация, назначение обследования) | 2200 |
| Прием врача хирурга повторный, амбулаторный (осмотр, интерпретация результатов лабораторных и инструментальных методов обследования, назначение лечения) | 2200 |
| Консультация врача хирурга, кандидата медицинских наук | 2500 |
| Консультация врача хирурга, доктора медицинских наук, профессора | 3100 |
| Прием врача хирурга для интерпретации результатов обследования, проведенного в другом медицинском учреждении | 3400 |
| Консультация анестезиолога | 2200 |
| Удаление липомы урогенитальной области | 3000 |
| Удаление липомы, в том числе нагноившейся | от 5 000 |
| Удаление липом при липоматозе | от 9 000 |
Хирургический метод оказывает положительное действие у больных с локализованным процессом, особенно при поражении илеоцекального отдела кишечника при угрозе или возникшем осложнении (перфорация, кровотечение), и заключается в резекции илеоцекального угла или правосторонней гемиколэктомии. При полностью удаленной НХЛ у больного имеются большие шансы на выздоровление при меньшей интенсивности и продолжительности лечения. С другой стороны, важно иметь в виду, что выполнение неоправданно тяжелых и обширных оперативных вмешательств может привести к отсрочке химиотерапии, что будет способствовать генерализации процесса и ухудшению прогноза заболевания.
В случае предполагаемой радикальной операции хирург должен:
1) выполнить операцию таким образом, чтобы имелась возможность своевременно начать химиотерапию;
2) убедиться в том, что опухоль не прорастает жизненно важные органы; при этом необходимо помнить, что хирургическое удаление больших участков кишки, почек, матки, яичников, селезенки, легкого и пр. является серьезной ошибкой, так как специфическая инфильтрация этих органов, как правило, подвергается обратному развитию на фоне химиотерапии;
3) быть уверенным в том, что риск операции не чрезмерен и через 3—5 дней ребенок сможет начать лечение;
4) иметь информацию, что у больного нет поражения костного мозга и/или ЦНС — в противном случае показана лишь биопсия опухоли.
В случае полного удаления опухоли проводят тщательную ревизию брюшной полости и удаляют лимфатические узлы более 1 см в диаметре. Операция считается нерадикальной, если не удалось удалить регионарные или отдаленные лимфатические узлы более 1 см в диаметре при макроскопически резецированной опухоли.
В ряде случаев для принятия решения об объеме оперативного вмешательства у больных НХЛ и с целью проведения дифференциальной диагностики с другими новообразованиями инграоперационно выполняются отпечатки на стекле со срочным цитологическим исследованием опухолевых клеток.
При выполнении биопсии хирург обязан:
1) вместе с онкогематологом определить, какие лимфатические узлы выбрать для биопсии. Типичной ошибкой является удаление наиболее легкодоступного образования, в то время как пораженные узлы могут располагаться более глубоко;
2) взять достаточное количество материала для необходимых исследований; целесообразно удалять не менее двух лимфатических узлов (вместе с капсулой) размером более 1,5 см в диаметре и плотных на ощупь; для выполнения отпечатков узел разрезают вдоль, при этом плоскость разреза должна проходить через ворота лимфатического узла;
3) бережно относиться к биоптату, помня, что разрушенные ткани непригодны для исследования;
4) путем тщательной ревизии определить объем и распространенность опухолевого процесса.
У больных с локализацией неходжкинских лимфом в средостении торакотомию или медиастинотомию выполняют лишь при отсутствии увеличенных периферических лимфатических узлов, плеврального выпота или поражения костного мозга. При этом операция заключается в биопсии, так как хирургический метод не является лечебной процедурой при лимфомах средостения.
Повторная операция показана больным с локальной НХЛ, сохраняющейся после проведения индуктивной химиотерапии для дифференциальной гистологической диагностики между резидуальной опухолью и фиброзными изменениями. При обнаружении небольшой резидуальной опухоли и отсутствии поражения костного мозга и ЦНС ее по возможности удаляют.
Тактика лечения крупноклеточных анапластических лимфом зависит от стадии заболевания и группы риска и в основном совпадает с таковой при В-клеточных НХЛ.
Тактика сопроводительной терапии при лечении не-В- и В-клеточных неходжкинских лимфом у детей. В настоящее время разработан целый комплекс мер, позволяющих уменьшить частоту и тяжесть побочных реакций и осложнений во время проведения химиотерапии НХЛ у детей.
Принципы сопроводительной терапии:
- обеспечение надежного долгосрочного центрального венозного доступа с помощью туннелизируемых катетеров;
- обеспечение возможности адекватной заместительной терапии тромбоконцентратами для поддержания уровня тромбоцитов >20 000/мкл, а при появлении абдоминальной симптоматики или пневмонии — >50 000/мкл;
- проведение селективной оральной деконтаминации, включающей антибиотики, антимикотики, а также профилактику мукозита с первых дней циторедуктивной фазы;
- для лечения инфекционных осложнений в период нейтропении — применение цефалоспоринов III генерации с антипсевдомонадной активностью (фортум, цефобид, цефтриаксон) и/или В-лактамных пенициллинов с аминогликозидами, метронидазола, амфотерицина-В;
- проведение парентерального питания (частичного или полного) при невозможности продолжить полноценное энтеральное, при потере массы тела >10 %, подозрении на нейтропенический энтероколит.
В начале лечения главную опасность представляют синдром лизиса опухоли и развитие мочекислой нефропатии с острой почечной недостаточностью. Главным условием предупреждения развития токсических реакций, вызванных этим синдромом, является применение массивной инфузионной терапии в дозе 3000 мл/м2 в сутки (125 мл/м2 в час) в составе: 5 % глюкоза — 1500 мл/м2 в сутки; 0,9 % NaCl — 1320 мл/м2 в сутки; 4 % NaHC03 — 180 мл/м2.
Диурез стимулируется введением лазикса. В профилактике мочекислой нефропатии важную роль играет назначение аллопуринола в дозе 300 мг/м2 в 3 приема в сутки (10 мг/кг), в первые 3—8 дней лечения.
Тромбоконцентрат переливается для поддержания количества тромбоцитов на уровне 50 • 109/л, позволяющем избежать кровотечения (особенно в случаях высокого бластного лейкоцитоза).
Эритроцитная масса переливается для поддержания гематокрита на уровне 30 %, исключая случаи с инициальным гиперлейкоцитозом, когда трансфузия эритроцитной массы может резко повысить риск церебрального лейкостаза.
Инфекционные осложнения могут появиться на любом этапе лечения, однако наиболее опасны при развитии агранулоцитоза в периферической крови (с количеством гранулоцитов ниже 500/м3).
При развитии агранулоцитоза в периферической крови необходимы изоляция ребенка и проведение соответствующей терапии.
Иммунология, иммунотерапия и иммунокоррекция при НХЛ
Известно, что неходжкинская лимфома является опухолью иммунной системы. Проведенные исследования иммунной системы позволили обнаружить у больных детей существенные нарушения Т- и В-клеточного звена иммунитета, которые еще более усугубляются у больных после применения интенсивной химиотерапии. При обследовании детей с НХЛ до начала химиотерапии было обнаружено, что содержание Т-лимфоцитов было снижено у 76,8 % больных, а функциональная активность лимфоцитов была подавлена в 2,5 раза у 90,2 % больных НХЛ по сравнению с группой здоровых детей. Кроме того, у 71,3 % больных отмечено снижение содержания В-лимфоцитов периферической крови, а также уровня иммуноглобулинов А и М классов соответственно в 96,3 и 87,4 % случаев.
В результате изучения у больных неходжкинской лимфомой синтеза интерферона отмечено нарушение способности мононуклеаров периферической крови вырабатывать гамма- и альфа-интерферон, что проявляется в виде синдрома недостаточности интерферона, ведущего к нарушениям иммунного ответа. При изучении прогностического значения способности мононуклеаров периферической крови вырабатывать гамма-интерферон на течение НХЛ выяснилось, что эта способность была снижена в 2 раза у больных, умерших в течение первого года от начала заболевания в связи с прогрессированием процесса, по сравнению с детьми, у которых в последующем имелось безрецидивное течение НХЛ более 1 года, а титр выработки гамма-интерферона у них составил 253,24 ЕД/мл.
В настоящее время доказано, что интерферон обладает антивирусным, антипролиферативным, противоопухолевым и антиметастатическим действием.
С целью улучшения выживаемости детей, больных неходжкинской лимфомой и находившихся в полной ремиссии, показана интерферонотерапия и иммунокоррекция препаратом тактивин, что приводит к повышению 2- и 5-летней выживаемости больных, получавших такое лечение.
При сравнении различных препаратов выяснилось, что наилучшие показатели 2- и 5-летней безрецидивной выживаемости были у больных, получавших реаферон в сочетании с тактивином, а наихудшие — у больных, получивших только человеческий лейкоцитарный интерферон.
Учитывая эти данные, нужно считать оправданным применение у детей, больных НХЛ, под контролем иммунного статуса различных иммуномодуляторов (тактивин, имунофан; витамины группы А — бета-каротин; витамин С), а также гамма- и альфа-интерферона.
Контроль за состоянием иммунитета и выработки интерферона, а также применение иммуностимуляторов будут способствовать уменьшению частоты инфекционных осложнений, рецидивов заболевания и повышению выживаемости больных.
Рецидивы при НХЛ у детей
Перед началом лечения рецидива НХЛ необходимо точно установить его существование. Некоторые состояния могут симулировать наличие лимфомы. Так, большие проблемы могут возникнуть у больных с крупными абдоминальными опухолями или опухолями средостения в момент диагностики. После проведения противоопухолевой терапии эти новообразования могут сократиться в размерах, но не исчезнуть полностью.
При повторной биопсии очень часто выявляют фиброзные или жировые изменения без наличия жизнеспособной ткани. Однако такие явления чаще всего обнаруживаются у пациентов с нодулярной лимфомой, в которой коллагеновое вещество не изменяется под воздействием лечения. Лучевая терапия в случае ее применения у больных с резидуальным процессом может еще более усложнить ситуацию, приводя к усилению фиброза, особенно в легочной ткани, прилегающей к средостению.
Другая проблема может быть связана с плевральным выпотом. Необходимо тщательное исследование плевральной жидкости у больных с негативными цитологическими данными в отношении злокачественного процесса. В этих случаях целесообразно изучить поверхностные маркеры, применить проточную цитометрию и в ряде случаев использовать цитогенетические методы. При этом следует помнить, что констриктивный перикардит как осложнение лучевой терапии может симулировать злокачественный процесс. Однако в этом случае жидкость будет иметь характеристики транссудата.
При подозрении на рецидив лимфомы необходимо предпринять попытку биопсии резидуальной опухоли. При этом можно выполнить эксцизионную биопсию или, при локализации процесса в брюшной полости, игловую аспирационную биопсию.
При лечении неходжкинской лимфомы по различным интенсивным программам рецидивы возникают не часто: при В-НХЛ — у 9,5 %, а при Т-НХЛ — у 16 % больных. У детей с В-клеточной НХЛ большинство рецидивов выявляется в первые 6—8 мес, а после года вероятность их выявления практически равна нулю. При Т-клеточной НХЛ наиболее часто рецидивы диагностируются в первые 2 года, затем частота их с каждым годом уменьшается.
Обычно рецидив возникает не в области первичного очага, а в костном мозге или ЦНС. При этом возможно изолированное поражение головного мозга.
Несмотря на высокую чувствительность лимфомы Беркитта к химио- и лучевой терапии, прогноз у рецидивных больных до последнего времени был неудовлетворительным и длительная выживаемость почти не отмечалась. Успехи появились лишь с момента применения высокодозной химиотерапии в сочетании с трансплантацией аутологичного костного мозга (АуТКМ).
После того как была показана взаимосвязь дозы и эффекта, появились подтверждающие это мнение исследования с использованием различных химиотерапевтических режимов. При этом наблюдался высокий непосредственный эффект у больных с рецидивом заболевания. Последующие длительные ремиссии и вероятное полное выздоровление ряда больных подтвердили эффективность такого подхода у больных лимфомой Беркитта. Тем не менее остается ряд нерешенных проблем, связанных с показаниями и техникой АуТКМ при лимфоме Беркитта. К ним относятся вопросы: 1) каков оптимальный химио-терапевтический режим и нужно ли добавлять тотальное облучение тела (ТОТ); 2) каким больным показана АуТКМ и можно ли ее проводить в период первой полной ремиссии.
В настоящее время существуют различные высокодозные химиотерапевтические режимы, используемые в сочетании с АуТКМ.
Первоначально предложенный режим ВАСТ (кармустин, цитарабин, циклофосфамид, тиогуанин) был впоследствии интенсифицирован за счет тройного увеличения дозы BCNU. Режим BEAM (этопозид, мелфалан) был разработан с целью снижения токсичности комбинации ВАСТ. Применение тотального облучения тела (ТОТ) до настоящего времени ставится под сомнение. Место ТОТ в процессе подготовительного режима у больных с лейкозом не вызывает сомнений у большинства исследователей, но не у всех, так как некоторые виды интенсивной терапии не приводят к санации костного мозга. Однако при лимфоме Беркитта ТОТ не является необходимым, так как приживление трансплантата не проблема при АуТКМ.
Существуют и другие подготовительные режимы, используемые при лимфоме Беркитта в сочетании с ТОТ или без него: циклофосфамид + кармустин; циклофосфамид; циклофосфамид + доксорубицин + винбластин + цитарабин + метотрексат и др.
Кроме того, добавление ТОТ усиливает токсичность за счет увеличения частоты интерстициального пульмонита и энцефалопатии, а у маленьких детей необходимо помнить об отдаленных последствиях.
В настоящее время на основании имеющегося опыта можно сделать заключение о том, что около 20 % детей с лимфомой Беркитта являются потенциальными кандидатами для высокодозной химиотерапии в сочетании с АуТКМ.
К ним относятся:
- больные с частичным эффектом после первичного лечения;
- дети с рецидивом, чувствительным к химиотерапии;
- пациенты с поражением ЦНС в момент диагностики, особенно с вовлечением в процесс более 25 % костного мозга.
Больные с рецидивом лимфобластной лимфомы также являются кандидатами для трансплантации костного мозга при наличии чувствительности к химиотерапии. У большинства больных, получавших циклофосфамид в сочетании с ТОТ, выживаемость лучше, чем у пациентов, которым проводилась только химиотерапия во время рецидива. Стратегия лечения у этой категории больных должна быть такой же, как у больных с лейкозом, и при достижении ремиссии и наличии совместимого донора — АлТКМ.
При В-клеточной лимфоме возможно достижение второй ремиссии, однако, как правило, она бывает короткой, а вероятность излечения не превышает 5 %.
После завершения интенсивной программы лечения в течение 1,5—6 мес (в зависимости от группы риска) дети с В-клеточной неходжкинской лимфомы не получают дополнительной поддерживающей терапии. Контроль в динамике заключается в клинической оценке, анализах крови (клинический и биохимический) с обязательным исследованием ЛДГ, УЗИ очагов первичного поражения. При необходимости проводится детальное обследование, аналогичное первичному.
После завершения всей интенсивной программы лечения, проводящейся в течение 4,5—6,5 мес в зависимости от группы риска и облучения головного мозга, дети с Т-клеточной НХЛ получают поддерживающую терапию в течение 24 мес, включая первоначальное лечение. Динамический контроль осуществляется по тем же принципам, как и при В-клеточной НХЛ.
После окончания интенсивной терапии в течение 4—6 мес в зависимости от группы риска больные с крупноклеточной анапластической лимфомой (ККАЛ) не получают поддерживающего лечения. Однако в настоящее время изучается вопрос о применении у больных с ККАЛ поддерживающего лечения, особенно с III и IV стадиями заболевания. Динамический контроль включает клиническую оценку, клинический и биохимический (ЛДГ) анализы крови, УЗИ брюшной полости и рентгенографию грудной клетки.
Несмотря на всевозможные усилия, направленные на снижение токсичности терапии, режимы ее остаются достаточно агрессивными, что может сопровождаться непосредственными и отдаленными осложнениями. Для их профилактики и лечения используется сопроводительная терапия, которая не менее важна, чем сама цитостатическая терапия. Основные принципы сопроводительной терапии дают возможность не только перенести интенсивное лечение, но в основном предупредить поздние осложнения, что в итоге обеспечивает качество жизни онкологических больных. Отдаленные осложнения могут быть связаны с нарушением функций различных органов и систем, а также с развитием вторых опухолей.
Как результат применения алкилирующих препаратов и ионизирующего излучения возможны нарушения со стороны ЦНС, эндокринной системы, сердца и легких, печени и почек. Применение антрациклинов, особенно в комбинации с циклофосфаном, метотрексатом и облучением средостения и позвоночника, способствует возникновению осложнений со стороны сердца. Кумулятивная доза антрациклиновых антибиотиков, превышающая 450 мг/м2, может привести к появлению серьезных и порой необратимых изменений в сердечной мышце, требующих в раде случаев пересадки органа.
Вторые опухоли развиваются у 4 и более процентов больных в сроки от 4 до 10 лет после завершения лечения. Как правило, возникают нелимфобластные лейкозы, хотя возможны и другие опухолевые заболевания. В последние годы появились сообщения о развитии вторых опухолей в более ранние сроки (через 15—20 мес) при лечении эпиподофилотоксинами (вепезид, тенипозид) с увеличением среди них доли ОЛЛ.
Это следует иметь в виду при наблюдении за детьми, перенесшими лечение по поводу неходжкинской лимфомы. В связи с этим нельзя ставить вопрос о формальном снятии с учета этой категории больных — они должны находиться под наблюдением врача в течение длительного периода времени.
Выявленные нарушения со стороны различных органов и систем должны лечиться соответствующими специалистами совместно с онкологом. В реабилитационный курс целесообразно включать санаторно-курортное лечение по специализированным программам.
Многие больные, излеченные от НХЛ, нуждаются в психологической реабилитации, медико-генетическом консультировании по вопросам семьи и брака, а также в социологической помощи при выборе специальности.

В сентябре 2017 года моя мама заболела лимфомой.

Мама из Северодвинска, это Архангельская область. Местные врачи поставили диагноз только через полгода. После этого мы год боролись с лимфомой и на какое-то время победили.
В этой статье я расскажу, сколько мы потратили на лечение и где взяли деньги. Предупреждаю сразу, что конец у этой истории будет печальный.
Как маме диагностировали лимфому
Онкологию начали подозревать только спустя пару месяцев. Тогда сделали биопсию лимфоузлов, но она получилась не с первого раза: несколько раз ее брали неправильно, поэтому результатов не было.
В конце концов диагноз все-таки подтвердили, хотя анализы еще на всякий случай отправили в областную онкологическую больницу в Архангельске для проверки. Это заняло еще три недели.

Что такое лимфома

Обычно первый симптом лимфомы — увеличение лимфоузлов. Не всегда это периферические лимфоузлы, которые можно увидеть при простом осмотре. Иногда в патологический процесс сразу вовлечены внутригрудные лимфатические узлы. Пациента может беспокоить сухой кашель, чувство нехватки воздуха, одышка. Если поражены внутрибрюшные лимфоузлы, то возникает боль, тяжесть, чувство переполнения в области живота.
При этом иногда даже при массивной опухоли у пациента может не быть значимых изменений в анализах крови. Только у части пациентов проявляются симптомы опухолевой интоксикации:
- Снижение массы тела на 10% за последние 6 месяцев.
- Повышение температуры выше 38 °C не менее трех дней подряд без признаков воспаления.
- Очень сильная ночная потливость.
Это все значит, что лимфому не так-то легко диагностировать.
Я узнала об исследовании, которое называется ПЭТ КТ — это метод диагностики онкологических заболеваний, в котором используют позитронно-эмиссионную (ПЭТ) и компьютерную томографию (КТ). Насколько я разобралась, ПЭТ КТ показывает очаги опухоли и помогает оценить развитие болезни.
Это довольно новое исследование: по ОМС в России его стали делать только несколько лет назад. В нашей региональной больнице его не упоминали. Но когда я спросила о нем на врачебном консилиуме, мы без вопросов получили направление.
Оборудование для ПЭТ КТ на тот момент было всего в 17 городах России: Москве, Санкт-Петербурге, Воронеже, Белгороде, Липецке, Екатеринбурге, Красноярске, Орле, Казани, Тамбове, Тюмени, Магнитогорске, Курске, Уфе, Челябинске, Хабаровске и Ханты-Мансийске. Ближайший к Северодвинску город — Санкт-Петербург, поэтому врач дал нам направление в петербургское отделение Российского научного центра радиологии и хирургических технологий. Без направления сделать ПЭТ КТ тоже можно, но это дорого: например, в 2019 году в этом центре исследование всего тела стоило 42 500 рублей.
стоит исследование ПЭТ КТ всего тела в 2020 году
Оказалось, что с городом нам повезло: нас готовы были принять уже через 2—3 дня после звонка в центр. В Москве даже за деньги исследование предлагали сделать самое раннее через полторы недели. По итогам повторной биопсии и результатов ПЭТ КТ врачи подтвердили, что у мамы лимфома, и довольно агрессивная.


Как диагностируют лимфому
Врач может заподозрить лимфому при увеличении лимфатических узлов, но диагноз ставят только по результатам биопсии. Если человек обнаружил у себя увеличенные лимфоузлы — лимфаденопатию — требуется обратиться к врачу. Дальше врач по совокупности клинических данных выбирает дальнейшую тактику обследования. При нарастающей лимфаденопатии — если лимфоузлы продолжают увеличиваться — нужно делать биопсию с обязательным гистологическим и иммуногистохимическим исследованием.

В Санкт-Петербурге на базе Северо-Западного государственного медицинского университета имени И. И. Мечникова работает Центр дифференциальной диагностики лимфаденопатий. Тут жителям Санкт-Петербурга и других регионов делают биопсию лимфоузла с гистологическим и иммуногистохимическим исследованием по ОМС.
Как мы выбрали больницу
Когда мы получили диагноз, стало понятно, что нужно как можно быстрее начинать лечение. Пять лет назад мама уже лечилась от рака шейки матки в областной онкологической больнице и все прошло хорошо, поэтому она была готова снова довериться местным врачам.
Но оказалось, что лимфому в Архангельской области лечат не в онкологической больнице, где хорошее финансирование и материально-техническая база, а в общей областной больнице. По очереди в эту больницу маму могли взять только через два месяца. Это слишком долго.

Мы стали искать подходящие больницы в других городах. Остановились на Центре онкогематологии и трансплантологии при Северо-Западном государственном медицинском университете имени И. И. Мечникова в Санкт-Петербурге. Там мы смогли начать лечение через 10 дней вместо двух месяцев.
Сразу после лечения врач сказал, что если бы мы не поторопились, скорее всего, мама была бы уже мертва. Такой вид лимфомы убивает человека меньше чем за год.
Почему важно время
Существуют разные варианты лимфом, они делятся на индолентные и агрессивные подгруппы.

Агрессивные лимфомы характеризуются высокой скоростью деления опухолевых клеток. Это приводит к быстрому распространению патологического процесса по организму, поэтому так важно в кратчайшие сроки поставить диагноз и начать химиотерапию.
Как получить квоту на лечение
Когда мы выбирали, где лечить лимфому, решили не рассматривать лечение за границей. Как нам сказали врачи, российские стандарты лечения лимфомы совпадают с европейскими, потому нет разницы в эффективности лечения в России и, скажем, в Германии.
Но есть разница в стоимости: лечение гражданам РФ покрывает бюджет. Полиса ОМС для этого не хватит, но можно получить квоту. Т—Ж уже писал, как выглядит процесс получения квоты на операцию в отдельной статье. Я расскажу, как было у нас.

Сначала мы собрали пакет документов:
- Результаты исследований ПЭТ КТ.
- Протокол решения врачебной комиссии архангельской больницы с направлением на лечение по программе высокотехнологичной медицинской помощи и выпиской из карты об анамнезе.
- Справку архангельской больницы о диагнозе мамы.
- Направление на госпитализацию, выданное в северодвинской больнице.
- Заявление о согласии на обработку персональных данных.
С документами мы пришли к своему лечащему врачу больницы в Северодвинске. Она передала документы вместе с заявлением на получение квоты в областную больницу, и мы стали ждать подтверждения. По закону на это у областной больницы три дня.
После этого все наши документы направили в лечебное заведение, которое было указано в заявлении. Как только областная больница подтверждает направление, пациенту выдают 14-значный номер, по которому можно отслеживать процесс на специализированном портале по ВМП.
Через неделю из Центра онкогематологии пришло положительное заключение. Какие документы нужны для госпитализации и когда приезжать, я уточняла по телефону.

Справка архангельской больницы с диагнозом мамы 
Направление на госпитализацию из северодвинской больницы
Приключения перед госпитализацией
По телефону мы договорились с заведующей отделения гематологии в петербургском Центре онкогематологии о сроках госпитализации. И тут начались неприятности.
На фоне долгого приема обезболивающих у мамы открылась язва. Ей сделали полостную операцию, поэтому она не смогла приехать в Санкт-Петербург к дате госпитализации. Был риск, что начало лечения серьезно сдвинется.
Поскольку у мамы были очень неспецифичные для лимфомы симптомы, врачи в Центре онкогематологии хотели еще раз проверить ее биопсию. На это уходит примерно 14 дней. Но начать проверку без биоматериала мамы они не могли, а он был в Северодвинске. Кроме того, они могли провести исследование по ОМС только своим пациентам — а мама еще формально им не была.
мы заплатили за дополнительную биопсию
Результаты анализа подтвердили диагноз архангельских врачей, и маму наконец-то взяли на лечение.
Как маме лечили лимфому
Маме прописали шесть курсов химиотерапии по четверо суток каждый. Курс химиотерапии — это отдельная история с поступлением в больницу, исследованиями, подготовкой к процедуре, самой химией и восстановлением в больнице. Перерыв между курсами — 28 дней.
Чтобы этого избежать, пациенту ставят подключичный порт. Он позволяет избежать многочисленных внутривенных инъекций. Для установки подключичного порта нужна отдельная операция, которую проводит сосудистый хирург. Маме ее тоже сделали по квоте.
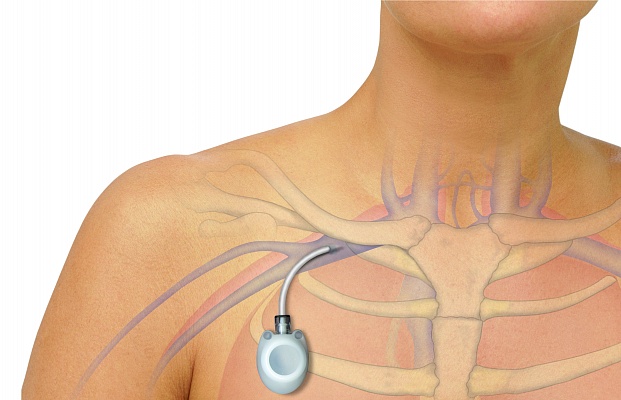
Установка подключичного порта выглядит так. Источник: Городская клиническая больница имени С. С. Юдина
После окончания шести курсов химиотерапии развитие заболевания у мамы остановилось. Далее ей предстояла пересадка костного мозга. В Центре онкогематологии пересадку не проводят, и нам дали направление в другую больницу, Исследовательский центр онкологии им. Петрова — тот самый, где ранее маме делали ПЭТ КТ. Для пересадки костного мозга у мамы дважды брали клетки, но их не хватило. В итоге пересадку не провели.
Квота покрыла все расходы на лечение. Кроме самой химиотерапии и операции по установке подключичного порта в лечение вошли консультации врачей, исследования, медицинские манипуляции вроде забора крови и установки капельницы. Если бы у нас получилось сделать пересадку костного мозга, квота покрыла бы и ее.

Мне было неловко спрашивать врачей, сколько стоит та или иная манипуляция. Судя по словам маминого врача, для россиян лечение всегда бесплатно: если не хватает полиса ОМС, оформляют квоту. Для иностранцев курс стоит от 50 до 200 тысяч и более. На сайте НМИЦ онкологии им. Петрова я нашла стоимость всех услуг.
Для примера я свела в таблицу некоторые процедуры и операции, которые делали маме, и их стоимость.
Читайте также:

