Можно ли удалять желчный пузырь при раке печени

Выработка желчи в организме очень важна, чтобы ускорить процесс переваривания жиров, стимулировать активность желудочно-кишечных ферментов, выводить токсические вещества. Эти функции выполняет желчный пузырь, находящийся под печенью, который активно участвует в пищеварительном процессе. Однако зачастую работа органа дает сбои, которые приводят к желчнокаменной болезни, холециститу (воспалению внутренней оболочки), дискинезии, холангиту (поражению желчевыводящих протоков). Самый тяжелый из недугов – рак желчного пузыря.
Особенности развития
Эта редкая форма онкологии встречается в основном у людей в возрасте старше 40 лет, причем женщины болеют в 4 раза чаще, чем представители сильного пола.
- плохая экологическая обстановка;
- повышенный радиационный фон;
- нерациональное питание (чрезмерное употребление жирного мяса и другой животной пищи);
- склонность к алкоголизму;
- наличие сопутствующих хронических заболеваний;
- ожирение;
- женский пол;
- наследственность;
- сахарный диабет;
- накопление кальция в стенках пузыря и камней в желчевыводящих протоках.
Рак желчного пузыря имеет высокий уровень метастазирования. Метастазы распространяются по лимфатическим путям в клетки печени, переходят в брюшину, поджелудочную железу. При этом медики отмечают неблагоприятный прогноз.
Если имеет место доброкачественная опухоль (аденома, папиллома, липома, фиброма), остается вероятность (хотя достаточно малая) ее озлокачествления. Такие новообразования представляют некую опасность из-за возможности перерождения. Их выявление может являться поводом для холецистэктомии.
Классификации
Рак желчного пузыря имеет ряд стадий, характеризующихся тяжестью течения болезни:
- Преинвазивная (предраковая, нулевая) – клетки поражают слизистую органа и далее под влиянием этиологических (способствующих развитию) факторов трансформируются в злокачественную опухоль. На указанном этапе симптомы не выражены.
- Начальная (первая, А, В) – процесс распространяется со слизистой на мышечную ткань. Ранние признаки рака могут проявиться, но не всегда. Если недуг диагностирован на этой стадии, есть шанс полного выздоровления.
- Средней тяжести (вторая) – метастазы переходят в печень, почки и другие органы. Симптомы рака могут быть приняты за признаки других недугов. Шансы выздороветь снижаются.
- Тяжелая (третья) – болезнь поражает региональные и отдаленные лимфатические узлы. Состояние человека резко ухудшается. В лечении используют методы снижения интенсивности симптоматики и пытаются предотвратить распространение заболевания.
- Осложненная (четвертая) – метастазы поражают отдаленные органы: яичники, плевру, брюшную полость, сальник. Может одновременно развиться рак печени. Доктора назначают поддерживающую терапию, чтобы на определенный период продлить жизнь больного.
Виды рака желчного пузыря по гистологии:
- аденокарцинома (она развивается в более чем 80% случаев в железах клеток, выстилающих желчный пузырь);
- плоскоклеточный (по частоте распространения стоит на втором месте, прорастает в периневрий или лимфатические сосуды);
- скиррозный (с плотной соединительнотканной основой);
- солидный (опухоль состоит из клеток, расположенных пластинами);
- низкодифференцированный (раковые клетки имеют неправильные ядра и аномальное строение).
Самый распространенный вид – аденокарцинома желчного пузыря – обычно возникает в участке шейки или дна органа и может прогрессировать по внутрипеченочным желчным протокам.
По сосредоточению опухоли желчного пузыря рак бывает локализованный (начальная степень, когда его можно побороть оперативным путем, полностью удалив пораженную часть), неоперабельный (метастазы поражают другие органы – почки, печень) и рецидив (появление вторичной опухоли после проведенного лечения).
Почему возникает болезнь
Согласно статистическим данным, среди злокачественных опухолей желудочно-кишечного тракта рак желчного пузыря занимает пятое место. В двух случаях из трех он развивается из протекающей длительное время желчнокаменной болезни или хронического холецистита. Зачастую опухоль возникает при наличии камней, особенно опасных, если они большого размера. Перемещаясь внутри, они травмируют слизистую органа, способствуя канцерогенезу.
К сопутствующим заболеваниям, которые способствуют развитию недуга, относятся полипы и кисты, кальциноз, сальмонеллез, инфицирование бактерией Хеликобактер пилори.
Вероятность болезни увеличивают встречающиеся врожденные аномалии поджелудочной железы и желчных протоков: наросты, неправильное соединение железы и протоков.
В 50 процентах случаев наличие небольшой аденокарциномы желчного пузыря (диаметром 5-10 мм) сочетается с желчнокаменной болезнью и является дополнительным поводом для хирургического вмешательства.
Первые симптомы
Сразу после начала болезни пациента ничего не беспокоит. Специфические признаки начинают проявляться, когда клетки опухоли выходят за пределы пораженного органа.
Первые симптомы рака желчного пузыря:
- общая слабость в теле;
- горький привкус во рту;
- тошнота;
- отсутствие аппетита;
- тянущая боль в правом боку.
Если заблокирован желчевыводящий проток, боль может быть резкой. На этом фоне пациент начинает худеть, терять килограммы.
Вторая стадия характеризуется рвотой, желтизной кожи, глазных белков, зудом. Моча становится более темной, а кал – светлеет.
Рак третьей стадии известен тем, что опухоль переходит на клетки печени, развивается печеночная недостаточность, появляются чувство апатии, сильная вялость, заторможенность. Опухоль может закупорить желчные протоки, это заканчивается скоплением жидкости в желчном пузыре, воспалением желчных протоков (холангиту), циррозом печени.
Полное истощение жизненных сил (кахексия), злокачественное поражение брюшной полости (канцероматоз), водянка (асцит), тяжелая интоксикация вплоть до сепсиса – таковы признаки рака желчного пузыря четвертой стадии.
Онкопатологические стадии
Выделение этапов заболевания позволяет доктору выбрать правильные и своевременные терапевтические процедуры.
Для дифференцирования степени распространения опухоли медики чаще всего используют систему TNM (аббревиатура от англ. Tumour (первичная опухоль), Nodes (лимфоузлы), Metastases (отдаленные метастазы), разработанную во Франции Международным противораковым союзом. T – указывает на величину и распространение опухоли; N – поражение лимфатических узлов; M – проникновение опухоли в другие органы.
- Tx – нельзя определить размеры и местное распространение первичной опухоли;
- ТО – признаки первичной опухоли не проявляются;
- Ta – преинвазивная папиллярная карцинома;
- Tis – плоская опухоль;
- T1-Т4 – прорастание через слои и ткани желчного пузыря;
- T4a – попадание в другие органы: предстательную железу, влагалище, матку;
- T4b – прорастание в брюшину или тазовую стенку.
- Nx – невозможно дать оценку региональных лимфоузлов;
- NO – отсутствие метастазов;
- N1 – наличие метастазов в единичном лимфоузле малого таза;
- N2 – присутствие метастазов в нескольких лимфоузлах малого таза;
- N3 – метастазы в подвздошных лимфоузлах.
- Mx – нельзя дать оценку отдаленным метастазам;
- MO – метастазы отсутствуют;
- М1 – имеются отдаленные метастазы.
Согласно другой системе, медики выделяют 4 стадии:
- Первая. Самая ранняя, когда злокачественный процесс еще не проник в ближайшие ткани и органы, а локализуется лишь внутри желчного пузыря. По классификации TNM, соответствует ТО, NO, MO;
- Вторая. Рак в желчном пузыре прорастает через мышечный слой его стенки в соединительную ткань, но остается в пределах органа. Идентичен T2, NO, MO;
- Третья. Подразделяется на 2 подгруппы:
• 3A – опухоль проросла через стенки желчного пузыря, злокачественных клеток в лимфоузлах нет. Соответствует 3, NO, MO;
• 3B – новообразование располагается в границах внешнего слоя или поразило лимфоузлы. Идентификация с T1, T2 или T3, N1 или MO; - Четвертая. Метастатический рак. Делится на 4A, 4B:
• 4A – процесс поражает ведущую к печени артерию, распространяется в нескольких органах. Затрагиваются лимфоузлы. Соответствие T4, NO или N1, MO;
• 4B – рак, поразивший лимфоузлы и давший метастазы (T, N2, MO; T, N, M1).
Методы диагностики заболевания
В связи с бессимптомным протеканием болезни о раке желчного пузыря пациенты зачастую узнают слишком поздно – когда наступает его поздняя неоперабельная стадия. Это происходит в 70% случаев.
При обращении пациента онколог собирает анамнез, осматривает больного, прощупывает живот, чтобы определить, не увеличен ли он. Может иметь место патологическое увеличение печени – гепатомегалия; селезенки – спленомегалия; желчного пузыря, иногда – инфильтрат в брюшной полости. Особое внимание доктор обращает на белки глаз и оттенок кожи – при наличии заболевания должна присутствовать желтизна. Шейные и паховые лимфатические узлы при осмотре могут быть увеличены.
После предварительного вердикта специалист назначает дополнительные обследования:
- специальные анализы крови – печеночные пробы (тесты, проверяющие функционирование печени и желчного пузыря), билирубин (высокий уровень которого указывает на проблемы с печенью или желчным пузырем);
- ультразвук (УЗИ-диагностика устанавливает, не распространился ли рак на стенки желчного пузыря);
- компьютерную томографию (КТ), которая показывает наличие или отсутствие опухоли желчного пузыря и желчных протоков, лимфоузлов и печени.
С помощью специфического лабораторного теста можно определить в крови маркер – раковый антиген 19-9.
Если в результате сканирования выявлены аномальные области в желчном пузыре или вокруг него, назначают рентген с помощью эндоскопа (обследование ЭРХПГ), которым врач обследует внутреннюю часть тонкого кишечника и берет биопсию с подозрительных участков.
Магнитно-резонансная холангиопанкреатография (МРХПГ) позволяет получить детальное изображение обследуемых органов. На сегодняшний день это лучший метод диагностики и определения стадии онкологического заболевания.
Определить, доброкачественная опухоль или злокачественная, поможет биопсия – взятие образцов тканей и их изучение под микроскопом. Процедуру выполняют разными способами: в момент лапароскопии, ЭРХПГ, путем тонкоигольной аспирационной биопсии.
Образцы клеток изучаются в лаборатории. Для выяснения, не распространился ли опухолевый процесс на печень или лимфоузлы, могут дополнительно взять пробы ткани.
Диагностика желчного пузыря может выявить наличие заболевания. Возникает необходимость дальнейших исследований для определения степени распространения процесса. В 80 процентах случаев диагностика показывает развитие онкологии.
Для назначения дальнейшей терапии могут быть показаны:
- МРТ с холангиографией, которые определят, блокируется ли поток желчи новообразованием, распространяется ли опухоль на воротную вену. Этот тест имеет противопоказания для тех, у кого в организме есть металл (например, кардиостимулятор);
- эндоскопическое УЗИ показывает рак желчного пузыря, его стадию, прорастание опухоли в стенку пузыря или печень. Это способствует облегчению планирования операции;
- холангиография – исследование желчных протоков при помощи красителей, рентгеновских лучей и эндоскопа. Помогает выявить опухоль протока, наличие или отсутствие блокировки (если она есть, ставят стент);
- диагностическая лапароскопия, при которой аппарат, оснащенный светом и камерой, вводят через небольшие разрезы в брюшную полость, чтобы проверить признаки онкологии. Манипуляция проводится под анестезией. В ее результате можно определиться с методом лечения.
Лечебная тактика
При начальной стадии рака проводят простую или расширенную холецистэктомию – хирургическим путем удаляют желчный пузырь. Рак желчного пузыря и печени (если имеются единичные метастазы) оперируют, подвергая резекции пораженной доли, дополнительно могут сделать резекцию правой части печени, удалить 12-перстную кишку и поджелудочную железу. Возможно удаление пораженных региональных лимфоузлов.
Альтернативный метод лечения представляет применение рентгеновского излучения (или других видов лучевой терапии), которое позволяет не только удалить пораженные части органа, но и уменьшить рост опухоли. Внешняя лучевая терапия – когда аппарат расположен в непосредственной близости к пациенту. Внутренняя – радиоактивные вещества вводятся в организм с помощью игл, трубок, катетеров. В последнее время применяют радиосенсебилизаторы, повышающие чувствительность злокачественной опухоли к лучам. Это позволит ликвидировать больше метастазированных клеток.
Если рак вошел в неоперабельную стадию, назначают паллиативные хирургические вмешательства, чтобы облегчить состояние больного и продлить ему жизнь. Для нормализации оттока желчи устанавливают трубки в желчные ходы, иногда формируют искусственный свищ для вывода желчи.
После удаления опухоли желчного пузыря и при неоперабельном раке проводят дополнительные мероприятия:
- химиотерапию, при которой курсом вводят лекарственные препараты, уничтожающие онкологические клетки. Болевой синдром уменьшается, но появляются побочные эффекты: общее недомогание, отсутствие аппетита, рвота);
- лучевую терапию – уничтожение патологических клеток рентгеновскими лучами и подавление их роста;
- радиационную терапию, которая в комплексе с лучевой дает положительный результат и увеличивает продолжительность жизни пациента на несколько лет.
К вспомогательной терапии можно отнести народную медицину, средства которой не заменяют основного лечения, но в отдельных случаях могут облегчить состояние заболевшего. Популярными в народе считаются рецепты с использованием настоя рылец кукурузы (стакан кипятка на 10 г сырья, пьют в течение 45 суток); черной белены (бутылка водки на 20 г сырья, настаивают 2 недели, принимают по 2 капли однократно ежедневно перед едой); меда и сока из редьки в одинаковых пропорциях (по 50 г два раза в день перед едой).
Метастазы
При раке в желчном пузыре метастазы часто распространяются в печень, желудок, брюшную полость, желудочные, брызжеечные и забрюшинные лимфоузлы, в поясничный лимфатический ствол, ткани поджелудочной железы, селезенку, а также в плевру и яичники. Отдаленные метастазы проникают в паховые лимфоузлы и образуют вторичные злокачественные новообразования в легких.
Метастазы могут распространяться:
- через лимфоузлы (лимфогенный путь);
- с пораженного органа (путем прорастания в прилежащие органы – поджелудочную железу, печень, кишечник, лимфатические сосуды);
- с кровью по сосудам (гематогенный путь).
Если метастазы имеют место, излечение от недуга невозможно. Паллиативная терапия должна быть направлена на поддержание работы жизненно важных органов, облегчение симптомов, замедление развития заболевания, улучшение (насколько это возможно) качества жизни пациента.
Прогноз выживаемости
Если на ранней стадии выявлен рак желчного пузыря, лечение в 80 процентах случаев даст благоприятный результат после удаления пораженного органа (холецистэктомии). Онкологи настаивают на операции, убеждая, что удаление опухоли – единственный шанс продлить годы существования.
Если рак проник в мышечную ткань (первая раковая стадия), общий прогноз – не очень благоприятный. По статистике, лишь 50 процентов пациентов живут после поставленного диагноза 5 и более лет. Результат напрямую зависит от прогрессирования опухоли и ее стадии. Обычно в связи с поздно поставленным диагнозом вылечить болезнь тяжело.
Третья и четвертая стадии – это проникновение метастазов в окружающие ткани и лимфоузлы. При их удалении можно получить контроль над карциномой в течение некоторого времени. На этой стадии около 5 лет живут менее 10 процентов заболевших.
Если заболевание возвращается после проведенного лечения, речь идет о рецидиве. Агрессивная форма – рецидив рака желчных протоков – быстро развивается и трудно поддается лечению. В большинстве случаев пациент с таким диагнозом живет не больше года.
Профилактические меры
Специфической профилактики заболевания не существует. Общие врачебные рекомендации включают советы по нормализации массы тела, правильному рациону с уменьшением доли животной пищи и увеличением количества витаминов и питательных элементов. Рекомендуется регулярно заниматься спортом, отказаться от пагубных пристрастий, закаливать организм.
Чтобы избежать формирования рака желчного пузыря, необходимо придерживаться правил:
- полноценно и рационально питаться;
- проходить регулярные медицинские осмотры, в том числе УЗИ;
- проводить очищение печени (по назначению врача).
Помните, что своевременное обнаружение рака — залог вашего скорейшего выздоровления и возврата к обычной, полноценной жизни! При любых неприятных симптомах следует немедленно обращаться к врачу.
Лечение раковых опухолей направлено на то, чтобы полностью удалить или уничтожить злокачественную опухоль, а также все ее метастазы. Такая терапия называется куративной. На поздних стадиях заболевания, когда полное излечение уже невозможно, применяется паллиативная терапия, направленная на улучшение качества жизни больного.
Рак печени (гепатома, гепатоцеллюлярная карцинома) встречается довольно редко.
Печень — самый крупный и один из самых сложных по строению внутренних органов человека.
После сбора анамнеза врач проводит клиническое обследование.
Реабилитация и наблюдение являются важными составляющими лечения онкологических больных.
В настоящее время при раке печени шанс на полное выздоровление есть только в случае успешного оперативного лечения. Существует два варианта удаления опухоли: удаление части органа (частичная резекция печени, гепатэктомия) и пересадка (трансплантация) печени.
Трудность заключается в том, что в большинстве случаев общее состояние пациента не позволяет провести оперативное вмешательство.
В ходе частичного удаления (резекции) печени хирургическим путём удаляется опухоль и часть окружающей её здоровой ткани. Различают анатомическую и атипичную резекцию печени.
Анатомическая резекция подразумевает удаление правой или левой половины печени (гемигепатэктомия), причем граница удаляемого участка не совпадает с границами долей печени, а определяется в зависимости от его кровоснабжения.
В некоторых случаях нужно удалять до 85 % ткани печени, но, если оставшаяся часть органа здорова, то он может нормально функционировать.
Однако если оставшаяся ткань печени поражена циррозом, есть вероятность, что после операции она уже не будет справляться со своими функциями, и пациент может умереть вследствие отказа печени.
Атипичная резекция печени проводится, чтобы сохранить как можно больше ее ткани. Она заключается в том, что иссекается только сама опухоль с минимальным количеством окружающей её здоровой ткани. Эта операция может быть альтернативой для больных циррозом печени, тем не менее, если цирроз находится на прогрессирующей стадии, то она не принесёт желаемого эффекта и её проведение исключается.
Кроме того, цирроз печени зачастую приводит к развитию портальной гипертензии (повышенного давления в воротной вене). В этом случае проведение операции также связано с большим риском.
Резекция печени не исключает вероятность возникновения рецидива. Причиной могут стать микроскопические части опухоли, которые не были удалены в ходе операции. Кроме того, иногда в оставшейся части печени развивается новая опухоль.
Пересадка печени (трансплантация) подразумевает полное удаление печени пациента и замену её здоровым донорским органом.
Этот метод лечения прежде всего рассматривается при циррозе печени с портальной гипертензией, так как трансплантация одновременно избавляет и от этого заболевания. Кроме того, пересадка печени показана пациентам с множественными мелкими очагами опухоли.
Обязательным условием для проведения трансплантации является хорошее общее состояние пациента и отсутствие сопутствующих заболеваний.
После пересадки печени пациент должен в течение долгого времени принимать специальные препараты для подавления активности иммунной системы, чтобы избежать отторжения трансплантата. При ослабленном иммунитете даже самое безобидное инфекционное заболевание может стать угрозой для жизни.
После трансплантации вероятность возникновения новой опухоли существует лишь с том случае, если в организме остались опухолевые клетки вне печени.
Если опухоль нельзя удалить, необходимо сдерживать её рост. В настоящее время существует много возможностей местного лечения опухолей печени, а так как злокачественные новообразования этого органа редко дают метастазы, это позволяет значительно продлить жизнь пациенту и улучшить её качество.
Цель местного лечения — остановить рост опухоли либо разрушить её. Для этого проводится либо склерозирование опухоли, либо остановка её кровоснабжения (эмболизация).
Печень снабжается кровью через две сосудистые системы: печеночную артерию и воротную вену. При этом в опухоль кровь практически всегда поступает по ветвям печеночной артерии. Эта особенность позволяет применять для разрушения опухоли трансартериальную химиоэмболизацию (TACE). Суть этого метода заключается в том, что артерии, по которым кровь поступает в опухоль, закупориваются, в результате чего раковые клетки погибают, а опухоль уменьшается.
В ходе трансартериальной химиоэмболизации через бедренную артерию под местной анестезией вплоть до сосуда, снабжающего опухоль, вводится тонкая трубочка (катетер). Затем в него впрыскивается смесь из нескольких медикаментов: средств, способствующих закупорке сосудов, контрастного вещества или цитостатических препаратов, уничтожающих раковые клетки. Таким образом, происходит двойное воздействие на опухоль: останавливается её кровоснабжение и разрушаются злокачественные клетки.
В ходе лечения может возникнуть ряд побочных эффектов, например, боли в верхней части брюшной полости, повышенная температура и тошнота. Эти симптомы хорошо поддаются лечению и обычно исчезают по окончании терапии.
Обязательным условием для проведения трансартериальной химиоэмболизации является проходимость как печеночной артерии, так и воротной вены. При нарушении проходимости воротной вены эта процедура не проводится, так как в противном случае кровоснабжение печени будет полностью остановлено, что приведёт к смерти пациента.
Одним из видов лечения при помощи теплового воздействия является радиочастотная термоабляция (РЧА). Она заключается в том, что в опухоль через кожу вводится специальный зонд, нагревание которого приводит к гибели раковых клеток.
РЧА проходит под контролем УЗИ или компьютерной томографии. Введение зонда абсолютно безболезненно, так как осуществляется под местным или общим обезболиванием. Сама процедура также не вызывает болевых ощущений, так как в печени нет нервных окончаний.
Аналогичной процедурой является микроволновая абляция (МВА).
Этот инновационный метод (Selective internal radiation therapy, SIRT) основан на введении мельчайших радиоактивных микросфер в опухолевые очаги печени. Они вводятся в организм через катетер в печёночную артерию, откуда частицы попадают в кровеносные сосуды, снабжающие опухоль. В результате происходит остановка кровоснабжения опухоли, а раковые клетки подвергаются радиоактивному облучению. В настоящее время эта терапия активно исследуется.

Лучевая терапия (радиотерапия) является одним из важнейших методов в лечении рака. Ионизирующее излучение воздействует на ядро клетки. Оно разрушает её генетическую информацию (ДНК), в результате чего клетка больше не может делиться. В то время как здоровые клетки в большинстве случаев восстанавливаются после таких изменений, раковые клетки не могут справиться с повреждениями, нанесёнными излучением, и поэтому погибают.
Особенность клеток печени состоит в том, что они не могут регенерироваться после облучения и погибают вместе с раковыми. Поэтому лучевая терапия при лечении опухолей печени применяется только для болеутоления, лечения метастазов и в рамках клинических исследований.
Если опухоль печени уже метастазировала, или же, если очаг расположен так, что проведение локального лечения затруднено, используется системная терапия, воздействующая на весь организм. Под ней подразумевают биологическую, антигормональную или химиотерапию.
В последние годы для лечения рака печени применяют специальные молекулы, подавляющие рост опухолевых клеток (биотерапия). В настоящее время единственным официально разрешенным препаратом является сорафениб. Этот препарат рекомендуется только тем пациентам, чье состояние оценивается как стадия А по Чайлд-Пью.
Эффективность этого метода при раке печени пока не доказана.
Зачастую в ходе операции не удаётся удалить все раковые клетки, например, когда некоторые из них через лимфатические и кровеносные сосуды успели попасть в другие части тела, или если раковая опухоль уже дала отдалённые метастазы. В этом случае назначается химиотерапия.
В ходе химиотерапии разрушаются быстро делящиеся клетки. Медикаменты (цитостатические средства), используемые для этого вида терапии, препятствуют их делению, таким образом предотвращая дальнейшее разрастание опухоли. Кровь распределяет медикаменты по всему организму (системная терапия). Но у этого метода есть недостаток — разрушаются и здоровые быстро делящиеся клетки. К ним относятся, например, клетки слизистых оболочек и волосяных луковиц.
Для лечения рака печени химиотерапия применяется очень редко. Она эффективна только для лечения редкого вида опухоли печени, фиброламеллярной карциномы, при условии отсутствия цирроза печени.
Новые подходы к лечению рака печени с помощью химиотерапии находятся в настоящее время в процессе разработки.
На поздних стадиях, когда состояние пациента оценивается как стадия C по Чайлд-Пью, применение лечения считается нецелесообразным, так как существующие методы терапии не дают положительных результатов и тяжело переносятся пациентами. В таком случае принимается совместное решение врача и пациента о дальнейших действиях, с учетом их преимуществ и недостатков.

Цель генной терапии — встроить в опухолевые клетки такую генетическую информацию, которая приведёт к их гибели.
Например, в ДНК раковых клеток помещаются такие вещества, которые влияют на выработку определённых белков. Эти белки, в свою очередь, могут подавить рост раковой опухоли.
Кроме того, генная терапия подразумевает использование так называемых костимуляторов, благодаря которым иммунная система начинает активно бороться с опухолевыми клетками.
Активация иммунной системы для борьбы против опухоли возможна также при помощи специальной вакцины. Данный метод существует только в рамках исследований и ещё не применялся для лечения людей.
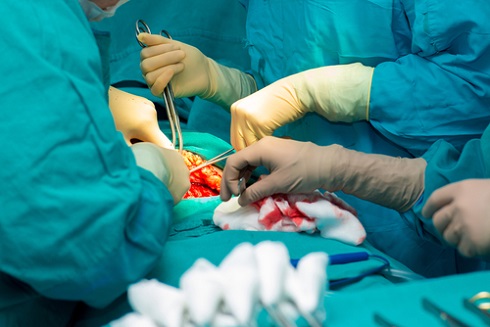
При раке желчных протоков оперативное лечение — единственный шанс на полное выздоровление.
Зачастую опухоль расположена так, что требуется не только удаление самой опухоли, но и удаление значительной части печени. Поэтому оперирование рака желчных протоков — это, как правило, очень обширное вмешательство. Чтобы его перенести, пациент должен находиться в хорошем общем состоянии.
Хирургическое лечение имеет смысл только в том случае, если опухоль резектабельна, то есть если её с технической точки зрения можно полностью удалить. Поэтому на поздних стадиях и при наличии метастазов оперативное вмешательство нецелесообразно.
Иногда перед операцией необходимо выполнить дренирование желчных протоков или эмболизацию (закупорку) сосудов печени, снабжающих опухоль кровью. При местно распространённой опухоли желчных протоков в большинстве случаев требуется расширенная гемигепатэктомия, подразумевающая удаление шести из восьми сегментов печени. Оставшейся части печени обычно достаточно, чтобы этот орган нормально функционировал. Затем удаляется часть желчных протоков и желчный пузырь. Оставшийся желчный проток (правый или левый) соединяется с тонкой кишкой.
Иногда действительный размер опухоли можно оценить только в ходе операции. Поэтому в некоторых случаях, если хирург понимает, что опухоль слишком большая и полностью удалить её не удастся, операцию останавливают.
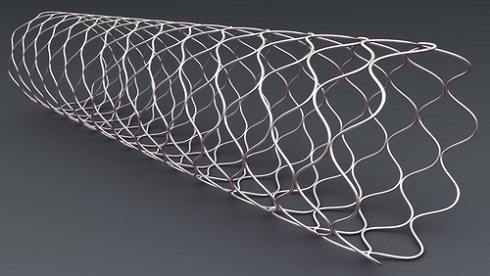
Раковая опухоль желчных путей и желчного пузыря может привести к их закупорке, в результате чего возникает воспаление желчных протоков. Поэтому пациентам, страдающим от желтухи, необходимо восстановить отток желчи. Это требуется как перед оперативным вмешательством, так и в том случае, когда операция невозможна.
Дренирование обычно проводят в ходе эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) — в желчные протоки устанавливаются специальные трубочки (стенты). Стенты бывают пластиковыми — их необходимо заменять каждые три месяца, и металлическими — их заменять не требуется.
Иногда установки стента бывает недостаточно для восстановления нормального оттока желчи. В этом случае применяется дренирование наружным способом (через печень и кожу). Установка такого дренажа происходит под рентгеновским контролем.
После такого дренирования необходим постоянный контроль дренажной трубки. Ее закупорка очень быстро приводит к воспалению желчных протоков.
На ранних стадиях опухоли желчных протоков обычно относительно небольшого размера, однако в некоторых случаях их расположение не позволяет провести удаление оперативным путём. В этом случае применяется фотодинамическая терапия с использованием лазера.
Фотодинамическая терапия проводится в 2 этапа. На первом этапе, который длится один-два дня, пациенту в форме инъекции вводится специальное вещество (фотосенсибилизатор), которое накапливается в опухоли и делает её восприимчивой к лазерному излучению. На втором этапе в рамках эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) в желчный проток вводят эндоскоп с закреплённым на нём источником лазерного излучения, разрушающего раковые клетки. В здоровой ткани фотосенсибилизатор почти не накапливается, поэтому лазер её не повреждает или повреждает очень незначительно.
Побочным эффектом этого метода лечения является повышенная светочувствительность кожи в течение месяца после лечения.
Эффективность данного вида терапии также изучена не до конца.

Лучевая терапия (радиотерапия) является одним из важнейших методов в лечении рака. Ионизирующее излучение воздействует на ядро клетки, разрушая её генетическую информацию (ДНК), в результате чего клетка больше не может делиться. В то время как здоровые клетки в большинстве случаев восстанавливаются после таких изменений, раковые клетки не могут справиться с повреждениями, нанесёнными излучением, и поэтому погибают. Излучение, используемое при лучевой терапии, аналогично рентгеновскому, но намного сильнее.
В некоторых случаях для симптоматического лечения рекомендуется местная брахитерапия, которая заключается в том, что облучение опухоли производится изнутри. Для этого при помощи гибкой трубки в область опухоли доставляется радиоактивный источник. Брахитерапия уменьшает риск закупорки желчных протоков и, следовательно, возникновения желтухи. Зачастую она проводится в сочетании с фотодинамической терапией.
В некоторых случаях брахитерапия применяется для лечения метастазов.
Для лечения рака желчных протоков химиотерапия применяется только в том случае, если опухоль невозможно удалить оперативным путём, а также, если желчные протоки проходимы. Тем самым замедляется рост новообразования и продлевается жизнь пациента.
В рамках клинических исследований химиотерапия применяется в сочетании с лучевой терапией, после чего проводится трансплантация печени.
Во многих случаях на поздних стадиях рак желчных протоков не поддаётся лечению. В этом случае применяется паллиативная терапия, задача которой заключается в повышении качества жизни больного.
Читайте также:

