Сунитиниб при лечении рака почки
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Рак почки (РП) – одно из наиболее распространенных онкоурологических заболеваний. Около 210 тыс. новых случаев РП диагностируется в мире ежегодно, что в структуре онкологической заболеваемости составляет примерно 2% [1].
В 2007 году в России выявлено 16770 больных со злокачественными новообразованиями почки, что составило 4,13% у мужчин и 2,87% у женщин среди всех злокачественных новообразований. По темпам прироста онкологической заболеваемости в России РП устойчиво занимает третье место после рака предстательной и щитовидной железы (35,83 %). Ежегодно в России от РП умирает более 8 тыс. человек. Стандартизованный показатель заболеваемости населения России злокачественными опухолями почки – 8,09 на 100 тыс. населения [2].
Рост заболеваемости РП частично обусловлен как улучшением диагностики на основе современных инструментальных исследований, таких как трансабдоминальное ультразвуковое исследование (УЗИ) и компьютерная томография (КТ), магнитно–резонансная томография (МРТ), так и ростом истинной заболеваемости РП. В настоящее время в 25–40% случаев заболевание выявляют случайно при профилактическом обследовании.
РП относится к агрессивным и непредсказуемым в своем течении злокачественным опухолям. При первичном обращении у 25–30% больных имеются отдаленные метастазы, а после хирургического лечения больных с локализованной и местнораспространенной стадиями заболевания вероятность возникновения рецидива и метастазов составляет 20–30% [1,3]. Наиболее часто метастатические очаги обнаруживают в легких (55%), лимфатических узлах (34%), костях (32%), печени (32%), надпочечниках (19%), контралатеральной почке (11%) и головном мозге (5,7%) [4].
Показатели общей выживаемости больных диссеминированным РП также разочаровывают: медиана общей выживаемости не превышает 13 месяцев, 5–летняя выживаемость – не более 5%, поэтому проблема лечения данной группы больных крайне актуальна [1,3].
Хирургическое вмешательство – единственный эффективный метод лечения РП, позволяющий излечить большинство больных на ранних стадиях заболевания [5].
Злокачественные опухоли почки нечувствительны к химиотерапии и гормонотерапии, что обусловлено наличием гена множественной лекарственной устойчивости РП. Несмотря на наличие эстрогеновых рецепторов в почечно–клеточных опухолях, использование гормональных препаратов не приводило к улучшению результатов лечения. Общий ответ на гормональную и химиотерапию составляет менее 5% [5,6].
Лучевая терапия используется только у больных РП с нерезектабельными метастазами в головной мозг или костными метастазами, не отвечающими на другие консервативные методы лечения. Лучевая терапия костных метастазов позволяет значительно снизить болевой синдром и улучшить качество жизни больных [5].
На протяжении двух последних десятилетий неспецифическая иммунотерапия прочно занимала ведущие позиции в лечении метастатического РП. В настоящее время накоплен достаточный опыт применения препаратов интерферона–2 и интерлейкина–2, как в монорежиме или в сочетании друг с другом, так и в комбинации с различными химио– и гормонопрепаратами. Суммарный ответ на иммунотерапию колеблется от 10 до 20%, при этом эффект лечения нестойкий, ремиссии непродолжительные, а частота побочных реакций остается высокой. По данным ряда исследователей, иммунотерапия цитокинами эффективна не более чем у 20% больных [6,7].
Во многих клинических исследованиях убедительно доказано влияние целого ряда прогностических параметров на результаты лечения цитокинами и выживаемость больных РП. В 1999 г. R. Motzer и соавт. на основании многофакторного анализа выделили 5 независимых параметров, коррелирующих с выживаемостью 670 больных диссеминированным РП, наблюдавшихся в Memorial Sloan–Kettering Cancer Center (MSKCC) с 1975 по 1996 г. Неблагоприятными прогностическими факторами являлись: соматический статус по шкале Карнофского 10 мг/дл), уровень гемоглобина
В 2002 году этот же автор усовершенствовал данную прогностическую модель и продемонстрировал ее эффективность в отношении 463 больных распространенным РП в качестве первой линии системной терапии. Медиана выживаемости больных в группах плохого, умеренного и благоприятного прогноза составила 5, 14 и 30 месяцев соответственно [9].
Отсутствие эффективного и безопасного метода лечения диссеминированного РП послужило причиной дальнейшего поиска новых вариантов и подходов.
РП встречается в виде двух форм – наследственной и ненаследственной (спорадической). Возникновение спорадического РП в 65% связано с биаллельной инактивацией опухоль–супрессорного гена von Hippel–Lindau (VHL) посредством делеции, мутации или метилирования [10].
Гиперэкспрессия факторов роста и их рецепторов, возникающая в результате инактивации опухоль–супрессорного VHL гена, является важнейшим механизмом активации ангиогенеза в опухолевой ткани и представляет собой потенциальную терапевтическую цель при распространенном ПКР [10,11].
В условиях нормоксии α –субъединица фактора, индуцированного гипоксией (HIF– α – Hypoxia–Inducible Factor– α ) связывается с белком–продуктом гена VHL, который стимулирует разрушение HIF– α по протеосомному пути. При мутации гена VHL HIF– α аккумулируется и активизирует транскрипцию элементов, индуцированных гипоксией, и приводит к гиперэкспрессии сосудисто–эндотелиального фактора роста (VEGF – Vascular Endothelial Growth Factor), тромбоцитарного фактора роста (PDGF – Platelet–Derived Growth Factor) и трансформирующего фактора роста α и β (TGF– α и β –transforming growth factor), которые активируют расположенные вблизи опухолевой ткани клетки эндотелия для построения новой сосудистой сети. Рост сосудов приводит к увеличению поступления в опухолевую ткань кислорода и питательных веществ, что позволяет опухоли развиваться и дальше [10,11].
Прогресс в понимании молекулярной биологии привел к открытию новых препаратов для лечения метастатического РП, относящихся к группе ингибиторов ангиогенеза: сунитиниб ( Сутент), сорафениб, темсиролимус, бевацизумаб и другие. Основным патогенетическим механизмом всех этих препаратов является антиангиогенный эффект, направленный на предотвращение неоангиогенеза опухоли [5].
В 2007 году для лечения метастатического РП в России зарегистрирован таргетный препарат Сутент (сунитиниб). Сунитиниб – таблетированный ингибитор тирозинкиназ, который воздействует на все известные виды рецепторов к PDGF и VEGF (VEGFRs, PDGFR– α , PDGFR– β , c–KIT и FLT–3), участвующих в процессе роста опухоли, патологическом ангиогенезе и метастазировании.
Сунитиниб продемонстрировал эффективность в двух последовательных многоцентровых исследованиях 2 фазы у пациентов с метастатическим РП, не получивших эффекта от терапии цитокинами (интерферон– α 2 и интерлейкин–2) (табл. 1). Дизайн обоих исследований 2–й фазы был идентичный: включали больных метастатическим РП, спрогрессировавших после первой линии цитокиновой иммунотерапии с наличием измеряемых очагов, соматический статус по шкале ECOG 0 или 1 (ECOG – Eastern Cooperative Oncology Group). Сунитиниб назначали циклами по 6 недель (50 мг перорально, 1 раз в сутки): 4 недели лечения с последующим 2–недельным перерывом до прогрессирования заболевания, развития выраженных побочных эффектов или прекращения участия в исследовании по желанию пациента [12,13].
В первое исследование II фазы было включено 63 больных преимущественно со светлоклеточным метастатическим РП (87%). Медиана времени до прогрессирования заболевания составила 8,7 месяцев, в то время как медиана общей выживаемости – 16,4 месяцев. У 25 из 63 пациентов (40%) зарегистрирован частичный ответ, у 17 больных (27%) зафиксирована стабилизация заболевания более 3 месяцев. Неблагоприятные явления 3 и 4 степени токсичности, связанные с лечением, чаще всего включали: нейтропению (13%), слабость (11%), диарею (3%), тошноту (3%) и стоматит (2%) [12].
Во второе исследование II фазы включили 106 больных со светлоклеточным метастатическим РП, перенесших предшествующую нефрэктомию. На основании прогностической модели MSKCC было включено 58, 39 и 4% больных с благоприятным, умеренным и плохим прогнозом соответственно. У 55 и 45% больных соматический статус по шкале ECOG соответствовал 0 и 1 соответственно. Частичный ответ зарегистрирован у 36 (34%) из 105 больных, и у 30 больных (29%) зафиксирована стабилизация заболевания более 3 месяцев. Токсические явления со степенью токсичности >3, связанные с лечением, включали нейтропению (16%), слабость (11%), кожные реакции на конечностях (7%), гипертензию (6%), стоматит (5%), диарею (3%) и в 2,4% случаев снижение фракции выброса левого желудочка [13].
По обновленным данным, во втором исследовании II фазы безрецидивная выживаемость составила 8,8 месяцев и медиана общей выживаемости – 23,9 месяца. 38 больных живы при медиане наблюдения 30 месяцев. По данным независимого центрального пересмотра данных, частота объективных ответов составила 33% [14].
После получения этих обнадеживающих данных было инициировано международное многоцентровое рандомизированное исследование III фазы, сравнивающее сунитиниб с интерфероном– α (ИНФ– α ) в качестве первой линии лечения у 750 больных метастатическим РП. Дизайн исследования включал наличие гистологически подтвержденного светлоклеточного РП, измеряемых очагов, соматический статус по шкале ECOG 0 или 1, отсутствие предшествующей системной терапии. В исследование включали преимущественно больных с благоприятным и промежуточным прогнозом на основании прогностической модели MSKCC. Группы были сбалансированы по основным демографическим и прогностическим критериям. Пациентов рандомизировали 1:1, по 375 человек в каждую лечебную группу, режим дозирования сунитиниба 50 мг ежедневно в течение 4 недель, затем перерыв – 2 недели или ИНФ– α подкожно 3 раза в неделю в дозе 3 млн. ЕД на первой неделе, 6 млн. ЕД на второй неделе и 9 млн. ЕД впоследствии [15].
Медиана безрецидивной выживаемости оказалась существенно более продолжительной для больных, принимавших сунитиниб (11 месяцев), чем для тех, кто принимал ИНФ– α (5,1 месяцев), p α . В группе промежуточного и плохого прогноза медиана безрецидивной выживаемости была также более продолжительной в группе больных, принимавших сунитиниб, чем у пациентов, получавших ИНФ– α (10,8 мес. против 3,8 мес. и 3,9 мес. против 1,2 мес., соответственно) [15–17].
Окончательный анализ общей выживаемости продемонстрировал, что медиана общей выживаемости в группе сунитиниба составила более 2–х лет (26,4 мес.), по сравнению с 21,8 мес. в группе принимавших ИНФ– α (р=0,051). Медиана общей выживаемости после цензурирования больных, перешедших из группы интерферона– α в группу сунитиниба, составила 26,4 мес. для леченных сунитинибом и 20 мес. для больных, принимавших интерферон– α (р=0,0362) [16,17].
Согласно двум исследовательским и независимой центральной оценкам объективный ответ статистически значимо (p α (8%) (табл. 2). Независимая оценка зафиксировала частичный ответ у 143 пациентов (39%), получавших сунитиниб, и у 29 пациентов (8%), получавших ИНФ– α . Стабилизация заболевания наблюдалась у 146 пациентов (40%), получавших сунитиниб, и у 165 пациентов (48%), получавших ИНФ– α [16,17].
Наиболее часто сообщаемые негематологические побочные эффекты всех степеней в клиническом исследовании III фазы включали диарею, утомляемость, тошноту, изменения ротовой полости, рвоту, гипертонию и ладонно–подошвенный синдром. Наиболее клинически значимые негематологические побочные эффекты 3 и 4 степени тяжести выявлялись более часто в группе сунитиниба, чем в группе пациентов, получавших ИНФ– α (p α , чем сунитиниб (12% против 7%, p α (p α (23%), в сравнении с сунитинибом (16%) [16].
Следует отметить, что общая частота зарегистрированных побочных эффектов 3 и 4 степени тяжести относительно низка и составляет не более 10%, а большинство побочных эффектов обратимы и не заканчиваются прекращением приема сунитиниба. При необходимости нежелательные явления могут быть купированы подбором дозы или перерывом в приеме препарата. Сунитиниб обладает важным преимуществом по сравнению с другими ингибиторами тирозинкиназ: препарат выпускается в трех различных дозировках (50 мг, 37,5 мг, 25 мг), что предоставляет врачу возможность гибко регулировать дозу в зависимости от выраженности токсических проявлений.
В настоящее время исследование препарата продолжается в качестве адъювантного лечения в двух крупных исследованиях по изучению безрецидивной выживаемости больных, принимавших сунитиниб, сорафениб или плацебо ( ASSURE ) и по использованию сунитиниба или плацебо у пациентов высокого риска с Т3, Т4 или N+ заболеванием ( S–TRAC ). Кроме того, планируется изучение роли сунитиниба у больных с несветлоклеточным вариантом опухоли почки и сочетание с другими таргетными или химиотерапевтическими препаратами.
Заключение . Данные многоцентровых рандомизированных клинических исследований, изучавших Сутент (сунитиниб) в качестве первой и второй линии лечения на большой когорте больных метастатическим РП, показали его высокую эффективность при низкой частоте зарегистрированных побочных эффектов. В настоящее время Сутент является безопасным и эффективным препаратом для лечения больных метастатическим РП благоприятного и промежуточного прогноза и может быть рекомендован как препарат выбора у данной группы пациентов.
Согласно данным 3 фазы клинического исследования S-TRAC, сунитиниб после нефрэктомии на 24% увеличивает выживаемость без прогрессирования (ВБП) у больных почечно-клеточным раком (ПКР) высокого риска. В статье, недавно опубликованной в Annals of Oncology, исследователи оценили качество жизни пациентов.
В исследовании приняли участие более 600 больных ПКР, которые после нефрэктомии, находясь в группе высокого риска, принимали плацебо или сунитиниб 50 мг в режиме 4/2. Лечение продолжалось до 9 циклов или до прогрессирования или непереносимой токсичности. Сунитиниб на 24% снижал риск рецидива во всей популяции исследования и особенно в группе больных с наибольшим риском (T3/T4 с изменениями в лимфоузлах) – на 27%.
В группе сунитиниба пациенты получали лечение в среднем 9,5 месяца, в группе плацебо – 10,3 месяца. Из 306 пациентов, которые получали сунитиниб, 71% продолжали лечение более 8 месяцев (6 циклов), 56% получили весь запланированный объем. Нежелательные явления в группе сунитиниба реализовывались в среднем в течение первого месяца лечения. Допускали задержки лечения и редукция дозы до 37,5 мг в сутки. Медиана времени до первой редукции дозы составила 2,9 месяца. Если задержка лечения составляла более 6 недель или требовалась редукция дозы более чем 37,5 мг, пациента исключали из исследования.
В группе сунитиниба общий соматический статус при использовании шкалы EORTCQLQ-C30 был значительно ниже. Пациенты докладывали о симптомах, характерных для сунитиниба: снижение аппетита, диарея. Наиболее частыми нежелательными явлениями были диарея (56,9% в группе сунитиниба против 21,4% в группе плацебо), ладонно-подошвенный синдром (ЛПС; 50,3% против 10,2%), артериальная гипертензия (36,9% против 11,8%).
В общей сложности уровень нежелательных явлений соответствовал данным, известным для сунитиниба ранее (например, при применении при метастатическом ПКР). Исключение составил ЛПС 3-4 ст., который чаще встречался в исследовании S-TRAC. Также ЛПС часто встречался в исследовании ASSURE с сорафенибом и сунитинибом и в исследовании PROTECT с пазопанибом.
Опубликованы отдаленные результаты исследования 3 фазы IBCSG 23-01, из которых следует, что подмышечная лимфодиссекция у больных ранним раком молочной железы (РМЖ) при наличии микрометастазов в сторожевых лимфоузлах не увеличивает безрецидивную выживаемость (БВ).
Примерно у трети больных немелкоклеточным раком легкого (НМРЛ) заболевание диагностируется в III стадии. Это очень разнородная группа больных, которую делят на IIIA стадию с наличием N2 (метастазы в медиастинальные лимфоузлы со стороны поражения) и IIIB стадию с N3 (метастазы в контралатеральные медиастинальные и надключичные лимфоузлы).
Результаты II фазы рандомизированного клинического исследования, в котором комбинация атезолизумаба и бевацизумаба сравнивалась с монотерапией сунитинибом или атезолизумабом у пациентов с метастатическим почечно-клеточным раком (мПКР) , ранее не получавших лечение, были…
FDA приняло дополнительное заявление на регистрацию и предоставило право приоритетного рассмотрения по расширенным показаниям к применению лекарственного препарата церитиниб (ceritinib, Зикадия) компании Новартис (Novartis) для первой линии терапии пациентов с метастатическим…
Компания Tesaro на ежегодной конференции Общества онкогинекологии представила результаты III фазы клинического исследования (NCT01847274) по эффективности противоопухолевого препарата нирапариб (niraparib) у пациенток, страдающих от рака яичников, чувствительного к препаратам…
Компания TG Therapeutic объявила о результатах III фазы клинического исследования GENUINE (NCT02301156), в котором оценивалась эффективность комбинации ублитуксимаба (ublituximab, TG-1101) и ибрутиниба (ibrutinib, Imbruvica) по сравнению с монотерапией только ибрутинибом у…
Компания AstraZeneca анонсировала предварительные результаты III фазы клинического исследования OLYMPIAD (NCT02000622), в котором изучалась эффективность и безопасность использования противоопухолевого препарата олапариб (olaparib) в монотерапии по сравнению со стандартом…
Примерно 10-12% больных немелкоклеточным раком легкого (НМРЛ) европейской популяции имеют активирующую мутацию гена рецептора эпидермального фактора роста EGFR.
В журнале The Lancet опубликованы убедительные результаты клинических исследований регорафениба (regorafenib, Стиварга) в терапии прогрессирующей гепатоклеточной карциномы .
Ключевыми и долгожданными событиями 2016 года можно назвать регистрацию в Государственном реестре лекарственных средств трех препаратов, относящихся к новому классу иммуноонкологических препаратов – ингибиторов точек иммунного ответа: ингибитора CTLA-4 - Ервой® (ипилимумаб);…
По результатам второй фазы рандомизированных клинических испытаний, проведенных в Институте рака Dana-Farber в США, экспериментальный противоопухолевый препарат кабозантиниб (cabozantinib) превзошел по эффективности стандартную терапию в первой линии у пациентов с…
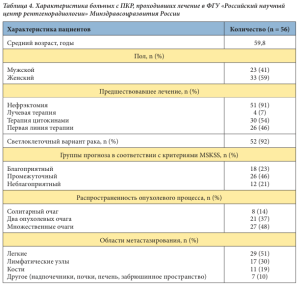
На рак почки в структуре онкологических заболеваний приходится около 4%. По темпам прироста онкологической заболеваемости в России почечно-клеточный рак (ПКР) устойчиво занимает у женщин третье место после рака полости рта и глотки и центральной нервной системы (ЦНС), а у мужчин – четвертое место после рака предстательной и щитовидной желез и ЦНС. Ежегодно в России от рака почки умирают более 8 тыс. человек. Стандартизованный показатель заболеваемости населения России злокачественными опухолями почки составляет 8,09 на 100 тыс. населения [1]. Рост заболеваемости раком почки частично обусловлен как улучшением диагностики на основе современных инструментальных исследований, таких как трансабдоминальное ультразвуковое исследование (УЗИ), компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), так и ростом истинной заболеваемости раком почки. В настоящее время в 25–40% случаев заболевание выявляют случайно при профилактическом обследовании. Мужчины болеют в 2 раза чаще, чем женщины, в основном на 5–7-м десятилетии жизни. Частота почечно-клеточного рака постепенно увеличивается. Пятилетняя выживаемость при этой патологии достигает 60%. Однако при наличии метастазов 2-летняя выживаемость колеблется от 0 до 20%. От 25 до 50% больных имеют метастазы на момент установления диагноза. Более того, приблизительно у половины больных после радикальной нефрэктомии впоследствии появляются метастазы.
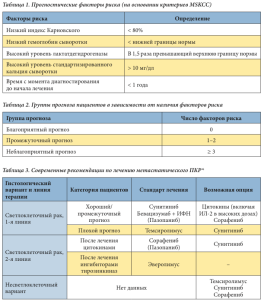
Ангиогенез является одним из ключевых патогенетических механизмов роста злокачественного новообразования и диссеминации опухолевого процесса, в связи с чем одними из основных целей противоопухолевой таргетной терапии являются внутриклеточные мишени, вовлеченные в процесс стимуляции ангиогенеза и опухолевого роста. В настоящее время разработано несколько препаратов, влияющих на разные внутриклеточные мишени, относящиеся к патогенетическому пути, связанному с инактивацией гена VHL. Сунитиниб – таблетированный ингибитор тирозинкиназ, который воздействует на все известные виды рецепторов к PDGF и VEGF (VEGFRs, PDGFR-a, PDGFR-b, c-KIT и FLT-3), участвующих в процессе роста опухоли, патологическом ангиогенезе и метастазировании. Препарат был одобрен в Европе с 2007 г. в качестве первой и второй линий терапии распространенного рака почки и в настоящее время рекомендован в качестве стандарта лечения больных с благоприятным и промежуточным прогнозом заболевания по критериям MSKCC (Memorial Sloan-Kettering Cancer Center) (табл. 1). Основываясь на числе имеющихся факторов риска, R.J. Motzer и соавт. [2, 3] предложили стратифицировать больных на три группы прогноза (табл. 2). На основании проведенных многоцентровых международных исследований [4–6] была разработана и предложена тактика проведения лечения данной болезни в зависимости от группы прогноза (табл. 3).
Материалы и методы
Мониторинг выполнялся каждые 30 дней. При визитах выявлялись нежелательные явления, проводились лабораторные исследования: биохимический анализ крови (глюкоза, билирубин общий, щелочная фосфатаза, аланиновая трансаминаза, аспарагиновая трансаминаза, мочевина, креатинин, коагулограмма), общий анализ мочи. Один раз в 3 месяца выполнялась КТ грудной клетки, брюшной полости, органов малого таза с болюсным усилением; один раз в 6 месяцев – остеосцинтиграфия, по показаниям – электрокардиограмма, при наличии клинических проявлений – КТ головного мозга.
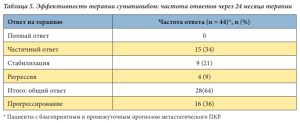
Представлен анализ результатов лечения сунитинибом для пациентов с благоприятным и промежуточным прогнозом заболевания в первой и второй линии терапии (n = 44). Через 24 месяца терапии частичный ответ зарегистрирован у 15 (34%) из 44 больных, стабилизация – у 9 (20%) и регрессия – у 4 (9%). Помимо этого, у 12 (27%) больных отмечена стабилизация в течение 15 месяцев, у 4 (9%) больных – стабилизация в течение 9 месяцев с последующим прогрессированием заболевания (табл. 5). Шесть больных погибли в течение первых шести месяцев лечения. Данные больные относились к группе неблагоприятного прогноза метастатичес- кого ПКР, имели множественные метастазы, в большинстве случаев – костные.
Основными побочными действиями препарата были повышение артериального давления, диарея, слабость. Степень тяжести побочных действий не превышала 2-й. Все побочные действия хорошо контролировались и медикаментозно купировались.
В процессе применения сунитиниба в стандартном режиме первой и второй линии терапии ПКР нами было выявлено, что безрецидивная выживаемость в общей исследуемой популяции больных почечно-клеточным раком в среднем составила 13 месяцев, общая выживаемость – 22 месяца. Было показано, что результаты терапии сунитинибом лучше в группе пациентов с единичными паренхиматозными метастазами, чем у больных, имеющих метастазы в кости и/или множественные метастатические очаги (> 2).
Применение сунитиниба у больных ПКР увеличивает общую и безрецидивную выживаемость. Терапия сунитинибом редко осложняется развитием выраженных нежелательных явлений (3–4-й степени тяжести), требующих проведения специального лечения и/или отмены проводимой терапии, и в целом хорошо переносится.
Литература:
1. Чиссов В.И., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2007 г. М., 2008.
2. Motzer R.J., Bacik J., Murphy B.A. et al. Interferon-alfa as a comparative treatment for clinical trials of new therapies against advanced renal cell carcinoma // J. Clin. Oncol. 2002. Vol. 20. No 1. P. 289–296.
3. Motzer R.J., Hutson T.E., Tomczak P. et al. Sunitinib versus interferon alfa in metastatic renal-cell carcinoma // N. Engl. J. Med. 2007. Vol. 356. No 2. P. 115–124.
4. Feldman D.R., Kondagunta G.V., Ronnen E.A. et al. Phase I trial of be- vacizumab plus sunitinib in patients (pts) with metastatic renal cell carcinoma (mRCC) // J. Clin. Oncol. 2009. Vol. 27. No 9. P. 1432–1439.
5. Минимальные клинические рекомендации Европейского общества медицинской онкологии (ESMO) / под ред. С.А. Тюляндина, Д.А. Носова, Н.И. Переводчикова. М.: Издательская группа РОНЦ им. Н.Н. Блохина РАМН, 2010. 436 с.
6. Giberti C., Oneto F., Martorana G. et al. Radical nephrectomy for renal cell carcinoma: long-term results and prognostic factors on a series of 328 cases // Eur. Urol. 1997. Vol. 31. No 1. P. 40–48

Таргетная терапия - одна из новейших разработок в лечении рака. Она препятствует его развитию на молекулярном уровне. Таргетные препараты нарушают кровоснабжение злокачественных клеток и противодействуют их воспроизводству. Они блокируют команды, сигнализирующие патологическим клеткам о росте.
В отличие от стандартной химиотерапии, которая влияет на все клетки организма, таргетная воздействует только на злокачественные. Ее задача – препятствовать специфическим молекулам, вовлеченным в рост опухоли, чтобы сдерживать развитие и распространение болезни. Поэтому данный вид лечения вызывает меньшее количество побочных эффектов.
Почки изобилуют числом кровеносных сосудов, что способствует росту опухолевых клеток. По этой причине при раке почек таргетная терапия эффективна, предлагая ангиогенные препараты. Они воздействуют на сосуды, которые ведут к злокачественному новообразованию.
Лечение рака почки в Израиле является персонализированным и включает наиболее передовые методы лечения с наименьшим количеством возможных побочных эффектов – лапароскопическую и роботизированную хирургию, криодеструкцию и радиочастотную абляцию, таргетную терапию.
Таргетные препараты рекомендуются:
- при неоперабельной первичной опухоли;
- при метастатическом раке почки;
- в рамках клинических испытаний, чтобы предотвратить рецидив заболевания после хирургического вмешательства.
Лечение предполагает применение одного или нескольких лекарственных средств, для каждого пациента подбирается индивидуальный план лечения. С целью определения наиболее эффективного варианта используется система стратификации риска, применяется генетическое тестирование. Состояние здоровья, особенности конкретного случая болезни влияют на выбор. Во время консультации с врачом в Израиле у пациента есть возможность задать интересующие вопросы (примерный список):
- Принесет ли результаты в конкретном случае таргетная терапия, окажет ли помощь?
- Какие препараты доступны?
- Почему мне была предложена таргетная терапия?
- Что является целью лечения?
- Есть ли другой выбор?
- Каковы краткосрочные и долгосрочные побочные эффекты?
- Какие меры можно предпринять, чтобы снизить действие нежелательных побочных явлений или предотвратить их?
- Как долго будет длиться лечение?
Препараты таргетной терапии рака почки первой линии
В основном данные виды лекарств используются, чтобы уменьшить или контролировать течение болезни при распространенном опухолевом процессе. По результатам исследований и отзывам таргетная терапия рака почек останавливает или замедляет развитие болезни на нескольких месяцев, а иногда - лет.
Обычно лекарственные средства принимают, пока они способны контролировать заболевание. Пациент встречается с врачом каждые 4-6 недель, также сдает анализы крови. Раз в три месяца выполняется сканирование, что выяснить, результативно ли лечение.
Рассмотрим схемы таргетной терапии рака почки. Сунитиниб (Сутент) в основном рекомендуют первым при наличии вторичных очагов. Другой распространенный препарат - Пазопаниб (Pazopanib). Эти лекарства блокируют сигналы о росте в злокачественных клетках и называются ингибиторами тирозинкиназы. Также в ряде случаев назначают сорафениб (Nexavar).
Сунитиниб (Sunitinib)
Сунитиниб имеет другие название - сутент. Его используют на 3 или 4 стадии заболевания. Принимается в капсулах, ежедневно на протяжении 4-х недель с последующим перерывом в 2 недели.
Этот препарат относится к группе ингибиторов тирозинкиназы. Он блокирует внутриклеточные белки под названием тирозинкиназы в опухолевых клетках, которые дают сигналы к росту и делению, связывают клетки с ядром и клеточными структурами. Помимо этого, сутент препятствует кровоснабжению, лишая патологические клетки поступления питательных веществ и кислорода.
Возможные нежелательные последствия приема включают усталость, повышенный риск инфекции в связи с низким уровнем лейкоцитов, анемию, изменения вкусовых ощущений, диарею, кожную сыпь и зуд, ладонно-подошвенную кератодермию, артериальную гипертензию. Сунитиниб может ухудшить работу щитовидной железы, по этой причине больной регулярно сдает анализы крови, чтобы проверить это.
Пазопаниб (Pazopanib)
Пазопаниб – ингибитор роста рака, врач может порекомендовать препарат в качестве первичного лечения при распространенном опухолевом процессе и как вторичное после применения интерферона или интерлейкина-2. Выпускается в таблетках, его принимают каждый день. К потенциальным отрицательным последствиям приема относят: диарею, ладонно-подошвенную кератодермию, сыпь и зуд кожи, повышенную утомляемость, тошноту.
Препараты таргетной терапии рака почки второй линии
Если лечение перестает работать и рак начинает снова расти, врач назначает вторую линию терапии. Назначен может быть один из упомянутых выше препаратов. Либо врач предложит бевацизумаб (Авастин) внутривенно с интерфероном. Другие лекарства - Темсиролимус (Torisel) или эверолимус (Afinitor). Они блокируют сигналы о росте, и называются MTOR блокаторами (MTOR – белок, управляющий ростом, делением и метаболизмом клетки).
Авастин в таргетной терапии рака почки и интерферон
Бевацизумаб (Авастин) – моноклональное антитело, препятствует развитию кровеносных сосудов в опухолевом новообразовании. Препарат назначают внутривенно каждые две недели, интерферон - три раза в неделю в виде инъекций.
Чаще всего при приеме интерферона наблюдаются гриппоподобные симптомы на протяжении недели – двух. Прием парацетомола за полчаса до инъекции может помочь – предотвратит их или уменьшит. Среди других нежелательных явлений отмечают кровотечения из носа, запор – диарею, депрессию, тошноту, гипертонию.
Темсиролимус (Torisel)
Темсиролимус дают внутривенно один раз в неделю. Он блокирует сигналы о росте в злокачественных клетках, относится к препаратам MTOR ингибиторам. Рекомендуется при распространенном опухолевом процессе в качестве вторичной таргетной терапии рака почки. К нежелательным явлениям терапии относят: сыпь, зуд и красноту кожи, тошноту, потерю аппетита, диарею, воспаление в полости рта; низкие уровни клеток крови.
Эверолимус (Afinitor)
Эверолимус выпускается в таблетках, его принимают раз в день. Как и темсиролимус, Afinitor – это ингибитор MTOR, блокирующий сигналы о росте для злокачественных клеток. Врачи применяют его в качестве второй линии таргетной терапии рака почки при метастазах, когда нет реакции на сутент и сорафениб.
К возможным нежелательным явлениям терапии относят низкую устойчивость к инфекции, усталость и одышку из-за недостаточного уровня эритроцитов, повышенное содержание холестерина и сахара в крови, воспалительный процесс в полости рта; высыпания, зуд и сухость кожи; тошноту.
Сорафениб (Nexavar)
Принимается ежедневно, перорально. Он работает в двух направлениях таргетной терапии рака почки: блокирует сигналы о росте и процесс агиогенеза в злокачественном новообразовании. Используется при наличии вторичных очагов рака почки, когда неэффективны препараты биологической терапии, у пациента наблюдается непереносимость к сутенту.
Среди потенциальных нежелательных явлений отмечают: диарею, чрезмерную утомляемость, ладонно-подошвенную эритродизестезию, тошноту, истончение волос.
На сегодняшний день нет методов лечения, уменьшающих вероятность рецидива рака почки после хирургии. Но проводится большое количество исследований в мире, в рамках которых изучаются таргетные препараты. Также разрабатываются новые лекарства данного вида лечения.
У каждого препарата - свои побочные действия. Большинство людей, принимая их, испытывают усталость. В зависимости от назначенного лекарства побочные эффекты включают: диарею, кожные высыпания, боль в руках и ногах. Врач подробно обсуждает с пациентом этот вопрос и консультирует, как лучше справляться с ними.
Читайте также:

