Шелехов а в лечение осложненного рака прямой кишки
Полный текст:
- Аннотация
- Об авторах
- Список литературы
- Cited By
Представлены ближайшие результаты рентген-эндоваскулярного гемостаза пациентов, страдающих злокачественными новообразованиями ректосигмоидного отдела толстой кишки и прямой кишки, осложненных кровотечением. Пациенты были распределены на основную (n=16, проводился рентгенэндоваскулярный гемостаз) и контрольную группу (n=17, проводились консервативные методы гемостаза). После гемостаза больным раком прямой кишки в сравниваемых группах проводилась предоперационная лучевая терапия с последующей радикальной операцией, при раке ректосигмоидного отдела – оперативное лечение. При одинаковой медиане кровопотери в основной группе использовалось значимо меньшее количество и объем продуктов донорской крови, чем в контрольной (p
доктор медицинских наук, профессор кафедры онкологии, Иркутская государственная медицинская академия последипломного образования Минздрава России (г. Иркутск, Российская Федерация)
доктор медицинских наук, профессор кафедры онкологии, Иркутская государственная медицинская академия последипломного образования Минздрава России (г. Иркутск, Российская Федерация)
доктор медицинских наук, профессор кафедры онкологии, Иркутская государственная медицинская академия последипломного образования Минздрава России (г. Иркутск, Российская Федерация)
кандидат медицинских наук, ассистент кафедры онкологии, Иркутская государственная медицинская академия последипломного образования Минздрава России (г. Иркутск, Российская Федерация)
1. Александров В.Б. Рак прямой кишки. М.: Вузовская книга; 2001, 208 с.
2. Francisco R., Díaz G., Cadahia V., Velázquez R.F., Giganto F., González O., Rodrigo L. Lower GI bleeding secondary to a stromal rectal tumor (rectal GIST). Rev Esp Enferm Dig. 2006 May; 98 (5): 387–9.
3. Ohhigashi S., Nishio T., Watanabe F., Matsusako M. Experience with radiofrequency ablation in the treatment of pelvic recurrence in rectal cancer: report of two cases. Dis Colon Rectum. 2001 May; 44 (5): 741–5.
4. Breen E. Pathophysiology and natural history of lower gastrointestinal bleeding // Semin. Colon Rectal Surg. 1997; 8 (12). P. 128–138.
5. Hoedema R.E., Luchtefeld M.A. The management of lower gastrointestinal hemorrhage. Dis Colon Rectum. 2005 Nov; 48 (11): 2010–24.
6. Liu L., Cao C., Zhu Y., Li D., Feng H., Luo J., Tang Z., Liu P., Lu K., Ju H., Zhang N. Preoperative chemoradiotherapy with 5-fluorouracil and oxaliplatin for locally advanced rectal cancer: long-term results of a phase II trial. Med Oncol. 2015 Mar; 32 (3): 70. doi: 10.1007/s12032-015-0512-3.
7. Воробьев А.И., Городецкий В.М., Шулутко Е.М., Васильев С.А. Острая массивная кровопотеря. М.: ГОЭТАР-МЕД; 2001, 176 с.
8. Ермолов А.С., Сахарова Е. А., Худенко Н.В., Тихомирова Н.И., Хватов В.Б. Количественная оценка объема и степени тяжести интраоперационной кровопотери в хирургической практике. Гематология и трансфузиология. 2005; Т. 4, № 50: 27–32.
9. Бессмертный Б.С. Математическая статистика в клинической, профилактической и экспериментальной медицине. М.: Медицина; 1967. 304 c.
10. Begg C., Cho M., Eastwood S., Horton R., Moher D., Olkin I., Pitkin R., Rennie D., Schulz K.F., Simel D., Stroup D.F. Improving the quality of reporting of randomized controlled trials: the CONSORT statement JAMA. 1996 Aug 28; 276 (8): 637–9.
11. Tohmé C., Chakhtoura G., Abboud B., Noun R., Sarkis R, Ingea H, Farah P, Ghossain A. Subtotal or total colectomy as surgical treatment of left-sided occlusive colon cancer. J Med Liban. 2008 Oct-Dec; 56 (4): 198–202.
12. Hsu T.C. One-Stage resection and anastomosis for acute obstruction of the left colon. Diseases of the Colon & Rectum. 1998; 41 (Issue 1): 28–32.
13. Vetter C. Preoperative radio-chemotherapy in rectal carcinoma. Forestalling colostomy. MMW Fortschr Med. 2003 Oct 9; 145 (41): 13.
14. Coco C., Verbo A., Manno A., Mattana C., Covino M., Pedretti G., Petito L., Rizzo G., Picciocchi A. Impact of emergency surgery in the outcome of rectal and left colon carcinoma. World J Surg. 2005 Nov; 29(11): 1458–64.
15. Corsale I., Foglia E., Mandato M., Rigutini M. Intestinal occlusion caused by malignant neoplasia of the colon: surgical strategy. G Chir. 2003 Mar; 24 (3): 86–91.
16. Афанасьев С.Г., Старцева Ж.А., Тарасова А.С., Усова А.В., Самцов Е.Н. Результаты комбинированного лечения рака прямой кишки с применением пролонгированной предоперационной химиолучевой терапии. Сибирский онкологический журнал; 2012. № 6: 5–12.
17. Ольшанский М.С., Коротких Н.Н., Евтеев В.В. Ближайшие и отдаленные результаты использования селективной масляной химиоэмболизации ректальных артерий в комплексном лечении рака прямой кишки. Медицинские науки. 2012; 2: 321–324.
18. Bloomfeld R.S., Rockey D.C., Shetzline M.A. Endoscopic therapy of acute diverticular hemorrhage. Am J Gastroenterol. 2001 Aug; 96 (8): 2367–72.
19. Jensen D.M., Machicado G.A., Jutabha R., Kovacs T.O. Urgent colonoscopy for the diagnosis and treatment of severe diverticular hemorrhage. N Engl J Med. 2000 Jan 13; 342 (2): 78–82.
20. Kovacs T.O., Jensen D.M. Recent advances in the endoscopic diagnosis and therapy of upper gastrointestinal, small intestinal, and colonic bleeding. Med Clin North Am. 2002 Nov; 86 (6): 1319–56.
21. Vernava A.M., Moore B.A., Longo W.E., Johnson F.E. Lower gastrointestinal bleeding. Dis Colon Rectum. 1997 Jul; 40 (7): 846–58.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
В статье проанализированы особенности медицинских методологических подходов к ведению пациентов с местнораспространенным раком прямой кишки с гнойно-воспалительными осложнениями. Описаны возможности и преимущества предоперационной химиолучевой терапии. Представлен собственный клинический опыт ведения пациентки с гнойными осложнениями рака прямой кишки.
В статье проанализированы особенности медицинских методологических подходов к ведению пациентов с местнораспространенным раком прямой кишки с гнойно-воспалительными осложнениями. Описаны возможности и преимущества предоперационной химиолучевой терапии. Представлен собственный клинический опыт ведения пациентки с гнойными осложнениями рака прямой кишки.
Проблема лечения рака прямой кишки актуальна во всем мире. Зачастую добиться успеха в лечении мешают ранние проявления осложнений опухоли прямой кишки.
По данным многочисленных медицинских статистических исследований, местнораспространенный колоректальный рак (МРКРР), или рак прямой кишки, является широко распространенной злокачественной патологией. Его доля в структуре злокачественных новообразований неуклонно растет [1, 2]. Ежегодно в мире этим видом рака заболевают около 1 млн человек, причем не менее 50% пациентов умирают в первый год наблюдения [3]. В России в общей структуре онкопатологии злокачественные опухоли толстой кишки занимают порядка 7,6%, прямой кишки – 5,9% [1]. Рак толстой и прямой кишки развивается быстро, практически незаметно и бессимптомно. Поэтому у большинства пациентов опухоль обнаруживается на стадии метастазирования в печень или осложнений, что существенно усугубляет течение патологического процесса.
Методология лечения
Нередко рак прямой кишки осложняется параканкрозным деструктивным нагноением [4, 5]. Одно из таких осложнений – анальный свищ. Данная патология вызывает задержку в назначении специального противоопухолевого лечения, а иногда и вовсе становится поводом для отказа от противоопухолевой лекарственной терапии.
Следует отметить, что аноректальный свищ может быть не следствием рака прямой кишки, а его причиной: у пациентов с длительно существующим (до 20 лет) анальным свищом выявляются в дальнейшем опухоли в данной области [6]. Такое осложнение может проявиться при метастатическом поражении промежности на фоне новообразования толстой кишки [7]. В ряде случаев формирование свищевого хода может повлечь за собой ухудшение состояния пациента за счет присоединения новых осложнений, таких как гангрена Фурнье, парапроктит, забрюшинная флегмона, что делает невозможным противоопухолевое лечение [8].
Кроме того, не следует забывать о совокупности ряда осложнений, затрудняющих процесс излечения. К таким неблагоприятным прогностическим факторам относят:
- локализацию опухоли в нижнеампулярном отделе прямой кишки, лишенном фасциального футляра;
- инвазию опухоли в стенки сосудов или нервную ткань;
- значительное поражение регионарных лимфатических узлов;
- распространение опухоли в ткани в сторону предполагаемого края резекции [9, 10].
Методология лечения основана на двух важнейших аспектах – неуклонном прогрессе хирургических технологий и внедрении новейших методик лучевой и лекарственной противоопухолевой терапии [11]. В настоящее время широко используется комбинированный принцип лечения. Однако многофакторность осложнений может затруднить выбор оптимального метода лечения и вероятностный прогноз. Кроме того, выбор зависит от точности и полноты диагностики и полученной на этапе дооперационного исследования информации о генезе и локализации опухоли [12].
Общепринятой тактикой лечения в таких случаях, а также в случае местнораспространенного рака прямой кишки без подобного осложнения является предоперационная химиолучевая терапия с последующим хирургическим этапом спустя 6–10 недель [13].
В исследованиях показано, что послеоперационное облучение не оказывает должного эффекта на лечение осложненного МРКРР и не влияет существенно на выживаемость пациентов [14]. В связи с этим возникла идея предоперационной химиолучевой терапии (ХЛТ), которая способствует значительной предварительной гибели опухолевых клеток, а значит, снижению вероятности распространения живых опухолевых клеток в органы и ткани во время операции. В процессе использования данного метода располагающим фактором была названа такая причина, как более высокая оксигенация и чувствительность к облучению клеток опухоли до операции. По мнению исследователей, предварительная регрессия раковой опухоли повышает возможность сфинктер-сберегающих операций и снижает глубину пагубного воздействия облучения органов малого таза [15].
На сегодняшний день доказана целесообразность и перспективность применения неоадъювантной ХЛТ с фторпиримидинами и оксалиплатином в сочетании с оперативным лечением [9]. Использование пероральных фторпиримидинов показано для профилактики инфузионных осложнений. Хорошо апробированным фторпиримидином является капецитабин, который в сочетании с оксалиплатином демонстрирует эффективность, сопоставимую с таковой типовой химиотерапии в режиме FOLFOX [16].
Предоперационная ХЛТ с 5-фторурацилом – классический прием в лечении МРКРР. По итогам примененного предоперационного лечения отмечается статистически значимое снижение количества пациентов с глубоким прорастанием опухоли в мезоректальную клетчатку и поражением регионарных лимфоузлов [9].
По мнению ряда авторов, осложнения рака прямой кишки могут быть серьезным противопоказанием к проведению неоадъювантной лучевой терапии [15, 17]. В этом случае некоторые клиницисты рекомендуют эндохирургические методы, позволяющие восстановить толстокишечный пассаж, и неоадъювантную лучевую терапию [5, 18].
Латеральный край резекции (pCRM) служит важнейшим критерием качества проведенного оперативного вмешательства и ведущим фактором, воздействующим на развитие рецидивов и метастазирование у пациентов с диагнозом МРКРР [3, 12]. Клиницистами было показано, что частота вовлечения pCRM возрастает при внедрении новообразования в мезоректальную клетчатку, фасцию, серозную оболочку прямой кишки и не зависит от локализации опухоли и поражения лимфоузлов. На безрецидивную выживаемость пролеченных больных негативно влияют стадия заболевания и радикальность операции [9].
Тактика ведения пациентов с диагнозом МРКРР остается неопределенной при инфильтрации опухолью мезоректальной фасции или внедрении за ее пределы. Осложненное течение МРКРР определяет необходимость применения нестандартных подходов и проведения комплексного лечения с применением предоперационной ХЛТ и последующей хирургической резекцией. Показан персонализированный подход к пациентам с различными осложнениями. Разработка разновекторных программ лечения с использованием новейших сенсибилизаторов является одним из актуальных направлений в области онкопроктологии [19].
Клиницисты отмечают, что больным МРКРР, которым проведены радикальные комбинированные операции, при наличии выраженного гнойного воспаления с абсцессом, формированием свищей с органами, вовлеченными в процесс, и их вскрытием во время мобилизации кишки необходимо выполнять операцию по удалению кишки. Удельный вес операций, позволяющих сохранить сфинктер, значителен – 62,2%. Осложнения после клинически радикальных операций отмечаются у 9,6% пациентов. Летальность в таком случае среди пациентов в возрасте старше 60 лет составляет 7,9% и, как правило, связана с осложнениями и вовлечением в процесс других органов. В этой связи для больных МРКРР с осложнениями выполнение подобных операций целесообразно и оправданно при дополнительной предоперационной ХЛТ [20].
В результате многолетних наблюдений установлено, что наиболее эффективным методом предупреждения постоперативных гнойно-воспалительных осложнений является адекватная антибиотическая профилактика, нацеленная на те виды микроорганизмов, которые с наибольшей вероятностью могут инфицировать зону операции и вызывать нагноение. Антибиотики пациентам с МРКРР назначаются всегда, поскольку при большом объеме операции имеет место вскрытие кишки, что создает условия для попадания бактерий в брюшную полость. Необходимо учесть, что больные МРКРР по иммунному статусу являются больными с высоким риском инфицирования. Гнойно-воспалительные и септические осложнения чаще регистрируются у пациентов с лишним весом и сопутствующими соматическими заболеваниями [21].
Клинический случай
Больная О., 58 лет, обратилась в Краснодарский клинический онкологический диспансер № 1 в ноябре 2017 г. с жалобами на патологические выделения из прямой кишки, в том числе крови. Перечисленные жалобы отмечала с 2015 г., однако за медицинской помощью в течение двух лет не обращалась.
При обследовании выявлена распадающаяся опухоль нижнеампулярного отдела прямой кишки с формированием параканкрозного воспаления и свищевого хода в центре с гнойным отделяемым. По данным компьютерного рентгенологического исследования органов грудной, брюшной полостей и малого таза, визуализирована инфильтративная бластома прямой кишки с распространением на анальную область и мягкие ткани правой ягодицы, тазовая, внутренняя подвздошная, двусторонняя паховая лимфаденопатия. Метастатического поражения паренхиматозных органов не выявлено. Патоморфологически опухоль представлена высокодифференцированной аденокарциномой. При анализе соматических мутаций в гене KRAS методом полимеразной цепной реакции в режиме реального времени мутаций в кодонах 12/13 и 61 гена KRAS не обнаружено.
В качестве первого этапа лечения выполнена разгрузочная илеостомия.
С учетом клинической картины синдрома системной воспалительной реакции, локальных гнойно-некротических изменений тканей проведение предоперационной химиолучевой терапии на момент первичного лечения представлялось невозможным. Было принято решение о проведении комплекса мероприятий по санации свищевого хода и назначении антибактериальной терапии в адекватном объеме для предотвращения гнойно-септических осложнений. В ходе бактериологического исследования отделяемого свищевого хода и прямой кишки были выделены возбудители Escherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa. Согласно данным антибактериальной чувствительности, назначена терапия комбинацией цефтаролина фосамила 600 мг дважды в сутки и амикацина 1,5 г один раз в сутки. По стабилизации состояния и стихании воспалительной реакции на восьмые сутки антибактериальной терапии начата химиотерапия по протоколу FOLFOX4. Реализовано четыре курса химиотерапии с выраженным клиническим эффектом в виде значительного стихания признаков локального воспаления, отсутствия отделяемого из свищевого хода, регрессии астении, нормализации температуры тела. Токсичность терапии была управляемой, отсрочек курсов не было.
Рентгенологическая картина в динамике представлена на рис. 1–3.
По решению мультидисциплинарного консилиума, 15 мая 2018 г. проведена дистанционная лучевая терапия (ДЛТ) на область опухоли и паховые области (40 Гр). Результаты контрольного обследования показали положительную динамику основной опухоли. Спустя шесть недель после ДЛТ выполнен хирургический этап лечения – брюшнопромежностная экстирпация прямой кишки с резекцией задней стенки влагалища. После удаления опухоли с ее ткани осуществлен посев, выделен возбудитель Staphylococcus epidermidis. Согласно данным антибиотикограммы, проведена антибактериальная терапия: пиперациллин + тазобактам 4,5 г трижды в сутки каждые восемь часов в течение семи дней. От проведения послеоперационной химиотерапии пациентка воздержалась.
Пациентка находится под наблюдением врача. На последнем визите в августе 2019 г. признаков прогрессирования заболевания не обнаружено.
Таким образом, удалось добиться полной ремиссии, безрецидивный период составляет 16 месяцев.
Рассмотренный случай – успешный пример реализации мультидисциплинарного подхода к лечению распространенного рака прямой кишки (участие хирургов, химиотерапевтов, радиотерапевтов, клинических фармакологов, специалистов по паллиативной помощи и поддерживающей терапии).
Среди факторов успешного лечения необходимо отметить тщательную санацию очагов гнойных осложнений местнораспространенного процесса с выключением прямой кишки из пассажа кишечного содержимого, тщательный подбор антибактериальной терапии, согласно данным посевов из свищей, опухоли, отделяемого дренажей. Таким образом, даже у непростой категории больных можно планировать и осуществлять адекватный объем противоопухолевого лечения.

- Группа особого риска: причины рака прямой кишки
- Полипы кишечника
- Стадии рака прямой кишки
- Чем может проявляться рак прямой кишки?
- Метастазы при раке прямой кишки
- Симптомы рака прямой кишки
- Диагностика рака прямой кишки
- Лечится ли рак прямой кишки?
- Варианты лечения рака прямой кишки на разных стадиях
- Профилактика рака прямой кишки
- Продолжительность жизни
- Цены на лечение рака прямой кишки
Группа особого риска: причины рака прямой кишки
В большинстве экономически развитых стран, за исключением Японии, рак прямой кишки — один из самых частых типов рака, встречающийся и у мужчин, и у женщин. Статистически достоверна взаимосвязь частоты развития рака прямой кишки и большого количества употребляемых в пищу мяса и животных жиров, дефицита в рационе питания грубой клетчатки и пищевых волокон, а также малоподвижного образа жизни. Рак прямой кишки занимает стабильное 3-е место в структуре заболеваемости злокачественными новообразованиями органов желудочно-кишечного тракта, составляет 45-55% среди новообразований кишечника.
К предраковым заболеваниям прямой кишки относят хронические воспалительные заболевания толстого кишечника: хронический проктит, хронический неспецифический язвенный проктосигмоидит, болезнь Крона.
Полипы кишечника
К заболеваниям с наиболее высокой онкогенностью относят полипоз кишечника из-за высокой частоты малигнизации (озлокачествления). Трансформация в рак происходит как при одиночных полипах в прямой кишке, так и при наличии множественных очагов. Особенно это касается случаев наследственного полипоза в семье.
В соответствии с классификацией Всемирной Организации Здравоохранения, аденомы кишки делятся на три разновидности: тубулярные, ворсинчато-тубулярные и ворсинчатые. Важную роль имеет первичная гистологическая диагностика биопсии полипов, полученной в ходе колоноскопии: например, ворсинчатые аденомы малигнизируются в 35-40% случаев, а в случае трубчатых аденом риск озлокачествления ниже - до 2-6%. Риск озлокачествления увеличивается в зависимости от размеров аденомы, особенно если ее диаметр более 1 см.

Когда опухоль прорастает в подслизистую основу, такой рак уже считается инвазивным, он может распространяться в лимфатические узлы и давать отдаленные метастазы.
Стадии рака прямой кишки
Опухоли прямой кишки классифицируются в соответствии с общепринятой системой TNM, в которой учитываются характеристики первичной опухоли (T), наличие очагов поражения в регионарных лимфатических узлах (N) и отдаленных метастазов (M).
Буква T может иметь индексы is, 1, 2, 3 и 4. Tis – опухоль, которая находится в пределах поверхностного слоя слизистой оболочки, не распространяется в лимфатические узлы и не метастазирует. T4 – рак, который пророс через всю толщу стенки прямой кишки и распространился в соседние органы.
Буква N может иметь индексы 0, 1 и 2. N0 – опухолевых очагов в регионарных лимфоузлах нет. N1 – очаги в 1–3 регионарных лимфоузлах или поражение брыжейки. N2 – очаги более чем в трех регионарных лимфатических узлах.
Буква M может иметь индексы 0 или 1. M0 – отдаленные метастазы отсутствуют. M1a – отдаленные метастазы в одном органе. M1b – отдаленные метастазы в двух и более органах, либо опухолевое поражение брюшины .
В зависимости от этих характеристик, выделяют пять стадий:
Чем может проявляться рак прямой кишки?
Прямая кишка (лат. rectum) — это конечный участок толстого кишечника длиной около 14-18 см, в котором заканчиваются пищеварительные процессы и происходит формирование каловых масс. Прямая кишка состоит из нескольких анатомических участков, имеющих различное эмбриональное происхождение и гистологическое строение , что обуславливает существенные различия в характере течения рака прямой кишки в зависимости от уровня её поражения.
Прямая кишка делится на 3 части:
- анальную (промежностную), длиной 2,5 – 3,0 см, в которой расположены мышцы-сфинктеры, управляющие процессом дефекации,
- среднюю – ампулярную, длиной 8,0-9,0 см, в которой происходит всасывание жидкой части пищевого комка и формируются каловые массы,
- надампулярную, покрытую брюшиной, длиною около 4,0-5,0 см.
Злокачественные новообразования прямой кишки чаще всего локализуются в ампулярном отделе (до 80 % случаев), реже всего - в аноректальном отделе (5-8 %).
В ампулярном и надампулярном отделах прямой кишки, покрытом однослойным железистым эпителием, чаще наблюдается железистый рак - аденокарцинома, солидный рак, перстневидно-клеточный, смешанный, скирр. В целом аденокарцинома составляет 96% от всех случаев колоректального рака. Эта опухоль развивается из железистых клеток слизистой оболочки, которые продуцируют слизь. Чаще всего, употребляя термин "колоректальный рак", врачи имеют в виду именно аденокарциному.
Аноректальный отдел прямой кишки, выстланный многослойным плоским неороговевающим эпителием, чаще поражает плоскоклеточный рак и меланома. Плоскоклеточный рак составляет около 90% злокачественных опухолей аноректального отдела.
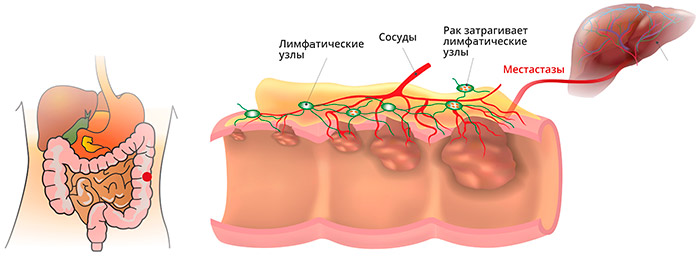
Метастазы при раке прямой кишки
Анатомические особенности прямой кишки, ее кровоснабжения и лимфооттока, определяют и характер преимущественного распространения метастазов:

Симптомы рака прямой кишки
- Первыми признаками рака прямой кишки при большинстве локализаций являются нарушения стула в виде хронических запоров и поносов, ощущения неполноценной дефекации, ложные позывы к ней (тенезмы), выделения из анального канала (слизь, кровь, гной).
- Кроме того, у большинства пациентов рано появляется болезненность при дефекации, обусловленная прорастанием опухолью стенок кишки и нарушением функции соответствующих нервов.
- При поражении мышц, формирующих анальные сфинктеры , развивается недержание кала и газов.
- Боли являются первым признаком рака прямой кишки только при раке аноректальной зоны c вовлечением в опухолевый процесс сфинктера прямой кишки. Характер боли при раке прямой кишки на ранних стадиях эпизодический, далее она может стать постоянной.
- При растущих в просвет кишки (экзофитных) и блюдцеобразных опухолях, опухолях-язвах первыми проявлениями онкологического заболевания может стать кровотечение или воспалительный процесс. Кровотечение отмечается у 75-90 % больных раком прямой кишки чаще всего в виде примеси крови в кале.
- Вместе с кровью на поздних стадиях рака могут выделяться слизь и гной.
- Ухудшение общего самочувствия (общая слабость, быстрая утомляемость, анемия, похудение, бледность кожных покровов), обусловленное длительной хронической кровопотерей и опухолевой интоксикацией, характерно для поздних стадий злокачественных образований прямой кишки.
Диагностика рака прямой кишки
Основу диагностики рака прямой кишки составляют эндоскопические методики и биопсия. Опухоль можно выявить с помощью проктоскопа – специального инструмента с миниатюрной видеокамерой, который вводят в прямую кишку. При этом врач может увидеть новообразование, определить его размеры, положение, оценить, насколько близко оно расположено по отношению к сфинктеру.
Колоноскопия позволяет оценить состояние не только прямой, но и всей толстой кишки. При этом через задний проход вводят колоноскоп – инструмент в виде тонкой длинной гибкой трубки с видеокамерой. Его проводят через всю толстую кишку, осматривая ее слизистую оболочку. Колоноскопия – безболезненная процедура, во время нее пациент находится в состоянии медикаментозного сна.
Во время эндоскопии проводят биопсию: врач получает фрагмент патологически измененного участка слизистой оболочки и отправляет в лабораторию для цитологического, гистологического исследования.
Для оценки стадии рака прямой кишки и поиска метастазов применяют УЗИ брюшной полости, рентгенографию грудной клетки, МРТ, компьютерную томографию, ПЭТ-сканирование. Трансректальное УЗИ проводят с помощью специального ультразвукового датчика, который вводят в прямую кишку. Исследование помогает оценить, насколько опухоль распространилась в окружающие ткани за пределами кишки.
Лечится ли рак прямой кишки?
В соответствии с международными протоколами по результатам диагностического обследования определяется распространенность рака прямой кишки. При этом в дополнение к международной классификации TNM, часто применяют разделение рака на 1-4-ю стадии, а также классификацию Дюка, учитывается гистологическое строение опухоли, степень дифференцировки и особенности метастазирования в зависимости от расположения в прямой кишке, наличие осложнений.
Правильно поставленный диагноз стадии опухолевого процесса при раке прямой кишки позволяет выбрать наиболее рациональную схему лечения с учетом международных руководств, включив в нее хирургическую операцию, лучевую терапию, химиотерапию и терапию таргетными препаратами.
Варианты лечения рака прямой кишки на разных стадиях
На выбор тактики лечения при раке прямой кишки влияют разные факторы, но ведущее значение имеет стадия опухоли.
На 0 и I стадии обычно показано только хирургическое вмешательство. Иногда можно ограничиться удалением полипа – полипэктомией. В других случаях выполняют трансанальную резекцию прямой кишки, низкую переднюю резекцию, проктэктомию с коло-анальным анастомозом, абдоминально-промежностную резекцию. Если операция не может быть проведена из-за слабого здоровья пациента, применяют лучевую терапию,
На II стадии хирургическое лечение сочетают с химиотерапией и лучевой терапией. Наиболее распространенная схема выглядит следующим образом:
- На начальном этапе пациент получает курс химиотерапии (обычно 5-фторурацил или капецитабин) в сочетании с лучевой терапией. Это помогает уменьшить размеры опухоли и облегчить ее удаление.>
- Затем выполняется хирургическое вмешательство. Обычно это низкая передняя резекция, проктэктомия с коло-анальным анастомозом или абдоминально-промежностная резекция – в зависимости от локализации опухоли.
- После операции снова проводится курс химиотерапии, как правило, в течение 6 месяцев. Применяют разные комбинации препаратов: FOLFOX, CAPEOx, 5-фторурацил + лейковорин или только капецитабин.
На III стадии схема лечения будет выглядеть аналогичным образом, но объем хирургического вмешательства будет больше, так как в процесс вовлечены регионарные лимфатические узлы.
На IV стадии тактика зависит от количества метастазов. Иногда они единичные, и их можно удалить, как и первичную опухоль. Операцию дополняют химиотерапией и лучевой терапией. Для борьбы с очагами в печени может быть применена внутриартериальная химиотерапия, когда раствор лекарственного препарата вводят непосредственно в артерию, питающую опухоль.
Если метастазов много, удалить их хирургическим путем невозможно. В таких случаях бывают показаны лишь паллиативные операции, например, для восстановления проходимости кишки, если ее просвет заблокирован опухолью. Основным же методом лечения является применение химиопрепаратов и таргетных препаратов. Врачи в Европейской клиники подбирают лечение в соответствии с международными протоколами и особенностями злокачественной опухоли у конкретного больного.
Профилактика рака прямой кишки
Хотя защититься от рака прямой кишки, как и от других онкологических заболеваний, на 100% невозможно, некоторые меры помогают снизить риски:
- Ешьте больше овощей и фруктов, сократите в рационе количество жирного мяса.
- Откажитесь от алкоголя и курения.
- Регулярно занимайтесь спортом.
- Некоторые исследования показали, что защититься от колоректального рака помогает витамин D. Но прежде чем принимать его, нужно проконсультироваться с врачом.
- Если в вашей семье часто были случаи рака прямой кишки, вам стоит проконсультироваться с клиническим генетиком.
- Если у вас диагностировали наследственное заболевание, которое приводит к образованию полипов и злокачественных опухолей кишечника, вам нужно регулярно проходить колоноскопию. Запись на консультацию круглосуточно
Читайте также:

