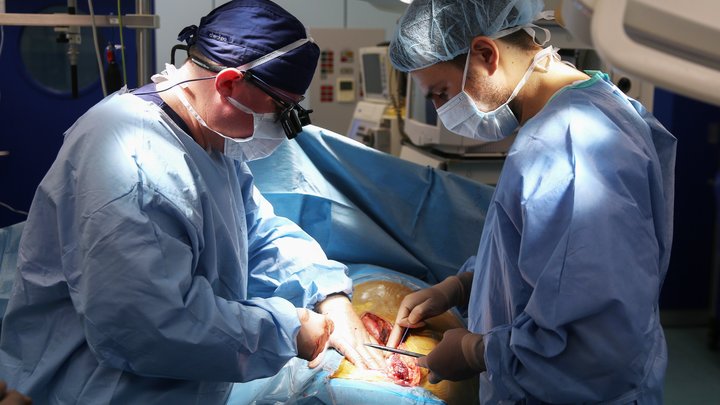
Робот лечащий от рака

В современной медицине нет таблетки, которая действует напрямую на какое-либо заболевание. В идеале лекарство должно попадать только в больные клетки, не нанося вреда здоровью других, но на деле отличить больную клетку от здоровой очень сложно. Яркий пример — химиотерапия при раке. Чтобы облучить больные клетки, приходится жертвовать и здоровыми, поэтому лечение так тяжело дается.
Почему отличить сложно? Большинство лекарств замечает только одно несоответствие в сигналах клетки, однако оно может быть и в здоровом соединении.
С этой проблемой борется группа ученых из подмосковного МФТИ и Института общей физики РАН. Они смогли создать умный материал, который анализирует полностью всю клетку и ее окружение, причем обладают сверхчувствительностью.

Ведущий научный сотрудник лаборатории нанобиотехнологий МФТИ делает тестовые полоски для ДНК-теста. Источник фото: МФТИ
Нет, ученые не придумали лекарство, которое сразу выявляет проблему и лечит ее за считаные секунды. Они лишь приблизились к созданию такого препарата. Пройдут десятилетия, прежде чем на его основе можно будет выпускать лекарства.
Общепринятые способы доставки лекарств напоминают письмо с указанием города и улицы, но без номера дома и квартиры. Для эффективной доставки нужно уметь анализировать больше параметров

Аспирантка МФТИ готовит образцы для проверки. Источник фото: МФТИ
Вообще, ДНК-тест помогает узнать о заболеваниях, которые пока никак себя не проявили, но могут вдруг проснуться. Анализ показывает предрасположенность к каким-то болезням, помогает определить причину неясных симптомов, открывает глаза на непереносимость тех или иных препаратов. ДНК-тест рассказывает и о вероятности осложнений во время беременности у женщин, о склонности к алкоголизму и еще о многих интересных (или печальных) особенностях организма.
Даже в современном мире сделать ДНК-анализ — целая операция. Нужно дорогое оборудование, особые реактивы и лицензия. Всего этого нет у небольших клиник. Для пациента это тоже испытание: сначала нужно сдать материал для анализа (мазок с поверхности щеки, слюну, кровь, волосяные луковицы, ушную серу и так далее), потом это все едет в лабораторию и исследуется минимум неделю.
Разработанная российскими учеными технология делает ДНК-тест настолько простым, что его можно проводить чуть ли на дому. Причем пациент получит результаты быстрее, да и эффективность лечения серьезных заболеваний будет выше.
Удачные эксперименты провели и подмосковные ученые, но по другому направлению. Исследователи разработали сильнейший анальгетик.
Мы не показали лечение, мы показали наночастицу, которую дальше надо испытывать и в живых организмах. Пока их эффективность не показана на животных, но мы создали частицу, которая может узнавать раковую клетку по нескольким параметрам, причем анализировать параметры очень чувствительно
Никитин подчеркнул: его команда не создала лекарство от рака и других серьезных болезней. Однако ученые смогли разработать нанороботов, способных находить болячки, обнаружить которые раньше было либо очень трудно, либо вообще невозможно.
Пока слишком рано говорить, что конкретно мы можем диагностировать с помощью этой технологии. Она настолько нова, что позволяет детектировать те вещи, которые раньше было либо сверхсложно детектировать, либо невозможно. А мы можем это детектировать в очень быстром, легком формате

Схема работы умного материала. Источник фото: МФТИ
Если в течение пяти лет исследования покажут пользу малых молекул для диагностики рака, тогда ученые смогут быстро диагностировать болезнь. Если покажут связь с атеросклерозом, то появится тест, определяющий наличие этого вида заболевания.
Сила этой технологии — она открывает направление потенциальных тестов, но мы впереди фундаментальной науки, которая должна сказать нам, какую мишень детектировать для какого заболевания
В следующем году отечественные медики получат в свое распоряжение уникальную систему "Онкоробот". Это устройство предназначено для контактной лучевой терапии рака предстательной железы. Над созданием робота-хирурга трудятся специалисты петербургского Центрального научно-исследовательского и опытно-конструкторского института робототехники и технической кибернетики (ЦНИИ РТК).
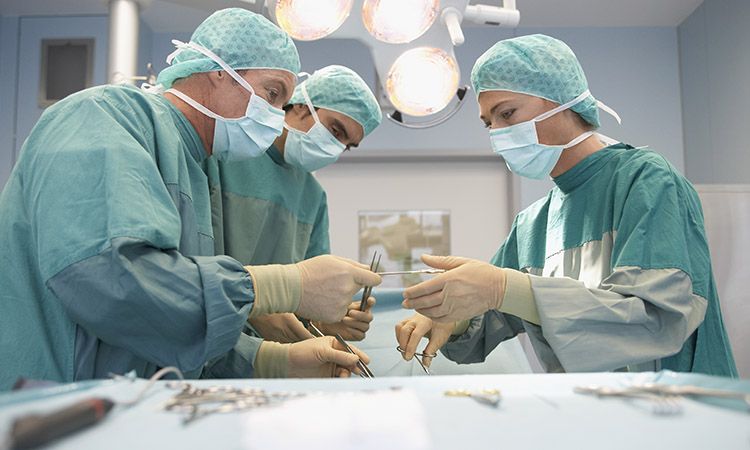
Фото: GLOBAL LOOK press/ Jochen Sand
Кибернетическое устройство окажет неоценимую помощь хирургам при операциях на пораженной раковыми клетками предстательной железе. "Онкоробот" позволит с высокой точностью вводить радиоактивные микроисточники в ткани опухоли, передают "Известия".
Руководитель проекта, заместитель директора ЦНИИ РТК по научной работе Николай Грязнов рассказал о том, что в ходе операции хирург сможет при помощи системы управления в режиме реального времени водить специальной иглой внутри пациента.
Оборудование будет представлять собой манипулятор с шестью степенями подвижности и устройством для управления движением иглы в мягких тканях пациента. "Картинку" на экран будет передавать система внутритканевой визуализации на базе УЗИ. Устройство сможет работать в ручном, полуавтоматическом и автоматическом режимах. "Онкоробот" будет монтироваться на тележку на колесах либо размещаться на кронштейнах, закрепленных на потолке.
В ЦНИИ РТК сообщили, что первый опытный образец прибора появится в четвертом квартале 2018 г., а завершение испытаний запланировано на конец 2019-го. Специализированные медучреждения уже проявляют интерес к этой разработке. Среди них - Национальный медицинский исследовательский радиологический центр Минздрава, НИИ онкологии имени Петрова и клиническая больница №122 имени Соколова.
Индустриальным партнером проекта может стать Научно-производственное объединение "Сплав", которое входит в госкорпорацию "Ростех". Эта организация уже участвовала в разработках робототехнических средств доставки микроисточников в ткань опухоли и накопила в подобных изысканиях некоторый опыт.
Финансовую поддержку проекту оказывает Министерство образования и науки РФ. В ведомстве отметили, что новое устройство не только повысит эффективность лечения онкозаболеваний, но и поможет защитить персонал от вредных излучений: врачам и медсестрам в ходе операции не нужно будет находиться рядом с радиоактивным источником.
Разрабатываемое в РФ роботизированное устройство для брахитерапии (контактной лучевой терапии) является не единственным в своем роде. Его аналоги в настоящее время разрабатываются за рубежом. Однако в условиях западных санкций изготовление подобного устройства в нашей стране позволит решить задачу импортозамещения и снизить затраты медучреждений на импортное оборудование и комплектующие. Стоимость зарубежных аппаратов для брахитерапии доходит до 40-50 млн руб., тогда как цена серийно выпускаемого российского робота будет в разы меньше.
В последние годы импортозамещение в отечественной онкологии идет полным ходом. По данным главного внештатного онколога Минздрава РФ, директора Российского онкологического научного центра имени Блохина Михаила Давыдова, три года назад около 90% лекарств для профилактики и лечения рака были зарубежного производства, тогда как сейчас доля отечественных препаратов достигает 75-80%.
Пластический хирург, онколог Дмитрий Петровский прокомментировал новость о последней разработке ученых из Санкт-Петербурга, которые создали наноробота для поиска и убийства раковых клеток. Врач объяснил, что подобные разработки ведут и зарубежные ученые. Российские исследователи открыли один из "механизмов прикрепления этого ДНК робота к опухолевой клетке". Медик убеждён, что "за этим будущее".
Онколог, маммолог и пластический хирург Дмитрий Петровский прокомментировал разработку российских ученых, которые создали наноробота для борьбы с онкологическими заболеваниями. Как объясняют создатели концепции, онкологические заболевания провоцирует сбой в геноме клетки, когда она начинает кодировать "плохие" белки. В конце концов клетки начинают бесконтрольно размножаться, опухоль всё разрастается. Чтобы победить болезнь, можно попытаться остановить процесс "выработки белков". В результате раковые клетки больше не смогут размножаться и будут отмирать. Российские учёные выработали ферменты ДНК, которые могут расщеплять клеточные связи при определённых условиях.
"Эти работы ведутся во всём мире и достаточно успешно, достаточно давно. Прорывные технологии были предложены китайскими учёными, американскими учёными. Достаточно много разработок на эту тему в Европе. Потому ребята из Питера, насколько я понимаю, не стали первыми, не что-то открыли такое сверхнеординарное. Это давно длящаяся история. Их разработка, в принципе, нова в том, что они начали исследовать один их механизмов прикрепления этого ДНК робота к опухолевой клетке, который раньше не исследовали, и собственно, они в этом молодцы, и это хорошо. Но этих механизмов прикрепления достаточно много. Ещё новое в их исследовании - то, что они предложили не только механизм воздействия на опухолевую клетку, но заодно эту опухолевую клетку они помечают. Соответственно, две сразу ипостаси этого наноробота. В том, чтобы эту опухолевую клетку повредить, соответственно, из-за этого умрёт опухолевая, и заодно её пометить, и это упростит диагностику метастазов и первичной опухоли", - рассказал Петровский.
При этом он подчеркнул, что впереди еще долгие тесты и исследования. До исследований в лабораторных условиях пройдет еще не меньше 10-12 лет. Пока же еще не проходило даже тестов на животных.
"Именно за этим, собственно говоря, будущее. Именно это принесёт действительно возможность излечения человеческого организма от злокачественной опухоли. Это один из перспективных методов излечения. Поэтому работа идёт. Насколько она будет дёшева именно в производстве уже, насколько будет она эффективна, могут показать только клинические испытания, которые будут проведены, по самым оптимистичным прогнозам, через 10-12 лет", - подчеркнул онколог.
Кроме того, Петровский рассказал, что проходит много исследований по лечению злокачественных опухолей. Но пока прорывов нет.
"Есть достаточно много исследований в иммунотерапии различных форм рака. Это стимулирование защитных свойств, защитных механизмов человеческого организма. То есть вводятся катализаторы, которые побуждают клетки человеческого организма атаковать опухолевые клетки и разрушать их. У каждого человека ежедневно образуется примерно около 10 тысяч опухолевых клеток. И соответственно, специфические противораковый имунитет, который есть у каждого человека, с ними борется и эти клетки уничтожает. В силу каких-то причин противораковый иммунитет может страдать. То есть он не сможет уже справиться с этими 10 тысячами. Или наоборот, в силу каких-то причин этих опухолевых клеток стало не 10 тысяч, а, например, 150 тысяч. Его просто не хватает. Соответственно, из-за этого возникает опухоль", - объяснил врач.
Онколог сообщил, что разработки ведутся во всех странах мира. Обычно в это вкладываются корпорации, так называемая Биг Фарма. Однако в России пока основная часть финансирования идёт от государства.
В крупном исследовании в области наномедицины ученые Аризонского государственного университета (ASU) в сотрудничестве с исследователями из Национального центра нанонауки и технологии (NCNST) Академии наук Китая успешно запрограммировали нанороботы для сокращения опухолей путем отсечения их от притока крови.
Успешная демонстрация технологии, первое в своем роде исследование у млекопитающих с использованием моделей рака молочной железы, меланомы, яичников и легких, была опубликована в журнале Nature Biotechnology.
Найти и уничтожить
Хао Янь является экспертом в области ДНК-оригами, которая в последние два десятилетия существенно продвинулась в построения все более сложных структур наномасштаба, в тысячу раз меньшем, чем ширина человеческого волоса. Технология дает надежду на революцию в медицине.
И такая революция может случиться в один прекрасный день – может быть даже немного быстрее, чем ожидалось.
Наномедицина – это новая отрасль медицины, которая стремится сочетать обещание нанотехнологий открывать совершенно новые возможности для лечения, такие как наночастицы размером с молекулы, чтобы диагностировать и лечить сложные заболевания, особенно рак.
До сих пор проблема продвижения наномедицины была затруднена, потому что ученые хотели разработать, построить и тщательно контролировать нанороботы, чтобы активно искать и уничтожать раковые опухоли, не нанося вреда никаким здоровым клеткам в организме.
Международная команда исследователей преодолела эту проблему, используя, казалось бы, простую стратегию – очень избирательно искать и изолировать опухоли.
Эта работа была начата около 5 лет назад. Исследователи NCNST сначала захотели отключить кровоснабжение опухоли, вызвав коагуляцию крови с использованием ДНК-наноносителей. Опыт профессора Хао Яна помог модернизировать подход, чтобы сделать полностью программируемую роботизированную систему, которая способна выполнять свою миссию полностью самостоятельно.
Чтобы выполнить свое исследование, ученые воспользовались известной моделью опухоли мышей, когда человеческие раковые клетки вводят в мышь, чтобы вызвать агрессивный рост опухоли.
Как только опухоль выросла, нанороботы были развернуты в организме, чтобы прийти на помощь.
Каждый наноробот выполнен из плоского, прямоугольного листа ДНК-оригами, размером 90 на 60 нанометров. К поверхности прикрепляется ключевой кровянистый фермент, называемый тромбином.
Тромбин может блокировать кровоток в опухоли путем свертывания крови в сосудах, которые питают рост опухоли, вызывая у опухоли своего рода мини-сердечный приступ и приводя к гибели опухолевой ткани.
В среднем четыре молекулы тромбина были прикреплены к плоским каркасам ДНК. Затем плоский лист сворачивали, как лист бумаги, чтобы сделать полую трубку, похожую на цилиндр.
После чего, такие трубки-роботы вводили в мышь, а затем они путешествовали по всему кровотоку, перемещаясь к опухолям.
Ключ к программированию наноробота, который атакует только раковую клетку, включает специальную полезную нагрузку на поверхности, называемую аптамером ДНК. Аптамер ДНК может специфически нацеливаться на белок, называемый нуклеолин (ядрышковый белок), который производится в больших количествах только на поверхности эндотелиальных клеток опухоли и не находится на поверхности здоровых клеток.
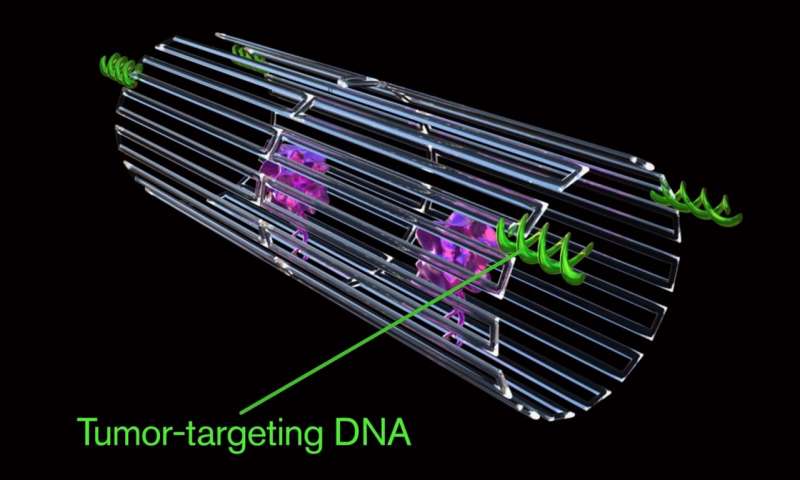
Аптамер ДНК, выделен зеленым цветом.
Изображение: Jason Drees, Arizona State University
Закрепляясь на поверхности кровеносного сосуда, наноробот действует, как пресловутый троянский конь, чтобы доставить свой груз к опухоли, обнажая фермент под названием тромбин, который является ключом к свертыванию крови.
Далее нанороботы работают оперативно, собравшись в большом количестве, чтобы быстро окружить опухоль через несколько часов после инъекции.
Безопасный и надежный
В первую очередь, команда показала, что нанороботы были безопасными и эффективными в деле сокращении опухолей.
Самое главное, не было доказательств распространения нанороботов в мозг, где это могло вызвать нежелательные побочные эффекты, такие как инсульт.
Лечение блокировало кровоснабжение опухоли и вызывало повреждение опухолевой ткани в течение 24 часов, не влияя на здоровые ткани. После нападения на опухоль большинство нанороботов были очищены и выведены из организма через 24 часа.
Через два дня наблюдались признаки прогрессирующего тромбоза, а через 3 дня наблюдались тромбы во всех опухолевых сосудах.
Ключ состоит в том, чтобы вызвать тромбин только тогда, когда он находится внутри кровеносных сосудов опухоли. Кроме того, в модели мышиной меланомы 3 из 8 мышей, получавших терапию нанороботами, показали полную регрессию опухолей. Среднее время выживания более чем удвоилось, от 20,5 до 45 дней.
Ученые также пробовали свою систему в тесте на первичную модель рака легкого у мышей, которая имитирует клинический курс пациентов с раком легких. Они показали усадку опухолевых тканей после двухнедельного лечения.
Нанороботы могут многое
Хао Янь и его сотрудники в настоящее время активно проводят клинические испытания для дальнейшего развития этой технологии.
Больше информации: A DNA nanorobot functions as a cancer therapeutic in response to a molecular trigger in vivo, Nature Biotechnology (2018). nature.com/articles/doi:10.1038/nbt.4071
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.

Наши эксперты – специалисты-онкологи, участники Российского общества клинической онкологии (RUSSCO):

заместитель директора по научной и инновационной работе ФГБУ НМИЦ онкологии им. Н. Н. Блохина Минздрава РФ, член-корреспондент РАН, профессор, доктор медицинских наук Всеволод Матвеев;

ведущий научный сотрудник отделения амбулаторной химиотерапии ФГБУ НМИЦ онкологии им. Н. Н. Блохина Минздрава РФ, доктор медицинских наук Елена Артамонова;

ведущий научный сотрудник лаборатории клинической иммунологии опухолей ФГБУ НМИЦ онкологии им. Н. Н. Блохина Минздрава РФ, академик РАЕН, заслуженный деятель науки, профессор, доктор медицинских наук Заира Кадагидзе.
Джуди (на фото с мужем) – первая пациентка, чей иммунитет полностью уничтожил рак.
Наступило прозрение!
Практически единственным способом лекарственного лечения рака до недавнего времени была химиотерапия – тяжело переносимая и чреватая многими побочными эффектами. Но сегодня, хотя химия по-прежнему остаётся методом № 1, у неё появилась реальная и в некоторых случаях более эффективная альтернатива.
Иммунитет играет важную роль в развитии рака. Ведь именно нарушения в его работе способствуют бесконтрольному размножению клеток опухоли. Наша защитная система просто не замечает растущее в организме зло, принимая клетки опухоли за свои.
Ранее учёные не знали, как эффективно воздействовать на иммунитет, а все методы сводились в основном к его стимуляции. Но оказалось, что у иммунной системы существуют так называемые контрольные точки, которые как раз и останавливают противоопухолевый иммунный ответ. Блокада этих точек может перезагрузить иммунную систему и восстановить её работу. Применяемые сегодня иммунные препараты помогают нашей защитной системе прозреть и приняться за дело, для которого, собственно, она и нужна. То есть бороться с нарушителями работы организма, в данном случае с раком.

Взаимодействие иммунной системы и опухоли проходит три этапа.
– прогрессия опухоли. За счёт усиленного деления злых клеток, способных подавлять иммунную систему или уклоняться от её воздействия, новообразование продолжает захватывать организм.
Современная стратегия иммунотерапии рака связана с открытием так называемых контрольных точек иммунитета, которые не позволяют нашей защитной системе проявлять свою противоопухолевую активность. Именно эти точки и защищают опухоль, делая её невидимой для иммунитета. Соответственно, заблокировав их с помощью инновационных препаратов, можно перезапустить иммунную систему, добившись от неё формирования адекватного противоопухолевого ответа. В результате переученные Т‑лимфоциты уже могут распознавать, атаковать и уничтожать чужеродные раковые клетки. При этом таких побочных эффектов, как при химиотерапии, при иммунотерапии не возникает и госпитализация не требуется – всё делается амбулаторно.

Не теряя надежды
Сегодня уже существует большой ряд иммунных препаратов, а несколько сотен других (в том числе и отечественных) готовятся выйти на рынок, а пока проходят клинические испытания в разных фазах. Это даёт реальный шанс больным даже с раком 4‑й стадии, что их болезнь из фазы метастазирования уйдёт в хроническую фазу и жизнь будет продолжаться. Исследуются и возможности иммунных лекарств в отношении профилактики рака. И хотя пока нет данных об эффективности их использования у больных с высоким риском рецидива, тем не менее поиски в этом направлении ведутся.
Разумеется, ещё далеко до того, чтобы научить иммунную систему на корню уничтожать рак. Но, как утверждают специалисты, мы стоим на пороге новых достижений, благодаря которым иммуноонкология будет главным направлением в лечении злокачественных опухолей в ближайшие годы.
Кому это доступно
Хотя иммунные препараты достаточно дороги, их стоимость с каждым годом снижается. А некоторые из них уже вошли в список жизненно важных лекарственных препартов (ЖНВЛП), отпускаемых за государственный счёт в рамках ОМС. Больные их могут получить в онкодиспансерах после решения врачебной комиссии. Кроме того, у пациентов есть возможность пролечиться бесплатно, участвуя в клинических исследованиях новых препаратов или в программах раннего доступа, которые организуются фармацевтическими компаниями при выпуске первых партий лекарств на рынок.

Помогает не всем
Несмотря на обнадёживающие новости, иммунотерапия пока всё же не является заменой химиотерапии. Это лишь альтернативный метод лечения рака, применяемый по строгим показаниям. И помогает такое лечение не всем, поэтому врачам очень важно выявлять тех пациентов, которым он подходит, чтобы не тратить средства понапрасну там, где это не даст результата.
Тем не менее исследования доказали, что у 15–20% больных с прогрессированием опухоли после предшествующей химиотерапии удаётся получить длительный (иногда многолетний) клинический выигрыш. Сегодня во всём мире проводятся широкомасштабные исследования биомаркеров, способных предсказать высокую эффективность иммунных препаратов для лечения рака. Иммунотерапия уже показала эффективность при метастатическом раке почки, головы и шеи, раке лёгкого, меланоме, лимфомах и некоторых других злокачественных новообразованиях. Например, больные с диссеминированной меланомой, раньше погибавшие в течение месяцев, на иммунных препаратах живут уже более 10 лет.
— Пётр Михайлович, не могли бы вы рассказать, в чём заключается суть вашего метода?
— Есть вирусы, которые могут подавлять рак. Они обладают онколитическими свойствами. И они безвредны для здоровья человека. Этот способ лечения практически не даёт побочных эффектов. Возможно только кратковременное повышение температуры, что является положительным признаком, говорящим о том, что вирус в организме прижился и оказывает реакцию. Это легко снимается обычными жаропонижающими средствами.
— Когда метод станет широко применяться в практической медицине?
— Сейчас основная наша задача — сертифицировать те препараты, которые у нас есть. Эта работа поддерживается Минздравом и Минобрнауки. У нас есть несколько грантов, по которым мы испытываем эти препараты. Мы делаем новые варианты онколитических вирусов с усиленными свойствами. Скоро должны начаться доклинические испытания в институте имени Смородинцева в Санкт-Петербурге. Мы уже передали туда препараты. Врачи говорят, что на испытания уйдёт месяцев пять-шесть. Учитывая ситуацию с коронавирусом, я думаю, что в начале 2021 года испытания могут быть закончены и тогда мы уже сможем договариваться с клиниками о проведении клинических испытаний.
— Что собой представляет препарат, который должен пройти испытания?
— Препарат — это живой вирус, который выращивается на культурах клеток. Это лекарство нового типа, которого не нужно много. Важно, чтобы он попал в организме в те клетки, которые чувствительны к нему. А дальше он сам размножается. То есть лекарство само себя воспроизводит уже в том месте, где оно нужно. Это раствор, 100 млн вирусных частиц в 1 мл. Но самая большая проблема в этом лечении — это способ доставки вируса в опухоль, в случае с глиобластомой — в мозг, в ту область, где находится опухоль.
Если препарат ввести просто внутривенно, то очень небольшая часть вируса может попасть в опухоль. В кровотоке есть неспецифические факторы, которые этот вирус быстро инактивируют. Кроме того, в мозгу есть гематоэнцефалический барьер, который препятствует попаданию туда всяких нежелательных агентов, в том числе и вирусов. Поэтому вирусу очень трудно добраться до опухоли.
— Как вы смогли решить эту проблему?
Эти клетки, как торпеды, идут в очаги воспалений, где находится опухоль. Там вирус выходит из них и начинает убивать опухолевые клетки. Этот метод мы уже отработали на нескольких пациентах. Есть хорошие примеры, когда на МРТ или КТ видно, как опухоль уменьшается и исчезает. Но это происходит не у всех.
— Почему же одни и те же вирусы не справляются с одними и теми же видами опухолей?
— Дело в том, что каждый конкретный вирус нашей панели действует только на 15—20% пациентов. Остальные оказываются к вирусу устойчивы. Однако у нас есть много разных вирусов, и мы можем подобрать свой для любого пациента. Но для этого нужно иметь живые клетки пациента.
Сейчас мы разрабатываем такие тесты, которые могут по обычной биопсии быстро показать, к какому вирусу опухоль будет чувствительна. Это очень сложная работа. Возможно, в будущем специальные клинические лаборатории будут получать от пациентов все необходимые материалы и в режиме конвейера проводить тестирование, подбирать препараты и далее — лечение.
Но сейчас к нам обращаются те, кому уже никто не может помочь. Некоторые из них лечатся у нас по полгода и более. Если идёт стабилизация и видно, что опухоль не растёт, мы делаем перерыв до тех пор, пока рост не возобновится. Но есть случаи, когда рост не возобновляется. У нас есть пациент, который живёт уже четыре года, притом что шансов у него не было. Глиобластома — это смертельное заболевание, средняя продолжительность жизни с ним — 12—15 месяцев с момента постановки диагноза.
— Прежде всего должен сказать, что пока это экспериментальное лечение. Когда Макаров доложил об этом методе на совещании у президента, мне кажется, он не рассчитывал на то, что это вызовет такой резонанс. Сейчас меня буквально атакуют письмами десятки больных с просьбой помочь.
Мне кажется, что не стоило рассказывать про Заворотнюк. Я знаю, что родные Анастасии долгое время вообще не комментировали её состояние и не хотели, чтобы в прессе поднимали этот вопрос. Сам я Анастасию ни разу не видел. Ко мне обращались её близкие с просьбой о помощи. Я сказал, что мы могли бы на первом этапе протестировать её клетки.
Дело в том, что во время операции были забраны живые клетки опухоли и переданы в один из институтов, где их удалось вывести в культуру клеток, чтобы они делились в пробирке. Мы взяли их и протестировали на чувствительность к нашим онколитическим вирусам, которые мы рассматриваем как средство лечения глиобластомы. Обнаружилось, что из 30 вирусов 7—8 вполне подходящие. И на этом этапе мы остановились, потому что муж Анастасии Пётр Чернышов сказал, что сейчас ситуация более-менее спокойная, если будет крайняя необходимость, они к нам обратятся. Это всё, что касается Заворотнюк.
Но всё это мы делали и делаем в очень ограниченном масштабе. Сейчас, когда всё выплеснулось в СМИ, мы просто не справимся с таким валом пациентов.
— Можете ли вы прокомментировать связь между ЭКО и появлением глиобластомы? Есть такие исследования?
— Как я понимаю, этот вопрос опять поднят историей Заворотнюк. В данном случае у неё было ЭКО. Но это никак не говорит о том, что есть какая-то связь. Во-первых, ЭКО не так много делают и глиобластомы — это 1% всех опухолей. Глиобластома встречается не только у женщин. Я думаю, что никакой связи нет. Ведь как может воздействовать ЭКО? Повышается уровень половых гормонов. Но тех гормонов, которые достаточно физиологичные, и так всегда есть в организме. Они просто появляются в другое время и в другой дозе. И вряд ли могут оказать влияние именно на глиальные клетки, с тем чтобы они переродились.
— В мире ведутся подобные исследования по лечению глиобластомы? Что вам известно об этом?
— Мы не первые, кто проверяет вирусы на глиобластоме. Сейчас это очень горячая тема во всём мире. И разные вирусы тестируют для лечения разной онкологии во многих странах. Я знаю один случай, который начали лечить в 1996 году вирусом болезни Ньюкасла, это птичий вирус. И больной до сих пор живёт с глиобластомой. Это опубликованные данные. И есть ещё несколько случаев лечения с помощью рекомбинантных вирусов герпеса.
В прошлом году вышла нашумевшая работа о том, что 20% больных глиобластомой могут быть вылечены вакциной рекомбинантного вируса полиомиелита.
Но нейрохирурги — люди консервативные. Они ни за что не согласятся даже в порядке эксперимента проводить такие опыты на людях. Потому что они очень сильно рискуют, если будет осложнение. Поэтому мы должны дождаться доклинических испытаний, с тем чтобы потом убедить их опробовать схему с прямым введением вируса прямо в опухоль.
— А кто и когда впервые заметил действие вируса на раковые клетки?
— Ещё в начале ХХ века учёные заметили, что опухолевые клетки особенно хорошо размножают вирусы. После инфекционных вирусных заболеваний у некоторых больных при разных видах рака наблюдались ремиссии. И уже тогда возникла мысль о том, что в будущем можно будет лечить онкобольных с помощью вирусов.
В 1950-е годы в Америке проводились эксперименты по лечению рака безнадёжных больных с помощью патогенных вирусов. Считалось, что это меньшее зло по сравнению с самим раком. И тогда были получены положительные результаты. Но поскольку многие больные умирали от инфекционных заболеваний, возник очень большой резонанс. Врачи, которые начали это делать, дискредитировали всю эту область на долгие годы. Были введены дополнительные этические правила. Само упоминание о том, что вирусом можно лечить рак, стало табу.
В 1990-е годы уже стало понятно, как устроены вирусы, структура их генома. Учёные научились вносить изменения в геном вирусов, чтобы сделать их безвредными. И тогда во всём мире начался бум разработки препаратов на основе вирусов для лечения рака. Но тут новая беда. Этому стали сопротивляться фармацевтические компании. Потому что это совершенно другой способ лечения, который подрывает базу их благосостояния.
В начале 10-х годов нашего века многие небольшие компании разрабатывали препараты, которые потом проходили какие-то клинические испытания, были показаны какие-то многообещающие свойства. Но фармацевтические компании скупали эти разработки и практически прекращали деятельность этих небольших стартапов.
— Удалось ли кому-нибудь преодолеть фармацевтическое лобби и зарегистрировать препарат?
— Сейчас в мире зарегистрировано три препарата онколитических вирусов. Один препарат разрешён к использованию в США для лечения злокачественных меланом. Ещё один рекомбинантный аденовирус — в Китае, и один энтеровирус — в Латвии. Но, в общем-то, каждый из этих препаратов находит пока очень ограниченное применение, из-за того что все они действуют только на часть пациентов.
— Пётр Михайлович, а как давно вы ведёте свои исследования?
— Всю жизнь, ещё с 1970-х годов. Мне выпало такое время, когда мы вначале практически ничего не знали о вирусах. И по мере того, как мы что-то узнавали, мы вносили какой-то вклад в эту науку и сами учились. И я начинал как раз с вирусов. Потом переключился на проблему рака — фундаментальные механизмы деления клеток: как нормальная клетка превращается в рак. А потом снова вернулся в вирусологию.
Должен сказать, что и мои родители были вирусологами, они занимались противополиомиелитной кампанией. Моя мать в 1970-е годы изучала, как у детей образуются антитела к полиомиелитной вакцине, и она обнаружила, что у многих детей не образуются антитела. Оказалось, что в кишечнике у детей в это время шла бессимптомная инфекция другого безвредного энтеровируса. И он вызывал неспецифическую защиту от вируса полиомиелита. Поэтому вакцинный полиовирус не мог индуцировать антитела у этих детей. Эти безвредные вирусы были выделены из кишечника здоровых детей. И на их основе были созданы живые энтеровирусные вакцины, которые испытывались для того, чтобы предотвращать какие-то ещё неизвестные инфекции.
И вот мы решили возобновить тот подход, который был предложен моей мамой, когда используется панель энтеровирусов. Оказалось, что те больные, которые нечувствительны к одному вирусу, могут быть чувствительны к другому. Возникла идея подбора вируса под пациента. Мы разработали целую панель собственных вирусов, которые могут также обладать усиленными свойствами. Мы продолжаем эту разработку.
— Ваши вирусы могут побеждать рак. А есть вирусы, которые вызывают развитие опухоли?
— Да. Например, рак шейки матки в 95% случаев вызывается вирусом папилломы. Сейчас уже есть даже вакцины против онкогенных папилломовирусов 16—18-го серотипа, которые применяются для девочек, чтобы не заболевали раком шейки матки. Но это самый большой пример. У большинства видов рака сейчас можно полностью исключить вирусную природу.
— Вы используете естественные вирусы или конструируете их?
— У нас разные есть вирусы. Как я говорил, первая панель была выделена из кишечника здоровых детей. Это природные непатогенные вирусы, которые, кстати говоря, хорошо защищают детей от многих вирусных инфекций. Кроме того, мы делаем синтетические и рекомбинантные вирусы, когда мы вводим определённые изменения в их состав, которые усиливают их онколитические свойства.
— На планете есть ещё места, где может быть очень много вирусов, о которых мы ещё и понятия не имеем. Например, те, что живут в океанских глубинах. Как вы считаете, если вдруг кто-то возьмётся за изучение океана именно с точки зрения вирусов, там могут найтись полезные для вас?
— Да, и сейчас это тоже очень горячая тема. Когда разработали метод секвенирования геномов, ДНК, РНК, то возник соблазн: профильтровать сточные воды, океанические воды, из прудов, морей. Уже пробурили скважину в Антарктиде к древнему озеру, чтобы посмотреть, что там, выделить оттуда биологические компоненты и секвенировать их. И оказывается, что нас окружает огромное количество вирусов, которые абсолютно безвредны. И такое впечатление, что наше исходное представление о вирусах как о чём-то вредном и вызывающем только болезни неверно. Болезнетворный вирус — скорее исключение, чем правило.
Читайте также: