Результаты хирургического лечения рака легкого
Отдаленные результаты хирургического лечения рака легкого во многом зависят от стадии, в которой была произведена операция, и гистологической формы опухоли. Результаты значительно лучше при операциях в I—II стадии, чем III стадии рака. При эпидсрмондном раке результаты лучше, чем при недифференцированных формах. Отмечаются также лучшие результаты после лобэктомии по сравнению с пульмон-эктомией. Это связано с двумя основными факторами: во-первых, лоб-эктомия, как правило, производится при меньшей распространенности ракового процесса: во-вторых, лобэктомия легче переносится больными и значительно реже приводит к легочной недостаточности, которая является причиной смерти ряда больных в отдаленные сроки после пульмоиэк-томнн. Через 5 лет после лобэктомнн продолжают жить 35—40%, после лульмонэктомии — 25—30% больных. Большинство случаев смерти от рецидивов и метастазов рака приходится на первые 2—3 года после операции. Если больные благополучно переживают этот срок и при контрольном исследовании рецидив или метастазы у них не обнаруживаются, прогноз в значительной степени является благоприятным. После радикальных операций по поводу рака легкого больные подлежат диспансерному наблюдению в онкологических учреждениях.
Лучевое лечение рака легкого применяется широко. В отличие от старых методов рентгенотерапии современное мегавольтипс облучение позволяет, не повреждая кожу, интенсивно воздействовать на глубоко расположенную опухоль. Под влиянием облучения раковые клетки подвергаются дегенерации и некрозу, а опухоль часто уменьшается и в отдельных случаях даже исчезает. Облучение обычно оказывает положительное влияние и на воспалительную реакцию вокруг опухоли. Уменьшение опухоли и воспалительной реакции может способствовать улучшению бронхиальной проходимости, ликвидации ателектазов. Для лучевого лечения рака легкого применяются гамма-терапевтические установки "Рокус", "Луч", линейные ускорители, бетатрон. Облучают как зону опухоли, так н зону предполагаемого метастазирования. Разовая доза 200 -250 рад. суммарная — до 6000—8000 рад.
В настояшее время получают распространение и интенсивно изучаются различные комбинированные методы лечения рака легкого. Наиболее пажнымн из них являются облучение с последующей операцией и облучение в сочетании с химиотерапией. Предоперационное облучение проводят в течение 2—3 нед в суммарной дозе 3000—4000 рад. Операцию производят через 12—15 дней после окончания облучения.
Химиотерапия рака легкого пока малоэффективна. Лишь у небольшого числа больных она позволяет получить временный терапевтический эффект: улучшение самочувствия, уменьшение кашля и болей. Размеры опухоли уменьшаются редко. Химиотерапия проводится главным образом в тех случаях, когда нельзя оперировать или облучать. Наиболее употребительными препаратами, применяемыми для лечения рака легкого, являются циклофосфан, тиофосфамид (ТиоТЭФ), 5-фторурацил. Вводят их внутривенно согласно прилагаемым инструкциям. При раковых плевритах во время пункций с отсасыванием жидкости рационально вводить в плевральную полость 60—70 мг тиофосфамида (суммарная доза до 300 мг). Этот препарат способствует прекращению накопления жидкости в полости плевры. Введение химиопрепаратов через катетер в легочную артерию и бронхиальные артерии не имеет выраженных клинических преимуществ по сравнению с внутривенным путем введения, поэтому теперь оставлено.
Облучение в сочетании с химиотерапией (химиолучевое лечение) наиболее целесообразно для лечения неоперабельных больных с недифференцированными формами рака легкого, а также для больных с рецидивами и метастазами рака после операций. Во время такого лечения важно переливать кровь, насыщать больных витаминами. Необходимо следить, чтобы число лейкоцитов в крови не падало ниже 3*109/л (3000 в 1 мкл), а тромбоцитов — ниже 100*109/л (100000 в 1 мкл). Если такое падение наблюдается, в химиолучевом лечении нужно сделать перерыв или прекратить его.
Профилактика рака легкого основывается на знании факторов, которые предрасполагают к его возникновению. Пока все профилактические меры сводятся к рациональной гигиене дыхания. В крупных городах важно добиваться уменьшения выброса дыма в атмосферу системами домового отопления и промышленными предприятиями. Для этого совершенствуются способы сжигания топлива и создаются специальные улавливатели дыма. При составлении планов гралостронтельства следует учитывать необходимость создания санитарно-защитных зон у промышленных предприятий. Автомобильные двигатели для уменьшения загрязнения воздуха канцерогенными веществами нужно хорошо регулировать, а двигатели с большим износом снимать с эксплуатации. Кроме этих широких санитарно-гигиенических мероприятий, важное значение следует придавать пропаганде отказа от курения, а также предупреждению и лечению заболеваний дыхательной системы, которые нарушают механизмы ее самоочищения.
До настоящего времени рак легкого в большей части случаев диагностируется еще поздно — в III и даже IV стадиях болезни. Главными причинами поздней диагностики являются недостаточная онкологическая настороженность врачей, особенно работающих в поликлинической сети, а также скрытое течение н недостаточное внимание ряда больных к появившимся симптомам заболевании и врачебным рекомендациям.
Раннее распознавание рака легкого — одна из важных задач здравоохранения. Основное значение имеет профилактическое обследование легких с помощью флюорографии. Такое обследование следует проводить не реже раза в год и в первую очередь среди групп населения с повышенным риском заболеваемости раком легкого: мужчин старше 40 лет, работников газовой, горной, кожевенной, табачной промышленности, лиц, занятых производством и обработкой камня, асфальта, смол, хроматов, асбеста, никеля. Чрезвычайно важно повышение квалификации врачей, к которым в первую очередь обращаются больные раком легкого,— терапевтов, фтизиатров, рентгенологов.
Хирургическая резекция (удаление части лёгкого, пораженной опухолью) является одним из наиболее эффективных методов лечения немелкоклеточного рака легкого. Такая операция подходит не всем. Для оценки возможности хирургического лечения рака легкого необходимо определить стадию заболевания (с помощью ПЭТ/КТ) и спрогнозировать переносимость операции (оценить степень проявления сопутствующих заболеваний, функцию легких и сердца, а также реабилитационный потенциал пациента). Всестороннее обследование имеет большое значение при подготовке к операции!
Методы хирургического лечения рака лёгкого:
Выбор метода радикального хирургического лечения рака легкого зависит от локализации опухоли, ее размеров, признаков прорастания соседних структур и поражения лимфатических узлов. По объему можно выделить следующие хирургические операции:
- Лобэктомия – удаление одной доли легкого. Является основной выполняемой при периферическом раке легкого операцией. Позволяет сохранить большую часть легочной ткани, поэтому, как правило, не влияет на функцию дыхания в последующем. В то же время, обеспечивает хорошую радикальность вмешательства в большинстве случаев периферического рака легкого ранних стадий.
- Пневмонэктомия – удаление всего легкого. Выполняется при центральном расположении опухоли, вовлечении в процесс главного бронха или крупных сосудов. Может приводить к ограничению переносимости физических нагрузок в отдаленном периоде после операции, что, однако, оправдано, если в результате операции достигается полное удаление опухоли.
- Билобэктомия и лобэктомия с бронхопластикой или ангиопластикой – хирургические операции, занимающие по объему промежуточное положение между двумя предыдущими видами операций. Целью их является сохранение максимально возможного объема легочной ткани при удалении распространенных опухолей легкого. Данный объем операции может позволить избежать пневмонэктомии и сохранить хорошую дыхательную функцию при достаточной радикальности операции.
- Сегментэктомия – удаление сегмента – части доли легкого. Данная операция возможна только при малых размерах опухоли (1 стадия) и используется у пациентов со значительно сниженной функцией легких при опасности выполнения им лобэктомии. В последние годы появились данные о достаточной радикальности этой операции у пациентов с ранней стадией аденокарциномы in situ.
При выявлении рака легкого на ранней стадии, когда нет прорастания соседних органов и размеры опухоли менее 5-6 см, возможно хирургическое лечение рака легкого малоинвазивным доступом – с использованием видеоторакоскопии и малых разрезов. Это позволяет:
- снизить травматичность хирургического вмешательства,
- ускорить восстановление физической активности,
- уменьшить выраженность болевого синдрома,
- значительно сократить сроки лечения,
- добиться хорошего косметического эффекта.
Преимущества ЕМС:
В EMC операции выполняют опытные торакальные хирурги-онкологи, владеющие всеми современными хирургическими методиками. Это:
- главный внештатный специалист-торакальный хирург Департамента здравоохранения города Москвы, к.м.н. Евгений Тарабрин;
- руководитель Хирургической клиники EMC, к.м.н. Андрей Волобуев.
В ЕМС доступны все современные методики лечения рака лёгкого:
- Хирургическое вмешательство. Этому виду лечения отдается предпочтение в случае рака легкого I или II стадии.
- Послеоперационная адъювантная химиотерапия. Улучшает выживаемость у пациентов с II стадией заболевания, в некоторых случаях может быть рекомендована пациентам с IB стадией заболевания.
- Стереотаксическая лучевая терапия (SBRT) или традиционная лучевая терапия. Проводится пациентам с I или II стадией заболевания, которым не может быть выполнена хирургическая резекция.
- Фотодинамическая терапия также может быть полезной в качестве первичного лечения у пациентов с поверхностными поражениями дыхательных путей.
- Комбинированная химиолучевая терапия. Применяется в случае гистологически подтвержденной III стадией заболевания.
Прогнозирование объема операции проводится по результатам обследования и совместным решением междисциплинарного консилиума EMC.

Данные статистики показывают, что рак легкого является одним из самых распространенных онкологических заболеваний, и частота его продолжает расти 3.
Хирургическое лечение этой патологии продолжает оставаться основным, оно включает резекционные методы, такие как пневмонэктомия, лоб- или билобэктомия 5. Радикальное хирургическое лечение имеет негативные стороны: высокая травматичность, трофические и репаративные расстройства, гнойно-воспалительные осложнения достигают 30 % и дают летальность до 9 % 9. Бронхиальные свищи – самые грозные осложнения радикального лечения рака легкого [7, 10, 11]. Во многих хирургических клиниках мира, специализирующихся на лечении больных раком легкого, данное осложнение после пневмонэктомий достигает 12 % 2, а послеоперационная летальность – 50 % и выше 9. Из-за образования бронхиального свища через культю бронха циркулирует воздух, что способствует ухудшению общего состояния больных из-за развития дыхательной недостаточности и эндотоксикоза [8, 9, 11].
Хирурги, которые исследовали данное осложнение, считают основными этиологическими факторами образования бронхиальных свищей ухудшение репарации на фоне злокачественных новообразований, операционную травматичность удаления лимфатических коллекторов, нарушение кровоснабжения культи бронха [2, 4, 5]. Для снижения риска образования бронхиальных свищей после пневмонэктомий предлагаются различные методики укрепления культи бронха, которые на протяжении многих лет оптимизируются, что свидетельствует об актуальности и нерешенности данной проблемы 6.
Некоторые хирурги применяют для закрытия культи бронха перикард, что значительно уменьшает риск возникновения бронхиальных свищей после пульмонэктомии [5].
В литературных источниках имеются сообщения, что предпочтения в хирургических пособиях лечения рака легкого нужно отдавать резекционным методам сосудов и бронхов, в результате которых снижается частота осложнений, летальность, смертность, повышается выживаемость. Оперативное пособие циркулярной резекции может включать изолированно резекцию бронха или сочетать резекцию бронха и легочной артерии 1.
По данным зарубежных и отечественных клиник, летальность при циркулярной резекции не превышает 4 %. В структуре резекций легких у больных злокачественными новообразованиями легких количество выполненных лобэктомий достигает 70 %, летальность – 3 % [1, 2, 9].
Радикальные хирургические вмешательства у больных раком легкого с сопутствующей сердечно-сосудистой патологией остаются предметом дискуссии 7.
В представленных нами источниках литературы результаты исследований показывают, что онкологические заболевания легких с сопутствующей ишемической болезнью сердца (ИБС) наблюдаются у 28 % больных. Данные сообщения, как правило, носят описательный характер, алгоритма тактических действий по выполнению оперативных пособий на сердце и легком не представляют [1, 2, 11].
В настоящее время совершенствование хирургического и консервативного лечения больных злокачественными новообразованиями легких сохраняет свою актуальность.
Целью нашего исследования явилось сравнительная оценка результатов хирургического лечения больных раком легкого I-III стадии.
Материалы и методы исследования
Мы провели проспективное и ретроспективное исследование 236 пациентов с немелкоклеточным раком легких I-III стадии за период с 2010 по 2017 год. Первоначальный выбор сделан из 310 больных.
Индикаторами включения в работу были: возраст больных от 39 лет и старше, оба пола, рак легких I-III стадии, радикальное хирургическое лечение (пневмонэктомия, лоб- и билобэктомия).
Пациенты в возрасте менее 39 лет, с неоперабельным раком легких, острыми нарушениями мозгового кровообращения и острой сердечно-сосудистой недостаточностью в анализ не включались.
Все анализируемые нами больные находились на стационарном лечении в Ульяновском областном онкологическом диспансере.
Для достижения цели настоящего исследования были применены клинико-лабораторные, рентгенологический, эндоскопический, ультразвуковой, гистологический методы исследования. По показаниям выполняли эхокардиографическое исследование.
Исследование больных раком лёгкого в предоперационном периоде включало клинико-инструментальную оценку местной и отдалённой распространённости опухолевого процесса, а также результаты лабораторного и функционального исследования органов и систем организма. Для этого использовали: рентгенографию в двух проекциях (прямой и боковой); контрастное исследование пищевода для оценки состояния бифуркационных лимфатических узлов; компьютерную томографию грудной клетки; цитологическое исследование мокроты; бронхологическое исследование; ультразвуковое исследование органов брюшной полости, забрюшинного пространства, надключичных зон; трансторакальную (чрескожную) пункцию при периферической опухоли.
Предоперационная лучевая и/или химиотерапия не проводилась. В зависимости от способа хирургического лечения пациенты были разделены на 3 группы.
В первой группе больных (n=63) применялась только пневмонэктомия, закрытие культи бронха сшивающим аппаратом (УО–40).
Во второй группе больных (n=143) выполняли лоб- или билобэктомию, закрытие культи бронха сшивающим аппаратом (УО–40).
В третьей группе больных (n=30) выполняли лоб- или билобэктомию, закрытие культи бронха сшивающим аппаратом(УО–40)и отдельными П-образными узловыми швами (викрил 3-0) от 4 до 6 узлов.
Всем больным после торакотомии выполняли дренирование плевральной полости двумя дренажами у куполу плевральной полости и в синус.
Во всех трех группах послеоперационное лечение выполнялось по стандарту.
Все больные давали информированное добровольное согласие на хирургическое вмешательство и проводимое в послеоперационном периоде лечение (одобрено Этическим комитетом Института медицины, экологии и физической культуры Ульяновского государственного университета в соответствии с законодательством РФ и в соответствии с Хельсинкской декларацией 1975 г.).
Статистическая обработка результатов производилась с помощью пакета программ Statistica 6. При сравнении полученных параметров нами использовался t-критерий Стьюдента для независимых парных выборок и х2-тест. Статистически значимыми признавались различия с уровнем доверительной вероятности не менее 95 % с учетом поправки Бонферрони для множественных сравнений.
Результаты и обсуждение
Исследуемые пациенты в трех группах были сопоставимы по возрасту (табл. 1) и полу (p

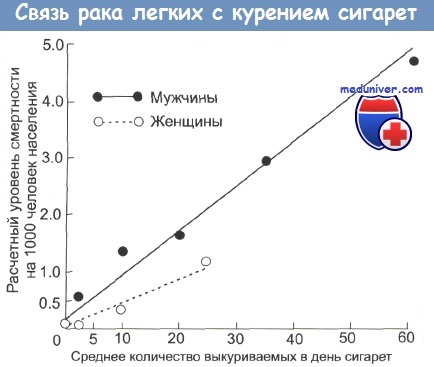
Рак легких — одно из самых распространенных онкозаболеваний во всем мире. Ежегодно он уносит больше жизней, чем в совокупности рак кишечника, предстательной железы, молочных желез и яичников. Основной фактор риска — курение. Чем дольше человек курит и чем больше сигарет выкуривает ежедневно, тем выше у него риск возникновения злокачественной опухоли в легких. Расставаться с вредной привычкой не поздно ни в каком возрасте: в любом случае риски постепенно снизятся.
- Причины рака легкого
- Прогноз при раке легкого
- Как помочь больному раком легкого?
- Методы лечения рака легких
- Химиотерапия при раке легкого
- Хирургическое лечение рака легкого
- Таргетная терапия при раке легкого
- Раковое поражение плевры
- Плевродез
- Лечение рака легких 4 стадии с метастазами
- Паллиативное лечение рака легкого в Европейской клинике
- Этапы лечения рака легкого на разных стадиях
- Врачи Европейской клиники знают, как помочь
- Где лучше лечить рак легкого: в России или за границей?
- Стоимость лечения рака легких в Европейской клинике
Причины рака легкого
В случае с большинством онкологических заболеваний корректнее говорить не о причинах, а о факторах риска. Они не приводят к раку со стопроцентной вероятностью, но повышают риск заболеть:
- Как мы уже упомянули, основной фактор риска рака легких — курение. Причем, не только активное, но и пассивное. Если рядом с вами постоянно кто-то курит, ваше здоровье в опасности.
- Некоторые люди на рабочем месте контактируют с такими веществами, как асбест, никель, хром, мышьяк. Эти канцерогены повышают риск рака легких.
У некоторых людей отягощенная наследственность. Риски повышены, если злокачественная опухоль в легких диагностирована у одного из родителей, родного брата или сестры. - В почве, скальных породах и воде содержится небольшое количество урана. Он распадается с образованием газа радона, который затем попадает в воздух. Иногда он скапливается в помещениях в опасных концентрациях.
Прогноз при раке легкого
Серьезность прогноза предстоящей жизни при диагностированном раке легкого для жизни очевидна. Обычно для оценки прогноза опухоли используется показатель пятилетней выживаемости, он зависит от вида опухоли, стадии заболевания и наличия (распространенности) метастазов.
На ранних стадиях заболевания (немелкоклеточный рак легкого в первой стадии) 5-летняя выживаемость при раке легких отмечается примерно у 60% пациентов; во II стадии — примерно у 40% пациентов, в IIIa стадии — около 15%. На поздних стадиях заболевания шансы достигнуть 5-летней выживаемости стремятся к нулю.
Успешное лечение немелкоклеточного рака легкого зависит от возможности проведения адекватного хирургического пособия. Своевременное применение современных схем полихимиотерапии в совокупности с таргетными препаратами увеличивает продолжительность жизни до 6–8 месяцев, а у 20–25% пациентов — свыше года.
Виды злокачественных опухолей легких
Выбор тех или иных методов лечения сильно зависит от того, какой тип рака легких обнаружен у пациента. Выделяют два основных типа, в зависимости от того, как раковые клетки выглядят под микроскопом:
- Чаще всего встречается немелкоклеточный рак легкого, который включает разные подтипы опухолей:плоскоклеточный рак, аденокарциному, крупноклеточный рак.
- Менее распространен мелкоклеточный рак легкого. Он встречается практически только у курильщиков.
Как помочь больному раком легкого?
К сожалению, психологический шок, вызываемый диагнозом онкологического заболевания вообще и рака легких в частности, лишает многих людей способности трезво оценивать ситуацию и доверять мало-, а то и совсем непроверенным методам народной медицины.
Вокруг лечения онкологии легких существует множество не имеющих под собой никакого основания мифов об эффективности лечения березовым грибом, настойками лопуха, календулы с ромашкой, мухоморов, водки с прополисом, вплоть до самых анекдотичных методов.

Методы лечения рака легких
Современная доказательная медицина в обосновании лечения онкологии легких исходит из строго научного обоснования применения тех или иных протоколов. Основой выбора, осуществляемого лечащим врачом, служит морфологическая характеристика опухоли, ее распространенность, наличие или отсутствие метастазов, общее состояние больного.
Помимо хирургического лечения при раке легкого могут использоваться различные программы лучевой терапии в сочетании с химиотерапией. Психологические сложности и душевные переживания, возникающие у пациента и родственников, помогут решить специалисты-психоонкологи.
Химиотерапия при раке легкого
В последнее время наиболее перспективными для лечения немелкоклеточного рака считаются таргетные препараты (небольшие молекулы и моноклональные антитела, целенаправленно действующие на определенные тканевые мишени — фактор роста эпителия и образования новых сосудов в злокачественной опухоли. Препараты этого ряда гефитиниб (Иресса) и эрлотиниб (Тарцева) используют в качестве терапии второй или третьей линии при некоторых видах рака легких, экспрессирующих определенный вид рецепторов – EGFR. В значительном количестве случаев химиотерапия позволяет не только добиться уменьшения размеров опухоли, предупреждения ее метастазирования и восстановления качества жизни, но и добиться стойкой долгосрочной ремиссии или выздоровления пациента.
Хирургическое лечение рака легкого
Немелкоклеточный рак легкого поддается хирургическому лечению, как правило, лучше, чем мелкоклеточный. В зависимости от размеров и расположения опухоли, врач может удалить ее, захватив некоторое количество здоровой ткани вокруг, или полностью удалить легкое. Обычно хирургическое вмешательство дополняют курсом адъювантной химиотерапии или лучевой терапии. Это помогает уничтожить оставшиеся раковые клетки и снизить вероятность рецидива.
В настоящее время хирурги все чаще применяют миниинвазивные вмешательства, когда на стенке грудной клетки делают прокол, и внутрь вводят гибкий тонкий торакоскоп, оборудованный источником света и видеокамерой.
Иногда при немелкоклеточном раке легкого прибегают к лечению радиочастотной аблацией. В опухоль вводят тонкую иглу и подают на нее электрический ток, который сжигает раковые клетки.
Мелкоклеточный рак значительно чаще по сравнению с немелкоклеточным является неоперабельным. Приходится прибегать к другим методам лечения.
Лучевая терапия при раке легкого
Лучевая терапия эффективна как при немелкоклеточном, так и при лечении мелкоклеточного рака легкого. Врач может назначить этот метод лечения с разными целями:
- Перед хирургическим лечением (неоадъювантная лучевая терапия). Это помогает сократить опухоль в размерах, хирургу становится проще ее удалить, а пациент лучше переносит вмешательство.
- После хирургического лечения (адъювантная лучевая терапия). Нужна для того, чтобы уничтожить опухолевые клетки, которые остались в организме после операции, и предотвратить рецидив.
- В качестве самостоятельного метода лечения для борьбы с симптомами запущенного рака легкого: болью, кровотечением и др.
Иногда курс лучевой терапии сочетают с химиотерапией. Такое лечение называется химиолучевой терапией.
Таргетная терапия при раке легкого
Чтобы бесконтрольно размножаться, выживать и защищаться от иммунной системы, раковые клетки используют некоторые молекулярно-генетические механизмы. Знания о них помогают создавать особые таргетные препараты. По сравнению с химиопрепаратами, они действуют более прицельно, блокируют лишь определенные вещества, которые находятся в раковых клетках.

При раке легкого применяют следующие таргетные препараты:
- Блокаторы ангиогенеза (роста новых сосудов в злокачественной опухоли): бевацизумаб (Авастин), рамуцирумаб (Цирамза).
- Блокаторы EGFR (белка-рецептора, который в норме активирует деление клеток, а в раковых клетках становится слишком активным и способствует их бесконтрольному размножению): эрлотиниб (Тарцева), афатиниб (Гилотриф), гефитиниб (Иресса).
- Блокаторы ALK (мутантного белка, который обычно возникает у некурящих людей и тех, которые курят понемногу): кризотиниб (КСАЛКОРИ), церитиниб (Зыкадия), алектиниб (Алеценса), бригатиниб (Алунбриг).
- Блокаторы BRAF (мутантный белок, который заставляет клетки бесконтрольно размножаться): дабрафениб (Тафинлар), траметиниб (Мекинист).
Раковое поражение плевры
Лечение пациентов с опухолевым плевритом начинается с плевроцентеза — эвакуации жидкости из плевральной полости, что сразу приводит к улучшению самочувствия, уменьшению одышки, болей и улучшению качества жизни больного. Исследование удаленной жидкости, проводимые непосредственно после плевроцентеза позволяет более точно установить причину опухолевого плеврита. Уточнить степень распространенности не только плеврита, но и специфических изменений, которые вызвали это состояние помогает целый арсенал современных методов исследования, доступный пациентам клиники (рентгенологическое исследование, компьютерная томография органов грудной полости, ультразвуковое исследование и пр.).
Через некоторое время после пункции в плевральной полости может снова скапливаться выпот. Если жидкость нужно повторно вывести менее чем через месяц после плевроцентеза, врач может установить внутриплевральную порт-систему – небольшую титановую емкость с силиконовой мембраной, которую помещают под кожу и соединяют катетером с плевральной полостью. В дальнейшем, для того чтобы вывести плевральный выпот, нужно всего лишь нащупать под кожей мембрану порт-системы и ввести в нее специальную иглу.
Также через внутриплевральную порт-систему можно вводить химиопрепараты. Внутриплевральная химиотерапия помогает уменьшить образование выпота. Она особенно эффективна у больных с мезотелиомой, раком легкого и молочной железы.
При необходимости возможно проведение видеоторакоскопии, которая позволяет исследовать плевральную полость через прокол в грудной стенке с помощью специального инструмента – торакоскопа произвести прицельную биопсию подозрительного участка ткани с последующим морфологическим исследованием, что в большинстве случаев позволяет установить точный диагноз.
Системная химиотерапия не только воздействует на саму раковую опухоль, но и при хорошей чувствительности к химиопрепаратам может привести к ликвидации плеврита у большинства пациентов.
Плевродез
При невозможности химиотерапии возможно проведение плевродеза в результате которого листки плевры спаиваются между собой за счет введения различных химических веществ с местным противоопухолевым действием.
Внутриплевральная терапия при раке может быть дополнена иммунотерапией LAK-клетками, рекомбинантным интерлейкином – 2 или их сочетанием.
Выбор в пользу того или иного варианта иммунотерапии или последовательности иммунотерапевтического воздействия проводится онкологом на основании результатов обследования пациента с учетом скорости накопления жидкости, общего состояния, чувствительности к химиопрепаратам, ранее проводимого лечения и т.д.). Плевроцентез проводится опытными специалистами при помощи специального устройства Pleurocan (США) и только под ультразвуковой навигацией, что обеспечивает безопасность, быстроту и точность вмешательства.
Лечение рака легких 4 стадии с метастазами
На 4 стадии рака легкого (распространенной по организму опухоли), возможно паллиативное или симптоматическое лечение в Москве. Паллиативное лечение — это вынужденный подход, при невозможности имеющимися на сегодняшний день средствами победить онкологию, оно направлено на уменьшение страданий, продление и улучшение качества жизни больных. Наши пациенты получают адекватное обезболивание, кислородотерапию, детоксикацию, при необходимости проводятся паллиативные операции (наложение трахеостомы, торакоцентез, плевродез и т.д.). При раковых пневмониях осуществляется все необходимое противовоспалительное лечение, при легочных кровотечениях — гемостатическая терапия.
Паллиативное лечение рака легкого в Европейской клинике
Отделение симптоматической и паллиативной терапии клиники располагает всеми необходимыми возможностями ухода за тяжелобольными пациентами, не способными себя обслужить, включая дополнительное наблюдение за пациентом силами патронажной сестры, медицинской сестры или врача-реаниматолога.
Используются современные европейские протоколы интенсифицированного лечения больных злокачественными заболеваниями легкого для уменьшения массы опухоли и торможения темпов ее роста. При необходимости производится эвакуация полостных выпотов, различные виды обезболивания, дезинтоксикационная, противорвотная терапия, общеукрепляющее лечение, многокомпонентная терапия, направленная на поддержку функционирования жизненно важных органов (сердца, печени, почек, легких), предпринимаются все меры, направленные на улучшение самочувствия и качества жизни больного.
Правильное лечение рака легких 4 степени с метастазами помогает продлить жизнь пациента, повысить её качество. В современной онкологии изменилось само понимание неизлечимых злокачественных опухолей. Такой диагноз воспринимается не как приговор, а как хроническое заболевание, при котором пациенту все еще можно помочь. В Европейской клинике для этого есть всё необходимое.
Этапы лечения рака легкого на разных стадиях
Если подводить итог всему вышесказанному, то лечение злокачественных опухолей легких в Москве в зависимости от стадии будет выглядеть следующим образом:
- При раке стадии 0, когда опухоль не прорастает за пределы слизистой оболочки, обычно ограничиваются хирургическим вмешательством. Лучевая терапия и химиотерапия не требуется.
- На стадии 1 также зачастую ограничиваются хирургическим лечением. При высоком риске рецидива проводят адъювантную химиотерапию или лучевую терапию. Во время операции может быть удалена доля или меньшая часть легкого, а также некоторые лимфоузлы, которые находятся в средостении.
- На 2 стадии перед хирургическим вмешательством врач может назначить курс неоадъювантной химиотерапии или лучевой терапии. Объем операции может быть разным, вплоть до удаления всего легкого. После удаления опухоли всегда проводят курс химиотерапии, иногда — лучевой терапии.
- Лечение рака легкого 3 стадии начинают с химиотерапии и лучевой терапии. Затем, если опухоль может быть удалена, и состояние пациента позволяет, проводят операцию. В противном случае лучевая терапия и химиотерапия становятся основными методами лечения рака легких 3 степени..
- При немелкоклеточном раке легкого 4 стадии проводится паллиативная и симптоматическая терапия.
Врачи Европейской клиники знают, как помочь
Мы уверены, что помочь можно всегда, поэтому беремся за лечение пациентов с раком легкого на любой стадии:
- В Европейской клинике выполняются сложные хирургические вмешательства.
- Наши врачи, применяются оригинальные препараты последних поколений с доказанной эффективностью.
- У нас функционирует уникальное для России отделение паллиативной помощи.
- Для пациентов, у которых дальнейшее лечение нецелесообразно, мы предоставляем услуги хосписа с неограниченным временем пребывания.
- Мы знаем, как повысить эффективность химиотерапии, что делать, если назначенное лечение не помогает.
- Наши доктора умеют бороться с плевритом и другими осложнениями рака легких.
- Мы применяем эффективную поддерживающую терапию, которая помогает справиться с побочными эффектами и хорошо перенести основное лечение.
Где лучше лечить рак легкого: в России или за границей?

Среди российских онкобольных, решивших лечиться за границей, наибольшей популярностью пользуются израильские, европейские, в меньшей степени (из-за высокой стоимости услуг) — американские клиники. Несомненно, за рубежом зачастую можно получить более качественную медицинскую помощь.
Но и в России есть клиники, где доступны практически те же процедуры, препараты, врачи работают по международным протоколам. В Европейской клинике есть все необходимое. Здесь лечат не хуже, чем в известных европейских или израильских клиниках. Причем, для пациента это обходится дешевле.
В Европейской клинике больных регулярно консультируют наши коллеги из-за рубежа. А в случаях, когда это действительно необходимо, мы помогаем нашим пациентам получить медицинские услуги за границей у ведущих специалистов.
Читайте также:

