Рак легкого лечение медицинская литература
Рак лёгкого (бронхогенный рак, бронхогенная карцинома) – злокачественное новообразование легкого, происходящее из эпителиальной ткани бронхов различного калибра. В зависимости от места появления подразделяется на центральный, периферический и массивный (смешанный).
Персонализированный подход к терапии
немелкоклеточного рака легкого
Рак легкого – одно из самых распространенных онкологических заболеваний в мире как среди мужчин, так и среди женщин. По данным доклада Всемирной организации здравоохранения World Cancer Report [1], в 2012 году было выявлено 1,82 миллиона новых случаев рака легкого в мире и 1,56 миллиона смертей от этого заболевания, что составило около 20% в структуре онкологической смертности. Именно рак легкого является ведущей причиной смертности от онкологических заболеваний среди мужчин и второй причиной после рака молочной железы – у женщин [1]. Прогноз заболевания, как правило, неблагоприятен: пятилетняя выживаемость составляет не более 17,7% [2]. При этом в большинстве случав рак легкого выявляется уже на поздней стадии, когда полное хирургическое удаление опухоли уже невозможно и терапевтические возможности ограничиваются химиолучевым лечением [3]. В связи с этим одной из важнейших задач онкологии становится своевременная диагностика и скрининг рака легкого, а также первичная профилактика и, прежде всего, борьба с табакокурением – главным фактором риска развития заболевания.
По данным некоторых исследований, около 90% случаев заболевания ассоциировано с курением [4], что, в свою очередь, обусловлено высоким содержанием в сигаретном дыме канцерогенов. По статистике, из-за рака легкого, развившегося вследствие курения, ежегодно погибает 1,5 миллиона человек, и при сохранении существующей тенденции к 2020-2030 годам их число увеличится до 2 миллионов смертельных случаев [5].
Известен и ряд других факторов риска развития рака легкого:
- Мутагенное воздействие радона, образующегося вследствие распада радиоактивного радия
- Лучевая терапия, применяющаяся для лечения других злокачественных заболеваний
- Канцерогенное действие токсинов, содержащихся в окружающей среде (асбеста, мышьяка, никеля, ионизирующего излучения и так далее)
- Легочный фиброз
- ВИЧ-инфекция
- Наследственность
- Канцерогенное воздействие кулинарных жиров, используемых для термической обработки пищи [6]
Как правило, клиническая картина появляется уже на поздних стадиях заболевания вследствие распространения первичной опухоли, появления метастазов, а также паранеопластических синдромов.
К наиболее распространенным симптомам заболевания относятся:
- Кашель, который продолжается длительное время или постепенно ухудшается
- Кашель с кровью или мокротой цвета ржавчины
- Боль в груди, усиливающаяся при глубоком дыхании, кашле или смехе
- Охриплость
- Потеря веса, отсутствие аппетита
- Одышка
- Усталость, слабость
- Рецидивирующие инфекции дыхательных путей (бронхит, пневмония)
При метастазирующем раке легкого в зависимости от локализации метастатического процесса могут появляться боли в костях, головная боль, онемение конечностей, головокружение, пожелтение кожи и склер, увеличение лимфатических узлов. В связи с проникновением в кровоток гормоноподобных веществ развиваются паранеопластические синдромы, которые могут быть первыми симптомами рака легкого: гиперкальциемия, синдром Кушинга, различные изменения в крови, гипертрофическая остеоартропатия, полимиозиты, дерматомиозиты и др.
При подозрении на рак легкого, прежде всего, проводят тщательный клинический осмотр пациента. Выявление явных признаков заболевания может свидетельствовать о прогрессирующем заболевании.
Основными мероприятиями, на основании которых устанавливается диагноз рака легкого, являются радиографические методы исследования и, прежде всего, компьютерная томография (КТ) грудной клетки с контрастированием, позволяющая оценить расположение опухоли и планировать прицельную биопсию. Чувствительность КТ составляет 55%, специфичность – 81% [7]. Однако с помощью КТ зачастую не удается идентифицировать метастазы, в том числе и в лимфоузлах средостения. В таких случаях преимущество отдается позитронно-эмиссионной томографии (ПЭТ), которая позволяет визуализировать как первичную опухоль, так и метастазы, а также оценивать промежуточную эффективность лечения. Также целесообразно выполнение совмещенного ПЭТ/КТ исследования.
ВОЗ в 2015 году предложила обновленную классификацию опухолей легкого [8], в соответствии с которой выделяются девять типов аденокарциномы легкого: со стелющимся ростом (lepidic), ацинарная, папиллярная, микропапиллярная, солидная, а также четыре подтипа инвазивной муцинозной аденокарциномы – смешанная инвазивная муцинозная и немуцинозная, коллоидная, фетальная и кишечная. Кроме того, выделяют три типа преинвазивных образований: атипическая аденоматозная гиперплазия, аденокарцинома in situ (немуцинозная и муцинозная) и минимально инвазивная аденокарцинома (также муцинозная и немуцинозная).
Отдельным типом опухоли является аденосквамозная карцинома, плоскоклеточный рак (ороговевающий, неороговевающий, базалоидная плоскоклеточная карцинома), крупноклеточная карцинома, а также нейроэндокринные опухоли, к которым отнесены мелкоклеточная и крупноклеточная нейроэндокринная карцинома, типичный и нетипичный карциноид.
Наряду с гистологической оценкой опухоли важное значение в определении терапевтической тактики имеет стадирование заболевания, которое проводится в соответствии с AJCC TNM (The Tumor, Node, Metastasis – опухоль, узел, метастазы) классификацией [9]. Она основана на оценке трех параметров опухоли: T – размера и локализации первичной опухоли, N – вовлеченности в опухолевый процесс лимфатических узлов средостения и M – наличия отдаленных метастазов в другие органы, включая другое легкое. Прогноз рака легкого коррелирует как с клинической, так и с патологической стадией заболевания.
- Мутация EGFR является предиктором чувствительности к ингибиторам тирозинкиназы EGFR – гефитинибу, эрлотинибу и афатинибу
- Транслокация ALK ассоциируется с высокой чувствительностью к ингибиторам ALK кризотинибу, а также церитинибу и алектинибу. Последние два препарата пока не зарегистрированы в РФ
- Транслокация ROS1 связана с положительным ответом на терапию кризотинибом
- При мутации BRAF целесообразно назначение комбинации дабрафениба и траметиниба, а также низкомолекулярных ингибиторов тирозинкиназы вемурафениба и дабрафениба
- MET-аномалии считаются предиктором чувствительности к ингибитору МЕТ кризотинибу
- Транслокации RET ассоциированы с положительным ответом на таргетную терапию RET-ингибиторами кабозатинибом, вандетинибом и алектинибом
Со временем к таргетной терапии формируется устойчивость – чаще всего это происходит в течение года после начала лечения. При развитии резистентности к ингибиторам тирозинкиназы EGFR целесообразно назначать таргетный препарат третьего поколения осимертиниб, который в таких случаях, по данным исследования III фазы AURA3, более эффективен, чем стандартные режимы химиотерапии [12].
При прогрессировании на фоне приема ингибитора ALK кризотиниба у пациентов с ALK-позитивным НМРЛ целесообразен перевод на таргетные препараты второго поколения бригатиниб, алектиниб или церитиниб. Следует отметить, что препараты второго поколения ингибиторов ALK в России еще не зарегистрированы.
Выбор терапевтической тактики при НМРЛ зависит от ряда факторов и прежде всего стадии заболевания.
Терапия I и II стадий НМРЛ
Лечение раннего НМРЛ основывается на хирургической резекции опухоли. Процедурой выбора считается лобэктомия, позволяющая, в отличие от пневмонэктомии, сохранить легочную функцию. Уменьшить последствия хирургического вмешательства, улучшить качество жизни и увеличить переносимость постоперационной адъювантной химиотерапии позволяет проведение операции с помощью видеоторакоскопии, которая обеспечивает меньшую инвазивность по сравнению с открытой торакотомией 16.
С целью снижения риска прогрессирования заболевания после радикальной резекции НМРЛ показана адъювантная химиотерапия, которую назначают по окончании восстановления пациента после хирургического вмешательства, но не позже 8 недель. Длительность лечения составляет от 3 до 4 циклов. Для химиотерапии (за исключением НМРЛ IA стадии) используются любые платиносодержащие комбинации с включением препаратов 3 поколения или этопозида.
После полной резекции опухоли рекомендовано каждые 6 месяцев на протяжении первых двух лет проходить физический осмотр и проводить КТ грудной клетки. В дальнейшем обследование проводят один раз в год.
Терапия III стадии НМРЛ
Терапевтическая тактика при НМРЛ III стадии зависит от вовлеченности в опухолевый процесс медиастинальных лимфоузлов, которая выявляется с помощью КТ или ПЭТ. При отсутствии таковой проводят хирургическое удаление опухоли с последующей оценкой состояния лимфоузлов, как и при начальном раке. После резекции назначают адъювантную химиотерапию. В случаях, когда подтверждена инвазия в медиастинальные лимфоузлы, пациентам показан двух- или трехмодальный подход.
Терапия IV стадии НМРЛ
Целью лечения IV стадии НМРЛ является замедление прогрессирования заболевания, уменьшение выраженности клинической картины и минимизация побочных эффектов лекарственных препаратов. Терапия на этой стадии рассматривается исключительно как паллиативная [17].
По окончании начальной терапии назначается последующая, в составе которой целесообразно применять иммунотерапевтические препараты, при наличии мутации EGFR ингибиторы тирозинкиназы (гефитиниб, эрлотиниб, афатиниб, а пациентам, прогрессирующим на фоне терапии ИТК EGFR 1 и 2 поколения – представитель 3 поколения осимертиниб), а транслокации ALK – церитиниб или алектиниб [18].
Наряду с этим назначается терапия, направленная против очагов заболевания в головном мозге, костной ткани и так далее, а также симптоматическое лечение. Также крайне важную роль в терапии рака легкого на поздних стадиях играет поддерживающая терапия [19].

Онкология - Ганцев Ш. X. - Учебник
Описание: Учебник отличается от аналогов по ряду позиций. Во-первых — строгим соответствием учебной программе. Во-вторых — использованием опыта ведущих клиник и ученых России в рамках единой образовательной концепции. В-третьих — впервые в отечественной педагогической практике медицинских вузов изложены стандарты диагностики и лечения в онкологии. Студент, обучающийся на кафедрах, получит первоначальные знания о стандартизации лечебно-диагностического процесса, что на сегодняшний день очень важно. Можно и дальше перечислять плюсы учебника, но мне представляется, что главным экспертом издания является студент. Учебник создан для него, и он его по достоинству оценит.

Онкология - В.И. Чиссов, С. Л. Дарьялова - Учебник с компакт-диском
Описание: В учебнике представлена современная информация об этиологии, патогенезе, клинической картине, диагностике, лечении, профилактике и прогнозе онкологических заболеваний. В самостоятельных разделах приводятся сведения по общим вопросам онкологии, а также по особенностям онкологических заболеваний у детей. Учебник включает приложение на компакт-диске, содержащее тестовый экзамен, дополнительные иллюстрации и разнообразные справочные материалы.
Учебник подготовлен в соответствии с действующей программой по онкологии и предназначен для студентов медицинских вузов.

Молекулярная онкология: клинические аспекты - Имянитов Е.Н., Хансон К.П.
Описание: Бурное развитие молекулярной генетики, в частности открытие онкогенов и антионкогенов, кардинально видоизменило представления о механизмах возникновения новообразований. Тем не менее принято считать, что прогресс в теоретической области практически не отразился на состоянии дел в клинической онкологии. Содержание настоящего издания призвано продемонстрировать несостоятельность подобных утверждений.
Действительно, если 70-е и 80-е гг. XX века характеризовались прогрессом преимущественно в экспериментальной области, символом последнего десятилетия стали именно практические достижения молекулярной онкологии. К настоящему моменту молекулярно-генетические подходы рутинно используются на всех этапах онкологической помощи, т. е. в профилактике, диагностике, лечении и мониторинге пациентов. Наиболее заметные успехи отмечены в развитии лабораторных методов выявления групп онкологического риска, поиске диагностических и прогностических маркеров новообразований, разработке патогенетически обоснованных подходов к химиопрофилактике и химиотерапии неоплазм и, наконец, в генотерапии рака.

Лечение хронической боли онкологического генеза - Г.А. Новиков - Учебное пособие
• МРЛ — мелкоклеточный рак лёгкого
• НМРЛ — немелкоклеточный рак лёгкого.
ЭПИДЕМИОЛОГИЯ Наибольшая распространённость рака лёгкого среди населения отмечена в возрасте от 75 до 79 лет. В 2001 г в России выявлено 10 183 случая рака лёгкого у женщин и 51 962 у мужчин. Стандартизованная заболеваемость в РФ — 43,23 на 1 ООО ООО населения (оба пола, 2001 г.): у мужчин — 62,86, у женщин — 7,18. Умерли в 2001 г. 48227 мужчин и 8791 женщина. Средний возраст умерших мужчин — 64,3, женщин — 68,2 года. После облучения в зоне Чернобыльской АЭС у участников ликвидации последствий аварии рак лёгкого занимает первое ранговое место, составляя 35% всех онкологических заболеваний.
РАННЯЯ ДИАГНОСТИКА РАКА ЛЁГКОГО
ПРОФИЛАКТИКА
• Поскольку 80% случаев рака лёгкого связано с курением сигарет, необходимость отказа от курения в рамках первичной профилактики этого заболевания не вызывает сомнений.
Лиц, контактировавших с радионуклидами и асбестом, рекомендуют наблюдать в течение длительного времени, однако эффективность подобных программ наблюдения пока не определена8.
При первом подозрении на профессиональное заболевание (включая рак лёгкого, мезотелиому, пневмофиброз и экссудативный плеврит), больным рекомендуют пройти диагностическое обследование в пульмонологической клинике или в специализированном отделении профессиональной патологии.
Необходимы регулярное и компетентное клиническое обследование и лечение лиц с заболеваниями, вызванными воздействием радионуклидов и асбеста (профессиональные болезни). Согласно инструкциям по технике безопасности многих стран, работы с асбестом недопустимы в закрытых помещениях. Использование и обработка материалов, содержащих асбест, в жилых домах абсолютно недопустимы.
КЛАССИФИКАЦИЯ
Клиникоанатомические формы
Принципиально важно выделять две основные формы рака лёгкого — центральную и периферическую. Они составляют 95% наблюдений этого заболевания. Центральный рак поражает крупные бронхи (до сегментарных включительно). Периферический рак локализуется в субсегментарных и более мелких бронхах. Центральная форма прорастает элементы корня, рано распространяется на главные бронхи и трахею. Периферический рак обычно формирует шаровидный узел в паренхиме лёгкого.
Атипичные формы (развиваются чаще всего при МРЛ): периферический рак с синдромом Панкоста (рак Панкоста, апикальный рак или опухоль верхней борозды лёгкого, как его называют за рубежом); медиастинальный рак; первичный карциноматоз лёгких.
РАННИЕ ЭТАПЫ ДИАГНОСТИКИ
ОТНОСИТЕЛЬНО РАННИЕ СИМПТОМЫ (>50% СЛУЧАЕВ)
Кашель или изменение характера кашля.
Кровохарканье.
Боль (в груди или вне грудной клетки).
Одышка.
Потеря аппетита, снижение массы тела.
ДАННЫЕ ФИЗИКАЛЬНОГО И ИНСТРУМЕНТАЛЬНОГО ОБСЛЕДОВАНИЯ
• Области затенения на обзорных рентгенограммах органов грудной полости.
Увеличение шейных, надключичных, подмышечных лимфатических узлов.
Метастазы (в головном мозгу, костях, печени, надпочечниках).
Стридор или характерные хрипы при аускультации (обтурация опухолью крупного бронха).
СЕМИОТИКА
Симптомы поражения лёгких: продуктивный кашель с примесью крови в мокроте; боль в груди, плевральный выпот, охриплость голоса (обусловлены сдавлением медиастинальной опухолью возвратного гортанного нерва); лихорадка; стридор; обструктивная пневмония (характерна для эндобронхиальных опухолей); одышка; синдром сдавления верхней полой вены (сочетание расширения вен грудной клетки, цианоза и отёка лица с повышением внутричерепного давления; вызван обструкцией сосуда опухолью средостения). Иногда болезнь может протекать стёрто. Внелёгочные симптомы
Внелёгочные метастазы сопровождаются снижением массы тела, недомоганием, признаками поражения ЦНС (эпилептиформные судороги, признаки карциноматоза мозговых оболочек), болями в костях, увеличением размеров печени и болями в правой подрёберной области, гиперкальциемией.
Паранеопластические проявления (внелёгочные проявления, не связанные с метастазами) возникают вторично вследствие действия гормонов и гормоноподобных веществ, выделяемых опухолью. Сюда относят синдром Кушинга, гиперкальциемию, остеоартропатии и гинекомастию. Эктопическая секреция АКТГ вызывает гипокалиемию и мышечную слабость, неадекватная секреция антидиуретического гормона приводит к гипонатриемии.
Опухоль Панкоста может вызывать симптомы, обусловленные поражением плечевого сплетения и симпатических ганглиев; возможно разрушение позвонков в результате прорастания опухоли. Возникают боли и слабость в руке, её отёк, синдром Хорнера (птоз, миоз, энофтальм и ангидроз, связанные с повреждением шейного отдела симпатического ствола).
АМБУЛАТОРНЫЙ ЭТАП
На амбулаторном этапе необходимо ответить на следующие вопросы.
Тип рака — немелкоклеточный рак лёгкого (НМРЛ) или мелкоклеточный (МРЛ).
Возможна ли радикальная операция.
Можно ли в принципе (перспективе) провести радикальное лечение у неоперабельного больного и при каких условиях.
В последнюю категорию можно отнести следующих больных:
Больные с возможностью резекции НМРЛ, но отягощенные тяжёлыми сопутствующими заболеваниями или отказавшиеся от операции (им можно провести лучевое и лекарственное лечение по радикальной программе).
Больные МРЛ.
Возраст сам по себе не может служить противопоказанием к радикальному лечению и влиять на выбор метода лечения, однако сопутствующие заболевания и риск токсических.реакций при химиотерапии необходимо строго учитывать.
Все больные с подтверждённым раком лёгкого или с подозрением на это заболевание должны пройти ряд исследований:
Сбор анамнеза и физикальное обследование (всех органов).
Оценку общего состояния, определение массы тела и степень похудания.
Рентгенографию грудной клетки.
Цитологическое или гистологическое подтверждение диагноза (анализ мокроты, бронхоскопия).
Гематологический и биохимический скрининг, включая определение концентрации кальция сыворотки крови и функциональные пробы печени0.
Крайне желательно у всех больных НМРЛ указать ориентировочную стадию заболевания уже на амбулаторном этапе.
В идеале диагноз должен быть подтверждён до операции при бронхоскопии, цитологическом анализе мокроты, бронхоальвеолярном смыве, абразионной или игловой биопсии. Если диагноз подтвердить не удалось, показана срочная криобиопсия на операционном столе во время торакотомии. При отсутствии морфологического подтверждения диагноза показана срочная биопсия во время торакотомии до выполнения резекции лёгкого0.
УГЛУБЛЁННОЕ ОБСЛЕДОВАНИЕ И ОПРЕДЕЛЕНИЕ СТАДИИ У БОЛЬНЫХ НМРЛ
Больным, которым предполагается радикальная операция или лучевая терапия, необходимо уточнить распространённость опухоли в средостении и в отдалённых органах в срок до 2 нед. При возможности желательно выполнить КТ(оценить дескрипторы Т, N и М). Углублённое обследование проводят в специализированных лечебных учреждениях.
НЕОПЕРАБЕЛЬНЫЕ БОЛЬНЫЕ: ОБЪЁМ ИССЛЕДОВАНИЙ
У неоперабельных больных НМРЛ необходимо оценить основные прогностические факторы: распространённость опухоли, общее состояние, степень потери массы тела, сдвиги биохимических тестов с учётом пола и гистологических особенностей опухоли.
Неоперабельным больным НМРЛ необходимо выполнить рентгенографию грудной клетки, цитологическое/гистологическое исследование, морфологический и биохимический анализы крови для уточнения возможностей проведения лучевой терапии по радикальной программе0.
КОНТАКТЫ СПЕЦИАЛИСТОВ С БОЛЬНЫМ И ИНФОРМАЦИОННАЯ ПОДДЕРЖКА
Психологическая работа с больным — важная задача для всего медицинского персонала. Отсутствие информации повышает нервозность, вызывает у больного чувство тревоги и неудовлетворённости. Больных следует информировать о характере заболевания и методах лечения в максимально короткие сроки (не более недели после подтверждения диагноза). В этот срок необходимо согласовать с больным и обсудить диагноз, выбрать метод лечения, сообщить о решении консилиума врачу общей практики. Таким образом, больной раком лёгкого в срок до 2 нед должен быть информирован о стадии заболевания, прогнозе и методах лечения. Необходимо периодически контролировать правильность представлений больного о тяжести его заболевания и возможных исходах8.
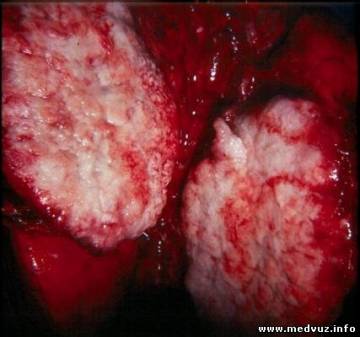
НЕМЕЛКОКЛЕТОЧНЫЙ РАК ЛЁГКОГО
Хирургическое вмешательство даёт наибольший шанс на полное излечение от НМРЛВ.
Хирургическое лечение. В большинстве случаев в качестве координатора выступает врач общей практики. Его вовлекают во все процессы от диагностики до паллиативных мероприятий. Информация о течении заболевания должна быть доведена до сведения больного и родственников0. Объём операции определяет специалистонколог или онкологический консилиум.
Лучевая терапия. Облучение как самостоятельный метод лечения показано при НМРЛ I и II стадий, а также у больных распространённым процессом в качестве адъювантного курса или паллиативного лечения. При III стадии НМРЛ радикальность лучевой терапии весьма сомнительна, но продлить жизнь больным удаётся в большинстве случаев0. Дооперационную лучевую терапию при НМРЛ не рекомендуют'*.
Если опухоль удалена не полностью (нерадикальная операция), обычно проводят дополнительную лучевую терапию. Эффективность такого лечения не подтверждена рандомизированными исследованиями. Лучевая терапия у больных НМРЛ показана после нерадикальных операций8.
Неоперабельным по обще медицинским противопоказаниям больным НМРЛ I'll стадий или отказавшимся от лечения показана лучевая терапия по радикальному плану*. У таких больных включение средостения в зону облучения приносит больше вреда, чем пользы. При III стадии НМРЛ эффективность лучевой терапии по радикальной программе весьма сомнительна0.
Паллиативная лучевая терапия обычно даёт хороший симптоматический эффект при боли в груди, кашле и кровохарканье0.
В учреждениях, оборудованных аппаратурой для внутрибронхиальной радиотерапии (типа микроселектрона), показано паллиативное облучение стенозированного участка дыхательных путей с использованием эндостатов. Химиотерапия. У больных НМРЛ N2 (но не N1) показана послеоперационная лучевая терапияА. У больных распространённым НМРЛ (III—IV стадии) с локальными симптомами опухоли показана химиотерапия по паллиативной программе.
МЕЛКОКЛЕТОЧНЫЙ РАК ЛЁГКОГО
Основные факторы прогноза при МРЛ: распространённость опухоли, общее состояние больного, уровень лактатдегидрогеназы сыворотки крови, функциональные пробы печени, уровень натрия в крови.
Операбельным больным МРЛ показано полное обследование, включая биопсию костного мозга, для исключения отдалённых метастазов. Больным операбельным МРЛ показана адъювантная лучевая и химиотерапия8. При неожиданном подтверждении распространённого МРЛ во время торакотомии следует отказаться от резекции в пользу химиолучевой терапии0.
Химиолучевая терапия. Послехимиолучевого лечения в прогностически благоприятных случаях МРЛ три года живут около 20% больных МРЛ. В случаях ремиссии рекомендуют продолжить химиотерапию до 6 курсов лечения по схемам: доксорубицин, циклофосфамид, этопозид (АСЕ), ифосфамид, карбоплатин, этопозид (ICE) или препарат платины, этопозид (РЕ)А. Сочетание облучения с химиотерапией повышает токсичность лечения.
В связи с высоким риском поражения головного мозга больным распространённым МРЛ показано профилактическое облучение черепа. Оно не даёт тяжёлых осложнений, но несколько снижает риск метастазирования в головной мозг. Одновременное проведение химиотерапии не рекомендуют, необходимо выждать месяц после облучения черепаА. Лечение больных МРЛ с неблагоприятным прогнозом. Большинству больных распространённым МРЛ с нарушением общего состояния показаны 4 курса полихимиотерапии А.
Поддерживающая терапия. Больным и врачам общей практики следует получить письменные инструкции с описанием симптомов осложнений операции и химиолучевого лечения, проявляющихся в срок до 10 дней. При выявлении признаков нейтропении больной должен быть срочно госпитализирован в специализированное отделение. Показана интенсивная антибиотикотерапия. Профилактическое применение антибиотиков широкого спектра и миелоидных факторов роста не рекомендуют0.
ОБСЛУЖИВАНИЕ НЕИЗЛЕЧИМЫХ БОЛЬНЫХ
Часто можно улучшить качество жизни больного раком лёгкого, даже если излечение невозможно. Речь идёт не о продлении страданий, а об обеспечении достойного и безболезненного умирания. Как правило, паллиативное и симптоматическое лечение рака лёгкого практически не отличается от мероприятий при раке другой локализации. В бригаду паллиативного лечения обязательно входят медицинские сестры. Они должны вовремя сигнализировать о существенных изменениях в состоянии больного, а в некоторых случаях и самостоятельно принимать решения в экстренной ситуации0.
Работа с родственниками — обязательная часть комплексной симптоматической поддержки больных. Тяжёлый психологический стресс — обычное состояние ухаживающего за неизлечимым больным персонала0.
В фокусе внимания команды, осуществляющей симптоматическое лечение онкологического больного, должна быть семья, а не только сам больной.
СПЕЦИФИЧЕСКИЕ ОСЛОЖНЕНИЯ ПРИ ПРОГРЕССИРОВАНИИ РАКА ЛЁГКОГО
ДАЛЬНЕЙШЕЕ НАБЛЮДЕНИЕ
Всех больных раком лёгкого наблюдает амбулаторно врач общей практики, консультирует онкологпульмонолог. Обычно в течение первых 2 лет обследование больного проводят каждые 3 мес, до 5 лет — каждые 6 мес, а затем — 1 раз в год.
Основные методы обследования о Аускультация лёгких, пальпация лимфатических узлов о Обзорная рентгенография органов грудной клетки о Определение активности ферментов печени, СОЭ, проведение общего анализа крови о Оценка общего состояния, контроль массы тела.
Раковоэмбриональный Аг(сывороточный раковоэмбриональный Аг) можно использовать как маркёр НМРЛ (аденокарциномы). Маркёр мелкоклеточного рака лёгкого — нейронспецифическая енолаза (сывороточная нейроноспецифическая енолаза). Эти маркёры имеют значение, только если до лечения было выявлено повышение их концентрации.
Оценка отдалённых результатов лечения в рамках поликлиники или диспансера должна включать: 1) общую выживаемость; 2) безрецидивную выживаемость; 3) качество жизни.
ПРОГНОЗ
Немелкоклеточный рак. Пятилетняя выживаемость в целом не превышает 5— 10% (при учёте всех заболевших). После радикального лечения 5 лет живут в среднем 25%, при I—II стадиях заболевания — 5070%.
Мелкоклеточный рак. Двухлетняя выживаемость после полной ремиссии в результате успешной химиотерапии (иногда с операцией или облучением) составляет 20%. Основная масса больных МРЛ умирает в сроки до 8 мес.
Рак легких на сегодняшний день является одним из наиболее часто встречающихся видов злокачественных новообразований. В среднем в мире на 100 000 человек приходится 40 страдающих раком легких, причем у мужчин болезнь диагностируется в десять раз чаще, чем у женщин, а доля городских жителей в составе всех заболевших в несколько раз больше сельских. Тем не менее современная медицина располагает мощным арсеналом для лечения этого вида онкологии: при своевременном обращении за помощью высока вероятность не только приостановить развитие заболевания, но и забыть о нем навсегда.
Рак легких: характеристика заболевания и прогноз излечения
Ежегодно в мире от рака легких умирает около пяти миллионов человек. Этот вид злокачественного новообразования также называют бронхогенной карциномой или бронхогенным раком. Опухоль развивается из покровного эпителия слизистой оболочки бронхов, альвеол и эпителия бронхиальных желез. Несмотря на то что этиология заболевания до сих пор остается неясной, к основным причинам его возникновения относят:
- курение, в том числе пассивное, — основной фактор риска (вызывает примерно 90% случаев рака легких);
- облучение (проводимая ранее лучевая терапия по причине других опухолей внутригрудной локализации);
- фиброз легких;
- ВИЧ и некоторые другие виды вирусной инфекции (вирус папилломы человека, JC вирус, обезьяний вирус 40, BK вирус и цитомегаловирус);
- генетические факторы;
- алкоголь;
- плохое питание;
- факторы внешней среды, например: повышенная концентрация пылевых частиц в воздухе, воздействие радона и некоторых канцерогенов (наиболее опасным для легких является минерал асбест, а также мышьяк).
Патогенез рака легких на сегодняшний день недостаточно изучен. Что касается роста опухоли, то здесь выделяют три стадии: трансформация нормальной клетки в злокачественную, активизация опухоли и стадия ее прогрессирования. Второй этап наиболее важен, так как злокачественные клетки могут долгое время находиться в неактивном состоянии. Активизации способствует регулярное воздействие вредных факторов, которые стимулируют размножение патогенных клеток. Кроме того, на образование опухоли влияет нарушение защитных функций организма (снижение противоопухолевого иммунитета).
Российская статистика
По заболеваемости рак легкого занимает первое место среди других злокачественных опухолей у мужчин в России, а по смертности — первое место среди мужчин и женщин как в России, так и в мире. От рака легкого ежегодно умирает больше людей, чем от рака простаты, молочной железы и толстой кишки вместе взятых [1] .
При отсутствии должного лечения рака легких прогноз неутешительный: 87% больных умирает в течение двух лет. При использовании хирургических методов выживаемость больных составляет 30% в течение пяти лет. Одновременное использование нескольких методов лечения поднимает данный показатель еще на 40%. Кроме того, шансы на излечение существенно возрастают при раннем обнаружении опухоли, достигая 80%.
Различают четыре стадии рака легких. Нулевой стадии предшествует скрытая, когда раковые клетки можно обнаружить только в результате проведения бронхоскопии, цитологического, гистологического исследования.
Международная классификация стадий злокачественных новообразований TNM (tumor, nodus, metastasis) была разработана французским хирургом Пьером Денуа в 1943–1952 годах. Данная классификация применяется прежде всего для описания анатомического распространения опухоли. В основе классификации лежат три компонента:
- Показатель T характеризует распространенность первичной опухоли.
- Показатель N говорит о наличии и распространенности метастазов в регионарных лимфатических узлах.
- Показатель M иллюстрирует наличие или отсутствие отдаленных метастазов.
Существует множество классификаций рака легких, построенных на разнообразных признаках.
Согласно гистологической классификации рак легких подразделяется на следующие типы:
- аденокарцинома;
- аденосквамозная карцинома;
- плоскоклеточный рак;
- крупноклеточный рак;
- веретеноклеточный рак;
- нейроэндокринная карцинома;
- диффузная идиопатическая легочная гиперплазия.
Самым частым является плоскоклеточный вид, который диагностируется в 80% случаев. Он распространяется медленнее и поддается хирургическому лечению. Мелкоклеточный рак составляет порядка 17% случаев и является особенно опасным, так как для него характерно быстрое распространение на другие органы, за пределы легочной ткани. Выживаемость при мелкоклеточном раке составляет 40% в течение трех лет.
Особенности локализации
По расположению рак легких подразделяется на центральный и периферический. В первом случае первичный опухолевый узел возникает в бронхах (главном, промежуточном, долевом, сегментарном и субсегментарном). По направлению роста выделяют [2] :
- экзофитный (эндобронхиальный) рак, когда опухоль растет в просвет бронха;
- эндофитный (экзобронхиальный) рак с преимущественным ростом опухоли в толщу легочной паренхимы;
- разветвленный рак с муфтообразно перибронхиальным ростом опухоли вокруг бронхов;
- со смешанным характером роста опухоли с преобладанием того или иного компонента.
Периферический рак легкого затрагивает эпителий более мелких бронхов или локализуется в паренхиме легкого. Различают узловую округлую опухоль, пневмониеподобный рак и рак верхушки легкого с синдромом Панкоста.
В большинстве случаев клинические проявления рака легких наблюдаются уже при поздней стадии заболевания — это кашель с выделением крови в мокроте, одышка, боль за грудиной, шумы при дыхании [3] . Симптомы могут возникать вследствие распространения первичной опухоли, метастазирования. Вследствие отдаленных эффектов, не связанных с метастазами, могут возникать паранеопластические синдромы [4] .
На разных стадиях рак легкого может сопровождаться тромбофлебитом, различными вариантами нейро- и миопатии, своеобразными дерматозами, нарушениями жирового и липидного обмена, артралгическими и ревматоидноподобными состояниями. Нередко проявляется остеоартропатией (утолщением и склерозом костей голеней и предплечий, мелких костей кистей и стоп, припухлостью суставов, утолщением фаланг пальцев кистей).
При периферическом раке верхушки легкого возможно появление синдрома Бернара — Горнера, при котором поражается одна сторона лица — опущение века, сужение зрачка и уменьшение потоотделения. Сочетается с болями в плечевом суставе и плече, прогрессирующей атрофией мышц предплечья. Поскольку вышеперечисленные симптомы проявляются вне легких, они довольно часто не распознаются пациентом и не всегда определяются в качестве онкосимптомов.
Помимо специфических, рак легких имеет ряд общих симптомов, таких как потеря аппетита и общая слабость, повышение температуры тела, потливость, потеря веса. Однако следует помнить, что некоторые разновидности данного заболевания долгое время не проявляют себя и не имеют заметных симптомов. Именно в таких случаях решающее значение имеет качественная и своевременная диагностика.
Основными методами диагностики рака легких являются:
- Компьютерная томография (КТ) (предпочтительно) — это наиболее информативный метод в выявлении очаговых изменений легочной ткани.
- Рентгенологическое обследование, которое может включать в себя флюорографию и рентгенографию.
- Бронхоскопия — это обязательное исследование при подозрении на рак легкого. Бронхоскопия дает возможность визуально исследовать трахею, главные, долевые, сегментарные, субсегментарные бронхи и в некоторых случаях бронхи 6-го, 7-го и более порядка. Во время бронхоскопии осуществляется забор материала на биопсию.
- Позитронно-эмиссионная томография (ПЭТ КТ) применяется для определения степени распространения метастазов (в соответствии с результатами производится подбор схемы лечения) и для последующего динамического контроля.
- Эндобронхиальное (EBUS) и эндоскопическое УЗИ (EUS) — современный метод, позволяющий хирургам получить образцы тканей лимфатических узлов в области грудной клетки с помощью одной лишь иглы с оптическим прибором и ультразвука (не прибегая к технике надрезов на шее). Метод позволяет диагностировать увеличенные лимфатические узлы в грудной клетке и точно установить стадию рака легких для планирования лечения.
- Обследование с помощью системы бронхолегочной электромагнитной навигацииSuperDimension Bronchus System™ — новейший метод, который дает возможность при помощи гибкого зонда исследовать пораженный участок, расположенный глубоко внутри лимфоузла или легкого. Данный способ позволяет пульмонологам диагностировать злокачественные новообразования на более ранних стадиях заболевания, что дает возможность выбрать соответствующее лечение рака легких и избежать тяжелых последствий.
- Торакоскопия, или трансторакальная биопсия (VATS), — это визуальное исследование поверхности легких и плевральной полости через грудную стенку при помощи прокола, в который вводится торакоскоп. Дает возможность рассмотреть поверхность легких и плевру, взять образцы опухолевого материала для иммуногистохимии с целью получения гистологического заключения, удалить подозрительные легочные узелки.
- Молекулярно-генетическое тестирование опухолевой ткани: PD-L1, EGFR, ALK; другие мутации — ROS1, BRAF, RET, TRK, MET and KRAS. Цель молекулярно-генетического тестирования заключается в выделении пациентов, которым показана таргетная терапия.
Это важно!
Современный высокоточный метод стадирования рака легкого — ПЭТ/КТ (позитронная эмиссионная томография, совмещенная с компьютерной томографией) всего тела. Исследование проводится при всех стадиях заболевания и показано перед операцией. ПЭТ/КТ может обнаружить очаги опухоли в лимфатических узлах, не детектируемые с помощью КТ, а также отдаленные метастазы в других органах. Зачастую по результатам ПЭТ/КТ пересматриваются первоначальная стадия и тактика лечения [5] .
Качественная диагностика легочной онкологии является крайне важной, поскольку от нее зависит выбор подходящих методов лечения. Основными методами являются хирургическое вмешательство, химио- и лучевая терапия. Благодаря бурному развитию медицинских технологий, данные подходы становятся все более безопасными и эффективными.
После завершения диагностического этапа проводится междисциплинарный консилиум, в рамках которого обсуждают этапы комплексного лечения.
Хирургическое лечение рака легких
Хирургическое лечение проводится на ранних стадиях заболевания и при условии технической возможности удаления опухоли в полном объеме. Обязательным этапом операции, независимо от объема удаляемой легочной ткани, является превентивное удаление лимфатических узлов в зоне регионарного метастазирования, включая средостенные.
Современной тенденцией лечения рака легких является использование малоинвазивных методов, которые производятся с применением миниатюрной видеокамеры. Методика носит название Video-Assisted Thoracoscopic Surgery (VATS). Такие операции сопровождаются менее выраженными болевыми ощущениями, а процесс реабилитации после них протекает быстрее. Данный метод применяются в тех случаях, когда удается диагностировать болезнь на клинической 1-й стадии.
Химиотерапия
Основной метод лечения для большинства пациентов, страдающих раком легких. Ее суть заключается в приеме лекарственных препаратов, разрушающих раковые клетки. Химиотерапия может проводиться в одном из двух режимов:
- Неоадъювантная — назначается перед проведением хирургической операции, чтобы остановить рост злокачественных клеток, уничтожить их и оценить эффективность стандартного лечения.
- Адъювантная — используется для уничтожения оставшихся раковых клеток после операции или курса радиотерапии и позволяет снизить риск рецидива болезни.
Таргетная (целевая) терапия рака легкого
Такие препараты распознают злокачественные клетки по их специфическим признакам и уничтожают их, воздействуя на жизненно важные функции (рост, деление). Кроме этого, такие препараты нарушают кровоснабжение опухоли. Таргетная (целевая) терапия может назначаться как самостоятельный метод лечения или в комбинации с химиотерапией в целях повышения эффективности лечения.
Иммунотерапия
Радиотерапия
Лучевую терапию применяют как самостоятельное лечение, а также в сочетании с химиотерапевтическим методом.
Облучение опухоли мощным пучком гамма-лучей, в результате чего раковые клетки погибают (приостанавливают рост и размножение). При радикальном лучевом лечении облучению подвергают как саму опухоль, так и зоны регионального метастазирования. Лучевая терапия применяется также при мелкоклеточном раке. Новейшие медицинские разработки в области радиотерапии включают в себя:
- дистанционную радиотерапию (External Beam Radiation Therapy — EBRT) — воздействие на раковые клетки производится с помощью наружного источника, расположенного вне человеческого тела;
- стереотаксическую лучевую терапию — методика SBRT — возможность лечения рака легкого первой стадии с помощью облучения опухоли высокой дозой;
- высокодозную брахитерапию (High Dose Rate Brachytherapy — HDR Brachytherapy) — воздействие посредством источника, имплантированного в тело пациента и располагающегося в непосредственной близости от опухоли (или внедренного в опухоль).
Одним из новейших методов лечения рака легких является радиотерапия IMRT RapidArc®, которая позволяет подавать всю дозу облучению исключительно на больную ткань без повреждения здоровых тканей. Применяется в том случае, если раковый процесс затрагивает более одной доли легких, но не распространился за их пределы.
Лучевая терапия зачастую проводится совместно с химиотерапией с целью достижения максимального эффекта лечения.
Паллиативное лечение рака легких
Применяется для неизлечимых больных, когда противоопухолевое лечение противопоказано по определенным причинам или возможности лечения исчерпаны. Паллиативное лечение направлено на борьбу с симптомами, а также повышение качества жизни. Паллиативная помощь может быть оказана в рамках стационара, а также на дому. Объем лечения определяется индивидуально.
Этот вопрос мы адресовали представителю многопрофильного медицинского центра. Рассказывает онколог Европейского медицинского центра Оксана Овсий:
«Рак легких — очень коварное заболевание, зачастую на первых стадиях протекающее бессимптомно. По этой причине при ухудшении общего самочувствия рекомендуется не затягивать с обращением к врачу и прохождением диагностического обследования. Помимо сотрудников государственных онкоцентров, помощь могут оказать и специалисты частных клиник.
Чтобы получить доступ к мировым методикам лечения, не уезжая за рубеж, рекомендую обратиться в Институт онкологии ЕМС в Москве, осуществляющий диагностику и лечение рака по современным американским и европейским протоколам.
Мы оказываем весь комплекс диагностических и лечебных процедур пациентам с раком легких:
- прием (осмотр, консультация) врача-онколога, радиотерапевта и других (первичный, повторный, ежедневный);
- компьютерная томография органов грудной полости, средостения и верхних отделов брюшной полости;
- позитронная эмиссионная томография, совмещенная с компьютерной томографией;
- бронхография, в том числе избирательная;
- аспирационная биопсия из нижних дыхательных путей;
- торакоцентез;
- клиническая лабораторная диагностика, включая сложные диагностические услуги (лабораторный, функциональный, инструментальный, рентгенорадиологический и другие методы исследования), формирующие диагностические комплексы;
- назначение лекарственных препаратов при онкологическом заболевании у взрослых;
- хирургическое лечение;
- радиотерапия;
- химио-, таргетная и иммунотерапия злокачественных опухолей;
- услуги по медицинской реабилитации пациента, перенесшего операцию по поводу онкологического заболевания, химиотерапию, лучевую терапию;
- прием (осмотр, консультация) врача по паллиативной медицинской помощи (первичный и повторный).
Институт онкологии EMC обладает новейшими системами для проведения лучевой и стереотаксической лучевой терапии. Стоит отметить, что высокотехнологичное оборудование позволяет выполнять облучение опухоли с миллиметровой точностью, не допуская облучения здоровой ткани и позволяя успешно бороться с раком легкого 1-й стадии. Во время сеанса аппарат контролирует положение пациента и отклонение мишени облучения в режиме online.
- медицинскую деятельность на основании лицензии ЛО-77-01-019876, выданной Департаментом здравоохранения города Москвы 10 апреля 2020 года;
- высокотехнологичную медицинскую деятельность на основании лицензии ФС-99-01-009514, выданной Федеральной службой по надзору в сфере здравоохранения 25 апреля 2018 года.
** Аккредитация Объединенной международной комиссии (Joint Commission International), полученная Европейским медицинским центром (госпиталь на ул. Щепкина, 35), распространяется на период с 7 апреля 2018 года по 6 апреля 2021 года.
Читайте также:

