Препараты для лечения рака альфа
Препарат человеческого АФП был создан в рамках темы 82/1 ГКНТ РФ: "Создание новых лекарственных средств методами химического и биологического синтеза" (регистрационное удостоверение МЗ РФ № 99/136/12 от 19.04.99) по авторской технологии (патенты РФ № 2100031 и № 2121350) и разрешен к применению в качестве иммуномодулятора при состояниях иммунодефицита и нарушениях в системе цитокинов (инструкция по применению утверждена МЗ РФ 19.04.99). РЕГИСТРАЦИОННЫЙ № ЛС-000941 от 10.06.2010 г.
СОСТАВ: Активное вещество: Альфа-фетопротеин человеческий 0,06 – 0,09 мг. Вспомогательное вещество: Реополиглюкин 4 – 6 мг.
Таким образом, АФП фактически усиливает информационный контроль за правильностью реализации генетической программы всех растущих клеток и в значительной мере влияет на уровень их функциональной активности.
Немного примеров из практики пользования Альфа-фетопротеина. ТЕРАПИЯ ХРОНИЧЕСКИХ ВИРУСНЫХ ГЕПАТИТОВ В И С Динамика клинико-лабораторных показателей лечения с применением препарата "Альфа-фетопротеина" Мед.картотека №2, 2001 Садыков К.Б., Решетников С.С., Утешев Т.А., Жангабылов А.К., Давлятшин Т.И., Нургалиева Ж.Т., Молдагалиева Ж.Т., Седых В.А., Сагитова Е.М., Садыков Н.К., Хлопова И.Н., Калымбетов А.Б., Садыкова С.С., Жилкибаев Б.З.
Выводы: 1. Включение препарата альфа-фетопротеина в комплекс терапии хронических вирусных гепатитов В и С позволяет существенно улучшить результаты лечения и сократить его сроки. 2. Применение альфа-фетопротеина значительно повышает эффективность терапии хронического вирусного гепатита В, в том числе при низкой активности трансаминаз. 3. Использование альфа-фетопротеина в комплексной терапии хронического вирусного гепатита С у детей позволяет добиться быстрого подавления репликации вируса более чем у 90% больных. У взрослых этот показатель ниже и составляет приблизительно 70%. 4. У 80% лиц с положительными результатами лечения ХВГ типа С полученный эффект носит стойкий характер (по результатам трехлетних наблюдений). 5. Применение альфа-фетопротеина в комплексной терапии хронических вирусных гепатитов способствует нормализации показателей иммунной системы.
ИММУНОТЕРАПИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ АЛЬФА-ФЕТОПРОТЕИНОМ ЧЕЛОВЕКА, КАК ЭТАП КОМБИНИРОВАННОГО И КОМПЛЕКСНОГО ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ БОЛЬНЫХ
Представлены предварительные результаты применения альфа-фетопротеина человека (АФП) у 58 больных злокачественными опухолями различных локализаций в III - IV стадии в зависимости от гистологической характеристики опухоли.
Общее количество пациентов составило 58 человек. Из них 51 - онкологический больной с гистологически верифицированным диагнозом рака различных локализаций в III - IV стадии заболевания и гистологической характеристикой дифференцировки опухолей; 7 онкологических больных - после радикально выполненных хирургических вмешательств, находящихся в ремиссии. Кроме того, с целью контроля переносимости 13 условно здоровых людей (добровольцы), получали препарат АФП.
Здоровые добровольцы в течение 4 недель в аналогичной дозе и способе введения также получали препарат АФП.
В ходе лечения периодичность промежуточного обследования составляла один раз в 2 недели. Все больные, независимо от стадии онкопроцесса, органной локализации и гистологического варианта опухоли получали препарат АФП внутривенно струйно (АФП+10,0 мл, 0,9% р-ра NaCl) 1 раз в сутки 4-8 недель из расчета 2 - 4 мкг/кг массы тела.
Оценка непосредственных результатов лечения АФП проводилась по критериям ВОЗ (не ранее чем через 3 недели после завершения курса терапии).
Так, у больных в ходе лечения препаратом АФП мы отметили единую для всех пациентов клиническую картину. Независимо от вида и локализации опухолевых очагов и метастазов у всех больных, в промежутке от 1 до 15 суток лечения препаратом АФП, отмечено усиление болевого синдрома в местах локализации очагов неоплазм после введения препарата.
Также отмечено, что после введения препарата АФП в интервале от 2 до 12 часов у больных наблюдался подъем t0 тела (максимально до 380С), который купировался самостоятельно без использования антипиретиков.
В период наблюдения за состоянием больных отмечено усиление синдрома эндогенной токсемии. Она была более выражена у больных, имевших опухоли и метастазы во внутренних органах и тканях. У пациентов с локализацией очагов опухолевого роста снаружи - эндотоксемия была умеренной.
Перечисленные явления были обусловлены тем, что под влиянием АФП очаги опухолевого роста подвергались тотальному некрозу через реакции острого иммунного воспаления.
Это было подтверждено динамическими гистологическими исследованиями (при возможности доступа к опухоли), когда картина на микроскопическом уровне выглядела как тотальный некроз с обильной макрафагально-лейкоцитарной инфильтрацией и соответствовала после завершения курса лечения II-IV степени терапевтического патоморфоза.
По данным КТ и МРТ-исследования в динамике у больных, получавших лечение препаратом АФП, отмечается более быстрая регрессия опухолевых очагов через элементы воспаления, с последующим замещением фиброзной тканью и склерозированием.
Пример в пульмонологии:
Ренгенологическая динамика у больного с диагноз: метастаз перстневидно - клеточного рака желудка в нижней доле правого легкого, в процессе лечения препаратом АФП. а - ренгенограмма органов грудной полости до лечения (в нижней доле правого легкого определяется метастатический очаг); б - ренгенограмма органов грудной полости через 14 суток лечения (в нижней доле правого легкого определяется метастатический очаг в состоянии некроза с образованием полости); в - ренгенограмма органов грудной полости через 30 суток лечения (в нижней доле правого легкого определяются мелкие кальцинаты).
В резолюциях IV и V Всероссийских съездов онкологов было определено, что одним из наиболее перспективных направлений в онкологии является разработка лекарственных средств, обладающих апоптотическим воздействием на опухолевую клетку.
Возможный механизм девитализации опухолевых клеток при АФП терапии - апоптоз, то есть включение запрограммированной клеточной гибели. Такая клетка поглощается фагоцитами при отсутствии воспалительного процесса, характерного для некроза.
1. Черешнев Валерий Александрович - доктор медицинских наук, профессор, академик РАН, директор НИИ экологии и генетики микроорганизмов УрО РАН, директор НИИ иммунологии и физиологии УрО РАН, председатель УрО РАН. Адрес: 117334, Москва, В-334, Ленинский проспект, 32а, тел.(095) 9381858; 620219, Екатеринбург, ГСП-169, ул. Первомайская, 91, тел.(3432) 744133. 2. Родионов Сергей Юрьевич - кандидат медицинских наук, зам. директора по производству ЗАО "Институт новых медицинских технологий". Адрес: 614059, Пермь, ул. Красногвардейская, 7, кор. 2, кв. 111, тел. (3422) 677307, 410300. 3. Васильев Николай Владимирович - доктор медицинских наук, профессор, академик РАМН, зам. директора по науке Томского НИИ онкологии СО РАМН, зам. директора по науке НИИ им. Мечникова г. Харьков, Украина. 4. Орлов Олег Алексеевич - доктор медицинских наук, зав. курсом онкологии ГОУ ВПО "Пермская медицинская академия МЗ РФ". Адрес: 614000, Пермь, ул. Пушкина, д. 66, кв.37; тел. (3422) 270472, 127864. 5. Черкасов Владимир Аристархович - доктор медицинских наук, профессор, академик РАЕН, зав. кафедрой госпитальной хирургии с курсом онкологии, ректор ГОУ ВПО "Пермская государственная медицинская академия МЗ РФ". Адрес: 614000, Пермь, ул. Куйбышева, 39, тел.(3422) 904410
При внутримышечном введении максимальная концентрация АФП в плазме достигается через 1-2 часа. Полувыведения альфа-фетопротеина может составлять от 4 до 10 суток (обычно в пределах 4 - 6 суток). В организме АФП частично подвергается биодеструкции сходно с альбумином, частично выводится в неизмененном виде или в виде комплексов с различными метаболитами, например, билирубином, с желчью, слюной, мочой и через кишечник.
Побочных реакций не выявлено. Реакций в месте введения и аллергических реакций не выявлено.
Данные о передозировке отсутствуют.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ:
Гиперчувствительность, беременность, кормление грудью.

Во время деления клеток в нашем организме периодически возникают ошибки. Это неизбежно. Если что-то пошло не так, после деления дочерние клетки имеют неправильное строение, могут становиться раковыми. Иммунная система всегда настороже и готова их уничтожить.
Однако, иммунитет справляется со своей функцией не всегда — в противном случае ни у кого бы не возникали злокачественные опухоли.
Раковые клетки коварны, они могут обзавестись разными видами защиты:
- Если раковая клетка вырабатывает недостаточно много чужеродных веществ, иммунитет её не замечает.
- Некоторые опухоли умеют вырабатывать вещества, которые подавляют работу иммунных клеток.
- Иногда ведущая роль принадлежит микроокружению опухоли — клеткам и молекулам, которые окружают раковые клетки. Микроокружение тоже может подавлять иммунитет.
Для того чтобы иммунная система начала расправляться с опухолью, её нужно активировать, либо предоставить ей необходимые компоненты. Современные врачи и ученые знают, как это сделать. Такое направление лечения рака называется иммунотерапией. Существует несколько её разновидностей.
Какие бывают разновидности иммунотерапии?
На данный момент онкологам доступны разные виды иммунотерапии:
Многие ученые считают, что за иммунотерапией будущее в лечении рака. Исследования в этом направлении продолжаются, в лабораториях разрабатывают и тестируют новые препараты.
Моноклональные антитела
Чужеродные вещества в организме человека называют антигенами. В ответ на их внедрение иммунная система вырабатывает специфические белковые молекулы — антитела. Каждое антитело связывается с соответствующим ему антигеном, после чего происходит ряд событий, приводящий к уничтожению чужеродного агента.
Моноклональные антитела — по сути искусственные заменители собственных антител человека. Каждое из них находит в организме свою молекулу-мишень и связывается с ней. В случае с онкологическими заболеваниями такой мишенью является определенное вещество, которое раковые клетки вырабатывают в достаточно большом количестве, а здоровые — в очень малом, или не вырабатывают вообще.
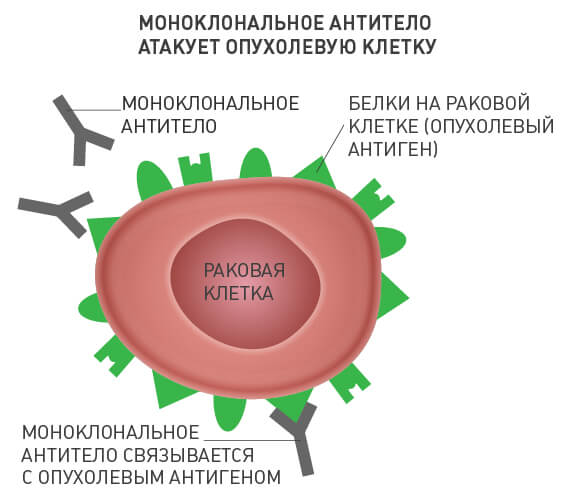
Различные моноклональные антитела действуют по-разному:
Моноклональные антитела можно использовать для доставки к раковым клеткам других лекарств. Например, можно прикрепить к молекуле антитела радиоактивную частицу или химиопрепарат.
За последние годы в мире было одобрено и внедрено в клиническую практику более десятка разных моноклональных антител. Они применяются для лечения ряда злокачественных опухолей, обладающих определенными молекулярно-генетическими характеристиками. В настоящее время ученые работают над созданием новых препаратов, некоторые лекарства проходят испытания и, возможно, вскоре будут введены в клиническую практику.
Кейтруда (Пембролизумаб)
PD-1 – это рецептор, который находится на поверхности T-клеток. Когда он взаимодействует с белком PD-L1, замедляется размножение иммунных клеток, они перестают выделять цитокины и атаковать опухолевую ткань. Кейтруда разрывает эту связь и снимает блок с лимфоцитов:
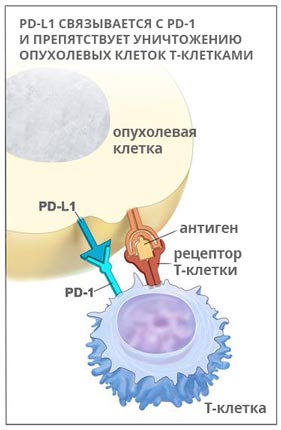
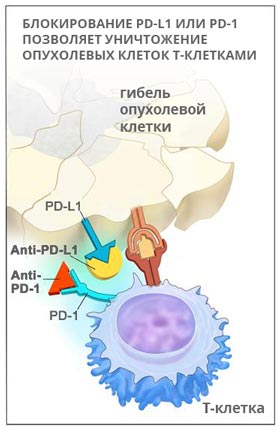
Пембролизумаб был одобрен к применению в Америке в сентябре 2014 года. В настоящее время его используют для лечения меланомы, немелкоклеточного рака легких, опухолей головы и шеи. Кейтруду обычно назначают при некурабельных опухолях, которые невозможно удалить хирургически, если другие методы лечения не помогают.
Ниволумаб (Опдиво)
Ниволумаб, как и Кейтруда, является ингибитором белка-рецептора PD-1. В декабре 2014 года этот препарат был одобрен в Америке для лечения меланомы. В настоящее время основными показаниями к применению Ниволумаба являются: метастатическая и неоперабельная меланома, местнораспространенный или метастатический мелкоклеточный и немелкоклеточный рак легких, почечно-клеточный рак на поздних стадиях. В ряде случаев ниволумаб сочетают с другим ингибитором контрольных точек – ипилимумабом (Ервой).

Ритуксимаб (Мабтера, Ритуксан)
Мишень для ритуксимаба — рецептор CD20, который находится на поверхности B-лимфоцитов. Соединяясь с рецептором, препарат заставляет NK-клетки (натуральные киллеры — разновидность иммунных клеток) атаковать B-лимфоциты, как злокачественные, так и нормальные. После курса лечения организм производит новые нормальные B-лимфоциты, их количество восстанавливается.
Ритуксимаб был одобрен к применению достаточно давно — еще в 1997 году. В настоящее время его используют для лечения аутоиммунных и онкологических заболеваний: хронического лимфолейкоза, вульгарной пузырчатки, неходжкинской лимфомы, идиопатической тромбоцитопенической пурпуры.
Ипилимумаб (Ервой)
Ервой связывается с молекулой CTLA-4 и активирует иммунную систему, для того чтобы она могла бороться с раком. Исследования показывают, что препарат помогает надолго остановить рост опухоли, а в 58% случаев способствует уменьшению её размеров, как минимум, на треть.
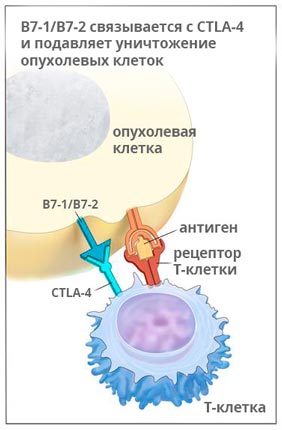
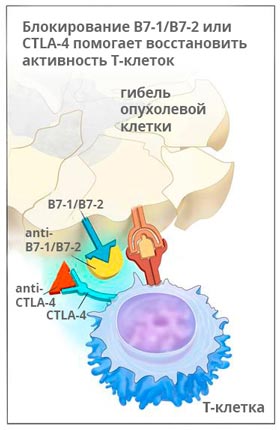
Ипилимумаб применяют у пациентов, страдающих меланомой на поздних стадиях, раком легкого, простаты.
Цитокины
Цитокины – это неспецифические стимуляторы иммунитета. Они активируют иммунную систему не против какого-то определенного антигена, а в целом. В настоящее время в онкологии главным образом применяют два препарата – интерлейкин-2 (ИЛ-2) и интерферон-альфа.
Интерлейкин-2 представляет собой молекулу, которая переносит биохимические сигналы между лейкоцитами. Он ускоряет рост и размножение иммунных клеток. Этот препарат находит применение при распространенном раке почек, метастатической меланоме. Иногда ИЛ-2 сочетают с химиотерапией и другими цитокинами. При этом его действие усиливается, но повышается риск серьезных побочных эффектов.
В настоящее время ведутся исследования по возможности применения в онкологии других типов интерлейкинов, таких как ИЛ-7, ИЛ-12, ИЛ-21.
Интерфероны – вещества, которые принимают участие в борьбе с вирусами и раковыми клетками. Существует три типа интерферона, названных по буквам греческого алфавита – альфа, бета и гамма. Для лечения рака применяют препараты интерферона-альфа. Они помогают усилить противоопухолевый иммунный ответ, непосредственно замедлить рост раковых клеток и кровеносных сосудов, которые обеспечивают опухоль кислородом и питательными веществами.
Интерферон-альфа применяют при раке почек, меланоме, волосатоклеточном лейкозе, некоторых типах лимфомы, саркоме Капоши.
Иммунотерапия при раке легкого
Рак легких — одно из самых распространенных онкологических заболеваний. По заболеваемости и уровню смертности он занимает первое место у мужчин и третье место у женщин. Почти 20% пациентов, умерших от злокачественных опухолей, погибли от рака легкого. В группе повышенного риска находятся курильщики в возрасте старше 50 лет. На каждые 3–4 миллиона выкуренных сигарет приходится одна смерть от рака легких.
Заболевание часто диагностируют на поздних стадиях, когда многие виды лечения оказываются неэффективны. В таких случаях пользу может принести иммунотерапия.
При раке легкого применяют такие препараты, как ниволумаб (Опдиво), ипилимумаб (Ервой), пембролизумаб (Кейтруда), атезолизумаб (Тецентрик).
В Европейской клинике применяются наиболее современные методы лечения рака легкого, меланомы и других онкологических заболеваний. Благодаря сотрудничеству с зарубежными коллегами, мы может предоставить пациентам возможность пройти курс иммунотерапии, персонализированного лечения в нашем центре иммунотерапии. Мы знаем, как продлить жизнь и избавить от мучительных симптомов при запущенном раке. Мы знаем, как помочь.
Иммунотерапия при меланоме
Меланома — далеко не самая распространенная (всего 2%) форма рака кожи, но она очень агрессивна и чаще других опухолей приводит к смерти. Так, в 2012 году в мире было диагностировано 232 000 новых случаев меланомы, 55 000 больных погибли. Меланома рано метастазирует, после чего многие методы лечения становятся неэффективны.
На поздних стадиях для лечения меланомы применяют пембролизумаб (Кейтруда), ипилимумаб (Ервой), ниволумаб (Опдиво).
Отзыв пациента о лечении меланомы иммунотерапией:
Мне 41, я бывший спортсмен-байдарочник, волосы черные, глаза карие — то есть, я нормально переношу загар, кожа смуглеет быстро, а ожогов у меня не бывает. Я, конечно, слышал, что длительное пребывание на солнце чревато всякими проблемами, а так как основную часть времени я проводил как раз на солнце, регулярно проверялся у дерматолога. От него и узнал, что есть такая беда, как меланома — рак кожи. Но, по его словам, мне она не грозит, как раз ввиду особенностей моей кожи.
Ну, и, конечно, у меня нашли меланому. Причем, что обидно, не на спине или плечах, что было бы логично — эти места постоянно под лучами, а на бедре.
В первую очередь, по совету дерматолога, отправился в одну небезызвестную клинику. Приняли охотно, сказали, что вероятность хорошего исхода большая, так как обнаружена она достаточно рано.
Но, этот выигрыш они благополучно спустили на недельные обследования. По результатам мне назначили операцию ещё через неделю, а потом Интерферон. Я обратился к тому же дерматологу, который послушал меня, и несколько удивился. Ничего толком не сказал, но намекнул на то, что можно бы получить и второе мнение, да побыстрее.
Иммунотерапия при раке желудка
При раке желудка I–III стадии основным методом лечения является хирургическое удаление опухоли, нередко его дополняют курсом химиотерапии и лучевой терапии. На IV стадии, когда опухоль распространяется за пределы органа и дает метастазы, шансы на полную ремиссию стремятся к нулю. В таких случаях проводят лечение, направленное на замедление роста опухоли, сокращение её размеров, продление жизни пациента.
Именно на IV стадии, когда рак желудка не реагирует на другие виды лечения, может принести пользу иммунотерапия. Эффективны такие препараты, как трастузумаб и рамуцирумаб. В настоящее время исследования в отношении иммунотерапии при раке желудка ведутся в четырех основных направлениях: ингибиторы контрольных точек, таргетная иммунотерапия моноклональными антителами, противораковые вакцины и клеточная иммунотерапия.
Иммунотерапия при раке почки
При лечении рака почек иммунотерапией применяет две группы иммунопрепаратов:
- Цитокины — белки, которые активируют иммунную систему и заставляют её бороться с раком. Для лечения применяют искусственно синтезированные аналоги этих белков: интерлейкин-2 (IL-2) и интерферон-альфа.
- Ингибиторы контрольных точек. Контрольные точки — это особые молекулы иммунной системы, которые она использует, чтобы сдерживать себя от атаки здоровых клеток. Иногда они мешают бороться против опухолевых клеток. При раке почек применяют Ниволумаб (Опдиво) — он блокирует PD-1, белок, который находится на поверхности T-лимфоцитов.
Иммунотерапия при раке яичников
В последние годы хирургическое лечение и химиотерапия при раке яичников значительно продвинулись вперед, и все же ситуация пока еще далека от идеальной. У многих женщин опухоль рецидивирует, перестает реагировать на препараты, которые помогали ранее. Из иммунопрепаратов при раке яичников в настоящее время применяется Бевацизумаб (Авастин) — представитель группы моноклональных антител, который блокирует фактор роста эндотелия сосудов. Раковые клетки синтезируют это вещество в большом количестве, чтобы стимулировать рост новых сосудов, обеспечить себя кислородом и питательными веществами. Некоторые методы иммунотерапии при раке яичников в настоящее время находятся на стадии разработки и тестирования: моноклональные антитела, ингибиторы контрольных точек, иммуномодуляторы, противораковые вакцины, иммуноклеточная терапия, онколитические вирусы.
Побочные эффекты иммунотерапии
Лечение иммунотерапевтическими препаратами имеет некоторые общие моменты с химиотерапией. Такое сходство заключается в том, что клетки опухоли погибают в пределах органов и тканей тела, и организму приходится избавляться от них, как от чужеродного вредоносного материала. Это очень ресурсоёмкая задача, поэтому пациент может испытывать симптомы, вызванные перенапряжением различных систем организма.
Иногда иммунотерапия активирует иммунные клетки чрезмерно, и они начинают атаковать нормальные ткани организма. Из-за этого могут возникать некоторые побочные эффекты:
- При поражении слизистой оболочки полости рта и глотки на ней возникают болезненные язвы, которые могут инфицироваться. Обычно они проходят в течение 5–14 дней после окончания лечения.
- Кожные реакции: покраснение, отечность, сухость, повышение чувствительности к свету, трещины на кончиках пальцев.
- Симптомы, напоминающие грипп: слабость, разбитость, повышенная температура, озноб, кашель.
- Тошнота и рвота.
- Головные боли, головокружения.
- Повышение или снижение артериального давления.
- Мышечные боли.
- Одышка.
- Отеки на ногах.
- Увеличение веса из-за задержки жидкости в организме.
- Диарея.
У разных иммунопрепаратов побочные эффекты выражены по-разному. Лучше заранее поговорить с врачом и спросить, каких проблем можно ожидать во время курса лечения, как с ними бороться.
Иммунотерапия: за и против
Однако, не всё так гладко. У иммунопрепаратов есть и минусы. Они работают далеко не у всех пациентов. Иногда опухоль удается уничтожить полностью, а иногда — лишь замедлить её рост. Ученые пока не могут объяснить, почему результаты лечения бывают такими разными. Несмотря на то, что побочные эффекты встречаются не так часто, как при химиотерапии, иногда они могут быть весьма серьезными.
Иммунотерапия — это всегда длительное лечение. Со временем иммунопрепарат, который помогал пациенту ранее, может перестать работать. К минусам можно отнести и достаточно высокую стоимость иммунотерапии при раке. Таким образом, в каждом случае решение нужно принимать индивидуально. Прежде чем назначить иммунотерапию, врач обязательно взвесит все возможные преимущества и риски.
Ещё один минус иммунотерапии — она подходит не для всех типов рака. Существует не так много онкологических диагнозов, для которых разработан препарат, способный точно и эффективно воздействовать на клетки данного рака. Однако это путь, по которому онкология продолжает идти, открывая всё новые и новые препараты и их комбинации, способные воздействовать на новые виды опухоли. Всё остальное — это исключительно преимущества, которые могут отменить остальные виды лечения уже в обозримом будущем.
Сколько стоит иммунотерапия?
Иммунотерапия — это самый современный медикаментозный метод лечения рака. Стоимость иммунотерапии рака немаленькая. Особенно в сравнении с другими известными методами. Стоимость лечения зависит от вида применяемого иммунопрепарата, типа и стадии опухоли, ее степени агрессивности. Высокая цена иммунотерапии связана с тем, что производство иммунопрепаратов — сложный и дорогой процесс.
В России очень немного клиник, которые проводят лечение иммунотерапией. В большинстве случаев, чтобы пройти курс иммунотерапии, россиянину приходится обращаться к посредникам для лечения за границей. В основном это Израиль, Германия и США. В таком случае стоимость перелёта и лечения составит огромную сумму. Но теперь в России есть возможность пройти иммунотерапевтическое лечение рака в Европейской клинике, что делает его доступным для многих пациентов.
Показания к применению препарата Интерферон-Альфа
- инфекционные вирусные заболевания: гепатит В, С, D, скрытые половые инфекции, вирус герпеса, энцефалит;
- онкологические заболевания: лейкозы различных типов, рак яичников, мочевого пузыря, почки, меланома;
- рассеянный склероз.
Способ применения
Противопоказания к применению препарата Интерферон-Альфа
Побочные эффекты от применения препарата Интерферон-Альфа
- на озноб, головную и суставную боль, миалгии, напоминающие проявления гриппа;
- диспепсические расстройства: тошноту, рвоту, диарею или запоры, изменение вкусовых ощущений, появление стоматита;
- головокружение, изменение показаний АД, аритмию.
Популярные зарубежные онкологические клиники и центры

Центр радиохирургии в Крефельде обладает высоким авторитетом не только в Германии, но и во всем остальном медицинском мире. Центр является поистине уникальным радиохирургическим лечебным учреждением, так как сертификации качества подвергается весь процесс терапии онкологических заболеваний. Перейти на страницу >>

В немецкой Клинике онкологии, гематологии и клинической иммунологии при Униклинике Дюссельдорфа успешно осуществляют все виды лечения онкологических заболеваний крови, в том числе и с выполнением пересадки стволовых клеток. Клиника практикует методы генной инженерии, использует радиоиммунную терапию. Перейти на страницу >>

Лечение онкологических заболеваний является одним из приоритетных направлений деятельности клиники Хеундэ Пэк в Южной Корее. Медицинское учреждение имеет в своем распоряжении современное оборудование и технику для проведения ранней и высокоточной диагностики рака и его последующей терапии. Перейти на страницу >>

Британская Клиника Лондон Бридж Хоспитал считает диагностику и лечение злокачественных опухолей одним из приоритетных направлений в своей деятельности. Специалисты клиники эффективно лечат рак любой локализации и сложности. Штат сотрудников состоит из врачей, имеющих большой опыт и высокую квалификацию. Перейти на страницу >>

Центральный Венский Клинический Госпиталь в Австрии имеет в своем подразделении Онкологическое отделение, успешно занимающееся лечением многих онкологических заболеваний. В распоряжении отделения имеется самое современное оборудование и техника, штат укомплектован опытными врачами-онкологами. Перейти на страницу >>
Каким должно быть питание при онкологических заболеваниях? Какие продукты абсолютно противопоказаны при той или иной форме рака?
Фитотерапия способна оказать существенную помощь не только в лечении онкологических заболеваний, но также и в их профилактике.
Многих людей, имеющих у себя или у родственников онкологическое заболевание, интересует вопрос: передается ли рак по наследству?
Лечение рака во время беременности является довольно сложным, ведь большинство лекарственных средств обладает токсичностью.
Какие перспективы у беременности после перенесенного онкологического заболевания? Следует ли выдерживать срок после лечения рака?
Профилактика является важной частью общей борьбы с онкологическими заболеваниями. Как же уменьшить вероятность возникновения рака?
Что представляет из себя паллиативное лечение рака? Как оно может повлиять на качество жизни онкологического больного и изменить ее к лучшему?
Учеными разработано достаточно много перспективных методов лечения рака, пока еще не признанных официальной медициной. Но все может измениться!
Как найти силы для борьбы с раком? Как не впасть в отчаяние от возможной инвалидности? Что может послужить надеждой и смыслом жизни?
Бытует такое мнение, что постоянные стрессовые ситуации способны привести к развитию онкологических заболеваний. Так ли это?
Многие онкологические больные часто страдают от резкой потери веса. Чем это вызвано и можно ли как-то справиться с этой проблемой?
Правила ухода за больными, вынужденными постоянно находиться в кровати, имеют свои особенности и их нужно обязательно знать.
Ингибиторы фактора некроза опухоли альфа (TNF-альфа) являются одним из видов терапии, которые подавляют часть иммунного ответа при саркоидозе и способны помочь справиться с симптомами заболевания.

Ингибиторы TNF-альфа
В обычном понимании ингибиторы считаются иммунодепрессантами. TNF-альфа является типом иммунного белка, который секретируется моноцитами и макрофагами. TNF-альфа регулирует различные биологические процессы, в том числе – развитие воспалительной реакции, что обычно используется в качестве защиты организма от инфекции или в ответ на различные повреждения.
При саркоидозе вырабатывается слишком много TNF-альфа, что приводит к хроническому отеку и воспалению в организме с повреждением здоровых тканей.
Ингибиторы фактора некроза опухоли блокируют действие данного белка за счет конкурентного связывания с его рецепторами, предупреждая дальнейшее развитие воспалительной реакции.
Существует несколько видов ингибиторов TNF-альфа (голимумаб, этанерцепт, цертолизумаб), которые одобрены для лечения различных патологических состояний, таких как воспалительное заболевание кишечника (НЯК – язвенный колит) или ревматоидный артрит. Подавляющее большинство из этих препаратов не используются в терапии саркоидоза.
В лечении саркоидоза из ингибиторов TNF-альфа разрешены лишь адалимумаб (Хумира) и инфликсимаб (Ремикад). Обычно они назначаются при резистентности (невосприимчивости) заболевания к другим видам терапии, где используется пентоксифиллин или кортикостероиды. В некоторых случаях иммунодепрессанты используются вместо преднизолона для снижения побочных явлений гормональной терапии.
Ингибиторы TNF-альфа в испытаниях
Было проведено несколько клинических испытаний, подтверждающих безопасность и эффективность ингибиторов TNF-альфа при саркоидозе.

Например, в исследовательской работе были изучены эффекты Ремикарда по сравнению с плацебо у 138 пациентов с саркоидозом легких. Результаты были опубликованы в Американском журнале респираторной медицины в далеком 2006 году. Отмечался значительный положительный эффект со снижением или исчезновением легочных симптомов заболевания.
Улучшение состояния было более выраженным у пациентов с высоким уровнем С-реактивного белка (СРБ) в крови (маркер воспалительной реакции).
Дополнительная информация
Поскольку ингибиторы TNF-альфа влияют на иммунную систему, у пациентов, использующих эти препараты, наблюдается значительное повышение риска развития инфекций, в том числе тяжелых.
Ингибиторы TNF-альфа вводятся преимущественно подкожно в область бедра или живота однократно в неделю. В некоторых случаях может быть использовано внутривенное введение препарата. Опираясь на способы получения лекарства, побочными эффектами могут служить воспалительные изменения в месте инъекций.
Среди других побочных явлений следует выделить тошноту, изжогу, головные боли, насморк, появление белых пятен во рту и зуд влагалища (за счет развития грибковой инфекции на фоне снижения иммунитета).
Альтернативным лекарственным препаратом, который также считается иммунодепрессантом является и Тофацитиниб.

Преднизолон и саркоидоз

Метотрексат при саркоидозе

Противомалярийные препараты в лечении саркоидоза
Читайте также:

