Осложнения при лечении миеломы
Описание
Симптомы
Для болезни характерно бессимптомное начало. На ранней стадии единственным признаком изменений в организме является увеличение скорости оседания эритроцитов (СОЭ). Дальнейшее развитие патологического процесса проводит к проявлению неспецифических симптомов миеломы:
- слабости;
- быстрой утомляемости;
- снижения физической активности;
- шаткости походки;
- снижения аппетита;
- тошноты;
- рвоты.
- Основной симптом множественной миеломы — наличие болевых ощущений. В большинстве случаев боль локализуется в дорсальном и поясничном отделах позвоночника. В начальной стадии неприятные ощущения беспокоят пациентов во время движения. Как правило, боли проявляют тенденцию к нарастанию и с трудом поддаются обезболиванию при использовании даже сильнодействующих анальгетиков. Локализация боли постоянного характера в конкретных участках может указывать на переломы.
- Дальнейшее прогрессирование болезни приводит к развитию костномозгового синдрома. Размножение злокачественных клеток в костном мозге становится причиной разрушения костей. В основном поражаются:
- черепные кости;
- ребра;
- тазовые кости;
- трубчатые кости (бедер, плеч).
- Разрушение костей приводит к оседанию тел позвонков и уменьшению роста человека на несколько сантиметров. Появляются симптомы сдавливания спинного мозга.
- Следствием эрозии костей становится также повышение уровня кальция в крови. Результатом является:
- увеличение количества выделяемой мочи и вследствие этого обезвоживание организма;
- тошнота, нередко сопровождаемая рвотой;
- сонливость;
- плохая ориентация в пространстве.
- Нарушение процесса созревания красных кровяных клеток приводит к проявлению следующих симптомов:
- слабости и повышенной утомляемости;
- бледности кожных покровов;
- головной боли;
- одышки.
- Дефицит тромбоцитов — еще один характерный симптом миеломы. Его следствием является повышенная кровоточивость. Наблюдаются:
- носовые кровотечения;
- кровоточивость десен;
- у женщин — обильные менструальные кровотечения.
- Возможно проявление симптоматики со стороны нервной системы:
- жгучая боль в верхних и нижних конечностях;
- снижение чувствительности рук и ног, в дальнейшем — ее потеря;
- паралич;
- потеря чувствительности нижней половины тела;
- недержание мочи.
- Синдром белковой патологии обусловлен выделением М-компонента опухолевыми клетками. Данный компонент представляет собой разновидность иммуноглобулинов, которые в норме должны отсутствовать. Данный процесс нередко приводит к поражению почек в результате скопления в них кальция и М-компонента. При этом проявляются следующие симптомы:
- частые ложные позывы к мочеиспусканию в основном в ночное время;
- сокращение количества выделяемой мочи днем.
Скопление синтезируемого опухолью белка в тканях различных внутренних органов становится причиной нарушения их нормального функционирования. Проявляются:
- перебои в работе сердца, сердцебиение;
- увеличение размеров языка, нарушение его подвижности;
- сокращение подвижности суставов;
- ощущение боли и дискомфорта — может возникать практически во всех частях тела и связано с повреждением нервных волокон.
- Синдром недостаточности антител является следствием нарушения нормального процесса кроветворения. При этом нередко наблюдается обострение инфекционных заболеваний. Проявляются следующие симптомы миеломы:
Со стороны дыхательной системы:
- заложенность носа;
- насморк;
- осиплость.
Со стороны мочеполовой системы:
- · ощущение жжения, рези во время мочеиспускания;
- · помутнение выделяемой мочи.
- Миеломная болезнь нередко распространяется на внутренние органы (печень, сердце, селезенку, суставы) и приводит к их поражению. В результате распространения опухолевого процесса могут возникать следующие симптомы:
- при поражении печени — болевые ощущения и тяжесть в правом подреберье;
- при поражении селезенки — локализация боли и неприятных ощущений слева;
- поражение сердца сопровождается болями ноющего характера в загрудинной области;
- если в патологический процесс оказываются вовлеченными суставы, болевой синдром локализуется в них.
Причины
Развитие миеломной болезни связано в первую очередь с неконтролируемым процессом роста плазматических клеток, продуцируемых костным мозгом. Следствием повышения уровня их содержания является скопление в костном мозге в виде плазмацитомы (преимущественно в позвоночнике, плоских костях черепа, костях таза, головках тазобедренных суставов). Результатом становится разрушение нормальной костной ткани и костного мозга.
На сегодняшний день пока не удалось выявить точные причины развития множественной миеломы. Однако на основе данных медицинской статистики можно выделить некоторые факторы, наличие которых повышает вероятность возникновения данной патологии:
- Возрастной фактор — болезнь диагностируется в основном у лиц старше 40 лет.
- Генетическая предрасположенность.
- Патологические нарушения структуры ДНК.
- Расовая принадлежность — миелома намного чаще поражает афроамериканцев.
- Воздействие неблагоприятных физических факторов:
- · рентгеновского облучения (в случае нарушения техники безопасности при работе на АЭС или в результате проведения рентгенотерапии);
- · ионизирующей радиации.
- Воздействие химических веществ:
- лекарственных препаратов — например, при длительной антибиотикотерапии или терапии солями золота;
- производственных химикатов: красок, лаков, продуктов нефтедобывающей промышленности и т.д.
- Биологические агенты:
- кишечные инфекции;
- вирусы;
- туберкулез.
- Проведенное ранее хирургическое вмешательство.
- Нервное напряжение, частые стрессы.
Диагностика

С целью диагностики множественной миеломы проводят следующие исследования и анализы:
Последние два метода диагностики миеломы являются более информативными для определения степени распространенности патологического процесса и дифференцирования миеломной болезни с другими патологиями костной ткани.
Дифференциальная диагностика проводится с остеомиелитом, лимфоплазмоцитарной лимфомой, костными метастазами других злокачественных новообразований.
- Остеомиелит поражает метафизарную часть трубчатой кости. Обнаруживаются явные признаки воспалительного процесса, анализ крови также обнаруживает воспалительную реакцию. При пункционной биопсии получается гнойное содержимое.
- Метастазирование в костную ткань характерно для таких заболеваний, как:
- · нейробластома;
- · лимфогранулематоз;
- · гемангиома;
- · злокачественная опухоль груди.
При их наличии во всех случаях есть первичный опухолевый очаг. Связь метастаза с опухолью подтверждается в результате гистологического исследования.
Симптомами лимфоплазмацитарной лимфомы являются:
- · изменения лимфоузлов патологического характера;
- · лейкемизация;
- · увеличенная селезенка;
- · поражение костного мозга;
- · наличие патологического парапротеина;
- · поражение легких.
Лечение
Выжидательная тактика считается оправданной только в случае вялотекущей (индолентной) формы миеломы, когда отсутствуют ее симптомы. Таким пациентам показано динамическое наблюдение. К лечению переходят в случае прогрессирования патологического процесса.
Основным методом лечения миеломы остается химиотерапия.
Моно- и полихимиотерпия проводится с применением следующих препаратов:
- Мелфалан — его начали применять еще в годах 20 века. В настоящее время используется как в монохимиотерапии, так и в полихимиотерапии. Ответ наблюдается примерно с половине случаев.
- Циклофосфан — используют в монотерапии или в сочетании с преднизолоном. В последнее время ученые получили положительные результаты после использования комбинаций препарата с новейшими средствами: леналидомидом и бортезомибом, а также со стероидными средствами.
- Бортезомиб. Основой механизма его действия является индукция апоптоза — регулируемого процесса программируемой клеточной гибели. Наступление ответа наблюдается в 43% случаев у больных с рецидивирующей формой миеломы. Применяется в монохимиотерапии и в сочетании с другими средствами: велкейд, дексаметазон для рецидивов болезни (VD); велкейд, мелфалан, преднизолон (VMP) — используется для лечения миеломы в первой линии терапии; велкейд, адриабластин, дексаметазон (PAD) и т.д. Использование препарата не исключает пересадку стволовых клеток.
- Леналидомид. При миеломной болезни оказывает двойной эффект: способствует активизации иммунных клеток самого организма, благодаря чему удается уничтожить опухолевые клетки, и подавляет образование новых кровеносных сосудов опухоли (его ангиогенез). Хороший результат можно получить при условии раннего использования. Оказывается эффективным в 60% случаев. Для лечения миеломы применяется в сочетании с дексаметазоном (является стероидным гормоном) и циклофосфаном (анкилирующими агентами). Монотерапия применяется при миеломной болезни NCCN для поддерживающей терапии .
Помимо химиотерапии, при лечении множественной миеломы применяют вспомогательные методы:
Осложнения и последствия
Миеломная болезнь с характерным для нее неконтролируемым ростом плазматических клеток может спровоцировать ряд тяжелых последствий:
- Основательное разрушение костной ткани, дробление костей. Возможна значительная компрессия спинного мозга, приводящая к слабости конечностей или их параличу.
- Серьезное нарушение процесса кроветворения в костном мозге.
- Нарушение кровообращения, риск тромбообразования и другие последствия увеличения вязкости крови вследствие значительного количества парапротеинов.
- Существенное подавление иммунитета по причине снижения синтеза нормальных иммуноглобулинов. Миелома тормозит производство антител, необходимых для нормальной иммунной защиты. В результате подавления иммунитета повышается риск развития инфекционных заболеваний: пневмонии, инфекций мочеполовой системы и т.д.
- Почечная недостаточность в результате изменений в почечных канальцах и клубочках. Эрозия костной ткани приводит к повышению уровня кальция, что оказывает негативное влияние на процесс фильтрации крови в почках. Отрицательное воздействие оказывают также производимые опухолевыми клетками протеины.
- Острые формы лейкоза — являются следствием продолжительного применения цитостатических средств или самой болезни.
- Развитие сепсиса.
- Инсульт.
- Инфаркт миокарда.
Профилактика
Говорить о профилактике миеломной болезни достаточно сложно ввиду невыявленности причин ее развития.
Выживаемость больных с множественной миеломой варьирует от случая к случаю, причем некоторые из них имеют очень скоротечную эволюцию (несколько месяцев), в то время как другие — 10—12 лет. Этим подразумевается выживаемость с момента постановки диагноза, так как доказано, что миелома имеет очень длительную эволюцию до клинической фазы, но которую до сих пор было невозможно обнаружить.
Среднее выживание больных с множественной миеломой, нелеченных или леченных уретаном длится приблизительно 7 месяцев (Osgood, Holland). Новые терапевтические средства привели к значительному увеличению жизненного срока. Большие статистики показывают выживаемость в 18—21 месяцев (Alexaninan и сотр., Medical Research Council, Bergsagel, George и сотр.). В статистике Бухарестского Института Внутренней Медицины, средняя выживаемость равняется 20 месяцам (Вегсеапг. и сотр.).
Делались попытки установить связь между секретируемой формой Ig и выживаемостью. Повидимому при миеломе IgD наблюдается более низкая средняя выживаемость — 60% больных умирают в течение первого года болезни (Jancelewicz). Протеинурия Бене-Джонса типа ламбда оказывает отрицательное влияние на эволюцию (Acute leukaemia Group В), факт, оспариваемый однако Witts и сотр..
Эффективным показателем эволюции является уровень мочевины в крови до лечения; так, больные, которые подвергаются первому курсу лечения, имея мочевину ниже 40 мг/100 мл сыворотки выживают в среднем 33 месяцев, в то время как пациенты, у которых в момент начала первого курса лечения, уровень мочевины в сыворотке превышает 80 мг/ 100 мл, выживают в среднем лишь 2 месяца (Medical Research Council).
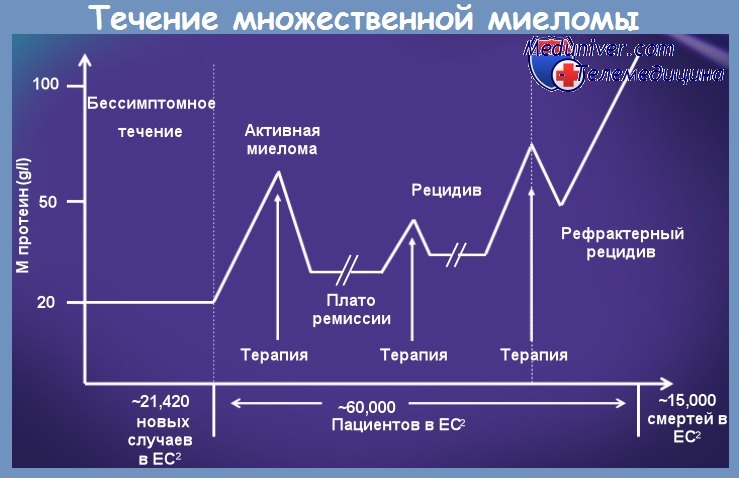
Эволюция множественной миеломы характеризуется периодами обострения и ремиссий. Вместе с развитием болезни во времени, боли усиливаются, приковывая больного к постели; к этому могут ассоциироваться параплегии вследствие позвоночных провалов. В конечной фазе наступает кахексия с суровой анемией и почечной недостаточностью.
До настоящего времени прогноз множественной миеломы остается неблагоприятным, а единственно известные излечения относятся к единичной плазмоцитоме, оперированной в начальной стадии.
Почечные осложнения множественной миеломы бывают чрезвычайно часто в течение множественной миеломы: они встречаются в 40% случаев. Их тяжесть варьирует от простых протеинурий до почечной недостаточности и уремической комы. Азотемия при множественной миеломе не сопровождается артериальной гипертензией.
У больных с миеломой цитируются случаи острой почечной недостаточности, вызванной обычно производством урографии (Myers и Witten). Главным разрешающим фактором является дегидратация, которая связана с урологическим исследованием.
На уровне мочевых путей часто происходят отложения кальция, которым способствует гиперкальцемия, гиперкальциурия, протеинурия, а также и изменение мочевого рН благодаря инфекциям.
Неврологические осложнения множественной миеломы происходят часто и бывают разнообразными. На первом плане стоят осложнения по поводу компрессий (10—30% случаев, согласно Silverstein и Doniger). Они вызваны позвоночными переломами и провалами, которые влекут за собой парезы и параличи. Их число повидимому возросло за последние годы, вероятно вследствие продления эволюции болезни в результате соответствующих лечений.
Туморальные инфильтраты, амилоидные или протеиновые, на уровне нервных корешков или же по протяжению периферических нервов могут порождать явления радикулитов или невритов и являются иногда первыми признаками болезни. Более редким неврологическим осложнением (6% случаев, согласно Cohen и Bundles) является периферическая невропатия, несвязанная с костными повреждениями или туморальными инфильтратами. Она может появляться и в случаях единичной плазмоцитомы и исчезает в результате местного лечения болезни.
Мочевым инфекциям, которые возникают также часто, благоприятствует наличие камней в почках и почечной недостаточности.
Миелома — зло злокачественная опухоль, которая происходит из клеток лимфоидной ткани, а если быть точным — из плазматических клеток. Для нее характерны следующие признаки:
- Инфильтрация костного мозга злокачественным клоном плазматических клеток. В норме в костном мозге располагается около 5 % плазмоцитов, но при миеломе их количество превышает 10%.
- В костях возникают очаги деструкции — из-за токсического действия опухолевых клеток происходит расплавление костной ткани. Это могут быть единичные очаги, либо диффузное поражение.
- В крови и моче обнаруживается специфический белок. У него много названий — М-белок, М-градиент, М-протеин, М-компонент и др. Это моноклональный иммуноглобулин, который имеет высокую молекулярную массу и негативно влияет на весь организм.
Причины миеломной болезни
Причиной миеломы является злокачественное перерождение клеток-предшественниц В-лимфоцитов, при этом образуются специфические мутации. Причины образования данных мутаций пока неизвестны. Пока речь идет только о факторах риска, при наличии которых вероятность развития заболевания увеличивается:
- Мужской пол.
- Возраст старше 40 лет.
- Негроидная раса.
- Наличие в анамнезе моноклональной гаммапатии. У 1% таких пациентов обязательно развивается миелома.
- Наличие вторичных иммунодефицитных состояний. К вторичным иммунодефицитам приводит иммуносупрессивная терапия, показанная при трансплантации органов, химиотерапия при злокачественных заболеваниях, ВИЧ и др.
- Наличие миеломы у кровных родственников.
- Наличие в анамнезе радиационного воздействия, в том числе прохождение лучевой терапии.
Виды миеломы
Миелома представляет разнородную группу заболеваний, часть из которых могут долгое время протекать относительно доброкачественно, а другие приводят к быстрому ухудшению состояния больного.
- Симптоматическая миелома. В данном случае имеется развернутая клиническая картина заболевания, с наличием характерных симптомов и признаков, полученных с помощью инструментального обследования.
- Вялотекущая, или тлеющая миелома. При ней нет повреждения костей, но в плазме крови обнаруживается М-протеин в концентрациях, превышающих 30г/л, или в костном мозге количество плазматических клеток превышает 10%.
- Плазмоцитома. Имеется единичный очаг миеломы в костях (солитарная плазмоцитома), либо во внутренних органах — экстрамедуллярная плазмоцитома.
Есть также редкие варианты множественной миеломы:
- Несекретирующая миелома.
- Биклональная миелома.
- Плазмоклеточный лейкоз и др.
Стадии болезни
1 стадия. Имеется анемия легкой степени (гемоглобин не менее 100г/л), кальций остается в норме, количество очагов остеодеструкции не превышает 5, уровень М-протеина низкий.

2 стадия. Анемия усугубляется, гемоглобин может опуститься до 85г/л, повышается уровень кальция до 3 ммоль/л, увеличивается количество очагов расплавления кости (их уже более 5, но менее 20), повышается уровень М-белка, а в моче определяется протеин Бенс-Джонса в количестве 4-12 г/сутки.
3 стадия выставляется, когда есть хотя бы один из следующих признаков:
- Тяжелая анемия, при которой гемоглобин не превышает 85 г/л.
- Уровень кальция в сыворотке крови превышает 3 ммоль/л.
- Уровень М-протеина более 70 г/л.
- Более 30 остеолитических очагов.
Проявления и осложнения миеломы
Проявление заболевания зависит от его стадии. В некоторых случаях оно может никак не проявлять себя, но по мере нарастания опухолевой массы, заболевание будет прогрессировать. При миеломе возникают следующие симптомы:
Рецидивируют ли миеломы
К сожалению, на сегодняшний день миелома является неизлечимым заболеванием. Даже после самого мощного лечения — тандемной высокодозной полихимиотерапии с трансплантацией стволовых клеток все равно развивается рецидив. Задача лечения отсрочить его развитие и затормозить прогрессирование заболевания.
Диагностика миеломы
- Лабораторные анализы:
- Общий анализ крови — определение уровня гемоглобина, подсчет лейкоцитарной формулы. Характерным, но не ключевым признаком миеломы является значительное увеличение СОЭ, у 70% больных оно превышает 30 мм/час, у отдельных пациентов — 100мм/час.
- Анализ мочи — определение уровня общего белка и М-протеина в частности.
- Биопсия костного мозга. Проводится подсчет миелограммы с определением процентного количества плазматических клеток, а также молекулярно-генетические тесты, которые позволяют выявить характерные для миеломы мутации.
- Иммунофенотипирование — позволяет выявить клон опухолевых клеток в пунктате костного мозга.
- Рентгенологические методы исследования, в частности рентген костей или компьютерная томография костей. Эти исследования позволяют выявить очаги остеодеструкции и определить их количество.
- МРТ проводится при наличии неврологической симптоматики для оценки поражения корешков спинномозговых нервов опухолевой массой или разрушенным позвонком. Также МРТ является обязательным исследованием при подозрении на солитарную миелому костей.
Лечение
На сегодняшний день лекарств, которые могли бы полностью излечить миелому, нет. Основные усилия направлены на достижение ремиссии и ее пролонгирование. Схема лечения миеломы будет определяться возрастом пациента и его состоянием. Используется несколько подходов к терапии:
- Стандартная химиотерапия с использованием мелфалана, преднизолона и бортезомиба. Такое лечение миеломы показано ослабленным пациентам и людям старше 65 лет, которые не смогут перенести более серьезное лечение. Для пациентов с тяжелой почечной недостаточностью проводят лечение с использованием бортезомиба и дексаметазона. В ряде случаев дексаметазон можно заменить на преднизолон, чтобы снизить токсическое действие. Также используются схемы лечения, включающие талидомид.
- Высокодозная полихимиотерапия. Наилучшие результаты достигаются при применении высокодозной полихимиотерапии (ВПХ) с последующей трансплантацией гемопоэтических стволовых клеток (ТГСК). Такое лечение показано пациентам младше 65 лет, а также пациентам 65- 70 лет при удовлетворительном состоянии и отсутствии противопоказаний. Возрастные ограничения обусловлены высокими рисками трансплантат-ассоциированной летальности, которая в данном случае может достигать 8%. Почечная недостаточность, даже в терминальной стадии, не является противопоказанием к ВПХ с аутотрансплантацией стволовых клеток при наличии в центре возможностей для проведения гемодиализа.
Схема лечения ВПХТ включает несколько этапов:
1 этап индукционный. На этапе индукции ремиссии рекомендуется применять трехкомпонентные схемы, не включающие мелфарман. Обычно это схемы PAD и VCD, но может использоваться и VD. При достижении полной ремиссии или очень хорошей ремиссии, пациенты направляются в трансплантационный центр для проведения ТГСК. Если опухоль оказалась резистентной, назначают терапию второй линии. Если и после нее нет хорошего эффекта, рассматривают вариант высокодозной полихимиотерапии.

2 этап лечения — трансплантационный. Он, в свою очередь, состоит из нескольких этапов:
- Мобилизация гемопоэтических стволовых клеток (ГСК). На этом этапе необходимо собрать, выделить и заготовить достаточное количество CD 34+. Обычно их выделяют из крови (периферические ГСК), но при необходимости допускается забор из костного мозга. Для мобилизации СК применяется химиотерапия циклофосфаном + гранулоцитарный колониестимулирующий фактор (он провоцирует пролиферацию стволовых клеток). Если не удалось собрать достаточное количество СК, или при проведении повторной мобилизации, вместо циклофосфана используют плериксафор.
- Предтрансплантационное кондиционирование. Этот этап должен начинаться не позже 6 недель после забора ГСК. Его целью является улучшение качества противоопухолевого ответа, которого добились на индукционном этапе. Кондиционирование проводится с использованием высоких доз мелфалана.
- После этого проводится ТГСК, которая для пациента выглядит, как обычное переливание крови.
- При миеломе лечение может включать две ТГСК. Такой режим называется тандемная ТГСК. При этом, повторная трансплантация планируется в период 3-6 месяцев после первой (оптимальные сроки — 3 месяца). Особенно она актуальна для пациентов, не достигших полной ремиссии. Помимо трансплантации собственных СК, по показаниям могут применяться СК донора.
Поддерживающая терапия назначается как после ТГСК, так и после стандартной ХТ. Ее целью является уничтожение остаточного клона миеломных клеток. Используется леналидомид или бортезомиб.
Хирургическое лечение используется в качестве паллиативных вмешательств при патологических переломах, компрессии спинного мозга или корешков спинногмозговых нервов . С этой целью проводятся различные реконструктивные операции, призванные устранить компрессию и зафиксировать костные отломки в нужном положении. Также могут быть проведены профилактические операции, при которых кости укрепляют с помощью металлических конструкций, не дожидаясь их переломов.
В ряде случаев при солитарной плазмоцитоме операция может применяться как самостоятельное лечение.
Как узнать, что лечение работает
Для оценки эффективности лечения, разработаны специальные критерии, включающие определение плазматических клеток в костном мозге, М-белка в крови и моче, а также количество очагов остеодеструкции. По этим критериям выделяют следующие формы ответа:
- Полная ремиссия — количество ПК входит в норму и не превышает 5%, в сыворотке и моче отсутствует М-белок, нет новых очагов остеодеструкции.
- Почти полная ремиссия — критерии такие же, как у ПП, но при использовании иммунофиксации в моче определяется М-белок.
- Очень хорошая частичная ремиссия — М-белок в крови снижается на 90% от исходного уровня или определяется только с помощью иммунофиксации.
- Частичная ремиссия — М-белок в крови снижается на 50% от исходного уровня, в моче — на 90%. Если это солитарная плазмоцитома, очаги также должны уменьшится на 50%.
Также могут быть варианты минимального ответа, стабилизации процесса, прогрессирования и развития рецидива.
Что будет, если лечение не дает результатов
Если опухоль резистентна к терапии первой линии, используют препараты второй линии с другим механизмом действия. Например, если в первой схеме применялся бортезумаб, его меняют на леналидомид.
При развитии рецидивов, возможно назначение ХТ первой линии, а также использование препаратов с более высокой противоопухолевой активностью в отношении миеломы — помалидомид, карфилзомиб и др.
Побочные эффекты от лечения миеломы
Побочные эффекты при лечении миеломы аналогичны таковым при любой химиотерапии. Сюда входят:
- Тошнота.
- Рвота.
- Общая слабость.
- Общетоксическое действие.
- Диареи.
- Анемии.
- Иммунодефициты.
- Кровотечения.
Боль при миеломе
Костные боли при миеломе являются очень серьезной проблемой. Для их купирования и предупреждения дальнейшей резорбции кости применяют бисфосфонаты. Препаратом выбора является золедроновая кислота. Также для устранения боли используется лучевая терапия и сильные анальгетики, вплоть до наркотических препаратов.
Продолжительность жизни при болезни
Продолжительность жизни определяется формой заболевания, его стадией и ответом на лечение. Тлеющая миелома может годами не прогрессировать и не угрожать жизни пациента. При активной миеломе средняя продолжительность жизни при 1 стадии составляет 6-7 лет, при 2 стадии — 3-4 года, при 3 — 2 года.
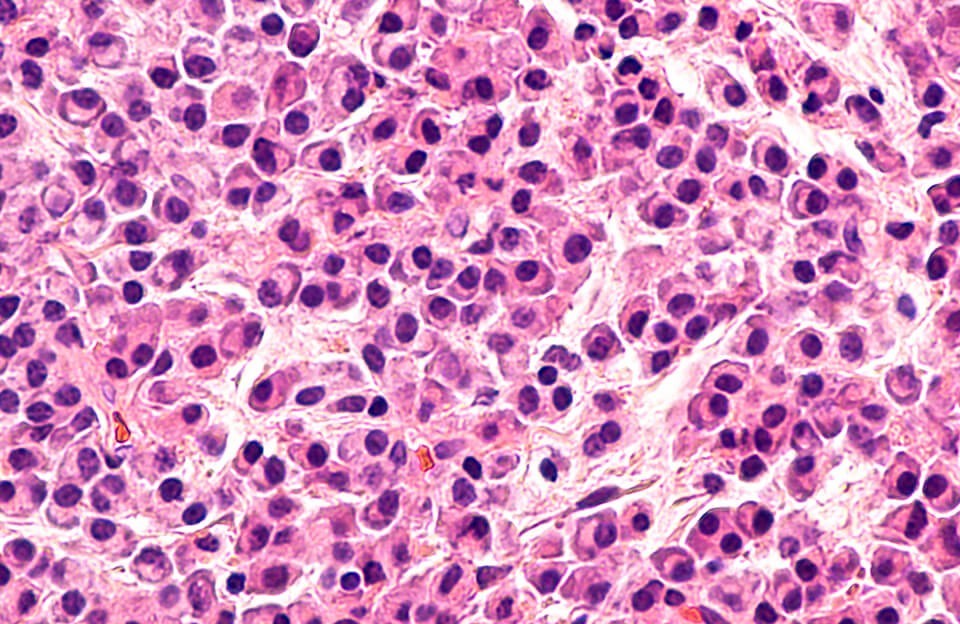
Что такое миеломная болезнь?
Это опухолевое заболевание, возникающее из плазматических клеток крови (подтип лейкоцитов, т.е. белых кровяных телец). У здорового человека эти клетки участвуют в процессах иммунной защиты, вырабатывая антитела. При миеломной болезни (ее еще называют миеломой) в костном мозге и в костях накапливаются измененные плазматические клетки, что нарушает образование нормальных клеток крови и структуру костной ткани. Иногда можно услышать о миеломе костей, миеломной болезни позвоночника, почек или крови, но это не совсем верные названия. Миеломная болезнь уже подразумевает поражение кроветворной системы и костей.
Классификация миеломной болезни
Болезнь неоднородна, можно выделить следующие варианты:
моноклональная гаммапатия неясного генеза - это группа заболеваний, при которых избыточное количество В-лимфоцитов (это клетки крови, которые участвуют в иммунных реакциях) одного вида (клона) вырабатывают аномальные иммуноглобулины разных классов, которые накапливаются в разных органах и нарушают их работу (очень часто страдают почки).
лимфоплазмацитарная лимфома (или неходжкинская лимфома), при которой очень большое количество синтезирующихся иммуноглобулинов класса М повреждает печень, селезенку, лимфоузлы.
плазмацитома бывает двух видов: изолированная (поражает только костный мозг и кости) и экстрамедуллярная (накопление плазматических клеток происходит в мягких тканях, например, в миндалинах или носовых пазухах). Изолированная плазмацитома костей в некоторых случаях переходит во множественную миелому, но не всегда.
Множественная миелома составляет до 90% всех случаев заболевания и обычно затрагивает несколько органов.
асимптоматическую (тлеющую, бессимптомную миелому)
миелому с анемией, поражением почек или костей, т.е. с симптомами.
Код миеломы по МКБ-10: С90.
Стадии миеломной болезни
Стадии определяют в зависимости от количества в сыворотке крови бета-2 микроглобулина и альбумина.
1 стадия миеломы: уровень бета-2 микроглобулина менее 3,5 мг/л, а уровень альбумина равен 3,5 г/дл или более.
2 стадия миеломы: бета-2 микроглобулин колеблется между 3,5 мг/л и 5, 5 мг/л или же уровень альбумина ниже 3,5, тогда как бета-2 микроглобулин ниже 3,5.
3 стадия миеломы: уровень бета-2 микроглобулина в сыворотке составляет более 5,5 мг/л.
Причины и патогенез миеломной болезни
Причины миеломы неизвестна. Есть ряд факторов, повышающих риск заболеть:
Возраст. До 40 лет миеломной болезнью почти не болеют, после 70 лет риск развития заболевания значительно повышен
Мужчины болеют чаще женщин
У людей с черным цветом кожи риск миеломы в два раза выше, чем у европейцев или азиатов
Имеющаяся моноклональная гаммапатия. У 1 из 100 человек гаммапатия трансформируется в множественную миелому
Семейная история заболевания миеломой или гаммапатией
Патология иммунитета (ВИЧ или применение лекарств, подавляющих иммунитет)
Воздействие радиации, пестицидов, удобрений
Костный мозг в обычных условиях вырабатывает строго определенное количество В-лимфоцитов и плазматических клеток. При миеломной болезни их выработка выходит из-под контроля, костный мозг заполняется аномальными плазматическими клетками, а образование нормальных лейкоцитов и эритроцитов снижается. При этом вместо антител, полезных в борьбе с инфекциями, такие клетки производят белки, способные повреждать почки.
Симптомы и признаки миеломной болезни
Признаки, которые помогут заподозрить миелому:
Боль в костях, особенно в ребрах и позвоночнике
Патологические переломы костей
Частые, повторяющиеся случаи инфекционных заболеваний
Выраженная общая слабость, постоянная усталость
Кровотечения из десен или носовые, у женщин - обильные менструации
Головная боль, головокружение
Тошнота и рвота
Диагностика миеломной болезни
Поставить диагноз бывает сложно, так как при миеломной болезни нет какой-то явной опухоли, которую можно заметить, а иногда заболевание вообще протекает без каких-либо симптомов.
Диагностикой миеломной болезни обычно занимается врач-гематолог. Во время расспроса врач выявляет основные симптомы заболевания у данного пациента, выясняет, нет ли кровотечений, боли в костях, частых простуд. Затем проводят дополнительные исследования, необходимые для точной постановки диагноза и определения стадии болезни.
Клинический анализ крови при миеломе часто указывает на увеличение вязкости крови и повышение скорости оседания эритроцитов (СОЭ). Нередко снижено количество тромбоцитов и эритроцитов, гемоглобина.
В результатах анализа крови на электролиты часто повышен уровень кальция; по данным биохимического анализа увеличено количество общего белка, определяются маркеры нарушения функции почек - высокие цифры мочевины, креатинина.
Анализ крови на парапротеин проводят для оценки типа и количества аномальных антител (парапротеинов).
В моче часто определяют патологический белок (белок Бенс-Джонса), который представляет собой моноклональные легкие цепи иммуноглобулинов.
На рентгенограмме костей (черепа, позвоночника, бедренных и тазовых костей) видны характерные для миеломы повреждения.
Пункция костного мозга - самый точный способ диагностики. Тонкой иглой берут кусочек костного мозга, обычно прокол делают в области грудины или кости таза. Затем полученный изучают под микроскопом в лаборатории на предмет перерожденных плазматических клеток и проводят цитогенетическое исследование для выявления изменений в хромосомах.
Компьютерная томография, магнитно-резонансная томография, ПЭТ-сканирование позволяют выявить участки повреждения в них.
Способы лечения миеломной болезни
В настоящее время используют разные методы лечения, прежде всего лекарственную терапию, при которой препараты применяют в разных комбинациях.
Таргетная терапия с использованием лекарства (бортезомиб, карфилзомиб (не зарегистрирован в России), которые за счет влияния на синтез белков вызывают гибель плазматических клеток.
Терапия биологическими препаратами, такие как талидомид, леналидомид, помалидомид, стимулируют собственную иммунную систему бороться с опухолевыми клетками.
Химиотерапия циклофосфаном и мелфаланом, которые тормозят рост и приводят к гибели быстрорастущих клеток опухоли.
Кортикостероидная терапия (дополнительное лечение, которое усиливает эффект основных препаратов).
Бисфосфонаты (памидронат, золендроновая кислота) назначают для повышения плотности костной ткани.
Обезболивающие, в том числе наркотические анальгетики, применяют при сильных болях (очень частая жалоба при миеломной болезни), для облегчения состояния пациента применяют хирургические методы и лучевая терапия.
Хирургическое лечение требуется, например, для фиксации позвонков с помощью пластин или других приспособлений, так как происходит разрушение костной ткани, в том числе позвоночника.
После проведения химиотерапии часто проводят пересадку костного мозга, при этом наиболее эффективной и безопасной является аутологичная трансплантация стволовых клеток костного мозга, Для осуществления этой процедуры проводят забор стволовых клеток красного костного мозга. затем назначают химиотерапию (как правило, высокими дозами противоопухолевых препаратов), которая уничтожает раковые клетки. После окончания полного курса лечения делают операцию по пересадке забранных ранее образцов, и в результате начинают расти нормальные клетки красного костного мозга.
Некоторые формы заболевания (прежде всего “тлеющая” меланома) не требуют срочного и активного лечения. Химиотерапия вызывает тяжелые побочные эффекты и в некоторых случаях - осложнения, а эффекты на течение болезни и прогноз при бессимптомной “тлеющей” миеломной болезни сомнителен. В таких случаях проводят регулярное обследование и при первых признаках обострения процесса начинают лечение. План контрольных исследований и регулярность их проведения врач устанавливает индивидуально для каждого пациента, и очень важно соблюдать эти сроки и все рекомендации врача.
Осложнения миеломной болезни
Сильные боли в костях, требующие назначения эффективных обезболивающих средств
Почечная недостаточность с необходимостью гемодиализа
Частые инфекционные заболевания, в т.ч. воспаление легких (пневмонии)
Истончение костей с переломами (патологические переломы)
Анемия, требующая переливания крови
Прогноз при миеломной болезни
При “тлеющей” миеломе заболевание может не прогрессировать десятки лет, но необходимо регулярное наблюдение у врача, чтобы вовремя заметить признаки активизации процесса, при этом появление очагов разрушения костей или увеличение в костном мозге количества плазматических клеток выше 60% говорит об обострении заболевания (и ухудшении прогноза).
Выживаемость при миеломе зависит от возраста и общего состояния здоровья. В настоящее время в целом прогноз стал оптимистичнее, чем еще 10 лет назад: 77 из 100 больных миеломой человек будут жить как минимум год, 47 из 100 - как минимум 5 лет, 33 из 100 - как минимум 10 лет.
Причины смерти при миеломной болезни
Чаще всего к смерти приводят инфекционные осложнения (например, пневмония), а также фатальные кровотечения (связанные с низким количеством тромбоцитов в крови и нарушениями свертываемости), переломы костей, тяжелая почечная недостаточность, тромбоэмболия легочной артерии.
Питание при миеломной болезни
Рацион при миеломе должен быть разнообразным, содержать достаточное количество овощей и фруктов. Рекомендуют уменьшить потребление сладостей, консервов и готовых полуфабрикатов. Специальной диеты можно не придерживаться, но так как миеломе часто сопутствует анемия, то желательно регулярно есть продукты, богатые железом (постное красное мясо, сладкий перец, изюм, брюссельская капуста, брокколи, манго, папайя, гуава).
В одном из исследований было продемонстрировано, что употребление куркумы предупреждает резистентность к химиотерапии. Исследования на мышах показали, что куркумин может замедлять рост раковых клеток. Также добавление в пищу куркумы во время химиотерапии может несколько облегчить тошноту и рвоту.
Все изменения в диете нужно согласовывать с лечащим врачом, особенно во время химиотерапии.
Читайте также:

