Опухоли панкреатодуоденальной зоны клиника диагностика лечение
Опухоли панкреатодуоденальной зоны (ПДЗ), или, периампулярные опухоли – собирательное понятие, включающее злокачественные новообразования желчевыводящих путей, двенадцатиперстной кишки и поджелудочной железы.
Благодаря тесной анатомической и функциональной связи этих структур сходны и клинические проявления, методы диагностики и лечения периампулярных опухолей.
Среди опухолей ПДЗ около 65 % приходится на рак поджелудочной железы (РПЖ). Реже, примерно в 20 % случаев встречаются опухоли Фатерова соска (аденокарцинома, реже – аденома), в 12–14 % – рак внепеченочных желчных протоков и в 1–3 % – рак двенадцатиперстной кишки. При относительно невысокой заболеваемости (6–10 случаев на 100 тыс. населения) РПЖ в структуре онкологической смертности занимает 4–5 место. Это объясняется крайне агрессивным течением заболевания, несвоевременной диагностикой и сложностью лечения.
Для механической желтухи опухолевого генеза характерны:
· быстрое развитие желтухи,
· незначительный болевой синдром,
· ахолия кала при вполне удовлетворительном общем состоянии,
· пальпируемый (у 30 % больных) увеличенный, эластической консистенции, безболезненный желчный пузырь – см Курвуазье– достоверный признак механической желтухи опухолевого генеза,
· признаки билиарной гипертензии при УЗИ – достоверный признак механической желтухи,
· преимущественное повышение уровня связанного билирубина и резкое повышение щелочной фосфатазы, при нормальном (или незначительном повышении) уровня трансаминаз.
Клиника и диагностика рака поджелудочной железы.
Отдельно рассматривают рак головки (85 %) и рак дистальных отделов поджелудочной железы. Они по-разному проявляются, так как головка и дистальные отделы поджелудочной железы имеют разные отношения с другими структурами.
Рак головки поджелудочной железы.
Боли. Могут быть различной интенсивности. Возникают чаще после еды. При синдроме окклюзии Вирсунгова протока сразу после еды возникает очень сильная боль в эпигастрии, мигрирующая затем по всему животу, появляются схваткообразные боли, вздутие живота и профузный понос плохо переваренной пищей. Опухоль из эпителия суживает Вирсунгов проток и ведёт к развитию отёчного панкреатита. Пища, поступающая в 12-перстную кишку, не переваривается там, так как нет пищеварительных ферментов поджелудочной железы и, поступая в тонкую кишку, вызывает метеоризм и понос. При прекращении стимуляции после еды больному становится легче. Рак поджелудочной железы может привести к панкреатиту и, в то же время, он может протекать, как панкреатит.
Анемия. Носит гипопластический характер.
Похудание из-за снижения аппетита, ограничения себя в пище, особенно белковой.
Пальпация опухоли (если опухоль большая).
Желтуха – самый главный признак. Прогредиентно нарастает, никогда не уменьшается. Билирубин достигает 600 мкмоль/л. Желтуха может начинаться, как при остром гепатите: несколько дней длится продромальный период, слабость, тошнота, повышение температуры до 38о С, затем эти явления стихают, а потом снова появляется желтуха. Течение её никогда не бывает ремиттирующим как при подвижных камнях.
Дифференциальный диагноз.
Нельзя полагаться на клинику и лабораторные данные, которые не позволяют различить механическую и паренхиматозную желтухи. Нельзя ориентироваться на биохимический анализ крови, так как желтуха почти сразу же приобретает смешанный характер. Для дифференциального диагноза желтух используют УЗИ. В норме просвет печёночных желчных протоков не определяется, они могут быть расширены до нескольких миллиметров только после еды. При механической желтухе любой этиологии они расширены. Если они не расширены, то это не механическая желтуха. Лабораторные анализы только подтверждают диагноз. УЗИ – основной способ диагностики причины желтухи. Желтуху могут вызывать опухоли, камни, стриктуры желчевыводящих путей, рак поджелудочной железы, панкреатиты, опухоли и отёк Фатерова соска, рак 12-типерстной кишки, метастазы рака в печень, циррозы печени, паразиты и др.
Физикальные данные. Симптом Курвуазье – пальпируется растянутый желчный пузырь (положителен только в 40 % случаев, так как часто попадаются очень жирные пациенты или вообще без желчного пузыря и т. д.).
ЭРХПГ – Эффективность 97–98 %. Выявляется и рак и причина. При Вирсунгографии выявляют деформацию и сужение протока, так как в основном раки растут из эпителия. Кроме того, смотрят Фатеров сосок. Многие опухоли прорастают в 12-перстную кишку и вызывают дуоденальный стеноз.
КТ – дорогостоящий метод. Можно делать одномоментно ЭРХПГ и КТ.

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого.

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).
Опухоли панкреатодуоденальной зоны (ПДЗ), или, периампулярные опухоли – собирательное понятие, включающее злокачественные новообразования желчевыводящих путей, двенадцатиперстной кишки и поджелудочной железы.
Благодаря тесной анатомической и функциональной связи этих структур сходны и клинические проявления, методы диагностики и лечения периампулярных опухолей. Частота опухолей ПДЗ за последние 10 лет увеличилась в России и Белоруссии в 2 раза и составляет в настоящее время 5–9 % от общего количества всех злокачественных опухолей и 9–17 % новообразований органов пищеварения.
Среди опухолей ПДЗ около 65 % приходится на рак поджелудочной железы (РПЖ). Реже, примерно в 20 % случаев встречаются опухоли Фатерова соска (аденокарцинома, реже – аденома), в 12–14 % – рак внепеченочных желчных протоков и в 1–3 % – рак двенадцатиперстной кишки. При относительно невысокой заболеваемости (6–10 случаев на 100 тыс. населения) РПЖ в структуре онкологической смертности занимает 4–5 место. Это объясняется крайне агрессивным течением заболевания, несвоевременной диагностикой и сложностью лечения. В США, например, одногодичная выживаемость при РПЖ составляет 8 %, пятилетняя – 2 %.
С повышенным риском заболевания опухолями ПДЗ, и прежде всего, РПЖ, сопряжены:
ü Избыточное употребление мяса и животных жиров, недостаток овощей в рационе (стимулирует выработку панкреозимина, вызывающего гиперплазию поджелудочной железы).
ü Курение табака – повышает риск РПЖ в 2 раза (нитрозамины и др. канцерогенные метаболиты попадают в желчь и при ее рефлюксе контактируют с тканью ПЖ; курение приводит к гиперлипидемии, которая способствует гиперплазии паренхимы ПЖ).
ü Алкоголизм (приводит к панкреатиту и секреторной недостаточности ПЖ).
ü Хронический панкреатит (в 50–60 % случаев сочетается с РПЖ).
ü Сахарный диабет (при СД выявляется гиперплазия ткани ПЖ; СД может развиваться на фоне панкреатита и рака).
ü ЖКБ (является этиологическим фактором рака желчных протоков и желчного пузыря; РПЖ чаще встречается в сочетании с холестериновыми камнями и после холецистэктомии).
ü Паразитарные заболевания желчевыводящих путей.
ü Промышленные канцерогены (чаще болеют лица. занятые в резиновой и деревообрабатывающей промышленности).
Рост и распространение опухолей ПДЗ происходит в результате их инвазивного роста, а также лимфогенного, гематогенного и, реже, имплантационного, или контактного, метастазирования.
Около 80 % больных с механической желтухой опухолевой этиологии, прежде чем "попасть" к онкологу, в течение 2–3 недель и более проходят лечение в инфекционном стационаре по поводу предполагаемого вирусного гепатита. От момента появления механической желтухи опухолевой этиологии до операции проходит, в среднем, около месяца. Радикальное оперативное вмешательство из-за высокого уровня холемии и печеночной недостаточности у больных с длительно существующей механической желтухой возможно лишь на втором этапе, примерно через 3–4 недели после предварительного наружного или внутреннего дренирования желчных путей и ликвидации желтухи. Запоздалое выполнение радикального вмешательства приводит к плохим отдаленным результатам, 5летняя выживаемость при раке головки поджелудочной железы не превышает 5 %.
Для механической желтухи опухолевого генеза характерны:
ü быстрое развитие желтухи,
ü незначительный болевой синдром,
ü ахолия кала при вполне удовлетворительном общем состоянии,
ü пальпируемый (у 30 % больных) увеличенный, эластической консистенции, безболезненный желчный пузырь – см Курвуазье– достоверный признак механической желтухи опухолевого генеза,
ü признаки билиарной гипертензии при УЗИ – достоверный признак механической желтухи,
ü преимущественное повышение уровня связанного билирубина и резкое повышение щелочной фосфатазы, при нормальном (или незначительном повышении) уровня трансаминаз.
гипогликемия, ахлоргидрия, “панкреатическая диаррея” (наблюдается при островковоклеточных опухолях, випомах, из них до 15% являются злокачественными);
синдром Золлингера-Элисона (обусловлен гастриномой, проявляющейся триадой - пептическими язвами, экстримальной секрецией, агрессивностью течения);
синдром Вермера-Моррисона (множественный эндокринный аденоматоз составляет 5% случаев от числа эндокринных опухолей);
карциноидный синдром (повышенная секреция серотонина).
Отсутствие функциональных нарушений.
Неопределённое функциональное состояние.
Диагностика:
Копрологический анализ, копроцитограмма.
Биохимический анализ крови: электролиты, трансаминазы, щелочная фосфатаза, билирубин, креатинин, NH3, амилаза.
Определение в крови серотонина, норадреналина, адреналина, кортизола, хромогранина А, гастрина, вазоактивного пептида, инсулина, С-пептида, панкреатического пептида, глюкагона, соматостатина.
Определение суточной экскреции с мочой адреналина, норадреналина, ванилилминдальной кислоты, 5-ГОИУК (при необходимости проба с резерпином).
Определение желудочной секреции.
Компьютерная томография и(или) ядерно-магнитно-резонансная томография, спиральная компьютерная томография с болюсным контрастным усилением.
Эндоскопическое ультразвуковое исследование.
Интраоперационное ультразвуковое исследование, поскольку большинство эндокринных опухолей имеют незначительный размер от 2 мм до 30 мм.
Ангиография (целиакография), в том числе селективная абдоминальная ангиография с взятием крови из панкреатических вен и определением в ней гормонов.
Ультразвуковое цветное допплеровское сканирование.
Сцинтиграфия с радиоактивным октреотидом (Октрео-Скан).
Дифференциальная диагностика:
кисты поджелудочной железы,
пенетрирующие язвы желудка и 12-перстной кишки,
опухоли брыжейки кишечника,
поражение поджелудочной железы при эхинококкозе и цистицеркозе.
Хирургическое лечение – удаление опухоли, гемирезекция поджелудочной железы при расположении опухоли в теле или хвосте поджелудочной железы. При злокачественных карциноидах и эндокринном раке с локализацией опухоли в головке поджелудочной железы – пилоросохраняющая панкреатодуоденальная резекция. Вопрос о целесообразности панкреатодуоденальной резекции, гастрэктомии или селективной ваготомии при гастриномах – остаётся открытым.
при низком коэффициенте пролиферации (Кі 67), доброкачественной нейроэндокринной опухоли с незначительным повышением хромогранина А, соответствующих гормонов и их метаболитов, умеренных клинических признаках гиперсекреторных синдромов используют сандостатин+омепразол;
при высоком коэффициенте пролиферации, значительном повышении хромогранина А, соответствующих гормонов и их метаболитов, гистологически подтверждённая малигнизация или выявленные метастазы показана полихимиотерапия (5-фторурацил, стрептозоцин, эпирубицин) + интрон-А+сандостатин+радиоактивный октреотид;
симптоматическая терапия при гастриномах предусматривает сочетанное лечение гистаминовыми Н2-блокаторами+ингибиторы „протонной помпы”+холинолитики.
При доброкачественных опухолях прогноз благоприятный - в 90% случаев достигается выздоровление.
Рак поджелудочной железы
Относится к наиболее агрессивным злокачественным опухолям, отличающийся высокой резистентностью к специальным методам лечения.
Эпидемиология.
Смертность от рака поджелудочной железы состовляет 4-9 случаев на 100 000 населения. В структуре заболеваемости злокачественными опухолями рак поджелудочной железы занимает 4-5 место и составляет 9,3 на 100 000. Соотношение больных мужчин и женщин составляет 1,5:1. Летальность у мужчин в возрасте от 35 до 54 года при раке ПЖ выходит на 3-4 место среди причин смертности от рака других локализаций. В последнее время заболеваемость РПЖ повсеместно выросла в 2-4 раза.
Резектабельность при РПЖ, даже в специализированных клиниках составляет всего 17-28%, а 5-ти летняя выживаемость – не превышает 1 –5%. 90% больных умирает на протяжении первого года с момента установки диагноза. Средняя продолжительность жизни – 3,5-6 мес.
Общая онкология. Организация онкологической помощи.
1. Определение понятия “опухоль”. Доброкачественные, пограничные и злокачественные опухоли. Основные свойства злокачественных опухолей.
2. Классификация опухолей в зависимости от гистогенеза. Пути и этапы метастазирования злокачественных опухолей.
3. Современная модель канцерогенеза. Основные группы канцерогенов.
4. Экзогенные и эндогенные факторы, повышающие риск развития новообразований. Факторы противоопухолевой резистентности организма. Профилактика онкологических заболеваний (первичная, вторичная, третичная).
5. Эпидемиология злокачественных опухолей. Структура онкологической заболеваемости и смертности в Республике Беларусь.
6. Организация онкологической службы в Республике Беларусь. Клинические группы онкологических пациентов. Учетная документация.
7. Деонтология в онкологии.
8. Основные закономерности клинических проявлений злокачественных опухолей. Диагностический алгоритм в онкологии: первичная и уточняющая диагностика. Виды биопсий.
9. Принципы классификации по системе TNM: основные и дополнительные предикторы. Стадии заболевания. Структура онкологического диагноза.
10. Хирургическое лечение злокачественных новообразований. Радикальные, паллиативные и симптоматические операции. Принципы радикальных операций, отличие от операций при неопухолевой патологии.
11. Радиобиологические основы применения лучевой терапии в онкологии. Правило Бергонье-Трибондо. Способы и виды лучевой терапии, в зависимости от задачи и методологии. Показания и противопоказания к лучевой терапии.
12. Химиотерапия опухолей. Основные группы противоопухолевых препаратов. Показания и противопоказания к химиотерапии.
13. Гормонотерапия в онкологии. Показания к гормонотерапии. Группы лекарственных препаратов.
14. Иммунотерапия злокачественных новообразований. Таргетная терапия. Основные группы препаратов. Показания к иммунотерапии.
15. Комбинированное и комплексное лечение злокачественных новообразований. Адъювантная и неоадъювантная терапия. Мультимодальное лечение: основные химио- и радиомодификаторы.
Опухоли кожи. Злокачественные лимфомы.
16. Эпидемиология опухолей кожи. Этиологические факторы. Факультативные и облигатные предраковые заболевания кожи.
17. Меланомоопасные пигментные невусы. Меланоз Дюбрея. Признаки активизации пигментных невусов. Лечебно-диагностическая тактика.
18. Рак кожи: гистологические формы, анатомические формы роста, особенности метастазирования. Диагностика рака кожи. Методы лечения пациентов с базальноклеточным и плоскоклеточным раком кожи. Прогноз. Профилактика.
19. Меланома кожи: формы роста, метастазирование. Клиника и диагностика.
20. Лечение меланомы кожи. Типовые лимфодиссекции. Прогноз. Профилактика.
21. Злокачественные лимфомы: эпидемиология, этиологические факторы, основные морфологические формы. Клиника: общие и местные симптомы.
22. Диагностика злокачественных лимфом. Классификация по стадиям. Методы лечения. Особенности тактики при индолентных лимфомах. Прогноз.
Рак щитовидной железы. Рак губы. Рак слизистой оболочки полости рта. Опухоли слюнных желез.
23. Эпидемиология рака щитовидной железы. Этиологические факторы. Морфологические формы рака щитовидной железы. Особенности их клинического течения.
24. Диагностика рака щитовидной железы. Папиллярный и фолликулярный рак: особенности метастазирования, диагностики и лечения. Лечение других морфологических форм рака щитовидной железы. Прогноз.
25. Рак губы: эпидемиология, этиологические факторы. Предраковые заболевания губы. Местное распространение и метастазирование рака губы. Клиника, диагностика, лечение, прогноз.
26. Рак слизистой оболочки полости рта: эпидемиология, этиологические факторы, гистологические формы. Местное распространение и метастазирование. Клиника, диагностика, лечение, прогноз.
27. Опухоли слюнных желез: эпидемиология, основные морфологические формы. Местное распространение и метастазирование злокачественных опухолей. Клиника, диагностика, лечение, прогноз.
Рак молочной железы.
28. Рак молочной железы: эпидемиология, этиологические факторы, гистологические и клинические формы, метастазирование.
29. Клиника узловой формы рака молочной железы. Симптомы, обусловленные поражением Куперовских связок. Признаки вовлечения кожи в опухолевый процесс (Т4В).
30. Клиника диффузных форм рака молочной железы. Клиника рака Педжета.
31. Рак молочной железы: диагностика и дифференциальная диагностика.
32. Рак молочной железы: методы лечения. Тактика, в зависимости от степени распространенности и морфологических особенностей опухоли.
33. Типовые радикальные операции при раке молочной железы: объем, показания к выполнению. Значение сигнальных лимфоузлов.
34. Профилактика рака молочной железы, прогноз. Скрининг рака молочной железы.
35. Диффузная и узловая мастопатия. Фиброаденома, филлоидная фиброаденома, протоковая папиллома, киста, олеогранулема молочной железы. Этиология, клиника, диагностика, лечение.
Рак легкого. Рак гортани.
36. Рак легкого: эпидемиология, этиологические факторы, основные морфологические формы. Особенности клинического течения бронхиолоальвеолярного рака. Клинико-анатомические формы рака легкого, их рентгенологические проявления.
37. Рак легкого: местное распространение и метастазирование. Клиника центрального и периферического рака, атипичных форм. Синдром Панкоста.
38. Диагностика рака легкого.
39. Методы лечения рака легкого. Тактика при мелкоклеточном и немелкоклеточных формах рака. Прогноз. Профилактика.
40. Рак гортани: эпидемиология, этиологические факторы, местное распространение и метастазирование.
41. Клиника и диагностика рака гортани. Лечение, прогноз, профилактика.
Рак пищевода. Опухоли средостения.
42. Рак пищевода: эпидемиология, этиологические факторы. Предопухолевые заболевания пищевода: лечебно-диагностическая тактика.
43. Гистологические и макроскопические формы рака пищевода. Местное распространение и метастазирование.
44. Клиника рака пищевода. Диагностика, лечение, прогноз, профилактика.
45. Классификация опухолей средостения и их топография. Клинические проявления. Диагностика. Лечение. Прогноз.
Рак желудка.
46. Рак желудка: эпидемиология, этиологические факторы. Предопухолевые заболевания желудка: лечебно-диагностическая тактика.
47. Основные гистологические и макроскопические формы рака желудка. Морфологические типы по классификации Лорена: особенности их клинического течения. Местное распространение и метастазирование рака желудка.
49. Диагностика рака желудка. Особенности эндоскопической и рентгенологической картины при эндофитных формах рака. Оценка распространенности опухолевого процесса.
50. Лечение рака желудка. Радикальные операции: объем и показания к выполнению. Паллиативные и симптоматические операции при осложненных формах рака желудка. Прогноз. Профилактика.
Опухоли панкреатодуоденальной зоны. Опухоли печени.
51. Опухоли панкреатодуоденальной зоны. Эпидемиология. Этиологические факторы. Основные морфологические формы рака поджелудочной железы, особенности их клинического течения.
52. Рак поджелудочной железы: местное распространение и пути метастазирования. Клиника рака головки поджелудочной железы: дожелтушный и желтушный периоды. Клиника рака тела и хвоста поджелудочной железы.
53. Диагностика рака поджелудочной железы. Дифференциальная диагностика механической и паренхиматозной желтухи.
54. Лечение рака поджелудочной железы. Радикальные операции: объем, показания к выполнению. Лечебная тактика в зависимости от высоты холемии. Паллиативные и симптоматические операции. Прогноз. Профилактика.
55. Рак фатерова соска. Клиника, диагностика, лечение, прогноз.
56. Рак внепеченочных желчных протоков. Клиника, диагностика, лечение, прогноз, профилактика.
57. Рак желчного пузыря. Клиника, диагностика, лечение, прогноз, профилактика.
58. Рак двенадцатиперстной кишки. Клиника, диагностика, лечение, прогноз.
59. Первичные и метастатические опухоли печени. Эпидемиология. Основные морфологические формы первичного рака печени. Этиологические факторы. Клиника и диагностика.
60. Лечение первичных и метастатических опухолей печени. Виды анатомических резекций печени. Воротный и фиссуральный методы резекции. Эндоваскулярные технологии в лечении опухолей печени. Прогноз. Профилактика первичного рака печени.
Колоректальный рак.
61. Колоректальный рак: эпидемиология, этиологические факторы. Предопухолевые заболевания ободочной и прямой кишки: их клинические проявления, лечебно-диагностическая тактика.
62. Колоректальный рак: основные гистологические и макроскопические формы. Местное распространение и метастазирование.
63. Клинические формы рака ободочной кишки, связь с локализацией. Клиника рака прямой кишки.
64. Диагностика колоректального рака. Методы скрининга.
65. Методы лечения рака ободочной кишки. Радикальные операции. Паллиативные и симптоматические операции.
66. Методы лечения рака прямой кишки. Радикальные операции: объем и показания к выполнению. Паллиативные и симптоматические операции.
67. Показания к комбинированным операциям при колоректальном раке. Циторедуктивные операции при наличии отдаленных метастазов. Лечебная тактика при острой кишечной непроходимости. Прогноз. Профилактика.
Опухоли мягких тканей. Опухоли забрюшинного пространства.
Опухоли костей.
68. Опухоли мягких тканей: эпидемиология, этиологические факторы, основные морфологические формы. Местное распространение и метастазирование злокачественных опухолей мягких тканей.
69. Клиника и диагностика опухолей мягких тканей. Методы лечения. Типовые радикальные операции. Тактика лечения, в зависимости от гистологической формы и степени дифференцировки. Радикальные операции. Прогноз.
70. Опухоли забрюшинного пространства: топография, основные морфологические формы неорганных забрюшинных опухолей. Местное распространение и метастазирование.
71. Клиника и диагностика неорганных забрюшинных опухолей. Лечение, прогноз.
72. Опухоли костей: эпидемиология, этиологические факторы. Основные морфологические формы. Местное распространение и метастазирование злокачественных опухолей костей.
73. Клиника опухоли костей. Диагностика, лечение, прогноз.
Раковые опухоли панкреато-дуоденальной зоны встречаются сравнительно часто и составляют от 4 до 6% всех злокачественных новообразований.
Рак поджелудочной железы, занимающий среди них первое место, одновременно является шестым по частоте среди всех раковых опухолей. Рак поджелудочной железы может поражать все отделы этого органа, однако в подавляющем большинстве случаев новообразование возникает в области головки поджелудочной железы, вызывая сдавление и прорастание интрапанкреатической части общего желчного протока. При дальнейшем росте опухоли в процесс вовлекается стенка двенадцатиперстной кишки в перифатериальной зоне или опухоль непосредственно переходит на фатеров сосок.
Раковые опухоли фатерова соска представляют собой злокачественные новообразования из незрелой эпителиальной ткани самого фатерова соска, его ампулы или терминальных отделов общего желчного и главного панкреатического протоков. Рак фатерова соска встречается намного реже, чем рак поджелудочной железы или магистральных желчных протоков и, согласно данным В. Х. Василенко (1960), наблюдается в 5% случаев раковых новообразований гепатопанкреатодуоденальной зоны.
Первичный рак двенадцатиперстной кишки - заболевание очень редкое, и случаи прижизненной дооперационной диагностики его вплоть до последнего времени были казуистическими.
Общим для перечисленных разновидностей опухолей является то, что они клинически проявляются и диагностируются, как правило, поздно, в далеко зашедшей стадии заболевания, когда со всей полнотой выступает основной общий для них клинический признак - синдром механической, обтурационной желтухи.

Рис. 60. Операционная холангиография. Рак фатерова соска. Выраженное расширение внепеченочных желчных протоков. Кривизна холедоха увеличена. Терминальный отдел протока конусовидно сужен, резко обрывается (1). Рефлюкс контрастного вещества в расширенный вирсунгов проток (2).
При частичной обтурации опухолью терминального отдела общего желчного протока наблюдается выраженное в большей или меньшей степени расширение всего желчного дерева, пузырного протока и желчного пузыря. Контрастное вещество, поступая в двенадцатиперстную кишку, узкой струей обтекает пристеночный, изъеденный и бугристый контур опухоли, давая характерную картину краевого дефекта наполнения. Степень расширения желчных протоков зависит от ширины просвета, оставшегося между опухолью и свободной стенкой протока. При опухолях фатерова соска, растущих в просвет кишки, контрастный раствор обтекает опухоль или определяются разрушение и стертость рисунка керкринговых складок с образованием в области проекции фатерова соска дефекта наполнения.
Рак головки поджелудочной железы, вопреки устоявшемуся мнению, чаще прорастает интрапанкреатическую часть общего желчного протока, вызывая полную обтурацию его, чем приводит к частичной непроходимости при сдавлении протока. Более того, прорастая общий желчный проток, раковая опухоль далеко не всегда ограничивается поражением только панкреатического отдела протока, а распространяется по нему в нисходящем и восходящем направлении, доходя до пузырного протока или прорастая желчный пузырь (рис. 61). Однако наиболее часто верхняя граница опухолевой обтурации располагается на уровне верхнего края головки поджелудочной железы.

Рис. 61. Операционная холангиография. Рак головки поджелудочной железы с прорастанием внепеченочных желчных протоков и инфильтрацией стенки желчного пузыря. Контур контрастной тени желчного пузыря зазубрен, изъеден. Желчный пузырь полностью блокирован (указано стрелкой).
При первичных опухолях гепатико-холедоха несколько чаще, чем при опухолях головки поджелудочной железы, наблюдается неполная обтурация желчных протоков. При частичном сдавлении просвета протоков опухолью контрастное исследование выявляет наличие более или менее протяженного пристеночного дефекта наполнения с супрастенотическим расширением вне- или внутрипеченочных желчных протоков, а при полной блокаде - резкий обрыв рентгеноконтрастной тени протока.
При полной, высокой раковой обтурации желчных протоков в процесс вовлекается либо общий печеночный проток, либо, что наблюдается чаще, опухоль захватывает устья печеночных протоков и приводит к их полному разобщению (рис. 62). Таковы в целом рентгенологические признаки опухолей желчевыводящей системы и панкреатодуоденальной зоны, зависящие в основном от степени нарушения оттока желчи и уровня блокады желчных путей.

Рис. 62. Операционная холангиография. Опухоль устья правого и левого печеночных протоков с полным разобщением их. Контрастное вещество введено раздельно в субкапсулярные, варикозно расширенные протоки правой и левой долей печени. Внутрипеченочные желчные протоки расширены, в особенности левой доли (1). Линия обрыва тени правого (2) и левого (3) печеночных протоков имеет замкнутый контур.
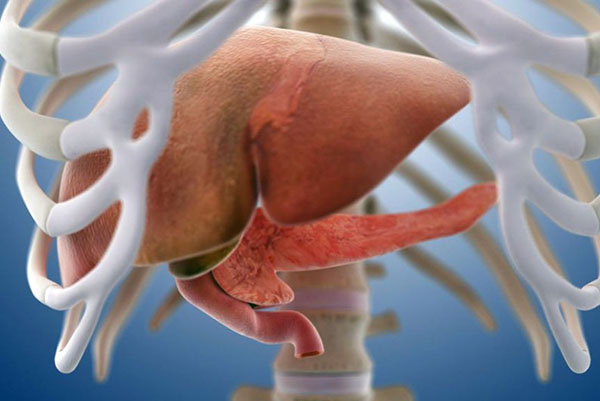
Заболевания органов панкреатодуоденальной зоны (ПДЗ) относятся к разряду трудно диагностируемых и часто поздно выявляемых патологических процессов, требующих в большинстве случаев выполнения сложных оперативных вмешательств. Большинство этих заболеваний являются злокачественными опухолями головки поджелудочной железы (ПЖ), Фатерова соска, двенадцатиперстной кишки (ДПК) и дистального отдела холедоха, которые сопровождаются стенозированием и обтурацией просвета общего желчного протока, главного протока поджелудочной железы и просвета двенадцатиперстной кишки [1].
Все указанные выше патологические процессы рационально рассматривать как обструктивные заболевания органов ПДЗ. Эти патологические процессы объединяет прогрессирующая обструкция панкреатического, общего желчного протоков и большого дуоденального сосочка (БДС) с развитием механической желтухи, реже – стеноз просвета двенадцатиперстной кишки (ДПК) с развитием дуоденальной непроходимости. Обструктивные патологические процессы включают злокачественные и доброкачественные заболевания, куда входят опухоли головки ПЖ, БДС и периампулярной зоны, опухоли и стриктуры терминального отдела холедоха, хронический панкреатит (ХП) с преимущественным фиброзом, кальцинозом и кистами в области головки ПЖ [1, 5].
Более 90% обструктивных заболеваний ПДЗ составляют злокачественные новообразования, среди которых превалирует протоковая аденокарцинома ПЖ. Во всем мире отмечается перманентный рост онкологической патологии органов ПДЗ, которая, по данным М.Ю. Кабанова и соавт. (2012), занимает 8-9 место среди всех онкозаболеваний, но в структуре смертности рак ПЖ занимает 4-5 место, и более 80% больных умирают в течение первого года. Причины неблагоприятного течения заболевания кроются в особенностях структуры и локализации рака ПЖ, раннем метастазировании с частыми инвазиями в крупные венозные и артериальные сосуды и периневральном распространении опухолевого процесса [4, 7].
Малая частота радикальных операций (15-26%), высокий уровень послеоперационных осложнений (30-50%) и летальности (7-17%) характеризуют особую сложность и тяжесть этой патологии, заставляя проводить дальнейшее активное совершенствование диагностики, дооперационной подготовки, хирургической техники и послеоперационного ведения больных с обструктивными заболениями органов ПДЗ [2, 4].
Эпидемиология
Заболеваемость раком ПЖ составляет 10-12 случаев на 100 тыс. населения в странах Европы и Северной Америки. В Японии заболеваемость раком ПЖ за последние 30 лет возросла в 1,5 раза и составляет 12,6 случаев на 100 000 населения для мужчин и 7,3 – для женщин. В Украине за последние 5 лет заболеваемость раком ПЖ остается на одном уровне – 10,3 на 100 тыс. (12,2 – для мужчин и 8,6 – для женщин). Частота рака ПЖ среди всех злокачественных опухолей – 3,4% (9 место) для мужчин и 2,8% (10 место) для женщин. Пик заболеваемости – в возрасте 65-75 лет. Показатели заболеваемости возрастают почти в 2 раза после 45 лет и продолжают неуклонно повышаться, демонстрируя резкий скачок после 65 лет [1, 3].
Этиология
Все типы хронического панкреатита (алкогольный, неалкогольный, наследственный, тропический) приводят к 10-20-кратному повышению риска возникновения РПЖ. Хронический панкреатит повышает риск развития рака ПЖ в 9-16 раз. Основная роль в развитии хронического панкреатита и рака ПЖ принадлежит панкреатическим звездчатым клеткам (PSC). Они формируют фиброз и одновременно стимулируют онкогенез [1, 4].
Более 90% опухолей ПЖ – протоковые аденокарциномы, в 70-75% случаев опухоли возникают в головке ПЖ, в 15 % – в теле, в 10% – в хвосте. По последним данным A. Masamune (2013), продуцируя экстрацеллюлярный матрикс, PSC индуцируют апоптоз и снижают продукцию инсулина в β-клетках, чем можно объяснить новый механизм возникновения сахарного диабета (СД). Одновременно с этим PSC повышают в стволовых клетках онкогенетические свойства, стимулируя возникновение и прогрессирование рака ПЖ. PSC в настоящее время рассматривают не только как профиброгенетические клетки, а как мультифункциональные клетки, активно взаимодействующие с другими типами клеток ПЖ (эндокринными и экзокринными), что привлекает пристальное внимание исследователей разных стран. На развитие рака ПЖ влияют факторы, подобные тем, что вызывают рак толстой кишки: так называемый западный тип диеты (еда с повышенным содержимым белков и жиров), недостаток витаминов в еде (особенно А и С), вредные привычки (алкоголь и курение, канцерогены в продуктах питания – нитриты, нитраты и тому подобное). Иногда рак ПЖ связан с СД, однако нужно иметь в виду, что у 10% больных раком ПЖ сахарный диабет является следствием опухолевого процесса. В отдельных случаях явно определяется генетический фактор: более чем в 80% опухолей ПЖ, удаленных при операции, обнаруживают мутации гена K-Ras [1, 4].
Отмечают рак ПЖ в семьях с мутацией гена р16 у больных с семейным раком грудной железы, колоректальным раком, семейным полипозом Пейтца-Егерса [2, 6].
Рак БДС выявляется в 0,5-1,6% случаев среди всех злокачественных новообразований и более чем в 2% случаев опухолей органов ЖКТ.
Рак внепеченочных желчных протоков встречается в 2,8-4,6% среди злокачественных опухолей ПДЗ. В странах Европы и Северной Америки заболеваемость холангиокарциномой составляет 1-2 случая на 100 000 населения в год, но ее уровень растет в течение последних десятилетий. К факторам риска развития холангиокарциномы относится наличие у пациента первичного склерозирующего холангита, врожденных пороков развития печени и желчевыводящих путей.
При раке ПЖ происходит около 63 генетических мутаций, которые меняют 12 клеточных сигнальных путей, включая реактивацию генов эмбриогенеза. Точные причины развития данного вида рака не выявлены, но существуют данные о роли определенных средовых факторов: курение, наследственный фактор, СД [1, 2].
Классификация опухолей ПЖ
Все опухоли ПЖ разделяют на две группы: эпителиальные (95-98%) и нейроэндокринные (2-5%). Эпителиальные опухоли ПЖ делятся на редко встречающиеся доброкачественные опухоли, редко диагностируемые пограничные опухоли (с неопределенным злокачественным потенциалом) и злокачественные.
К числу доброкачественных опухолей относят серозную и муцинозную цистаденому, внутрипротоковую папиллярно-муцинозную аденому и зрелую тератому.
К пограничным опухолям относят муцинозную цистаденому с умеренной дисплазией, внутрипротоковую папиллярную муцинозную опухоль с умеренной дисплазией (IPMN) и солидно-псевдопапиллярную опухоль.
К злокачественным опухолям ПЖ относят: протоковые аденокарциномы, серозные и муцинозные цистаденокарциномы (малигнизированные цистаденомы), ацинарноклеточный рак, панкреатобластома (чаще у детей), смешанноклеточная аденокарцинома (крайне редкая), а также внутрипротоковая папиллярно-муцинозная карцинома (малигнизированная IPMN). Наиболее часто встречающейся опухолью ПЖ (около 90%) является протоковая аденокарцинома, которая является высокоагрессивной опухолью с сильной десмопластической реакцией и частой васкулярной, лимфатической и периневральной инвазивностью (J. Kleef, H. Friess, M. Buchler, 2007). Предшественниками рака ПЖ являются муцинозные цистаденомы, внутрипротоковые муцинпродуцирующие неоплазмы (IPMN), а также панкреатическая внутриэпителиальная неоплазия (PanIN-I). Этот термин, введенный в литературу с 1999 г., заменил такие термины, как дисплазия, метаплазия и протоковое поражение ПЖ. Постепенная трансформация атипии от низкого до высокого уровня приводит к формированию PanIN-III, считающейся прединвазивной стадией рака in situ, не распространяющегося за пределы слизистой оболочки [2, 4].
При этом существует мнение, что от появления первых признаков генных мутаций до формирования неинвазивной опухоли проходит около 10 лет, еще около 5 лет длится процесс трансформации в инвазивную и метастатическую форму, после чего онкопроцесс активно прогрессирует, приводя в течение 1,5-2 лет к неблагоприятному исходу [4, 8].
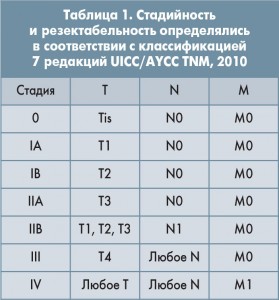
Приводим последнюю классификацию рака ПЖ по системе TNM, стадийность и резектабельность в соответствии с классификацией 7 редакций UICC/AYCC TNM, 2010 (табл. 1).
Первичная опухоль (Т):
Тх – недостаточно данных для оценки первичной опухоли;
Т0 – первичная опухоль не определяется;
Тis – carcinoma in situ;
Т1 – опухоль ограничена ПЖ, 2 см или меньше в наибольшем измерении;
Т2 – опухоль ограничена ПЖ, более 2 см в наибольшем измерении;
Т3 – опухоль распространяется за пределы ПЖ, но без поражения крупных сосудов: верхней брыжеечной вены, воротной вены, чревного ствола или верхней брыжеечной артерии;
Т-4 – опухоль распространяется на крупные кровеносные сосуды (неректабельная опухоль).
Лимфатические узлы:
Nx – недостаточно данных для оценки лимфатических узлов;
N0 – нет признаков поражения регионарных лимфатических узлов;
N1 – наличие метастазов в регионарных лимфатических узлах.
Отдаленные метастазы (М):
Мх – недостаточно данных для определения отдаленных метастазов;
М0 – отдаленные метастазы не определяются;
М1 – наличие отдаленных метастазов.
При стадии от 0 до IIВ – опухоль резектабельна, при III стадии – опухоль нерезектабельна, при IV стадии – опухоль неоперабельна.
Лабораторные показатели, подтверждающие наличие обструкции в панкреатодуоденальной зоне
Об активности воспалительного процесса в зоне обструкции, нарушении функций печени и ПЖ свидетельствуют данные лабораторных методов исследования, которые наиболее ярко проявляются в нарушении пигментного обмена – гипербилирубинемия за счет прямой фракции.
Гипербилирубинемия наблюдается одновременно с повышением уровня щелочной фосфатазы, что свидетельствует о нарушении экскреторной функции печени. Также повышен уровень трансаминаз в сыворотке крови при холестазе, что обусловлено некрозом или повреждением мембраны печеночной клетки и является показателем не только наличия воспалительного процесса в ткани печени, но также процесса цитолиза гепатоцитов на фоне холестаза.
Сочетание холемической интоксикации с желчной гипертензией и цитолитическим синдромом ведет к значительному нарушению белково-синтетической функции печени, что характеризуется гипопротеинемией, гипоальбуминемией, гипергаммаглобулинемией, снижением альбумино-глобулинового коэффициента.
При развитии синдрома цитолиза с нарушением синтетической функции печени наряду со снижением уровня сывороточного альбумина наблюдается, как правило, снижение синтезируемых печенью ферментов протромбинового комплекса.
Нарушение условий функционирования печеночной клетки, некроз большого количества гепатоцитов при одновременном перенапряжении оставшихся клеток на фоне холестаза ведет к значительному нарушению детоксикационной функции печени, развитию синдрома эндогенной интоксикации.
Значительно более информативным является определение уровня опухолевых маркеров в крови. Из всех известных маркеров наиболее чувствительным и специфичным (около 90%) при раке ПЖ является карбоангидратный гликопротеин (СА-19-9) эмбрионального происхождения. У здоровых лиц его содержание в крови не превышает 37 ед., в то время как при раке ПЖ этот показатель возрастает в десятки, а иногда в сотни и тысячи раз. К сожалению, уровень СА-19-9 при раннем раке ПЖ обычно не повышен, что существенно ограничивает применение данного метода в скрининговом исследовании на предмет выявления ранних форм рака ПЖ, даже у больных, входящих в группу риска.
Инструментальная диагностика обструктивных процессов панкреатодуоденальной зоны
Основными инструментальными методами исследования больных обструктивными заболеваниями ПДЗ являются УЗИ, эндо-УЗИ, ЭРХПГ, компьютерная томография (КТ), магнитно-резонансная томография (МРТ), позитронно-эмиссионная томография (ПЭТ), магнитно-резонансная холангиопанкреатография (МРХПТ), эндоскопическая фиброгастродуоденоскопия с биопсией, рентгенконтрастное исследование ЖКТ, фистулография, интраоперационная экспресс-биопсия, лапароскопия.
УЗИ является наиболее частым методом исследования, у многих больных – первичным методом инструментального обследования с установлением окончательного диагноза объемного обструктивного процесса в ПДЗ.
Одним из новых методов исследования является эндо-УЗИ – ультразвуковое исследование, выполняемое во время эндоскопии. Данное исследование позволяет неинвазивно диагностировать интраампулярные доброкачественные и злокачественные опухоли БДС при стандартном эндосонографическом исследовании панкреатобилиарной зоны и уже на ранних стадиях заболевания определять показания к радикальному оперативному лечению. По данным литературы, эндо-УЗИ является высокоинформативным методом уточняющей диагностики, характеризующимся превосходящей в сравнении с другими методами точностью (в оценке критерия T – 87%, критерия N – 80%, инвазии в сосуды – 95%).
ЭРПХГ является основным диагностическим методом выбора для определения уровня обтурации желчного и панкреатического протоков и уточнения диагноза. ЭРПХГ осуществляется с помощью дуоденоскопа с боковой оптикой и мобильной рентгеноскопической установкой по стандартной методике с применением водорастворимых рентгеноконтрастных препаратов (триомбраст, ультравист) (рис. 1, 2).
Читайте также:

