Неоадъювантная терапия при раке прямой кишки

Рак прямой кишки продолжает оставаться одной из наиболее актуальных проблем в современной онкологии. Он занимает положение в десятке наиболее часто встречаемых злокачественных опухолей – 5 место у мужчин и 6–7 место у женщин. Увеличение за последние 10 лет удельного веса колоректального рака в общей структуре злокачественных заболеваний в мире с 9 % до 13 % является очевидным этому подтверждением [2].
Имеются данные об эндо- и экзогенных факторах, оказывающих влияние на весь организм и его подсистемы в концепции канцерогенеза колоректального рака. Отмечено действие на орган-мишень, клеточный аппарат и микроокружение. В дальнейшем развиваются генетические мутации и неконтролируемая пролиферация клеток [8]. Особое значение имеет микроокружение в формировании колоректального рака и роль иммунологического ответа опухоли и макроорганизма [3].
Отправной точкой приложения начальной реализации опухолевых изменений являются эпителиальные клетки слизистой оболочки, разнородные по составу и функции [10]. На подавление опухолевого роста и направлена лучевая терапия. Она способствует также и подавлению циркулирующих опухолевых клеток, значению которых при колоректальном раке в последние годы уделяется большое внимание [4].
Современные технологии лучевой терапии позволяют получить высокий ответ на проводимое лечение (полная регрессия опухоли), уменьшение частоты и интенсивности острых лучевых повреждений: тяжелого раннего токсического мукозита (3–4 степени), использование объемно-модулированной лучевой терапии арками (VMA – Rapid.Arc) позволяет уменьшить время проведения одного сеанса лучевой терапии по сравнению с IMRT с 20 до 3–5 минут [6]. Химиолучевое лечение в предоперационном периоде приводит к увеличению сфинктеросохраняющих операций без увеличения числа послеоперационных осложнений, возможность получить в ряде наблюдений (до 16,6 % пациентов) полный гистологический ответ [9].
Работы последних лет убеждают, что при облучении в режиме динамического фракционирования дозы наблюдали менее выраженные лучевые реакции, как во время лечения, так и при его завершении. Повышение суммарной дозы с добавлением радиомодификаторов увеличивает частоту полных ответов при приемлемом уровне токсичности. При этом отмечено уменьшение болевого синдрома, купирование кровотечений [1,5].
Подход к лечению рака прямой кишки является мультидисциплинарным. Хирургия рака прямой кишки включает в последние годы следующие моменты: сохранение функции без ухудшения онкологических результатов и применение все более расширенных хирургических вмешательств. Лучевая или химиолучевая терапия при различных методиках фракционирования убедительно доказывает свою целесообразность [7].
Все вышеизложенное дало основание провести исследование по сопоставлению результатов лечения пролонгированной лучевой терапии и короткого курса.
Целью исследования явился анализ результатов предоперационной лучевой терапии рака прямой кишки при пролонгированном и коротком курсе.
Для решения вопроса о преимуществах короткого и пролонгированного курса лучевой терапии нами были проанализированы ретроспективные данные о 119 пациентах с резектабельным локализованным и местно-распространенным раком прямой кишки, прошедшим лечение в РНИОИ с применением современных технологий с 2013 по 2015 год.
Были поставлены следующие задачи:
- изучить переносимость пациентами лечения;
- сравнить объемы хирургических вмешательств и число послеоперационных осложнений;
- изучить непосредственные и отдаленные результаты лечения.
Больные были разделены на две группы: 67 пациентам проведена предоперационная пролонгированная химиолучевая терапия и 52 пациентам проведен предоперационный короткий курс лучевой терапии (РОД 5 Гр, 5 фракций, СОД 25 Гр). Распределение больных по полу и возрасту было сопоставимо. В группе с пролонгированным курсом ЛТ превалировали пациенты с пораженными л/узлами – почти 63 %. По гистологическому типу опухоли были представлены в большинстве случаев умеренно дифференцированной аденокарциномой. Проводилась оценка переносимости данных вариантов лечения.
Результаты и их обсуждение. В период проведения неоадъювантного лечения все пациенты удовлетворительно переносили назначенный курс, во всех случаях ЛТ была завершена в запланированном объеме. После окончания пролонгированного курса лучевые реакции наблюдались чаще и были более выраженными: в 64 % после пролонгированного курса и в 36,5 % после короткого. Однако через 6–8 недель наблюдалось купирование реакций и непосредственно к операции больные подходили с минимальным количеством их проявлений и отмечались реже в два раза, чем после короткого курса. При оценке лейкопении и анемии, в группе с пролонгированным курсом больные исходно были с худшими показателями крови: 15 % и 5,8 % соответственно. Но на фоне сопроводительной терапии и уменьшении кровотечений из прямой кишки на конец лечения состояние больных не ухудшилось. А после перерыва лейкопения и анемия III степени не отмечены. Клинический эффект от проводимой ХЛТ выражался, как правило, в значительном уменьшении, а в ряде случаев полном исчезновении, клинических симптомов опухолевого поражения прямой кишки. Наибольшая положительная динамика отмечена в группе с пролонгированным курсом в виде уменьшения болей и уменьшения кровянистых выделений. Одной из основных целей пролонгированного курса ХЛТ являлось уменьшение размеров опухоли прямой кишки.
При выполнении эндоскопического исследования после проведения пролонгированной лучевой терапии через 6–8 недель отмечалось уменьшение экзофитного компонента опухоли, вплоть до образования язвы, уменьшения протяженности опухоли и увеличение диаметра просвета прямой кишки. В группе с коротким курсом отмечался отек слизистой оболочки и незначительное уменьшение опухоли.
В группе больных с раком прямой кишки, которым проводилась пролонгированная лучевая терапия, протяженность опухоли уменьшилась в 1,7 раза. Расстояние от ануса до нижнего края опухоли увеличилось с 6,3 см до 7,6 см. А при проведении короткого курса лучевого лечения протяженность опухоли и расстояние до нижнего края опухоли остались прежними или изменения расстояния не происходило. В группе с локализацией опухоли в нижнеампулярном отделе после пролонгированного курса лучевой терапии в процессе лечения медиана расстояния от Z-линии увеличивалась в 2,5 раза, что давало возможность обеспечить условия для выполнения большего числа сфинктерсохраняющих вмешательств. По данным МРТ-исследования лечебный патоморфоз выражался в виде уменьшения опухоли и нарастания фиброзной ткани, увеличение расстояние от края опухоли до мезоректальной фасции, в сокращении метастатических л/у. При оценке клинических результатов по данным МРТ-исследования через 6–8 недель после завершения ХЛТ полный клинический регресс был достигнут у 14,9 % пациентов. Частичный регресс выявлен в 56,7 % случаев, стабилизация в 28,4 %. После завершения курсов лучевой терапии, как пролонгированной, так и короткофокусной выполняли оперативные вмешательства. При сравнении объемов оперативного вмешательства у больных с локализацией опухоли в нижнеампулярном отделе сфинктеросохраняющие операции в группе с пролонгированной химиолучевой терапией были выполнены в 26 % случаев, в группе с коротким курсом в 6 %. В процессе выполнения хирургического этапа лечения каких-либо особенностей в сравниваемых группах не отмечено. При анализе особенностей послеоперационного периода общее количество осложнений в сравниваемых группах практически не отличалось – 15,6 % и 13,5 % соответственно.
Таким образом, проведение различных вариантов предоперационного лечения не выявило различий влияния на течение репаративных процессов. Доказательством проводимой терапии явилось морфологическое исследование операционного материала. Морфологические изменения в группе больных с коротким курсом сводились к некробиотическим и дистрофическим процессам в опухоли, незначительной десмопластической реакции стромального компонента. Сохранялся высокий пролиферативный (Ki-67) и апоптический (p 53) потенциал опухоли. Патоморфоз опухоли на проводимое лечение I–II степени достигал 95 %.
Длительный курс ХЛТ вызывал в опухоли значительные изменения, которые заключались в некробиотических и дистрофических и апоптатических процессах, выраженной воспалительной реакции, обширных очагах развития фиброзной ткани на месте опухоли, замещающей паренхиматозный компонент. Маркер пролиферативной активности Ki 67 и апоптотический индекс Р53 были снижены (рис.1).

Рис. 1. Патоморфоз после пролонгированного курса: А – экспрессия Ki-67,
Б – экспрессия Р 53
В фиброзной ткани наблюдали образование петрификатов. (рис. 2). Патоморфоз достигал IV степени в 17 % наблюдений и в 72 % случаев – III степени.
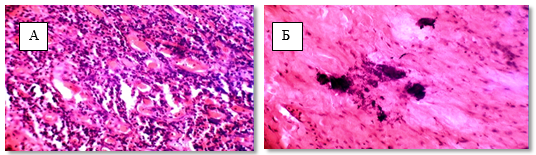
Рис. 2. Патоморфоз после пролонгированного курса: А – 4 степень стромальный компонент, Б – 4 степень петрификаты
Учитывая сроки проведения операции после крупных фракций, незначительное повреждающее действие лучевой терапии, была проведена ДНК-цитометрия.
Исследование ДНК-цитометрии удаленных во время операции опухолей прямой кишки, показало значительное снижение злокачественного потенциала опухоли после крупнофракционной лучевой терапии, определяемое по достоверному снижению темпа пролиферации клеток опухоли вследствие снижения доли клеток в S-фазе и снижению в 1,6 раза индекса пролиферации опухоли.
После пролонгированной лучевой терапии не обнаружено столь выраженных изменений при ДНК-топометрическом анализе, что, вероятно, обусловлено исследованием через 6–8 недель после окончания лечения. К этому времени, по всей видимости, уже происходит восстановление пролиферативной активности оставшихся после лучевой терапии опухолевых клеток. Эти данные свидетельствуют о недопустимости превышения интервалов между этапами лечения.
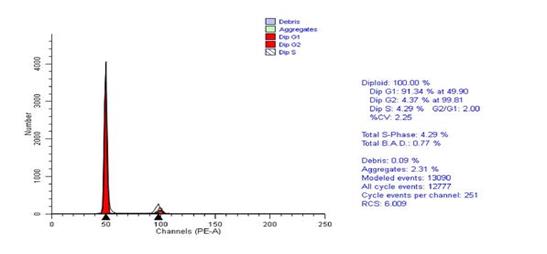
Рис.3. Гистограмма распределения по фазам клеточного цикла. Короткий курс
о недопустимости превышения интервалов между этапами лечения.
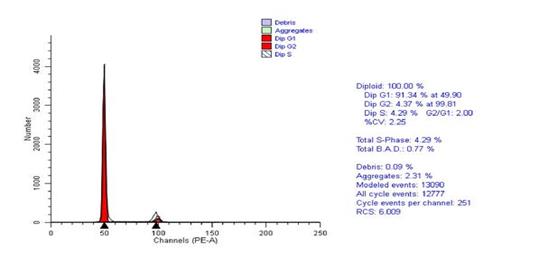
Рис. 4. Гистограмма распределения по фазам клеточного цикла. Пролонгированный курс
Общее число рецидивов в группе с пролонгированной ЛТ составило 6,25 %, в группе с коротким курсом 6,5 %.
Больше половины рецидивов в обеих группах составили опухоли, локализующиеся в нижнеампулярном отделе. Из пациентов с опухолями нижнеампулярного отдела в группе с пролонгированной лучевой терапией (27 пациентов) отмечено 7,4 % рецидивов. В группе с коротким курсом лучевой терапии в 11,8 % случаев отмечены рецидивы с опухолями нижнеампулярного отдела в сроки от 12 до 15 месяцев. В этих наблюдениях у больных были опухоли с исходными метастазами в регионарных л/у. Отдаленные метастазы были диагностированы у 4,7 % пациентов в группе с ПЛТ, у 6,5 % в группе с КЛТ в сроки от 13 до 35 месяцев. Все пациенты имели подтвержденные исходно метастазы в регионарных лимфатических узлах.
Несмотря на тенденцию к увеличению применения неоадъювантной пролонгированной ХЛТ, короткий курс лучевой терапии не дает худшие результаты лечения. Последнее обстоятельство находит свои доказательства в отсутствии существенных различий в показателях безрецидивной выживаемости и отдаленного метастазирования, послеоперационных осложнений. Дифференцированное применение того или иного подхода зависит от целей предоперационного лечения.
Заключение. Таким образом, проведенное исследование позволяет сделать следующее заключение о целесообразности применения того или иного курса предоперационного лечения.
Пролонгированная лучевая терапия показана:
- Пациентам с опухолями, требующим регресса.
- Пациентам с опухолями, локализующимися в нижнеампуллярном отделе, так как дает возможность проведения сфинктеросохраняющих операций и отмечается меньшее количество рецидивов при данной локализации.
- Пациентам с Т4, а также при пораженных лимфатических узлах с любым Т.
Короткий курс крупнофракционной лучевой терапии показан:
- Пациентам с опухолями Т3N0, не требующим регресса, когда предоперационной лечение не может повлиять на объем хирургического вмешательства.
- Пациентам, которым невозможно проведение пролонгированного курса.

Рецензент материала
Профессор Капранов С.А. — Доктор медицинских наук, дважды Лауреат Государственных Премий Правительства Российской Федерации в области науки и техники, Лауреат Премии Ленинского Комсомола, автор более 350 научных работ по медицине, 7 монографий, и 10 патентов на изобретения по медицине, за 30 лет личного опыта провел более чем 10 000 различных эндоваскулярных операций
По числу смертности рак прямой кишки занимает 2-е место среди женщин, и 4-е среди мужчин по всему миру. За несколько последних лет распространенность онкологической болезни постепенно возрастает, ранее данное заболевание встречалось среди людей старше 60, сейчас злокачественные болезни прямой кишки можно обнаружить у сорокалетних.
Ведущим методом терапии рака прямой кишки является хирургическое вмешательство. Химиотерапия назначается в рамках комбинированного способа при метастатической или местно распространенной форме болезни. Химиотерапия при раке прямой кишки используется для достижения нескольких целей:
- системное действие на новообразование для уменьшения или полного уничтожения метастазов, сюда также относятся микрометастазы, которые могут сейчас не диагностироваться;
- замедление роста опухолей на максимально долгое время;
- перевод неоперабельных опухолевых узлов в резектабельное состояние для дальнейшего удаления.
Долгое время во время лечения онкологии использовался 5-флорурацил. Препарат и сейчас не утратил свою популярность, но он назначается совместно с прочими лекарствами – медикаменты платины 3-го поколения – Оксалиплатин, антагонистами пиримидинов – Капецитабин, а также камптотецинами – Иринотеканом.
Разновидности химиотерапии
Назначение адъювантной химиотерапии происходит после радикального оперативного вмешательства при местно распространенных опухолях или, когда есть региональные метастазы. Длительность лечения рака в данном случае составляет не меньше 6 месяцев.
Минимальным вариантом химиотерапии являются схемы с добавлением фторпиримидинов. Зачастую назначается схема, предполагающая использование Лейковарина совместно с Фторурацилом. Лекарства вводятся на протяжении 5 дней, после делаются паузы. Следующий курс начинается на 29 день. Подходящий вариант послеоперационной терапии это введение Оксалиплатина совместно с фторпинимидинами по схемам FOLFOX или же XELOX. Если во время подобной терапии проявляются признаки нейротоксичности, то требуется отменить медикаменты платины и продолжать монотерапию с использованием фторпиримидинов. В это время не требуется назначение таргетной терапии моноклональными антителами. Принцип таргетной терапии основывается на том, что лечение осуществляется за счет воздействия на молекулярные мишени, играющие главную роль во время патогенеза злокачественной опухоли.
Использование неоадъювантной терапии показано для метастатических и диссеминированных видов болезни. Иссечение метастазов хирургическим методом позволяет значительно улучшить прогноз пациентов и повысить на 30-40% пятилетнюю выживаемость. В случае радикального удаления показатель выживаемости можно увеличить до 60%. Радикальное оперативное вмешательство у пациентов на 4 стадиях удается провести только на 10-20% больных, у оставшихся случаях диагностируется неоперабельность. Таким пациентам начинается неоадъювантная терапия. Она необходима для повышения резектабельности опухоли и/или продления жизни пациента. Данную химиотерапию проводят по нескольким схемам FOLFIRI, FOLFOX или же XELOX.
Сейчас данный метод используется во время комбинированного лечения до операции и на послеоперационном этапе. Проводится дистанционное лучевое лечение при разовых дозах 2 Гр до общей очаговой дозы на область с региональными метастазами 44 Гр, на новообразование отводится 50-60 Гр, в зависимости от того, где локализируется опухоль и степени ее распространения. Облучение осуществляется курсами по 5 дней, между которыми перерывы в 2 дня. Данный процесс сопровождается химиотерапией с использованием фторпиримидинов или же с Оксалиплатином.
Лечение химическими препаратами в зависимости от стадии
Лечение рака прямой кишки во многом зависит от стадии заболевания:
- Злокачественные новообразования на первой стадии проростают в глубокие стенки, но еще остаются в прямой кишке. Сюда относятся раковые опухоли, которые переродились из доброкачественных полипов. Химиотерапию в данном случае назначают, если в ходе операции врач выявил, что рак распространился сильнее, чем предполагалось. Из медикаментов используется Капецитабин и Фторурацил.
- Опухоли на 2 стадиях прорастают сквозь стенки кишечника, внедряясь в ткани, расположенные поблизости. На данном этапе болезнь еще не распространяется на лимфатические узлы. Большинству больным раком прямой кишки требуется терапия химическими препаратами. После операции назначают дополнительную химиотерапию, длящуюся в сумме полгода. Пациенту может назначаться схема FOLFOX (Оксалиплатин, Фторурацил и Лейковорин), Фторурацил в сочетании только с Лейковорин, CapeOx (назначается Капецитабин в комбинации с Оксалиплатином), или же монотерапия Капецитабином.
- Для рака прямой кишки 3 стадии характерны злокачественные образования, распространившиеся в ближайшие лимфоузлы, но их нет в других частях тела. Химиотерапию назначают после операции, ее продолжительность составляет полгода. Врачи назначают такие же протоколы лечения, что и при вторых стадиях заболевания. Есть альтернативный вариант – изначально пациент принимает только химиотерапические средства, а затем следует химиолучевое лечение.
Вылечить 4 стадию заболевания достаточно сложно, в данном случае злокачественные опухоли распространяются в других отдаленных органах и тканях – печень, легкие и прочие. Методики борьбы с раком прямой кишки могут быть разными, все зависит от сложности патологии. Если рак операбелен и все следы болезни можно устранить при помощи хирургического вмешательства (к примеру, диагностировано только несколько опухолей в легких и печени), то может использоваться:
- Хирургическое вмешательство для удаления новообразования и отдаленных метастазов, после которого назначают химиотерапию. В некоторых случаях может добавляться и лучевое лечение.
- Курс применения химических препаратов с последующей операцией для удаления отдаленных метастазов и самого злокачественного образования. Как правило, после завершения операции дополнительно назначают химиолучевую терапию.
- Использование химиотерапевтических средств, затем химиолучевая терапия и после операция для вырезания опухоли прямой кишки и метастазов. Также после операции могут назначать дополнительную химиотерапию.
- Прием химических средств, лучевое лечение и дальнейшее хирургическое вмешательство. После операции также может назначаться повторный цикл химиотерапевтических веществ.
Вышеперечисленные методы борьбы с раком прямой кишки позволяют повысить выживаемость пациентов, а в некоторых случаях и полностью исцелить недуг. Если обнаруживаются вторичные очаги поражения заболеванием только в печени, то врач назначает химиотерапию, при этом препараты вводят напрямую по артерии, которая ведет к печени – инфузия в печеночной артерии. Во время поступления химиотерапевтических средств прямо через кровоток сразу в печень достигается более выраженный положительный эффект, нежели при пероральном использовании препаратов или внутривенном введении.
Также на четвертых стадиях может диагностироваться неоперабельность опухоли. Если образование более распространено и не подлежит хирургическому удалению, то лечение зависит от отсутствия или наличия кишечной непроходимости. Если она есть, то требуется срочная операция. Если нет, то с раком начинают бороться при помощи химических препаратов, также эффективность проявляет таргетная терапия.
Как должны питаться пациенты, проходящие химиотерапию?
Во время борьбы с раком пациент должен соблюдать сбалансированный рацион питания. Грамотно подобранный рацион позволит укрепить иммунитет, даст организму возможность справиться с тяжелыми последствиями лечения онкологии, восстановить силы и защититься от инфекционных заболеваний. Пациентам, у кого диагностирован рак прямой кишки, в дневной рацион нужно добавить:
- растительное масло – кунжутное, оливковое и прочие;
- морепродукты;
- травяные чаи;
- каши и цельнозерновой хлеб;
- нежирную кисломолочную пищу;
- чеснок;
- нежирное мясо – птицу или кролик;
- фрукты;
- паровые, тушеные, отварные или просто свежие овощи (особенно полезной будет капуста брокколи, поскольку ее добавление в пищу показано именно при этом заболевании).
Больным раком стоит отказаться от сладостей, фастфуда, крепкого чая и кофе, алкогольных напитков, жирного мяса, рыбы и молочных продуктов, кетчупа и майонеза, газированной воды и пакетированного сока, соленых, жаренных, копченых и консервированных блюд.
Какие последствия имеет химиотерапия рака прямой кишки?
В борьбе с заболеванием используются сильнодействующие химические препараты с высоким уровнем токсичности, которые могут существенно ухудшить самочувствие больного. Пациенты, проходящие химиотерапию, могут столкнуться со следующими осложнениями:
- Приступы тошноты и рвоты. Для купирования или устранения данных симптомов используются разнообразные антиэметики, к примеру, блокаторы серотонина, Дексаметазон и прочие.
- Диарея. Регидрационная терапия позволяет восполнить дефицит жидкости, для устранения признаков диареи может использоваться Лоперамид или Аттапульгим, снизить болевой синдром помогут анальгетики и спазмолитики.
- Мукозит – специфический воспалительный процесс во рту. Чтобы его устранить используется дезинфицирующий раствор местного действия, ранозаживляющие и обволакивающие препараты совместно с анальгетиками.
- Дерматотоксичность – выражается в форме очагов высыпаний, зуда или гиперпигментации. Могут наблюдаться симптомы ладонно-подошвенного синдрома с отечностью, покраснением, зудом на коже рук и стоп. При данном побочном эффекте необходимо снизить дозы химии или отменить их прием.
- Миелотоксичность. Угнетение кроветворения требует коррекции дозировок цитостатиков.
В любом случае, курсы использования химических препаратов не проходят бесследно, поэтому нужно быть готовым к многочисленным негативным реакциям.
Как определяется эффективность лечения рака прямой кишки?
Перед тем как начать химиотерапию проводится сканирование, следующее делается спустя 3 месяца. Проводятся измерения величины опухоли, поэтому через время определяется эффективность терапии. Может быть несколько вариантов:
- опухоль уменьшилась в размерах;
- образование осталось такого же размера;
- возросло.
Если размеры опухоли остались на месте, то доктор консультирует больного о дальнейшем лечении – стоит его продолжать или нет. Если же она уменьшилась в объеме, то необходимо проводить химиотерапию еще 4-6 месяцев. Лечение длиться, пока не появится слишком большое количество негативных реакций, после можно остановить лечение на время. Как правило, раз в 2 или 3 месяца делается КТ, МРТ или УЗИ для определения эффективности.
Если наблюдается прогрессирование рака прямой кишки, то лечение химическими средствами прекращается и пациенту советуют другой метод.
Методы борьбы с рецидивирующим раком
Рецидив ракового заболевания – это повторное развитие опухоли, после того как пациент прошел химиотерапию или любой другой метод лечения. Зачастую рецидивы случаются в первые 2-3 года после хирургического вмешательства, но в некоторых ситуациях рецидив заболевания может встретиться более позднее. Опухоль может рецидивировать рядом с тем местом, где располагалось первичное новообразование (местно) или же локализироваться в других отдаленных внутренних тканях и органах – печень, легкие:
- Местные рецидивы. Если рецидив заболевания обнаруживается в тазовой полости (местно), злокачественные раковые клетки по возможности стремятся удалить при помощи хирургической операции. Подобное оперативное вмешательство носит более обширный характер, нежели первичное. В некоторых случаях во время операции может осуществляться лучевая терапия, но также процедуры облучения могут назначаться уже после того, как произошло удаление злокачественных клеток. Также после операций могут прописываться химиотерапевтические препараты.
- Системные рецидивы. Когда опухоль проявляется на отдаленном внутреннем органе, в данной ситуации все зависит от того, удастся ли удалить злокачественные клетки хирургически. Если злокачественное новообразование невозможно вырезать с использованием хирургического вмешательства, то пациенту назначают химиотерапию или прописывают лечение таргетной терапией. Для удаления недоброкачественных опухолей, характеризующимися определенными характеристиками по итогам лабораторного исследования, врачи могут назначать прием ингибиторов контрольных точек иммунного ответа – Ниволумаб или же Пембролизумаб. Схема борьбы с заболеванием зависит от прошлых методов терапии и общего самочувствия больного. Если новообразование не уменьшается в размерах, то онколог назначает другое сочетание химических препаратов.
Чтобы выявить первые признаки рецидива и своевременно отреагировать на них химиотерапией или прочими способами борьбы с недугом, нужно регулярно проходить обследования и консультации с лучащим онкологом.
Даже в настоящее время единственным методом лечения опухолей прямой кишки является проведение операции. Однако с последние десятилетия в практику онкологов прочно внедрилось применение химитерапевтических препаратов, которые обладают выраженным эффектом, увеличивая среднюю выживаемость. Они способны как уничтожать атипичные клетки, так и замедлять их рост, поэтому их активно используют также для профилактики рецидивов и метастазирования процесса.
Разновидности химиотерапии

Использование химиотерапевтических средств необходимо обычно на 3-4 стадиях онкологического забоелвания. Это позволяет не только замедлить ее распространение, но в некоторых случаях даже достигнуть значительной регрессии.
Применяют следующие виды химиотерапии:
- Неоадъювантная;
- Адъювантная;
- Паллиативная
Химиотерапевтическое лечение онкологии происходит под контролем соответствующего врача-специалиста, который подбирает необходимые препараты и рассчитывает дозу. Он также решает вопрос о том, где больной будет получать терапию – в стационаре или на дому.
Такой вид химиотерапии проводится довольно редко. Он предназначен для стабилизации опухолевой прогрессии и возможно некоторого уменьшения размеров новообразования. В особых случаях врач может назначить ее на 2 стадии с целью замедления роста клеток. Препараты вводят внутривенно, обычно в условиях онкологического диспансера. Это необходимо для контроля за состоянием больного и возможного оказания помощи, если оно резко ухудшится.
Проведение химиотерапии в предоперационном периоде часто способствует улучшению локорегионального контроля (делает более четкими границы опухоли) на 3-4 стадиях, также угнетая возможное метастазирование. В связи с этим повышаются шансы на выполнение сфинктеросохраняющих оперативных вмешательств.
Основной целью адъювантной терапии при раке кишечника является уничтожение отдаленных метастатических очагов, что увеличивает продолжительность безрецидивного периода и, соответственно, жить больных.
Всем больным, у которых после операции имеется стадия T1-4 N1-3 N0 проведение курсов химиотерапии является обязательным. Лечение назначают не позже 45 дней с того момента, как было выполнено хирургическое вмешательство, с контролем раково-эмбрионального антигена (онкомаркер) каждые 3 месяца в течение 1 года.
Также медикаментозное лечение необходимо получать, если имеются следующие факторы, ухудшающие прогноз:
- Глубокая инвазия опухоли на всю толщу кишки;
- Низкая дифференцировка раковых клеток;
- Молодой возраст больного;
- РЭА превышает норму через 4 недели после оперативного вмешательства.
Паллиативную химиотерапию выполняют как самостоятельный вид лечения в следующих случаях:
- Неоперабельный рак прямой кишки (прорастание в брюшину и соседние органы, генерализованный метастатический процесс);
- С целью улучшения самочувствия больного при невозможности оперативного лечения;
- Контроль роста опухоли в течение средней медианы выживаемости при нерезектабельном раке (около 20 месяцев);
- Быстрый рецидив опухоли (прогностически неблагоприятный фактор), массивное метастазирование.
Решение о получении паллиативной помощи определяется тяжестью состояния больного или его личным согласием при наличии показаний.
Основные препараты
Медикаментозные препараты для проведения курсов химиотерапии должны отвечать следующим требованиям:
- Цитотоксичность – возможность уничтожения раковой клетки;
- Цитостатичность – замедление роста опухолевой ткани.
К сожалению, большинство таких препаратов не являются высокоспецифичными. Они воздействуют на клетки с активным делением. Прежде всего к ним относятся опухолевые, но параллельно страдают здоровые ткани (желудочно-кишечного тракта, костного мозга, кожи, слизистая оболочка рта и другие).
Наибольшее применение нашли такие группы медикаментов:
- Непрямые ингибиторы тимидилат синтетазы (фторпиримидины);
- Прямые ингибиторы тимидилат синтетазы;
- Ингибиторы топоизомеразы I;
- Аналоги производных платины
Осложнения от применения 5-ФУ различны, что зависит от дозировки, режима и способа введения препарата. Наиболее частые токсические эффекты – угнетение костного мозга (миелосупрессия), диарея и мукозит.
Также необходимо учитывать, что при получении длительных инфузий 5-ФУ нужна постановка центрального катетера. Само это мероприятие опасно ввиду развития ряда осложнений (тромбоз, присоединение вторичной инфекции, кровотечение).
Это послужило причиной разработки фторпиримидинов для применения внутрь (перорально) пролонгированного действия, что имитирует непрерывную инфузию. К ним относятся следующие представители:
При сравнении действия и вероятности появления осложнений этого препарата с 5-ФУ выяснилось, что он обладает сопоставимой результативностью. В некоторых случаях проводится коррекция изначальных дозировок, что связано с развитием следующих эффектов:
- Повышение печеночных трансаминаз (АЛТ, АСТ) в 13%;
- Прибавка массы тела более чем на 5%;
- Улучшение общего состояния;
- Снижение выраженности клинических проявлений.
Использование этого цитостатика как монопрепарата позволяет увеличить выживаемость больных до 45%, тогда как при терапии 5-ФУ она составляет 32%
Схемы лечения
Проведение радикальных операций при раке прямой кишки чаще всего сопровождается химиотерапией. Это обосновано в первую очередь тем, что на 3-4 стадиях поражения практически в 1/3 случаев уже имелись метастазы с субклиническим (стертым) течением.
Химиотерапия при раке прямой кишки назначается в таких формах:
- В качестве адъювантной после операции;
- В составе комбинированной терапии с хирургическим вмешательством и лучевой;
- В качестве самостоятельного (паллиативного) метода лечения.
Каждая схема имеет свои особенности введения, дозировки и чередования препаратов. Эти параметры устанавливаются также в индивидуальном порядке конкретному больному ввиду прогностического риска развития тех или иных осложнений.
Читайте также:

