Лучевой пневмонит лечение при раке молочной железы
В последние годы отмечены определенные положительные сдвиги в результатах лечения больных со злокачественными опухолями; при этом свыше 50% пациентов практически излечиваются. Достижения современной клинической онкологии прежде всего связаны с ранним выявлением злокачественной опухоли и совершенствованием мультимодальной терапии с использованием современных методов лечения - хирургического, лучевого, лекарственного и иммунологического.
Посттерапевтические пульмониты (ПП) сопровождаются выраженными клиническими проявлениями, ухудшают качество жизни больных и требуют назначения соответствующей лекарственной терапии. Учитывая, что в результате лучевого (химиолучевого) лечения рака легкого полная резорбция новообразования наступает у 10-86% больных в зависимости от морфологического строения опухоли и методики терапии, во многих случаях сохраняется остаточная опухоль [1, 4]. Поэтому крайне важно тщательно дифференцировать посттерапевтические повреждения легочной ткани и остаточную опухоль или рецидив. В диагностике и дифференциальной диагностике ПП и рака легкого ведущее значение имеет рентгенологический метод.
Появившиеся в последнее время новые технологии медицинской визуализации: рентгенодиагностические комплексы с цифровой обработкой изображения, многосрезовая компьютерная томография (КТ) с высоким разрешением позволяют обнаружить тонкие структурные изменения легочной паренхимы и бронхиального дерева, идентифицировать ранние признаки повреждения легких, провести четкую дифференциальную диагностику.
В НИИ онкологии и медицинской радиологии им. Н.Н. Александрова выполнены исследования с целью разработки алгоритма дифференциальной диагностики ПП и РЛ. При этом вначале изучены результаты обследования 207 больных (рак легкого - 127 человек, лимфогранулематоз - 31, рак молочной железы - 61), получавших ЛТ на область грудной клетки с захватом ткани легкого. Это позволило уточнить имеющиеся данные по рентгеносемиотике ПП и предложить при обследовании больных РЛ после курса лучевой/химиолучевой терапии последовательность рентгенологического исследования с целью дифференциации пульмонита и резидуальной опухоли или рецидива рака легкого.
Схема обследования предусматривает 3 этапа визуализации, так как проходя последовательные стадии развития, постлучевой пульмонит имеет различную рентгенологическую картину.
На I этапе спустя 1,5-2 месяца после завершения ЛТ выполняется стандартное рентгенологическое исследование.
Характерными рентгенологическими признаками пульмонита на этом этапе, по нашим данным, являются: небольшая деформация легочного рисунка и/или наличие малоинтенсивных очаговых теней без четких контуров. Изменения локализуются в прикорневой области, а также в задних сегментах легкого (SII, VI, X), что соответствует полям облучения. Невыраженное подтягивание корня легкого кверху, незначительная приподнятость купола диафрагмы, едва заметное смещение тени средостения в сторону поражения может свидетельствовать о возникновении пульмонита и раннем фиброзировании легочной паренхимы. Однако эти симптомы также имеют место и при объемном уменьшении легочной ткани, обусловленном нарушением проходимости бронха, т.е. сдавлением или обтурацией его просвета опухолью. Дифференцировать эти два патологических состояния по данным стандартной рентгенографии, как правило, затруднительно. Линейная томография в 80% случаев позволяет определить состояние бронхов - их проходимость, ширину просвета, а также оценить степень регрессии опухоли.
При использовании этой технологии дополнительно выявляются важные рентгенологические симптомы пульмонита: периваскулярная (усиление, обогащение легочного рисунка) и перибронхиальная (утолщение стенок и нечеткость контуров сегментарных и субсегментарных бронхов) инфильтрация, уплотнение межуточной ткани, а также формирование нежной фиброзной тяжистости, обеднение бронхососудистого рисунка в плащевом слое легкого.
Уменьшение размеров тени опухоли по сравнению с исходной, а также восстановление проходимости бронхов, выявляемые на DFR-томограммах, позволяют с наибольшей вероятностью рассматривать указанные изменения в легком как признаки пульмонита и дифференцировать с нарастающей гиповентиляцией вследствие продолжения роста опухоли легкого и обтурации просвета бронха.
Методика КТ с высоким разрешением позволяет более точно оценить состояние паренхимы легкого в кортикальном и медуллярном слоях, выявить проходимость сегментарных и субсегментарных бронхов, наличие перибронхиальной опухоли.
В инфильтративной (ранней) фазе пульмонита затемнение в кортикальном слое может быть однородным (безвоздушный участок) либо неоднородным при частично сохраненной воздушности. Изменения в медуллярном слое проявляются перибронховаскулярной инфильтрацией.
На III этапе рентгенологическое исследование выполняется через 6 месяцев и в более поздние сроки по мере явки больного на контрольное обследование. На стандартных рентгенограммах определяется заметное уменьшение объема легкого вследствие фиброзных изменений. Ткань легкого неоднородно затемнена, корень его гомогенизирован, подтянут кверху, купол диафрагмы значительно приподнят, подвижность его при дыхании ограничена. Тень средостения смещена в сторону поражения. Кроме того, выявляется плевральная реакция в виде плевральных наслоений, плевродиафрагмальных спаек.
Реконструкция томограмм с помощью специального алгоритма высокого разрешения позволяет точно разграничить тень опухоли (узловатая форма, солидная плотность, бугристые контуры) и неравномерный фиброз с участками просветления, которые являются отображением поперечного сечения расширенных бронхов и вздутых альвеол. При этом в медуллярном слое превалируют расширенные бронхи, а в кортикальном - вздутые альвеолы.
Завершающим моментом на всех этапах дифференциальной диагностики при подозрении наличия в легком опухоли является бронхоскопия со взятием материала для морфологического исследования.
Таким образом, предложенная схема диагностики позволяет дифференцировать ПП и рецидив РЛ или остаточную опухоль, а благодаря своевременному и правильно установленному диагнозу и адекватной терапии можно избежать серьезных ошибок в дальнейшем лечении пациентов.
1. Артемова И. А., Муравская Г.В., Минайло И.И. Неоперируемый эпидермоидный рак легкого: традиционный или нетрадиционный варианты облучения? // Актуал. пробл. онкол. и мед. радиол. - Мн., 2002. - С. 283-294.
2. Голдобенко Г. В., Канаев С. В. Современные проблемы радиационной онкологии // Вопр. онкол. - 1997. - № 5. - С. 481-487.
3. Иваницкая В.И., Кисличенко В.А., Геринштейн И. Т. Лучевые повреждения легких: Осложнения лучевой терапии у онкологических больных. - М., 1989. -132 с.
4. Козлов AM., Москалик К.Г., Афанасьев Б.П., Байкова B.C. Тактика лучевой терапии при лечении мелкоклеточного рака легкого // Мед. радиол. и радиац. безопасность. - 2003. - № 5. - С. 73-82.
5. Лучевая терапия злокачественных опухолей: Рук-во для врачей / Е. С. Киселева, Г. В. Голдобенко, С. В. Канаев и др.; Под ред. Е.С Киселевой.- М.: Медицина, 1996.- 464 с.
6. Мус В.Ф. Лучевая терапия неоперабельного рака легкого: Автореф. дис. д-ра мед. наук: - СПб., 1997. - 41 с.
7. Forrest L. J., Mahler P. A., Vail DM. et al. Computed tomographic evaluation of radiation pneumonitis in a canine model // Radiat. Oncol. Investig. - 1998. - № 6.- P. 128-134.
Кузнецова Т.Д., Минайло И. И., Артемова Н. А, Муравская Г.В., Голуб Г.Д., Серова Т.Н.
НИИ онкологии и медицинской радиологии им. Н.Н. Александрова.

Несмотря на совершенствование средств и методик облучения при (лучевом) лечении опухолей грудной полости и рака молочной железы, т.е. когда в зону облучения попадает ткань легкого, в ряде случаев развиваются лучевые повреждения легких. Это обусловлено тем, что реализация современных радикальных программ дистанционной лучевой терапии, предусматривающих необходимость облучения относительно больших объемов тканей и подведения к опухоли высоких уровней поглощенных доз, неизбежно проводится на грани толерантности нормальных органов, что не исключает риска развития постлучевых повреждений. Одним из наиболее частых осложнений лучевой терапии является постлучевой пневмонит. Частота встречаемости варьирует от 15,4 до 61% случаев, причем у 3,7% пациентов заболевание является причиной смерти (Н.Л. Семищева и соавт., 2014).
Лучевые повреждения легких возникают в связи с тем, что толерантность легочной ткани к лучевым воздействиям находится в пределах 35 - 40 Гр, а при лечении злокачественных опухолей используют суммарные очаговые дозы около 60 - 80 Гр. В ходе лучевого воздействия на первом этапе поражаются клетки альвеолярного эпителия и эндотелия капилляров: в результате повреждения альвеолоцитов II типа уменьшается синтез сурфактанта, повышается поверхностное натяжение альвеол, происходит спадение альвеолярных стенок; повреждение эндотелиальных клеток капилляров, ведет к тромбообразованию, изменению тонуса сосудов и обструкции просвета сосуда.
В настоящее время общепринято лучевые повреждения делить на ранние и поздние. К ранним лучевым повреждениям относят любые лучевые повреждения легких, развившиеся в процессе облучения или на протяжении первых трех месяцев после окончания лучевой терапии. Развитию более ранних и выраженных постлучевых повреждений легких способствуют: проведение повторных курсов лучевой терапии, пневмосклерозы, хронические воспалительные процессы и ателектазы легочной ткани, пожилой возраст больных. К поздним лучевым повреждениям относят любые патологические изменения в облученной зоне легкого, развившиеся спустя три месяца после лучевой терапии. В этот период чаще всего наблюдается развитие фиброзно-склеротических процессов структурных элементов легкого.
На основе классификации Г.А. Зедгенидзе (1962), М.С. Бардычев и А.Ф. Цыб (1985) предложили следующую классификацию лучевых повреждений легких:
I. Ранние лучевые повреждения.
-
1. Острая лучевая пневмония (острый лучевой пневмонит):
1.1. с преобладанием повреждения альвеолярной системы (очаговая инфильтрация);
1.2. с преобладанием перибронхиально-периваскулярных изменений (интерстициальная инфильтрация);
1.3. с развитием массивных инфильтратов (сливная инфильтрация);
1.4. с развитием долевого и субдолевого отека.
2. Первично-хроническая лучевая пневмония.
3. Вторично-хроническая лучевая пневмония.
-
1. Поздняя лучевая пневмония (поздний лучевой пневмонит).
2. Поздний лучевой фиброз I-III степени.
-
0 - нет изменений;
1 - слабые симптомы сухого кашля или одышки при нагрузке;
2 - постоянный кашель, требующий наркотических противокашлевых средств, одышка при минимальной нагрузке, но не в покое;
3 - сильный кашель, не купируемый наркотическими противокашлевыми средствами, одышка в покое, рентгенологическое выявление острого пневмонита, периодическое назначение кислородотерапии и стероидов;
4 - выраженная дыхательная недостаточность, длительная кислородотерапия или вспомогательная искусственная вентиляция легких.
Диагностика основывается на данных анамнеза о проводившейся радиационной терапии, площади и локализации облученного поля легких, числе сеансов и их продолжительности. Важным признаком служит односторонность поражения. Следует учитывать также общие симптомы лучевой реакции: слабость, головную боль, потерю аппетита, раздражительность, различные расстройства сердечно-сосудистой системы, лейкопению, тромбоцитопению и пр., которые нередко предшествуют местным легочным проявлениям лучевого воздействия. Диагноз осложняется в случае присоединения вирусных и бактериальных (вторичных) пневмоний, возникающих вследствие подавления иммунологической защиты организма ионизирующей радиацией. Постлучевые повреждения необходимо дифференцировать с метастатическим поражением легочной ткани, возникающем при прогрессировании основного заболевания. Следует помнить и о лекарственных пневмонитах, возникающих при токсическом поражении легочной ткани лекарственными препаратами, обладающими пневмотропным токсическим действием. КТ (компьютерная томография) высокого разрешения позволяет идентифицировать ранние признаки повреждения легких и провести четкую дифференциальную диагностику.
Лечение в острую стадию лучевых реакций легочной ткани заключается в приеме кортикостероидов, антибиотиков, антикоагулянтов, которые назначаются ввиду угрозы тромбоза легочных капилляров. Благоприятное действие кортикостероидов проявляется уже к 3 - 4-му дню лечения, воспалительный процесс постепенно стихает. Однако если в указанный срок положительный эффект гормональной терапии отсутствует, дальнейшее применение кортикостероидов бесполезно и, постепенно снижая дозу, их следует отменить. Назначение кортикостероидов и антибиотиков в период проведения лучевой терапии не предотвращает развитие патологического процесса. Также имеет значение наблюдение за общим состоянием больного – прекращение облучения при появлении стойкой лейкопении и тромбоцитопении, а также при появлении кашля и кровохарканья. Лечение постлучевого фиброза легких - сложное и продолжительное занятие. Важно понимать, что поврежденные радиацией участки легких функционально уже не восстановятся. Поэтому лечение направлено на сохранение здоровых участков и повышение эффективности их работы.
1. С целью снижения частоты развития постлучевых пульмонитов наиболее целесообразным является выполнение следующих рекомендаций: лучевую терапию по радикальной программе у больных раком легкого предпочтительно проводить с использованием тормозного излучения 20-42 МэВ и метода динамического мультифракциониро-вания с малой "сенсибилизирующей" дозой.
4. При невозможности применения разработанного комплекса лечебных препаратов в полном объеме приемлемо использование отдельных его компонентов, наиболее эффективными из которых являются сочетание солкосерила и антибиотиков, а также - ЭОАК и антибиотиков.
Это повреждение лёгочной ткани, развивающееся под действием высоких доз ионизирующей радиации. Он относится к локальным радиационным поражениям лёгочной паренхимы.Частота встречаемости варьирует от 15,4 до 61% случаев.

Пусковым механизмом служит превышение толерантной дозы радиоактивного воздействия на лёгочную ткань. В ходе лучевой терапии в фокус облучения попадает зона лёгкого с предельной переносимостью 35-40 Гр, вследствие чего развиваются радиационные поражения.
Частота возникновения, течение патологического процесса напрямую зависят от величины суммарной очаговой дозы.
Возраст пациента
Согласно исследованиям, больные старше 70 лет страдают от осложнений радиотерапии в 1,5 раза чаще, чем 40-60-летние. У детей толерантность респираторных органов к лучевой нагрузке в 2,5 раза ниже, чем у взрослых.
Локализация очага
Установлена прямая зависимость частоты превмонита от расположения очага, на который производится воздействие. Чем ближе по отношению к средостению находится фокус облучения, тем реже и позднее выявляются проблемы. Больше страдают периферические участки лёгких.
Комплексное и комбинированное лечение
Сочетание радиотерапии с хирургическим лечением и (или) химиотерапией увеличивает количество случаев постлучевого пневмонита, провоцирует его раннее развитие, утяжеляет течение. Противоопухолевые препараты способны самостоятельно негативно воздействовать на дыхательную систему, вызывать пневмопатии.
После облучения легкого происходит поражение альвеолярных клеток II типа и раннее уменьшение синтеза сурфактанта (особое вещество, выстилающее изнутри альвеолы легких. Основной его функцией считается поддержание поверхностного натяжения). Следствием этого является спадение стенок альвеол. Эти два события определяются в течение минут-часов и не имеют признаков проявления по клиническим и радиографическим методам.
Кроме того, лучевая терапия вызывает также поражение капиляров, что развивается как правило через 5 дней после облучения, и ведет к образованию микротромбов и обструкции просвета сосудов.
Ярко выраженные клинические проявления встречаются у 15-60% получающих радиотерапию по поводу рака легких и молочной железы.
Острый постлучевой пневмонит является ранним радиационным повреждениям органов дыхания. Возникает на фоне облучения или в течение первых трёх месяцев после него. Стабильные изменения, обнаруженные в более поздние сроки, расцениваются как пневмофиброз.
Периодическая терпимая боль в грудной клетке, приступы кашля. Ощущается нехватка воздуха при ходьбе.
Заболевание, как правило, начинается остро, с кашля. При этом его интенсивность варьирует от редкого покашливания до постоянных мучительных приступов.
Может отделяться светлая слизистая мокрота, которая при присоединении вторичной инфекции становится гнойной жёлто-зелёной. Иногда возникает кровохарканье.
Одышка вызывается нагрузкой, в тяжёлых случаях беспокоит при разговоре, в состоянии покоя.
Боль в груди может отсутствовать или появляться эпизодически; при наличии фибринозного плеврита становится постоянной и интенсивной.
Температурная реакция колеблется от стойкого субфебрилитета до гипертермии.
Встречаются и общие реакции: пациент становится раздражительным, появляются жалобы на слабость, головную боль, головокружение, бессонницу, возникают перебои в сердечной деятельности, нарушения работы пищеварительного тракта (тошнота, рвота, диарея, снижение аппетита, извращение вкуса).
Основные мероприятия направлены на восстановление респираторных функций организма, минимизацию последствий.
Системные кортикостероиды
Назначаются с целью стимуляции продукции сурфактанта. Уменьшают воспалительную реакцию лёгкого, сглаживают симптомы. Положительный ответ наступает быстро, обычно на 2-4 день. Если за этот промежуток времени состояние пациента не улучшилось, дальнейшее применение кортикоидных гормонов не имеет смысла.
Антикоагулянты
Препятствуют образованию тромбов в капиллярах малого круга кровообращения. Снижают риск развития тромбоэмболии лёгочной артерии.
Антибиотики
Применяются для лечения бактериальных осложнений в условиях снижения иммунитета. Назначаются с учётом чувствительности микрофлоры мокроты к антибактериальным средствам. При отсутствии данных предпочтение отдаётся препаратам с широким спектром действия.
Другие препараты: отхаркивающие средства, ангиопротекторы, аскорбиновая кислота.
При острой респираторной недостаточности показаны наркотические противокашлевые препараты, кислородная поддержка.
Для улучшения дренажной функции легких, профилактики застойных явлений рекомендовано:
- ЛФК;
- активная дыхательная гимнастика;
- постуральный дренаж;
- ингаляционная терапия с отхаркивающими средствами, гормонами;
- низкочастотная магнитотерапия на очаг поражения;
- массаж грудной клетки.
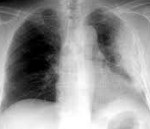
Постлучевой пневмонит – повреждение лёгочной ткани, развивающееся под действием высоких доз ионизирующей радиации. Проявляется одышкой, сухим или продуктивным кашлем, плевральными болями, сопровождается повышением температуры тела. Диагноз выставляется на основании анамнестических данных и клинических симптомов, подтверждается результатами спирометрии, рентгенологического исследования, компьютерной томографии и МРТ органов грудной клетки. Лечение пневмонита проводится с помощью фармакотерапии кортикостероидными гормонами, антибиотиками, антикоагулянтами; оксигенотерапии, физиотерапии.
МКБ-10

- Причины
- Патогенез
- Классификация
- Симптомы постлучевого пневмонита
- Осложнения
- Диагностика
- Лечение постлучевого пневмонита
- Профилактика и прогноз
- Цены на лечение
Общие сведения
Постлучевой пневмонит (лучевой пульмонит, радиационная пневмония) относится к локальным радиационным поражениям лёгочной паренхимы. Ионизирующим излучением повреждается участок альвеолярной ткани, отсюда другое название – лучевой альвеолит. Ярко выраженные клинические проявления встречаются у 15-60% получающих радиотерапию по поводу рака легких и молочной железы. В 3-4% случаев постлучевой пневмонит приобретает крайне тяжёлое течение и заканчивается летально. У некоторых больных протекает латентно, характерные изменения выявляются только специальными методами исследования.

Причины
Пусковым механизмом служит превышение толерантной дозы радиоактивного воздействия на лёгочную ткань. При лучевой терапии онкологических заболеваний грудной полости, рака молочной железы доза радиации составляет в среднем 70-80 Гр. В фокус облучения попадает зона лёгкого с предельной переносимостью 35-40 Гр, вследствие чего развиваются радиационные поражения. Частота возникновения, течение патологического процесса напрямую зависят от величины суммарной очаговой дозы. Большое значение имеют следующие факторы:
- Возраст пациента. Согласно исследованиям в области онкологии и пульмонологии, больные старше 70 лет страдают от осложнений радиотерапии в 1,5 раза чаще, чем 40-60-летние. У детей толерантность респираторных органов к лучевой нагрузке в 2,5 раза ниже, чем у взрослых.
- Локализация очага. Установлена прямая зависимость частоты радиационно-индуцированного пульмонита от расположения очага, на который производится воздействие. Чем ближе по отношению к средостению находится фокус облучения, тем реже и позднее выявляются проблемы. Больше страдают периферические участки лёгких.
- Комплексное и комбинированное лечение. Сочетание радиотерапии с хирургическим лечением и (или) химиотерапией увеличивает количество случаев постлучевого пневмонита, провоцирует его раннее развитие, утяжеляет течение. Противоопухолевые препараты способны самостоятельно негативно воздействовать на дыхательную систему, вызывать пневмопатии.
Патогенез
Ионизирующее излучение повреждает клетки альвеолярного эндотелия. Нарушается продукция сурфактанта, альвеолы спадаются. Одновременно поражается внутренняя оболочка капилляров, что приводит к тромбообразованию, частичной закупорке и повышению проницаемости сосудов. Страдает газообмен. Изменения по типу экссудативного альвеолита возникают в первые дни. В течение 1-3 месяцев повреждённый эндотелий частично восстанавливается, происходит реканализация ряда сосудов. Активируются фибробласты, погибшие клетки заменяются соединительной тканью.
Макроскопически определяются полнокровные участки лёгочной паренхимы плотноэластической консистенции, фибринозный выпот в плевральной полости. При микроскопическом исследовании выявляется утолщение альвеолярной мембраны, повреждения капиллярной сети с признаками тромбоза, стаза и полнокровия. В области межальвеолярных перегородок формируются зоны фиброза.
Классификация
Острый постлучевой пневмонит является ранним радиационным повреждениям органов дыхания. Возникает на фоне облучения или в течение первых трёх месяцев после него. Стабильные изменения, обнаруженные в более поздние сроки, расцениваются как пневмофиброз. Американскими онкологами разработана классификация заболевания в зависимости от степени тяжести:
- I степень. Болевые ощущения в груди отсутствуют или минимальные. Кашель редкий. Одышка появляется при значительной физической нагрузке. Определяется снижение жизненной ёмкости лёгких (ЖЕЛ) на 10-25% от должного значения. Имеются косвенные рентгенологические признаки болезни.
- II степень. Больного беспокоит периодическая терпимая торакалгия, приступы кашля. При ходьбе ощущается нехватка воздуха. ЖЕЛ находится в пределах 50-75% от нормальной величины. На рентгенограмме видны очаговые тени.
- III степень. Боль становится интенсивной, кашель - постоянным. Одышка возникает при малейшей нагрузке. ЖЕЛ составляет 25-50 % от нормы. Размеры инфильтрации на снимке соответствуют облучённому участку.
- IV степень. Стойкий болевой синдром, непрекращающийся кашель требуют назначения наркотических анальгетиков. Дыхание затруднено в покое. Наблюдается значительное (более чем на 75%) снижение ЖЕЛ. При рентгенографии выявляется одностороннее субтотальное или тотальное затенение. Пациент нуждается в респираторной поддержке.
Симптомы постлучевого пневмонита
Заболевание начинается остро. Ведущим симптомом является кашель. Его интенсивность варьирует от редкого покашливания до постоянных мучительных приступов. Может отделяться светлая слизистая мокрота, которая при присоединении вторичной инфекции становится гнойной жёлто-зелёной. Иногда возникает кровохарканье. Одышка вызывается нагрузкой, в тяжёлых случаях беспокоит при разговоре, в состоянии покоя. Боль в груди может отсутствовать или появляться эпизодически; при наличии фибринозного плеврита становится постоянной и интенсивной. Температурная реакция колеблется от стойкого субфебрилитета до гипертермии.
Классической клинической картине иногда предшествует общая лучевая реакция. Пациент становится излишне раздражительным, предъявляет жалобы на слабость, головную боль, головокружение, бессонницу. Развивается миокардиодистрофия, возникают перебои в сердечной деятельности. Нарушения работы пищеварительного тракта проявляются тошнотой, рвотой, диареей. Резко снижается аппетит, наблюдается извращение вкуса, избыточное отделение слюны.
Осложнения
Небольшой по объёму постлучевой пневмонит часто распознаётся несвоевременно. Обнаруживается на стадии пневмофиброза с бронхоэктазами, плевродиафрагмальными спайками, смещением средостения. Из-за массивного склеротического процесса возникают необратимые дыхательные нарушения. Формируется хроническое лёгочное сердце, значительно ухудшается качество жизни. При обширных изменениях развивается тяжёлая острая дыхательная недостаточность, требующая перевода на искусственную вентиляцию лёгких. Может наступить летальный исход.
Диагностика
Чёткая связь респираторных нарушений с проводимой радиотерапией позволяет пульмонологу заподозрить постлучевой пневмонит. При сборе анамнеза уточняются дозы, количество и давность сеансов облучения, сочетание с химиотерапией или операцией. Особое внимание уделяется локализации и размерам очага. Следует учитывать наличие общей реакции. Основные диагностические мероприятия включают:
- Физикальное исследование. Определяются зоны притупления перкуторного звука на стороне поражения. Аускультативно выслушиваются непостоянные средне- и мелкопузырчатые хрипы, шум трения плевры.
- Лабораторные анализы. Такие проявления лучевой реакции, как угнетение гемопоэза, иммунные нарушения, выявляются лабораторными методами. В клиническом анализе крови наблюдается снижение уровня лейкоцитов, тромбоцитов, эозинофилия.
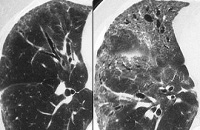
- Рентгенография и КТ лёгких. На рентгенограмме заметны усиление и деформация лёгочного рисунка, фокусы инфильтрации в проекции зоны облучения, плевральный выпот. Одностороннее поражение является патогномоничным признаком заболевания. КТ позволяет раньше выявить и более точно определить границы повреждения.

Дополнительно выполняется исследование газового состава крови и функции внешнего дыхания. В неясных случаях для уточнения диагноза используется МРТ. Постлучевой пневмонит следует дифференцировать с метастатическим обсеменением, бактериальной пневмонией, а также с туберкулёзом и микозами, которые могут быть спровоцированы вторичным иммунодефицитом.
Лечение постлучевого пневмонита
При подтверждении радиационной пневмонии назначается консервативная терапия. Применяются фармакологические средства, физиотерапевтические методы, лечебная физкультура. Основные мероприятия направлены на снижение смертности, восстановление респираторных функций организма, минимизацию последствий. Для достижения терапевтического эффекта комплексно используются следующие группы препаратов:
- Системные кортикостероиды. Назначаются с целью стимуляции продукции сурфактанта. Уменьшают воспалительную реакцию лёгкого, сглаживают симптомы. Положительный ответ наступает быстро, обычно на 2-4 день. Если за этот промежуток времени состояние пациента не улучшилось, дальнейшее применение кортикоидных гормонов не имеет смысла.
- Антикоагулянты. Препятствуют образованию тромбов в капиллярах малого круга кровообращения. Снижают риск развития смертельно опасного осложнения – тромбоэмболии лёгочной артерии.
- Антибиотики. Применяются для лечения бактериальных осложнений в условиях снижения иммунитета. Назначаются с учётом чувствительности микрофлоры мокроты к антибактериальным средствам. При отсутствии данных предпочтение отдаётся препаратам с широким спектром действия.
Дополнительно используются отхаркивающие средства, ангиопротекторы, аскорбиновая кислота. При острой респираторной недостаточности показаны наркотические противокашлевые препараты, кислородная поддержка. Из физиотерапевтических методов рекомендуются ингаляции с димексидом, переменные магнитные поля. В восстановительном периоде широко применяются массаж и дыхательная гимнастика.
Профилактика и прогноз
Для предотвращения нежелательных реакций при проведении лучевой терапии пациенту рекомендуется сбалансированное калорийное питание, прогулки на свежем воздухе. Необходимо контролировать показатели крови, общее состояние больного. При появлении тромбопении, лейкопении, кровохарканья лучевую терапию следует прекратить. Рациональный индивидуальный подход, использование методов фигурных полей облучения позволяют значительно снизить частоту возникновения индуцированных радиацией осложнений. При радикальной радиотерапии рака лёгкого в профилактических целях рекомендуется одновременное переливание облучённой аутокрови, использование энтеросорбентов.
Прогноз во многом определяется течением основного заболевания, площадью повреждения лёгкого. Адекватно пролеченные небольшие пульмониты нередко подвергаются обратному развитию. Формирование фиброза продолжается от 6 месяцев до 2 лет, после чего изменения носят стабильный характер, и нарушения становятся необратимыми. Реабилитационные мероприятия способны влиять на процесс фиброзирования. Острый респираторный дистресс-синдром в ряде случаев заканчивается смертью.
Читайте также:

