Лучевая терапия головного мозга при лейкозе
Лечение лейкоза должно проводиться поэтапно. Первые 3 этапа заключаются в достижении, закреплении и поддержании ремиссии, а последний, четвёртый, это профилактика осложнений. Если рак крови диагностирован своевременно, лечение подобрано правильно и проводится адекватно, человек, которому поставлен диагноз лейкемия, может долгие годы жить полноценной жизнью.
Тактика, по которой будет проводиться лечение лейкемии, должна быть составлена правильно. В основу её ложатся результаты, которые показала диагностика лейкоза.

При подборе курса терапии специалист обязательно учитывает несколько факторов: разновидность и стадию заболевания;
- характер течения патологического процесса;
- общее самочувствие больного;
- возрастную категорию пациента;
- реакцию организма на определённые препараты.
На сегодняшний день лечение лейкоза проводится с помощью нескольких методов, давно доказавших свою высокую эффективность при раке крови:
- Химиотерапия, основополагающий метод лечения онкологии крови.
- Лучевая терапия и иммунотерапия, используемые, как вспомогательные методики.
- Пересадка костного мозга, являющаяся золотым стандартом, применяемым в лечении рака крови.
Химиотерапия в лечении лейкоза
Химиотерапевтический метод в лечении рака крови признан в мировой онкологической практике основным, т. к. благодаря химии у пациентов достигается максимально длительные периоды ремиссии.
Лечение лейкоза химиопрепаратами состоит из 2-х этапов:
- Первичное разрушение основной массы мутировавших клеток. С этой целью используют противоопухолевые препараты, обладающие высокой агрессивностью.
- Повторный курс химии, направленный на уничтожение сохранившихся после первого этапа злокачественных клеток. Его целью является предотвращение развития рецидива болезни.
Современные противоопухолевые препараты отличаются высокой результативностью и минимальным риском развития серьёзных побочных эффектов.
Несмотря на то, что химиопрепараты, используемые в современной гематоонкологии, признаны достаточно безопасными для организма человека, на каждого пациента они влияют по-разному. Чтобы подобрать препарат и правильно составить курс терапии, лечащий врач проводит предварительную подготовку к процедуре, которая начинается с изучения физических параметров больного.
Дальнейшие подготовительные мероприятия заключаются в проведении ряда диагностических исследований, в которые входят следующие процедуры:
- Анализы крови, выявляющие количественный состав здоровых и повреждённых кровяных телец.
- ЭКГ, эхокардиография и УЗИ сердца, оценивающие его работу.
- Функциональные тесты, определяющие состояние лёгких.
- Диагностическое исследование печени и почек.
- Анализы на гепатит и ВИЧ.
Если химиотерапия предстоит молодым мужчинам, им рекомендуют перед началом химиотерапевтического воздействия сохранить сперму, т. к. существуют высокие риски после проведённого курса лечения развития бесплодия.
Лечение лейкоза противоопухолевыми препаратами продолжается приблизительно 2 года, до того момента, когда клетки опухоли будут полностью уничтожены. Успешность терапии подтверждается нормализацией состава крови, отсутствием злокачественных клеток в биопсийном материале костного мозга и восстановлением здоровых кроветворных тканей.
Химиотерапия при лейкемии проводится одним из нескольких способов:
- пероральное употребление препаратов;
- внутривенное или чрезкатеторное введение лекарственных средств;
- посредством инъекций в цереброспинальную жидкость или позвоночник.
Стоит знать! Всем маленьким пациентам и некоторым взрослым для проведения процедуры применяют специальный резервуар Оммайя. Это специфический катетер, имплантируемый в желудочки головного мозга. Преимуществом данного способа является его низкая травматичность и минимум болезненных ощущений, которые сопровождают инъекционное введение химиопрепаратов в позвоночный столб инъекционным способом.
Химиотерапия при лейкемии проводится несколькими циклами, продолжающимися 3-7 дней, после чего делается определённый перерыв, позволяющий организму больного человека восстановиться. Во время восстановительного периода костный мозг начинает продуцировать здоровые клетки, а состояние больного улучшается за счёт уменьшения влияния побочных эффектов. Для терапии онкопоражения крови применяются Антрациклины (Даунорубицин) и антиметаболиты (Цитарабин).
Лечение лейкоза обычно проводят по следующей схеме:
- Цитарабин вводят 7 суток в дозе 100-200 мг/м2/сут посредством непрерывной в/в инфузии.
- Даунорубицин вводят в первые 3 дня курса. Вливание этого химиопрепарата должно быть в/в струйным, а дозировка составляет 45 мг/м2/сут в/в струйно.
Чаще всего при лейкемии требуется провести 4 цикла такой терапии, во время которых пациент регулярно сдаёт кровь, что позволяет врачу контролировать состояние больного.
После того, как проведено химиотерапевтическое лечение лейкоза, организму пациента необходимо восстановиться. Реабилитационный период занимает некоторое время. Его продолжительность имеет непосредственную зависимость от типа и дозы препаратов, индивидуальной переносимости химиотерапевтического лечения, и общего состояния здоровья пациента.
Реабилитационный курс должен включать следующие мероприятия:
- психологическую поддержку;
- специальный диетический комплекс питания;
- лечебную физическую и дыхательную гимнастику.
На некоторых людей химиотерапия оказывает очень сильное влияние, вызывая физическое и нервное истощение. Таким пациентам рекомендуется на весь реабилитационный период взять больничный или перейти на частичную занятость. Для оценки и контроля своего состояния необходимо регулярно сдавать анализы крови.
Пересадка костного мозга при лейкозе
При лечении рака крови пересадка костного мозга – лучшее терапевтическое мероприятие, благодаря которому возможно полное исцеление больного человека, т. к. прижившиеся здоровые кроветворные ткани начинают производить нормально функционирующие кровяные тельца.
Лечение лейкемии методом трансплантации костного мозга может быть выполнено 3-мя способами:
- переливание пуповинной крови;
- пересадка кроветворной ткани костного мозга;
- трансплантация стволовых клеток из кровяного русла.
В зависимости от метода получения биоматериала выделяют 2 вида пересадки:
- аутотрансплантация (собственная кроветворная ткань пациента);
- аллогенная, проводимая донорскими стволовыми клетками.
Основным показанием к такой операции при лечении рака крови является тяжёлая форма онкологии и неэффективность других методик. Среди противопоказаний к трансплантации можно выделить острые инфекционные процессы, функциональную недостаточность жизненно важных органов и плохое общее состояние онкобольного.
Метод трансплантации, с помощью которого проводится лечение лейкоза, состоит из 4-х этапов:
- Подготовительный. Продолжается 1-2 недели и заключается в подготовке к предстоящей процедуре организма реципиента, а именно проведении агрессивного курса химиотерапии, во время которого уничтожается максимальное количество клеток кроветворной ткани.
- Непосредственно процедура пересадки, похожая на переливание крови.
- Снижение иммунитета онкобольного.
- Приживление стволовых клеток.
Лечение лейкемии на трансплантации костного мозга не заканчивается. Для его благополучного приживления требуется длительный реабилитационный период, который начинается сразу же после проведения операции. Всё время реабилитации (1,5-3 месяца) пациент находится в антибактериальной камере под постоянным наблюдением специалистов. Прооперированному человеку обязательно назначаются противовирусные препараты и антибиотики, снижающие риски проникновения в организм инфекции, а также симптоматическое лечение, купирующее возможные побочные эффекты. Выписка пациента возможна только в том случае, если его организм в течение определённого времени не отторг донорский материал.
Использование лучевой терапии при раке крови
Лучевая терапия при лейкозе назначается достаточно редко, но в случае принятия специалистами решения о её необходимости при лечении рака крови, пучки ионизирующих лучей направляют на зоны расположения лимфатических узлов. Такое направленное действие имеет целью уничтожение как можно большего количества мутировавших клеток, ведь именно в лимфатических узлах и находятся скопления атипичных элементов.
Лечение лейкемии с помощью облучения назначают нечасто, т. к. её эффективность при раковых поражениях крови исследована не полностью. В основном лучевая терапия применяется в тех случаях, когда требуется экстренное уничтожение аномальных клеток – перед трансплантацией костного мозга или уменьшения размеров опухоли, разрастающейся в непосредственной близости от трахеи и оказывающей на неё давление, вследствие чего у человека перекрывается дыхание.
Лечение лейкоза посредством облучения мутировавших клеток ионизирующими лучами проводится, как правило, на протяжении двух недель. За это время выполняется 8-10 сеансов.
Облучение, так же как и химиотерапия, оказывает негативное воздействие на организм онкобольного, поэтому лечение лейкоза с помощью радиационных лучей должно сопровождаться рядом реабилитационных мероприятий, к которым относятся:
- избегание стрессовых ситуаций;
- нормализация режима дня;
- длительные прогулки;
- коррекция питания;
- фитотерапия.
Лечение лейкоза в зависимости от стадии распространения онкопатологии
Лечение лейкоза проводится несколькими методами, в зависимости обширности поражения и стадии болезни:
- Предлейкоз (скрытая форма). Если заболевание удалось выявить на этом этапе, терапевтические мероприятия не требуются пациенту достаточно динамического наблюдения.
- Первая атака (острый лейкоз). На этом этапе лечение лейкоза проводится агрессивная химиотерапия, которую могут дополнять курсы облучения.
- Ремиссия (полная, неполная). При затихании болезни продолжают динамическое наблюдение пациента, дополненное симптоматической терапией, устраняющей присутствующие негативные признаки.
- Вторичная атака (рецидив). Если болезнь достигла этого этапа, единственным шансом на выживание становится пересадка костного мозга.
- Терминальная стадия лейкоза. Заключительный, неизлечимый этап болезни, на котором все лечебные мероприятия сводятся к паллиативной терапии, облегчающей мучительную симптоматику.
Где лечить рак крови?
В современном мире вопросы того, можно ли вылечить рак крови и где лечить рак крови, стают очень остро, ведь ежедневно количество пациентов с лейкемией различных возрастов и социальных групп растет с пугающей скоростью. То, как лечить рак крови, определяют онкологи и гематологи для каждого конкретного больного после различных методов диагностики и анализов.
Некоторые способы лечения в виде химиотерапии проводятся внутри страны, тогда как пересадкой костного мозга занимаются лишь специализированные клиники Израиля, Германии, США и других высокоразвитых государств, в связи с чем стоимость лечения рака крови очень высока. Далеко не все страны осуществляют поддержку и предоставляют государственную помощь в лечении онкологии, и преобладающее количество расходов, связанных с борьбой с данным заболеванием, ложится на плечи самих больных их семей, и знакомых.
Информативное видео
а) Терминология:
1. Сокращения:
• Экстрамедуллярные лейкемические опухоли (ЭЛО)
• Экстрамедуллярная миелобластома, экстрамедуллярные миелоидноклеточные опухоли (ЭМКО)
2. Синонимы:
• Гранулоцитарная саркома, хлорома
3. Определения:
• Солидная опухоль, состоящая из миелобластов/миелоцитов/промиелоцитов:
о У пациентов с миелопролиферативным заболеванием
• Множественные иные внутричерепные проявления лейкоза/осложнений терапии:
о Синдром задней обратимой энцефалопатии (СЗОЭ):
о Инвазивный микоз
о Развитие кавернозных ангиом в позднем периоде после проведения лучевой терапии
о Посттрансплантационная лимфопролиферативная болезнь (ПЛБ) после трансплантации костного мозга
о Венозный тромбоз в сочетании с химиотерапией (L-аспараги-наза)
о Васкулит:
- Основное проявление лейкоза
- Развивается в ответ на терапию (транс-ретиноевая кислота)
- Развивается в ответ на инфекцию (например, аспергиллез)
б) Визуализация:
1. Общие характеристики лейкоза головного мозга:
• Лучший диагностический критерий:
о Гомогенная контрастируемая опухоль(и) у пациентов с диагностированным или предполагаемым миелопролиферативным заболеванием
о Наиболее частое осложнение острого миелоидного лейкоза (ОМЛ)
• Локализация:
о Менингеальные (с основанием в твердой или мягкой мозговой оболочке) > интрапаренхиматозные поражения
2. КТ при лейкозе головного мозга:
• Бесконтрастная КТ:
о Изо-/гиперденсное по отношению к мозговым тканям образование
- Быстро может стать гиподенсным (некротические изменения, расплавление)
о Может проявляться в виде гематомы (или имитировать ее)
о Оцените вовлечение основания черепа/околоносовых пазух
• КТ с контрастированием:
о Гомогенный характер контрастирования:
- Повышенная КТ-плотность или наличие кровоизлияния могут маскировать накопление контраста
о Может наблюдаться кольцевой характер контрастирования, имитирующий абсцесс
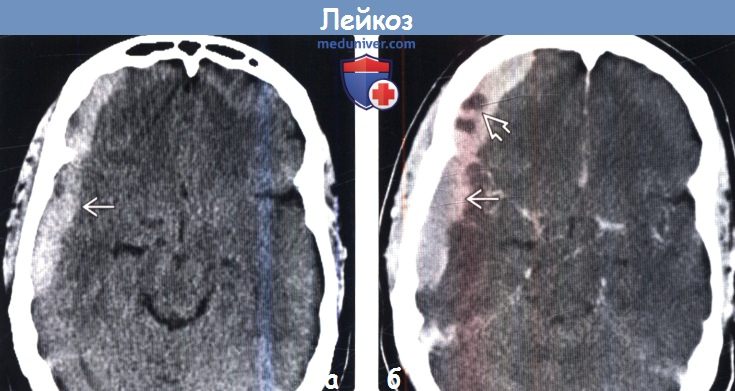
(а) Бесконтрастная КТ, аксиальный срез: у пациента с острым миелоцитарным лейкозом определяется гиперденсное объемное образование с основанием в твердой мозговой оболочке, которое имитирует субдуральную гематому.
(б) КТ с контрастированием, аксиальный срез: определяется гомогенное контрастирование образования, что исключает кровоизлияние. Мелкие неконтрастируемые участки обусловлены скорее некротическими изменениями/расплав-лением, чем интенсивным кровотечением. Подобные находки характерны для лейкозных инфильтратов с основанием в твердой мозговой оболочке у пациентов с ОМЛ.
3. МРТ при лейкозе головного мозга:
• Т1-ВИ:
о Гипо-/изоинтенсивный по отношению к мозговой ткани сигнал о Может позволить дифференцировать острую гематому от негеморрагического объемного образования
• Т2-ВИ:
о Вариабельный сигнал, может быть гипоинтенсивным
о Поражение мягкой мозговой оболочки может распространяться по периваскулярным пространствам, визуализируется как очаги гиперинтенсивного сигнала в БВ
• FLAIR:
о Более чувствительно к образованиям мягких мозговых оболочек, чем Т2-ВИ
• Т2* GRE:
о Полезно для определения кавернозных ангиом-крайне поздних осложнений лечения лейкоза
• ДВИ:
о Возможно ограничение диффузии (гиперинтенсивное на ДВИ, гипоинтенсивное на ИКД)
о Помогает дифференцировать ишемические осложнения от ЗЭО
• Постконтрастные Т1-ВИ:
о Гомогенный характер контрастирования:
- Может стать гетерогенным при некротических изменениях/расплавлении
о Контрастирование мягких мозговых оболочек или периваскулярного пространства
о Методики подавления жира крайне важны для оценки поражений основания черепа
• МР-ангиография:
о Возможен вазоспазм при наличии СЗЭО
о Позволяет определить наличие васкулита сосудов среднего калибра
• МР-венография:
о Необходима для оценки геморрагических образований
о Оцените наличие или выраженность венозного тромбоза
4. Радионуклидная диагностика:
• Сцинтиграфия костей:
о Tc-99m MDP используется при поражении костей при лейкозе
о Поглощение мягкими тканями обычно является проявлением гиперкальциемии, а не хлоромы
• ПЭТ:
о Интенсивное поглощение ФДГ при проведении ПЭТ
5. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о МРТ с контрастным усилением
• Советы по протоколу исследования:
о МРТ с получением постконтрастных Т1-ВИ в режиме подавления сигнала от жира
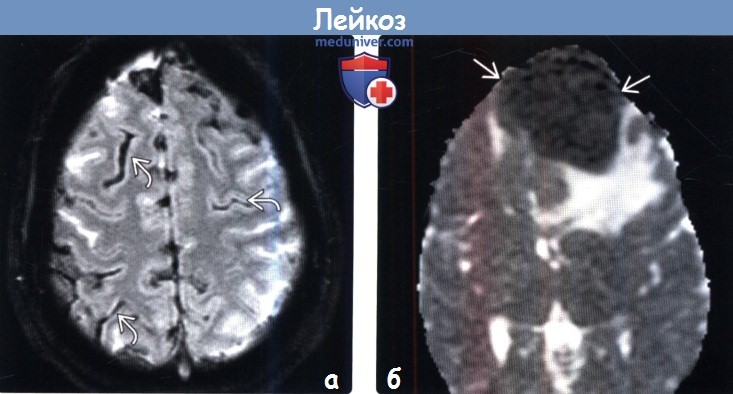
(а) MPT, Т2* GRE, аксиальный срез: у пациента с острым миелобластным лейкозом (ОМЛ) и бластным кризисом определяется гипоинтенсивный сигнал от лептоменинкс. При исследовании СМЖ были выявлены кровоизлияние и лейкоцитарные инфильтраты.
(б) МРТ, ИКД, аксиальный срез: у девочки 13 лет с синуситом и отеком кожи головы определяется выраженно гипоинтенсивное ограничивающее диффузию объемное образование, которое было гиперденсным при КТ и интенсивно накапливало контраст (изображения не представлены). При биопсии и исследовании крови был выявлен острый лимфобластный лейкоз (ОЛЛ) высокой степени риска.
в) Дифференциальная диагностика лейкоза головного мозга:
3. Внемозговая гематома:
• Отек внечерепных мягких тканей или перелом черепа
• При отсутствии характерного анамнеза предполагайте возможность жестокого обращения с ребенком
4. Экстрамедуллярный гематопоэз:
• Выражение гипоинтенсивный на Т2-ВИ сигнал
• Одинаковая популяция пациентов по группе риска
5. Гистиоцитоз из клеток Лангерганса (ГКЛ):
• Деструкция без периостальной реакции
• Несахарный диабет
6. Саркома Юинга:
• Агрессивный характер роста
• Деструкция прилегающей кости
7. Нейросаркоидоз:
• Имитирует поражение лептоменинкс
• Менее часто проявляется в виде объемных образований с основанием в твердой мозговой оболочке
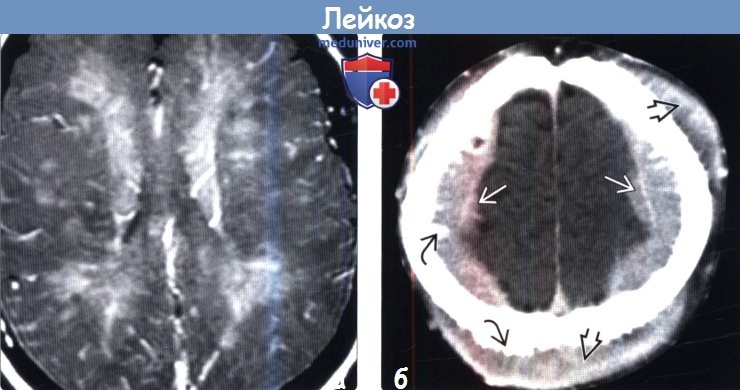
(а) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у пациента с лейкемией и прогрессирующей энцефалопатией определяются множественные контрастируемые интра- и периваскулярные инфильтраты. Карциноматозный энцефалит является редким осложнением лейкоза.
(б) КТ с контрастированием, аксиальный срез: у пациента с лейкозом и поражением костей черепа определяются крупные двусторонние, конвекситальные, эпидуральные лейкозные объемные образования. Обратите внимание на поднадкостничную локализацию опухолей. Игольчатый вид наружной и внутренней пластинок костей свода черепа является признаком экстенсивного вовлечения костного мозга.
г) Патология:
г) Клиническая картина:
1. Проявления лейкоза головного мозга:
• Наиболее частые признаки/симптомы:
о Появление клинических симптомов может опережать диагностику лейкоза по анализу костного мозга
о В 50% случаев диагностируются только при аутопсии
о Для поражений ЦНС характерна клиническая манифестация
о Очаговая симптоматика вследствие локального масс-эффекта
о Головная вследствие кровоизлияния
• Клинический профиль:
о Ребенок с ОМЛ, у которого появились новые неврологические симптомы
2. Демография:
• Возраст:
о 60% пациентов африканских детей
3. Течение и прогноз:
• Общая выживаемость при ОМЛ - 40-50%
• Хлорома как часть другого миелопролиферативного синдрома:
о Предполагается бластная трансформация
о Признак неблагоприятного прогноза
4. Лечение:
• Индукционная химиотерпия:
о Цитарабин (Ара-С)
о Антрациклин
• Трансплантация костного мозга с целью консолидации ремиссии
• Обратите внимание: лечение метотрексатом может приводить к развитию инсультоподобных симптомов:
о МРТ → округлые поражения БВ с ограничением диффузии
д) Диагностическая памятка:
1. Обратите внимание:
• Экстрамедуллярный гемопоэз может быть в той же популяции пациентов со схожими проявлениями
• Геморрагические поражения у детей с ОМЛ могут являться манифестацией хлоромы или осложнениями терапии
2. Советы по интерпретации изображений:
• Множественные поражения множественной локализации позволяют поставить диагноз
• Хлоромы с кольцевым характером контрастирования (редко) могут имитировать абсцесс
е) Список литературы:
- Bar М et al: Central nervous system involvement in acute myeloid leukemia patients undergoing hematopoietic cell transplantation. Biol Blood Marrow Transplant. 21 (3):546-51, 2015
- Cheng CL et al: Risk factors and clinical outcomes of acute myeloid leukaemia with central nervous system involvement in adults. BMC Cancer. 15(1):344, 2015
- Bhojwani Detal: Methotrexate-induced neurotoxicity and leukoencephalopathy in childhood acute lymphoblastic leukemia. J Clin Oncol. 32(9):949—59, 2014
- Rozovski U et al: Incidence of and risk factors for involvement of the central nervous system in acute myeloid leukemia. Leuk Lymphoma. 1-6, 2014
- Morioka S et al: Effects of chemotherapy on the brain in childhood: diffusion tensor imaging of subtle white matter damage. Neuroradiology. 55(10):1251—7, 2013
- Spataro R et al: Neurological picture. Petechial brain haemorrhages in acute lymphoblastic leukaemia. J Neurol Neurosurg Psychiatry. 84(8):908, 2013
- Farad M et al: Magnetic resonance imaging in childhood leukemia survivors treated with cranial radiotherapy: a cross sectional, single center study. Pediatr Blood Cancer. 57(2):240-6, 2011
- Dicuonzo F et al: Posterior reversible encephalopathy syndrome associated with methotrexate neurotoxicity: conventional magnetic resonance and diffusion-weighted imaging findings. J Child Neurol. 24(8): 1013-8, 2009
- Koenig MK et al: Central nervous system complications of blastic hyperleukocytosis in childhood acute lymphoblastic leukemia: diagnostic and prognostic implications. J Child Neurol. 23(11): 1347-52, 2008
- Hakyemez В et al: Parlak M. Intracranial myeloid sarcoma: conventional and advanced MRI findings. Br J Radiol. 80(954):e109-12, 2007
Редактор: Искандер Милевски. Дата публикации: 5.4.2019
Раком крови в непрофессиональном общении называют злокачественные новообразования, первично поражающие кроветворную ткань и циркулирующие в крови лейкоциты. В официальной медицинской терминологии такие заболевания называются лейкозами или лейкемией. Иногда раком крови называют лимфомы, но это не совсем так, поскольку в этом случае поражение костного мозга служит лишь следствием метастазирования.
Злокачественное перерождение при лейкозах происходит на уровне стволовых клеток. Процессы патологического деления и клонирования атипичных клеток, подавление естественной клеточной гибели приводят к замещению нормальных форменных элементов крови опухолевыми.
Основы классификации
- Клеточный фенотип — совокупность всех происходящих в клетке процессов.
- Степень дифференциации на момент клинических проявлений. Все разнообразные клетки организма берут общее начало от стволовых. По мере своего созревания они постепенно приобретают узкую специализацию. Чем выше степень дифференциации, тем клетка больше отличается от стволовых предшественников
Таким образом, выделяют 4 основных лейкоза, каждый из которых делится на множество подтипов:
- Острый лимфоцитарный лейкоз — самое распространенное онкологическое заболевание у детей. Представлен незрелыми и аномально долго живущими лимфоцитами.
- Хронический лимфоцитарный лейкоз. Чаще встречается в зрелом и пожилом возрасте. Представлен атипичными, но морфологически созревшими лимфоцитами.
- Острый миелоцитарный лейкоз — самый распространенный лейкоз у взрослых, который может носить вторичный характер. Представлен клетками-предшественниками миелоидного ряда — гранулоцитов и моноцитов.
- Хронический миелоцитарный лейкоз. Встречается в любом возрасте и представлен большим количеством незрелых клеток миелоидного ряда.
В отдельную группу выделяют так называемые миелодиспластические синдромы — целую группу заболеваний, при которых наблюдается неправильное развитие (дисплазия) клеток-предшественников различных линий кроветворения и дефицит зрелых форменных элементов в крови. У пациентов с такими заболеваниями повышается риск развития острого миелоидного лейкоза, но у большинства больных этого не случится.
Различные типы лейкоза имеют свои особенности, обусловливающие клиническую картину, течение заболевания, прогноз для жизни. Возможны бластные кризы, при которых заболевание приобретает характеристики острой патологии и угрожает жизни пациента.
Причины и факторы риска
Истинные причины большинства лейкозов пока неизвестны. Существуют факторы, которые возможно увеличивают риск развития заболевания:
- проникающая радиация;
- действие некоторых химических соединений, например, бензола;
- лечение некоторыми цитостатиками (химиотерапия);
- инфицирование вирусом Эпштейна–Барра;
- хромосомные нарушения, в том числе синдром Дауна;
- иммунодефицитные состояния.
Следует отметить, что, несмотря на то, что перечисленные факторы повышают риск развития лейкемии, у подавляющего большинства людей этого не происходит.
Клинические появления
Острые лейкозы обычно развиваются достаточно стремительно, и первые симптомы дают знать о себе за несколько недель до постановки диагноза. Нарушение нормального кроветворения приводит к таким частым симптомам лейкемии, как анемия и повышенная кровоточивость. В то же время другие проявления патологии неспецифичны и не всегда позволяют объективно ее заподозрить. Это слабость, недомогание, лихорадка, снижение веса. Обычно причины лихорадки при этом неизвестны, хотя в некоторых случаях дефицит гранулоцитов способствует быстрому развитию бактериальных инфекций.
Повышенная кровоточивость проявляется склонностью к образованию гематом, петехиальными высыпаниями, носовыми кровотечениями, менструальными нарушениями. Поражение костного мозга может вызвать боли в костях, что особенно характерно для детей с острыми лимфолейкозами. Возможно появление признаков инфильтрации атипичным клетками тех или иных органов: увеличение печени, селезенки, лимфатических узлов.
Хронические лимфолейкозы прогрессируют медленно. Нередко они вообще не имеют клинических проявлений или сопровождаются неспецифическими симптомами — незначительной лихорадкой или немотиврованной слабостью. Клинические проявления на ранних стадиях хронического миелолейкоза похожи, но спустя определенный промежуток времени происходит избыточное накопление опухолевых клеток и заболевание переходит в фазу бластного криза с резким ухудшением состояния пациента.
Прогноз
Значимые различия в природе и течении лейкозов обусловливают разный общий прогноз заболевания и эффективность проводимого лечения.
Ремиссия после стандартной терапии у детей имеет место в более чем 95% случаев. Более того, пятилетняя выживаемость без признаков заболевания, которую можно расценивать как выздоровление, у детей достигает 75% и более. У взрослых эти показатели составляют 70–90% и 30–40% соответственно.
Ремиссию удается достигнуть у 50–85% пациентов. В 20-40% случаев отмечают длительный безрецидивный период. Последний показатель несколько повышается при проведении интенсивной химиотерапии или пересадки стволовых клеток.
В отсутствие лечения, пациенты на начальных стадиях заболевания живут в среднем 5-20 лет, на поздних — 3-4 года после постановки диагноза. Меньшая продолжительность жизни связана с быстрым развитием недостаточности спинного мозга. Излечение при этой патологии обычно невозможно, а задача терапии состоит в увеличении продолжительности жизни и улучшении ее качества.
До появления таргетных цитостатиков, и в частности иматиниба, в течение двух лет после постановки диагноза погибало до 10% пациентов. Сегодня, если лечение начато в хроническую фазу, пятилетняя выживаемость превышает 90%. Основная опасность этого типа лейкозов заключается в бластных кризах, после которых в течение достаточно короткого времени погибает абсолютное большинство больных.
Диагностика
В постановке диагноза и дифференциальной диагностике ключевую роль играют лабораторные исследования:
- Общий анализ и мазок периферической крови. Можно отметить снижение уровня гемоглобина и тромбоцитопению, нарушение дифференцировки лейкоцитов, появление бластных клеток. Содержание белых кровяных телец может колебаться от 1*109/л до 200*109/л.
- Коагулограмма. Возможны различные нарушения в свертывающей системе крови, особенно при промиелоцитарном лейкозе.
- Аспирационная биопсия костного мозга. В биоптате обнаруживают высокое содержание бластов — до 95%.
- Иммунофенотипирование — лабораторный метод, позволяющий определить тип лейкоза, что крайне важно для определения тактики лечения.
- Цитогенетическое исследование. Проводится для определения хромосомных аномалий, которые могли привести к развитию заболевания.
- Биохимический анализ крови. Позволяет определить общее состояние организма, например, обнаружить почечную или печеночную недостаточность.
Помимо этого, для выявления инфильтрации клетками различных органов применяются методы лучевой диагностики: УЗИ, КТ, рентгенография.
Лечение
Тактика терапии при различных типах лейкемии может существенно отличаться. Основные методы лечения:
- Химиотерапия. Применяется для достижения ремиссии и ее закрепления практически при всех типах лейкемии.
- Терапия моноклональными антителами. Сравнительно молодой метод таргетной терапии, обеспечивающий избирательное уничтожение клеток опухоли. Применяется при острых и хронических лимфолейкозах.
- Дистанционная лучевая терапия. Вспомогательный метод лечения, в большей степени востребованный при поражении ЦНС или с паллиативной целью при хроническом лимфолейкозах.
- Пересадка гемопоэтических стволовых клеток. Высокоэффективный, но не всегда доступный метод лечения, который может применяться при большинстве лейкемий.
В каждом случае перед врачом стоит задача выбора наиболее оптимальной тактики в зависимости от типа лейкемии и ее стадии. Так, например, агрессивное ведение хронического миелолейкоза подчас оказывается опаснее для пациента, чем лечение в недостаточном объеме.
Томотерапия при раке крови
Лучевая терапия при лейкозах имеет ограниченное применение. Повреждающее действие ионизирующего излучения на здоровые ткани отнюдь не способствует улучшению общего состояния пациента и плохо влияет на общий прогноз. С учетом того, что химиотерапия позволяет достаточно эффективно добиваться ремиссии, классическая лучевая терапия отходит на второй план.
| Наименование услуги | Цена, руб. | Ед. измерения |
|---|---|---|
| Консультация врача онколога радиотерапевта | 0 | шт. |
| Консультация врача детского онколога | 0 | шт. |
| Повторная консультация специалистов | 500 | шт. |
| Топометрия на специализированном компьютерном томографе первичная | 15 000 | процедура |
| Топометрия на специализированном компьютерном томографе повторная | 7 000 | процедура |
| Дозиметрическое планирование лучевой терапии (томотерапии) первичное | 20 000 | шт. |
| Дозиметрическое планирование лучевой терапии (томотерапии) повторное | 7 000 | шт. |
| Лучевая терапия (томотерапия), включая IMGRT (*) | 223 000 | курс |
| Лучевая терапия (томотерапия) стереотаксическая радиохирургия(*) | 250 000 | курс |
| Лекарственная сопроводительная терапия: внутривенные введение в процедурном кабинете (без учета стоимости лекарственных препаратов) | 1 000 | процедура |
| Лекарственная сопроводительная терапия: внутримышечное введение в процедурном кабинете (без учета стоимости лекарственных препаратов) | 200 | процедура |
| Топометрическая разметка | 750 | процедура |
Вид лучевой терапии и количество сеансов курса определяется врачебной комиссией индивидуально для каждого пациента исходя из локализации, нозологии опухоли и с учетом анамнеза.
Часто задаваемые вопросы
Сколько стоит курс лечения?
Курс лечения вместе с предлучевой подготовкой стоит 258 000 рублей. Есть возможность оформления рассрочки на весь период лечения.
Есть ли онлайн-консультация?
Для жителей других регионов, а также для тех, кому визит к врачу затруднителен, наш центр предоставляет возможность бесплатной онлайн - консультации.
Документы, которые необходимы для получения онлайн-консультации?
Для получения консультации о возможности получения томотерапии, вам необходимо направить нам все имеющиеся у вас медицинские выписки и обследования, включая гистологическое заключение. Направление на бесплатную консультацию не требуется.
Возможно ли лечение детей?
Томотерапия наиболее благоприятна для лечения детей, так как лучевая терапия проходит щадящим методом, не задевая здоровые органы и ткани развивающегося ребенка.
На какой стадии можно применять лучевую терапию?
В современной онкологии возможности лучевой терапии применяются очень широко на любой стадии. Однако каждому пациенту требуется индивидуальный подход, так как выбор тактики и плана лечения зависит от многих факторов: расположения опухоли, сопутствующих заболеваний, возраста и общего состояния пациента. Поэтому для получения информации о возможности лечения, необходимо получить консультацию врача-радиотерапевта.
Дата написания: 07.09.18
Дата обновления: 29.11.19
Проверил: Моров Олег Витальевич
Читайте также:

