Лечение рака при паркинсоне
Существуют данные, согласно которым патогенетические механизмы, лежащие в основе нейродегенеративных заболеваний, в особенности болезни Паркинсона, могут перекликаться с патогенетическими механизмами развития определенных типов рака. Выявление этих взаимосвязей может помочь разобраться в патогенетических изменениях, происходящих при обоих заболеваниях, а также обеспечат дополнительный инструмент для оценки риска развития рака у пациентов с болезнью Паркинсона и их родственников.
Для выяснения взаимосвязи между болезнью Паркинсона и раком исследователи из университета штата Юта (Солт-Лейк-Сити) проанализировали данные, содержащиеся в архиве и онкологическом регистре штата. В последнем содержится информация о 100 817 пациентах с онкологическими заболеваниями. При проведении анализа было идентифицировано 2 998 человек, в качестве причины смертей которых, произошедших в период с 1904 по 2008 гг., была указана болезнь Паркинсона.
Сопоставление результатов анализа двух баз данных выявило выраженное увеличение риска развития рака предстательной железы у пациентов с болезнью Паркинсона и их родственников. Анализ данных о 22 147 пациентах с раком предстательной железы и их родственниках подтвердил существование аналогичной закономерности, то есть повышении риска развития болезни Паркинсона в данной популяции.
Такая же двунаправленная закономерность выявлена и для меланомы. В данном случае выводы сделаны на основании анализа данных о 7 841 пациенте с данным онкологическим заболеванием и их родственниках.
Полученные результаты свидетельствуют о существовании одновременной наследственной предрасположенности к нейродегенеративным заболеваниям и определенным типам рака. Авторы считают, что результаты их работы предоставляют основу для будущего выявления генетических вариаций, приводящих к нейродегенерации у одних и развитию рака кожи или предстательной железы у других людей. Более того, они могут повлиять на стратегии скрининга, направленного на раннее выявление этих злокачественных заболеваний.
Читать статьи по темам:
Читать также:
Причина седины – сигнальный путь Wnt
Поседение обусловлено нарушением сигнального механизма, опосредованного белком Wnt, участвующим в регуляции множества биологических процессов, в т.ч. – взаимодействия между двумя типами стволовых клеток волосяных фолликулов.
Упаковка противоопухолевых антител в пористые частицы из химически модифицированного оксида кремния повышает эффективность их действия на злокачественную опухоль кожи – меланому.
День диагностики меланомы
18 мая 2009 года в России уже в 3 раз пройдет День диагностики меланомы. Жители 27 крупнейших городов РФ смогут бесплатно получить консультацию и пройти обследование пигментных образований на коже.
Экспресс-тест выявит меланому
Развивающуюся меланому и доброкачественную родинку теперь можно различить с помощью экспресс-теста на пять маркерных белков опухоли. Разработчики довели специфичность своего метода до 95%, а чувствительность до 91%, что для онкологии весьма впечатляющие результаты.
Идентифицирован механизм, обеспечивающий метастазирование меланомы
Расшифровка мехнизма запуска сигнального каскада, повышающего подвижность и инвазивность опухолевых клеток, открывает еще одну потенциальную молекулярную мишень для лечения меланомы, а, возможно, и других типов рака, в том числе рака молочной железы и желудка.
Электронное СМИ зарегистрировано 12.03.2009
Свидетельство о регистрации Эл № ФС 77-35618

ТАСС, 16 декабря. Нилотиниб, популярный препарат для борьбы с раком крови, успешно прошел клинические испытания в качестве лекарства от болезни Паркинсона. Эти опыты подтвердили не только его безопасность, но и эффективность даже в крайне малых дозах, пишут ученые в журнале JAMA Neurology.
- Невесомость применили для реабилитации пациентов с болезнью Паркинсона
- Ученые в Новосибирске приступили к клиническим испытаниям лекарства от болезни Паркинсона
- Редактирование генов научились использовать для лечения болезни Паркинсона
"Наши наблюдения показывают, что пациенты, принимавшие нилотиниб, впоследствии лучше справлялись с тестами на подвижность и меньше страдали от различных проблем с качеством жизни, чем члены контрольной группы. Это говорит, что данный препарат стабилизировал болезнь, чего мы не наблюдали в опытах с любыми другими лекарствами", - заявил Фернандо Паган, профессор университета Джорджтауна (США), чьи слова приводит пресс-служба журнала.
Болезнь Паркинсона, как объясняет ученый, развивается в результате разрушения так называемой черной субстанции в мозге - особого отдела, который генерирует дофамин, гормон удовольствия, и направляет его в двигательные центры в глубинных слоях мозга. Разрушение черного вещества приводит к тому, что человек начинает плохо двигаться, теряет баланс и испытывает боль при движении.
Как и в случае со многими другими нейродегенеративными заболеваниями, ученые пока не до конца понимают природу развития болезни Паркинсона и не знают, как ее можно вылечить или хотя бы остановить ее развитие. Существующие препараты, такие как леводопа или стимуляторы активности дофаминовых рецепторов, могут лишь подавлять некоторые ее симптомы на первых этапах развития, а также обладают серьезными побочными эффектами.
Примерно пять лет назад, как отмечают Паган и его коллеги, их команда и другие группы ученых заметили, что популярное лекарство от рака - нилотиниб - не только замедляет размножение опухолевых клеток, но и мешает формированию токсичных белковых молекул, альфа-синуклеина и тау-белка, считающихся главной причиной смерти нейронов в черном веществе мозга.
Новая надежда
Данное свойство нилотиниба натолкнуло нейрофизиологов на мысль, что это вещество может замедлить развитие болезни Паркинсона. Ученые давно хотели провести клинические испытания с применением данного лекарства, однако этому мешало то, что нилотиниб считался крайне опасным для здоровых людей из-за небольшой, но существенной вероятности вызвать внезапную смерть при приеме в дозах, необходимых для лечения рака.
Недавно Паган и его команда получили разрешение на подобные эксперименты, в рамках которых они использовали минимальные дозы нилотиниба. Для этих опытов ученые собрали группу из семи десятков пожилых людей, страдавших от тяжелых форм болезни Паркинсона, согласившихся принимать противораковый препарат на протяжении года.
Изначально, как отмечает нейрофизиолог, эти эксперименты были нацелены только на проверку безопасности лекарства для здоровья пациентов, однако вскоре ученым стало ясно, что даже небольшие дозы нилотиниба заметно улучили состояние их подопечных. В частности, концентрация альфа-синуклеина и тау-белка уменьшилась на 20% и 30% соответственно, а концентрация дофамина в их организме выросла на 50%.
Кроме того, когнитивные показатели и уровень контроля над телом не изменился у пациентов, принимавших лекарство, тогда как и то, и другое значительно ухудшилось у представителей контрольной группы. Это означает, что нилотиниб остановил или резко замедлил развитие болезни Паркинсона.
Как подчеркивают ученые, ни один из добровольцев, принимавших небольшие количества нилотиниба, не жаловался на побочные эффекты и не вышел из эксперимента по подобным причинам. По мнению авторов статьи, все это говорит о том, что в ближайшее время следует начать более масштабные клинические испытания третьей фазы. Успешное завершение испытаний позволит бороться с болезнью Паркинсона при помощи этого препарата.
Болезнь Паркинсона – хроническое неврологическое заболевание, отличающееся медленной прогрессией. Согласно статистике, этим заболеванием страдают около ста человек на каждые сто тысяч населения, причем, мужчин оно по какой-то причине поражает чаще, чем женщин. Обычно эта болезнь развивается у людей в возрасте старше шестидесяти лет, но бывают и печальные исключения. Сама по себе эта болезнь – большое несчастье, поскольку пока не поддается лечению.
Однако ученые из Тайваня недавно сообщили о том, что, помимо всех проблем и сложностей, которые приносит с собой болезнь Паркинсона, согласно результатам их исследований, данное заболевание может также резко увеличить риск развития определенных онкологических заболеваний.
Такие выводы были сделаны тайваньскими исследователями, вопреки опубликованным ранее многочисленным научным работам, авторы которых заявляли, что наличие у пациента болезни Паркинсона как раз снижает для него риск возможности развития злокачественных опухолей.
Свои необычные выводы, ученые из Тайваня сделали по результатам изучения более чем шестидесяти двух тысяч историй болезни мужчин и женщин, граждан их страны, страдающих болезнью Паркинсона. Важно отметить, что диагноз этим пациентам был поставлен в течение 4 лет, в период с 2010 по 2014 год.
Результаты исследования сравнивались учеными с медицинскими историями более чем ста двадцати четырех тысяч жителей Тайваня обоих полов, у которых на момент начала исследования не было обнаружено никаких неврологических заболеваний. Они составляли в исследовании так называемую контрольную группу.
Изучая и сравнивая истории болезней людей из обеих групп, исследователи из Тайваня выяснили, что наличие болезни Паркинсона повышает риск развития таких видов злокачественных опухолей, как рак кожи, рак легких, онкология мочеполовых органов, злокачественные образования желудочно-кишечного тракта, онкологию мозга, рак предстательной железы и так далее – всего наличие болезни Паркинсона может спровоцировать развитие шестнадцати видов онкологии. Практически все они относятся к широко распространенным видам раковых заболеваний, ежегодно уносящих тысячи жизней во всем мире.
Однако, подчеркивают тайваньские ученые, в этот список не входят злокачественные новообразования яичников, онкология щитовидной железы и самая распространенная среди женщин, онкология молочной железы.
Исследователи из Тайваня считают, что данными их работы обязательно должны воспользоваться врачи-неврологи, занимающиеся лечением болезни Паркинсона – по необходимости им стоит направлять своих пациентов на онкологические обследования.
Любопытно, что причины связи болезни Паркинсона и онкологических заболеваний учеными до сих пор не обнаружены, однако они уверены в существовании связующего фактора – фактора риска и в настоящее время работают над тем, чтобы выявить его и определить принцип его действия.
Задать вопрос врачу онкологу
Диагностка и лечение онкологии в медицинских центрах Израиля подробная информация
Подпишитесь на рассылку Новости онкологии и будьте в курсе всех событий и новостей в мира онкологии.
Отделение кардиологии и кардиохирургии
Отделение пластической хирургии
Лечение псориаза на Мертвом море
Лечение радиоактивным йодом
Отделение внутренних болезней
CHECK-UP в Израиле
Передовые методы лечения

Согласно новому исследованию, проведенному учеными из Лестерского университета, пациенты с болезнью Паркинсона могут извлечь пользу из приема лекарств, используемых для лечения онкологических заболеваний.
В своей работе, опубликованной в Science Matters, исследователи предположили, что фолиновая кислота, которая применяется в терапии рака кишечника, может защитить нейроны, связанные с болезнью Паркинсона у плодовых мушек.
Болезнь Паркинсона – это неврологическое заболевание, которое на данный момент является неизлечимым. После того, как дофаминергические нейроны в организме пациента гибнут, врачи могут использовать лишь несколько паллиативных вариантов лечения симптомов болезни. Поэтому так важно разработать способы терапии, которые предотвратят, либо замедлить развитие заболевания на ранней стадии.
Фолиновая кислота уже используется врачами в качестве адъюванта во время химиотерапии. Она может применяться перорально, внутривенно и в форме пищевой добавки. Таким образом, угроза безопасности препарата очень низкая, а разработка нового лекарственного средства на основе фолиновой кислоты для лечения болезни Паркинсона будет более быстрой, чем разработка другого нового препарата.
В своем исследовании ученые изучили плодовых мушек с дефектными митохондриями, которые были вызваны мутациями, имитирующими болезнь Паркинсона у человека. Они выяснили, что фолиновая кислота оказывала влияние на нейроны у плодовых мух.
Ученые сообщили, что необходимо протестировать фолиновую кислоту в клинических исследованиях и определить, может ли она стать потенциальным профилактическим или паллиативным терапевтическим средством для пациентов с болезнью Паркинсона.

Процесс терапии неврологии в Израиле может подразумевать хирургическое лечение или принятие пациентов определенной группы лекарственных препаратов.

Исследование на плодовых мушках. Включение в рацион ниацина может помочь в лечении наследственной формы болезни Паркинсона.

Ученые создали алгоритм прогнозирования когнитивных нарушений у пациентов с болезнью Паркинсона. Он может помочь предотвратить когнитивный спад и разработать новые лекарства.

Открытие структуры нитей тау-белка поможет в разработке препаратов для лечения болезни Альцгеймера
Ученые разработали новый препарат, который может уничтожить раковые клетки нейробластомы и остановить метастазирование.
Для связи с медицинским консультантом заполните форму:
Отправляя форму Вы соглашаетесь с политикой конфиденциальности
Точечный удар по раку

Этим и объясняется тот факт, что лучевая терапия и другие меры помогают не всем, поскольку раковые клетки каждого человека реагируют на лечение индивидуально.
Преимущества новой диагностики по сравнению со старыми методами в том, что каждого пациента можно будет лечить персонально, назначать ему наиболее эффективный набор лекарств. Научные разработки в этом направлении ведутся во всём мире. В Казани подходит к концу цикл тестирования метода на животных. Скоро - черёд испытаний на людях.
Маркировка недуга
Ещё одна разработка казанских учёных, но на этот раз под руководством московского коллеги академика Михаила Угрюмова из Института биологии развития им. Н.К.Кольцова РАН – маркёры для распознавания рисков заболевания болезнью Паркинсона на доклинической стадии. По ним, предположительно, можно будет определять предрасположенность пациента к заболеванию. В скором времени учёные проверят свои исследования на реальных пациентах. Экспедиция отправится в один из районов Татарстана, где будет обследовано более 150 человек на ранней стадии болезни.

Дело в том, что болезнь Паркинсона в течение 20-30 лет может протекать скрыто. Еcли предрасположенность к ней заметить вовремя и начать лечение, то проявления её симптомов – неконтролируемого дрожания частей тела – можно если не исключить, то резко замедлить. - За притормаживание работы мышц в организме отвечают специальные нейроны, - рассказывает профессор кафедры нормальной физиологии КГМУ Разина Нигматуллина. - У нездорового человека нейроны постепенно отмирают, и когда их количество становится меньше определённого значения (порога), мышцы начинают трястись. Задача учёных – отсрочить гибель нейронов на длительное время и не допустить достижения пороговых показателей. Когда это удастся сделать, значительная часть больных не будет испытывать дискомфорта до естественной смерти.
Результатом разработки должен стать набор маркёров DiaPark, с помощью которых кровь пациента будут исследовать на состояние тех самых нейронов.
По словам Разины Рамазановны, сейчас в мире нет безопасной и доступной диагностики по выявлению заболевания. Поэтому цель учёных - найти способ недорогого и качественного обследования. Важно, чтобы оно стало доступным на всех уровнях медучреждений, вплоть до районных больниц. Если верить статистике, сейчас в России болезнью Паркинсона страдают 2,2 млн человек, ещё 4-6 млн их родственников обеспокоены своим здоровьем и хотят пройти обследование. Самый современный способ диагностики болезни Паркинсона сегодня – позитронный томограф. Приборы уже используют в Израиле, Европе и Америке, в России их пока ещё нет. Существенный недостаток томографа в том, что он не может обеспечить высокую пропускную способность, его не применяют при диспансеризации населения. Новые способы ранней диагностики при помощи DiaPark можно будет использовать во время массовых медосмотров населения начиная с 35-40-летнего возраста.
Плохие новости для любителей газировки: употребление двух или более стаканов напитка в день значительно повышает шансы летального исхода. Напротив, максимум один стакан в месяц существенно снижает соответствующие риски. В исследовании, результаты которого представлены в журнале JAMA Internal Medicine, в течение 19 лет приняли участие свыше 450 тыс. человек. К моменту начала наблюдений ни у кого из них не было выявлено рака, диабета или инсульта.
Как показал эксперимент, выпивавшие в день не менее двух стаканов (0,5 л) подслащенных безалкогольных напитков мужчины и женщины увеличивали свои шансы умереть от недугов, связанных с ЖКТ, в то время как употребление простой газировки приближало риск смерти от сердечно-сосудистых заболеваний.
«Наши данные свидетельствуют о том, что высокий уровень сахара в крови, вызванный в том числе газированными напитками,
может спровоцировать воспаление кишечника, изменив кишечную микробиоту и повысив восприимчивость к кишечным инфекциям.
Помимо прочего, употребление газировки в больших объемах приводит к повышению риска болезни Паркинсона, отмечают ученые.
В свою очередь, президент Совета по контролю калорий (CCC) Роберт Рэнкин подверг исследование критике, отметив, что оно дает искаженную картину вредности конкретных продуктов для потребителей. По его словам, низкокалорийные подсластители досконально изучены и являются безопасными.
Другое исследование, охватившее более 100 тыс. жителей Франции, показало, что употребление всего лишь трети банки или 100 мл сладкой газировки увеличивает риск возникновения рака до 18%.
Вероятность заболевания раком молочной железы возрастает при этом до 22%.
Эта же статистика актуальна для свежевыжатых соков.
Фанатам газировки ученые рекомендуют пить воду с добавлением кусочков ягод или фруктов.
Кроме того, на 20% возрастает риск онкологического заболевания у людей, употребляющих до 76 гр красного мяса в день. Алкоголь повышает вероятность развития рака на 8%.
Весьма опасным является растительное масло для жарки, которое влияет на развитие воспалительных заболеваний кишечника и провоцирует рак толстой кишки. Специалисты советуют использовать масло в свежем и холодном виде.
Ранее ученые из Массачусетского университета в Амхерсте установили, что жареная на растительном масле пища может привести к осложнению ракового заболевания.
По словам исследователей, многие люди в США в той или иной степени имеют проблемы с ЖКТ, однако не отказывают себе в удовольствии употреблять фаст-фуд и вредную жареную еду.
В целях получения необходимых сведений ученые ставили эксперименты на мышах: опухоль у грызунов двукратно увеличивалась в размерах, а также прогрессировал колит. Исследователи предлагали своим подопытным комбинации из пищи, в том числе приготовленной с использованием менее вредного оливкового масла. Эксперименты доказали, что растительное масло ухудшало состояние здоровья грызунов в каждом случае.
Жирная пища является одним из факторов, повышающих риск возникновения раковых опухолей.
Ранее ученые назвали пять главных онкозаболеваний в России, расположив их по убыванию: 13,2% – молочная железа; 11,3% – легкие (в основном мужчины, но в последнее время растет обнаружение рака легких у молодых некурящих женщин); 7,4% – простата; 6,5% – желудок; 4,8% – тело матки. Остальные 56,9% делят между собой другие виды рака.
О возникновении ракового заболевания могут свидетельствовать не проходящий долгое время кашель, охриплость голоса, не связанная с простудой, и трудности при глотании слюны, а также диарея или запор.
К симптомам рака относятся пониженный уровень эритроцитов, анемия, участившееся мочеиспускание, которое становится болезненным, кровь в моче и не проходящее на протяжении месяца увеличение лимфатических узлов.
При этом медики считают, что сдавать кровь на онкомаркеры для выявления заболеваний не имеет большого смысла.
Необходимо ограничиться УЗИ брюшной полости и малого таза, фиброгастроскопией, а женщинам еще следует делать маммографию. Также указывается, что нужно сдавать анализ кала на скрытую кровь — это позволит диагностировать рак кишечника.
Почему ученые не могут понять, как возникает болезнь Паркинсона, можно ли ее унаследовать и когда может появиться первое эффективное лекарство от заболевания?
Сотрудница Института трансляционной биомедицины СПбГУ Наталия Католикова рассказывает о проблемах в изучении и лечении болезни Паркинсона.
Как проявляется болезнь Паркинсона
— Болезнь Паркинсона относится к так называемым нейродегенеративным заболеваниям, для которых характерна постепенная гибель различных типов нейронов, что приводит к снижению или выпадению каких-либо функций центральной нервной системы. К этой же группе относится и болезнь Альцгеймера.
Почему болезнь Паркинсона нельзя диагностировать до первых симптомов
— Ранняя диагностика этой болезни — очень большая проблема. И поиск новых методов диагностики — одна из приоритетных задач, которые стоят перед исследователями. Сейчас диагноз ставится на основании клинических проявлений, а они появляются, только когда погибли уже около 80 % дофаминергических нейронов.
Также в постановке диагноза может помочь позитронно-эмиссионная томография (ПЭТ) головного мозга, но это достаточно дорогостоящая процедура и провести ее возможно не везде.
Первые проявления болезни бывают разные. Мне сложно сказать, какие симптомы станут первыми, поскольку я не работаю с пациентами, но, насколько я знаю, чаще всего поводом для обращения к врачу становится появление тремора рук и некоторая заторможенность пациентов. На остальные же симптомы больные обращают внимание уже после визита к врачу, когда им начинают задавать конкретные вопросы [о симптомах].
Кто подвержен болезни Паркинсона и почему причины ее возникновения неизвестны
— Паркинсон — это болезнь пожилых людей. Около 1–2 % вероятность возникновения после 60 лет, до 3 % — после 80. Бывают и более ранние формы болезни, но они встречаются очень редко. У молодых людей возникновение болезни Паркинсона может быть связано с каким-то токсическим воздействием.
Развивается болезнь тоже очень по-разному. У кого-то быстро, у кого-то — на протяжении 20 лет. С чем это связано, пока не очень понятно. Скорее всего, с особенностями генетического бэкграунда каждого человека.
Говорить о причинах возникновения болезни Паркинсона сейчас очень сложно. Исследователи рассматривают генетические причины, но процент таких случаев очень небольшой, около 20 %. Есть некоторое количество генов, мутации в которых, предположительно, могут привести к болезни. Так что генетика в данном случае имеет влияние, но не прямое. Болезнь родственников, например, не повлияет на развитие Паркинсона.
То есть причины могут быть разными, но в целом науке сейчас неизвестно, что является непосредственной причиной болезни Паркинсона.
Многие заболевания, связанные с центральной нервной системой, сложны в расшифровке, потому что сама эта система очень сложно организована. Отсюда и проблемы с диагностикой и изучением причин развития болезни Паркинсона.
Как лечат болезнь Паркинсона и почему она прогрессирует даже при лечении
— На данный момент болезнь Паркинсона неизлечима, есть только симптоматическое лечение. Основной препарат для лечения болезни Паркинсона — L-DOPA. Это предшественник дофамина, который в мозге человека превращается в дофамин и на какое-то время восполняет его недостаток.
Помимо L-DOPA используются и другие препараты, которые влияют на дофаминергическую систему, а также препараты, убирающие некоторые симптомы болезни. Но в двух словах можно сказать, что суть лечения сводится к стимулированию дофаминергической системы, чтобы восполнять утраченные функции мозга.
Но у современного лечения есть много недостатков. Во-первых, лекарства не лечат саму болезнь, и она постоянно прогрессирует. Во-вторых, препараты не могут полностью заместить утраченные функции. В-третьих, прием L-DOPA приводит к развитию побочных эффектов, основной из которых — привыкание, необходимость постоянного увеличения дозы препарата.
Кроме того, возникает L-DOPA-индуцированная дискинезия — неконтролируемые движения, связанные с приемом препарата. Чем именно вызвана дискинезия, на данный момент неясно, и поэтому непонятно, как это можно лечить.
Современное лечение нельзя назвать достаточно эффективным. Но его всё равно нужно обязательно проходить: оно облегчает жизнь и на какое-то время позволяет вернуться к относительно нормальному состоянию и контролировать проявления болезни. Кому-то это лечение может помогать не один десяток лет.
Когда может появиться эффективное лекарство от болезни Паркинсона
— Сейчас есть большой интерес к заместительной клеточной терапии, то есть созданию определенного типа клеток, которые помогут замещать утраченные функции. Болезнь Паркинсона стала одним из первых направлений, где такое лечение уже дошло до клинических испытаний, проверки эффективности и безопасности препарата на людях.
Несколько клинических испытаний лечения от болезни Паркинсона уже начаты. Еще несколько должны начаться в конце 2019-го — начале 2020-го. В каждом случае используются разные источники дофаминергических нейронов. При этом надо отметить, что исследователи в разных частях мира не работают по-отдельности, пытаясь опередить друг друга, а объединились в сообщество, которое встречается раз в год и делится полученными результатами. Вместе они выявляют какие-либо сложности, особенности, новые подходы. Именно это и нужно для как можно более быстрого решения проблемы.
Первые испытания были начаты в прошлом году в Японии, и уже в ноябре 2018 года первому пациенту пересадили [необходимые клетки]. В Китае тоже начали клинические испытания, но я не знаю, на каком этапе они находятся. Также в ближайшее время должны быть начаты клинические испытания в Швеции и США. Надеюсь, что со временем подключится и Россия.
Результаты японских испытаний должны стать известны к 2023 году.
Что делать, чтобы снизить риск заболевания
Специфической профилактики болезни Паркинсона нет. Но есть рекомендации по профилактике нейродегенеративных заболеваний в целом.
Сводятся эти рекомендации к ведению здорового образа жизни. Нужен нормальный режим работы, физическая активность: было доказано, что бег значительно снижает прогрессию таких заболеваний. Показана любая мелкая моторика и игра на музыкальных инструментах. Кроме того, здоровое питание. Некоторые наркотические вещества могут быть токсичными для дофаминергических нейронов, так что стоит избегать вредных привычек.
Именно в этот день, только несколько столетий назад, 11 апреля 1755 года, родился английский врач Джеймс Паркинсон. Именно он первый описал эту болезнь. После чего ее так и стали называть - болезнь Паркинсона.
А семь лет назад Всемирная организация здравоохранения решила отмечать эту дату ежегодно. Чтобы постоянно информированность людей о заболевании, окоторое представляет собой прогрессивные дегенеративные нарушения центральной нервной системы.
По данным ВОЗ, в России им страдают 200 человек из каждых 100 тысяч - в равной степени как мужчины, так и женщины. И причины возникновения болезни до конца не известны - это и атеросклероз сосудов мозга, и травмы, и генетические дефекты…
При этом паркинсонизм относится в заболеваниям возрастным - среди людей старше 60 лет с ней живут 2%. Хотя первые звоночки могут появиться в 40 лет и даже раньше, как, к примеру, у Мохаммеда Али.
Есть целый ряд симптомов, сопутствующих данной болезни - потеря равновесия, вялость в движении, иногда запор, нарушения сна, изменения настроения и так далее. Но главное проявление паркинсонизма - это дрожание и непроизвольные движения рук и ног. Так называемый тремор.
И для того, чтобы облегчить жизнь людям с тремором, был создан необычный девайс. По сути, он представляет из себя перчатки. На тыльной стороне каждой закреплена батарея, управляющая платой и гироскопом - именно он противодействует дрожанию конечностей благодаря своему постоянному вращению.
Такая “противофаза" гасит от 80 до 90% дрожания рук. При этом сами движения становятся плавными и размеренными (люди, которые участвовали в контрольных исследованиях, отмечали, что у них возникало ощущение, будто рука перемещается в вязком сиропе или мёде).
Как правило, болезнь Паркинсона развивается постепенно, а потому незаметно для человека. Когда же недуг становится явным, поделать ничего уже нельзя. Поэтому для обнаружения когнитивных изменений, которые сигнализируют о начале проблем, исследователи из Массачусетского технологического института создали специальную компьютерную программу, которая позволяет ставить диагнозы на ранних стадиях заболевания.
По сути она представляет из себя цифровое перо, с помощью которого пациента просят нарисовать рисунок, например, часовой циферблат. При этом перо фиксирует и передает в компьютерную программу каждый момент “художества”, направление и положение руки рисовавшего, контролирует тысячи мельчайших элементов рисунка, определяет,сколько штрихов пациент сделал, сколько времени думал, прежде чем сделать рисунок, насколько часы можно считать законченными, нет ли в рисунке разрывов и неровностей. Это все позволяет выявить когнитивные нарушения со стопроцентной точностью!
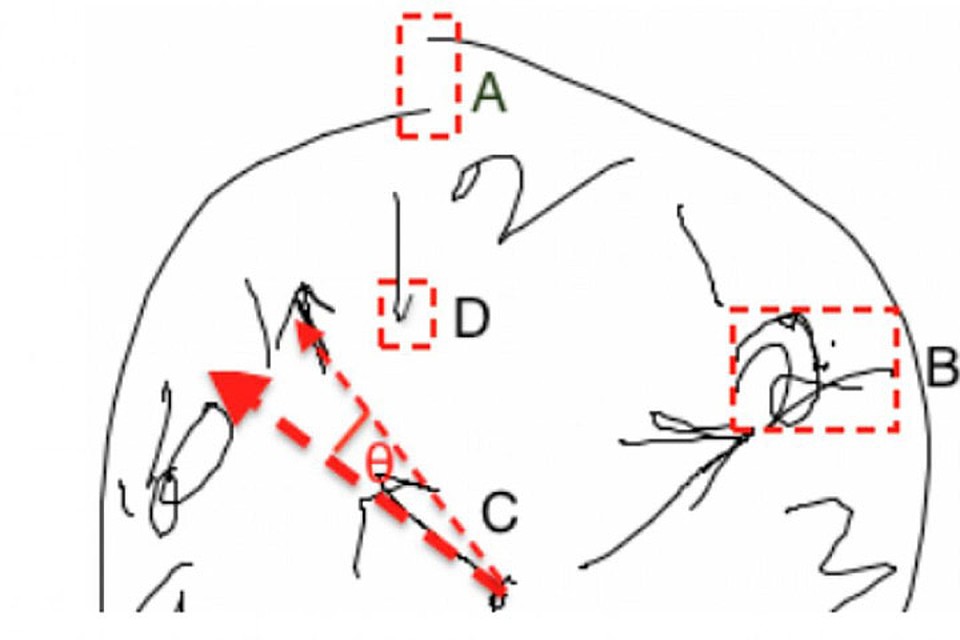
А еще диагностировать нейродегенеративные заболевания на ранней стадии поможет скрин кожи. Специалисты из Университета Сан-Луис-Потоси выяснили, что кожная проба позволяет обнаружить определенные белки, связанные с заболеваниями Альцгеймера и Паркинсона.
А вот ученые Университетского колледжа Лондона обнаружили, что смерть синапсов в мозге связана с активностью неправильно работающих белков Wnt. Они атакуют синапсы - соединения клеток мозга, и те отмирают. Как результат развивается болезнь Паркинсона.
Следовательно, если воздействовать на эти белки, (как называют их специалисты - "агенты"), то можно остановить развитие болезни. Каким образом? Создать лекарство, которое будет контролировать работу Wnt.
Неврологу Патрику Верстрекену с коллегами из Северного Иллинойсского университета удалось справиться с генетическим дефектом, вызывающим болезнь Паркинсона - за счет витамина К2. Известно, что митохондрии вырабатывают энергию в клетке, перенося электроны. У пациентов с паркинсонизмом в первую очередь нарушается эта функция. То есть клетка лишается энергии и начинает угасать, связи нейронов рушатся. И сигнал от мозга к конечностям идет неполноценный.
А инъекции витамина К2, отвечающего за свертываемость крови и сосудистую проводимость, улучшали выработку энергии в митохондриях. И нейронные связи восстанавливались. Во всяком случае испытания на лабораторных животных дали хорошие результаты.
Основные симптомы болезни Паркинсона:
1. Скованность и замедленность движений, как правило, начинаются в правой половине туловища, а затем, через некоторое время, постепенно захватывают и другую сторону.
3. Походка становится шаркающей и семенящей. У человека смещается центр тяжести, он теряет равновесие и даже падает.
4. Когда пациент не двигается, его руки и подбородок отчетливо дрожат, а вот во время движения тремор не наблюдается.
6. Несмотря на то, что интеллект сохраняется, мышление и внимание замедлены.
7. Как сопутствующие нарушения встречаются: снижение обоняния, запоры, нарушения мочеиспускания.
ЧИТАЙТЕ ТАКЖЕ:
10 признаков надвигающейся болезни Альцгеймера
Если вы обнаружите у себя хотя бы один из нижеследующих симптомов, немедленно обратитесь к врачу - в данном случае лучше перебдеть. Будем надеяться, что это окажется ложной тревогой. А при раннем обнаружении деменции развитие можно замедлить (дальше).
Читайте также:

