Лечение рака крови новейшие методы лечения
По данным Минздрава РФ, только в 2018 году в мире было зарегистрировано около 18 миллионов новых случаев рака и других злокачественных новообразований. Всемирная организация здравоохранения (ВОЗ) утверждает, что с онкологическими заболеваниями сталкивается каждый пятый мужчина и каждая шестая женщина.
Новые методы лечения рака позволяют помочь пациентам, которые ранее могли рассчитывать только на паллиативную помощь.
Люди, далекие от медицины и сами врачи связывают терапию онкологических заболеваний с массивными, калечащими операциями, изнуряющей химиотерапией, которая переносится тяжелее, чем сами симптомы болезни, долгим восстановлением и постоянным страхом, что болезнь вернется.
Как развивается рак
Клетки организма размножаются делением и начинают умирать после 50-52 циклов. Процесс естественной гибели называется апоптоз. Зараженные вирусом, мутирующие клетки выставляют на своих оболочках специальные маркеры. Их распознает и немедленно уничтожает иммунная система. Соседние клетки утилизируют продукты распада.
Бесконтрольное размножение приводит к тому, что клетки не успевают созревать, утрачивают свои свойства. Они распространяются в окружающие ткани или мигрируют с кровью, лимфой, образуя метастазы. Канцерогенез - процесс перерождения обычных клеток в атипичные.
Как работает традиционное лечение
Стандартные современные методы лечения рака направлены на уничтожение опухоли различными способами:
- оперативное вмешательство;
- введение химиопрепаратов;
- лучевая или радиотерапия
- иммунотерапия
При хирургическом лечении врач удаляет массив атипичных клеток. К недостаткам метода относят невозможность убедиться на месте, что рак удален в полном объеме, и сложность проведения операции в труднодоступных местах.
Во время химиотерапии пациент получает лекарства, которые нарушают жизнедеятельность, тормозят размножение клеток опухоли или стимулируют их апоптоз. Препараты воздействуют и на здоровые ткани организма, что ухудшает переносимость лечения. У ряда пациентов рак может и не реагировать на стандартные средства.
Радиотерапия борьба с опухолью различными видами излучения. Она повреждает ДНК быстро делящихся клеток, приводя к их гибели. Недостаток метода заключается в невозможности прицельного воздействия только на патологический очаг.
Чтобы стандартное лечение помогло пациенту, необходимо стечение обстоятельств:
- небольшой размер и хорошая доступность первичной опухоли,
- низкая злокачественность и хороший ответ на препараты,
- хорошая переносимость курса терапии.
А как же быть тем, чья история борьбы с раком осложнена отягчающими обстоятельствами? В области онкологии новости лечения связаны с преодолением стандартных проблем терапии:
- нечувствительность рака к препаратам или облучению;
- невозможность воздействия только на клетки опухоли;
- большой объем образования и риск непереносимости терапии;
- риск оставить рак на месте после операции.
Если иммунная система пропускает начало опухолевого процесса, болезнь прогрессирует. Раковые клетки действуют хитростью, маскируя свои рецепторы специальными белками.
Микробиологи изобрели так называемые моноклональные антитела. Это белковые молекулы, имеющие сродство только к определенным рецепторам. Антитела связываются с раковыми клетками, не только делая их видимыми для иммунной системы, но активируя их уничтожение.
Моноклональные антитела созданы для молекул, отвечающих за развитие разных заболеваний. Этот принцип лег в основу таргетной (прицельной) терапии. Например, препарат Ритуксимаб эффективен при лечении B-клеточных лимфом, Цетуксимаб для борьбы с раком толстой и прямой кишки, опухолями головы и шеи. Бевацизумаб применяют при опухоли молочной железы, толстого кишечника, головного мозга и немелкоклеточном раке легких.
Эти медикаменты доступны и в России. Первое время их производством занимались только иностранные компании. Пациенты с нечувствительностью к стандартной химиотерапии могли опасаться, что препарат не придет вовремя или будет стоить дороже. С 2012 года российская компания Biocad производит биоаналоги: Гертикад, Авегра, Ацеллбия.
CAR-T – найти и уничтожить
Универсальный рецептор на поверхности позволяет настраивать иммунитет против разных опухолевых антигенов. T-клетки легко проникают внутрь раковой опухоли. Так CAR-T позволяет уничтожать самые мелкие метастазы в головном и спинном мозге, снижая риск рецидива. Генную терапию считают более эффективной по сравнению с моноклональными антителами.
Достижения иммунной терапии
Среди последних новостей в онкологии – официальное разрешение американской федерации FDA на применение CAR-T в борьбе с B-клеточными лимфомами. Препарат Yescarta - лишь второе такое средство за всю историю генной терапии.
Ученые доказали, что применение моноклональных антител в комплексе с CAR-T – один из самых эффективных методов лечения рака у пациентов с плохой переносимостью и резистентностью к традиционной химиотерапии. Так у пациентки с 4 стадией карциномы молочной железы уменьшился в объеме первичный очаг и его метастазы.
В 2018 году Нобелевская премия за метод лечения рака была присуждена двум ученым Джеймсу Эллисону (США). Их исследования продолжались более 20 лет и привели к открытию белка PD-1 и рецепторов CD152 на лимфоцитах, мешающих иммунитету находить и уничтожать раковые клетки. Затем ученые синтезировали препараты, которые решают эту проблему. В перспективе средства позволят увеличить выживаемость при опухолях различной локализации, в том числе при наличии метастазов.
Эти новые методы лечения рака доступны и в России. Среди зарегистрированных зарубежных препаратов: Китруда, Ервой, Тецентрик.
Диагностика и лечение с помощью света
Фотодинамическая терапия основана на использовании светочувствительных веществ (фотосенсибилизаторов) и лазерной установки. Их молекулы поглощают кванты света, уничтожая раковые клетки и разрушая сосуды, питающие опухоль. Невозможность прицельного воздействия лазера позволяла применять его только для видимых кожных опухолей.
Нижегородские ученые синтезировали флуоресцентный белок, который позволяет обнаруживать клетки опухолей. В 2012 году они получили патент на воспроизведение пептида, уничтожающего рак шейки матки в поле лазера.
Прицельное воздействие на опухоль
Радиотерапия сопряжена с риском получения массивного облучения. Во время лечения повреждаются не только раковые, но и здоровые клетки. К самым сложным локализациям опухоли относят голову и шею ввиду опасности повреждения головного мозга и крупных сосудов. Поражение зрения, слуха неизбежно снижает качество жизни пациента. Кроме того, до ряда опухолей нельзя добраться хирургическим путем.
Уничтожить такой рак помогает стереотаксическая гамма-терапии (или гамма-нож). Лучевые диагносты определяют точную локализацию и размеры образования, после чего в патологический очаг направляют до 200 лучей из разных точек. Единственная процедура занимает несколько часов и дает результат, сопоставимый с 30 сеансами облучения.
Гамма-нож – неинвазивная хирургическая процедура, которая позволяет пациентам возвращаться домой в день ее проведения. В 2019 году в России действует 6 установок, позволяющих помочь 3 тысячам пациентов в год. Новости онкологии в этой области обнадеживают онкобольных перспективами открытия 20 таких центров в стране.
Снизить повреждение окружающих тканей возможно благодаря замене рентгеновского излучения на протонное. Оно лучше концентрируется в очаге. В 2018 году немецкие ученые из Центра им. Гельмгольца Дрезден-Россендорф успешно соединили протонную терапию с МРТ-сканером. Ранее визуализацию опухолей выполняли с помощью компьютерной томографии, на которой хорошо отображаются только неподвижные костные образования. Среди новостей в лучевом лечении рака в 2019 году – создание прибора, позволяющего ввести протонное облучение в клиническую практику.
Экспериментальное лечение рака
Внедрение новых методик терапии возможно благодаря клиническим исследованиям. В ходе экспериментального лечения используются методы, эффективность и безопасность которых полностью не изучена. Онкологи проводят набор пациентов с определенным заболеванием. Они полностью обследуют кандидатов и отсеивают тех, кто не подходит по состоянию здоровья.
Лица, прошедшие скрининг, получают бесплатную экспериментальную терапию. К ней относят:
- генное лечение;
- локальное замораживание тканей;
- точечный нагрев тканей;
- применение бактерий-анаэробов;
- вакцины против рака;
- лечение лазером;
- нанотехнологии.
Участие в клинических исследованиях дает шанс выйти в ремиссию пациентам, которым не помогают стандартные схемы лечения.
Можно ли считать, что экспериментальная терапия позволяет победить рак? Исследователи рассказывают о протоколах с ошеломляющими результатами. Так при испытании препарата Китруда в 2013 году около 76% участников почувствовали облегчение, а полностью излечилось от рака около 20%. Так препарат был включен в схемы лечения различных агрессивных опухолей.
При обнаружении немедленных или отсроченных негативных последствий протоколы закрывают, а средства или методы не допускают до рутинной практики.
С 2018 года работает сервис, позволяющий онкологам России искать больницы, в которых проводят экспериментальную терапию, и направлять туда пациентов. Он создан непосредственно Агентством клинических исследований и Российским онкологическим обществом RUSSCO.
Последние новости в онкологии: что ожидать в 2019 году?
Специалисты в области клинической иммунологии, радиологии, регенеративных технологий из России принимали японских коллег. Трансляция семинара позволила коллегам из 38 регионов получить актуальную информацию о применении новых дендритно-клеточных вакцин от рака, культивировании стволовых клеток с помощью роботов, инженерных методиках.
Кроме того, среди новостей онкологии 2019 года в России - успешное внедрение органосохраняющих операций при раке легких и эндоскопическое удаление новообразования желудка и толстого кишечника.
1. Люминисценция. Метастазы рака заставляют светиться. Фотодинамическая терапия
Итак, ученые уже много лет проводят эксперименты не только над растениями. Свойства люциферазы и других генов, белков, ферментов или веществ (например, 5 - аминолевулиновой кислоты), способных давать люминисценцию активно исследуются для выявления новых методов диагностики и лечения рака уже более десяти лет.
-
Флуоресцентные нанозонды. Сегодня большинство операций по удалению опухолей и метастазов очень травматичны, т.к. не всегда можно визуализировать, где заканчивается опухоль и начинается здоровая ткань. В 2017 году профессор химии Хайинь Лю (Haiying Liu) из Мичиганского технологического университета (Michigan Technological University) нашел способ заставить клетки светиться так, что рак в буквальном смысле стало видно. Благодаря антителам, которые крепятся только к раковым клеткам, злокачественные опухоли светятся в около-инфракрасном диапазоне — другие ткани светятся зеленым или синим цветом. Этот же метод может позволить хирургу убедиться, что все клетки опухоли действительно удалены и не был пропущен ни один метастаз.
Помимо диагностики и лечения онкологии, разрабатываемые нанозонды могут применяться для диагностики других инфекционных, воспалительных, иммунных заболеваний и для адресной доставки лекарственных препаратов. Например, если вы заболели, вы принимаете антибиотики, которые накапливаются в тканях всего организма, убивая в том числе и полезные бактерии, негативно влияя на печень и другие внутренние органы. При помощи новых технологий лекарство будет доставляться только в участок инфекции или воспаления. Не влияя на здоровые ткани и органы. Российские и корейские ученые в Национальном исследовательском ядерном университете МИФИ совместно с Пхоханским университетом науки и технологии уже работают в этом направлении.



2. Генная терапия и вирусы
Иммунитет человека может бороться с онкологией сам. Но почему же этого не происходит? Дело в том, что рак, маскируется под нормальные, здоровые клетки человека, поэтому иммунитет его не распознает. Например, у раковых клеток больных лейкемией на поверхности есть белок CD19, который маскирует злокачественные клетки под нормальные, и они остаются незамеченными для иммунитета человека. Ученые нашли способ добавить к лимфоцитам больных гены рецепторы CD19 и вернут измененные клетки в организм больных лейкемией при помощи обезвреженных ретровирусов, обладающих способностью встраиваться в ДНК человека. Потерявшие маскировку раковые клетки были атакованы модифицированными лимфоцитами. 90% испытуемых, больных тяжелой формой лейкемии пошли на поправку.
Активно изучаются возможности использования вирусов для генной терапии:
не вызывает защитного ответа в раковых клетках

Настоящий прорыв совершили зарубежные учёные, найдя новый способ борьбы с раком крови, теперь, благодаря уникальным разработкам, победить этот страшный недуг можно даже в его последней стадии.
Как известно, лейкемия занимает одно из лидирующих мест в числе онкологических заболеваний. Именно эта форма рака характеризуется наиболее тяжёлым течением, а также для неё характерна ураганная форма развития. Болезнь прогрессирует стремительно, а чем тяжелее её стадия, тем сложнее оказать эффективную помощь.
Для борьбы с лейкемией сегодня в зарубежных клиниках используются самые разные методики, и результативность многих из них весьма высока. Тем не менее, способа гарантировано победить лейкемию до сих пор не существовало.
Американские учёные использовали в своих инновационных разработках генетическое программирование. Это самые современные технологии, доступные на сегодняшний день человечеству. Суть метода заключается в том, что у больных лейкемией, успешно излечившихся от недуга, отбирали кровь, программировали её на генетическом уровне, и на выходе получали вакцину, которую можно вводить больным лейкемией на любой стадии заболевания.
В результате введения такой запрограммированной вакцины злокачественные клетки начинали разрушаться, вступая во взаимодействие с вакциной. На данный момент испытания были проведены на экспериментальной группе, в состав которой вошли 30 человек. Испытания проводились на протяжении шести месяцев, при этом у всех испытуемых лейкемия была в стадии без шансов на излечение. По прогнозам врачей каждому из больных оставалось жить не более двух-трёх месяцев в условиях стационара.
По истечении шести месяцев из 30-ти испытуемых в живых осталось 23 человека, при этом 19 человек из 23-ёх полностью выздоровели, то есть находятся в стадии полной ремиссии. С учётом того, что все, кто принимал участие в эксперименте, имели неизлечимую форму лейкемии, можно говорить о невероятных результатах и эффективности терапии.
Где лечить онкологические заболевания?
На нашем сайте собрана информация о сотнях зарубежных медицинских учреждений, в которых можно провести высокоточную диагностику и эффективное лечение различных онкологических заболеваний. Это могут быть, например, такие клиники и центры, как:

Немецкий Онкологический клинический центр г. Фридрихсхафен предлагает пациентам эффективное лечение широкого диапазона злокачественных новообразований и обладает высоким авторитетом в мировой медицине. Помимо терапии, центр оказывает и услуги высокоточной диагностики различных форм рака. Перейти на страницу >>

Центр рака груди Klinik Pyramide am See в Швейцарии специализируется на диагностике и лечении рака молочной железы. Помимо высококачественных медицинских услуг и прекрасной технической оснащенности, центр отличается отличным сервисом и уютной атмосферой, созданной для каждого своего пациента. Перейти на страницу >>

Центр изучения рака в г. Эссен в Германии осуществляет свою деятельность при местном медицинском университете. Основная специализация центра - медикаментозное лечение широкого ряда онкологических заболеваний. Наряду с использованием классической химиотерапии, врачи внедряют и инновационные методики. Перейти на страницу >>

В работе швейцарского госпиталя Bethesda-Spital Basel заметное место отведено диагностике и лечению онкологических заболеваний. Кроме стандартных способов терапии рака, например, хирургического лечения или химиотерапии, врачи госпиталя успешно осуществляют на практике инновационные разработки. Перейти на страницу >>

Израильская клиника Пория располагает в своем составе Институтом онкологической дневной госпитализации, который предоставляет широкий спектр услуг для пациентов, страдающих различными онкозаболеваниями. В распоряжении Института имеется высокоточное оборудование для диагностики и лечения рака. Перейти на страницу >>
Каким должно быть питание при онкологических заболеваниях? Какие продукты абсолютно противопоказаны при той или иной форме рака?
Фитотерапия способна оказать существенную помощь не только в лечении онкологических заболеваний, но также и в их профилактике.
Многих людей, имеющих у себя или у родственников онкологическое заболевание, интересует вопрос: передается ли рак по наследству?
Лечение рака во время беременности является довольно сложным, ведь большинство лекарственных средств обладает токсичностью.
Какие перспективы у беременности после перенесенного онкологического заболевания? Следует ли выдерживать срок после лечения рака?
Профилактика является важной частью общей борьбы с онкологическими заболеваниями. Как же уменьшить вероятность возникновения рака?
Что представляет из себя паллиативное лечение рака? Как оно может повлиять на качество жизни онкологического больного и изменить ее к лучшему?
Учеными разработано достаточно много перспективных методов лечения рака, пока еще не признанных официальной медициной. Но все может измениться!
Как найти силы для борьбы с раком? Как не впасть в отчаяние от возможной инвалидности? Что может послужить надеждой и смыслом жизни?
Бытует такое мнение, что постоянные стрессовые ситуации способны привести к развитию онкологических заболеваний. Так ли это?
Многие онкологические больные часто страдают от резкой потери веса. Чем это вызвано и можно ли как-то справиться с этой проблемой?
Правила ухода за больными, вынужденными постоянно находиться в кровати, имеют свои особенности и их нужно обязательно знать.
2020. Tafasitamab - новый препарат от рака крови - на подходе

Американская фармакомпания Incyte выкупает у немецкого биотек-стартапа MorphoSys права на препарат Tafasitamab почти за $2 млрд. Это препарат на основе антител для лечения B-клеточной лимфомы, хронического лимфоцитарного лейкоза (ХЛЛ) и В-клеточной неходжкинской лимфомы. Препарат усиливает работу иммунных B-клеток, которые цепляются к раковым клеткам и привлекают макрофаги для их уничтожения. На данный момент Tafasitamab проходит последнюю стадию клинических испытаний и его эффективность сравнима с более дорогой CAR-T терапией. Incyte надеется выпустить препарат в продажу уже в этом году.
2019. В России создали нейропроцессор для диагностики рака крови

Российский научно-технический центр Модуль разработал нейросетевое устройство, которое умеет анализировать микроснимки анализа крови и выявлять атипичные клетки, которые могут быть связаны со злокачественным заболеванием кроветворной системы. Нейросеть обучалась на массиве данных лаборатории патологической анатомии одной из малазийских клиник. Разработчики говорят, что точность диагноза от нейросети составляет 98%, а анализ проводится всего за несколько секунд. В перспективе нейросеть Модуля сможет определять раковые клетки по результатам биопсии других видов рака. Сейчас устройство готовят к сертификации FDA в США.
2017. В США одобрили вторую генную терапию для лечения рака крови

Американский регулятор FDA одобрил вторую генную терапию для борьбы с раком крови: препарат Yescarta (компании Kite Pharma). Он предназначен для лечения агрессивной лимфомы у взрослых. Первым одобренным антираковым генотерапевтическим препаратом стал Kymriah (компании Novartis). В Yescarta применяется та же технология (CAR-T), что и в первой генной терапии. Она редактирует иммунные Т-клетки так что они начинают атаковать раковые клетки. Стоит Yescarta немного дешевле - 373 тыс. долларов для одного пациента. Причем есть потенциал к снижению этой стоимости, т.к. в США - более 7 тысяч пациентов в год, которым подходит эта технология. А чем больше пациентом покупают препарат, тем дешевле он становится.
2017. Антираковая генотерапия CAR-T сертифицирована в США
Технология CAR-T и препарат Kymriah (Кимрия) швейцарской компании Novartis, которая уже доказала свою эффективность в лечении острого лимфобластного лейкоза, была сертифицирована американским регулятором FDA (что еще раз подтверждает ее действенность). Суть технологии в том, что врачи берут образец белых кровяных телец пациента, а потом в лаборатории перепрограммируют их в убийц опухолей. Затем клетки возвращают в тело, где они быстро группируются и уничтожают раковые клетки. Конечно, стоимость такого лечения - не всем по карману - $475,000. Правда, Novartis обещает вернуть деньги, если организм пациента не отвечает на лечение.
2017. Наночастицы перепрограммируют Т-клетки прямо в организме для борьбы с лейкемией
2017. Лекарство Гливек показывает отличные результаты в лечении лейкоза
2016. Персонализированная вакцина остановила рак крови

Медицинский центр Beth Israel Deaconess, расположенный в Бостоне, провел успешные клинические испытания новой вакцины, изготавливаемой из собственных клеток пациента, которая предназначена для лечения острого миелоидного лейкоза. Вакцина использует технологию иммунотерапии, т.е. стимулирует собственные имунные Т-клетки для уничтожения опухоли. Испытания начались 4 года назад, когда 17 пациентам со средним возрастом 63 года начали вводить вакцину после сеансов химиотерапии. В результате 12 из них до сих пор показывают ремиссию. На фото - руководитель проекта - Дэвид Авиган.
2016. Технология Cellectis вылечила уже второго ребенка от лейкемии

Франко-американская компания Cellectis, похоже, заняла лидирующую позицию на многообещающем рынке иммунотерапии рака. В конце прошлого года ее технология TALEN (основанная на методе CAR-T) помогла вылечить годовалую девочку от лейкемии, а недавно они объявили о второй успешной операции, проведенной в том же лондонском госпитале. Смысл технологии в том, что ДНК иммунных клеток (Т-лимфоцитов) модифицируется в пробирке, а затем они вводятся в организм, где уничтожают поврежденные при лейкемии кровяные клетки. Есть еще три перспективных стартапа, разрабатывающих подобные технологии (Novartis, Juno Therapeutics и Kite Pharma). Но отличие технологии Cellectis в том, что она использует донорские Т-клетки, т.е. потенциально может создать универсальный и дешевый препарат, который можно быстро ввести любому пациенту.
2015. Генная инженерия и иммунотрапия спасли девочку от лейкемии
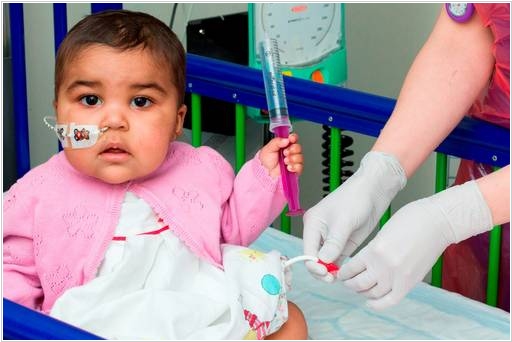
В Лондонской больнице Грейт-Ормонд-Стрит врачи использовали уникальный метод CAR-T для лечения лейкемии (рака крови) у маленькой девочки Лейлы (1 год). Химиотерапия и пересадка костного мозга ей не помогли, поэтому медики решились испробовать новый вид иммунотерапии. Они взяли иммунные клетки донора, генетически-модицифировали их так чтобы они распознавали и уничтожали раковые клетки и при этом сами не воспринимались иммунной системой, как чужеродные, и ввели их в организм девочки. Через три месяца Лейле снова пересадили костный мозг: здоровые иммунные клетки распознали генно-модифицированные клетки как чужеродные и уничтожили их. Таким образом, сейчас в организме девочки не осталось генетически модифицированных клеток. Пока о полном излечении Лейлы говорить рано, но она жива и хорошо себя чувствует. Полноценные клинические испытания этой технологии начнутся в 2016 году. Технология разработана французской биотехнологической компанией Cellectis.
2014. Создан искусственный костный мозг для выращивания стволовых клеток крови
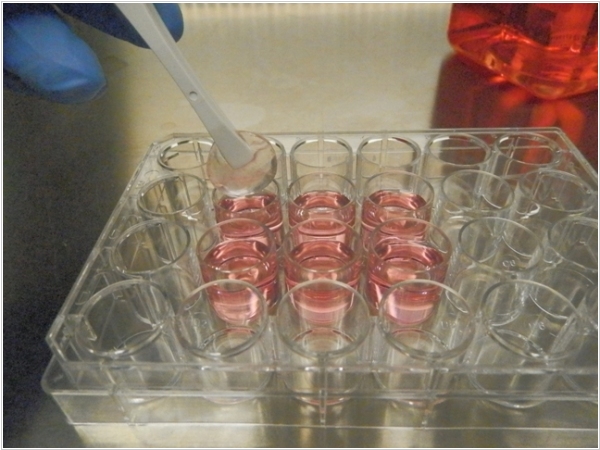
Все клетки крови (эритроциты, лейкоциты. ) формируются из так называемых гемопоэтических стволовых клеток, которые, содержатся в костном мозге человека. И иногда человеку требуется замена этих стволовых клеток. Например, при лейкемии, когда собственные стволовые клетки превращаются в раковые. Или после лучевой терапии, когда собственные стволовые клетки погибают. В таких случаях проводят трансплантацию костного мозга, и это очень-очень дорогая операция, в основном из-за сложности поиска совместимого донора. В России с этим делом - вообще комедия. Вот было бы здорово, если б можно было взять у человека чуть-чуть стволовых клеток крови, размножить их в лаборатории, а потом ввести обратно в костный мозг. Именно над такой идеей работают ученые из нескольких ведущих научных центров Германии. И у них уже кое-что получилось. Они создали искусственную пористую структуру, имитирующую губчатое вещество кости в области кроветворного костного мозга. ***
2013. В Ханты-Мансийске проводят трансплантацию стволовых клеток при лечении рака крови
Югорский научно-исследовательский институт клеточных технологий, созданный четыре года назад, вроде-как успешно применяет свою технологию лечения рака крови с помощью стволовых клеток. На базе Сургутской ОКБ они провели уже 34 трансплантации стволовых клеток, и говорят, что все пациенты до сих пор живы. Кроветворные стволовые клетки НИИ получает от доноров (из костного мозга и пуповинной крови), проводят ДНК анализ (для определения совместимости) и хранит этот материал в своем криобанке. Затем стволовые клетки добавляют в кровь пациента каким-то уникальным методом. По словам Сергея Щукина, заместителя директора Департамента здравоохранения Югры, стоимость пересадки стволовых клеток на западе - порядка 420 тысяч долларов. А у нас по стране, хотя такие операции - редкость, но делаются они бесплатно, за счет средств бюджета.
2020. Tafasitamab - новый препарат от рака крови - на подходе

Американская фармакомпания Incyte выкупает у немецкого биотек-стартапа MorphoSys права на препарат Tafasitamab почти за $2 млрд. Это препарат на основе антител для лечения B-клеточной лимфомы, хронического лимфоцитарного лейкоза (ХЛЛ) и В-клеточной неходжкинской лимфомы. Препарат усиливает работу иммунных B-клеток, которые цепляются к раковым клеткам и привлекают макрофаги для их уничтожения. На данный момент Tafasitamab проходит последнюю стадию клинических испытаний и его эффективность сравнима с более дорогой CAR-T терапией. Incyte надеется выпустить препарат в продажу уже в этом году.
2019. В России создали нейропроцессор для диагностики рака крови

Российский научно-технический центр Модуль разработал нейросетевое устройство, которое умеет анализировать микроснимки анализа крови и выявлять атипичные клетки, которые могут быть связаны со злокачественным заболеванием кроветворной системы. Нейросеть обучалась на массиве данных лаборатории патологической анатомии одной из малазийских клиник. Разработчики говорят, что точность диагноза от нейросети составляет 98%, а анализ проводится всего за несколько секунд. В перспективе нейросеть Модуля сможет определять раковые клетки по результатам биопсии других видов рака. Сейчас устройство готовят к сертификации FDA в США.
2017. В США одобрили вторую генную терапию для лечения рака крови

Американский регулятор FDA одобрил вторую генную терапию для борьбы с раком крови: препарат Yescarta (компании Kite Pharma). Он предназначен для лечения агрессивной лимфомы у взрослых. Первым одобренным антираковым генотерапевтическим препаратом стал Kymriah (компании Novartis). В Yescarta применяется та же технология (CAR-T), что и в первой генной терапии. Она редактирует иммунные Т-клетки так что они начинают атаковать раковые клетки. Стоит Yescarta немного дешевле - 373 тыс. долларов для одного пациента. Причем есть потенциал к снижению этой стоимости, т.к. в США - более 7 тысяч пациентов в год, которым подходит эта технология. А чем больше пациентом покупают препарат, тем дешевле он становится.
2017. Антираковая генотерапия CAR-T сертифицирована в США

Технология CAR-T и препарат Kymriah (Кимрия) швейцарской компании Novartis, которая уже доказала свою эффективность в лечении острого лимфобластного лейкоза, была сертифицирована американским регулятором FDA (что еще раз подтверждает ее действенность). Суть технологии в том, что врачи берут образец белых кровяных телец пациента, а потом в лаборатории перепрограммируют их в убийц опухолей. Затем клетки возвращают в тело, где они быстро группируются и уничтожают раковые клетки. Конечно, стоимость такого лечения - не всем по карману - $475,000. Правда, Novartis обещает вернуть деньги, если организм пациента не отвечает на лечение.
2017. Наночастицы перепрограммируют Т-клетки прямо в организме для борьбы с лейкемией
2017. Лекарство Гливек показывает отличные результаты в лечении лейкоза
2016. Персонализированная вакцина остановила рак крови

Медицинский центр Beth Israel Deaconess, расположенный в Бостоне, провел успешные клинические испытания новой вакцины, изготавливаемой из собственных клеток пациента, которая предназначена для лечения острого миелоидного лейкоза. Вакцина использует технологию иммунотерапии, т.е. стимулирует собственные имунные Т-клетки для уничтожения опухоли. Испытания начались 4 года назад, когда 17 пациентам со средним возрастом 63 года начали вводить вакцину после сеансов химиотерапии. В результате 12 из них до сих пор показывают ремиссию. На фото - руководитель проекта - Дэвид Авиган.
2016. Технология Cellectis вылечила уже второго ребенка от лейкемии

Франко-американская компания Cellectis, похоже, заняла лидирующую позицию на многообещающем рынке иммунотерапии рака. В конце прошлого года ее технология TALEN (основанная на методе CAR-T) помогла вылечить годовалую девочку от лейкемии, а недавно они объявили о второй успешной операции, проведенной в том же лондонском госпитале. Смысл технологии в том, что ДНК иммунных клеток (Т-лимфоцитов) модифицируется в пробирке, а затем они вводятся в организм, где уничтожают поврежденные при лейкемии кровяные клетки. Есть еще три перспективных стартапа, разрабатывающих подобные технологии (Novartis, Juno Therapeutics и Kite Pharma). Но отличие технологии Cellectis в том, что она использует донорские Т-клетки, т.е. потенциально может создать универсальный и дешевый препарат, который можно быстро ввести любому пациенту.
2015. Генная инженерия и иммунотрапия спасли девочку от лейкемии

В Лондонской больнице Грейт-Ормонд-Стрит врачи использовали уникальный метод CAR-T для лечения лейкемии (рака крови) у маленькой девочки Лейлы (1 год). Химиотерапия и пересадка костного мозга ей не помогли, поэтому медики решились испробовать новый вид иммунотерапии. Они взяли иммунные клетки донора, генетически-модицифировали их так чтобы они распознавали и уничтожали раковые клетки и при этом сами не воспринимались иммунной системой, как чужеродные, и ввели их в организм девочки. Через три месяца Лейле снова пересадили костный мозг: здоровые иммунные клетки распознали генно-модифицированные клетки как чужеродные и уничтожили их. Таким образом, сейчас в организме девочки не осталось генетически модифицированных клеток. Пока о полном излечении Лейлы говорить рано, но она жива и хорошо себя чувствует. Полноценные клинические испытания этой технологии начнутся в 2016 году. Технология разработана французской биотехнологической компанией Cellectis.
2014. Создан искусственный костный мозг для выращивания стволовых клеток крови

Все клетки крови (эритроциты, лейкоциты. ) формируются из так называемых гемопоэтических стволовых клеток, которые, содержатся в костном мозге человека. И иногда человеку требуется замена этих стволовых клеток. Например, при лейкемии, когда собственные стволовые клетки превращаются в раковые. Или после лучевой терапии, когда собственные стволовые клетки погибают. В таких случаях проводят трансплантацию костного мозга, и это очень-очень дорогая операция, в основном из-за сложности поиска совместимого донора. В России с этим делом - вообще комедия. Вот было бы здорово, если б можно было взять у человека чуть-чуть стволовых клеток крови, размножить их в лаборатории, а потом ввести обратно в костный мозг. Именно над такой идеей работают ученые из нескольких ведущих научных центров Германии. И у них уже кое-что получилось. Они создали искусственную пористую структуру, имитирующую губчатое вещество кости в области кроветворного костного мозга. ***
2013. В Ханты-Мансийске проводят трансплантацию стволовых клеток при лечении рака крови

Югорский научно-исследовательский институт клеточных технологий, созданный четыре года назад, вроде-как успешно применяет свою технологию лечения рака крови с помощью стволовых клеток. На базе Сургутской ОКБ они провели уже 34 трансплантации стволовых клеток, и говорят, что все пациенты до сих пор живы. Кроветворные стволовые клетки НИИ получает от доноров (из костного мозга и пуповинной крови), проводят ДНК анализ (для определения совместимости) и хранит этот материал в своем криобанке. Затем стволовые клетки добавляют в кровь пациента каким-то уникальным методом. По словам Сергея Щукина, заместителя директора Департамента здравоохранения Югры, стоимость пересадки стволовых клеток на западе - порядка 420 тысяч долларов. А у нас по стране, хотя такие операции - редкость, но делаются они бесплатно, за счет средств бюджета.
Читайте также:

