Лечение рака кишечника операция

- Удаление опухоли при колоноскопии или ректороманоскопии
- Осложнения при колоректальном раке
- Формирование колостомы
- Операция Гартмана
- Стентирование
- Нет ли риска, что вмешательство будет способствовать распространению опухоли и возникновению рецидивов?
- Подготовка к операции на толстой кишке
- Диета после операции и особое питание
- Обследования после успешно проведенного лечения рака толстой кишки
Лапароскопия в колоректальной хирургии
Определить возможность выполнения операции с помощью лапароскопической техники можно уже на первичном приёме. Современные технологии позволяют провести резекцию пораженного опухолью участка кишки через небольшие разрезы на коже (5 — 12 мм) при полном соблюдении правил абластики — проведения онкологических операций для защиты здоровых тканей от заражения раковыми клетками удаляемой опухоли.
Помимо выраженных эстетических преимуществ, лапароскопическая операция позволяет сократить послеоперационный период, ускорить заживление и уменьшить болевой синдром, количество послеоперационных, в т.ч. инфекционных осложнений, в том числе межкишечных спаек.
Восстановление нормальной деятельности кишечника происходит в сжатые сроки и позволяет пациентам не прерывать надолго свою привычную жизнь.
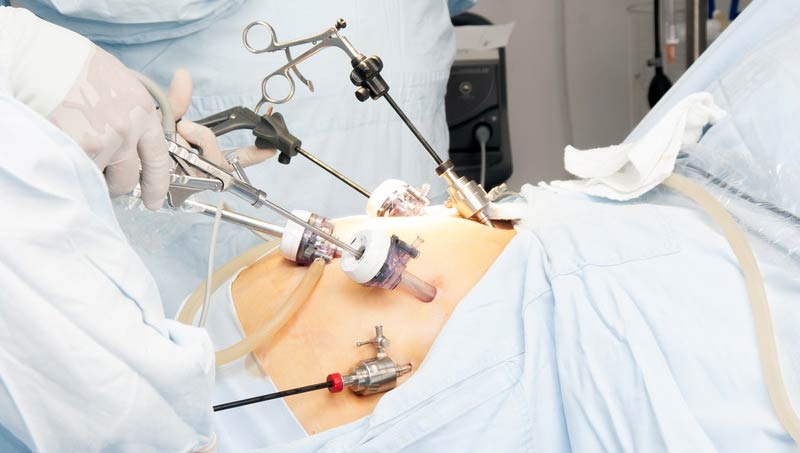
Отличительная особенность лапароскопических вмешательств при низких раках
В Европейской клинике есть все возможности для проведения уникальных по своей структуре операций с помощью лапароскопических технологий. Так при низком расположении опухоли мы можем делать операции без вывода кишки на переднюю брюшную стенку. Выполняется операция низведения вышележащих отделов ободочной кишки или в анус, или в рану промежности, для защиты данного вида оперативного пособия иногда выводится как и в других случаях временно колостома.
При удалении анального канала (экстирпация прямой кишки) можно выполнить низведение сигмовидной кишки в рану промежности – по сути та же колостома, только в привычном месте, при определённом уходе возможна относительно комфортная жизнь и сохранение работоспособности. Данное оперативное вмешательство требует отдельного обсуждения и решения совместно с пациентом.
Удаление опухоли при колоноскопии или ректороманоскопии
В некоторых случаях (при преинвазивном и микроинвазивном или внутрислизистом раке) возможно и эндоскопическое внутрипросветное удаление опухолей во время проведения колоноскопии, которую можно сочетать с электро- и аргоноплазменной коагуляцией.
Эндоскопическое лечение применяется и у пациентов в тяжёлом состоянии (преклонный возраст с полиорганной недостаточностью, тяжелые хронические сопутствующие заболевания), при невозможности традиционного хирургического лечения. В частности, при развитии кишечной непроходимости в Европейской клинике осуществляется эндоскопическая установка стента в толстую кишку. Такое лечение называется паллиативным и направлено на продление жизни и улучшение ее качества у пациентов, имеющих опухоль в далеко зашедших стадиях.
Осложнения при колоректальном раке
Рак толстой кишки – это тяжелое заболевание, приводящее к метастазированию как в ближайшие лимфоузлы, так и в отдаленные органы (печень, лёгкие, кости), кахексии, прорастание опухоли в соседние органы и ткани. Развивающееся как при метастазировании колоректального рака, так и при инвазивном росте опухоли толстой кишки в области ворот печени собственно поражение печени может приводит к формированию механической желтухи, распространение опухоли по брюшине вызывает канцероматоз брюшины, приводит к асциту, и т.д.
Однако, самыми частыми и опасными осложнениями являются ситуации, связанные непосредственно с ростом опухоли:
- обтурационная кишечная непроходимость,
- острое и хроническое кровотечение из тканей опухоли,
- перфорация кишки с развитием перитонита,
- прорастание опухоли в соседние органы и развитие межорганных свищей,
- гнойно-воспалительные процессы (параколит, паранефрит, флегмона забрюшинного пространства и брюшной стенки).
Все вышеперечисленные осложнения могут комбинироваться друг с другом в любой форме и значительно осложнять лечение пациентов с колоректальным раком.

Полная или частичная кишечная непроходимость – частое осложнение при раке толстой кишки, которое чаще развивается в левых, меньшего диаметра отделах – сигмовидной и нисходящей ободочной кишках. Для опухолей этих отделов характерен рост в просвет кишки (эндофитный), и здесь уже формируются более плотные и оформленные по сравнению с полужидким содержимым высоких отделов кишечника каловые массы. Поэтому даже небольшое сужение просвета кишечника вызывает нарушение прохождения каловых масс.
При развитии кишечной непроходимости в зависимости от ситуации проводятся экстренные и плановые хирургические вмешательства. В Европейской клинике проводятся все виды операций на толстой кишке как традиционным методом, так и с помощью лапароскопических технологий.
Формирование колостомы
Во-первых, нужно заметить, что колостомы не нужно бояться. Использование современных средств по уходу за пациентами, включая современные калоприемники позволяет социализировать пациента, а в ряде случаев восстановить работоспособность и таким пациентам. В целом, установка временной колостомы позволяет существенно облегчить общее состояние пациента. А затем в ряде случаев с помощью повторной операции восстанавливается нормальный пассаж пищи по кишечнику.
Во-вторых, формирование колостомы проводится не во всех случаях операций по поводу рака толстой кишки. Многое определяется расположением опухоли, её размерами, вовлеченностью окружающих тканей, общим состоянием пациента. Колостома формируется в тех случаях, когда невозможно провести радикальную операцию по удалению опухоли и сохранить нормальное функционирование кишечника.
У ряда больных мы проводим хирургическое лечение в два этапа:
- На первом этапе удаляется кишка с первичной опухолью и формируется двуствольная колостома.
- Через несколько месяцев участки кишки сшивают между собой, и колостому закрывают.
Это так называемые двух-, в ряде случаев и трёхэтапные операции.
При отсутствии отдаленных метастазов выполняются радикальные операции, во время которых удаляется опухоль вместе с пораженными тканями и регионарными лимфатическими узлами. Если позволяет клиническая ситуация, то проводятся одномоментные операции без формирования колостомы:
- право- или левосторонняя гемиколэктомия с регионарной лимфаденэктомией,
- резекция поперечно-ободочной кишки с регионарной лимфаденэктомией,
- резекция сигмовидной кишки с регионарной лимфаденэктомией,
- при раке прямой кишки — передняя резекция прямой кишки с регионарной лимфаденэктомией или экстирпация прямой кишки с регионарной лимфаденэктомией и др.
Операция Гартмана
Для лечения рака сигмовидной кишки, ректосигмоидного отдела, а также опухолевого поражения верхне-ампулярного отдела прямой кишки (при невозможности формирования анастомоза – сшивания двух участков кишки) применяется операция Гартмана: резекция пораженного опухолью участка толстой кишки и наложение одноствольной колостомы с возможностью последующего отсроченного восстановления кишечника.
Каждое из этих вмешательств может быть окончательным (обычно при раке 4-й стадии) или временным, производимым для подготовки больного к последующим этапам. Эти оперативные вмешательства направлены на устранение непосредственной угрозы жизни больному. Последующие этапы выполняют в течение 4-6 месяцев после первичной операции, в это время проводится в условиях Европейской клиники адъювантная химиотерапия, а пациент находится под нашим наблюдением.
Стентирование
В тяжелых случаях и при неоперабельных опухолях у больных в тяжелом состоянии с частичной кишечной непроходимостью декомпрессия желудочно-кишечного тракта может достигаться эндоскопической установкой стента в толстую кишку.
Почти у 55% больных с колоректальным раком из-за особенностей венозного оттока из толстой кишки выявляются метастазы в печень. Часто, помимо опухолевой интоксикации и болевого синдрома, они утяжеляют ситуацию, вызывая сдавление желчевыводящего тракта и создавая условия для развития механической желтухи. В нашей клинике проводится удаление метастазов хирургическим путем во время проведения резекции печени, кроме того может быть использована радиочастотная аблация, химиоэмболизация сосудов печени, питающий метастатический очаг.

Нет ли риска, что вмешательство будет способствовать распространению опухоли и возникновению рецидивов?
Во-первых, при проведении экстренной операции взвешиваются все риски, и если лечащий врач идет на операцию, значит, другого выбора уже нет, и промедление приведет к смерти пациента.
Во-вторых, операции, как экстренные, так и плановые, проводятся со строгим соблюдением правил абластики. В частности, сначала пережимаются все кровеносные сосуды, питающие опухоль и лишь потом максимально удаляется пораженный участок кишки. Вместе со значительной частью здоровых тканей с обеих сторон пораженного кишечника кровеносными и лимфатическими сосудами и лимфоузлами в области удаляемого сегмента.
Подготовка к операции на толстой кишке
При проведении планового хирургического лечения перед операцией на толстой кишке оперирующий хирург подробно объясняет пациенту и его родственникам особенности подготовки к операции, её ход, обезболивание и ожидаемые объём и результаты. Для подготовки кишечника к операции пациенту назначают лечебное питание, очистительные клизмы за три-пять дней до вмешательства и прием слабительных средств, таких как флит, дюфалак, фортранс.
Важная часть подготовки к операции — поддержка, такт, выдержка, внимание, чуткость в общении с пациентом, возможность неограниченного общения с родственниками. Медицинская часть подготовки больного в Европейской клинике обеспечивается слаженной совместной работой специалистов-онкологов (хирургов, химиотерапевтов, радиологов), а также младшего и среднего медицинского персонала.
Диета после операции и особое питание
Питание в послеоперационный период регулируется лечащим врачом в зависимости от течения. По окончании реабилитационного периода рекомендуется включать в рацион больше фруктов и овощей, минимизировать животные жиры, в умеренном количестве употреблять легкоусвояемое мясо диетической обработки.

После резекции кишечника питательные компоненты усваиваются организмом хуже, в связи с этим следует употреблять только легкоусвояемую и качественную пищу, медленно и тщательно её пережевывая, обеспечивая достаточную обработку пищи слюной, что само по себе служит важным этапом пищеварения. Для более быстрого налаживания работы желудочно-кишечного тракта важен режим питания не реже 5 раз в сутки небольшими порциями.
При хорошей переносимости можно добавлять к рациону отруби или их отвар, другие овощи зелёного или жёлтого цвета, кисломолочные продукты, цельнозерновые каши, морепродукты. Большое количество антиоксидантов и полезных микроэлементов содержат малина, цитрусовые, финики, авокадо, овощи: томаты, все виды капусты (кольраби, цветная, брокколи, белокочанная и краснокочанная), редис, баклажаны, репа, сладкий перец, лук, имбирь, все виды орехов, тыквенные семечки, морская жирная рыба, морская капуста, зеленый чай, цельные крупы и соя, ростки пшеницы, растительное и оливковое масло. В выборе продуктов следует ориентироваться на собственные предпочтения и переносимость тех или иных продуктов. Запрет касается только тяжелой жирной пищи.
Обследования после успешно проведенного лечения рака толстой кишки
В первые два года после радикальной операции необходимо каждые 2-3 мес. сдавать анализ на уровень РЭА в крови, каждые 3-6 мес. – анализ кала на скрытую кровь и проходить ректальное исследование у онколога. Кроме того, один раз в год проводить диагностическую колоноскопию, рентген грудной клетки, гастроскопию. УЗИ брюшной полости в первый год каждые 3-4 месяца, а при необходимости компьютерное исследование органов брюшной и грудной полостей.
В дальнейшем, по согласованию с лечащим врачом, контрольные промежутки могут увеличиваться, однако наблюдение обязательно на период не менее 5 лет.
Своевременно и грамотно проведенное правильное лечение часто позволяет нашим пациентам с впервые диагностированным раком толстой кишки в короткий промежуток времени восстановить силы и трудоспособность до уровня, предшествовавшего операции. В течение 6-12 месяцев после хирургического лечения колоректального рака рекомендуется избегать тяжелого физического труда, подъема тяжестей, находится под прямыми солнечными лучами.
В случае проведения паллиативных вмешательств и при необходимости многоэтапных операций, правильный подбор в послеоперационном периоде современных средств по уходу, деликатное обучение пациентов и их родственников персоналом клиники правилам ухода за колостомой, позволяют минимизировать неудобства, связанные с ней и обеспечить сохранение образа жизни, максимально приближенного к привычному.
Задача всего медицинского персонала Европейской клиники сделать всё возможное и невозможное для продления жизни пациента. Мы стремимся к этому всеми доступными и известными на сегодняшний день средствами и методами.
- Все виды оперативных вмешательств выполняются с применением современных методик и техник выполнения.
- Во время операции используются современные сшивающие одноразовые аппараты, современный медицинский инструментарий, шовный материал.
- Операции выполняются преимущественно лапароскопическим методом, осуществляется ревизия брюшной полости, удаляется первичная опухоль.
- При необходимости выполняются различные комбинированные или сочетанные операции (на печени, селезёнке, органах малого таза, почках и мочеточниках, тонкой кишке).
Колоректальный рак — одно из самых распространенных онкологических заболеваний в России. Если объединить рак толстой и прямой кишки, то, по данным Московского онкологического института имени Герцена, в 2018 году они заняли по распространенности на территории нашей страны второе место после рака кожи с меланомой.

Есть позитивная динамика: колоректальный рак является одним из наиболее успешно излечимых онкологических заболеваний. Если опухоль обнаружена на ранней стадии, её можно удалить хирургически. На поздних стадиях, когда ремиссии достичь невозможно, пациенту все еще можно помочь: существуют методы лечения рака кишечника, которые помогают купировать симптомы и справиться с осложнениями, повысить выживаемость, помочь больному жить полноценной, достаточно активной жизнью.
В клинике Медицина 24/7 применяются наиболее современные методы лечения колоректального рака, в том числе инновационные, недоступные во многих других российских клиниках. Мы беремся за лечение пациентов со злокачественными опухолями на любой стадии.
Ниже мы поговорим об основных методах и о том, как проводится лечение рака кишечника на разных стадиях.
Хирургические методы лечения рака кишечника
На самых ранних стадиях рака кишечника (0 и I) злокачественную опухоль можно удалить во время эндоскопического исследования толстой кишки — колоноскопии. Если обнаруживает полип на ножке, в котором могут присутствовать раковые клетки, он удаляет его с помощью проволочной петли. Такая операция называется полипэктомией. Небольшое новообразование, которое находится в пределах слизистой оболочки и не прорастает глубже, можно иссечь, немного захватив окружающие здоровые ткани.
Если опухоль проросла глубже, проводят хирургическое вмешательство, во время которого удаляют часть кишки: сегментарную резекцию, частичную колэктомию или гемиколэктомию. Необходимо удалить саму злокачественную опухоль, а также неизмененные участки выше и ниже. Чаще всего приходится резецировать от одной четвертой до одной трети кишки. Операцию можно выполнить двумя способами:
- Через разрез.
- Лапароскопически — без разреза, через несколько проколов в брюшной стенке. Такие вмешательства сопровождаются более низкими рисками, и пациенты легче их переносят.
Эксперты из Американского Онкологического Общества рекомендуют удалять во время операции по поводу рака кишечника не менее 12 близлежащих лимфатических узлов.
На более поздних стадиях хирургическое лечение онкологии кишечника направлено на борьбу с симптомами и улучшение состояния.
Если просвет кишки заблокирован злокачественной опухолью, можно провести стентирование. Это эндоскопическое вмешательство. В заблокированный участок устанавливают стент — трубку, стенка которой представляет собой сетку из металла или пластика.
В случаях, когда установить стент не получается, выполняют колостомию или илеостомию. Подвздошную или ободочную кишку пересекают, и её верхний конец выводят в отверстие на кожу для отхождения каловых масс. Иногда приходится накладывать временную колостому после радикальной операции по поводу рака толстой кишки. После заживления проводят вторую операцию, во время которой отверстие закрывают и соединяют концы кишки.
Лечение рака кишечника с помощью химиотерапии
Химиопрепараты при раке кишечника используют в трех случаях:
- В качестве основного метода лечения — на поздних стадиях, когда злокачественная опухоль неоперабельна.
- Неоадъювантная химиотерапия применяется перед операцией. Она помогает уменьшить размеры злокачественной опухоли, в результате чего ее становится проще удалить хирургическим путем. Этот вид лечения чаще используется при раке прямой кишки.
- Адъювантная химиотерапия проводится после операции. Её цель — уничтожить опухолевые клетки, которые остались в теле пациента, с целью профилактики рецидива.
Чаще всего лечение рака кишечника проводят такими химиопрепаратами, как капецитабин (Кселода), , оксалиплатин (Элоксатин), иринотекан (Камптозар), трифлуридин/типирацил. В большинстве случаев комбинируют два химиопрепарата с разными механизмами действия. Иногда назначают один химиопрепарат в сочетании с таргетным препаратом.
Врачи в клинике Медицина 24/7 проводят лечение противоопухолевыми препаратами последних поколений, в соответствии с последними версиями международных протоколов.
Таргетная терапия
Таргетные препараты — противоопухолевые средства, созданные на основе достижений молекулярной биологии. Они направлены против молекул, которые нужны раковым клеткам для быстрого размножения и распространения в организме, поддержания жизнедеятельности. Этим таргетные препараты кардинально отличаются от классических химиопрепаратов, которые по сути являются клеточными ядами и повреждают все быстро размножающиеся клетки.
Лечение онкологии кишечника проводят с помощью разных групп таргетных препаратов:
- Ингибиторы EGFR блокируют , который находится на поверхности опухолевых клеток и активирует их размножение. К этой группе относятся препараты: панитумумаб (Вектибикс), цетуксимаб (Эрбитукс). Их вводят внутривенно раз в неделю или раз в две недели.
- Ингибиторы VEGF блокируют ангиогенез — процесс роста новых кровеносных сосудов, которые снабжают опухолевые клетки кислородом и питательными веществами. К ингибиторам ангиогенеза относят таргетные препараты: рамуцирумаб (Цирамза), бевацизумаб (Авастин), (Залтрап). Их часто сочетают с химиопрепаратами, вводят внутривенно один раз в 2 или 3 недели.
- Ингибиторы киназ. Киназы — это сигнальные белки, которые активируют размножение клеток или рост кровеносных сосудов. Разные виды киназ ингибирует таргетный препарат регорафениб (Стиварга). Он выпускается в виде таблеток, обычно его назначают в случаях, когда пациент страдает раком кишки на поздних стадиях, и не помогают другие методы лечения.
Иммунотерапия при раке кишки
Иммунотерапия — направление в лечении онкологических заболеваний, которое использует для борьбы с раком ресурсы иммунной системы. В некоторых случаях у людей с раком кишки применяются иммунопрепараты из группы ингибиторов контрольных точек. Они блокируют молекулы, которые мешают иммунным клеткам распознавать и уничтожать опухолевые клетки. В норме эти контрольные точки предотвращают аутоиммунные реакции, направленные против собственных органов, но при онкологических заболеваниях они начинают мешать.
Ингибиторы контрольных точек при раке кишки могут быть назначены в следующих случаях:
- Если опухоль неоперабельна.
- Если рак прогрессирует или метастазировал на фоне лечения стандартными противоопухолевыми препаратами.
- При рецидиве злокачественной опухоли после лечения.
- Если в раковых клетках присутствуют определенные генетические маркеры: высокий уровень микросателлитной нестабильности, дефекты в генах восстановления несоответствия.
Применяются препараты из разных групп:
- Ингибиторы . Данная молекула находится на поверхности и при взаимодействии с её лигандом — белком ¬- снижает активность иммунных клеток. К этой группе относятся препараты пембролизумаб (Китруда) и ниволумаб (Опдиво). Их вводят в виде растворов внутривенно через каждые 2–3 недели.
- Ингибитор . Этот белок также находится на поверхности и подавляет иммунный противоопухолевый ответ. При раке толстой кишки применяют препарат ипилимумаб (Ервой). Его также вводят внутривенно, через каждые 3 недели, курс включает 4 процедуры.
Лучевая терапия
Лучевую терапию применяют при колоректальном раке с разными целями:
- В качестве неоадъювантного лечения перед хирургическим вмешательством.
- В качестве адъювантной терапии после удаления рака.
- Интраоперационно — иногда злокачественные опухоли облучают прямо на операционном столе, во время хирургического вмешательства.
- В сочетании с химиотерапией, когда пациенту противопоказано хирургическое вмешательство. Такое лечение называется химиолучевой терапией. Оно действует более эффективно по сравнению с каждым из этих методов лечении в отдельности.
- Для борьбы с метастазами рака.
- Для улучшения состояния больного и борьбы с некоторыми симптомами при поздних стадиях рака. Например, лучевая терапия может быть назначена, если злокачественная опухоль вызывает кишечную непроходимость, если развилось кровотечение.
Лечение рака кишечника с метастазами в печень
Рак толстой кишки очень часто метастазирует в печень. Из всех пациентов, впервые обратившихся к онкологу, 14–18% уже имеют печеночные метастазы. В некоторых случаях, при единичных вторичных очагах, можно выполнить резекцию печени.
Но даже если при поражении печени нельзя выполнить хирургическое вмешательство, пациенту все еще можно помочь. В клинике Медицина 24/7 применяются наиболее современные методы лечения рака кишечника с метастазами в печень:
- Внутриартериальная химиотерапия — когда химиопрепарат вводят непосредственно в артерию, питающую злокачественную опухоль. При этом можно использовать высокие дозы лекарства: оно практически не поступает в системный кровоток, и нет риска серьезных побочных эффектов.
- Химиоэмболизация — процедура, во время которой вместе с химиопрепаратом вводят эмболизирующие частицы. Они закупоривают просвет сосуда и нарушают приток крови к опухолевым клеткам, в результате чего те погибают.
- Радиоэмболизация — введение эмболизирующих частиц, которые являются источниками излучения.
- Радиочастотная аблация — процедура, во время которой в опухолевый узел под контролем УЗИ или компьютерной томографии вводят и подают на нее радиоволны высокой частоты. За счет этого опухолевая ткань нагревается и погибает.
У некоторых пациентов развивается механическая желтуха — состояние, вызванное нарушением оттока желчи. В данном случае можно выполнить дренирование или стентирование. В первом случае в желчные протоки устанавливают трубку, по которой желчь оттекает в просвет двенадцатиперстной кишки или наружу. Во втором случае в заблокированный участок помещают стент — трубку с сетчатой стенкой из металла или пластика.
Основным методом лечения рака толстой кишки остаётся радикальное удаление опухоли и зоны её регионального лимфогенного метастазирования.
Общие принципы хирургического лечения рака толстой кишки: радикальность, абластичность, асептичность и создание беспрепятственного отхождения кишечного содержимого, по возможности, естественным путём.
Успех хирургического лечения, соблюдение его принципов в значительной степени зависит от правильной подготовки толстой кишки. Существует несколько вариантов подготовки. До настоящего времени наиболее распространённым методом остаётся назначение бесшлаковой диеты, слабительных препаратов и очистительных клизм за 3-5 сут до операции. В последнее годы всё большее распространение получает ортоградное общее промывание желудочно-кишечного тракта с помощью специальных препаратов.
Абластичности и асептичности при хирургическом лечении рака толстой кишки достигают соблюдением комплекса мероприятий: бережным обращением с толстой кишкой и избеганием контакта с опухолью, ранней перевязкой основных питающих сосудов, мобилизацией кишки острым путём. Радикальность операции может быть обеспечена адекватным объёмом резекции толстой кишки с опухолью и удалением соответствующей зоны регионального лимфогенного метастазирования.
При наличии отдалённых метастазов радикальность операции становится сомнительной, даже при удалении видимых очагов поражения. Однако паллиативные (циторедуктивные) вмешательства всё же следует выполнять для профилактики развития осложнений в неудалённой опухоли (кровотечение, выраженное перифокальное воспаление, значительный болевой синдром).
Из-за запущенности заболевания в ряде случаев хирургическое лечение носит характер симптоматического: формирование колостомы из-за явлений кишечной непроходимости при невозможности удаления опухоли.
По объёму оперативные вмешательства подразделяют на типичные, комбинированные, расширенные и сочетанные.
Типичные операции предполагают объём резекции, необходимый для данной локализации и стадии опухоли. Так, например, для рака средней трети сигмовидной кишки в стадии I и II типичной операцией будет сегментарная резекция сигмовидной кишки, но для той же локализации в III стадии адекватной будет уже только левосторонняя гемиколэктомия.
Комбинированными называются операции, при которых из-за распространения опухоли резецируют не только толстую кишку, но и какой-либо другой орган.
Расширенные резекции - операции, при которых увеличивают объём резекции (по сравнению с типичным объёмом резекции толстой кишки) из-за распространения опухоли или наличия синхронных опухолей.
К сочетанным операциям относят удаление или резекция наряду с толстой кишкой каких-либо других органов из-за сопутствующих заболеваний (холецистэктомия, овариоэктомия и т.д.).
Хирургическое лечение рака ободочной кишки
При раке ободочной кишки объём резекции в зависимости от локализации опухоли колеблется от дистальной резекции сигмовидной кишки до субтотальной резекции ободочной кишки. Наиболее часто выполняют дистальную резекцию сигмовидной кишки, сегментарную резекцию сигмовидной кишки, левостороннюю гемиколэктомию, резекцию поперечной ободочной кишки, правостороннюю гемиколэктомию (рис. 64-1).

Рис. 64-1. Варианты резекции ободочной кишки: а - сигмовидной кишки; б - левосторонняя гемиколэктомия; в - правосторонняя гемиколэктомия; г - резекция поперечной ободочной кишки.
При поражении лимфатических узлов следует выполнять расширенные объёмы резекции. Резекции ободочной кишки следует заканчивать формированием анастомоза с восстановлением естественного кишечного пассажа при соблюдении следующих условий: хорошая подготовка кишки, хорошее кровоснабжение анастомозируемых отделов, отсутствие натяжения кишки в зоне предполагаемого анастомоза.
Для формирования анастомоза наибольшее распространение получил двухрядный узловой шов атравматической иглой. Возможно также использование и других вариантов анастомозирования: механический скрепочный шов, механический шов из рассасывающегося материала или металлом с памятью формы, однорядный ручной шов и др.
При осложнениях опухоли, при срочных или экстренных операциях на неподготовленной кишке предпочтение следует отдавать многоэтапному лечению. На первом этапе следует не только устранить возникшие осложнения, но и стремиться удалить саму опухоль, на втором - восстановить естественный кишечный пассаж.
К таким способам хирургического лечения относят операцию Микулича с формированием двуствольной колостомы и операцию Хартманна - формирование одноствольной колостомы и ушивание дистального отрезка толстой кишки наглухо. Восстановление естественного кишечного пассажа производят через 2-6 месяцев нормализации состояния больных.
Хирургическое лечение рака прямой кишки
Долгое время в онкопроктологии господствовало мнение о том, что наиболее радикальным вмешательством при раке прямой кишки любой локализации является экстирпация органа, подразумевающая удаление не только самой прямой кишки, но и всех структур её запирательного аппарата. Работы В.Р. Брайцева (1910), С.А. Холдина (1977) и их последователей по изучению схемы оттока лимфы из прямой кишки заставили изменить эти представления.
Установлено, что лимфа от прямой кишки оттекает в основном по двум направлениям. Если условно разделить прямую кишку поперечной плоскостью на уровне 6 см от края заднего прохода, то из отделов, лежащих ниже этой плоскости (анальный канал, нижнеампулярный отдел), отток лимфы происходит в основном по ходу средне- и нижнепрямокишечных сосудов, т.е. вниз и в стороны.
Основные зоны метастазирования, наряду с параректальными узлами, - это паховые, тазовые и подвздошные лимфоузлы. От отделов, лежащих выше 6 см (средне- и верхнеампулярный отделы), отток лимфы осуществляется по ходу верхних прямокишечных сосудов, поэтому при такой локализации опухоли нет необходимости в удалении заднего прохода, пересечении порций леватора и широкого удаления тазовой клетчатки.
При выборе метода оперативного вмешательства необходимо учитывать локализацию опухоли (рис. 64-2).

Рис. 64-2. Выбор метода оперативного вмешательства в зависимости от места расположения опухоли в прямой кишке: 1 - брюшно-промежностная экстирпация прямой кишки; 2 - брюшно-анальная резекция прямой кишки; 3 - передняя резекция прямой кишки.
При расположении опухоли в анальном канале и нижнеампулярном отделе прямой кишки целесообразно выполнение брюшно-промежностной экстирпации прямой кишки с формированием забрюшинной плоской колостомы. Суть операции заключается в удалении прямой кишки вместе с замыкательным аппаратом, при этом полностью убирают параректальную клетчатку, пересекают мышцу, поднимающую задний проход, и убирают клетчатку малого таза. В левой подвздошной области формируют забрюшинную плоскую колостому. Лапаротомную и промежностную раны ушивают наглухо.
При расположении опухоли на 7-11 см от края заднего прохода возможна брюшно-анальная резекция, которую выполняют две бригады хирургов - брюшная и промежностная (так же как и при проведении экстирпации прямой кишки). Промежностная бригада хирургов через трансанальный доступ циркулярно рассекает все слои кишечной стенки сразу за верхней границей анального канала. Операцию заканчивают одним из трёх способов: формированием колоанального анастомоза ручным швом, или низведением отделов ободочной кишки в анальный канал с избытком и созданием бесшовного адгезивного анастомоза, либо наложением временной концевой колостомы. Выбор способа окончания брюшно-анальной резекции определяется состоянием больного, выраженностью перифокального воспаления, наличием других осложнений, например кишечной непроходимости.
Благодаря развитию хирургической техники и созданию нового поколения сшивающих аппаратов, при этой локализации опухоли возможно выполнение низких передних резекций.
Трансанальное эндомикрохирургическое иссечение новообразований выполняют в случае расположения опухоли в стадии Tis-T2N0M0 менее 3 см в диаметре выше зубчатой линии до 15 см от края заднего прохода с помощью операционного ректоскопа с оптической насадкой и микрохирургического инструментария, позволяющего иссечь опухоль в пределах здоровых тканей и восстановить дефект стенки кишки.
Трансанальная резекция нижнеампулярного отдела прямой кишки позволяет не прибегать к абдоминальному доступу при наличии высокодифференцированного рака прямой кишки менее 3 см в диаметре в стадии T1-T2N0M0, располагающегося в пределах 0-3 см выше зубчатой линии. В случае расположения дистального края высокодифференцированной аденокарциномы прямой кишки менее 3 см в диаметре в стадии T1-T2N0M0 ниже зубчатой линии альтернативным подходом может быть выполнение секторальной резекции прямой кишки и анального канала.
Комбинированное и комплексное лечение рака толстой кишки
При многофакторном воздействии на опухолевый процесс (антибластика) происходит девитализация опухолевых клеток, уменьшение массы опухоли, что создаёт благоприятный фон для последующего хирургического вмешательства. Для этой цели используют различные виды комбинированного и комплексного лечения.
Наши данные свидетельствуют о значительной радиочувствительности аденокарциномы ободочной кишки, для облучения которой используется тормозное излучение бетатрона с энергией 25 Мэв. Более чем у половины больных после облучения существенно уменьшаются размеры опухоли вследствие девитализации раковых клеток. Это создаёт более благоприятные условия для хирургического вмешательства и снижает возможность имплантации опухолевых клеток; повышается не только антибластичность, но и асептичность, так как значительно уменьшается и перифокальное воспаление.
Отдалённые результаты комбинированного лечения рака ободочной кишки свидетельствуют о значительном эффекте этого метода лечения, особенно при локализации опухоли в правой половине кишки. Целесообразно облучать местнораспространённые опухоли. При комбинированном и комплексном лечении рака прямой кишки картина несколько иная. Используемое при этой локализации химиолучевое лечение (телегамматерапия; фторурацил, тегафур) также вызывает непосредственный эффект в виде уменьшения массы опухоли, девитализации опухолевых клеток, не увеличивая числа пред-, интра- и послеоперационных осложнений. Однако выживаемость больных раком прямой кишки значительно не улучшается, что, скорее всего, связано с невозможностью во время операции убрать лимфатические узлы во всех зонах предполагаемого метастазирования; 5-летняя выживаемость больных, которым проводили комбинированное и комплексное лечение, незначительно превышает таковую после хирургического лечения.
Существует множество схем комплексного и комбинированного лечения, состоящих из пред- и послеоперационного химиолучевого воздействия, использования по отдельности лучевой и химиотерапии, а также их различных комбинаций.
Поскольку установлена невысокая эффективность лучевой и химиотерапии как самостоятельных видов лечения рака толстой кишки, их можно рекомендовать только с паллиативной целью, когда невозможно применить другие методы.
Прогноз
Прогноз при раке толстой кишки зависит от стадии опухолевого процесса. В начальных стадиях заболевания (I стадия, T1N0M0) 5-летняя выживаемость после радикальных операций достигает 90%. С увеличением стадии заболевания результаты значительно ухудшаются. У больных с поражением лимфатических узлов этот показатель составляет не более 50%, а при правосторонней локализации опухоли ободочной кишки - не более 20%. Отдалённые результаты операций по поводу рака прямой кишки несколько хуже. В среднем 5-летняя выживаемость пациентов, перенёсших радикальные операции, составляет 50%, при этом также прослеживается зависимость отдалённых результатов от стадии процесса.
Необходимо регулярно обследовать лиц, оперированных по поводу колоректального рака, поскольку в дальнейшем у них возможно появление рецидива заболевания и отдалённых метастазов. Нельзя ограничиваться только опросом и осмотром явившихся с какими-либо жалобами больных, так как на ранних стадиях рецидив рака толстой кишки может никак себя не проявлять.
Осмотр нужно проводить каждые три месяца с использованием пальцевого исследования, ректороманоскопии, колоноскопии или ирригоскопии оставшихся отделов толстой кишки; 1 раз в 6 мес - УЗИ печени, брюшной полости и полости малого таза, рентгенография грудной клетки. Из лабораторных анализов может быть полезным определение уровня канцероэмбрионального антигена. При подозрении на рецидив для более точной диагностики необходима КТ, возможно использование МРТ.
85% местных рецидивов выявляют в течение первых 2 лет после операции, а средний срок появления рецидивов равен 13 мес. По данным ГНЦ колопроктологии, при своевременном обнаружении рецидивов и метастазов у трети больных можно выполнить их хирургическое удаление. Остальным пациентам, к сожалению, приходится рекомендовать паллиативное лечение (лучевое и химиотерапию), которое несколько облегчает их положение.
Читайте также:






