Лечение гематурии при раке мочевого пузыря
На рак мочевого пузыря, по данным ВОЗ 2001 г., приходится около 3% всех злокачественных новообразований. По степени распространенности он уступает только опухолям желудка, пищевода, легких и гортани. По количеству клинических
На рак мочевого пузыря, по данным ВОЗ 2001 г., приходится около 3% всех злокачественных новообразований. По степени распространенности он уступает только опухолям желудка, пищевода, легких и гортани. По количеству клинических проблем, разнообразию и сложности хирургических операций раку мочевого пузыря отводится одно из первых мест в онкоурологии.
Среди всех онкоурологических заболеваний новообразования мочевого пузыря занимают второе место по заболеваемости после рака предстательной железы. Ежегодно в мире регистрируется более 150 тыс. новых случаев рака мочевого пузыря. Рак мочевого пузыря занимает пятое место у мужчин и 11-е у женщин по распространенности в Европе из всех форм этого заболевания (А. С. Переверзев, С. Б. Петров, 2001). Из морфологических форм наиболее часто встречается переходно-клеточный рак, на него приходится до 90%. Менее 10% составляют аденокарцинома, плоскоклеточный рак и сквамозно-клеточная карцинома.
Около 80% всего первичного рака мочевого пузыря (РМП) представлено поверхностными опухолями. Лечение данного вида заболевания включает трансуретральную резекцию (ТУР), иммуно- и химиотерапию. Но риск рецидива у этих пациентов составляет до 70%. Почти в 30% случаев рецидивов отмечается повышение стадии заболевания и/или степени злокачественности, т. е. поверхностный РМП прогрессирует в инвазивную форму. У 50% таких больных через два года после подобного локального лечения выявляются метастазы.
Несмотря на успехи в диагностике и лечении, все последние годы отмечается рост заболеваемости раком мочевого пузыря. Все вышесказанное объясняет внимание клиницистов к этому опасному заболеванию.
В самом начале заболевания клинические проявления рака мочевого пузыря скудные и во многом зависят от стадии болезни, наличия осложнений, сопутствующих заболеваний, особенно хронического пиелонефрита и хронической почечной недостатости. Основными симптомами эпителиальных опухолей мочевого пузыря следует считать гематурию и дизурию.
Гематурия является самым частым и наиболее ранним признаком опухоли мочевого пузыря. Как первый признак болезни макрогематурия отмечается примерно у 70% больных раком мочевого пузыря. Гематурия при опухоли мочевого пузыря может быть терминальной и тотальной. Длительность и частота кровотечений при опухолях мочевого пузыря колеблются в широких пределах. Иногда гематурия бывает кратковременной, повторяется с многомесячными и даже многолетними интервалами. В ряде случаев она длится несколько дней (и даже недель) подряд и повторяется часто. При запущенных распадающихся опухолях мочевого пузыря гематурия обычно имеет постоянный характер.
Вторым по распространенности симптомом является дизурия, которая наблюдается в 15—37% случаях. Она обусловлена раздражением слизистой мочевого пузыря и характеризуется жжением при мочеиспускании, частыми позывами на мочеиспускание, поллакиурией. В основном дизурия характерна для опухолей, локализующихся в области шейки и опухолей с инфильтративным ростом. Мочеиспускание становится не только учащенным, но и затрудненным и болезненным. При прогрессировании опухолевого процесса у больных появляются боли в надлобковой области, которые носят постоянный характер. Боли усиливаются в конце мочеиспускания. Интенсивность боли зависит от локализации и характера роста опухоли. При шеечной локализации боль появляется рано. Экзофитные новообразования могут достигать больших размеров, не вызывая болей. Эндофитный рост опухолей сопровождается постоянной тупой болью над лоном и в полости малого таза. В случае прорастания опухоли стенки мочевого пузыря с переходом на паравезикальную клетчатку и соседние органы могут возникать симптомы тазовой компрессии, проявляющиеся отеком нижних конечностей, мошонки, флебитом, болевым синдромом в промежности, ягодицах, крестце, поясничной области, половых органах.
При прогрессировании заболевания происходит сдавление устьев мочеточников, что и определяет клинические проявления.
Диагностика рака мочевого пузыря включает также определение функции почек и состояния уродинамики верхних и нижних мочевых путей. Такая задача не менее важна, чем определение стадии опухоли, ее локализации и распространенности. Традиционные методы, применяемые для этих целей (экскреторная урография, цистография), находят сейчас ограниченное применение. Их используют в настоящее время по показаниям.
Еще недавно цистоскопия была первой диагностической процедурой, которая выполнялась при подозрении на РМП. В настоящее время она проводится на завершающем этапе диагностики, когда больному назначается лечение. Как отдельная процедура цистоскопия выполняется только при моноторинге больных РМП. В основном цистоскопию совмещают с лечебно-диагностической трансуретральной резекцией мочевого пузыря.
Ультразвуковая диагностика — высокоинформативный безболезненный и абсолютно безвредный метод, позволяющий оценить состояние внутренних органов. При плановом обследовании больных РМП ведущим методом диагностики сейчас считается ультрасонография мочевого пузыря. Ультразвуковое исследование (УЗИ) позволяет в какой-то мере оценивать опухоль по стадиям, выявлять изменения в забрюшинной и тазовой клетчатке и пораженные метастазами лимфоузлы. При этом используют трансабдоминальное и трансректальное исследования. Но проведение УЗИ только с каким-то одним из датчиков нецелесообразно. Ошибки в оценке местного распространения РМП возможны и при всех видах ультрасонографии (УС). Они могут быть вызваны рубцовыми изменениями стенок мочевого пузыря вокруг опухоли, их трабекулярностью, наличием цистита и многими другими причинами. УЗИ также не позволяет с высокой степенью точности выявлять опухоли небольшого размера (менее 10 мм) и опухоли в трабекулярном мочевом пузыре. По оценкам разных авторов, частота ошибок при таких исследованиях составляет от 17 до 30%.
С внедрением в практику внутриполостных датчиков значительно повысились диагностические возможности выявления ранних стадий рака мочевого пузыря. Трансуретральная ультрасонография (цистоэндосонография) достаточно достоверно позволяет диагностировать поражение мышечного слоя. В отличие от трансабдоминальной и трансректальной УС, цистоэндосонография делает возможным детальное изучение местного распространения процесса даже при очень небольших размерах ( 0,5 Т) МРТ-систем компактностью и экономичностью при удовлетворительном качестве изображений и значительно меньшей стоимости.
В настоящее время разработаны методы ранней диагностики РМП, основанные на тумор-ассоциированных антигенах. Кроме этого, создано большое количество моноклональных антител, специфичных для переходно-клеточного РМП. Данные антитела взаимодействуют с антигенными структурами, присутствующими только на клетках переходно-клеточного РМП и отсутствующими на клетках нормального уротелия. К ним относятся тест ВТА-Stat, ВТА-Stat и NMP22. Многие из перечисленных маркеров еще изучаются и не нашли своего практического применения.
Отдельно хочется остановиться на тесте ВТА-Stat, который представляет собой иммуннохроматографический метод, позволяющий производить с использованием моноклональных антител быстрый специфический анализ антигена опухоли мочевого пузыря в моче. Большим достоинством метода является простота и доступность выполнения в амбулаторных условиях. Техника исследования проста: моча обследуемого пациента вносится в тест-лунку, спустя 5 мин оценивается результат. Положительной проба может считаться в том случае, если в окошечке появится красно-коричневая полоска.
В последние годы все более широкое развитие получает еще один метод раннего выявления РМП — фотодинамическая диагностика. Метод основан на возможности стимуляциии выработки внутриклеточного флюоресцирующего протопорфирина 9 из -5-аминолевулиновой кислоты (5АЛК), выборочно, преимущественно в опухолевой клетке. Также считается, что этот метод может лечь в основу нового направления в лечении рака мочевого пузыря благодаря происходящим фотохимическим реакциям, в результате которых происходит гибель опухолевых клеток. Впервые принцип окрашивания опухоли был применен в дерматологии для демаркации и фотодинамической терапии кожных заболеваний. С середины 90-х гг. появился опыт применения фотодинамической диагностики в урологии. Актуальность этой проблемы в отношении рака мочевого пузыря связана с несколькими основными положениями. Во-первых, с наличием плоских опухолей, практически не различимых при эндоскопии в белом свете. Во-вторых, с высоким процентом резидуальных опухолей после трансуретральной резекции.
Для проведения флюоресцентной цистоскопии необходимы некоторый минимальный набор оборудования, основной частью которого является источник света, обладающий, прежде всего, в синей области спектра очень высокой мощностью для возбуждения флюоресценции, и специальный эндоскоп. Особое преимущество заключается в том, что все приборы, разработанные для флюоресцентной цистоскопии, без ограничения могут использоваться и для цистоскопии в белом свете. Кроме того, их можно как угодно комбинировать с подходящими стандартными инструментами. Побочные явления в результате внутрипузырной инстилляции 5-аминолевулиновой кислоты минимальны. До настоящего времени не было сообщений о проявлении кожной сенсибилизации. Также не наблюдалось и фототоксических реакций кожи, как это случается при системно применяемых синтетических порфиринах. При этом только около 7% больных жалуются на учащенное мочеиспускание.
При инвазивном РМП ТУР рассматривается как диагностическая процедура, позволяющая выявить степень инвазии. С паллиативной целью ТУР выполняется у больных, которые отказываются от цистэктомии или из-за фона сопутствующих заболеваний не в состоянии перенести. Цель резекции — удаление всей опухоли с участком нормальной мышечной ткани с целью определения степени инвазии. ТУР может выполняться также под фотодинамическим контролем.
На современном этапе хирургическое лечение поверхностного рака мочевого пузыря должно обязательно дополняться внутрипузырной иммунохимиотерапией для профилактики рецидивов и предупреждения прогрессирования опухоли. Для этой цели используется целый ряд препаратов для внутрипузырной химиотерапии.
Все вышеуказанные вещества обладают приблизительно одинаковой эффективностью. Возможно, единственное исключение составляет митомицин, который показывает более высокие результаты.
В последние годы иммунопрофилактика и иммунотерапия рака мочевого пузыря получили широкое распространение. Из числа известных иммуномодуляторов чаще всего используют вакцину БЦЖ. Механизм противоопухолевого действия вакцины БЦЖ до конца не изучен, однако многочисленные исследования показали, что в его основе лежит стимуляция клеточных механизмов иммунитета, в которой задействованы Т-лимфоциты, макрофаги и целый ряд цитокинов. БЦЖ вводится внутрипузырно и по эффективности превосходит все другие препараты. Существуют различные схемы применения вакцины БЦЖ, но указаний на то, что какая-либо из них предпочтительней другой, нет. Мы применяем схему 120 мг в 50 мл физраствора в течение шести недель еженедельно через три-четыре недели после ТУР. БЦЖ терапия назначается: 1) для профилактики рецидивов у пациентов без опухолей; 2) при лечении больных с рецидивными опухолями; 3) при лечении пациентов с карциномой in situ. Помимо БЦЖ заслуживают упоминания еще два препарата, оказывающих иммуномодулирующее действие: интерлейкин-2 и ИФ. Они обладают доказанной иммуномодулирующей и противоопухолевой активностью, но по эффективности уступают БЦЖ.
Радикальная цистэктомия является методом выбора в лечении инвазивного рака мочевого пузыря при благоприятном прогнозе, касающемся продолжительности жизни пациента. Большинство урологов выполняют это вмешательство на стадиях Т2b и Т3, а также при мультифокальном и\или быстрорецидивирующем поражении в стадии Т1 с гистологическими признаками низкодифференцированного роста, раке in situ, резистентном к БЦЖ терапии. В зависимости от степени прорастания околопузырной клетчатки, предстательной железы у мужчин и внутренних половых органов у женщин, а также вовлечения в процесс регионарных лимфатических узлов, выполняют удаление одного только мочевого пузыря или расширенную цистэктомию, включающую, наряду с удалением пузыря, удаление предстательной железы с семенными пузырьками у мужчин и удаление уретры, передней стенки влагалища и матки у женщин. При расширенной цистэктомии во всех случаях подлежат удалению околопузырная клетчатка, тазовые лимфоузлы и прилегающая брюшина.
Предложено множество различных методик деривации мочи после цистэктомии, которые можно разделить на шесть основных групп. Выбор способа лечения связан, прежде всего, с возрастом пациента, соматическим статусом, тяжестью основного заболевания и наличием осложнений: 1) создание артифициального мочевого пузыря; 2) пересадка мочеточников в непрерывную кишку; 3) пересадка мочеточников в изолированный сегмент кишки; 4) непосредственное дренирование почек (нефро- или пиелостомия); 5) пересадка мочеточников на кожу; 6) трансуретероанастомоз с односторонней нефростомией.
Послеоперационная летальность при раке мочевого пузыря за последние 25 лет снизилась с 46% до 3-4%. Но в большинстве медицинских центров она по-прежнему достаточно высока. Основными причинами летальных исходов являются перитонит, почечная недостаточность, восходящий пиелонефрит и уросепсис.
Учитывая большой объем операции, неудовлетворительное качество жизни с мочеприемниками, многие больные отказываются от цистэктомии.
В этом случае, как и при отдаленных метастазах, единственный метод помощи — химиотерапия. РМП чувствителен к цисплатину, доксорубицину, винбластину, ифосфамиду, фторурацилу, циклофосфамиду, карбоплатину, митоксантрону, метотрексату. Из препаратов, появившихся в 90-х гг., привлекают внимание паклитаксел, доцетаксел и гемзар; комбинация из препаратов выбора — М-VАС (метотрексат, винбластин, доксорубицин и цисплатин). Эффект достигается у 40—60% пациентов, в том числе и симптоматический, средняя выживаемость — 13 месяцев. Хорошие результаты показывает гемцитабин — это одно из наиболее эффективных средств для монотерапии. Кроме того, он хорошо переносится пациентами.
В мировой практике сложилось неоднозначное отношение к лучевой терапии при раке мочевого пузыря. В США первичная лучевая терапия рака мочевого пузыря практически не применяется. В Великобритании и Европе это основной метод лечения распространенного рака мочевого пузыря, а цистэктомия выполняется лишь при снижении радиочувствительности. В нашей стране лучевая терапия при раке мочевого пузыря применяется как самостоятельно, так и в сочетании с хирургическим и/или химиотерапевтическим лечением. Облучение может осуществляться как на аппаратах для дистанционной, так и контактной лучевой терапии. Причем оптимальная методика лучевой терапии выбирается в зависимости от локализации опухолевого процесса в мочевом пузыре и степени его внепузырного распространения. Так, при прорастании опухолью мышечной стенки или наличии метастатического поражения зон регионарного лимфооттока, необходимо проведение послеоперационной лучевой терапии. При раке мочевого пузыря можно применять и брахитерапию (внутриполостная и внутритканевая лучевая терапия). Однако из-за сложности проведения и дороговизны она проводится, в основном, в экономически развитых странах, где есть крупные специализированные центры. При внутриполостном облучении разовая очаговая доза составляет, как правило, 3—5 Гр, а суммарная очаговая доза доводится до 45—50 Гр. При сочетанном облучении доза при внутриполостной лучевой терапии составляет, в среднем, 30—35 Гр.
На основании личного клинического опыта мы можем утверждать, что при лечении опухолей мочевого пузыря есть возможность ограничиться одной лишь ТУР только при наличии поверхностного (неинвазивного) дифференцированного рака. Во всех остальных случаях за ней должна следовать цистэктомия или лучевая терапия по радикальной программе.
Несомненно, наилучшие результаты при лечении рака мочевого пузыря, как и большинства других злокачественных новообразований, получены при использовании комбинированного метода. Так, Б. П. Матвеев (1999) указывает на то, что, в среднем, рецидив опухоли после ТУР мочевого пузыря в течение трех лет встречается у 45—55% больных. В то же время даже после радикальных операций рецидивы возникают в 30—60% случаев, тогда как после комбинированного лечения — всего в 28%. В связи с этим не стоит забывать о вопросах, связанных с качеством жизни больных после проведенного лечения. На наш взгляд, приоритетными направлениями в лечении рака мочевого пузыря станут органосохраняющие или максимально щадящие мочевой пузырь методики, основанные на сочетании неоадъювантной и адъювантной химиолучевой терапии, и разработка адекватного способа деривации мочи с созданием ортотопического мочевого пузыря.
А. Д. Каприн, кандидат медицинских наук
А. А. Костин
Российский научный центр рентгенорадиологии МЗ РФ, Москва
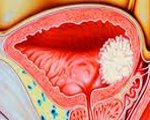
Рак мочевого пузыря – это злокачественная опухоль слизистой оболочки или стенки мочевого пузыря. Проявлениями патологии служат гематурия, дизурия, боли над лобком. Диагностика требует проведения цитологического исследования мочи, ТУР-биопсии, цистографии, УЗИ мочевого пузыря, томографии. Программа лечения заболевания может включать хирургический подход (ТУР мочевого пузыря, цистэктомию, лазерную en-bloc резекцию) или консервативную тактику (системную химиотерапию, лучевую терапию). С целью профилактики рецидивов используется внутрипузырная химиотерапия и БЦЖ-терапия.
МКБ-10

- Причины
- Классификация
- Симптомы
- Осложнения
- Диагностика
- Лечение рака мочевого пузыря
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Рак мочевого пузыря встречается в 70% случаев всех новообразований мочевыводящих органов, с которыми сталкиваются специалисты в сфере клинической онкоурологии. В структуре общей онкопатологии доля неоплазий данного органа составляет 2-4%. Среди злокачественных опухолей различных локализаций по частоте развития рак мочевого пузыря занимает 11-е место у женщин и 5-е у мужчин. Патология чаще встречается у жителей индустриально развитых стран; возраст заболевших преимущественно старше 65-70 лет.

Причины
Общепризнанной гипотезы в отношении этиологии рака мочевого пузыря не существует. Однако известны отдельные факторы риска, которые в значительной степени способствуют развитию злокачественной опухоли:
- Редкое мочеиспускание. Ряд исследований указывает на повышенную вероятность возникновения неоплазии при длительном стазе мочи в мочевом пузыре. Различные метаболиты, содержащиеся в моче в высоких концентрациях, обладают опухолегенным действием и вызывают злокачественную трансформацию уротелия.
- Заболевания мочеполовой сферы. Длительной задержке мочи в мочевом пузыре может способствовать различная урогенитальная патология: простатит, аденома и рак простаты, дивертикулы мочевого пузыря, уролитиаз, хронический цистит, стриктуры уретры и др.
- Инфекции. Вопрос о роли папилломавирусной инфекции в этиологии новообразования остается дискуссионным. Паразитарная инфекция - мочеполовой шистосомоз в значительной мере способствует канцерогенезу.
- Профвредности. Доказана корреляция между частотой случаев рака мочевого пузыря и профессиональными вредностями, в частности, длительным контактом с ароматическими аминами, фенолами, фталатами, противоопухолевыми препаратами. В группе находятся риска водители, маляры, дизайнеры, художники, работники кожевенной, текстильной, химической, лакокрасочной, нефтеперерабатывающей промышленности, медработники.
- Прочие канцерогены. Высоким канцерогенным потенциалом обладает курение табака: курильщики страдают от оухолей мочевого пузыря в 2-3 раза чаще, чем некурящие. Неблагоприятное воздействие на уротелий оказывает употребление хлорированной питьевой воды, увеличивающее вероятность возникновения новообразований в 1,6-1,8 раз.
- Наследственность. В некоторых случаях неоплазия может быть детерминирована генетически и связана с семейной предрасположенностью.
Классификация
Рак мочевого пузыря различается по гистологическому типу, степени дифференцировки клеток, характеру роста, склонности к метастазированию. Учет этих характеристик чрезвычайно важен при планировании лечебной тактики. По морфологическим признакам наиболее часто встречаются переходно-клеточные (80-90%) и плоскоклеточные опухоли (3%), аденокарцинома (3%), папиллома (1%), саркома (3%). По степени анаплазии клеточных элементов различают низко-, умеренно- и высокодифференцированные неоплазии.
Практическое значение имеет степень вовлеченности в опухолевый процесс различных слоев стенки органа, в связи с чем говорят о поверхностном раке низкой стадии или высокостадийном инвазивном раке. Новообразование может иметь папиллярный, инфильтративный, плоский, узелковый, внутриэпителиальный, смешанный характер роста. Согласно международной системе ТNМ различают следующие стадии неоплазии:
- Та - неинвазивная папиллярная карцинома
- Tis – плоская карцинома in situ
- Т1 – опухолевая инвазия затрагивает субэпителиальную ткань
- Т2 – рак распространяется на мышечный слой (Т2а - поверхностный, Т2b - глубокий)
- Т3 – в процесс вовлекается паравезикальная клетчатка
- Т4 – инвазия затрагивает прилежащие органы (влагалище, матку, предстательную железу, брюшную стенку)
- N1-3 – выявляется метастазирование в одном (N1) или многих (N2) регионарных лимфоузлах либо в общих подвздошных лимфатических узлах (N3).
- М1 - обнаруживается метастазирование в отдаленные органы
Симптомы
Ранним проявлением рака мочевого пузыря служит выделение крови с мочой – микрогематурия или макрогематурия. Незначительная гематурия приводит к окрашиванию мочи в розоватый цвет, может быть эпизодической и не повторяться длительное время. В других случаях сразу же развивается тотальная гематурия: при этом моча становится кровавого цвета, могут выделяться сгустки крови. Длительная или массивная гематурия иногда вызывает развитие тампонады мочевого пузыря и острой задержки мочи, происходит прогрессирующее снижение гемоглобина и анемизация пациента.
По мере разрастания опухоли больных начинают беспокоить дизурические симптомы и боли. Мочеиспускание, как правило, становится болезненным и учащенным, с императивными позывами, иногда – затрудненным. Отмечаются боли в области лона, в паху, в промежности, в крестце. Вначале болевые ощущения возникают только на фоне наполненного мочевого пузыря, затем, при прорастании мышечной стенки и прилежащих органов, становятся постоянными.
Многие симптомы рака мочевого пузыря не являются специфичными и могут встречаться при других урологических заболеваниях: цистите, простатите, мочекаменной болезни, туберкулезе, аденоме простаты, склерозе шейки мочевого пузыря и т. д. Поэтому зачастую пациенты на ранних стадиях длительно и неэффективно лечатся консервативно. В свою очередь, это затягивает своевременную диагностику и начало лечения, ухудшая прогноз.
Осложнения
Сдавление устья мочеточника вызывает нарушение оттока мочи из соответствующей почки. Развивается гидронефроз, острый болевой приступ по типу почечной колики. При сдавливании обоих устьев нарастает почечная недостаточность, которая может закончиться уремией. Некоторые виды рака с инфильтрирующим ростом склонны к распаду и изъязвлению пузырной стенки. На этом фоне легко возникают мочевые инфекции (цистит, пиелонефрит), моча приобретает гнойный характер и зловонный запах. Прорастание неоплазии в прямую кишку или во влагалище приводит к образованию пузырно-прямокишечных и пузырно-влагалищных свищей, сопровождающихся соответствующей симптоматикой.
Диагностика
Для выявления рака и определения стадии онкопроцесса требуется проведение комплексного клинико-лабораторного и инструментального обследования. Стандарт лабораторной диагностики включает проведение общего анализа мочи для определения гематурии, цитологического исследования осадка для обнаружения атипичных клеток, бактериологического посева мочи для исключения инфекции, теста на специфический антиген ВТА. Исследование крови обычно подтверждает анемию различной степени, указывающую на кровотечение.
- УЗИ мочевого пузыря. Выявляет опухолевые образования диаметром более 0,5 см, расположенные преимущественно в области боковых пузырных стенок. Для обнаружения неоплазии в зоне шейки наиболее информативно трансректальное сканирование. Иногда используется трансуретральная эндолюминальная эхография, проводимая с помощью датчика, введенного в полость мочевого пузыря.
- Томографическая диагностика. Наиболее ценные и информативные методы - КТ и МРТ мочевого пузыря. Позволяют оценить глубину распространения опухолевого процесса, выявить опухоли незначительных размеров, которые не доступны эхографической визуализации.
- Эндоскопия мочевого пузыря. Обязательным визуализирующим методом диагностики служит цистоскопия, при которой производится уточнение локализации, размеров, внешнего вида опухоли, состояния устьев мочеточников. Эндоскопическое исследование может дополняться биопсией, позволяющей провести морфологическую верификацию новообразования.
- Рентгенодиагностика. Из методов лучевой диагностики при раке мочевого пузыря проводится цистография, выявляющие дефект наполнения и деформацию контуров пузырной стенки и позволяющие судить о характере роста опухоли. Тазовую венографию и лимфангиоаденографию проводят для выявления вовлеченности тазовых вен и лимфатического аппарата.
Для выявления местных и отдаленных метастазов рака мочевого пузыря прибегают к проведению УЗИ органов брюшной полости, рентгенографии грудной клетки, УЗИ малого таза, сцинтиграфии костей скелета.

Лечение рака мочевого пузыря
Радикальное лечение может быть выполнено только хирургическими способами. При этом способ и вид операции коррелирует со стадией онкопроцесса. Виды оперативных вмешательств при раке мочевого пузыря:
- ТУР мочевого пузыря. При мышечно неинвазивном раке выполняется эндоскопическая операция - трансуретральная резекция стенки мочевого пузыря с опухолью. В ходе ТУР опухоль удаляется с помощью резектоскопа через мочеиспускательный канал.
- Лазерная en-bloc резекция. Наиболее современный метод - лазерная тулиевая en-bloc резекция. Данный метод позволяет убрать опухоль единым блоком вместе с мышечным слоем, что очень важно при гистологическом исследовании для оценки степени инвазии.
- Цистэктомия. К резекции мочевого пузыря (открытой, лапароскопической, робот-ассистированной) в последние годы прибегают все реже ввиду высокого процента рецидивов, осложнений и низкой выживаемости. В большинстве случаев при инвазивном раке мочевого пузыря показана радикальная цистэктомия. При проведении данной операции мочевой пузырь удаляют единым блоком с предстательной железой и семенными пузырьками у мужчин; придатками и маткой у женщин. Одновременно производится удаление части или всей уретры, тазовых лимфоузлов.
Для замещения удаленного органа используются следующие способы:
- имплантация мочеточников в кожу - уретерокутанеостомия
- отведение мочи в сигмовидную кишку - способ деривации мочи по Брикеру
- формирование кишечного резервуара по Штудеру (ортотопического мочевого пузыря) из тканей тонкой кишки, желудка, толстой кишки. Радикальная цистэктомия с кишечной пластикой является оптимальной, поскольку позволяет сохранить возможность удержания мочи и мочеиспускания.
Хирургическое лечение может дополняться дистанционной или контактной лучевой терапией, системной или внутрипузырной иммунотерапией.
Прогноз и профилактика
При неинвазивном раке показатель 5-летней выживаемости составляет около 85%. Гораздо менее благоприятен прогноз для инвазивно растущих и рецидивирующих опухолей, а также рака мочевого пузыря, дающего отдаленные метастазы. Снизить вероятность развития опухоли поможет отказ от курения, исключение профессиональных вредностей, употребление очищенной питьевой воды, ликвидация уростаза. Необходимо проведение профилактического УЗИ, исследования мочи, своевременного обследования и лечения у врача-уролога при симптомах дисфункции мочевых путей.
Рак мочевого пузыря — заболевание, при котором в слизистой оболочке или стенке мочевого пузыря образуется злокачественное образование. Первые симптомы такого образования: кровь в моче, боль над лобком. У мужчин болезнь встречается в несколько раз чаще женщин, что связано с болезнями предстательной железы, ведущих к застою мочи. Симптомы могут долго отсутствовать, что приводит к поздней диагностике и затруднению лечения.
Лечение рака передовыми методами проводится в Юсуповской больнице. Одним из ведущих направлений клиники является онкоурология, специализирующаяся на лечении и диагностике злокачественных образований мочеполовой системы.
Причины рака мочевого пузыря
Конкретной причины, вызывающей РМК не обнаружено. Известно, что метаболиты, содержащиеся в высоких концентрациях в моче, повреждают уротелий и вызывают его озлокачествление. Такими свойствами обладают ароматические амины и их производные (бензидин, нитрозамины, аминобифенил, анилин), бензол, моющие и красящие вещества. Для возникновения новообразования потребуется около 20 лет контакта с канцерогеном. Опухоль может быстро развиваться и затрагивать глублежащие слои.
Врачи относят к факторам риска РМП следующее:
- Работу на потенциально опасных предприятиях: красильных, резиновых, текстильных, алюминиевых, пластмассовых, каучуковых и нефтяных;
- Проживание на расстоянии менее 1 км от промышленных объектов, загрязняющих окружающую среду дымом, копотью, химическими веществами;
- Работу на автомобильном и сельскохозяйственном транспорте: водители грузовиков, трактористы, комбайнеры, шоферы, заправщики;
- Курение более 10 лет. Курильщики страдают РМП в 3 раза чаще. Особенно опасны папиросы и сигареты без фильтра и черный табак из-за высокого содержания аминов;
- Постоянный мочевой катетер провоцирует нарушение воспаление слизистой и присоединение инфекции;
- Хромосомные мутации, инактивация генов-супрессоров;
- Длительное употребление больших доз спиртного;
- Воспаление органов малого таза: циститы, камни МП. Увеличение предстательной железы в размере и её поражение может привести к застою и нарушению вывода мочи.
Доказано влияние лекарственных препаратов на появление злокачественных образований МП. Анальгетики, содержащие фенацетин, при длительном применении оказывают токсическое воздействие на почки и эпителий мочевыводящего органа. По результатам международных исследований химиотерапия с применением циклофосфамида увеличивает риск РМП.
Появлению РМП у женщин способствует облучение органов малого таза по поводу рака шейки, тела матки и яичников. У мужчин причиной облучения малого таза может быть рак предстательной железы.
Установлена связь между онкологией мочевого пузыря и шистосомозом. Эта паразитарная инфекция носит эндемичный характер на Ближнем Востоке, Юго-Востоке Азии и Северной Африке.
Рак мочевого пузыря: классификация
Опухоль мочевыводящего органа соответствуют по МКБ-10 коду С67. Классификация новообразований МП по МКБ-10. По расположение РМП делят на:
- Рак треугольника МП;
- Рак шейки МП;
- Рак боковой стенки МП;
- Рак задней стенки МП;
- Рак передней стенки МП;
- Рак купола МП.
Распространение новообразования в мышечный слой делит пациентов на 2 группы:
- С мышечно-инвазивный раком;
- С мышечно-неинвазивным раком МП.
Это разделение важно для выбора стратегии лечения больных так как неинвазивные (более раннее название – поверхностные) новообразования могут быть удалены трансуретральной резекцией МП (ТУР).
Морфологическая классификация подразумевает деление согласно гистологическому строению злокачественного образования:
- Эпителиальные (карцинома);
- Неэпителиальные (саркома).
Наиболее часто диагностируется переходно-клеточный рак. Другое название патологии уротелиальная карцинома. По степени злокачественности выделяют низкодифференцированную и высокодифференцированную карциному. Низкодифференцированная уротелиома является более опасной формой, хуже поддается лечению и чаще возвращается.
Переходно-клеточная карцинома мочевого пузыря in situ (in situ – на месте) представляет неинвазивное плоское образование, ограниченное одним слоем стенки моченакопительного органа — эпителием. Злокачественная трансформация не всегда поражает все слои. Иногда патологические образования находятся лишь в поверхностном или базальном слое в виде групп, расположенных среди нормальных эпителиальных клеток. Карцинома ин ситу — первичная стадия РМП, долгое время не вызывает симптоматику и зачастую диагноз ставится случайно на профосмотре. Прогноз для пациентов с карциномой ин ситу после лечения благоприятный — сто процентная пятилетняя выживаемость.
Уротелиальная промежуточно-клеточная опухоль мочевыводящего органа — обычно изолированное образование небольшого размера, выступающее в просвет органа. Чаще бывает у мужской половины населения в возрасте, рецидивирует в 8% случаев.
Нефрогенная опухоль нередко формируется на фоне хронического цистита, после травм и операций мочевыводящего органа. Может быть по ошибке принята за рак так как растет в виде полиповидного образования.
К неэпителиальным новообразованиям МП относятся:
- Опухоли фиброзной ткани: фибромы — зрелые и фибросаркомы — незрелые;
- Опухоли из мышечной ткани.
Для установления стадии болезни в онкологии применяют типологию TNM, которая состоит из трех составляющих:
- T (от лат. tumor – опухоль). Дополнительные цифры 1-2 определяют поверхностный опухолевый процесс. Цифры 3-4 указывают на прорастание образования в мышечный и глубоколежащие слои;
- N (от лат. nodus — узел). Дополнительно обозначается цифрой 0, если метастазы в регионарных лимфоузлах никак не формируются. N1 указывает на единичный пораженный лимфоузел, N2 метастаз в 2-5 лимфоузлах;
- M (от греч. metastasis — перемещение). При помощи буквы M онкологи отмечают присутствие или недостаток дальних метастазов.
1 стадия характеризуется наличием раковых клеток только в эпителиальном слое, метастазов нет. При своевременном лечении пятилетняя выживаемость может быть более 90%.
2 стадия. На это степень указывает распространение образования в мышечный слой. Пятилетняя выживаемость 70%.
3 стадия имеет менее благоприятный прогноз, пятилетняя выживаемость 55%. На этой степени развития помимо прорастания в мышечный слой характерно поражение региональных лимфоузлов.
На 4 стадию РМП указывают метастазы в регионарные и отдаленные лимфоузлы, опухоль неоперабельна.
Симптомы РМП
- Гематурия;
- Боль над лобком;
- Дизурия.
На начальном этапе заболевание протекает бессимптомно. Наиболее характерный ранним симптом РМП всех стадий — кровь в моче. Существует микро- и макрогематурия. Микрогематурия обнаруживается лишь микроскопическом анализе, макрогематурию можно обнаружить самостоятельно в виде капель крови в моче. Врачи выделяют терминальную и тотальную гематурию.
Терминальная макрогематурия выявляется в конце акта мочеиспускания и наблюдается при раке шейки МП. Тотальная макрогематурия характеризуется выделением сгустков крови на протяжении всего акта мочеиспускания. Этот тип определяется при образованиях МП любого положения. При этом цвет мочи изменяется на ярко-красный. В последних стадиях формирования новообразования и его распада моча принимает вид мясных помоев.
Кровотечение зачастую появляется безболезненно и внезапно, может повторяться неоднократно несколько суток. Сгустки крови способны закрывать просвет сфинктера и вызвать затруднения оттока мочи. Частая гематурия приводит к потере крови, развитию анемии и слабости.
Течение рака мочевого пузыря сопровождается расстройствами акта мочеиспускания. Дизурия является вторым по частоте признаком РМП. Больные жалуются на учащенное до 10 раз в сутки, болезненное мочеиспускание. По мере роста объемов злокачественного образования вместительность мочевыводящего органа и количество испражнений уменьшается, частота позывов увеличивается. При закрытии просвета мочеиспускательного канала новообразованием или сгустками крови наблюдается задержка мочи и приступ почечной колики. Длительный застой мочи вызывает развитие инфекций, таких как пиелонефрит и цистит.
Боль на первых стадиях болезни появляется над лобком и с увеличением размеров опухоли усиливается.
Боль при новообразованиях в мочевом пузыре способна иррадиировать в:
- Промежность;
- Область крестца;
- Головку полового члена;
- Задний проход;
- Нижние конечности.
Общие симптомы РМП:
- Стойкое повышение температуры;
- Быстрая утомляемость;
- Истощение, потеря веса;
- Нарушение сна;
- Появление отеков ног, промежности, мошонки на поздних стадиях заболевания;
- Хронические боли в надлобковой области;
- В терминальной стадии возникает синдром полиорганной недостаточности.
Метастазами при РМП поражаются следующие органы:
- Костная ткань. Опухолевые клетки приводят к усилению активности остеокластов;
- Легкие;
- Печень;
- Половые органы.
Диагностика РМП
Важнейший фактор успешного излечения подобных болезней — ранняя диагностика. Чем раньше опухоль будет обнаружена, тем меньше риск осложнений. РМП способен рецидивировать в 50% случаев поэтому важна не только диагностика, но и полное удаление очагов раковых клеток. Диагноз ставится на основании сбора анамнеза, физикального обследования, итогах лабораторной и приборной диагностики.
Диагностика РМП включает:
- Анализ жалоб пациента и последующее физикальное обследование. Во время осмотра больного врач проводит пальпацию мочевого пузыря, возможных зон метастазирования.
- Лабораторные анализы крови и мочи. Общие и биохимические исследования крови не дают нужной информации для установления диагноза РМП. Специфичным методом является определение белка UBS - антигена РМП. При положительном результате количество белка увеличено в 15 раз. Однако возможны ложноположительные результаты при воспалительных заболеваниях мочевыводящей системы. Среди других анализов мочи используется микроисследование осадка мочи на наличие патологических клеток. В Этом случае более информативно исследование смывов со стенок пораженного органа. Цистоскопия не всегда дает возможность определить безошибочное заключение и используется при наличии противопоказаний к цистоскопии или как скрининг-тест для определения РМП на ранней стадии;
- Инструментальные исследования. Наиболее информативный способ обнаружения РМП — цистоскопия. Этот инвазивный, но высокоинформативный метод позволяет установить размер, локализацию, форму и характер роста патологического очага. Цистоскопия предоставляет возможность взятия биопсии – куска ткани для дифференциальной диагностики рака и предракового состояния. При правильном проведении биопсии МП процедура не опасна для здоровья пациента и не влияет на темпы развития новообразования.
При помощи УЗИ органов малого таза определяют форму, характер роста, размеры патологического очага, а также наличие метастазов в лимфоузлах. Исследование высокоинформативное при размерах опухоли более 5мм.
Экскреторная урография отображает проходимость мочевыводящих путей, которая может быть нарушена вследствие давления образования или сгустком крови.
КТ и МРТ при раке мочевого пузыря устанавливает наличие опухоли, прорастания в близлежащие органы. КТ помогает определять стадию формирования РМП по TNM.
Для выявления распространения образования МП на соседние органы используют тазовую артериографию (изучение сосудов таза после введения контрастного вещества).
В Юсуповской больнице имеется все необходимое для сдачи анализов и проведения диагностики РМП. Достоинством клиники является комфортные условия обследования, современное высокотехнологичное оборудование в распоряжении специалистов различных профилей, профессионалов своего дела.
Лечение рака мочевого пузыря
Лечение РМП на первой стадии, когда раковые опухоли находятся на поверхностных слоях уротелия, следует начинать с ТУР мочевого пузыря. ТУР — трансуретральная резекция. На основе такой операции выносится решение о том, проросла или нет опухоль в мышечную оболочку стенки МП. Морфологический анализ вещества, выявленный с помощью ТУР является важным шагом в определении диагноза РМП.
В основе БЦЖ терапии рака мочевого пузыря лежат длительные наблюдения за пациентами с туберкулезом. Оказалось, что они намного реже остальных страдают подобными новообразованиями. Это период и стал причиной для углубленного исследования эффективности БЦЖ. БЦЖ — вакцина от туберкулеза, которая получила свое название от сокр.: Бацилла Кальметта-Герена (фр. «Bacillus Calmette — Guerin, BCG). При контакте клеток моченакопительного органа с препаратом иммунотерапии (БЦЖ), иммунная система усиливает синтез защитных клеток организма и лучше борется с атипичными клетками. Прибегают к БЦЖ терапии при большой вероятности повторного заболевания.
К удалению МП или цистэктомии прибегают только в крайних случаях, когда ни один другой способ не помог избавиться от патологии. Для подобной операции необходимы тщательная подготовка и диагностика, а также высокий профессионализм специалиста. Но больных чаще интересует не это, а вопрос выживаемости после подобной операции.
Существует несколько видов операций — цистэктомия, при которой удаляют МП. И радикальная цистэктомия, но её используют только в крайних случаях, когда необходимо дополнительно удалить близлежащие органы.
Показания к удалению МП:
- Стадия Т3, в случае поражения жировой капсулы;
- Сморщенный мочеполовой орган;
- Стадия Т4 — наличие образования за пределы МП;
- Множественные злокачественные папилломы.
Противопоказания к цистэктомии:
- Острая форма воспалительных заболеваний мочевой системы;
- Низкая свертываемость крови;
- Люди, которые могут не выдержать продолжительный наркоз.
Подготовка к удалению МП. Больной в обязательном порядке проходит консультацию у анестезиолога, так как операция длится от 3 до 9 часов. Пациент проходит диагностику, которая включает в себя различные процедуры. За неделю-две до хирургического вмешательства больной может пройти курс пробиотиков (препараты с полезными бактериями), чтобы снизить риски инфицирования после операции. С вечера перед операцией нельзя употреблять пищу, жидкости, никотин и т.д. Перед операцией необходимо иметь гладковыбритую паховую область.
Внутрипузырная химиотерапия — метод борьбы с РМП, когда препарат вводят не внутривенно, а в полость мочевыводящего органа для непосредственного контакта с патологическим очагом. Перед проведением такой химиотерапии пациенту запрещена любая жидкость. Побочные эффекты от подобной терапии, такие как рвота, ломкость ногтей, выпадение зубов, волос, нарушение памяти отсутствуют.
Эмболизация при раке мочевого пузыря — это инновационный способ борьбы с отдаленными метастазами, когда нет возможности быстро удалить новообразование.
Прогноз и выживаемость при РМП:
| Стадия | Описание | Лечение | Прогноз | Процент выживаемости |
| 1 | В этой стадии раковые опухоли находятся в поверхностных слоях. | Уменьшить или полностью удалить раковые опухоли с помощью процедуры под названием трансуретральная резекция (ТУР МП). Использование химиотерапии или иммунотерапии. | Быстрое восстановление. | Более 91 % |
| 2 | Клетки рака входят в мышечную стенку мочевого пузыря. | Трансуретральная резекция мочевого пузыря вместе с химиотерапией (реже лучевой терапией). | Быстрое восстановление. | Более 73 % |
| 3 | Раковые клетки распространились на ближайшие органы. | Часто удаляют МП, используют химиотерапию. | После операции рак может вернуться. | 50 % могут прожить более 5 лет. |
| 4 | Метастазы в регионарные и отдаленные лимфоузлы, опухоль неоперабельна. | Удаление рака хирургическим путем невозможно. Используют непроверенные клинические испытания. | Восстановление невозможно. Выход: помочь больному справляться с проявлениями болезни. | Меньше 7 %. |
Рак мочевого пузыря - лечение в Москве
Читайте также:

