Лапатиниб лечение рака молочной железы
Фармакологическое действие
Противоопухолевое средство, обратимый, селективный ингибитор внутриклеточной тирозинкиназы. Связывается с рецепторами эпидермального фактора роста (epidermal growth factor receptor - EGFR/ErbB1 и human epidermal growth factor receptor - HER2+/neu/ЕrbВ2+). Отличается от других быстрообратимых ингибиторов тирозинкиназы более медленной диссоциацией с ErbB1- и ЕrbВ2-рецепторами (период диссоциации 50% лиганда из лиганд-рецепторного комплекса составляет приблизительно 300 мин).
Помимо собственной активности in vitro была показана аддитивная активность лапатиниба и 5-фторурацила (активный метаболит капецитабина) при использовании в комбинации на четырех линиях опухолевых клеток. Ингибирующий эффект оценивался на обработанных трастузумабом клетках. Лапатиниб продемонстрировал значительную активность на линиях иммортализованных опухолевых клеток в средах, содержащих трастузумаб, что показывает отсутствие перекрестной резистентности между двумя лигандами HER2+/neu/ErbB2+.
Согласно результатам исследований лапатиниб является активным лекарственным препаратом, при его назначении в качестве монотерапии пациенткам с метастатическим раком молочной железы. Результаты исследования показали, что сочетанное применение лапатиниба с капецитабином при лечении пациенток с ЕrbВ2-позитивным распространенным раком молочной железы увеличивает время до прогрессирования и достоверно и значимо снижает риск прогрессирования заболевания.
Были выявлены тенденция к улучшению показателя выживаемости, и снижение риска летального исхода.
Фармакокинетика
Абсорбция после приема внутрь неполная и вариабельная. Коэффициент вариабельности AUC составляет примерно от 50 до 100%. Определяется в системном кровотоке в среднем через 0.25 ч (диапазон 0-1.5 ч). С mах достигается примерно через 4 ч после приема лапатиниба.
C ss max при ежедневном приеме в дозе 1250 мг составляет в среднем 2.43 (1.57-3.77) мкг/мл, AUC - 36.2 (23.4-56) мкг × ч/мл.
Биодоступность лапатиниба зависит от приема пищи. Системная экспозиция лапатиниба увеличивается при приеме препарата одновременно с пищей. AUC возрастает в 3 и 4 раза, C max приблизительно в 2.5 и 3 раза выше при приеме с пищей с низким или высоким содержанием жиров, соответственно.
Лапатиниб обладает высокой степенью связывания (более чем 99%) с альбумином и кислым альфа 1 -гликопротеином плазмы крови.
Лапатиниб подвергается интенсивному метаболизму, главным образом с помощью CYP3A4 и CYP3A5, в меньшей степени с CYP2C19 и CYP2C8 с образованием различных окисленных метаболитов.
In vitro лапатиниб в клинически значимых концентрациях ингибирует CYP3Aи CYP2C8. Лапатиниб незначительно ингибирует следующие микросомальные ферменты печени: CYP1A2, CYP2C9, CYP2C19 и CYP2D6.
T 1/2 увеличивается дозозависимо при приеме однократных доз. Равновесное состояние достигается через 6-7 суток приема, T 1/2 в равновесном состоянии составляет 24 ч.
В основном выводится кишечником - в среднем 27% в неизмененном виде, менее 2% принятой дозы выводится почками в неизмененном виде и в виде метаболитов.
Маловероятно влияние нарушения функции почек на фармакокинетику лапатиниба.
Фармакокинетика лапатиниба изучалась при умеренных (7-9 баллов по классификации Чайлд-Пью, n=8) и тяжелых (>9 баллов по классификации Чайлд-Пью, n=4) нарушениях функции печени. AUC лапатиниба после приема однократной дозы 100 мг увеличивается на 56% и 85% соответственно.
Показания активного вещества ЛАПАТИНИБ
Открыть список кодов МКБ-10| Код МКБ-10 | Показание |
| C50 | Злокачественное новообразование молочной железы |
Режим дозирования
Лапатиниб применяют в комбинации с капецитабином.
Рекомедуемая доза лапатиниба составляет 1250 мг 1 раз/сут, ежедневно. Лапатиниб принимают за 1 ч до или через 1 ч после приема пищи.
Пропущенные дозы лапатиниба не восполняются, т.е. принимать пропущенные дозы, уменьшая интервалы между приемами, не следует.
Одновременно применяют капецитабин по специальной схеме.
Лечение лапатинибом должно быть прекращено в случае появления симптомов снижения фракции выброса левого желудочка до 3 степени или больше (по классификации нежелательных явлений Национального Онкологического Института), или в случае снижения ниже границы допустимой нормы. Лечение лапатинибом может быть возобновлено не ранее чем через 2 недели в меньшей дозе (1000 мг/сут) и только если уровень фракции выброса левого желудочка находится в допустимых границах нормы.
Лечение лапатинибом должно быть прекращено в случае появления легочных симптомов свидетельствующих о развитии интерстициального легочного процесса/пневмонита 3 степени или больше (по классификации нежелательных явлений Национального Онкологического Института).
Решение о прекращении применения или изменении дозы лапатиниба может быть принято, когда уровень развивающихся токсических эффектов соответствует 2 степени и более по классификации нежелательных явлений Национального Онкологического Института. При снижении уровня токсических эффектов снизился до 1 степени и менее лечение может быть возобновлено в дозе 1250 мг/сут. В случае повторного возникновения токсических эффектов дозу лапатиниба следует уменьшить до 1000 мг/сут.
Побочное действие
Со стороны пищеварительной системы: очень часто - анорексия, диарея (которая может приводить к дегидратации), тошнота, рвота; иногда - гипербилирубинемия, повышение уровня АЛТ, АСТ, ЩФ.
Со стороны сердечно-сосудистой системы: часто - снижение фракции выброса левого желудочка (90% - симптоматическое). Разрешалось спонтанно у 60% пациентов после отмены препарата. Симптоматическое снижение фракции выброса левого желудочка наблюдалось у 0.1% пациентов (диспноэ, сердечную недостаточность, ощущение сердцебиения).
Со стороны дыхательной системы: иногда - интерстициальный легочный процесс/пневмонит.
Дерматологические реакции: очень часто - сыпь (включая акне).
Со стороны организма в целом: очень часто - слабость.
Лапатиниб в комбинации с капецитабином
Со стороны пищеварительной системы: очень часто - диспепсия.
Дерматологические реакции: очень часто - сухость кожи.
Наблюдавшиеся с одинаковой частотой в группе лапатиниб + капецитабин и в группе капецитабина
Со стороны пищеварительной системы: очень часто - стоматит, запор, боли в абдоминальной области, гипербилирубинемия.
Дерматологические реакции: очень часто - ладонно-подошвенная эритродизестезия.
Со стороны организма в целом: очень часто - мукозит.
Со стороны костно-мышечной системы: очень часто - боли в спине и конечностях.
Со стороны ЦНС: очень часто - бессонница; часто - головная боль.
Противопоказания к применению
Беременность, период лактации (грудного вскармливания), повышенная чувствительность к лапатинибу.
Применение при беременности и кормлении грудью
Применение при нарушениях функции печени
С осторожностью следует применять при нарушениях функции печени умеренной или тяжелой степени (7 и более баллов по шкале Чайлд-Пью).
У пациентов с нарушениями функции печени недостаточно данных для формирования конкретных рекомендаций по коррекции режима дозирования.
Применение при нарушениях функции почек
Пациентам с нарушениями функции почек не требуется коррекции режима дозирования.
Применение у детей
Опыта применения препарата у детей нет
Применение у пожилых пациентов
Не отмечено различий в эффективности, переносимости и безопасности лапатиниба в зависимости от возраста (пожилые пациенты).
Особые указания
Лечение лапатинибом следует проводить только под контролем специалиста, имеющего опыт проведения химиотерапии.
С осторожностью следует применять при состояниях, которые могут приводить к левожелудочковой недостаточности, нарушениях функции печени умеренной или тяжелой степени (7 и более баллов по шкале Чайлд-Пью).
Следует учитывать информацию о имеющихся противопоказаниях и безопасности применения капецитабина при сочетанном применении с лапатинибом.
Перед началом лечения необходимо оценить уровень фракции выброса левого желудочка. Во время лечения следует контролировать уровень фракции выброса левого желудочка, чтобы не допустить снижения данного показателя ниже допустимых значений. Лечение лапатинибом следует прекратить в случае снижения фракции выброса до 3 степени или более, или в случае снижения ниже границы допустимой нормы. Лечение лапатинибом может быть возобновлено не ранее чем через 2 недели в меньшей дозе (1000 мг/сут и только если уровень фракции выброса левого желудочка находится в допустимых границах нормы). Постоянное снижение фракции выброса левого желудочка в течение 9 недель лечения, как правило, ограничивает длительность проводимой терапии.
В период лечения пациенты должны находиться под наблюдением для выявления легочных симптомов, свидетельствующих о развитии интерстициального легочного процесса/пневмонита.
При первых симптомах диареи рекомендуется назначение противодиарейных препаратов. При диарее тяжелой степени может потребоваться назначение электролитов и жидкости для предупреждения дегидратации (внутрь или в/в), приостановление приема лапатиниба или его отмена.
До начала лечения, затем ежемесячно, либо по клиническим показаниям следует контролировать показатели функции печени (активность трансаминаз, ЩФ, содержание билирубина). При тяжелом нарушении функции печени лечение лапатинибом следует прекратить, повторное лечение не проводят. Известны случаи гепатотоксичности при назначении ингибиторов тирозинкиназы. У пациентов с нарушениями функции печени недостаточно данных для формирования конкретных рекомендаций по коррекции режима дозирования.
Использование в педиатрии
Опыта применения препарата у детей нет.
Влияние на способность к вождению автотранспорта и управлению механизмами
Механизм действия лапатиниба позволяет предположить отсутствие влияния на способности к концентрации внимания. Тем не менее, следует учитывать общее клиническое состояние пациента и возможное развитие нежелательных явлений при оценке способностей к управлению автомобилем и работе с механизмами, требующих быстроты реакции.
Лекарственное взаимодействие
Ингибиторы или индукторы CYP3A могут влиять на фармакокинетику лапатиниба. При одновременном применении лапатиниба и известных ингибиторов CYP3A (например, кетоконазол, итраконазол, грейпфрутовый сок) необходимо соблюдать осторожность и тщательно наблюдать за клиническим состоянием пациента и возможными нежелательными реакциями. При необходимости одновременного назначения пациенту сильного ингибитора CYP3A4 необходимо уменьшить дозу лапатиниба до 500 мг/сут, рассчитанной так, чтобы скорректировать AUC лапатиниба до величины, соответствующей применению лапатиниба без ингибиторов. Однако, в настоящее время нет клинических данных о применении лапатиниба при такой коррекции дозы у пациентов, получающих мощный ингибитор CYP3A4. После отмены сильного ингибитора, только после выведения его из организма, спустя приблизительно 1 неделю следует вновь увеличивать дозу лапатиниба до рекомендованной.
При одновременном применении лапатиниба и известных индукторов CYP3A4 (например, рифампицин, карбамазепин, фенитоин) и необходимо соблюдать осторожность и тщательно наблюдать за клиническим состоянием пациента и возможными нежелательными реакциями.
При необходимости одновременного назначения пациенту сильного индуктора CYP3A4 дозу лапатиниба следует подбирать основываясь на переносимости, постепенно повышая ее с 1250 мг/сут до 4500 мг/сут. Эта доза рассчитывается так, чтобы скорректировать AUC лапатиниба до величины, соответствующей применению лапатиниба без индукторов. Однако в настоящее время нет клинических данных о применении лапатиниба у пациентов, получающих сильный индуктор CYP3A4. После отмены сильного индуктора, только спустя приблизительно 2 недели следует вновь уменьшить дозу лапатиниба до рекомендованной.
Лапатиниб ингибирует in vitro CYP3A4 и CYP2C8 в клинически значимых концентрациях. Необходима осторожность при одновременном назначении лапатиниба и препаратов с узким терапевтическим диапазоном, являющихся субстратами этих ферментов. Лапатиниб является субстратом для транспортных белков гликопротеин P и BCRP. Ингибиторы и индукторы данных белков могут изменять действие и/или распределение лапатиниба.
Не исключено, что лапатиниб может влиять на фармакокинетику субстратов гликопротеина P (например, дигоксина), BCRP (например, топотекана) и ОАТР1В1 (например, розувастатина).











Лапатиниб при раке молочной железы
Лапатиниб – новый противоопухолевый препарат, двойной ингибитор тирозинкиназных рецепторов HER1/HER2. В настоящее время широко применяется в комбинации с капецитабином при распространенном и/или метастазирующем РМЖ с гиперэкспрессией HER2 рецепторов больных, ранее получавших терапию трастузумабом, при развитии резистентности к последнему. Продолжаются интенсивные исследования по оценке эффективности лапатиниба в сочетании с различными цитостатиками, препаратами эндокринотерапии, а также с другими таргетными агентами. Изучается возможность применения лапатиниба в качестве адъювантной и неодъювантной терапии.
Создание и внедрение в клиническую практику противоопухолевых препаратов нового поколения, к числу которых относится и низкомолекулярный ингибитор тирозинкиназных рецепторов эпидермального фактора роста ErbB1/EbB2 лапатиниб, стали возможными благодаря более глубокому пониманию биологии опухоли.
Тирозинкиназные рецепторы эпидермального фактора роста (Human Epidermal Growth Factor Receptors – HER/ErbB) располагаются на мембранах клеток нормальных тканей и опухолей, они регулируют постоянную активацию сигнальных путей, что стимулирует опухолевые клетки к митозу. Количество HER-рецепторов в опухолевых клетках больше, чем в нормальных тканях.
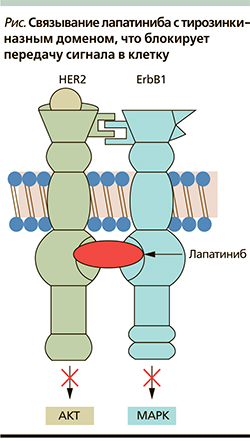
Семейство рецепторов эпидермального фактора роста состоит из четырех тирозинкиназных рецепторов: EGFR/HER1/ErbB1, HER2/ErbB2, HER3/ErbB3, HER4/ErbB4 [1, 2]. Для ряда опухолей, в т.ч. рака молочной железы (РМЖ), характерно увеличение числа копий генов (амплификация) и/или повышение уровней мРНК и белковых продуктов генов-рецепторов (гиперэкспрессия). Гиперэкспрессия ErbB2/HER2 при РМЖ встречается, по разным данным, в 10–37 % случаев [3, 4]. Тирозинкиназный рецептор состоит из внеклеточного лигандсвязывающего домена, трансмембранного домена и внутриклеточного каталитического или белкового тирозинкиназного домена [1, 5]. При связывании лиганда (фактора роста) с внеклеточным доменом происходит димеризация рецептора, т.е. объединение двух связанных с лигандом рецепторов в единый функциональный комплекс. В процессе димеризации образуются гомо- и гетеродимеры. После димеризации рецептора происходит активация внутриклеточного домена и аутофосфорилирование тирозинкиназы. Этот процесс инициирует сигнальные каскады с участием MAPK–ERK1/2 и PI3K/AKT и трансдукцию сигнала внутрь клетки [1, 6]. HER2, существующий в закрытой форме, не связывается с лигандом, но является предпочтительным партнером в формировании димера для других HER-рецепторов [7]. Коэкспрессия HER1 и HER2 обратно коррелирует со статусом рецепторов эстрогенов в опухоли, а гетеродимеры HER1/2 увеличивают метастатический потенциал клеточных линий РМЖ [9]. Поэтому возникло представление, будто двойное ингибирование обоих рецепторов может быть более эффективным, чем ингибирование каждого в отдельности [10].
Лапатиниб – двойной ингибитор тирозинкиназных рецепторов HER1/HER2. Он блокирует активацию рецептора и таким образом прерывает передачу сигнала внутрь клетки (см. рисунок). Предотвращение активации обоих рецепторов дает возможность эффективного применения препарата при HER2(+)-опухолях, резистентных к трастузумабу (Герцептину). In vitro была продемонстрирована аддитивная активность лапатиниба и фторурацила (активный метаболит капецитабина) при использовании в комбинации на четырех линиях опухолевых клеток. Ингибирующий эффект оценивался на обработанных трастузумабом клетках. Исследования I фазы показали, что лапатиниб в монорежиме характеризуется хорошей переносимостью и обладает противоопухолевой активностью при различных HER2+-солидных опухолях, в т.ч. при РМЖ [6, 11].
Лапатиниб – новый противоопухолевый препарат, активный при HER2-позитивном РМЖ, удобный в применении (пероральный прием) и относительно удовлетворительно переносимый, вызвал к себе значительный интерес. Первое клиническое исследование лапатиниба в сочетании с капецитабином на больных местнораспространенным и метастазирующим РМЖ, ранее получавших антрациклины, таксаны и трастузумаб, подтвердило противоопухолевую активность комбинации по сравнению с монотерапией капецитабином.
В рандомизированном исследовании III фазы EGF 100 151 больной распространенным HER2-позитивным РМЖ при прогрессировании после химиотерапии, включившей антрациклины, таксаны и трастузумаб, назначили капецитабин 2500 мг/м2/сут 1–14-й дни (201 пациентка) или капецитабин 2000 мг/м2/сут 1–14-й дни в комбинации с лапатинибом 1250 мг/сут (198 пациенток).
В группе больных, получавших комбинацию препаратов, медиана времени до прогрессирования (ВДП) составила 26,7 недели против 20,7 – в группе пациентов, получавших капецитабин в режиме монотерапии (отношение рисков [ОР] – 0,54; 95 % доверительный интервал [ДИ] – 0,28–1,03; p = 0,046). Медиана общей выживаемости составила 75 недель при комбинации препаратов и 64,7 – при монотерапии (ОР – 0,87; 95 % ДИ – 0,71–1,08; p = 0,21) [14, 15].
Таким образом, комбинация лапатиниба с капецитабином продемонстрировала значительный выигрыш в отношении медианы ВДП у больных метастатическим HER2-позитивным РМЖ по сравнению с капецитабином в монорежиме при удовлетворительной переносимости.
В другом исследовании сравнили эффективность паклитаксела и паклитаксела с лапатинибом для 579 больных метастазирующим РМЖ. Значительного различия в медиане ВДП среди HER2-негативных пациентов не отмечено. Лечение лапатинибом и паклитакселом 86 пациентов с HER2-позитивным РМЖ (15 %) привело к статистически значимому увеличению ВДП, частоты объективного эффекта и безрецидивной выживаемости [16, 17].
Однако в сравнительном рандомизированном исследовании COMPLETE [12] показано, что по противоопухолевой активности лапатиниб уступает трастузумабу. В нем 636 больных метастатическим HER2+ РМЖ получали в качестве 1-й линии лечения комбинацию лапатиниба или трастузумаба с таксанами (паклитаксел, доцетаксел). Безрецидивная выживаемость в группе больных, получавших лапатиниб, составила 8,8 месяца, в группе трастузумаба – 11,4. По общей выживаемости различий между группами не было.
В исследовании CEREBEL [13] сравнивали эффективность комбинаций капецитабина с трастузумабом и лапатинибом в отношении 475 больных HER2+-РМЖ с метастазами в ЦНС. Предшествующая терапия включала антрациклины или таксаны. Безрецидивная выживаемость в группе больных, получавших лапатиниб, составила 6,6 месяца, в группе получавших трастузумаб – 8. Медиана общей выживаемости также была ниже в группе лапатиниба: 22,4 против 27,3 месяца.
Таким образом, на основе представленных данных лапатиниб используется прежде всего больными HER2+-РМЖ, ранее получавшими трастузумаб и ставшими резистентными к нему.
Препарат продемонстрировал обнадеживающую активность в отношении метастазов в головной мозг. Результатом II фазы клинических исследований применения лапатиниба 39 больными HER2-позитивным РМЖ с метастазами в головной мозг стало достижение 1 частичной ремиссии (частота ответов – 3 %).
У 7 пациентов обеих групп с поражением и без поражения ЦНС медиана ВДП составила 16 недель. Данные об уровне безрецидивной выживаемости были оценены по критериям RECIST. Кроме того, в настоящее время изучаются возможности применения лапатиниба в комбинации с ингибиторами ароматазы и уже имеются данные о его эффективности в комбинации с летрозолом [17].
В исследовании ALTTO (Adjuvant Lapatinib and/or Trastuzumab Treatment Optimization) сравнивали 4 режима лечения: 1 год использовали трастузумаб, 1 год – лапатиниб, комбинация двух препаратов – в течение года, 3 месяца – трастузумаб с последующим 6-недельным перерывом и 7,5 месяцев – лапатиниб. В исследование включен 8381 пациент из 50 стран 6 континентов. Большинство женщин (4613) получали трастузумаб и/или лапатиниб после химиотерапии, остальные получали трастузумаб и/или лапатиниб одновременно или последовательно с химиотерапией. Медиана наблюдения составила 4,5 года. Комбинация лапатиниба с трастузумабом в качестве адъювантного лечения ранних стадий HER2+ РМЖ не показала статистически значимого преимущества в отдаленных результатах лечения [18, 31].
CALGB 40601 (Alliance) – рандомизированное исследование неоадъювантной химиотерапии III фазы с использованием паклитаксела и трастузумаба в еженедельном режиме с лапатинибом или без него. В исследование были включены 305 больных РМЖ. Пациенты получали паклитаксел (80 мг/м2/нед в/в) + трастузумаб (4 мг/кг далее 2 мг/кг/нед в/в) ± лапатиниб (750 мг/сут внутрь) в течение 16 недель перед оперативным лечением. В третьей группе больные получали паклитаксел с лапатинибом (1500 мг/сут). Эта группа вскоре была закрыта на основании отрицательных данных об эффективности и токсичности, полученных из предварительного исследования ALTTO. Частота полного патоморфологического эффекта при лечении паклитакселом, трастузумабом, лапатинибом составила 51 % (42–60 %), паклитакселом и трастузумабом – 40 % (32–49 %), паклитакселом и лапатинибом – 32 % (22–44 %); различия статистически недостоверны (p = 0,11) [19, 20].
В рандомизированном многоцентровом исследовании (NCT01013740) II фазы оценивались эффективность и токсичность комбинации лапатиниба с винорелбином или капецитабином в качестве первой и второй линий химиотерапии метастазирующего РМЖ с гиперэкспрессией HER2 [21].
В первую группу были включены 75 больных, во вторую – 37 (всего 112). Пациенты первой группы получали лапатиниб 1250 мг внутрь ежедневно + винорелбин 20 мг/м2 в/в 1-й, 8-й дни каждые 3 недели. Во второй группе назначали лапатиниб 1250 мг внутрь ежедневно + капецитабин 2000 мг/м2/сут внутрь в 2 приема с 12-часовым интервалом в 1–14-й дни каждые 3 недели. Медиана общей выживаемости в группе лапатиниба и винорелбина составила 24,3 месяца (95 % ДИ – 16,4–26,5), в группе лапатиниба и капецитабина – 19,4 (95 % ДИ – 16,4–27,2). Сорок два пациента при прогрессировании опухолевого процесса получали перекрестный режим, из них 29 – лапатиниб с капецитабином, 13 – лапатиниб с винорелбином. Медиана ВДП после перекреста составила 4 месяца (95 % ДИ – 2,1–5,8) при лечении лапатинибом и капецитабином и 3,2 месяца (95 % ДИ – 1,7–5,1) лапатинибом и винорелбином. Анализ выживаемости без прогрессирования и токсичности показал, что эти два режима сопоставимы.
Еще в одном рандомизированном многоцентровом исследовании (LPT111110; NCT00709618) II фазы оценивались эффективность и токсичность комбинации лапатиниба с винорелбином в качестве первой и второй линий химиотерапии метастазирующего РМЖ с гиперэкспрессией HER2 [22]. Больные получали лапатиниб 1500 мг внутрь ежедневно + винорелбин 20 мг/м2 в/в 1-й, 8, 15-й дни каждые 4 недели до прогрессирования или исключения из протокола. Оценивались частота объективного эффекта, безрецидивная выживаемость, общая выживаемость, время до достижения эффекта, продолжительность эффекта. В исследование были включены 44 больных. Частота объективного эффекта составила 41 % (95 % ДИ – 26,4–55,4; 4 – полных, 14 – частичных эффектов). Медиана безрецидивной выживаемости, составили 24,1 (95 % ДИ 16,9–36,7), медиана времени до достижения эффекта – 7,5 (95 % ДИ 7,1–8,1) и медиана продолжительности эффекта – 32,0 (95 % ДИ 18,0–42,3) недели соответственно.
В исследовании неоадъювантной терапии GeparQuinto частота патоморфологического эффекта при использовании стандартной антрациклин/таксан-содержащей химиотерапии в комбинации с лапатинибом была значительно ниже по сравнению с группой больных, получавших химиотерапию в сочетании с трастузумабом (22,7 против 30,3 %; р = 0,04) [23].
Для больных метастазирующим РМЖ в исследовании MA.31 лапа-тиниб в комбинации с таксанами оказался менее эффективным по сравнению с трастузумабом в комбинации с таксанами по ВДП (8,8 против 11,4 месяца; р = 0,01). По токсич-ности комбинация лапатиниба с таксанами оказалась выше за счет диареи [12].
В настоящее время известно, что лапатиниб не оказывает выраженного кардиотоксического действия.
В рандомизированном исследовании LETLOB II фазы оценивалась эффективность летрозола или летрозола и лапатиниба для пациенток в постменопаузе с гормонально-чувствительным HER2-негативным операбельным РМЖ. Побочные эффекты включали диарею, сыпь, общую слабость. Побочные эффекты III–IV степеней встречались редко [25]. Лапатиниб характеризуется потенциально низкой кардиотоксичностью по сравнению с трастузумабом и активирует аденозинмонофосфаткиназу, ключевой регулятор энергетического обмена и защиты клеток от ишемии [26]. Среди 2812 больных, получавших лапатиниб, только у 1,3 % наблюдалось снижение фракции выброса левого желудочка, которое имело обратимый характер приблизительно для половины пациентов [27].
В настоящее время продолжаются интенсивные исследования по оценке эффективности лапатиниба в сочетании с различными цитотоксиками, препаратами эндокринотерапии, а также с другими таргетными агентами. Изучается возможность применения лапатиниба в качестве адъювантной и неодъювантной терапии.
Международное многоцентровое исследование NeoALLTO показало возможность успешного сочетания лапатиниба и трастузумаба с паклитакселом. Больных инвазивным операбельным (Т > 2 см) HER2-позитивным РМЖ рандомизировали в 3 группы: 1) лапатиниб + паклитаксел, 2) трастузумаб + паклитаксел, 3) лапатиниб + трастузумаб + паклитаксел. После неоадъювантной терапии проведено оперативное лечение, затем 3 курса адъювантной химиотерапия по схеме FEC, далее назначалась терапия лапатинибом в первой группе, трастузумабом во второй и обоими препаратами в третьей группах. Суммарное время использования анти-HER-2-терапии составило 52 недели. Частота полного патоморфологического эффекта оказалась значительно выше в группе лапатиниба и трастузумаба – 51,3 %, тогда как в группе с лапатинибом она была 24 %, а в группе с трастузумабом – 29,5 %.
В клиническом исследовании IIb-фазы CHERLOB пациенты с HER2-позитивным первичным РМЖ (стадии II–IIIА) рандомизировались в группы, получавшие неоадъювантную химиотерапию с трастузумабом, лапатинибом или с обоими препаратами. Целью исследования стало достижение полного регресса опухоли. Результаты данного исследования показали преимущество сочетания лапатиниба и трастузумаба с химиотерапией по сравнению с использованием химиотерапии с трастузумабом или лапатинибом, подтвердив таким образом преимущество двойной ингибиции HER2 [29]
На основе представленных выше данных были разработаны следующие рекомендации по применению лапатиниба.
Лапатиниб показан: 1) при распространенном и/или метастазирующем РМЖ с гиперэкспрессией ErbB2+ (HER2+)-рецепторов в комбинации с капецитабином больным, ранее получавшим терапию с трастузумабом; 2) при распространенном гормонозависимом HER2-положительном РМЖ в сочетании с ингибиторами ароматазы.
Перед началом лечения необходимо оценить уровень фракции выброса левого желудочка, который следует контролировать во время терапии, чтобы не допустить снижения данного показателя ниже допустимых значений. Лечение лапатинибом следует прекратить в случае снижения фракции выброса до ≥ 3-й степени. Лече-ние лапатинибом может быть возобновлено не ранее чем через 2 недели в меньшей дозе (1000 мг/сут) и только если уровень фракции выброса левого желудочка находится в допустимых границах нормы. Постоянное снижение фракции выброса левого желудочка в течение 9 недель лечения, как правило, ограничивает длительность проводимой терапии [29].
Лечение лапатинибом должно быть прекращено и в случае появления легочных симптомов, свидетельствующих о развитии интерстициального легочного процесса/пневмонита ≥ 3-й степени (по классификации нежелательных явлений Национального онкологического института). Решение о прекращении применения или изменении дозы лапатиниба может быть принято, когда уровень развивающихся токсических эффектов соответствует ≥ 2-й степени по классификации нежелательных явлений Национального онкологического института. При снижении уровня токсических эффектов до 1-й степени и менее лечение может быть возобновлено в дозе 1250 мг/сут. В случае повторного возникновения токсических эффектов дозу лапатиниба сле-дует уменьшить до 1000 мг/сут.
Читайте также:

