Консервативное лечение при раке поджелудочной железы
Рак поджелудочной железы — агрессивная патология, входящая в десятку наиболее часто встречающихся онкологических болезней в мире. Согласно данным статистики, данное злокачественное новообразование в большинстве случаев поражает пожилых мужчин и характеризуется неблагоприятным прогнозом. Лечение рака поджелудочной проводится разными способами, выбор зависит от стадии болезни, наличия метастазов, возраста пациента, локализации и гистологического типа опухоли.
Показания к хирургическому лечению
Оперативное вмешательство, выполненное на ранних стадиях рака поджелудочной железы, является одним из наиболее действенных методов лечения и способно продлить жизнь пациента. Врач-онколог, после проведения тщательного обследования, назначает специализированное лечение с учетом результатов всех анализов, данных дополнительных исследований и общего состояния больного.

Решение о хирургическом лечении должно основываться на оценке операбельности больного и резектабельности новообразования поджелудочной. Под резектабельностью понимают возможность полного удаления органа и его пораженной части. Понятие операбельность включает в себя саму возможность проведения хирургического вмешательства данному больному.
При раке данной локализации операции по удалению новообразования проводятся преимущественно на начальных стадиях, когда отсутствуют отдаленные метастазы. Оценка резектабельности новообразования выполняется согласно данным компьютерной томографии.
При этом опухоль может быть:
- Резектабельной — отсутствует поражение брыжеечной и воротной вен, жировая клетчатка вокруг крупных магистральных артерий не вовлечена в опухолевый процесс.
- Сомнительно резектабельной — при вовлечении в онкологический процесс воротной или брыжеечной вены, поражение желудочно-двенадцатиперстной артерии может быть до 2 см (с возможностью ее восстановления).
- Нерезектабельной — тромбоз вен, поражение печеночной артерии, чревного ствола, невозможность полного удаления опухоли и выполнения сосудистой пластики.
При изначально резектабельной опухоли, операция проводится без предварительной подготовки. При сомнительных показаниях пациентам может быть назначен курс неоадъювантной лучевой или химиотерапии, с целью уменьшения массы опухолевых клеток. При изначально нерезектабельной опухоли, проводится курс консервативного лечения с дальнейшей диагностикой динамики процесса и повторным определением резектабельности.

В ходе операции, помимо пораженной части поджелудочной, резекции подлежат соседние органы, сосуды и лимфоузлы, вовлеченные в опухолевый процесс.
Оперативное лечение рака головки поджелудочной железы
Хирургическое лечение показано всем пациентам с резектабельной опухолью на 1–2 стадии развития заболевания. В некоторых случаях перед началом вмешательства может быть проведена диагностическая лапароскопия, с целью уточнения локализации и распространенности неопластического процесса. При этом через надрез небольшого размера (на передней брюшной стенке), вводится лапароскоп, с его помощью на экране компьютера врач получает изображение исследуемых органов. Если обнаружены метастазы, ранее не выявленные во время проведения КТ, операцию не проводят.
В случае если отсутствуют противопоказания, пациентам проводится операция. Чаще всего новообразования поджелудочной, локализуются в ее головке. При данном варианте расположения новообразования выполняется операция Уиппла, при ее проведении подлежат удалению:
- часть железы, которая поражена раком;
- дуоденум;
- часть желудка;
- верхняя часть тонкого кишечника;
- желчный пузырь и проток;
- ближайшие к новообразованию лимфоузлы.
Опухоли поджелудочной склонны к быстрому агрессивному прорастанию в ближайшие органы и сосуды. Именно поэтому, с учетом распространенности процесса, существует множество вариаций операции Уиппла. При поражении крупных сосудов производится их резекция с последующей ангиопластикой.
Наиболее важным этапом операции при раке поджелудочной железы является реконструкция. Она направлена на восстановление пищеварительной функции органов ЖКТ. В таком случае кишечник сшивают с сохранившейся частью поджелудочной и желудком.
Длительность вмешательства составляет в среднем 4–8 часов, после чего больной переводится в отделение реанимации или интенсивной терапии. В течение нескольких дней после проведенного лечения, пациент получает внутривенное питание, затем его переводят на специальное диетическое питание. В рамках послеоперационного периода, больному назначаются обезболивающие препараты и антибактериальные средства.

Важно! На начальных стадиях новообразований головки поджелудочной железы, врачи стараются сохранить пилорический отдел желудка в ходе операции Уиппла. Это позволяет ускорить процесс выздоровления и быстрее восстановить функции пищеварительного тракта.
Хирургическое лечение поражений других частей железы
В случае если диагностирован рак хвостовой части железы, выполняется дистальная панкреатоэктомия. При данной операции удалению подлежит хвост поджелудочной, селезенка, окружающая жировая клетчатка и лимфоузлы.
При обнаружении нескольких опухолей в разных частях поджелудочной, выполняется тотальная панкреатэктомия — полностью удаляется пораженная поджелудочная, части желудка и кишечника, селезенка, желчный, сосуды и лимфатические узлы, расположенные рядом с этими органами. Полное иссечение пораженного раком органа, в несколько раз снижает вероятность возникновения отдаленных метастазов.
При выполнении тотальной панкреатэктомии, важно помнишь о последствиях данной операции. Наиболее значимым недостатком является развитие сахарного диабета, трудно поддающегося коррекции, с приступами дневной и ночной гипогликемии.

Важно! Наиболее точным исследованием, помогающим определить распространенность онкологического процесса, является позитронно-эмиссионная томография. Данная процедура проводится как при первичной диагностике, так и после проведенного лечения с целью оценки его эффективности.
Консервативное лечение
Химиотерапия входит в состав комплексного лечения рака поджелудочной железы на любой его стадии. Введение цитостатических препаратов показано больным в следующих ситуациях:
- До хирургического вмешательство (неоадъювантная химиотерапия) — с ее помощью можно уменьшить объемы новообразования, достичь хорошей резектабельности.
- После операции с целью уничтожения оставшихся раковых клеток и профилактики рецидива.
- При распространенном раке в комбинации с облучением, иммунотерапией и гормональным лечением.
- В качестве паллиативного лечения на 4 стадии, при наличии множественных отдаленных метастазов.
Курсы химиотерапии проводятся циклами, препараты вводятся внутривенно или принимаются внутрь в таблетированной форме. Лечение может выполняться как в условиях дневного стационара, так и требовать госпитализации. Наиболее распространенными средствами, применяемыми для лечения рака поджелудочной, являются Гемзар, Таксотер, Пактитаксел, Цисплатин и Фторурацил. Применяться препараты могут как по отдельности, так и в составе полихимиотерапии.
Важно! Наиболее эффективной комбинацией, используемой для лечения новообразований поджелудочной, признано сочетание Гемзара и Фторурацила. Данная схема вызвала значительное уменьшение объема новообразований поджелудочной у 20% пациентов.
Таргетная и иммунотерапия
Одним из современных эффективных методов лечения онкологических болезней является тагретная терапия. В отличие от химии, которая помимо опухоли оказывает действие на другие быстроделящиеся клетки человеческого организма и вызывает массу побочных эффектов, таргетные препараты действуют избирательно, поражая только злокачественно перерожденные ткани. С целью лечения рака поджелудочной железы используется средство Эрлотиниб (Тарцева).
Еще одним методом лечения, используемым в современной онкологии, является применение иммунопрепаратов. Данные средства имеют биологическое происхождение, не токсичные, избирательно поражают только раковые клетки, также как собственные иммунные клетки организма поражают чужеродные, защищая его от вирусов и бактерий.
По механизму воздействия на опухоль различают:
- противораковые вакцины, с антигеном определенной опухоли;
- неспецифические иммуномодуляторы, повышающие иммунитет в целом;
- моноклональные антитела.
Иммунные препараты практически не обладают побочными эффектами. При их применении изредка могут возникнуть такие неспецифические явления как повышение температуры тела или признаки аллергической реакции при индивидуальной непереносимости компонентов лекарства.
Важно! Иммунотерапия является одним из самых молодых методов лечения онкопатологий. Для лучшего достижения результата и продления жизни пациентов она используется в комбинации с облучением и химиотерапией.
Радиологическое лечение
Самым распространенным способом, применяемым специалистами при новообразованиях панкреатодуоденальной зоны, является наружное облучение. В течение нескольких недель или месяцев, пациенту проводятся сеансы небольших доз облучения на пораженную область.

Радиологическая терапия проводится при:
- местно-распространенном раке до и после проведения оперативного вмешательства;
- с целью уменьшения болей при наличии метастазов;
- в составе комплексного лечения для профилактики рецидива новообразований.
Современные методики диагностики и компьютерного моделирования трехмерных изображений исследуемой области, позволяют воздействовать на новообразования с высокой точностью, не затрагивая при этом здоровые ткани. Это резко снижает вероятность появления нежелательных эффектов при данном виде лечения.
Важно! Лечение при раке поджелудочной железы должно быть своевременным и комплексным. Только сочетание нескольких методов (операции, таргетной и химиотерапии, облучения) позволяет достичь хороших результатов, продлить и улучшить качество жизни пациентов.
Подробнее о данном заболевании смотрите в видео ниже.
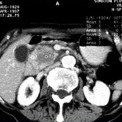
Лечение рака поджелудочной железы в полном объёме, включающем радикальную операцию и химио- или химиолучевую терапию, далеко не всегда осуществимо: на момент установления диагноза радикальная операция возможна только у 10-20% больных, а 25% из этого числа не смогут пройти химиотерапию в связи с неудовлетворительным общим состоянием после оперативного вмешательства.
Радикальная операция подразумевает полное удаление первичной опухоли и ряда регионарных лимфоузлов, которые могут быть поражены микроскопическими метастазами.
Раковые опухоли бывают резектабельными (если имеется техническая возможность выполнения радикальной операции) и нерезектабельными (если такой возможности нет).
Возможность выполнения радикальной операции по поводу аденокарциномы поджелудочной железы оценивается согласно критериям разработанных для этого шкал резектабельности и зависит от того, насколько вовлечены в патологический процесс магистральные сосуды – чревный ствол, общая печёночная артерия, верхняя брыжеечная вена с ветвями, портальная вена.
Причины столь низкой доли резектабельных опухолей:
- значительные трудности с ранней диагностикой;
- близкое соседство опухоли с крупными сосудами.
Ранняя диагностика рака поджелудочной железы затруднена ввиду того, что ранние симптомы (ощущение боли или дискомфорта в верхней части живота) характерны для массы других заболеваний, а надёжных тесты для выявления ранних стадий этой опухоли на сегодняшний день отсутствуют.
Кроме того, больной может быть неоперабельным по другим причинам, например, ввиду выраженного нарушения функций жизненно важных органов - как развившихся в связи с ростом опухоли, так и безотносительно к ней.
- радикальные хирургические вмешательства;
- нерадикальные вмешательства, направленные на поддержание важных функций;
- химио- или химиолучевую терапию;
- паллиативную помощь.
Однако даже радикальная операция в комбинации с химио- и лучевым лечением часто не способны отложить прогрессирование болезни на длительное время. Основная причина этого – раннее, ещё на стадии формирования, метастазирование опухоли. Микрометастазы в отдалённых органах невозможно выявить во время обследования, вследствие чего при установлении диагноза стадия бывает зачастую снижена. Соответственно, даже радикальное удаление первичной опухоли практически не влияет на неблагоприятный исход, а химиотерапия лишь замедляет рост метастазов. Печальная статистика – лишь 10-20% пациентов после радикальной операции живут пять и более лет.
Жёлчеотведение
Опухолевое поражение поджелудочной железы часто сопровождается обструкцией (нарушением проходимости) жёлчных путей, симптомы которой нарастают по мере роста опухоли и степени сдавления ею жёлчных протоков. Обструкция жёлчных путей – осложнение, характерное для локализации опухоли в головке поджелудочной железы.
Обструкция жёлчных путей сопровождается:
Зуд, желтуха и изменение цвета физиологических отправлений являются следствием холестаза (частичного или полного прекращения оттока жёлчи в кишечник) и поступления в кровь билирубина. Прямой билирубин – продукт естественного распада эритроцитов – в норме перерабатывается печенью, а затем поступает с жёлчью в желудочно-кишечный тракт, откуда выводится с калом и мочой. При обструкции жёлчевыводящих путей билирубин начинает накапливаться в крови.
Операция жёлчеотведения (декомпрессия жёлчных путей) применяется:
- для стабилизации больного перед радикальной операцией по поводу рака поджелудочной железы;
- для облегчения страданий больных на поздних стадиях, когда радикальное лечение невозможно.
Предоперационная декомпрессия назначается больным с обструкцией жёлчевыводящих путей, у которых опухоль признана резектабельной, однако откладывается из-за сопутствующего холестазу холангита (воспаления жёлчных путей), обменных нарушений, связанных с расстройством пищеварения (в котором жёлчь принимает непосредственное участие). Обычно предоперационная декомпрессия назначается при повышении билирубина в крови более 200 мкг/л.
В такой ситуации радикальная операция без предварительного жёлчеотведения чревата значительным повышением вероятности осложнений. Так, длительный холестаз (в течение месяца и более) может привести к кровотечению из стенок жёлчных протоков во время или после операции. В случае послеоперационных осложнений возникает необходимость откладывать химиотерапию, раннее начало которой улучшает прогноз.
Жёлчеотведение необходимо и лицам, которым перед операцией назначена химиотерапия или необходимо проведение дополнительных исследований.
В случае невозможности проведения радикальной операции (поздняя стадия рака, сердечно-сосудистая недостаточность и другие факторы, снижающие благоприятный исход операции), жёлчеотведение показано для улучшения качества жизни пациента.
Декомпрессия жёлчных путей осуществляется следующими методами:
- стентирование;
- наложение билиодигестивного анастомоза.
Стентирование – это введение в просвет протока пластикового каркаса, препятствующего сдавлению. Стентирование может осуществляться разными методами.
Билиодигестивный анастомоз – это операция по соединению жёлчного протока с двенадцатиперстной или тощей кишкой в обход сдавленного участка.
Выбор метода декомпрессии зависит от состояния больного, прогнозов, индивидуальных особенностей анатомических нарушений.
Общие принципы лечения больных с резектабельной опухолью
Резекция поджелудочной железы является основной (но не единственной) составляющей лечения рака, позволяющей максимально увеличить продолжительность жизни больного. Однако резекция должна обязательно дополняться химиотерапией или химиолучевой терапией.
Радикальная хирургическая операция направлена:
- на предотвращение местного рецидива новообразования;
- одновременно – на сохранение функции пищеварительной функции на таком уровне, который позволит максимально безопасно проводить химиотерапию (и чаще всего далеко не единственный курс).
Перед операцией врач должен убедиться, что:
- функциональное состояние жизненно важных органов позволит больному благополучно перенести и операцию, и последующее агрессивное консервативное лечение;
- нет отдалённых метастазов опухоли;
- опухоль соответствует критериям резектабельности.
Для этого проводится соответствующая диагностика. Только после полноценного обследования врач, а нередко – врачебный консилиум, принимает решение о целесообразности хирургического вмешательства. Тем не менее, после операции у четверти больных осуществление химиотерапии бывает невозможно.
Виды хирургических операций:
- гастропанкреатодуоденальная резекция (ГПДР) или панкреатодуоденальная резекция (ПДР);
- дистальная резекция поджелудочной железы;
- панкреатэктомия.
ГПДР – иссечение головки поджелудочной железы, части желудка, двенадцатиперстной кишки, общего жёлчного протока и жёлчного пузыря. При ПДР желудок не резецируется. Кроме того, в ходе операции удаляются регионарные лимфатические узлы, могут иссекаться сосуды и нервы. После иссечения проводится реконструкция желудочно-кишечного тракта, пластика сосудов. Операции в подобном объёме выполняются при раке головки поджелудочной железы. ГПДР и ПДР могут повлечь нарушения функций пищеварительной системы разной степени тяжести, панкреонекроз, внутренние и желудочно-кишечные кровотечения.
Дистальная резекция может выполняться в следующем объёме:
- удаление хвоста поджелудочной железы;
- удаление хвоста и тела;
- удаление хвоста, тела и перешейка;
- субтотальная дистальная резекция – удаление хвоста, тела, перешейка и большей части головки поджелудочной железы.
Такие операции в большинстве случаев сопровождаются удалением селезёнки ввиду нарушения её кровоснабжения. Операция выполняется при раке тела или хвоста поджелудочной железы, в случае внутрипротоковой аденокарциномы – только в объёме субтотальной резекции. При нейроэндокринныех опухолях (НЭО) высокой и умеренной дифференцировки (грубо говоря, низкой и умеренной степени злокачественности) возможна дистальная резекция в меньшем объёме, в том числе и с сохранением селезёнки. В зависимости от объёма операции, больному может потребоваться пожизненный контроль сахара в крови, приём инсулина.
Тотальная панкреатодуоденэктомия (панкреатэктомия) – удаление всей поджелудочной железы, двенадцатиперстной кишки, жёлчного пузыря и общего жёлчного протока, селезёнки, регионарных лимфатических узлов – выполняется в случае обнаружения нескольких очагов опухоли или распространения опухоли тела поджелудочной железы на хвост и головку. После операции требуется пожизненный частый контроль диабета и приём пищеварительных ферментов. Невозможность обеспечения такого контроля является противопоказанием к операции.
Адъювантная (послеоперационная) терапия является обязательным этапом лечения рака, поскольку:
- согласно данным новых исследований, аденокарцинома поджелудочной железы способна метастазировать ещё на этапе формирования первичной опухоли;
- отдалённые метастазы трудно выявить своевременно, и они являются основной причиной смерти после радикальной операции.
Химиотерапия замедляет рост отдалённых метастазов, отодвигая время их проявления, тем самым позволяя увеличить продолжительность жизни больного. С той же целью в комбинации с химиотерапией применяется лучевое лечение, но вопрос эффективности последней пока остаётся открытым. Больные, получающие послеоперационную химио- или химиолучевую терапию, живут в среднем в полтора-два раза дольше по сравнению с теми, кто её не получает, однако такое лечение может существенно снижать качество жизни.
Общие принципы лечения больных нерезектабельным раком поджелудочной железы
Основная задача лечения нерезектабельных опухолей – перевод их в категорию резектабельных. Иногда этого удаётся добиться при помощи неоадъювантной (предоперационной) химиотерапии (или химиолучевой терапии).
Нерезектабельные опухоли поджелудочной железы бывают разные – со значительным поражением местным распространением и лишь немного не соответствующие критериям нерезектабельности. Последние называют пограничнорезектабельными. Такие опухоли являются особенно перспективными в плане последующего осуществления радикальной операции.
Если опухоль достаточно чувствительна к химиотерапии, неоадъювантное противоопухолевое лечение подавляет рост не определённых на момент установления диагноза метастазов и замедляет местное распространение – поэтому, если в дальнейшем удастся провести радикальную операцию, такое лечение может улучшить прогноз.
В случаях резектабельной опухоли назначение дооперационной химиотерапии сопряжено с рисками: во-первых, за время консервативного лечения малочувствительная к химиотерапии опухоль может стать нерезектабельной, во-вторых, химиотерапия (и лучевое лечение), ввиду высокой токсичности, может привести к ухудшению общего состояния и невозможности выполнения операции.
Больные, перенёсшие адъювантное противоопухолевое лечение и последующую радикальную операцию, после хирургического вмешательства продолжают получать химиотерапию.
Паллиативное лечение рака поджелудочной железы
Паллиативное лечение направлено на устранение мучительных симптомов, которыми чаще всего сопровождается рак поджелудочной железы (особенно на 4 стадии).
Такое лечение не приостанавливает рост опухоли и процесс метастазирования, однако значительно облегчает жизнь больному.
Паллиативное лечение рака поджелудочной железы направлено на устранение:
- симптомов, обусловленных сдавлением опухолью жёлчевыводящих путей;
- развития нарушения проходимости двенадцатиперстной кишки (дуоденальной обструкции), также связанного с её сдавлением;
- изнуряющего болевого синдрома;
- симптомов, обусловленных интоксикацией: сильнейшей слабости, потери аппетита и прочих;
- психических нарушений, связанных как с самим фактом выявления смертельной болезни, так и с вызванными заболеванием физическими страданиями.
При обструкции жёлчевыводящих путей выполняется стентирование или билиодигестивный анастомоз.
При дуоденальной обструкции выполняется гастроэнтероанастомоз - формирование соединения желудка в обход двенадцатиперстной кишки с другими отделами тонкого кишечника
Несмотря на короткий срок жизни больных с распространённым раком поджелудочной железы, согласно данным ряда исследований, проведённых за рубежом, 40% доживает до того момента, когда начинает развиваться непроходимость двенадцатиперстной кишки. Поэтому некоторые зарубежные специалисты рекомендуют совмещать билиодигестивный анастомоз с гастроэнтероанастомозом. По наблюдениям этих авторов, такая операция позволяет продлить жизнь и улучшить её качество по сравнению со случаями, когда профилактическое наложение гастроэнтеростомоза не выполняется. В России, в целом, не принята тактика профилактического гастроэнтеростомоза, а соответствующие исследования не проводились.
Если на момент установления диагноза боль отмечается у 25-40% пациентов, в терминальной стадии этот симптом наблюдается уже у 80% больных раком поджелудочной железы. Боли бывают разной интенсивности, однако даже умеренная постоянная боль истощает, отнимает последние силы. Для купирования болевого синдрома применяются анальгетики, преимущественно - наркотические.
Хороший результат даёт в комбинации с медикаментозным лечением спланхникэктомия – хирургическое иссечение чревного узла солнечного сплетения или его разрушение с помощью введения химических веществ. В результате такой процедуры болевые импульсы из зоны, поражённой опухолью, перестают передаваться в мозг и боль перестаёт ощущаться.
При распространённом (местно или по всему организму) раке с целью продления жизни нередко назначается химиотерапия, но чаще всего качество жизни при этом весьма сомнительно.
Лечение народнеыми средствами
Лечить рак поджелудочной железы лучше в специализированных центрах, где опыт и навык специалистов несравнимо выше, чем в неспециализированных больницах. Например, в Москве это Институт хирургии им. А. В. Вишневского, Московский клинический научный центр, Московский научно-исследовательский онкологический институт им. П. А. Герцена.
Врач высшей категории, в медицине более 20 лет. Интерес к написанию популярных статей на медицинские темы появился несколько лет назад, когда всё чаще стала замечать на просторах Интернета тексты на онкологическую тематику, пестрящие фактическими ошибками и вводящие читателя в заблуждение…
Комментарии
Злокачественные опухоли поджелудочной железы делятся на две группы: опухоли экзокринной части (95% случаев) и опухоли эндокринной части (5% случаев). В казуистически редких случаях встречаются мезенхимальные опухоли и лимфомы.
Злокачественные опухоли поджелудочной железы делятся на две группы: опухоли экзокринной части (95% случаев) и опухоли эндокринной части (5% случаев). В казуистически редких случаях встречаются мезенхимальные опухоли и лимфомы. Данные рекомендации посвящены только карциномам
экзокринной части поджелудочной железы.
1. КЛАССИФИКАЦИЯ И ОПРЕДЕЛЕНИЕ СТАДИИ
Стадирование осуществляется на основании TNM классификации рака поджелудочной железы (РПЖ) (8-е издание, 2017 г.) (табл. 1).
Первичная опухоль (T):
• ТХ — недостаточно данных для оценки первичной опухоли
• Tis — carcinoma in situ
• T1 — опухоль ограничена поджелудочной железой до 2 см в наибольшем измерении
• Т2 — опухоль ограничена поджелудочной железой; более 2 см, но не более 4 см в наибольшем измерении
• Т3 — опухоль более 4 см в наибольшем измерении
• Т4 — опухоль распространяется на чревный ствол, верхнюю брыжеечную или общую печёночную артерию
Регионарные лимфатические узлы (N):
• NX — недостаточно данных для оценки состояния регионарных лимфоузлов
• N0 — нет признаков метастатического поражения регионарных лимфоузлов
• N1 — наличие метастазов в 1-3 регионарных лимфоузлах
• N2 — наличие метастазов в 4 или более регионарных лимфоузлах
К регионарным лимфоузлам для опухоли головки поджелудочной железы относятся лимфоузлы вдоль общего желчного протока, общей печёночной артерии, воротной вены, пилорические, инфрапилорические, субпилорические, проксимальные брыжеечные, чревные, передние и задние панкреатоду-оденальные, вдоль верхней брыжеечной вены и правой латеральной стенки верхней брыжеечной артерии. К регионарным лимфоузлам для опухоли тела и хвоста поджелудочной железы относятся лимфоузлы вдоль общей печёночной артерии, чревного ствола, селезёночной артерии, ворот селезёнки, а также забрюшинные и латеральные аортальные лимфоузлы. Адекватное послеоперационное стадирование предполагает морфологическое изучение не менее 10 лимфатических узлов.
Отдалённые метастазы (M):
• M0 — нет отдалённых метастазов
• M1 — наличие отдалённых метастазов
Таблица 1. Стадирование рака поджелудочной железы
Диагноз РПЖ устанавливается на основании анамнестических и лабораторных данных и результатов инструментального обследования. Морфологическое исследование является основой диагноза. Материал для него может быть получен во время операции или с помощью пункции/биопсии. Хирургическое вмешательство в ряде случаев может быть выполнено без морфологического подтверждения диагноза, в то время как консервативное лечение требует обязательной верификации ввиду значительной вероятности ложноположи-
тельных заключений инструментальных методов исследования, а также для исключения нейроэндокринных опухолей. В случае высокого риска осложнений, связанных с биопсией, при планировании гистологического исследования следует выполнить тонкоигольную пункцию образования (чрескожную или эндоскопическую). В план обследования должны быть включены:
• осмотр, сбор анамнеза болезни, семейного анамнеза;
• клинический анализ крови;
• биохимический анализ крови с оценкой функции печени, почек;
• УЗИ органов брюшной полости, забрюшинного пространства, шейно-надключичной области;
• УЗИ малого таза для женщин;
• R-графия органов грудной клетки;
• эндосонография для оценки распространённости и резектабельности, а также для навигации забора материала с целью морфологического исследования;
• КТ грудной клетки, брюшной полости и малого таза с в/в контрастированием (обязательно получение изображений в артериальную и портальную венозую фазы)для определения степени распространённости, резектабельности или оценки эффективности консервативного лечения;
• МРТ брюшной полости и малого таза с в/в контрастированием для определения степени распространённости, резектабельности или оценки эффективности консервативного лечения;
• ПЭТ/КТ для оценки первичной распространённости при решении вопроса о возможности выполнения радикальной операции или при планировании ЛТ;
• лапароскопия с целью определения распространённости, оценки резектабельности или взятия биопсии;
• ангиография с целью определения резектабельности;
• пункция/биопсия первичной опухоли или метастаза с целью морфологической верификации диагноза;
• при наличии в семейном анамнезе опухолевых заболеваний (>1 близкая родственница, страдавшая раком яичников в любом возрасте или раком молочной железы в возрасте до 50 лет, или два родственника, страдавших раком поджелудочной железы, яичников, молочной железы или предстательной железы)целесообразно генетическое консультирование и определение герминальной мутации BRCA 1 и 2.
3.1. Лечение неметастатического рака поджелудочной железы (любая Т, любая N, M0)
Решение о тактике лечения неметастатического РПЖ основано на оценке резектабельности первичной опухоли, которая должна производиться специалистами-хирургами, обладающими достаточным опытом хирургического
лечения больных с опухолями билиопанкреатодуоденальной области. В табл.2 приведена классификация, которая позволяет судить о резектабельности процесса по данным КТ.
Таблица 2. Оценка резектабельности неметастатического рака поджелудочной железы
(критерии клиники M. D. Anderson)
Не вовлечена;
нормальная
жировая про-
слойка между
опухолью
и артерией
Опухолевая инфильтрация 2 /сут. внутрь ежедневно в течение всего периода облучения. Применение гемцитабина в дозе 300 мг/м 2 еженедельно в качестве радиосенсибилизатора во время ЛТ является возможной альтернативой, однако существенно более токсичной, и, по-видимому, менее эффективной. При проведении стереотаксической ЛТ сочетанная ХТ не проводится, РОД составляет 7,5 Гр, 5 раз до СОД 37,5 Гр.
Основным дозолимитирующим фактором при стереотаксической ЛТ рака поджелудочной железы является наличие полых органов, таких как желудок, двенадцатиперстная кишка, тонкая или толстая кишка. Это обусловлено высоким риском развития тяжёлых постлучевых повреждений (расстояние между объёмом облучения и органами риска должно составлять не менее 5 мм).
Вовлечение этих органов в опухолевый процесс является противопоказанием к стереотаксической ЛТ.
3.1.3. Хирургическое лечение
Стандартным доступом при всех операциях на поджелудочной железе является срединная лапаротомия. При опухолях головки поджелудочной железы следует выполнять гастропанкреатодуоденальную резекцию. При опухолях тела или хвоста поджелудочной железы следует выполнять дистальную субтотальную резекцию
поджелудочной железы, включающую удаление тела, хвоста железы, а также селезёнки. Стандартный объём лимфодиссекции предполагает удаление следующих лимфатических узлов: надпилорических и подпилорических, лимфоузлов по ходу печёночной артерии и чревного ствола с его ветвями, лимфоузлов вдоль
общего желчного протока, лимфоузлов вокруг пузырного протока, ретропанкреатических лимфоузлов, лимфоузлов по нижнему краю головки поджелудочной железы, лимфоузлов по правой полуокружности верхней брыжеечной артерии, лимфоузлов по верхнему краю головки поджелудочной железы. При карциномах тела и хвоста поджелудочной железы рекомендовано удаление следующих групп лимфоузлов: лимфоузлов ворот селезёнки, лимфоузлов вдоль селезёночной артерии, лимфоузлов по нижнему краю поджелудочной железы.
Стандартная лимфаденэктомия должна включать удаление не менее 10 лимфатических узлов.
3.1.4. Адъювантная терапия
В случае предоперационной ХТ длительностью 6 мес. с последующим хирургическим лечением после операции рекомендовано динамическое наблюдение без адъювантной терапии. При длительности предоперационной ХТ
меньше 6 мес. рекомендовано применение адъювантной ХТ так, чтобы общая продолжительность ХТ составила 6 мес. В случае хирургического лечения без предоперационной ХТ адъювантная ХТ рекомендована всем пациентам вне зависимости от стадии и радикальности операции. Лечение должно быть начато в течение 3 мес. после операции (оптимально — в течение 6 нед.).
Если послеоперационные осложнения не позволяют начать ХТ в течение 3 мес., проведение адъювантной ХТ в более поздний период нецелесообразно, показано динамическое наблюдение и назначение лечения по факту прогрессирования болезни. Рекомендуемые режимы адъювантной ХТ представлены в табл. 3.
Таблица 3. Рекомендуемые режимы адъювантной химиотерапии при раке поджелудочной железы
mFOLFIRINOX 1 : оксалиплатин 85мг/м 2 в/в 120 мин., иринотекан 150мг/м 2 в/в 90 мин.,
кальция фолинат 400 мг/м 2 в/в 120 мин., 5-фторурацил 2400 мг/м 2 в/в инфузия в тече-
ние 46 часов, каждые 2 нед., всего 12 циклов
GEMCAP: гемцитабин 1000 мг/м 2 в/в капельно 30 мин. в 1-й, 8-й и 15-й дни + капецита-
бин 1660 мг/м 2 внутрь ежедневно с 1 -го по 21-й день каждые 4 нед., всего 6 циклов
• гемцитабин 1000 мг/м 2 в/в капельно 30 мин. еженедельно 7 нед., далее 1000 мг/м 2
в 1 -й, 8-й и 15-й дни каждые 4 нед., всего 6 циклов или
• капецитабин 2000-2500 мг/м 2 /сут. внутрь с 1 -го по 14-й день каждые 3 нед., всего
8 циклов или
• 5-фторурацил 425 мг/м 2 в/в струйно + кальция фолинат 20 мг/м 2 в/в струйно
с 1 -го по 5-й дни каждые 4 нед., всего 6 циклов
1 mFOLFIRINOXрекомендуется только пациентам в удовлетворительном общем состоянии (по шкале ECOG 0-1 балл, без серьёзных осложнений хирургического лечения, сопутствующих заболеваний и с уровнем общего билирубина 2
в/в 120 мин., иринотекан 180 мг/м 2
в/в 90 мин., кальция фолинат
400 мг/м 2 в/в 120 мин., 5-фторурацил
400 мг/м 2 в/в болюс, 5-фторурацил
2400 мг/м 2 в/в инфузия в течение 46
часов, каждые 2 нед.)
• состояние по шкале ECOG 0-1 балл;
• общий билирубин 2
в/в капельно 30 мин. + гемцитабин
1000 мг/м 2 в/в капельно 30 мин. в 1-й,
8-й, 15-й дни каждые 4 нед.
• состояние по шкале ECOG 0-2 балла;
• общий билирубин 2 в/в 1-й, 8-й
дни каждые 3 нед. в сочетании с од-
ним из производных платины:
• цисплатин 60-75мг/м 2 в/в в 1-й
день или
• карбоплатин AUC 4-5 в/в в 1-й
день или
• оксалиплатин 100-130мг/м 2 в/в
в 1-й день
• состояние по шкале ECOG 0-2 балла;
• общий билирубин 2 в/в 1,8, 15
каждые 4 нед.
• состояние по шкале ECOG 2 балла
• общий билирубин 2 или полная отмена) и инфузионного (до 2000 мг/м 2 ) введения 5-фторурацила;
• редукция дозы иринотекана (до 165 мг/м 2 );
• редукция дозы оксалиплатина (до 65 мг/м 2 ).
3.2.2. Лучевая терапия
Применение ЛТ возможно в случае локорегионарного рецидива после хирургического лечения, а также продолженного роста первичной нерезектабельной опухоли после ХТ при отсутствии отдалённых метастазов.
Оптимальная последовательность применения ХТ и ЛТ в таких ситуациях не определена.
Облучение проводится в РОД 1,8-2,0 Гр до СОД 45-54 Гр в сочетании с капецитабином в дозе 1600 мг/м 2 /сут. внутрь ежедневно в течение всего периода облучения. В случае применения стереотаксической ЛТ рекомендуется ис- пользовать 3 фракции до СОД 30-45 Гр или 5 фракций до СОД 25-45 Гр. В объём
облучения включаются первичная опухоль с вовлечёнными лимфатическими узлами или рецидивная опухоль.
3.2.3. Химиотерапия II линии
Рекомендуемые режимы ХТ II линии при РПЖ суммированы в табл. 5.
Таблица 5. Рекомендуемые режимы химиотерапии II линии рака поджелудочной железы
Режим ХТ (лечение до прогрессирования/
неприемлемой токсичности)
Критерии
выбора режима ХТ
Nab-паклитаксел 100-125мг/м 2 в/в капельно 30 мин. +
гемцитабин 750-1000 мг/м 2 в/в капельно 30 мин. в 1-й,
8-й, 15-й дни каждые 4 нед.
• ранее не использовался гемцитабин
и nab-паклитаксел;
• состояние по шкале ECOG 0-1 балл;
• общий билирубин 2 в/в в 1-й и 8-й дни каждые
3 нед. в сочетании с одним из производных платины:
• цисплатин 60-75 мг/м 2 в/в в 1-й день или
• карбоплатин AUC 4-5 в/в в 1-й день или
• оксалиплатин 100-130 мг/м 2 в/в в 1-й день
• ранее не использовался гемцитабин и про-
изводное платины;
• состояние по шкале ECOG 0-2 балла;
• общий билирубин 2 в/в в 1-й, 8-й, 15-й дни
каждые 4 нед.
• ранее не использовался гемцитабин;
• состояние по шкале ECOG 1-2 балла;
• общий билирубин 2 в/в 120 мин.,
иринотекан 165-180 мг/м 2 в/в 90 мин., кальция фолинат
400 мг/м 2 в/в 120 мин., 5-фторурацил 320-400 мг/м 2
в/в болюс, 5-фторурацил 2000-2400 мг/м 2 в/в инфузия
в течение 46 часов, интервал между циклами 2 нед.)
• ранее использовался гемцитабин;
• состояние по шкале ECOG 0-1 балл;
• общий билирубин 2 в/в 120 мин., кальция
фолинат 400 мг/м 2 в/в 120 мин., 5-фторурацил 400 мг/м 2
в/в болюс, 5-фторурацил 2400 мг/м 2 в/в инфузия в тече-
ние 46 часов, интервал между циклами 2 нед.);
XELOX (оксалиплатин 130 мг/м 2 в/в 120 мин. в 1-й день, ка-
пецитабин 2000 мг/м 2 /сут. внутрь 1-14 дни каждые 3 нед.);
FOLFIRI.3 (иринотекан 90 мг/м 2 в/в 60 мин. в 1-й день,
кальция фолинат 400 мг/м 2 в/в 120 мин. в 1-й день,
5-фторурацил 2000 мг/м 2 в/в инфузия в течение 46
часов, иринотекан 90 мг/м 2 в/в 60 мин. в 3-й день после
окончания инфузии 5-фторурацила, интервал между
циклами 2 нед.);
CAPIRI (иринотекан 200 мг/м 2 в/в 90 мин. в 1-й день, ка-
пецитабин 1600 мг/м 2 /сут. внутрь в 1-14-й дни каждые
3 нед.)
OFF (оксалиплатин 85 мг/м 2 в/в 120 мин. в 1 день,
кальция фолинат 200 мг/м 2 в/в 120 мин. в 1-й, 8-й, 15-й
дни, 5-фторурацил 2000 мг/м 2 в/в инфузия в течение 24
часов в 1 -й, 8-й, 15-й дни, интервал между циклами 3 нед.
• ранее использовался гемцитабин;
• состояние по шкале ECOG 0-1 балл;
• общий билирубин 2 /сут. внутрь в 1-14-й дни
каждые 3 нед.;
5-фторурацил 425 мг/м 2 в/в струйно + кальция фолинат
20 мг/м 2 в/в струйно в 1-5-й дни каждые 4 нед.
Читайте также:

