Интраоперационная терапия рака желудка диссертация

Автореферат диссертации по медицине на тему Интраоперационное облучение в комбинированном лечении рака желудка
РГБ ОД - 8 АПР «К
На правах рукописи
АФАНАСЬЕВ Сергей Геннадьевич
ИНТРАОПЕРАЦИОННОЕ ОБЛУЧЕНИЕ В КОМБИНИРОВАННОМ ЛЕЧЕНИИ РАКА .ЖЕЛУДКА
диссертации на соискание ученой степени кандидата медицинских наук
Работа выполнена в Научно-исследовательском Институте Онкологии Томского Научного Центра Сибирского Отделения Российской Академии Медицинских наук
Научные руководители: академик РАМН.профессор Зырянов В.Н.,
Официальные оппоненты: доктор медицинских наук,профессор Мардынский Ю.С., кандидат медицинских наук.с.н.с. Анисеня И.И.
Ведущая организация-.Онкологический Научный Центр лм.Н.Н.Блохина РАКШ
Защита состоится " 1996 г. ,в ^ на засе-
дании диссертационного совета Д.001.34,01 в Научно-исследовательском Институте Онкологии Томского Научного Центра Сибирского Отделения РАМН,по адресу 634050>г.Томск,пер.Кооперативный,5.
С диссертацией можно ознакомиться в библиотеке Научно-исследовательского Института Онкологии ТНЦ СО РАМН.
Автореферат разослан И Я? И суО 0,05).
Уровень послеоперационной летальности в исследуемых группах,в основном зависел от объема выполненной операции .В основной группе после гастрэктомии умер 1 пациентов из 18,что составило 5,55 + 5,18%.. В контрольной группе было 4 летальных•исхода на 29 экстирпаций желудка - 13,79 + 7,65%.После дистальной субтотальной резекции желудка в основной группе умер 1 из 16 больных и 3 из 36 больных,получивших оперативное лечение без облучения. Летальность составила 6,25 + 6,05% и 8,33 + 4,59%,соответственно.
Наиболее частой причиной смерти больных в сравниваемых группах явился послеоперационный перитонит.В основной группе панкре-
Исходы выполненных операщга при комбинированном и хирургическом
ЧИСЛО БОЛЬНЫХ Г А С Т Р Э ктомия ДИСТАЛЬНАЯ РЕЗЕКЦИЯ ПРОКСИМАЛЬНАЯ РЕЗЕКЦИЯ
МЕТОД ЛЕЧЕНИЯ всего умерли всего умерли всего умерли всего умерли
И О Л т 3 5 3 8,57+4,77% 1 8 51,43+8,65% 1 5,55+5,18% 1 6 45,71+8,42% 1 6,25+6,05% 1 2,86+1,37% 1 ! 1 0 0 %
ОПЕРАЦИЯ 6 7 7 10.44+4,16% 2 9 43,23+6,05% 4 13,75+7,65% 3 6 53,73+6,09% 3 3,33+4,59% о 2,99+2,73% -
ИТОГО 10 2 1 0 9,90+2,62% 4 7 46,07+3,26% 5 10,63+3,71% 5 2 50,98+3,29% 4 7,69+2,24% 3 2,94+0,91% 1 33,3+17,89%
атит тяжелой степени как причина летального исхода имел место у 2 больных, несостоятельности швов анастомоза не отмечено.В контрольной группе причиной перитонита чаще всего являлись недостаточность швов анастомоза (4 больных),либо послеоперационный панкреонекроз (3 больных).
Таким образом,применяемое интраоперационное облучение в однократной дозе 10 Гр. не увеличивает послеоперационную летальность при радикальных операциях по поводу рака желудка Ш ст.Не изменяется структура причин смертности.
На аутопсии больных,умерших после операции в сочетании с ИОЛТ, отмечено,что в зоне облучения преобладают рубцовые изменения и диффузное разрастание тугоэластичной серой ткани в виде постлучевого ожога. Последний имеет четкие границы,а по форме и размерам полностью совпадает с очертаниями коллиматора,применявшимся для формирования поля облучения.
При микроскопии гистологических препаратов из зоны ИОЛТ установлено, что преобладает фиброз жировой клетчатки к заместительный склероз.Вся фиброзная ткань обильно пропитана крупными лимфоцитами и плазматическими ¡метками.В некоторых полях зрения отмечаются скопления полиморфноклегочных лимфоцитов,которые следует расценить как склероз лимфатических узлов в бассейнах регионарного метастазирования,включенных в поле облучения.
Таким образом,отмеченные морфологические изменения в тканях, подвергшихся ИОЛТ соответствуют ранним лучевым повреждениям.Однако, выраженную лимфоцитарную инфильтрацию фиброзной ткани в этой зоне можно объяснить стимуляцией местного иммунитета.
Система иммунитета при интраоперационной лучевой терапии
Влияние ИОЛТ на показатели системы иммунитета исследовано у 72 больных раком желудка III стадии,у которых не наблюдалось осложнений в послеоперационном периоде.Из них, 26 больных получили комбинированное лечение,46 пациентов хирургическое лечение без дополнительного облучения (контрольная группа).
В обеих группах.через 2 недели после оперативного вмешательства не отмечено достоверных изменений в системе комплемента и в уровне Т- и В-лимфоцитов.В то же время количество Т-активных лимфоцитов у больных,перенесших комбинированное лечение - 43,5 +
Номер работы: 679057
Без учета скидки. Вы получаете файл формата pdf
Вы получаете первые страницы диссертации в формате txt
Просмотр 1 страницы = 3 руб
Оглавление диссертации:
Введение. Актуальность темы исследования. Эффективное лечение больных раком желудка по-прежнему остается одной из нерешенных проблем онкологии. Несмотря на устойчивое снижение заболеваемости, рак желудка сохраняет одно из ведущих мест в структуре онкологической патологии населения России; на него приходится 12,7% всех злокачественных новообразований. Рак желудка занимает второе место (16,7%) в структуре смертности от злокачественных новообразований [13;58]. К моменту постановки диагноза наиб
- терапии. Материалы Всероссийской конференции молодых ученых.Москва, 1-14 сентября 2001 г.
- С.46-47. 3. Бердов Б.А., Скоропад В.Ю., рака Пахоменко желудка с К.В., Хичева Г.А. и Комбинированное лечение интраоперационным 3(7).
- С. 35-44. предоперационным облучением. Практическая онкология.
- N 4. Скоропад В.Ю., Бердов Б.А., Мардынский Ю.С., Титова Л.Н., Пахоменко К.В. Результаты клинического исследования эффективности интраоперационной лучевой терапии
Глава 2. Материал и методы исследования.
. Решение поставленных в диссертационной работе задач осуществлено на основании изучения результатов обследования, лечения и последующего динамического наблюдения за 150 больными раком желудка. Исследование охватывает период с 1993 по 2004 годы, все фрагменты работы выполнены в МРНЦ РАМН. Подробная характеристика включенных в исследование больных приведена в 3-4
главах диссертационной работы. В 1993 году была проведена 1 фаза клинического исследования, основной задачей которой была оц
. Для анализа данных создано программное обеспечение, включающее в себя базу данных и комплекс программ для систематизации, группировки по различным признакам, анализа и статистической обработки информации на языке Visual FoxPro 5 на персональном компьютере. Для статистической обработки использовали коммерческий биомедицинский пакет Prism 3 (GraphPad Software, Inc., San Diego, USA). Достоверность различий между показателями оценивали с помощью точного критерия Фишера. При вычислении отдаленн
2.3. Классификации рака желудка, использованные в диссертационной работе. 1. КЛАССИФИКАЦИЯ РАКА ЖЕЛУДКА по системе TNM (UICC 5 издание, 1997) Приведена в приложении №1. 2. КЛАССИФИКАЦИЯ РАКА ЖЕЛУДКА в соответствии с Правилами Японского научного общества по изучению рака желудка. А. Локализация опухоли в желудке - соответствует классификации по системе TNM: выделяются 3 отдела - верхняя треть (С), средняя треть (М) и нижняя треть (А). По стенкам желудка выделяют: малую и большую кривиз
. Для установления диагноза рака желудка, определения локализации и степени распространенности опухолевого процесса использовали следующие виды исследований: рентгенографию желудка, фиброгастроскопию с биопсией, трансабдоминальное ультразвуковое исследование, рентгеновскую компьютерную томографию, эндосонографию верхних отделов желудочнокишечного тракта, рентгенографию легких. В качестве дополнительных диагностических методов при подозрении на наличие отдаленных метастазов использовали разл
2.5. Методики предоперационной и интраоперанпопной лучевой терапии. Предоперационное облучение больных раком желудка проводили на гамма-терапевтических установках типа Рокус и Агат Р и на ускорителе электронов Philips SL 20 с использованием фотонного излучения в статическом режиме с двух встречных (переднего - эпигастрального и заднего - паравертебралыюго) полей. Размеры полей облучения составляли 10-12x10-14 см в зависимости от величины и локализации опухоли. В зону облучения включали перви
2.6. Техническое обеспечение интраоперационной лучевой терапии. С целью клинического использования интраоперационной лучевой терапии в МРНЦ РАМН был построен и оснащен специализированный блок, состоящий из (1) стандартной операционной, которая через внутреннюю дверь напрямую сообщается с (2) комнатой дистанщюнного контроля, где располагается пульт управления ускорителем электронов и аппаратура визуального и мониторного наблюдения за больным, и (3) каньона ускорителя электронов (отечественный
. Протокол исследования предусматривал следующие основные критерии включения больных:
1) гистологическое подтверждение рака желудка;
2) клиническая стадия T1-4N0-2M0 по классификации TNM, 1987 (при подготовке диссертации все опухоли были перестадированы в соответствии с 5 изданием 1997 г.);
3) отсутствие противопоказаний для проведения лучевой терапии (декомпенсированный стеноз привратника, резко выраженная кахексия и анемия) и хирургического вмешательства (тяжелая сопутс
. Наблюдение за больными осуществлялось в амбулаторных условиях; при необходимости больные были госпитализированы в абдоминальное отделение для дифференциального диагноза и инвазивных методов исследования. В тех случаях, когда больной не являлся для обследования в МРНЦ РАМН, сведения о его состоянии запрашивались в медицинских учреждениях (областные онкологические диспансеры, городские и районные больницы) либо ЗАГСах и паспортных столах по месту жительства. На июнь 2004 г. медиана наблюдени
3.3 Влияние адъювантной лучевой терапиии на функциональные и структурные изменения в смежных органах попадающих в зону лучевого воздействия. Применение агрессивных методов лечения требует изучения их влияния на структуру и функцию жизненно важных органов, попадающих в зону их воздействия. Реакции смежных с желудком органов и тканей на преди интраоперационную лучевую терапию в раннем послеоперационном периоде были изучены и опубликованы ране.[38] Целью настоящего исследования было изучение сос
Глава 4 Результаты комбинированного лечения местно-распространснного рака желудка.
. Учитывая современный подход к лечению рака желудка, основным компонентом которого стало принципиальное выполнение лимфодиссекции в объёме D2, задачей этого раздела работы было разработать и апробировать в клинике в рамках 2 фазы клинического комбинированного исследования лечения новый местно- высокотехнологичный метод распространенного рака желудка, включающий преди интраоперационное облучение, а также расширенную лимфодиссекцию в объёме D2. Показать совместимость интенсивных методик луч
4.2. Характеристика больных, методов диагностики, и лечения. Основываясь на результатах рандомизированного исследования и данных мировой литературы, показаниями к данному виду комбинированного лечения считали рак желудка в фазе местно-регионарного распространения (Т24/N1-3 МО). Таким образом, задачей дооперационной и интраоперационной диагностики было исключение случаев раннего рака желудка (Т1), результаты хирургического лечения которого весьма удовлетворительные, а также генерализованног
Предоперационное облучение больные переносили хорошо, необходимости в перерыве курса облучения либо в отсрочке оперативного вмешательства не возникало. Легкие проявления общей лучевой реакции в виде тошноты, слабости, снижения аппетита имели место у 4 больных; еще у 3 больных была однократная рвота после первого сеанса облучения. Ни в одном случае нами не зарегистрировано интраоперационных осложнений, в том числе связанных с транспортировкой, укладкой больного и сеансом интраоперационного об
4.4. Отдаленные результаты лечения. На начало 2005 г., то есть более чем через 2 года после лечения последнего включенного в исследование больного, из 26 выписанных из стационара больных умерли 6, продолжают наблюдаться 20. Утеряны из-под наблюдения 4 больных. Максимальный срок наблюдения за больными составляет 58 мес, медиана - 25 мес. Рассчитанная по методу Kaplan-Meier выживаемость всей группы больных составила: 1-летняя - 90±6%, летняя - 75±9%. Сведения об умерших больных суммированы в та
. Таким образом, в рамках настоящего исследования разработан и апробирован в клинике в рамках 2 фазы клинического исследования новый высокотехнологичный метод комбинированного лечения местно- распространенного рака желудка, включающий преди интраоперационное облучение, а также расширенную лимфодиссекцию. В сжатые сроки - 9 - 10 дней - производится предоперационное облучение с целью повышения абластичности предстоящего оперативного вмешательства и профилактики интраоперационного метастазиров
Пахоменко Константин Валентинович. Пред-, интраоперационная лучевая терапия, лимфодиссекция D2 в лечении рака желудка : диссертация . кандидата медицинских наук : 14.00.19 / Пахоменко Константин Валентинович; [Место защиты: ГУ "Медицинский радиологический научный центр РАМН"].- Обнинск, 2007.- 144 с.: ил.
Актуальность проблемы
Рак желудка — одна из важнейших и не решенных проблем современной онкологии Несмотря на устойчивое снижение заболеваемости, рак желудка сохраняет одно из ведущих мест в структуре онкологической патологии населения России на него приходится 12,7% всех злокачественных новообразований Рак желудка занимает второе место (16,7%) в структуре смертности от злокачественных новообразований (Чиссов В И и др., 2005, Давыдов МИ и др, 2006) Заболевание характеризуется крайне высокими показателями летальности на 1-м году с момента установления диагноза - 56% (Давыдов М И и др, 2006)
К моменту постановки диагноза наибольшее число больных имеет местно-регионарное распространение опухолевого процесса, доля раннего рака желудка достаточно низка - от 3 до 15% Поэтому основные силы онкологов направлены на улучшение результатов лечения местно-распространенных форм Основным методом лечения рака желудка остается хирургический.
Комбинированное лечение проводится менее чем у 20% больных (Чиссов В И. и др, 2005)
Последние десятилетия ознаменовались значительным прогрессом в технике хирургических вмешательств, ростом их агрессивности, использованием расширенной лимфодиссекции Несмотря на это, частота развития рецидивов и отдаленных метастазов остается высокой, особенно при наличии и сочетании неблагоприятных прогностических факторов прорастании опухолью всей стенки желудка, наличии метастазов в регионарные лимфатические узлы, низко- и недифференцированном строении опухоли Данные клинических исследований, проведенных в конце прошлого и начале нашего века в России и за рубежом, показали, что лучевая терапия в составе комбинированного лечения является хорошо апробированным методом дополнительного воздействия, приводит к существенному снижению частоты развития локо-регионарного рецидива (который является важной проблемой в лечении рака желудка и развивается у 16-85% больных), а также в ряде клинических ситуаций способна улучшить выживаемость больных [Дарьялова С Л и др , 2000, Скоропад В Ю и др , 2004]
Таким образом, предотвращение развития локо-регионарного рецидива, профилактика интраоперационной диссеминации опухолевых клеток является важнейшей задачей в лечении рака желудка Наши собственные данные и анализ мирового опыта показывает, что только расширение хирургического пособия не может привести к однозначному улучшению результатов лечения рака желудка, а диссеминация клеток в процессе пересечения лимфатических стволов и увеличение операционной травмы при расширении лимфодиссекции может даже ухудшить результаты лечения (Ikeguchi М et al, 2000, Pughese R et al, 2004, Ikeguchi M. et al, 2005) Поэтому мы, как и многие другие авторы (Дарьялова С Л и др, 2000, Скоропад В Ю идр 2001, Привалов А В идр, 2006, Kim DY et al, 2006), считаем необходимым и оправданным применение комбинированного лечения рака желудка, включающего наряду с адекватным по объему оперативным вмешательством различные методы лучевой терапии
Цель исследования:
Разработка и клиническая реализация новых подходов к комбинированному лечению больных раком желудка, включающих предоперационную и интраоперационную лучевую терапию, а также оперативные вмешательства с лимфодиссекцией D2 для улучшения результатов лечения больных
Задачи исследования:
Проанализировать отдаленные результаты рандомизированного исследования эффективности комбинированного лечения рака желудка, включавшего пред-, интраоперационную лучевую терапию (ИОЛТ) и стандартные оперативные вмешательства с лимфодиссекцией в объеме D1
Исследовать реакции смежных органов почек, позвоночника, спинного мозга, поджелудочной железы на комбинированное воздействие в отдалённые после лечения сроки
Разработать и внедрить в клиническую практику методику лечения больных местно-распространенным раком желудка, включающую в себя интенсивное предоперационное, интраоперационное облучение ложа опухоли и зон регионарного
метастазирования, а также лимфодиссекцию D2 и расширено-комбинированные оперативные вмешательства
4 Изучить совместимость предоперационного
облучения и ИОЛТ с расширенными и расширенно-
комбинированными оперативными вмешательствами по критерию частоты послеоперационных осложнений, летальности и реакций смежных органов в раннем послеоперационном периоде
5. Изучить эффективность комбинированного лечения с
предоперационной лучевой терапией, ИОЛТ, расширенными и расширенно-комбинированными оперативными вмешательствами у больных местно-распространенным раком желудка по критерию медианы выживаемости и 1-3-летней выживаемости
Научная новизна:
Научная новизна исследования заключается в дальнейшей разработке нового направления в радиоонкологии, базирующегося на применении высоких однократных доз ионизирующего излучения во время оперативного вмешательства в сочетании с предоперационным фракционированным облучением, расширенными и расширенно-комбинированными оперативными вмешательствами, включающими в себя лимфодиссекцию в объеме D2 для решения актуальной проблемы - улучшения результатов лечения больных раком желудка Впервые с использованием факторного анализа изучены отдаленные (5-летняя выживаемость, медиана выживаемости) результаты эффективности ИОЛТ, полученные в рамках рандомизированного исследования Впервые в отдаленные после комбинированного лечения сроки изучено структурное и функциональное состояние ряда органов брюшной полости и забрюшинного пространства
Практическая значимость:
Разработка и создание технического и методического обеспечения ИОЛТ на ускорителях электронов дает возможность рекомендовать ее для практического применения в ведущих онкорадиологических центрах, а также других специализированных лечебных учреждениях Изучение совместимости интенсивной лучевой терапии с комбинированными и расширенно-комбинироваными оперативными вмешательствами позволяет обосновать использование предоперационной и интраоперационной
лучевой терапии для улучшения результатов лечения больных местно-распространенным раком желудка Разработанный метод лечения может быть реализован в короткие сроки — 9-11 дней, что дает выраженный экономический эффект
Реализация и внедрение результатов работы:
Результаты работы внедрены в отделах комбинированных методов лечения и лучевой терапии Государственного учреждения Медицинский радиологический научный центр Российской академии медицинских наук (акты внедрения)
Апробация работы:
Диссертация апробирована на научно-практической конференции клинического радиологического научного сектора ГУ МРНЦ РАМН 03 05.2007 г (протокол № 4)
Объём и структура диссертации:
Диссертация состоит из введения, обзора литературы, 3 глав собственных исследований, обсуждения, выводов и указателя литературы Работа изложена на 144 страницах формата А4, иллюстрирована 17 таблицами и 18 рисунками Список литературы содержит 182 наименования источников, в том числе 66 отечественных и 116 зарубежных авторов
- Отделение анестезиологии и реанимации
- Метастазы рака
- Химиотерапия
- Хоспис для онкологических больных
- Иммунотерапия в центре платной онкологии Медицина 24/7
- КТ-исследования
- МРТ-исследования
На долю злокачественных новообразований органов брюшной полости в структуре онкологической заболеваемости в странах Западной Европы приходится около 30% от всех локализаций. За 2016 г. в России было выявлено 581,6 случай злокачественных новообразований органов брюшной полости на 100 тыс. населения (рак желудка — 25,99; колоректальный рак — 42,6; поджелудочная железа — 11,7).
Опухоли тракта осложняются метастатическим поражением брюшины в 30–40% случаев, из них рак поджелудочной железы — примерно в 40%, рак желудка — в 30–40%, рак аппендикса — до 30–100%, колоректальный рак — до 10%. По данным российских и иностранных авторов, интраоперационно обнаруживают распространение опухоли по брюшине у 20–25% больных раком желудка [1, 2].
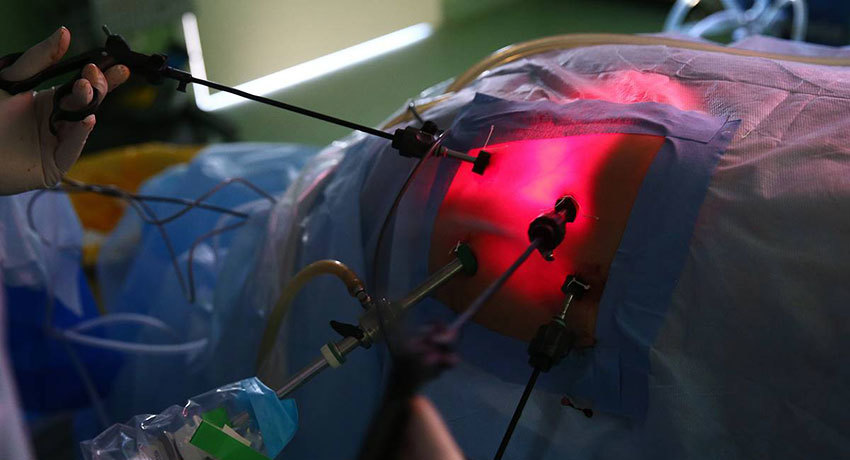
С целью снижения риска развития местного рецидива и метастатического поражения брюшины возможно применение различных методов дополнительного противоопухолевого воздействия на область операционного поля и брюшину, одним из таких методов является интраоперационная фотодинамическая терапия (ИОФДТ) [3].
Метод фотодинамической терапии основан на способности ряда лекарственных препаратов (фотосенсибилизаторов) избирательно накапливаться в опухолевой ткани. При воздействии лазерного излучения на сенсибилизированные ткани в них развиваются фотохимические реакции с освобождением синглетного кислорода, что приводит к гибели и разрушению сенсибилизированных клеток без негативного влияния на здоровые ткани и органы.
Материалы и методы
В МНИОИ им. проходили лечение 240 больных с диагнозом рак желудка стадии T3-4N0- . Данные больные были разделены на две группы: 140 больных (основная группа), которым были выполнены и паллиативные операции с применением интраоперационной фотодинамической терапии брюшины, и 100 больных (контрольная группа), которым были выполнены также и паллиативные операции (по объему соответствующие хирургическим вмешательствам у больных основной группы) без применения метода интраоперационной фотодинамической терапии.
Согласно данным гистологического исследования опухоли желудка: высокодифференцированная аденокарцинома диагностирована у 4 (1,7%) пациентов, умеренно дифференцированная аденокарцинома- у 26 (10,8%), низкодифференцированная аденокарцинома — у 51 (21,3%), перстневидноклеточный рак — у 62 (25,8%), сочетание перстневидноклеточного рака с аденокарциномой — у 97 (40,4%) больных.
Методика ИОФДТ состоит из трех этапов. На первом этапе больному вводили фотосенсибилизатор. На втором этапе фотосенсибилизатор накапливался в опухоли, продолжительность данного этапа зависела от применяемого фотосенсибилизатора и составляла: для фотосеанса — 2 часа и 48 часов для фотогема. Третьим этапом был сеанс ИОФДТ, который выполнялся как завершающий этап хирургической операции.
Результаты
Для оценки эффективности ИОФДТ был проведен анализ выживаемости. В качестве критического события была выбрана смерть больного от прогрессирования рака желудка. В основной группе пациентов максимальный срок наблюдения составил 72 месяца, в контрольной группе пациентов максимальный срок наблюдения составил 58 месяцев. В группе контроля годичная безрецидивная выживаемость 60,7±6,2%, 29,5±6,6%. В группе ИОФДТ годичная безрецидивная выживаемость 82,1±6,1%, 55,1±10%.
Выводы
Разработанная методика интраоперационной фотодинамической терапии — метод выбора лечения больных раком желудка с наличием перитонеальной диссеминации.
Литература:
- Каприн А.Д., Старинский В.В., Петрова онкологической помощи населению России в 2016 году. 2017; 7–18.
- Сулейманов Э.А., Каприн А.Д., Филоненко Е.В., Хомяков В.М., Гришин Н.А., Москвичева Л.И., Урлова флуоресцентная диагностика перитонеальной диссеминации у больных раком желудка // Biomedicalphotonics. — 2016. — T. 5, № 3. С. 9–18.
- Абдуллаев А.Г., Полоцкий Б.Е., Давыдов подходы к лечению псевдомиксомы брюшины // Российский онкологический журнал, 2013; 4–9.



ВВЕДЕНИЕ . ГЛАВА 1. Обзор литературы. ГЛАВА 2. Диагностические исследования. Методики предоперационной и интраоперационной лучевой терапии. ГЛАВА 3. Отдаленные результаты лечения. ГЛАВА 4. Непосредственные результаты лечения. Отдаленные результаты лечения
4. ГЛАВА 5. Обсуждение. Приложение 1 3
СПИСОК ЛИТЕРАТУРЫ. Используя исторический контроль, авторами был сделан вывод о значительном улучшении отдаленных результатов лечения по сравнению с ограниченной лимфодиссекцией. На ежегодном Конгрессе в г. Анализ результатов продемонстрировал, что 1 при 2 стадии рака желудка достоверно лучше показатели 5летней выживаемости отмечены при выполнении расширенной лимфодиссекции , чем при выполнении стандартной н модифицированной гастрэктомии ,5 и ,1 соответственно 2 при 3 стадии двукратное улучшение 5летней выживаемости отмечено после расширенных радикальных операций , чем после стандартных операций ,6 3 летальность после расширенных операций весьма низка, в с годы составляла 3. Таким образом, в Японии методика расширенной лимфаденэктомии стала стандартом хирургического лечения рака желудка, и именно с ее распространением связываются успехи в лечении рака желудка.
Удаление групп лимфатических узлов лежит в основе определения объма лимфаденэктомии, соответственно 4. В развитие расширенной лимфодиссекции заметный вклад внесли и отечественные хирурги, прежде всего, необходимо отметить работы Ю. Е. Берзова, . Е. Берегова, В. И. Пронин, Т. А. Ковель, Г. Н. Мслнкидзе, М. Сигала, Ф. Ш. Ахметзянов, и др. Наибольшее развитие в нашей стране данное направление получило в возглавляемом акад. РАМН М. И. Давыдовым отделении торакальной онкологии НИИ клинической онкологии ОНЦ РАМН, где последовательно проводится принцип лимфодиссекция должна являться стандартной процедурой, стать обязательной частью радикальных операций у больных раком желудка. Были оперированы 5 больных раком проксимального отдела желудка. Несмотря на увеличение числа комбинированных операций, и объема лимфодиссекции, роста послеоперационных осложнений и летальности не отмечено. ЯЗ ,2 3,6 6 больных. В Московском научноисследовательском онкологическом институте им. П. А. Герцена изучена эффективность лимфаденэктомий, выполненных 0 больным раком желудка. Выполнение расширенных лимфаденэктомий не приводило к росту послеоперационной летальности после расширенных операций умерли 6,3 больных, после стандартных 6,5. Э2лимфаденэктомий увеличилась на за счет сокращения числа локорегионарных рецидивов. В Красноярском краевом онкологическом центре прооперировано 0 больных раком желудка с применением расширенной забрюшинной лимфаденэктомии. Метастатическое поражение лимфоузлов обнаружено у ,3 больных, причем у ,3 их локализация соответствовала группам 2 и 3.

На правах рукописи
ЛИ АНДРЕЙ АНАТОЛЬЕВИЧ
СИНДРОМА ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
ПРИ КОМБИНИРОВАННОМ ЛЕЧЕНИИ РАКА ЖЕЛУДКА
С ПРИМЕНЕНИЕМ ИНТРАОПЕРАЦИОННОГО ОБЛУЧЕНИЯ
14.00.16 – патологическая физиология.
диссертации на соискание ученой степени
кандидата медицинских наук
Научные руководители: доктор медицинских наук
доктор медицинских наук
Официальные оппоненты: доктор медицинских наук
доктор медицинских наук
Ведущая организация – Российский онкологический научный центр им. РАМН (г. Москва)
С диссертацией можно ознакомиться в библиотеке НИИ онкологии ТНЦ СО РАМН.
Автореферат разослан _____________________________2007 г.
Ученый секретарь диссертационного совета,
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
АКТУАЛЬНОСТЬ ПРОБЛЕМЫ. Комбинированные виды лечения в последние годы занимают ведущее место в лечении онкологических больных. Большинство больных, страдающих опухолевыми заболеваниями желудка, подвергаются оперативному вмешательству, которое составляет основной этап комбинированного лечения. Сочетание хирургической операции с интраоперационной лучевой терапией (ИОЛТ) на 20-25% увеличивают 5-летнюю выживаемость ( и др., 1996; и др., 2002; , , 2005). Работами ряда авторов ( и др., 2000; и др., 2000) доказано, что противоопухолевый эффект лучевой терапии тем выше, чем выше доза ионизирующего излучения, подведенная к опухоли. Однако, подведенная однократная доза излучения, вызывает опасность повреждения здоровых тканей, повышая риск развития тяжелых послеоперационных осложнений ( и др., 2003; Kramling H.-J., 1998; Calvo F. A. et al., 2000). Поэтому, ИОЛТ в комбинированном лечении больных раком желудка является дополнительным повреждающим фактором, повышающим травматичность оперативного вмешательства.
Развитие злокачественных новообразований приводит к стресс-индуцированным реакциям, нарушению всех видов обмена, активации протеолиза, дисбалансу в системе перекисного окисления, энергодефициту ( и др., 2004; Barder M. D. et al., 2000). На этом фоне, хирургическое воздействие на опухолевые и окружающие здоровые ткани влечёт за собой также повреждение клеток, что ведёт к образованию и выбросу в кровь продуктов их жизнедеятельности, а также биологически активных веществ ( и др., 1992; и др., 2003). Биологическая активность эндотоксинов нарушает метаболизм органов и тканей, что приводит к развитию синдрома эндогенной интоксикации (СЭИ). Прогрессирование СЭИ, приводит к нарушению проницаемости клеточных мембран, развитию интерстициального отёка, нарастанию эндотоксикоза, нарушению центральной и периферической гемодинамики с развитием метаболического ацидоза, что может привести к развитию полиорганной недостаточности. Уровень эндогенной интоксикации зависит как от интенсивности образования токсинов, так и от состояния органов и систем, отвечающих за дезинтоксикационную функцию организма, основными из которых являются печень, почки и легкие. (, , 1990; , 1993).
Во время операции на этапе применения интраоперационной лучевой терапии (ИОЛТ), происходит дополнительная активация окислительных процессов, с образованием свободных радикалов, что является дополнительным источником эндотоксемии ( др., 1996; и др., 2000).
Таким образом, общий уровень интоксикации онкологического больного в раннем послеоперационном периоде при комбинированном лечении в сочетании с ИОЛТ, складывается из интоксикации связанной с опухолевым процессом, последствий хирургического вмешательства, действия электронного облучения на фоне повреждающего воздействия операционной травмы и препаратов наркоза.
Оценить эффективность методики периоперационной корригирующей медикаментозной терапии в повышении резистентности организма больных к повреждающему действию эндогенной интоксикации в условиях комбинированного лечения рака желудка с применением интраоперационного облучения.
1. Разработать методику анестезиологического обеспечения и интенсивной терапии в раннем послеоперационном периоде у больных раком желудка при проведении ИОЛТ.
2. Изучить реакцию стресс-реализующих гормонов в периоперационном периоде у больных раком желудка, получивших интраоперационное облучение.
3. Оценить динамику основных маркеров синдрома эндогенной интоксикации у больных раком желудка на этапах хирургического лечения с ИОЛТ.
4. Провести анализ эффективности разработанной методики корригирующей медикаментозной терапии на течение адаптационных процессов после радикальных операции с ИОЛТ.
5. Оценить влияние медикаментозной корригирующей терапии на частоту и степень тяжести послеоперационных осложнений у больных раком желудка.
Впервые исследована степень выраженности эндогенной интоксикации у больных раком желудка, получивших комбинированное лечение с применением ИОЛТ.
Изучена динамика параметров эндокринного ответа организма у больных радикально оперированных по поводу рака желудка с ИОЛТ, в течение операционного и раннего послеоперационного периодов.
На основании полученных данных разработана патогенетически обоснованная методика корригирующей медикаментозной терапии, направленная на снижение эндогенной интоксикации и профилактику периоперационных осложнений у больных раком желудка, оперированных с ИОЛТ.
Разработана и внедрена в клиническую практику методика анестезиологического обеспечения радикальных операций по поводу рака желудка с применением интраоперационного облучения.
Предложена эффективная методика корригирующей медикаментозной терапии, снижающая риск развития нехирургических осложнений в раннем послеоперационном периоде у больных раком желудка.
Результаты исследования внедрены в практику и успешно применяются в клиниках ГУ НИИ онкологии Томского научного центра СО РАМН.
ОСНОВНЫЕ ПОЛОЖЕНИЯ, ВЫНОСИМЫЕ НА ЗАЩИТУ
1. Уровень эндогенной интоксикации у больных получивших хирургическое лечение с ИОЛТ достоверно повышается в течение операционного и послеоперационного периодов по сравнению с исходным уровнем.
2. Повышение степени эндогенной интоксикации оказывает отрицательное влияние на резистентность организма, что увеличивает риск развития послеоперационных нехирургических осложнений.
3. Применение медикаментозной корригирующей терапии позволяет достоверно уменьшить степень эндогенной интоксикации у пациентов, перенесших комбинированное лечение с ИОЛТ и уменьшить частоту развития послеоперационных осложнений.
Математическая обработка полученных данных проводилась на персональном компьютере с применением пакета прикладных программ Statistica 6.0. Оценку достоверности различий при нормальном распределении коэффициента ассиметрии проводили с использованием t-критерия Стьюдента. При анализе распределения, отклоняющихся от нормального, использовали критерий Вилкоксона-Манна-Уитни.
Лечение больных осуществлялось в торако-абдоминальном отделении (рук. отделения – д. м.н. ) и отделении анестезиологии - реанимации (зав. отделением – д. м.н. ); лабораторные исследования проводились в клинической лаборатории (зав. лабораторией – ) ГУ НИИ онкологии Томского научного центра СО РАМН.
СТРУКТУРА И ОБЪЕМ ДИССЕРТАЦИИ
Диссертация состоит из введения, 3 глав, заключения, выводов и указателя литературы, изложена на 128 страницах машинописного текста. Работа иллюстрирована 19 таблицами, 13 рисунками. Указатель литературы содержит 220 названий работ, в том числе 139 отечественных и 81 зарубежных авторов.
По результатам диссертации опубликованы 12 печатных работ, в. т. ч. 1 статья в центральном журнале, 1 методические рекомендации.
В клиническое исследование включено 56 больных раком желудка с местным распространением опухоли, соответствующим Т3-Т4, с морфологически подтвержденным диагнозом рака желудка, которые до операции не получали какой-либо специальной противоопухолевой терапии. Пациенты находились на стационарном лечении в торако-абдоминальном отделении, в раннем послеоперационном периоде – в отделении анестезиологии и реанимации ГУ НИИ онкологии Томского научного центра СО РАМН. Всем пациентам выполнялись радикальные операции в сочетании с интраоперационным облучением.
Больные разделены на две репрезентативные группы:
I группа (основная) – 33 больных раком желудка, получивших хирургическое лечение с ИОЛТ в однократной дозе 10 Гр на фоне специальной корригирующей медикаментозной терапии (КМТ), направленной на предупреждение пери - и ранних послеоперационных осложнений.
II группа (контрольная) – 23 больных раком желудка III ст., получивших хирургическое лечение в сочетании с интраоперационным облучением однократной дозой 10 Гр.
Распределение больных в сравниваемых группах по виду операции (абс. ч.,%)
Вид оперативного вмешательства
Дистальная субтотальная резекция желудка
Проксимальная резекция желудка
Интраоперационная лучевая терапия проводилась по стандартной методике, разработанной в НИИ онкологии ТНЦ. Источником энергии служил малогабаритный бетатрон, генерирующий пучок быстрых электронов с энергией 6 МэВ. Излучатель быстрых электронов для ИОЛТ размещен непосредственно в операционной, на специальной подвеске. Проводилось облучение ложа удаленной опухоли и зон регионарного метастазирования в разовой дозе 10 Гр.
Методика анестезиологического пособия и ведения раннего послеоперационного периода, которая проводилась больным раком желудка, включенным в наше исследование, условно разделена на несколько этапов, что представлено в таблице 2.
Этапы анестезиологического пособия
1) подготовка больного к операции и наркозу + КМТ
1) подготовка больного к операции и наркозу
3) поддержание анестезии
3) поддержание анестезии
4) облучение + КМТ
5) ближайший послеоперационный период + КМТ
4) ближайший послеоперационный период
Методика корригирующей медикаментозной терапии
Пациентам основной группы дополнительно к стандартным мероприятиям анестезиологического пособия и интенсивной терапии в послеоперационном периоде, проводилась специально назначенная корригирующая медикаментозная терапия. Целью последней являлась предупреждение и коррекция избыточной активности систем перекисного окисления липидов и связанных с ними нарушений регуляции агрегатного состояния крови и детоксикации в предоперационном, операционном и послеоперационном периодах. Методика КМТ включала комплекс антиоксидантной терапии применение мексидола, токоферола ацетата в сочетании с антиферментными препаратами. КМТ начинали за 1 час до операции путем внутримышечного введения токоферола ацетата в дозе 300 мг и мексидола внутривенно в дозе 200 мг. На этапе хирургического удаления опухоли и выполнения лимфодиссекции, за 45-50 мин до проведения ИОЛТ в дозе 10 Гр, внутривенно вводили мексидол в дозе 400 мг и гордокс в дозе ЕД. После завершения оперативного вмешательства продолжалось внутримышечное введение токоферола ацетата в дозе 300 мг через 8 часов и мексидола в дозе 200 мг внутривенно через 6 часов в течение 3-5 суток раннего послеоперационного периода.
Эффективность методики корригирующей медикаментозной терапии проводили по оценке: функционального состояния гипоталамо-гипофизарно-надпочечниковой системы, щитовидной, поджелудочной железы; данных общеклинических, биохимических тестов; дополнительных лабораторных методов, отражающих уровень эндогенной интоксикации. Производилось определение эффективной концентрации альбумина, резерва связывающей способности альбумина, лейкоцитарный индекс интоксикации, ядерный индекс интоксикации, коэффициент интоксикации, молекулы средней массы. Забор материала для исследования осуществляли в установленные сроки: перед операцией, после завершения сеанса ИОЛТ, в 1, 3, 5 сутки раннего послеоперационного периода.
интоксикации можно объяснить проводимой медикаментозной коррекцией эндогенной интоксикации в основной группе. Таким образом, пациенты в основной группе показали
менее выраженную реакцию нейтрофильного ростка кроветворения.
Рис. 1. Значение ядерного индекса интоксикации у пациентов сравниваемых групп. Примечание: * – различия статистически значимы между сравниваемыми группами (p
Читайте также:





