Гормональная терапия рака и метастазы
Одним из сдерживающих моментов при назначении ЗГТ является риск возникновения злокачественных опухолей, особенно рака молочной железы и половых органов. Злокачественные опухоли репродуктивных органов составляют от 35 до 45% в структуре онкологической забо
А. Ф. Урманчеева, доктор медицинских наук
М. М. Бурнина
Медицинская академия последипломного образования, Санкт-Петербург
Одним из сдерживающих моментов при назначении ЗГТ является риск возникновения злокачественных опухолей, особенно рака молочной железы и половых органов. Злокачественные опухоли репродуктивных органов составляют от 35 до 45% в структуре онкологической заболеваемости женщин в развитых странах. В России в 1997 году у 210 144 женщин впервые в жизни было диагностировано злокачественное новообразование, подавляющее большинство заболевших было в возрасте 60-69 лет. Рак молочной железы лидирует в структуре онкологической заболеваемости, его удельный вес составил 18,4%, гинекологический рак занимает второе место (17,0%), третье место принадлежит колоректальному раку (11,2%) и четвертое — раку желудка (9,9%).
За последние годы в мире накоплен значительный опыт применения ЗГТ, что позволяет провести анализ некоторых исследований и сделать соответствующие выводы о возможном риске заболевания злокачественными опухолями в женской популяции, а также о применении ЗГТ у онкологических пациенток.
Результаты опубликованных с 1970 года более 50 когортных эпидемиологических исследований (выборочных, нерандомизированных) о ЗГТ и РМЖ были крайне противоречивыми и несопоставимыми по численности обследуемых и составу препаратов. Проведенные в 90-е годы метанализы этих исследований показали, что прием ЗГТ в период времени до 5 лет не увеличивал риск РМЖ, тогда как более длительное назначение способствовало росту РМЖ. Последний наиболее полный реанализ 51-го эпидемиологического исследования, охватывающего 52 тыс. больных РМЖ и 108 тыс. женщин без РМЖ, показал, что относительный риск РМЖ составляет 1,31% для женщин, принимавших ЗГТ в течение 5 лет и более. Риск одинаков для различных видов применяемых эстрогенов (конъюгированных или 17b-эстрадиола). С 1980 года с целью протективного действия на эндометрий в ЗГТ применяются прогестагены как в циклическом, так и в постоянном режиме. В первом крупномасштабном исследовании, проведенном в США, по комбинированной ЗГТ не было установлено увеличение риска РМЖ при добавлении прогестинов, хотя дальнейший метанализ выявил относительный риск при длительной (более 5 лет) комбинированной ЗГТ в странах Европы и США. В то же время в клиниках, где проводился опрос больных РМЖ, число пациенток, получавших ранее ЗГТ, было таким же, как и в общей женской популяции страны. Анализируя случаи РМЖ, развившиеся у пациенток, длительно принимавших ЗГТ, все клиницисты отмечают более прогностически благоприятное течение заболевания за счет высокой дифференцировки опухоли, меньших размеров и низкой потенции к метастазированию по сравнению с РМЖ у больных, ранее не получавших ЗГТ. Таким образом, ЗГТ длительностью до 5 лет не увеличивает риск РМЖ, но, учитывая повышение вероятности РМЖ при долговременной ЗГТ (более 5 лет), необходимо рекомендовать маммографию до начала ЗГТ и далее ежегодно. При этом надо помнить, что интерпретация маммограмм может быть затруднена из-за увеличения плотности ткани молочной железы на фоне ЗГТ.
Дискуссионным является вопрос о назначении ЗГТ больным РМЖ после излечения. Однако в настоящее время уже накоплен некоторый опыт в лечении климактерических расстройств у пациенток, ранее подвергавшихся лечению по поводу РМЖ. Несколько ретроспективных анализов исследований, включавших от 25, 65, 77 до 146 больных РМЖ, не выявили ухудшения прогноза заболевания, т. е. увеличения риска рецидивов заболевания по сравнению с контрольными группами больных РМЖ, не получавших ЗГТ. Исходя из этого, авторы полагают, что недлительная ЗГТ может быть назначена больным РМЖ, имевшим начальные формы рака без метастатического поражения лимфатических узлов. Однако учитывая тот факт, что длительная ЗГТ (более 5 лет) увеличивает риск РМЖ в популяции в 1,3-1,4 раза, необходимы рандомизированные исследования по ЗГТ больным РМЖ. Такого рода пилотное исследование запланировано в Англии и Италии. Нужно также отметить, что у больных, излечившихся от РМЖ, в два-пять раза выше риск развития РМЖ контрлатеральной молочной железы, а у женщин, у которых РМЖ был в молодом возрасте, — в десять раз.
Рак эндометрия (РЭ). В 70-е годы была отмечена отчетливая взаимосвязь между эстрогенной ЗГТ (ЭЗГТ) и увеличением риска РЭ. Впоследствии метанализ различных исследований позволил уточнить эту взаимосвязь; относительный риск сохранялся у больных, получавших эстрогены, и был минимален для не получавших. Риск РЭ возрастал в зависимости от длительности приема эстрогенов: от 1,4 при приеме менее 1 года до 9,5% при длительности более 10 лет. После прекращения приема эстрогенов риск снижался к концу второго года до показателей, отмеченных у больных, не использовавших ЭЗГТ, хотя он мог оставаться более высоким в течение 10 лет после прекращения ЭЗГТ. В дальнейшем с целью защиты эндометрия от пролиферативного влияния эстрогенов в ЗГТ были включены прогестины. При добавлении прогестинов риск РЭ зависел от длительности приема прогестинов: менее 10 дней он был 2,4%, более 10 дней — 1,1%, т. е. сохранялся на том же уровне, что и у использующих комбинированную ЗГТ. Хотя, по данным Бересдорфа, длительная комбинированная ЗГТ (5 лет и более) увеличивает риск РЭ в два раза, РЭ, развившийся на фоне ЗГТ, так же как и РМЖ, протекает менее агрессивно (в большинстве случаев он высокодифференцированный, стадии IA), и риск смерти от РЭ значительно ниже у пациентов, получавших ЗГТ, чем у не получавших.
Другим спорным моментом остается вопрос о применении ЗГТ больными РЭ после радикального лечения. К 1998 году были известны три когортных исследования по применению ЗГТ больным РЭ (153 человека) после радикальных экстирпаций матки с придатками. Анализ, проведенный в 1999 году, касается еще 130 больных РЭ, получавших ЭЗГТ. Как и предыдущие научные изыскания, он не выявил увеличения риска рецидивов РЭ, однако для окончательного утверждения также необходимы рандомизированные исследования. Следует считать, что ЗГТ может быть назначена больным РЭ с благоприятным прогнозом при безрецидивном периоде более 5 лет после радикального лечения, а также больным саркомой матки, исключая эндометрильностромальные формы.
Рак яичника (РЯ). Более чем в 300 публикациях по ЗГТ и РЯ не отмечено роста заболеваемости РЯ на фоне приема ЗГТ. Только в девяти работах говорится о некотором увеличении риска при длительной ЗГТ. В то же время клиническое исследование, проведенное Гвидоззи, Папонтом среди 130 больных РЯ, части из которых в послеоперационном периоде назначалась ЭЗГТ в течение 6-8 недель, не выявило ее негативного влияния на безрецидивный интервал и общую выживаемость по сравнению с лечением без ЭЗГТ.
Рак шейки матки (РШМ). РШМ не является гормонозависимой опухолью, в его этиологии основная роль отводится папилломавирусной инфекции, передающейся половым путем. При ретроспективном анализе риск инвазивного рака шейки матки у женщин, принимавших ЗГТ, оказался ниже, чем в общей популяции. Возможно, это связано с более тщательным скринингом, проводимым среди пациенток, которым назначается ЗГТ. Больным, подвергавшимся хирургическому вмешательству в объеме радикальных расширенных экстирпаций матки с придатками по поводу РШМ, как правило, назначается ЭЗГТ для ликвидации явлений постовариэктомического синдрома. Наш небольшой опыт ЗГТ диветреном (эстрадиол валерат + медроксипрогестерон ацетат) и дивигелем (17b-эстрадиол) среди больных РШМ (21 человек) в различные сроки после хирургического или комбинированного лечения (операция + облучение) представлен в табл. 1, 2. После шестимесячного приема препаратов модифицированный менопаузальный индекс (ММИ) снизился более чем на 40% (на 45,0% — при приеме дивитрена и на 42,4% — дивигеля). Положительная динамика в лечении постовариэктомического синдрома характеризовалась в первую очередь снижением почти на 50% выраженности психоэмоциональных и нейровегетативных симптомов. Изменение ММИ при оценке метаболических изменений также указывало на положительный эффект ЗГТ. Тем не менее сохранялись урогенитальные расстройства, свойственные не столько урогенитальному синдрому, сколько особенностям лечения рака шейки матки (радикализм операции в сочетании с лучевой терапией). Степень их выраженности, однако, значительно снижалась за счет исчезновения дизурических явлений, диспареунии, недержания мочи, никтурии. При исследовании гормонального спектра у 11 больных, получавших дивитрен, отмечено снижение на 20% уровня ФСГ при одновременном повышении на 90% уровня эстрадиола. При оценке липидного спектра крови установлено, что его показатели через 6 месяцев после начала лечения статистически не отличались от исходных. Благоприятным фактором, указывающим на безопасность данного метода лечения, является и снижение атерогенного индекса на 20%. Ни у кого из пациенток за время проведения ЗГТ и далее в течение последующих 12 месяцев не отмечено рецидива заболевания. По данным Плоха, пятилетняя выживаемость больных РШМ, получавших ЗГТ и не получавших ЗГТ, была одинаковой. В настоящее время в наших онкологических клиниках больным РШМ (более 60 человек) после радикального хирургического лечения уже в раннем послеоперационном периоде назначается ЗГТ дивигелем, эстрофемом, прогиновой, климара или комбинированная ЗГТ фемостоном, цикло-прогиновой, клименом, дивиной.
Рак вульвы и влагалища. Плоскоклеточный рак вульвы и влагалища, так же как и РШМ, не является гормонозависимым и развивается у женщин пожилого и старческого возраста. Работ по применению ЗГТ у больных раком вульвы и влагалища не проводилось.
Во всех исследованиях по изучению риска колоректального рака на фоне ЗГТ отмечается статистически достоверное снижение на 30-40% заболеваемости среди получавших ЗГТ. В опубликованном в 1996 году в Швеции отчете о статистическом исследовании заболеваемости и смертности среди женщин, получавших и не получавших ЗГТ, также указывается на значительное снижение заболеваемости колоректальным раком, небольшое снижение частоты гепатоцеллюлярного и церебрального рака и отсутствие влияния ЗГТ на частоту меланом, рака легкого и почек.
Представленные материалы свидетельствуют о возможности широкого применения ЗГТ не только в общей женской популяции, но и в реабилитации части онкологических больных после их излечения при тщательном динамическом наблюдении. Тем не менее необходимо продолжение кооперированных научно-клинических исследований по изучению онкологических аспектов ЗГТ.
На сегодняшний день в арсенале гормональной терапии метастазов рака имеется несколько методов. Цель данной терапии – это предотвращение воздействия женского полового гормона эстрогена на раковые клетки. Этот гормон оказывает непосредственное воздействие на опухоль, стимулируя ее рост. С чего же начинается гормональная терапия? Выбор того или иного антигормонального препарата зависит от эффективности применения гормональной терапии в прошлом, а также от менструального статуса, то есть наличия или отсутствия менструаций.
Если применение одного из препаратов гормональной терапии не оказало никакого влияния на течение опухоли, то выбирается другой тип препарата. Однако, если с момента последнего курса гормональной терапии до возникновения рецидива прошло более 2 лет, то применение первого антигормонального препарата может быть все еще эффективным.
Гормональная терапия в пременопаузе
Пременопауза означает, что у пациентки все еще имеются менструации. В таком случае применяются следующие виды гормональной терапии:
- Тамоксифен или
- Терапия, направленная на понижение функции яичников или
- Сочетание тамоксифена со снижением функции яичников или
- Мегестрол или
- Галотестин (флуоксиместерон).
Обычно препаратом выбора считается тамоксифен, после чего применяется терапия, направленная на понижение функции яичников, в результате чего в организме снижается уровень эстрогена:
- Хирургическое удаление яичников или
- Облучение яичников радиацией с целью снижения их функции или
- Золадекс (госелерина ацтетат), люпрон (лейпролид) или трелстар (трипторелин).
Препараты для гормональной терапии или галотестин в настоящее время применяются редко:
- Мегестрол – препарат, по действию схожий с гормоном прогестероном. Он менее эффективен, чем тамоксифен. Побочным эффектом его применения являются отеки и увеличение веса. Однако у некоторых женщин он может быть весьма эффективен.
- Галотестин – представляет собой производное мужского гормона тестостерона. Эффективность его ниже, чем у тамоксифена и мегестрола. Его побочные эффекты – это так называемая маскулинизация, то есть появление мужских вторичных половых признаков. Среди них – рост волос на лице. Однако несмотря на его побочные эффекты, применение галотестина может быть эффективно у некоторых пациенток, так как он может повышать содержание эритроцитов в крови.
У женщин в пременопаузе, прошедших курс лечения по снижению функции яичников, либо пациенток, у которых как побочный эффект химиотерапии наступила ранняя менопауза, применяется несколько иное лечение. У них применяется такая гормональная терапия, которая используется лишь в постменопаузе:
- Аримидекс (анастрозол), фемара (летрозол) или аромазин (эксеместан) и
- Фаслодекс (фульвестрант).
Гормональная терапия в постменопаузе
Лечение по поводу рака молочных желез очень часто сопровождается временным прекращением менструаций. Если после лечения у Вас в течение нескольких месяцев отмечается отсутствие менструаций, можно предположить, что наступила менопауза. Однако, это не обязательно так. Для того, чтобы убедиться в том, что женщина находится в постменопаузе необходимо проведение определенных анализов. Если факт менопаузы подтвержден, то в таком случае возможности гормональной терапии значительно расширены:
- Аримидекс
- Фемара
- Аромазин
- Тамоксифен
- Фаслодекс
- Фарестон
- Мегестрол
- Галотестин
- Сочетание указанных препаратов.
Все эти препараты применяются в таблетированной форме, за исключением фаслодекса, который применяется в виде инъекции один раз в месяц.
Вы можете задаться вопросом: а какой именно из этих всех препаратов подойдет Вам?
В течение более 20 лет лучшим препаратом для гормональной терапии считался тамоксифен. Однако недавние исследования показали, что у женщин постменопаузы более эффективно применение препаратов из группы ингибиторов ароматазы, которые имеют несколько меньшее число побочных эффектов. Поэтому, если анализы рака молочных желез показывают, что опухоль гормонально-зависимая, вероятнее всего Вам назначат какой-либо препарат из группы ингибиторы ароматазы:
- Аримидекс (анастрозол),
- Фемара (летрозол) или
- Аромазин (эксеместан).
Эти препараты пока что еще не сравнивались между собой в каких-либо исследованиях, поэтому отдать какое-то предпочтение какому-либо из них трудно. Поэтому какой именно препарат будет назначен Вам зависит от рекомендаций врача, от того, какие уже Вы применяли препараты и от того, как Вы переносите тот или иной препарат.
Однако тамоксифен также может найти свое применение, в случае неэффективности ингибиторов ароматаз. В случае неэффективности и тамоксифена, применяется фаслодекс. Опыта применения этого препарата пока что еще мало, однако в одном из исследований было выявлено, что он так же эффективен, как и аримидекс у женщин в постменопаузе, когда тамоксифен у них неэффективен.
Сочетание тамоксифена и аримидекса не применяется, так как это не повышает эффективность, но выраженность побочных эффектов усиливается. В настоящее время изучается эффективность сочетания аримидекса с фаслодексом.
Смена препарата
Побочные эффекты гормональной терапии
Кроме этого эффекта, при гормональной терапии могут отмечаться и проявления менопаузы:
- Приливы
- Сухость влагалища
- Болезненность во время половых сношений
- Перемены настроения.
Применение ингибиторов ароматазы, а также препаратов, направленных на снижение функции яичников, как и хирургическое их удаление приводить к некоторым изменениям со стороны костной структуры. Поэтому перед лечением, а также во время него необходимо контролировать состояние костной ткани. Иногда в этом случае назначаются препараты, укрепляющие костную ткань.
Очень редко применение тамоксифена приводит к тромбообразованию (сгустков крови) и раку матки. Однако риск этих состояний крайне низок и несопоставим с положительными эффектами этого препарата.
Следующий этап
Со временем через несколько месяцев или даже лет гормональное лечение перестает быть эффективным и рак начинает расти. В этой ситуации предлагается следующий этап лечения – химиотерапия. Некоторые пациентки могут сочетать химиотерапию и гормональное лечение. Другие же полностью переходят только на химиотерапию. Кроме того, химиотерапия может сочетаться и с таргет-терапией.
Следует помнить, что эффект применения гормональной терапии может начаться только через несколько месяцев. Наличие гормональных рецепторов на клетках опухоли обычно свидетельствует о том, что гормональное лечение может быть эффективным. Чем больше видов этих рецепторов имеется на поверхности опухоли, тем лучше:
- Если на клетках опухоли имеются как эстрогеновые, так и прогестероновые рецепторы, то эффект гормональной терапии наблюдается в 70 %.
- Если имеются рецепторы либо к эстрогену, либо к прогестерону, то эффект отмечается в 33 %.
- Если же состояние гормональных рецепторов раковых клеток неизвестно, то все равно шанс на эффективность составляет 10 %.
Кроме того, эффективность гормональной терапии повышается с возрастом, а также в случае, если метастазы или рецидив развились минимум через 2 года после выявления опухоли.
В большинстве случаев обследования больных с локализованными опухолями врач приходит к выводу, что болезнь носит преимущественно системный характер, и метастазы разовьются позже. Обнаружение многочисленных метастазов, часто спустя годы после проведения мастэктомии, а также в течение многолетнего наблюдения за больными подтверждает этот вывод.
Обычно появление метастазов приводит к смертельному исходу в пределах трех лет, хотя в случаях, когда лечение оказывается эффективным, пациентки могут жить дольше. Вероятность метастазирования опухоли сильно зависит от степени вовлечения подмышечных лимфатических узлов в патологический процесс, что определяется при гистологическом анализе образцов, взятых во время операции.
Существует взаимосвязь между количеством пораженных подмышечных лимфатических узлов и вероятностью распространения метастазов.
Со времени проведения первой операции терапевтической овариэктомии, проведенной Битсоном в 1896 г., стало очевидно, что при изменении гормонального статуса организма в случаях распространенного опухолевого процесса, по крайней мере для одной трети пациенток достигается симптоматический эффект.
Также применяли анаболические стероиды, глюкокортикоиды и прогестерон, проводили удаление надпочечников или гипофиза и назначали ингибиторы ароматазы (анастрозол или летрозол).
Стандартный подход основан на менструальном статусе пациентки. Для большинства больных с метастазирующими опухолями в пременопаузе и перименопаузе используется хирургическое удаление яичников или их облучение. Однако с появлением антагонистов гонадотропин-рилизинг-гормона эти процедуры стали применять реже.
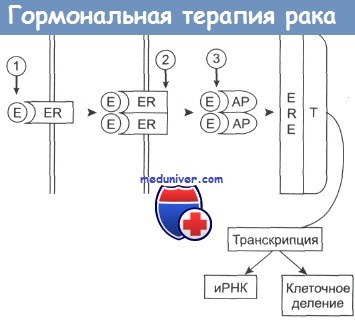
Эстроген (Е) связывается с рецептором (ER), который димеризуется.
Комплекс приобретает активность (АР) и присоединяется к эстроген-зависимым структурам (ERE) клеточного ядра.
Происходит активация таких белков, участвующих в транскрипции (Т), как РНК-полимераза II, что приводит к синтезу белка и делению клетки.
Гозерелин вызывает снижение уровня эстрогенов в плазме крови (1); фульвестран (2) предотвращает процесс димеризации рецептора и его активацию; тамоксифен (3) связывается с активным комплексом, подавляя его способность инициировать транскрипцию.
Антагонисты обеспечивают стойкое снижение уровня эстрогенов и вызывают у пациентки состояние менопаузы, которое длится в продолжении примерно двух месяцев с начала применения гозерелина. Препарат назначается ежемесячно в виде внутримышечных инъекций. Вместе с тем в качестве альтернативы снова стал популярным такой хирургический метод, как лапароскопическое удаление яичников.
Это достаточно безопасная и несложная операция, после которой пациентка на одну ночь остается в стационаре. Следует отметить, что перед операцией больные проходят тщательный отбор по критерию гормональной чувствительности опухоли, и тем, для кого не предполагается проявление лечебного эффекта, операция не проводится.
Для пациенток с опухолью в постменопаузе широко применяется тамоксифен, поскольку он практически не проявляет побочных эффектов. Препарат действует как антиэстроген, но, вероятно, оказывает и прямой цитотоксический эффект. В течение почти 20 лет тамоксифен использовался в качестве стандартного препарата адъювантной терапии.
Тамоксифен назначается перорально в ежедневной стандартной дозе 20 мг. Он обладает медленным кумулятивным действием. Побочные эффекты редки, однако могут наблюдаться приливы, тошнота, гиперкальциемия, тромбоцитопения, удержание жидкости и расстройство менструального цикла. После приема препарата большинство пациенток прибавляют 1-2 фунта в весе и некоторые отмечают ухудшение состояния кожи, волос и ногтей.
Гораздо более существенный эффект получен при назначении гормонотерапии пациенткам с гормонально зависимыми опухолями, в то время как при лечении гормонально независимых опухолей благоприятный эффект наблюдался лишь в редких случаях. Прогноз в случаях гормонально зависимых и независимых опухолей отличается. Для больных с гормонально-зависимыми опухолями характерен более длительный безрецидивный период и большая выживаемость.
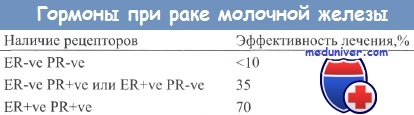
Совместное определение показателей ER и PR обеспечивает более точный прогноз в отношении чувствительности опухоли к гормонотерапии, чем это оказывается возможным при оперировании только показателем ER. Больные с PR-положительными опухолями также характеризуются более длительным безболезненным периодом.
На эффективность гормонотерапии сильно влияет характер распространения метастазов. Костные метастазы проявляют некоторую чувствительность к гормонам, хотя после лечения пациентки живут в среднем около 12-15 месяцев. Тем не менее некоторые больные с гормоночувствительными опухолями и с костными метастазами живут дольше, иногда несколько лет.
В большинстве случаев, при рецидиве опухоли, развившейся в пременопаузе, применяется гозерин (или его аналоги) или лапароскопическая овариэктомия (или облучение яичников). Эти меры эффективны для гормонально чувствительных опухолей. При опухолях в периоде постменопаузы обычно назначают тамоксифен, если пациентки раньше не получали этот препарат в качестве средства адъювантной терапии.
В любом случае можно ожидать, что выживаемость больных составит по крайней мере 30%. Экзогенные гормоны назначают до тех пор, пока не наступит эффект. В дальнейшем гормональную терапию продолжают только тем пациенткам, у которых проявился эффект первичного лечения. Предложены новые противоопухолевые препараты, относящиеся к группе ингибиторов ароматазы.
К числу их относится анастрозол, который блокирует биосинтез предшественников эстрогенов и их последующие превращения в тканях. Анастрозол действует при пероральном применении. Он хорошо переносится больными, так же как и другие родственные соединения, благодаря чему эти препараты быстро заняли место тамоксифена, который оказался неэффективным в лечении пациенток с гормонозависимыми опухолями, развивающимися в период постменопаузы. Рекомендуемая ежедневная доза препарата составляет 1 мг.
Если после первичного лечения возникает рецидив, то назначают другие препараты, например анаболические стероиды, прогестогены и глюкокортикоиды. Анаболические стероиды более эффективны у пациенток с опухолями, развившимися в постменопаузе, и, по-видимому, их особенно необходимо применять в случаях обнаружения костных метастазов.
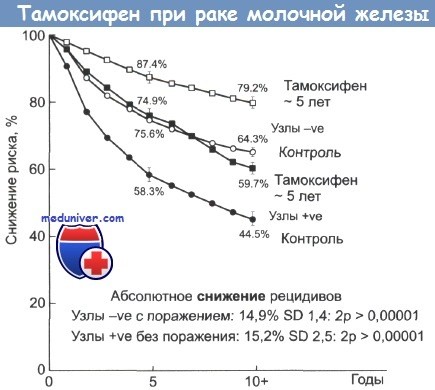
Абсолютное снижение риска возникновения рецидивов рака молочной железы при приеме тамоксифена.
Светлые значки — пациентки без признаков поражения лимфатических узлов; затемненные значки — пациентки с признаками поражения лимфоузлов.
Благоприятный эффект достигается примерно у 20% пациенток, однако недостатком применения стероидов является вирилизация. Удобным для применения является нандролон деканоат (Deca-Durabolin), который назначается в виде внутримышечных инъекций в дозе 50-100 мг каждые 3-4 недели. Если гормонотерапия раньше давала положительные результаты, то можно применять прогестогены. Наиболее часто используется ацетат медроксипрогестерона (МРА, Provera), который обычно назначают перорально в дозе 100 мг три раза в день.
Однако его применение ограничено из-за развития побочного эффекта — прибавления в весе. Такой же эффективностью обладает другое производное прогестерона — мегестрол-ацетат (Megace).
Широко обсуждается вопрос выбора метода лечения первого рецидива опухоли. Следует в этом случае использовать гормональный метод или же химиотерапию с использованием цитотостатиков? Если принимать во внимание количественные показатели, то выбирать надо между гормонотерапией (эффективна в 30% случаев) и комбинационной химиотерапией (эффективность которой в два раза выше). Однако это упрощенное решение вопроса, ответить на который на самом деле сложно.
Реакция опухоли на гормоны обычно носит более продолжительный характер, и у пациентки наблюдаются минимальные токсические проявления. При химиотерапии развивается более кратковременный эффект, который сопровождается токсическими и психологическими осложнениями. Большинство клиницистов в Великобритании в качестве средства первичного лечения предпочитают использовать гормональную терапию. Выбор облегчается все более широким применением метода анализа состояния рецепторов эстрогенов: гормональная терапия должна проводиться только среди пациенток с ER-положительными опухолями. Недавно предложен препарат фульвестрант (Faslodex), подавляющий функции рецепторов эстрогенов. Он может применяться у пациенток с гормоноустойчивыми опухолями, которые развились в постменопаузе. Одним из основных преимуществ этого препарата, по сравнению с агонистом эстрогенов, тамоксифеном, является отсутствие побочных эффектов. Он также не опустошает пул эстрогенов в женском организме, что происходит при применении ингибиторов ароматазы.

Гормональная терапия является первой опцией, которая рассматривается при метастазах рака молочной железы. В целом, лечение рака молочной железы 4 стадии с помощью антигормональных средств показано в ситуациях, если злокачественная опухоль содержит рецепторы эстрогена. Так как эстроген при данных опухолях является стимулятором роста и размножение раковых клеток, применение препаратов, которые блокируют данный рецепт или снижают выработку гормона в организме, позволяет успешно бороться с метастатическим процессом. Примерами данных препаратов являются Тамоксифен и Аромазин (экземестан).
В каком периоде вы находитесь — в пременопаузе или постменопаузе — влияет на выбор препарата гормональной терапии. Помимо этого, учитывается текущие и предыдущие лечение (если вы ранее получали препарат, а тем более если рецидив возник на фоне его приема, то большая вероятность, что ваша опухоль резистентна к данному варианту гормональной терапии). Иногда при метастатическом раке молочной железы может быть предложена оофорэктомия (удаление яичников). Это также считается одним из вариантов лечения гормонозависимого рака молочной железы.
Эстроген и рак молочной железы
Эстроген может выступать в роли драйвера роста опухоли, если её клетки содержат рецепторы к этому гормону. То есть при гормонозависимых опухолях эстроген стимулирует пролиферацию раковых клеток.
До наступления менопаузы основным источником эстрогенов являются яичники. В постменопаузальном периоде женские половые гормоны в основном вырабатываются жировыми клетками в результате превращения андрогенов в эстрогены. Этот процесс катализируется ферментом ароматазой, для подавления которого были синтезированы специальные лекарственные средства — ингибиторы ароматазы. Они эффективно снижают уровень эстрогенов в крови.
Порой опухоли, которые содержат рецепторы эстрогена (гормонозависимые), также могут быть HER2-позитивными. Поэтому такой рак молочной железы может одновременно лечиться с помощью гормональной терапии, а также таргетной терапии, направленной на блокировку белка HER2.
Гормональная терапия при метастазах рака молочной железы не используется в случае, если опухоль негативна по рецепторам эстрогена и рецептору прогестерона.
Гормональная терапия метастатического рака молочной железы в пременопаузе
Если вы находитесь в периоде пременопаузы, ваши яичники являются основными поставщиками эстрогена. Следовательно, в этой ситуации применимы две стратегии гормонотерапии: подавление выработки эстрогенов яичниками и блокировка рецепторов эстрогенов, расположенных на клетках злокачественной опухоли.
Тамоксифен — синтетический препарат, который по своей химической структуре является аналогом эстрогенов, входит в группу так называемых селективных модуляторов рецепторов эстрогена (selective estrogen receptor modulating agents, SERMs). Механизм действия препарата заключается в ингибировании действия эстрогенов путем конкурентного связывания с рецепторами эстрогенов, что приводит к торможению действия этих гормонов на чувствительные к ним клетки. Следствием этого в первую очередь является ингибирование роста эстрогензависимых опухолей.
Ингибиторы ароматазы считаются более эффективны, чем Тамоксифен. Однако без подавления яичников они не могут быть использованы в пременопаузе. Поэтому ваш врач может вам порекомендовать один из вариантов подавления яичников, чтобы снизить уровень эстрогенов в организме. Таким образом, открывается возможность применения ингибитора ароматазы.
Узнайте больше: Лечение рака молочной железы тамоксифеном
Это может быть достигнуто с помощью лекарств или хирургического вмешательства и приводит к так называемой медицинской менопаузе.
Золадекс (гозерелин)
Золадекс подавляет способность гонадотропинстимулирующего гормона, гормона, секретируемого гипофизом, который заставляет яичники вырабатывать эстроген.препараты для подавления функции яичников
Известный как антагонист гонадотропин-рилизинг-гормона, Zoladex вводится подкожно для подавления выработки эстрогена организмом.
Оофорэктомия (удаление яичника)
Оофорэктомия — хирургическая операция по удалению яичниковРеже, некоторые женщины выбирают удаление яичника с помощью процедуры, называемой овариэктомия. Эта операция представляет больший риск, чем золадекс, но в некоторых случаях она может быть предпочтительнее, например, у людей с предрасположенностью к раку яичников, а также к раку молочной железы.
После супрессивной терапии яичников с использованием любого метода женщины в пременопаузе могут получать те же лекарства, что и женщины в постменопаузе, или тамоксифен.
Гормональная терапия метастатического рака молочной железы в постменопаузе
После менопаузы основным источником эстрогена в организме является периферическое превращение андрогена в эстроген. Рак молочной железы в постменопаузе можно лечить тамоксифеном (чтобы блокировать связывание этого превращенного эстрогена с раковыми клетками), но ингибиторы ароматазы, по-видимому, более эффективны с меньшим количеством побочных эффектов.
Доступные ингибиторы ароматазы включают в себя:
- Аримидекс (анастрозол)
- Фемара (летрозол)
- Аромазин (экземестан)
Ингибиторы ароматазы могут использоваться отдельно или в комбинации с химиотерапевтическими препаратами. Например, комбинация Аромазина (экземестана) и Афинитор (эверолимуса). Всегда есть баланс при добавлении другого лекарства. Хотя комбинация может быть более эффективной, также наблюдается увеличение побочных эффектов.
Узнайте больше: Ингибиторов ароматазы — препараты, применяемые у женщин в постменопаузе с гормонозависимым раком молочной железы
Гормональная терапия при метастазах рака молочной железы — другие варианты
Если рак молочной железы продолжает расти или распространяться во время приема вышеуказанных лекарств, он обычно считается устойчивым к ним, и это почти всегда происходит в случаях метастатического рака молочной железы с течением времени.
Когда это произойдет, можно использовать несколько других гормональных препаратов, наиболее распространенным из которых является препарат под названием Фазлодекс (фулвестрант).
Фазлодекс вариант для женщин в постменопаузе, рак которых прогрессирует на тамоксифен или ингибитор ароматазы. Фазлодекс в настоящее время является единственным одобренным лекарством от рака молочной железы в категории, известной как селективные регуляторы эстрогенного рецептора (SERDs).
Гормональная терапия, которая используется реже, но может рассматриваться как лечение третьей или четвертой линии, включает:
- Фарестон (торемифен): Подобно тамоксифену, Fareston является агентом, модулирующим рецептор эстрогена. Иногда это может быть рассмотрено для женщин в постменопаузе с эстрогенным рецептор-положительным раком молочной железы, особенно для тех, кому не хватает фермента, который превращает тамоксифен в его активную форму в организме.
- Прогестины: Мегас (мегестрол) — это синтетическая форма прогестерона, которая иногда используется для людей с эстрогенным рецептор-положительным раком молочной железы, который становится резистентным к тамоксифену. 9 В прошлом он использовался чаще, до появления новых препаратов.
- Стероидные половые гормоны. Гормоны, такие как эстрогены и андрогены, могут иногда использоваться, когда другие гормональные препараты не помогли.
Мужчины с метастатическим раком молочной железы, который является гормональным рецептором, обычно получают тамоксифен.
Гормональная терапия при метастазах рака молочной железы — побочные эффекты
Негативные побочные эффекты следует учитывать при приеме любых лекарств. Обязательно обсудите возможные побочные эффекты гормональной терапии с врачом при принятии решения о лечении и сообщите о любых серьезных побочных эффектах после того, как вы начнете курс лечения.
Тамоксифен выполняет различные функции, имитируя действие эстрогена в одних частях тела и противодействуя ему в других.
Наиболее распространенные побочные эффекты тамоксифена включают в себя:
- Горячие вспышки
- Ломота в теле
Сочетание этих симптомов похоже на менопаузу. Тем не менее, эти боли в теле часто слабее, чем те, которые возникают в результате ингибиторов ароматазы.
Серьезные побочные эффекты включают повышенный риск:
- Сгустки крови в ногах (венозная тромбоэмболия), которые при отсутствии лечения могут вырваться и попасть в легкие (легочная эмболия)
- Маточное кровотечение (обычно после длительного использования)
- Развитие рака матки (обычно после длительного применения)
Ваши симптомы могут ухудшиться при приеме этого препарата, например, кожные метастазы становятся краснее или костные метастазы становятся более болезненными. Обычно это происходит в течение нескольких дней после начала приема лекарства и проходит через четыре-шесть недель.
Если это не помогает, возможно, вам придется отказаться от препарата. Серебряная подкладка заключается в том, что подобная вспышка реакции считается признаком того, что лекарство работает и будет эффективным. Золадекс также может вызывать аналогичную вспышечную реакцию.
Обратите внимание, что тамоксифен может вызвать:
- Нарушения функции печени
- малокровие
- Низкие тромбоциты
- Повышенный риск рака эндометрия
Наиболее частые побочные эффекты:
- Боли в теле, которые затрагивают до 50 процентов людей
- Потеря костной массы, которая может вызвать переломы даже без костных метастазов; Ваш врач может назначить анализы плотности костной ткани до и после лечения.
- Увеличьте риск сердечных заболеваний
Поскольку это антиэстрогенное лекарственное средство, большинство симптомов сходны с симптомами менопаузы, такими как тамоксифен и ингибиторы ароматазы.
Примерно 10% людей испытывают легкую тошноту, но в остальном это лекарство обычно хорошо переносится.
Этот препарат по существу вызывает вызванную медицинским путем менопаузу, и, таким образом, обычные симптомы менопаузы, такие как приливы и сухость влагалища, являются общими.
Как и в случае с тамоксифеном, у некоторых людей может возникнуть внезапная реакция (временное усиление симптомов рака) при первом запуске препарата.
Основными побочными эффектами, связанными с удалением яичников, являются, как и в случае медицинской гормональной терапии, нормальные симптомы, характерные для менопаузы. Вы также должны учитывать побочные эффекты и риски, связанные с хирургией в целом.
Оофорэктомия теперь может быть выполнена лапароскопически, с несколькими небольшими порезами на коже. Обычно это делается амбулаторно.
Статья по теме: Метастазы рака молочной железы — мониторинг заболевания
Список используемых источников:
Читайте также:

