Аппараты для лучевой терапии в онкологии

Что такое лучевая терапия?
Когда применяется лучевая терапия?
Лучевая терапия в онкологии играет важную роль. Этот вид терапии получают до 60 % всех больных злокачественными новообразованиями. Наравне с хирургическим и лекарственным методами лечения, лучевая терапия позволяет добиться при некоторых заболеваниях полного излечения, например, при лимфогранулематозе, раке кожи, раке предстательной железы, раке шейки матки, некоторых опухолях головы и шеи. Возможно, как применение лучевой терапии после операции по удалению опухоли, так и облучение до оперативного вмешательства. Многое зависит от расположения и типа новообразования.
При ряде заболеваний лучевая терапия и химиотерапия дополняют хирургическое лечение. Например, при злокачественных опухолях легкого, раке мочевого пузыря и др. Лучевая терапия рака молочной железы, прямой кишки также является важным компонентом комбинированного или комплексного лечения.
При ряде заболеваний лучевая терапия избавляет больного от мучительных симптомов заболевания. Например, при раке легкого лучевая терапия позволяет избавиться от боли, кровохарканья, затрудненного дыхания.
Лучевой метод используется и в лечении многих неопухолевых заболеваний. Сегодня этот вид лечения часто используется для лечения пяточных шпор, некоторых воспалительных заболеваний, при которых традиционные методы лечения оказываются неэффективными.
Методы лучевой терапии
Существующие способы облучения пациента можно разделить на две основные группы:
- дистанционное (наружное) облучение, когда источник излучения находится на расстоянии от больного;
- контактное облучение, при котором источники излучения размещаются либо в полости органа, либо внутри опухолевой ткани (соответственно внутриполостная и внутритканевая лучевая терапия).
Сочетание двух методов лечения лучевой терапией принято называть сочетанной лучевой терапией.
Виды лучевой терапии
- Конформная лучевая терапия (3D, IMRT, IGRT). При конформной лучевой терапии форма облучаемого объёма максимально приближена к форме опухоли. Здоровые ткани при этом почти не повреждаются.
- Лучевая терапия в сочетании с гипертермией. Повышение температуры внутри опухоли повышает эффективность лечения и улучшает его результаты.
- Брахитерапия рака предстательной железы и опухолей полости рта. В ходе брахитерапии источник излучения помещается непосредственно вглубь опухоли и мощно воздействует на неё.
Оборудование для лучевой терапии
Для контактной лучевой терапии, или, как её все чаще называют – брахитерапии, разработана серия шланговых аппаратов разной конструкции, позволяющих автоматизированным способом размещать источники вблизи опухоли и осуществлять её прицельное облучение. Этот вид лучевой терапии может применяться в качестве одного из методов лечения рака шейки матки и других новообразований.
Противопоказания к проведению лучевой терапии
острые соматические (заболевания внутренних органов) и инфекционные заболевания;
- соматические заболевания в стадии декомпенсации;
- тяжелые заболевания центральной нервной системы (эпилепсия, шизофрения и т.п.);
- прорастание опухолью крупных сосудов или её распад, угроза кровотечения из облучаемой области;
- анемия, лейкопения, тромбоцитопения;
- раковая кахексия (истощение организма);
- генерализация опухолевого процесса, выраженный синдром опухолевой интоксикации.
Как проводится лечение?
Лучевая терапия всегда начинается с планирования. Для этого выполняется ряд исследований (рентгенография, УЗИ, компьютерная томография, магнитно-резонансная томография и др.), при которых определяется точное месторасположение новообразования.
Врач-радиолог до начала лучевого лечения внимательно изучает историю заболевания, результаты проведенного обследования, осматривает пациента. На основании имеющихся данных врач принимает решение о способе лечения больного и обязательно рассказывает пациенту о планируемом лечении, риске возникновения побочных эффектов и мерах по их профилактике.
Ионизирующее излучение является небезопасным для здоровых тканей. Поэтому облучение проводится за несколько сеансов. Количество сеансов определяет врач-радиолог.
Во время сеанса лучевой терапии пациент не испытывает боли и каких-либо других ощущений. Облучение проходит в специально оборудованном помещении. Медицинская сестра помогает больному занять положение, которое было выбрано во время планирования (разметки). С помощью специальных блоков защищают от облучения здоровые органы и ткани. После этого начинается сеанс, который длится от одной до нескольких минут. Врач и медицинская сестра наблюдают за процедурой из кабинета, расположенного рядом с помещением, где проводится облучение.
Как правило, курс дистанционной лучевой терапии длится от 4 до 7 недель (без учета возможных перерывов в лечении). Внутриполостное (и внутритканевое) облучение занимает меньше времени. Существует методика, при которой за один сеанс дают большую дозу, при этом общая доза за курс меньше (при равном эффекте). В таких случаях облучение проводится в течение 3-5 дней. Иногда курс лучевой терапии можно провести амбулаторно, без госпитализации и круглосуточного пребывания в больнице.
Побочные эффекты лучевой терапии
При проведении и после лучевой терапии могут наблюдаться побочные эффекты в виде лучевых реакций и повреждения тканей, находящихся рядом с опухолью. Лучевыми реакциями называют временные, обычно самостоятельно проходящие функциональные изменения в тканях, окружающих опухоль. Степень выраженности побочных эффектов лучевой терапии зависит от локализации облучаемой опухоли, её размеров, методики облучения, общего состояния пациента (наличия или отсутствия сопутствующих заболеваний).
Лучевые реакции могут быть общими и местными. Общая лучевая реакция – это реакция всего организма больного на лечение, проявляющаяся:
- ухудшением общего состояния (кратковременным повышением температуры тела, слабостью, головокружением);
- нарушением функции желудочно-кишечного тракта (снижением аппетита, тошнотой, рвотой, диарей);
- нарушением сердечно-сосудистой системы (тахикардией, болями за грудиной);
- гемопоэтическими нарушениями (лейкопенией, нейтропенией, лимфопенией и др.).
Общие лучевые реакции возникают, как правило, при облучении больших объёмов тканей и имеют обратимый характер (прекращаются по окончании лечения). Например, при проведение лучевой терапии рака простаты может спровоцировать воспаление мочевого пузыря и прямой кишки.
В большинстве случаев все вышеуказанные изменения проходящие, при адекватной и своевременной коррекции имеют обратимый характер и не являются причиной прекращения курса лучевой терапии. Необходимо тщательное выполнение всех рекомендаций врача-радиолога в процессе лечения и после его окончания. Помните, что лучше предупредить осложнение, чем его лечить.
Тел. Колл-центра +7 495 – 150 – 11 - 22
Позвоните нам сегодня, чтобы мы смогли Вам помочь!
![]()
НМИЦ онкологии им. Петрова: Из-за рака пациенты теряют лицо![]()
Петербургский врач: Польза МРТ с контрастом превышает вред от возможных осложнений![]()
Молчание поневоле. Как помочь, если голос пропал
В комплексной терапии онкологических заболеваний используются 4 метода лечения: хирургия, химиотерапия, лучевая терапия, иммунотерапия. Сейчас самое большое финансирование и все внимание брошены на лекарственную терапию. Но со следующего года грядут изменения и в лучевой. А это для Петербурга – самое больное место.
Как говорит профессор Сергей Новиков, заведующий отделением лучевой терапии НМИЦ онкологии им Петрова, за последнее десятилетие лучевая терапия сделала большой рывок и ее стремительное развитие не останавливается. Появились новые аппараты, новые технологии, а с ними — новая идеология лучевой терапии.
- Сергей Николаевич, правда ли, что новые технологии в лучевой терапии когда-то заменят хирургию?
- Во многих случаях это уже происходит. Например, только что мы составляли план лечения пациента с ранним немелкоклеточным раком легкого. У него нет изменений в лимфоузлах, нет метастазирования. Но его невозможно прооперировать из-за сопутствующих заболеваний (перенес инфаркт, инсульт), так что операция угрожает жизни. В этой фактически патовой ситуации лучевая терапия позволяет провести радикальное лечение - мы можем подвести чрезвычайно высокую дозу излучения на очень маленький объем тканей. И это приведет не к продлению жизни, а именно к излечению. Опухоли объемом 1-5 см мы можем облучить, избежав при этом серьезного повреждения окружающих тканей. Это называется стереотаксическая лучевая терапия или радиохирургия.
- Вы имеете в виду лечение с помощью гамма-ножа и кибер-ножа?
- Эти технологии тоже относятся к стереотаксической лучевой терапии — гамма-нож применяют для лечения новообразований на головном мозге, а кибер-нож - для направленного радиотерапевтического воздействия на экстракраниальные опухоли (расположенные вне головного мозга). Но сейчас активно развиваются технологии радиохирургии и стереотаксической лучевой терапии на линейных ускорителях. Их преимущество в том, что это универсальные приборы: на одном аппарате может выполняться - стерео-, радио- или классическая лучевая терапия с избирательным воздействием на опухоль (обычная или 3D-конформная). У нас уже три таких аппарата, каждый из них имеет свои преимущества, а в целом умеют все.
- Для лечения какого вида рака они предназначаются, что умеют?
- Легче перечислить, что не умеют — не умеют облучать очень много очагов в головном мозге одномоментно, в отличие от гамма ножа. Но такая ситуация — редкость, а главное, пока нет доказательств целесообразности такой агрессивной терапии, она не продлевает жизнь.
С другой стороны, эти аппараты могут делать все в области высокотехнологичного облучения, когда требуется радиохирургия: используются в комплексном лечении новообразований в головном мозге, локализованных процессах в легких (немелкоклеточный рак), метастатических поражений легких, печени, надпочечников, костей, мягких тканей и т. д. Благодаря высокой точности направления воздействия, они незаменимы в лечении злокачественных новообразований головы и шеи. Например, опухоль языка — очень тяжелая патология, лечить ее хирургически или невозможно, или очень сложно. После операции пациента берем мы. Активно используем методы брахитерапии и стереотаксической лучевой терапии при раке предстательной железы.
Онкологи сегодня говорят, что иммунотерапия перевернула наше сознание в лечении некоторых видов рака. Но забывают упомянуть, что сочетание иммунотерапии с некоторыми видами лучевой терапии увеличивает эффективность практически в два раза. Поэтому трудно встретить протоколы лечения, в которых рекомендована иммунотерапия без лучевой терапии.
— Да, но для ослабленных и пожилых пациентов мы используем стереотаксис, потому что это неинвазивное - щадящее лечение. С моей точки зрения, пациенты с этим диагнозом должны получать прежде всего лучевую терапию, хотя на протяжении многих лет считалось, что главный способ лечения рака предстательной железы – хирургия. Но простатэктомия сопряжена с риском для жизни, с осложнениями — каждый пятый после хирургического вмешательства страдает недержанием мочи, у 70% перенесших операцию возникает нарушение эректильной функции. Эффективность хирургии, брахитерапии и стереотаксической лучевой терапии с точки зрения борьбы с опухолью одинаковая, в некоторых случаях лучевое лечение даже более результативно. Но недержание мочи после него – редкость, всего 1-2% случаев в сравнении с 20% после хирургического удаления предстательной железы и тут даже использование роботизированных хирургических методов не помогает улучшить результаты. Эректильная дисфункция, к сожалению, может возникнуть и после проведения лучевого лечения - у 30-40% пациентов мы отмечаем снижение эректильной функции. Но, к счастью, это существенно меньше 70-80% после хирургического лечения.
- Однако по-прежнему распространен миф о том, что лучевая терапия опасна, потому что может спровоцировать развитие лучевой болезни.
- Если под лучевой болезнью мы подразумеваем то, что происходит с организмом человека, оказавшегося в эпицентре взрыва ядерной бомбы, то даже в 1970 годы лучевая терапия ее не провоцировала. Другое дело, что когда использовали большие поля для облучения, это вызывало разного рода токсичность — развивались осложнения со стороны органов дыхательной или кроветворной системы, например. Я начал работать в 1980-е, и уже тогда были разработаны методы, которые позволяли избегать фатальной или очень серьезной токсичности. Хотя какие-то неприятности от лучевой терапии были, есть и будут. Например, если мы подводим очень высокие дозы в область опухоли предстательной железы, мы можем вызвать повреждения прямой кишки, если облучаем опухоль в легких, — повреждения легких, в мозге — здоровые ткани мозга. И иногда вынуждены рисковать, потому что понимаем: другой возможности спасти человека нет. Да, бывает, лучевая терапия балансирует между добром и злом, но зачастую альтернативы нет. Например, при метастазах в головном мозге — это пациенты, которым часто нейрохирурги уже помочь не могут, возможности химиотерапии, нередко, исчерпаны. А лучевая терапия у таких пациентов ассоциируется с 20-30% риском возникновения лучевого некроза. Но в оставшихся 70-80% случаев есть шанс, что мы поможем пациенту преодолеть на определенное время его проблемы.
- Стереотаксическая лучевая терапия – не самая распространенная технология в Петербурге, возможности для ее применения есть только у двух федеральных специализированных клиник и у одной негосударственной. Часто ли она востребована?
- Когда у нас только появился первый аппарат для стереотаксиса, мы пролечили всего 12 пациентов. Это была, можно сказать, эксклюзивная методика - все отделение собиралось смотреть. А в этом году стереотаксическую лучевую терапию получили уже 350 пациентов, то есть около 20% получивших лучевое лечение в НМИЦ онкологии им. Н.Н. Петрова.
- Парадокс: при том, что в Петербурге можно получить самые современные виды лучевой терапии, петербуржцев направляют на лучевое лечение в клиники, в которых их нет. Более того, на 2020 год из средств петербургского фонда ОМС выделяется 1 млрд рублей на 3D-конформную терапию, выполнять которую в городских специализированных клиниках, можно сказать, не на чем.
- Только кто и на каком оборудовании будет ее проводить? В городских медицинских учреждениях нет современных ускорителей. Да и старые регулярно выходят из строя.
- Мы сражаемся за то, чтобы петербуржцы могли получать современное эффективное лучевое лечение. Но НМИЦ им. Петрова не может принять всех, хотя пока мы никому не отказывали.
Что касается стереотаксической лучевой терапии, которая есть в единичных клиниках Петербурга, мы примерно на 30% увеличиваем объемы ежегодно. И готовы взять на себя столько пациентов, сколько нужно. Поскольку у нас стереотаксическая лучевая терапия проводится на тех же аппаратах, на которых проводится и классическая, чтобы освободить их от загрузки стандартной 3D-конформной лучевой терапией, мы приобрели еще один линейный ускоритель, на котором и будем ее выполнять.
- В Городском онкологическом центре в Песочном и в Городском онкологическом диспансере недостаточно современных линейных ускорителей, на которых можно проводить 3D-конформную лучевую терапию. И мне кажется, что на аппаратах, которые там есть, невозможно использовать сложные технологии, например, радиохирургическое лечение и стереотаксическую лучевую терапию. Поэтому важно, чтобы руководители городской онкологической службы наладили сотрудничество с федеральными учреждениями, частными клиниками, которые готовы и могут помочь петербуржцам.
Конечно, нужно обновлять парк оборудования. Потому что на аппаратах 2001-2005 года, которые морально устарели, а многие уже сняты с производства, можно выполнять паллиативную лучевую терапию, использовать простые методики облучения, но современные достижения радиационной онкологии на них недоступны.
У городских клиник есть рентген-терапия, которой, кстати, у нас нет, в онкодиспансере есть интраоперационный ускоритель, которого больше нет ни у кого в нашем городе.
Задача - дать пациентам возможность получать все существующие на сегодня виды лучевой терапии по показаниям: простую, когда ее достаточно, сложную, когда она необходима. Понимаете, если у мужчины выявили рак предстательной железы, и он попадает в учреждение, где нет аппаратов для проведения стереотаксической лучевой терапии, нет брахитерапии, то, на мой взгляд, он адекватной помощи в этих учреждениях получить не сможет. Потому что если будут подведены достаточно большие дозы на устаревших линейных ускорителях, серьезно вырастут осложнения, если дозы будут меньше, чем необходимы для борьбы с опухолью, то лечение не будет эффективным. Да, часть пациентов выздоровеет, но меньше, чем тот процент, который мог бы и должен был выздороветь. А пациенты, которым можно провести более простую лучевую терапию, должны лечиться там, где она есть, - нет смысла направлять их в НМИЦ онкологии.
То есть Петербургу нужна грамотная маршрутизация. Но это очень болезненный вопрос для городских властей. Тут все должны понимать, что его нужно решать, и мы к этому готовы.
- До сих пор федеральные клиники лечили, конечно, петербуржцев, но – по федеральным квотам. И объясняли это тем, что тарифы ОМС на лучевую терапию слишком малы. А количество квот всегда ограничено.
- Те тарифы, что действуют в системе ОМС сейчас, рассчитаны на ту простую лучевую терапию, что есть в городских клиниках. Мы работаем в рамках программы ВМП, потому что используем технологии, которых нет в городских медучреждениях. Программа ВМП рассчитана на то, что люди могут получить помощь там, где ее могут оказать. И ее финансирование было достаточным, чтобы применять в лечении сложные технологии: закупать дорогие расходники, заниматься техническим обслуживанием оборудования. Теперь, насколько я знаю, запланированные на 2020 год тарифы петербургского фонда ОМС эквивалентны тарифам, действующим в программе ВМП.
- На 1 миллиард рублей запланировано 4 тысячи курсов 3Д-конформной терапии. 4 тысячи пациентов ее получат – это много или мало?
- Немало, но 4 тысячи курсов это не 4 тысячи пациентов. Потому что некоторым приходится проводить их повторно. Например, прошла женщина курс терапии по поводу опухоли в молочной железе, но обнаружился метастаз в лимфоузле или в другом месте, его тоже нужно облучать. Я думаю, что это 3-3,5 тысячи пациентов.
Для сравнения: в НМИЦ онкологии в год лучевую терапию получают 2 тысячи пациентов. Приблизительно столько же - РНЦРХТ им. Гранова. Эту помощь могут оказывать в частных клиниках МИБС и есть один современный ускоритель и аппараты для брахитерапии в ПСПбГМУ им. Павлова. То есть в городе можно выполнять лучевую терапию любой сложности. Важно, чтобы средства были потрачены на ее эффективные методы.
- Люди по-прежнему едут за рубеж, чтобы получить лечение радиоактивным йодом. Почему в России оно до сих пор дефицитное, а в Петербурге его и вовсе нет?
- Это не сложная технология, но для ее применения у нас действуют очень строгие требования, вплоть до строительства специальных очистных сооружений. Чтобы выполнить все, что нужно по нормативам, надо выиграть большое сражение, но сначала вложить в его подготовку огромные деньги. Сейчас предпринимаются усилия, чтобы сделать наше законодательство более демократичным — смягчить требования для применения этой технологии. А мы уже фактически готовы к тому, чтобы использовать ее, даже обсуждаем возможность открытия коек для пациентов, нуждающихся в терапии радиоактивными источниками. Эта терапия — это огромная перспектива на будущее.
Сегодня это, в первую очередь, радиойодотерапия или паллиативная терапия при метастазах в кости - она позволяет сделать комфортной жизнь человека, страдающего от болевого синдрома. Это то, к чему мы уже сегодня готовы. Но есть еще много методик использования радиоактивных источников. Например, лечение препаратами, мечеными лютецием, — это широкий круг препаратов, которые избирательно накапливаются в опухоли и уничтожают ее. То есть это один из вариантов целенаправленной терапии.
- Магической пули, которая бьет только в цель пока нет. И при таргетной терапии избирательность условная, и при стереотаксическом — какая-то доза облучения все же приходится на здоровые ткани и они могут пострадать. Но все же воздействие современных лучей и химиотерапии, действительно, выигрывает в эффективности и точности направленного действия.
- Что нужно сделать, чтобы в лучевой терапии новые технологии появлялись не только в федеральных клиниках? Закупать новые аппараты?
- Я счастлив, что лучевая терапия в нашей стране начала осознано развиваться. Но это огромная машина, она не сдвинется с места мгновенно. Чтобы ее раскрутить, нужно потратить много сил и времени, грамотно использовать финансовые вложения.
То есть миллиарды сначала должны вкладываться не в оборудование, а в людей. Их нужно учить, в том числе за границей, нужно обеспечить их достойным заработком. А когда будут люди, способные работать на современном оборудовании, тогда и нужно его покупать.
- Сколько всего аппаратов для лучевой терапии работают у вас?
- Четыре ускорителя - от самого простого до самого сложного, и еще два аппарата – для брахитерапии. Плюс много компьютерных планирующих систем, задача которых сделать лучевую терапию максимально точной.
Мы не станем изучать искусственный интеллект, а обратим внимание на историю, которая привела к трагическим последствиям. Источником всех бед в ней стал именно человек, машина была лишь инструментом.
Содержание
Аппарат для лечения агрессивных форм рака
Лучевую терапию применяют давно и достаточно успешно, инженеры и медики совершенствуют технологии и оборудование, которое призвано помочь в борьбе со злокачественными образованиями. То и дело появляются революционные решения — сегодня они могут казаться устаревшими, но 30—40 лет назад считались прорывом.
В конце 1970-х годов канадское правительство инициировало разработку полностью компьютеризированной системы Therac-25 — аппарата лучевой терапии для лечения агрессивных форм рака, более эффективного с медицинской и экономической точки зрения, нежели предшественники Therac-6 и Therac-20.
Медицинский линейный ускоритель мог работать в двух режимах: с небольшой интенсивностью излучения и высокой (это упрощенное описание) в зависимости от того, на какой глубине в тканях находился очаг. Одним из ключевых отличий Therac-25 от Therac-20 стал переход на полностью программное управление.

Потенциальных покупателей системы именно этим и пытались заинтересовать: ведь вместо дорогостоящих сенсоров и аппаратных решений для защиты применялось сравнительно дешевое ПО. В прошлых же версиях системы для предотвращения неверных конфигураций применялись всевозможные ограничители, датчики, сенсоры и механизмы, обеспечивающие безопасность процедуры.
Оптимизация разработки
Поставки Therac-25 в медучреждения США и Канады начались в 1983 году, и первое время информации о сбоях не было. Системе было несложно пройти все инстанции и получить разрешения от регуляторов — в машине применялось уже существующее ПО, поэтому его пропустили без особых вопросов. В то время около 94% медицинского оборудования попадало на рынок именно таким образом, что упрощало, ускоряло и удешевляло вывод новых устройств. А как все это работало, вопрос другой.

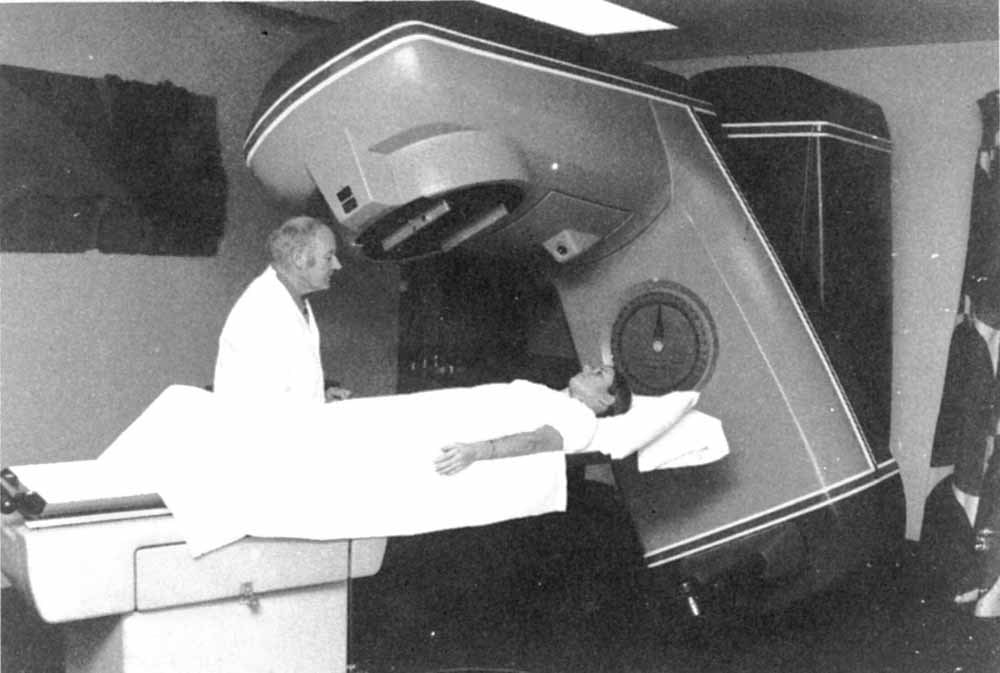
Позже оказалось, что в ПО существовала уйма критических ошибок. Одну из них называют race condition. В случае с Therac-25 использовалась одна и та же переменная для двух команд, которые могли выполняться в произвольном порядке, что для описываемого аппарата неприемлемо.
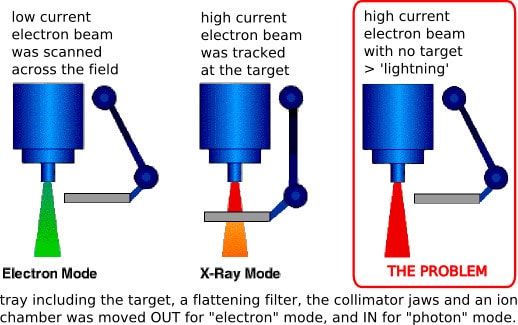
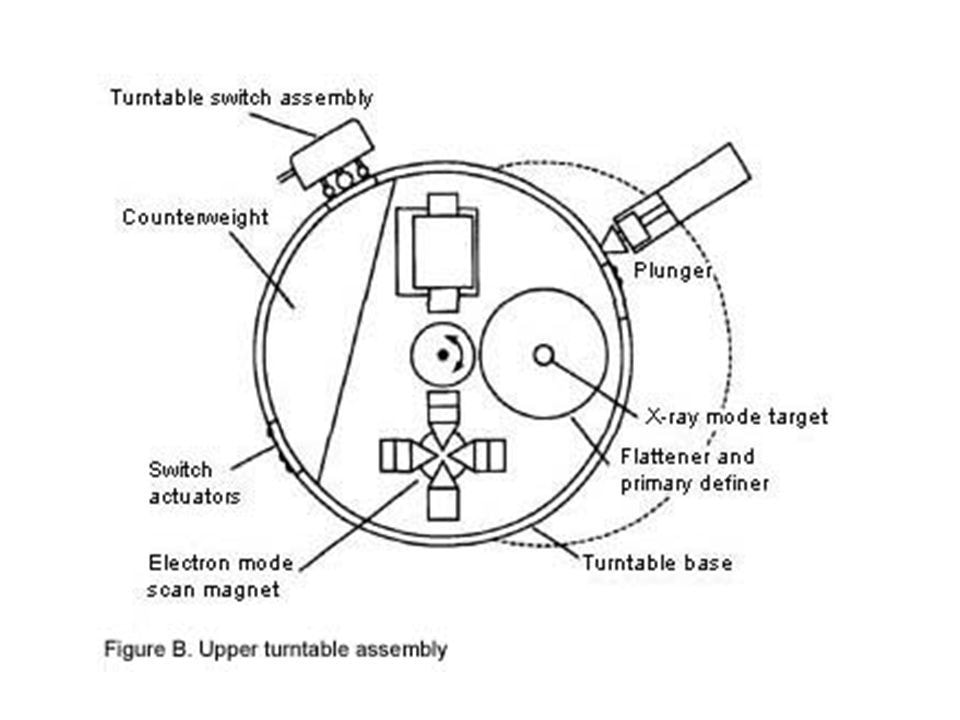
Были и другие программные недочеты: некорректные операции с нулем приводили к выводу мощности излучения на максимум, а неверно описанная переменная генерировала неправильное положение поворотного диска с набором инструментов (для разных режимов работы и настройки) 1 раз из 256, что могло привести к многократно завышенному уровню облучения.

Аппарат продолжил работу, а оператор, приняв уведомление за индикацию низкой дозы, повторила процесс облучения. Так как пациент находился в защищенном помещении вне поля зрения сотрудника, а предусмотренные системы связи были неисправными, оператор не знала, что человек за стеной скорчился от боли. Через некоторое время мужчина вскочил со стола и бросился к двери, пытаясь привлечь внимание человека за стеной.

Второй фатальный случай произошел в том же медицинском учреждении с участием того же оператора спустя месяц после предыдущего. Некоторые источники описывают техника как поднаторевшую во вводе команд в Therac-25 сотрудницу, и якобы именно стремительность ее действий стала одной из причин сбоев.
На этот раз интерком работал и оператор услышала стоны пациента, чье лицо оказалось под ударом радиации. Спасти человека не удалось — мужчина впал в кому и умер спустя три недели после инцидента.
Отрицание
Три других случая завершились чуть менее трагично. Самое странное, что все они произошли до трех фатальных инцидентов, однако действенных мер предпринято не было — какие-то изменения по требованию экспертов вносились, но система была настолько несовершенной, что результата это не принесло.
В июне 1985 года 61-летняя женщина проходила терапию после удаления раковой опухоли в груди. После сеанса лучевой терапии с использованием аппарата Therac-25 ее плечо и рука оказались парализованы, а грудь пришлось удалить. Канадская государственная корпорация AECL, которая выступала заказчиком ускорителей, отказалась признать вину.
Второй инцидент произошел спустя примерно месяц в другом медучреждении. На этот раз под излучателем оказалась 40-летняя пациентка. Во время сеанса машина сообщила о нулевой интенсивности излучения. Оператор ставил систему на паузу и возобновлял процедуру — аппарат был направлен в область таза. Это повторилось пять раз, потому что Therac-25 продолжал выдавать одно и то же уведомление — нулевая доза.

Признать ошибку и остановить работу
В 1987 году американский и канадский регуляторы потребовали остановить работу всех Therac-25 (их насчитывалось чуть менее полутора десятков в США и Канаде) до выяснения обстоятельств. За полгода AECL составила план и утвердила его, внедрив аппаратные системы защиты и доработав ПО. Оставшиеся в живых жертвы и их родственники подали иски, однако все вопросы были улажены сторонами в досудебном порядке.
Ну а история Therac-25 стала уроком о том, как нельзя проектировать системы с повышенными требованиями к безопасности.

Лучевая терапия — это один из ведущих методов противоопухолевого лечения, основанный на использовании ионизирующего излучения. Может применяться как самостоятельный вид терапии, так и в рамках комбинированного/комплексного лечения (совместно с другими методами), в качестве радикальной, нео- и адъювантной, консолидирующей, профилактической и паллиативной терапии.
- Виды лучевой терапии
- Этапы лучевой терапии
- Побочные эффекты лучевой терапии
- Химиолучевая терапия

Виды лучевой терапии
Уже несколько десятилетий человечество изучает воздействие ионизирующего излучение на организм человека. При этом акцентируется внимание как на положительном, так и отрицательном эффекте, возникающем при его применении. Разрабатываются новые методы, которые позволяют добиваться максимального лечебного эффекта при снижении отрицательного действия на организм. Улучшается оборудование для проведения лучевой терапии, появляются новые технологии облучения.
Сейчас классификация методов лучевой терапии довольно обширна. Мы остановимся только на самых распространенных методиках.
При контактной лучевой терапии источник излучения вводится непосредственно в опухоль или прилегает к ее поверхности. Это позволяет прицельно облучать новообразование с минимумом воздействия на окружающие его ткани.
К контактным видам лучевой терапии относятся:
- Аппликационная лучевая терапия. Применяется при лечении поверхностно расположенных опухолей, например, новообразований кожи, слизистых оболочек гениталий. В этом случае используются индивидуально изготовленные аппликаторы, которые накладываются непосредственно на поверхность новообразования.
- Внутриполостная лучевая терапия. Источник ионизирующего излучения вводится в просвет полого органа, например, в пищевод, мочевой пузырь, прямую кишку, полость матки или влагалища. Для облучения используются специальные аппликаторы (их называют эндостатами), которые заполняются радионуклидами.
- Внутритканевое облучение. Источник ионизирующего излучения вводится непосредственно в ткань опухоли. Для этого используются интростаты, которые могут иметь вид игл, шариков, трубочек, заполненных источником излучения.
Кроме того, существует такой вид лечения, как радионуклидная терапия. В этом случае используются открытые источники излучения в виде растворов радионуклидов (радиофармацевтический препарат — РФП), которые при попадании в организм прицельно накапливаются в опухолевых очагах и уничтожают их. Чаще всего РФП вводится внутривенно. Наибольшее распространение получили следующие виды радионуклидной терапии:
- Терапия радиоактивным йодом. Используется для лечения ряда видов рака щитовидной железы, поскольку йод избирательно накапливается в тиреоидной ткани.
- Применение остеотропных РФП используется для лечения метастазов в костях или костных опухолей.
- Радиоиммунотерапия — радионуклиды присоединяют на моноклональные антитела, чтобы добиться прицельного воздействия на опухолевую ткань.
При дистанционной лучевой терапии источник излучения находится на расстоянии от тела пациента, при этом на пути его прохождения могут лежать здоровые ткани, которые в процессе проведения терапии также подвергаются облучению, что приводит к развитию осложнений разной степени выраженности. Чтобы их минимизировать, разрабатываются различные технологии, позволяющие сконцентрировать максимальную дозу ионизирующего излучения непосредственно на в мишени (опухоли). С данной целью используются:
- Короткофокусная рентгенотерапия. При облучении используется рентгеновское излучение малой и средней мощности, которое способно проникать в ткани на глубину до 12 мм. Метод назван так из-за того, что источник располагается на коротком расстоянии от облучаемой поверхности. Таким способом лечат неглубокие опухоли кожи, вульвы, конъюнктивы и век, ротовой полости.
- Гамма-терапия. Этот вид излучения имеет большую проникающую способность, поэтому может использоваться для лечения более глубоко расположенных опухолей, нежели рентген-терапия. Однако сохраняющаяся большая нагрузка на окружающие органы и ткани приводят к ограничению возможности использования данного метода в современной онкологии.
- Фотонная терапия. Именно этим видом излучения проводится лучевое лечение большинства онкологических пациентов в современном мире. Достаточно высокая проникающая способность в сочетании с высокотехнологичными способами подведения дозы (IMRT и VMAT), достаточно совершенные системы планирования позволяют очень эффективно использовать этот вид излучения для лечения пациентов с приемлемыми показателями токсичности.
- Применение корпускулярного излучения (электроны, протоны, нейтроны). Эти элементарные ядерные частицы получают на циклотронах или линейных ускорителях. Электронное излучение используют для лечения неглубоких опухолей. Большие надежды возлагаются на протонную терапию, с помощью которой можно максимально прицельно подводить высокие дозы излучения к глубоко расположенным опухолям при минимальном повреждении здоровых тканей за счет выделения радиационной дозы на определённом отрезке пробега частиц, однако пока эти виды излучения играют сравнительно небольшую роль в лечении онкологических заболевания из-за своей высокой стоимости и ряда не до конца решённых технологических аспектов реализации метода.
Этапы лучевой терапии
Весь процесс проведения лучевой терапии делят на три этапа:
- Предлучевая подготовка (КТ-симуляция), этап выбора объёмов облучения и критических структур, этап дозиметрического планирования, верификации плана лучевой терапии.
- Этап облучения.
- Постлучевой этап.
Как правило, этап планирования занимает несколько дней. В это время проводятся дополнительные исследования, которые призваны дать возможность врачу более точно оценить границы опухоли, а также состояние окружающих ее тканей. Это может повлиять на выбор вида лучевой терапии, режима фракционирования, разовой и суммарной очаговых доз. Основой же данного этапа является выполнение так называемой КТ-симуляции, то есть компьютерной томографии необходимого объёма с определёнными параметрами и в определённом положении тела пациента. Во время КТ-симуляции на кожу пациента и/или его индивидуальные фиксирующие устройства наносятся специальные метки, призванные помочь правильно укладывать пациента в дальнейшем, а также облегчить задачу навигации по время проведения сеансов облучения.
Затем врач-радиотерапевт рисует объёмы облучения и критических структур (тех, на которые будет предписано ограничение дозы) на полученных срезах КТ с учётом данных других диагностических модальностей (МРТ, ПЭТ). Далее формируется задача для медицинского физика, включающая определение доз, которые должны быть подведены к мишени, мишеням или отдельным её частям, а также тех, которые не должны быть превышены в объёмах здоровых органов и тканей. Медицинский физик разрабатывает дозиметрический план в соответствии с заданными параметрами, при соблюдении которых и успешной верификации данного плана на фантоме, можно считать пациента готовым к лучевой терапии.
На этапе подготовки к лучевой терапии пациенту рекомендуется придерживаться нескольких правил:
- Отказаться от средств, раздражающих кожу.
- Если на коже в месте воздействия имеются повреждения или элементы сыпи, следует проконсультироваться с врачом.
- Если предполагается лучевая терапия в челюстно-лицевой области, требуется санация полости рта.
- Воздержаться от загара.
- Главное правило на любом этапе: обсудить все нюансы предстоящих подготовки и лечения с лечащим врачом-радиотерапевтом и строго придерживаться полученных рекомендаций!
Проведение этапа облучения будет зависеть от выбранного метода лучевой терапии.
Проведение дистанционной лучевой терапии
Продолжительность курса дистанционной лучевой терапии зависит от выбранного режима фракционирования, а также цели лечения. Паллиативные курсы, как правило, короче неоадъювантных и адъювантных, а те, в свою очередь, менее продолжительны, чем радикальные. Однако подведение радикальной дозы возможно и за один-несколько сеансов в зависимости от клинической ситуации. В таком случае курс дистанционной лучевой терапии называется стереотаксической радиотерапией или радиохирургией. Варьирует и кратность сеансов в день и в неделю: чаще всего используются схемы с пятью сеансами в неделю, однако могут быть предложены и 2-3 сеанса в день (гиперфракционирование) и схемы с 1-4 и 6 сеансами в неделю.
Во время облучения пациент в подавляющем большинстве случаев располагается лежа на столе специальной установки. Крайне необходимо соблюдать полную неподвижность во время сеанса облучения. Для достижения этого могут использоваться специальные фиксирующие устройства и системы иммобилизации.
Перед тем как включить установку, медперсонал покидает помещение, и дальнейшее наблюдение осуществляется через мониторы или окно. Общение с пациентом осуществляется по громкой связи. Во время выполнения сеанса, части аппарата и стол с пациентом совершают движения по заданной траектории. Это может создавать шум и беспокойство у больного. Однако бояться этого не стоит, поскольку вся процедура контролируется.
Сам сеанс лучевой терапии может длиться как 5-10, так и 60-120 минут, чаще — 15-30 минут. Само воздействие ионизирующего излучения не вызывает никаких физических ощущений. Однако в случае ухудшения самочувствия пациента во время сеанса (выраженной боли, судороги, приступа тошноты, паники), следует позвать медицинский персонал заранее оговоренным способом; установку сразу отключат и окажут необходимую помощь.
Контактная лучевая терапия (брахитерапия)
Брахитерапия проводится в несколько этапов:
- Введение в облучаемую зону неактивных проводников — устройств, в которые затем имплантируют источник ионизирующего излучения. При внутриполостной лучевой терапии используются приспособления, называемые эндостатами. Их устанавливают непосредственно в полость облучаемого органа и рядом с ним. При внутритканевой лучевой терапии используются интростаты, которые устанавливаются непосредственно в ткань опухоли по заранее просчитанной схеме. Для контроля их установки, как правило, используются рентгенологические снимки.
- Перемещение источника излучения из хранилища в интро- и эндостаты, которые будут облучать опухолевую ткань. Время облучения и особенности поведения пациента будут зависеть от вида брахитерапии и используемого оборудования. Например, при внутритканевой терапии, после установки источника ионизирующего излучения пациент может покинуть клинику и прийти на повторную процедуру через рекомендуемый промежуток времени. Весь этот период в его организме будет находиться интростат с радионуклидами, которые будут облучать опухоль.
Проведение внутриполостной брахитерапии будет зависеть от используемых установок, которые бывают двух типов:
- Установки низкой мощности дозы. В этом случае один сеанс облучения длится около 2-х суток. Под наркозом имплантируются эндостаты. После контроля правильности их установки и введения радионуклидов, пациент переводится в специальное помещение, где должен будет находиться все время, пока длится процедура, соблюдая строгий постельный режим. Разрешается только немного поворачиваться на бок. Вставать категорически запрещено.
- Установки высокой мощности дозы. Время облучения составляет несколько минут. Для установки эндостатов наркоза не требуется. Но во время процедуры все равно необходимо лежать абсолютно неподвижно. Внутриполостная лучевая терапия установкой высокой мощности проводится несколькими сеансами с интервалами от одного дня до одной недели.
При радионуклидной терапии пациент принимает радиофармпрепараты внутрь в виде жидкого раствора, капсул или инъекций. После этого он помещается в специальную палату, имеющую изолированную канализацию и вентиляцию. По истечении определенного срока, когда мощность дозы снизится до приемлемого уровня, проводится радиологический контроль, пациент принимает душ и переодевается в чистую одежду. Для контроля результатов лечения проводится сцинтиграфия, после чего можно покинуть клинику.
Лучевая терапия является серьезным стрессом для организма. У многих пациентов в этот период ухудшается самочувствие. Чтобы его минимизировать рекомендуется придерживаться следующих правил:
- Больше отдыхать. Минимизируйте физическую и интеллектуальную нагрузку. Ложитесь спать, когда почувствуете в этом необходимость, даже если она возникла в течение дня.
- Постарайтесь сбалансировано и полноценно питаться.
- Откажитесь на время проведения терапии от вредных привычек.
- Избегайте плотной обтягивающей одежды, которая бы могла травмировать кожу.
- Следите за состоянием кожи в месте облучения. Не трите и не расчесывайте ее, используйте средства гигиены, которые вам порекомендует врач.
- Защищайте кожу от воздействия солнечных лучей — используйте одежду и головные уборы с широкими полями.

Побочные эффекты лучевой терапии
Лучевая терапия, как и другие методы противоопухолевого лечения, вызывает ряд осложнений. Они могут быть общими или местными, острыми или хроническими.
Острые (ранние) побочные эффекты развиваются во время проведения радиотерапии и в ближайшие недели после неё, а поздние (хронические) лучевые повреждения — через несколько месяцев и даже лет после ее окончания.
Угнетенное эмоциональное состояние
Подавляющее большинство пациентов, проходящих лечение по поводу злокачественного новообразования, испытывают тревожность, страх, эмоциональное напряжение, тоску и даже депрессию. По мере улучшения общего состояния, эти симптомы стихают. Чтобы облегчить их, рекомендуется чаще общаться с близкими людьми, принимать участие в жизни окружающих. При необходимости рекомендуется обратиться к психологу.
Чувство усталости
Чувство усталости начинает нарастать через 2-3 недели от начала терапии. На это время рекомендуется оптимизировать свой режим дня, чтобы не подвергаться ненужным нагрузкам. В то же время нельзя полностью отстраняться от дел, чтобы не впасть в депрессию.
Изменение крови
При необходимости облучения больших зон, под воздействие радиации попадает костный мозг. Это в свою очередь приводит к снижению уровня форменных элементов крови и развитию анемии, повышению риска кровотечения и развития инфекций. Если изменения выражены сильно, может потребоваться перерыв в облучении. В ряде случаев могут назначать препараты, стимулирующие гемопоэз (кроветворение).
Снижение аппетита
Обычно лучевая терапия не приводит к развитию тошноты или рвоты, но снижение аппетита наблюдается довольно часто. Вместе с тем, для скорейшего выздоровления требуется полноценное высококалорийное питание с высоким содержанием белка.
Побочные реакции со стороны кожи
Вероятность развития кожных реакций и их интенсивность зависят от индивидуальных особенностей пациента. В большинстве случаев через 2-3 недели в области воздействия возникает покраснение. После окончания лечения оно сменяется пигментированием, напоминающим загар. Чтобы предотвратить чрезмерные реакции, могут назначаться специальные кремы и мази, которые наносятся после окончания сеанса. Перед началом следующего их необходимо смыть теплой водой. Если реакция выражена сильно, делают перерыв в лечении.
Реакции со стороны полости рта и горла
Если облучают область головы и шеи, могут развиться лучевой стоматит, который сопровождается болью, сухостью во рту, воспалением слизистых, а также ксеростомия вследствие нарушения функции слюнных желез. В норме эти реакции проходят самостоятельно в течение месяца после окончания лучевой терапии. Ксеростомия может беспокоить пациента в течение года и более.
Осложнения со стороны молочной железы
При прохождении лучевой терапии по поводу рака молочной железы могут возникать следующие реакции и осложнения:
- Покраснение кожи груди.
- Отек груди.
- Боль.
- Изменение размера и формы железы из-за фиброза (в некоторых случаях эти изменения остаются на всю жизнь).
- Уменьшение объема движения в плечевом суставе.
- Отек руки на стороне поражения (лимфедема).
Побочное действие на органы грудной клетки
- Воспаление слизистой пищевода, которое приводит к нарушению глотания.
- Кашель.
- Образование мокроты.
- Одышка.
Последние симптомы могут свидетельствовать о развитии лучевого пневмонита, поэтому при их возникновении следует немедленно обратиться к вашему врачу.
Побочные реакции со стороны прямой кишки/петель кишечника
- Расстройство стула — диарея или наоборот, запоры.
- Боли.
- Кровянистые выделения из заднего прохода.
Побочные действия со стороны мочевого пузыря
- Учащенное болезненное мочеиспускание.
- Наличие примеси крови в моче иногда может быть настолько выраженным, что моча приобретает кроваво-красный цвет.
- Наличие патологических примесей в моче — кристаллы, хлопья, гнойное отделяемое, слизь.
- Уменьшение емкости мочевого пузыря.
- Недержание мочи.
- Развитие везиковагинальных или везикоректальных свищей.
Побочные эффекты при облучении опухолей забрюшинного пространства, печени, поджелудочной железы
- Тошнота и рвота.
- Ознобы после сеансов.
- Боли в эпигастрии.
Химиолучевая терапия
Лучевая терапия довольно редко проводится в качестве самостоятельного лечения. Чаще всего она сочетается с каким-либо другим видом лечения: хирургическим, а чаще всего — с лекарственным. Это может быть как вариант одновременной химиолучевой терапии, так и последовательной, а также варианты сочетания лучевой терапии с иммунотерапией, таргетной и гормональной терапии. Такие виды лечения могут иметь ощутимо более высокую противоопухолевую эффективность, однако необходимо тщательно оценить риски совместных побочных эффектов, поэтому принятие решения о любом объёме лечения с онкологической патологией должен принимать мультидисциплинарный онкологический консилиум.
Читайте также:




