Адъювантная терапия при раке предстательной железы
Радикальная простатэктомия (РПЭ) на протяжении последних двух десятилетий остается одним из наиболее популярных методов лечения локализованного и местно-распространенного (Т3а) рака предстательной железы (РПЖ). В наблюдениях ведущих урологических клиник, имеющих большой опыт выполнения РПЭ, продемонстрированы высокие показатели безрецидивной выживаемости и хорошее качество жизни больных после проведенного хирургического лечения. В то же время, являясь одним из наиболее радикальных способов лечения РПЖ, оперативное вмешательство не во всех случаях приводит к полному излечению от заболевания. Развитие рецидива после РПЭ может быть связано как с недостаточно точным определением распространенности опухолевого процесса (невыявленная экстракапсулярная инвазия, инвазия семенных пузырьков, регионарные и отдаленные микрометастазы), так и с нерадикальным выполнением операции (позитивный хирургический край). В связи с этим проведение адъювантной послеоперационной лучевой и/или гормональной терапии (ГТ) (мультимодальное лечение) является привлекательной лечебной стратегией у больных локализованным и местно-распространенным РПЖ, относящимся к группе высокого риска прогрессирования опухолевого процесса.
Адъювантная лучевая терапия. Целью послеоперационной дистанционной лучевой терапии (ДЛТ) является профилактика развития местного рецидива опухоли после РПЭ. В связи с этим одной из основных проблем, возникающей при планировании адъювантного облучения, является отбор пациентов, у которых риск возникновения рецидива в области ложа предстательной железы (зоны везико-уретрального анастомоза) выше риска системного прогрессирования РПЖ. Кроме того, учитывая достаточно высокую вероятность развития осложнений при проведении ДЛТ после РПЭ, связанную со сложностями топометрии, и неочевидность пользы немедленного послеоперационного облучения, возникает вопрос, не лучше ли проводить отсроченную (\спасительную\) лучевую терапию уже при реализации местного рецидива опухоли или биохимического прогрессирования процесса?
Основными показаниями для проведения адъювантной (немедленной послеоперационной) ДЛТ являются неблагоприятные данные патоморфологического исследования: наличие положительного хирургического края (опухолевый рост по линии резекции), экстракапсулярная инвазия (ЭИ) опухоли, инвазия семенных пузырьков. Наиболее значимыми факторами риска для развития местного рецидива являются выход опухоли за пределы капсулы и позитивный хирургический край (ПХК). При этом для прогнозирования прогрессирования процесса важное значение имеет выраженность этих изменений (ограниченная или обширная ЭИ, фокальный или протяженный ПХК), а также их сочетание с различной дифференцировкой опухолевого процесса. Частота развития биохимического рецидива после РПЭ у больных с ЭИ и ПХК представлена в таблице 1.
Таблица 1. Безрецидивная (ПСА 0,2 нг/мл) у больных, получавших послеоперационное облучение, оказался на 88% меньше, чем у пациентов, которым было проведено только хирургическое лечение. 5-летняя безрецидивная выживаемость больных в группах комбинированного и хирургического лечения составила соответственно 89% и 55% (р 10,9 нг/мл и степень дифференцировки по шкале Глисона 4 + 3 балла являлись достоверными факторами прогноза развития рецидива после комбинированного лечения.
В работе Baylor College of Medicine проведен сравнительный анализ безрецидивной выживаемости больных с ПХК после РПЭ: 44 больным проведена адъювантная ДЛТ, 189 пациентам дополнительного лечения после операции не проводили (33). 5-летняя безрецидивная выживаемость в группе комбинированного лечения составила 90,9%, в группе хирургического лечения - 66,4%, 10-летняя безрецидивная выживаемость соответственно 90,9% и 54,5% (р=0,0012). Достоверными факторами риска развития рецидива в мультивариантном анализе являлись сумма Глисона > 7 баллов и протяженная ЭИ.
Неблагоприятное прогностическое влияние инвазии опухоли в семенные пузырьки на эффективность послеоперационной ДЛТ показано в исследовании, проведенном в Чикагском Университете и включающем 220 больных (34). Ни адъювантная, ни спасительная (при биохимическом рецидиве) лучевая терапия не приводила к достоверному увеличению безрецидивной выживаемости.
Таким образом, вышеперечисленные клинические и патоморфологические факторы прогноза имеют существенное значение для выбора активной (адъювантная ДЛТ) или выжидательной (наблюдение до прогрессирования) послеоперационной тактики у больных РПЖ. В нескольких исследованиях эффективность немедленного послеоперационного облучения сравнивается с результатами отсроченной (спасительной) ДЛТ (таблица 3).
Таблица 3. Немедленная (адъювантная) и отсроченная (спасительная) лучевая терапия у больных после РПЭ.
- English
- Русский







































Главное меню
- Редакционная коллегия
- Редакционный совет журнала
- Архив
- База авторов
- Порядок рецензирования статей
- Информация для авторов
- Информация для рекламодателей
- Издательский дом
- Политика редакции
- Обратная связь
Главное меню
- Редакционная коллегия
- Редакционный совет журнала
- Архив
- База авторов
- Порядок рецензирования статей
- Информация для авторов
- Информация для рекламодателей
- Издательский дом
- Политика редакции
- Обратная связь
Лечение рака предстательной железы (РПЖ) до настоящего времени остается сложной проблемой. В частности, это относится к вопросу: надо ли сочетать
гормональную терапию с другими вариантами основного лечения? Принципиально, гормональную терапию, так же как и химиотерапию, можно сочетать с основным
методом лечения (неоадъювантный или адъювантный вариант). Сложность проблемы состоит в том, что гормональная терапия не является безразличной для организма. При ее проведении меняется минеральная плотность костей, возрастает риск переломов (Daniell, 1997) (рисунок 1), развивается метаболический синдром, нарушения психики и т. д. Кроме того, сам по себе риск переломов значительно снижает продолжительность жизни больных (Oefelein et al., 2002). Таким образом, назначенная без показаний гормональная терапия является излишним и неоправданным методом лечения.
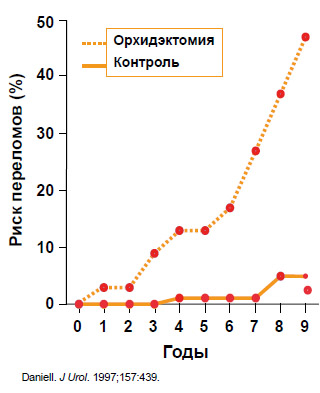
Рисунок 1. Андрогенная депривационная терапия увеличивает риск переломов
Неоадъювантная гормонотерапия РПЖ
В настоящее время существует 4 основных варианта неоадъювантной терапии рака предстательной железы.
- Неоадъювантная гормонотерапия (НеоГТ) + радикальная простатэктомия.
- Неоадъювантная химиотерапия(химиогормонотерапия) + радикальная простатэктомия.
- Неоадъювантная гормонотерапия + дистанционная лучевая терапия.
- Неоадъювантная гормонотерапия + брахитерапия и другие виды локального лечения.
Неоадъювантная гормонотерапия + радикальная простатэктомия
Вопрос о необходимости проведения гормонотерапии перед операцией остается дискутабельным. Существует теоретическое обоснование предоперационной гор-
монотерапии, включающее в себя следующее.
1. В 40-50% случаев клинически локализованного опухолевого процесса (Т1-Т2) при послеоперационном патоморфологическом исследовании выявляется экстракапсулярная инвазия (рТ3) (Zincke et al., 1994).
2. В эксперименте на животных (гормоно-чувствительная опухоль Shionogi) неоадъювантная гормонотерапия приводит к 50% снижению местных рецидивов и смертности от рака (Gleave et al., 1996).
Первым ученым, предложившим комбинированную или максимальную андрогенную блокаду, был Labrie (1993).
Таблица 1. Неоадъювантная гормонотерапия (НеоГТ) (Labrie et al., 1993)
(Labrie et al. 1993)
Однако существуют и некоторые особенности. Так, по данным Witjes et al. (1997), в группе больных с клинической стадией Т2 различия в частоте выявления опухоли по линии резекции оказались статистически достоверны в пользу НеоГТ,
в группе больных с опухолями Т3 – различия недостоверны (таблица 2).
Goldenberg et al. (1996), не отмечают различий в частоте осложнений
операции в группах пациентов, не получающих НеоГТ перед РПЭ, и пациентов, получивших данную терапию.
Таблица 2. Неоадъювантная гормонотерапия (НеоГТ) (Witjes et al., 1997)
Meyer F. et al. (2001), показали, что у 756 больных, получавших гормональную терапию более 3 месяцев, отмечено повышение безрецидивной выживаемости по сравнению с контрольной группой.
Hack М. и соавт. (2008), продемонстрировали, что НеоГТ в течение 6 месяцев при местно-распространенном, первично нерезектабельном (> сТ3) раке с высокими ха-
рактеристиками риска (Глисон > 8) или ПСА (> 20 нг/мл), увеличивала шансы для выживания без существенного риска пери- или постоперационных осложнений.
Таким образом, можно сделать следующие выводы:
Ни в одном из исследований не выявлено статистически достоверных различий в безрецидивной выживаемости и длительности периода до развития прогрессирования у больных, которым проводили НеоГТ и у больных, которым сразу выполняли оперативное вмешательство.
НеоГТ не может в настоящее время считаться стандартным методом лечения локализованного и местно-распространенного РПЖ.
Перспективным в изучении НеоГТ является назначение более длительного курса предоперационной гормонотерапии (возможно, до полного подавления уровня ПСА), более тщательный отбор больных (клиническая стадия Т2?, уровень
ПСА > 20 нг/мл?), поиск и применение новых схем гормонотерапии, химиотерапии, гормонохимиотерапии.
Неоадъювантная гормонотерапия перед дистанционной лучевой
терапией
Цель сочетанного применения лучевой терапии и гормонотерапии состоит в уменьшении объема опухоли и, соответственно, объема облучения, что приводит к снижению числа осложнений. При НеоГТ:
• 3-месячная неоадъювантная терапия агонистами ЛГРГ приводит к уменьшению объема предстательной железы на 37%;
• объем мочевого пузыря, на который приходится 95% дозы, уменьшается на 46%, объем прямой кишки – на 18% (Forman, 1995; Zelefsky, 1997).
• повышается эффективность лучевой терапии;
• снижается число клеточных клонов, которые должны быть уничтожены при лучевой терапии;
• индукция апоптоза увеличивается при сочетании гормонального и лучевого воздействия – переход клеток в S-фазу, что усиливает цитотоксическое действие облучения (Zietman, 1997; Pollak, 1997).
По данным Pilepich et al. в 2001, было выявлено, что комбинированная терапия (НеоГТ + лучевая) имеет ряд преимуществ перед монолучевой терапией.
Так, местные рецидивы при комбинированном лечении диагностированы в 30% случаев, а при лучевой терапии – в 42%.
Отдаленные метастазы выявлены соответственно у 34% и 45% больных.
Безрецидивная выживаемость составила 33% при комбинированной терапии и 21% – при лучевой. Общая выживаемость в подгруппе больных с суммой Глисона 2-6 баллов была 70% и 52% соответственно. В то же время общая выживаемость и локо-
регионарный контроль в подгруппе больных с суммой Глисона 7 и более баллов достоверно не отличались.
А по данным Канадского многоцентрового исследования, проведенного Klotz et al. в 2000 г., при среднем периоде наблюдения 3 года отмечено существенное увеличение периода до биохимического прогрессирования в группе больных,
получавших НеоГТ ципротерона ацетатом (рисунок 2).
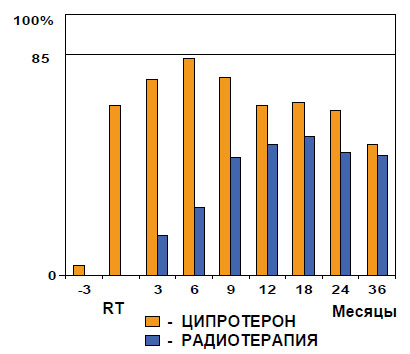
При среднем периоде наблюдения 3 года отмечено существенное увеличение периода до биохимического прогрессирования в группе больных, получавших НеоГТ ципротерона ацетатом
Рисунок 2. НеоГТ + лучевая терапия (Канадское многоцентровое исследование)
Следует отметить роль НеоГТ в уменьшении объема облучения. Результаты проведенных сравнительных исследований пациентов, находившихся на лечении в специализированных отделениях лучевой терапии в 2002-2003 гг. показали, что объем предстательной железы является прогностическим фактором токсичности при лучевой терапии локализованного РПЖ. НеоГТ может уменьшить объем железы
(рисунок 3), а следовательно и планируемый объем облучения. При трансректальном УЗИ объем простаты до ГТ был 50,65", а после лечения – 38,97" (p 7 (p = 0,0003) и позитивный хирурги-
ческий край (p Ключевые слова:
Глава 8. Лучевая терапия рака предстательной железы
Лучевая терапия является в настоящее время одним из ведущих консервативных специальных методов лечения рака предстательной железы как при локализованном, так и при местнораспространенном процессе.
Дистанционное облучение с применением мегавольтных источников излучения (гамма-установка, линейные ускорители и др.) рекомендуется сейчас при всех стадиях рака предстательной железы (Алиев Б.М., 1983, Свиридова Т.В., 1994, Amin P.P. et al. 1983, Bagschow М.A., 1983 и др.). Оно является альтернативой радикальной простатэктомии в начальной стадии заболевания, в случае невозможности операции в связи с сопутствующими заболеваниями или отказом больного от оперативного лечения. Лучевая терапия с успехом применяется как в случаях локализованного, так и местнораспространенного рака предстательной железы.
При этом в подходах к лучевому лечению у различных авторов имеются существенные различия, касающиеся техники и технологии облучения, объема лучевого воздействия и суммарных очаговых доз.
Противопоказаниями к проведению лучевой терапии считаются: общее тяжелое состояние больного, раковая кахексия, выраженный цистит и пиелонефрит, наличие большого количества остаточной мочи, хроническая почечная недостаточность, азотемия (Голдобенко Г.В., 1997).
Последнее десятилетие ознаменовалось значительным прогрессом в изучении возможностей лучевой терапии рака предстательной железы. Арсенал средств и методов лечения обогатился новыми подходами к лучевому лечению, ряд которых оказался весьма плодотворным. Популярность ее объясняется рядом очевидных преимуществ перед другими известными терапевтическими методами. Лучевая терапия не оказывает пагубного влияния на сердечно-сосудистую и свертывающую системы крови, изменения которых под воздействием гормонотерапии нередко приводят к преждевременным летальным исходам. В последние годы некоторыми исследователями, даже при ранних стадиях заболевания, лучевой терапии отдается предпочтение перед хирургическим лечением (радикальной простатэктомией), так как отдаленные результаты обоих методов приблизительно одинаковы, но облучение не вызывает столь серьезных лечебных последствий, как хирургическое лечение: 0.5-5% - послеоперационной летальности, 95-100% - импотенции, 10-15% - недержание мочи и пр.
Некоторые литературные данные о выживаемости больных раком предстательной железы, леченных лучевым методом представлены в табл. 34.
Таблица 34. Результаты лучевой терапии рака предстательной железы. Выживаемость за 5 и 10 лет.
| Автор | Кол-во больных | T1 | T2 | T3 | T4 | |||
| 5 лет | 10 лет | 5 лет | 10 лет | 5 лет | 10 лет | 5 лет | ||
| Kopper B., 1988 | 112 | 83% | 59% | 83% | 59% | |||
| Reed N., 1988 | 168 | 100% | 77% | 42% | ||||
| Howleu P., 1989 | 126 | 92% | 92% | 72% | ||||
| Maruoka M., 1989 | 129 | 100% | 100% | 75% | ||||
| Zagars G., 1989 | 114 | 84% | 68% | 84% | 68% | 72% | 47% | |
| Cuban D., 1990 | 96 | 61% | 61% | |||||
| Prestone J., 1990 | 191 | 79% | 75,5% | 52,5% | 0% | |||
| Abratt P.P., 1990 | 93 | 83% | 83% | 83% | ||||
| Jrumiyama K., 1990 | 33 | 100% | 100% | 65% | 50% | |||
| Lioyd-Da-Vies, 1990 | 209 | 67% | 32% | 67% | 32% | 67% | ||
| Fuse H., 1991 | 41 | 86% | 66% | 47% | ||||
| Kuten A., 1992 | 116 | 84% | 78% | 63% | ||||
| Kaprowsky C., 1992 | 176 | 95% | 80% | |||||
Эффективность радиотерапии больных раком предстательной железы во многом зависит от качества планирования облучения. Планированию лучевой терапии и ее клинико-дозиметрическому обоснованию обычно предшествует топометрическая подготовка больных. С этой целью широко применяются такие виды рентгенологического исследования как компьютерная томография, магнитно-ядерный резонанс и др.
В последние годы для оптимизации лучевой терапии широко применяются компьютерные программы и специальные устройства, так называемое конформальное (conformal) облучение, которые позволяют с учетом гетерогенности тканей и кривизны облучаемого участка в трех проекциях выбрать наиболее рациональные условия лучевого воздействия. В качестве критериев при этом выбрана лучевая нагрузка на наружные подвздошные и обтурационные лимфатические узлы, кожу передней и задней поверхности тела больного, тазобедренный сустав. Характер распределения доз определяют во фронтальной, сагиттальной и горизонтальной плоскостях облучаемого участка тела пациента. При оценке полученных данных исходят из того, что первичная опухоль и зоны регионарного метастазирования должны облучаться равномерно с допустимым градиентом дозы 90-100%, а лучевая нагрузка на тазобедренный сустав, заднюю стенку прямой кишки и на уровне кожных покровов не должна превышать их толерантность.
На основании полученной топометрической информации проводят тщательный анализ распределения доз при различных вариантах дистанционной гамма-терапии. Общим выводом из этих исследований явилось признание рациональности использования при локализованных формах рака предстательной железы подвижных методик дистанционной гамма-терапии, т.е. облучение только первичной опухоли; при распространенности опухоли на регионарные лимфатические узлы - сочетание вариантов подвижного и статического 4-х польного перекрестного облучения с соотношением доз с передних и задних полей 2:1. Показано, что при использовании этих вариантов облучения, лучевая нагрузка на заднюю стенку прямой кишки снижается почти на 20%, на кожные покровы ягодичной области - на 20-30% по сравнению с гамма-терапией с соотношением доз 1:1 и с однозонным подвижным облучением первичной опухоли с углом качания 240° или же двухзонным облучением с углом качания 180°. Лучевая нагрузка на уровне кожных покровов лобковой зоны с соотношением доз 2:1 находится на том же уровне, что и при старых вариантах гамма-терапии с соотношением доз 1:1, составляя 60% от величины очаговой дозы облучения.
На основе комплексного обследования, тщательной дозиметрической подготовки, а также в зависимости от распространенности опухолевого процecca, выделяют следующие варианты дистанционной лучевой терапии рака предстательной железы.
1. Облучение только первичной опухоли. В зависимости от размеров новообразования, распространения его на соседние органы и тканевые структуры, применяется одно- или двухзонная подвижная дистанционная гамма-терапия с требуемыми разведениями осей ротации, углами вращения 90°-120°. При инфильтрации одной или двух боковых стенок таза используется методика двухзонной ротации с углами качания 60°-90°. Размер поля на оси ротации, в зависимости от параметров опухоли, колеблется от 4 х 8 до 9 х 11 см. При этом в зону облучения включается первичная опухоль, шейка мочевого пузыря, передняя стенка прямой кишки с постепенным снижением поглощенных доз в направлении задней ее стенки, а также к тазобедренному суставу, до уровня ниже их толерантности. В зависимости от величины и конфигурации предстательной железы, изменяются размеры полей облучения, сектор качания и расстояние между осями качания в условиях двухзонного подвижного облучения. Если одна из долей железы увеличена, а другая имеет небольшие размеры, необходимо со стороны большего поражения железы увеличить только одно поле облучения. Разовая доза 1,8-2 Гр, суммарная - 65-70 Гр. Перерыв на дозе 30-40 Гр и продолжение облучения через 2-3 недели. Показания: ранние стадии заболевания - T1-2N0M0.
2. Облучение первичной опухоли и регионарных лимфатических узлов таза. Дистанционная гамма-терапия проводится с 4-х статических полей под углом 45° - два поля спереди, два сзади, с соотношением лучевой нагрузки с передних и задних полей 2:1. Для охвата опухоли и путей регионарного метастазирования 90-100% изодозой нижний край поля облучения располагается на уровне ануса, верхний - на уровне первого крестцового позвонка - места перехода внутренней и наружной цепочек лимфатических коллекторов в общую. Наружная граница поля проходит по линии, пересекающей внутренний край вертлужной впадины. После суммарной очаговой дозы 45 Гр поля уменьшаются в размерах и облучение проводится только на первичную опухоль одно- или двухзонной секторной ротацией до общей дозы 65-70 Гр. Углы качания варьируют при однозонной ротации от 90° до 120°, при двухзонной - от 60° до 90°. Облучение осуществляется в дозе 20-25 Гр (РОД 1,8-2 Гр) после перерыва в 2-3 недели. Показания: больные раком предстательной железы в стадии заболевания - T1-2N1-3M0, T3-4N0-x М0. При Т1-2NxM0 - суммарная доза на регионарные лимфатические узлы может быть ограничена дозой 45 Гр, на предстательную железу доза доводится до 65-70 Гр. При наличии метастатического поражения лимфатических узлов, общая суммарная доза на них доводится до 50-60 Гр.
3. Облучение первичной опухоли и лимфатических узлов таза с включением парааортальной и общей подвздошной групп лимфатических коллекторов. Лучевая терапия при этом проводится на фоне приема гормональных препаратов. Сначала облучению подвергается первичная опухоль и регионарные лимфатические узлы до общей очаговой дозы 40-45 Гр. На втором этапе расщепленного курса, после перерыва 2-3 недели, подключается облучение общих подвздошных и парааортальных лимфатических узлов с двух-фигурных полей, имеющих форму перевернутой буквы "U" с экранированием спинного мозга и почек до суммарной очаговой дозы 40 Гр. Затем продолжается облучение первичной опухоли суженными полями подвижным методом до общей очаговой дозы 65-70 Гр при значении разовой дозы 1.8-2 Гр. Показания: распространение опухоли на юкстарегионарные лимфатические узлы - Т1-4N2-3M0.
Больший объем тканей облучают на первом этапе лучевого лечения. Разовую очаговую дозу 1.8-2 Гр подводят ежедневно 5 раз в неделю. Суммарная очаговая доза достигает 45-50 Гр. Затем проводят облучение только предстательной железы и прилежащих тканей. Большинство авторов полагают, что рациональная суммарная очаговая доза, рассчитанная в центре железы должна составлять при Т0-1 - 60 Гр, при Т2 - 60-65 Гр, при Т3 - 65-70 Гр, при Т4 - более 70 Гр. При этом доза на расстоянии 4 см от центра железы должна достигать при Т0-2 -6 0 Гр, при Т3 - 65-70 Гр и при Т4 - более 70 Гр (Hanks G. et al., 1985).
При использовании высокоэнергетического излучения ускорителей (> 10 Мэв) облучение первичной опухоли и лимфатических узлов таза рекомендуется проводить с двух противолежащих полей (переднего и заднего), либо с четырех полей (переднего, заднего и двух боковых). Используя фотоны ниже 18 Мэв, передне-задними полями можно подвести дозу до 45 Гр и дополнительную дозу путем подключения боковых полей (Голдобенко Г.В., 1997).
Последние литературные данные свидетельствуют о серьезных достижениях лучевого метода лечения. Так группа RTOG привела отдаленные результаты лучевого лечения крупнейших лечебных учреждений, занимающихся этой проблемой. Они представлены в табл. 35.
Таблица 35. Отдаленные результаты лучевой терапии рака предстательной железы в % (RTOOG, Dearnaley D. ,1998).
| Стадия | Кол-во больных | Локальный рецидив | Безрецидивная выживаемость | Общая выживаемость | ||||||
| 5 лет | 10 лет | 15 лет | 5 лет | 10 лет | 15 лет | 5 лет | 10 лет | 15 лет | ||
| Т1 | 583 | 3-6 | 4-8 | 17 | 84-85 | 52-68 | 39 | 83-95 | 52-76 | 41-46 |
| Т2 | 1117 | 12-14 | 17-29 | 32-35 | 66-90 | 27-85 | 15-42 | 74-78 | 43-70 | 22-36 |
| Т3 | 2292 | 12-26 | 19-31 | 25-56 | 32-60 | 14-16 | 17-40 | 56-72 | 32-42 | 23-27 |
Bagshaw M.A. et al.,1994, сообщили отдаленные результаты дистанционной лучевой терапии у 1245 пациентов со стадией Т1-2 при сроке наблюдения 31.5 года (медиана - 7.8 лет). Общая 15-летняя выживаемость больных не имевших метастазов в лимфатические узлы составила 53%.
Hanks et al.,1997, приводят результаты 3-летней (биохимической) безрецидивной выживаемости 233 пациентов с клинической стадией Т3 в зависимости от уровня ПСА перед началом лечения.(табл. 36)
Таблица 36. 3-летняя безрецидивная выживаемость больных раком предстательной железы в стадии Т3 в зависимости от уровня ПСА перед лечением и дозы радиации (Hanks et аl .,1997).
| Доза | ПСА 10-19,9 | ПСА > 20 |
| 70 Гр | 69% | 36% |
| 75 Гр | 80% | 46% |
| 80 Гр | 89% | 57% |
Мнения относительно дополнительных лечебных мероприятий на фоне облучения расходятся. Так И.А. Клименко и соавт.(1976), М.С. Старичков и соавт. (1980), С.И. Ткачев (1982) рекомендуют облучение на фоне гормонотерапии больным в стадии T3-4, Green et al. (1975) считают эстрогенотерапию благоприятной при прогрессирующих опухолях перед началом лучевого лечения с целью уменьшения объема мишени предстоящего облучения. Некоторые авторы (Klosterhalfen et al., 1982) в стадии Т3 дополняют лучевое лечение гормонами и кастрацией. При наличии симптомов инфравезикальной обструкции с хронической задержкой мочи на первом этапе проводят трансуретральную резекцию предстательной железы (ТУР) или операции отведения мочи с последующей (на 2 этапе) лучевой терапией.
В последние годы определенную новизну представляют попытки разработать дифференцированные показания к лучевой терапии в зависимости от степени злокачественности опухоли. С точки зрения Алиева Б.М. (1985) лучевое лечение всех недифференцированных вариантов рака предстательной железы должно вестись на фоне гормонотерапии независимо от стадии. Свиридова Т.В. с соавт. (1984, 1994) расширяют показания к комплексному гормонально-химиолучевому лечению, полагая, что оно должно применяться во всех стадиях низкодифференцированного и анапластического рака, а лучевая терапия в самостоятельном варианте должна использоваться при стадиях Т1-3 высоко- и умеренно-дифференцированного рака без поражения регионарных лимфоузлов.
Данные последних лет свидетельствуют о преимуществе комбинированного гормоно-лучевого лечения у больных раком предстательной железы с неблагоприятным прогнозом. Так в исследовании EORTC, включающем 401 пациента раком предстательной железы в стадии Т1-2 G 3 и стадиях Т3 и Т4 без отдаленных метастазов показано улучшение результатов лечения при применении адъювантной терапии аналогами LНRH, в частности, золадексом (Воllа M. et аl., 1998). Эти данные представлены в табл. 37.
Таблица 37. 5-летние результаты адъювантной гормонотерапии в комбинации с лучевой терапией больных раком предстательной железы в % (EORTC, 1998).
Читайте также:

