Ядерное обследование на онкологию
Ежегодно в мире от рака умирает 8−9 миллионов человек. Вероятность наступления этого страшного заболевания напрямую связана с возрастом. В России количество диагностированных онкозаболеваний у женщин начинает экспоненциально расти с 25 лет. Риск практически удваивается каждые четыре года, достигая максимума между 60 и 70 годами. Вероятность появления рака у мужчин нарастает с 35 лет. До 55 лет она примерно на 30 процентов ниже, чем у женщин, в возрасте 55—59 лет сравнивается, а затем с 60 до 70 превосходит женские показатели.
При этом в России отмечено серьезное увеличение заболеваемости онкологией. Так, только в Ростовской области врачи диагностируют более 14 тысяч случаев рака в год, а в регионах с более тяжелой экологической ситуацией и наличием вредных производств цифры могут быть в разы выше. Однако такой диагноз вовсе не приговор: своевременная и точная диагностика может как помочь с выбором метода лечения, так и отследить его эффективность. Во многих случаях пациентам удается добиться ремиссии, а иногда и полного излечения.
Проблемой, особенно в регионах России, остается доступ к эффективной и квалифицированной диагностике онкологических заболеваний. Наиболее точным методом сейчас является позитронно-эмиссионная томография, сопряженная с компьютерной томографией (ПЭТ/КТ): ни ультразвуковые исследования (УЗИ), ни обычная КТ или МРТ не могут с достаточной точностью локализовать опухоль. При этом в ПЭТ/КТ-диагностике используются крайне дорогие в производстве радиофармпрепараты, срок хранения которых не превышает 6—12 часов. Из-за этого долгое время данный вид медицинских услуг был доступен исключительно в Санкт-Петербурге, Москве и Европе. При этом потребность в нем оставалась огромной во всех регионах страны.


В этом аспекте компания копирует передовой европейский опыт. Там уже на протяжении 10—15 лет работают производственные площадки с циклотронами, которые обслуживают до 10—12 клиник. При этом ключевым моментом является правильная организация логистики. В российских условиях это наиболее трудная задача из-за больших расстояний и транспортных проблем, однако ее удалось эффективно решить.
Синтез радиофармпрепарата начинается ранним утром, где-то около часа ночи по местному времени. Он продолжается два часа, в ходе которых идет наработка радионуклида в циклотроне — двадцатитонном циклическом ускорителе, где облучается так называемая обогащенная вода. Всего на один цикл требуется около 1,5 миллилитра обогащенной воды. Из них в результате ядерной реакции получается изотоп фтор-18, он перегоняется по специальным трубкам в модуль химического синтеза, и через 23 минуты в автоматическом режиме получается радиофармпрепарат — фтордезоксиглюкоза. Она отличается от обычной глюкозы только тем, что в ней гидроксильная группа OH второго атома углерода замещена на атом фтора, поэтому ее общая формула выглядит так: 2-фтор-[18F]-2-дезокси-D-глюкоза.
Стоимость партии (1,5 мл) радиофармпрепарата (два часа загруженности производства) составляет от 400 000 рублей. При этом общие вложения в циклотронный радиохимический комплекс превышают 400 миллионов рублей.
Далее с радиофармпрепаратом проводится 11 специальных анализов, требуемых по стандарту государственной фармакопеи. С контейнером в центр приходят и все документы, где полностью подтверждено, что этот препарат годен, активность его достаточная, а по химико-физическим показателям он полностью соответствует тем параметрам, что прописаны в стандартах.
Транспортный контейнер, доставляемый спецмашиной, весит 20 килограммов. Он сделан из вольфрама и, несмотря на небольшие размеры, очень тяжелый и надежный.

Фтордезоксиглюкоза — это неспецифический трейсер, она позволяет диагностировать до 95 процентов всех онкологических заболеваний. На нее полностью отсутствуют какие-либо аллергические реакции. Введенная внутривенно, фтордезоксиглюкоза повторяет начальный участок метаболического пути глюкозы, проникая из сосудистого русла в межклеточное пространство, а затем в клетки. Обычная глюкоза превращается в них в фосфат глюкозы, а трейсер — в [18F]-дезоксиглюкоза-6-фосфат. Он больше не вступает в какие-либо дальнейшие метаболические реакции и остается в клетках тканей человека в течение всего времени исследования, что позволяет измерить в них концентрацию радионуклида фосфор-18.
Так как весь персонал работает с радиоактивными веществами, один из самых важных вопросов — это его безопасность. Для ее обеспечения все сотрудники имеют разнообразные дозиметры и другие измерительные приборы.
ПЭТ/КТ-диагностика при помощи фтордезоксиглюкозы позволяет делать три вещи. Во-первых, определить стадию развития онкологического заболевания. Как известно, самыми тяжелыми стадиями рака являются третья, когда опухоль достигает больших размеров, прорастает в другие ткани и органы, появляются метастазы в близлежащих лимфатических узлах, а также четвертая — с поражением метастазами удаленных от первичной опухоли органов. Поэтому, чтобы начать лечение, врач-онколог должен простадировать злокачественное новообразование посредством системы TNM (Tumor — Nodus — Metastasis), точно и последовательно сказать, где и как располагается первичная опухоль, есть или нет регионарные и отдаленные метастазы.
ПЭТ/КТ-диагностика помогает клиницисту полностью сформировать данный диагноз за одно исследование, так как позволяет отследить распространенность процесса во всем теле (вот здесь есть опухолевый очаг и его размеры в 3D вот такие, его объем такой-то и метастазы есть там, там и там, в таких-то и таких-то анатомических зонах). Важно учесть, что ПЭТ/КТ не предназначена для скрининга (когда опухоль только на стадии зарождения). Ее цель — ранняя диагностика метастатического поражения, то есть четкой локализации опухоли и ее метастазов.
Вторая функция — это оценка качества лечения любого типа — химиотерапии, лучевой терапии, хирургии. Уже на третий-пятый день можно установить эффективность химиотерапии, так как накопление радиофармпрепарата станет меньше. Таким образом, диагностика состоит из базового исследования и исследования в динамике (прогресса заболевания и результативности его лечения).
В зависимости от вида трейсера существуют два протокола исследования. Первый (стандартный) — от затылочной кости до середины бедра. Второй (расширенный) — от затылочной кости до пяточной кости. Расширенный протокол применяется, например, при меланоме. А вот при лимфоме используется стандартный. Протокол и объем исследования выбирает исключительно лечащий врач пациента.


Вредно ли все это для пациента? Абсолютно нет. Россия — одна из самых жестких стран в области контроля за ядерной медициной и допуском радиофармпрепаратов. А вот благодаря наличию доступной диагностики продолжительность и качество жизни больных раком, особенно с третьей его стадией, могут быть существенно увеличены. Вопрос в другом — насколько много квалифицированных врачей-онкологов в регионах, способных в полной мере задействовать и использовать результаты современной диагностики.
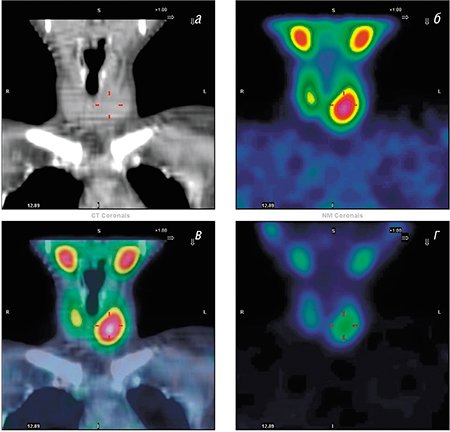
За последние годы и в России построено более десятка ПЭТ-центров, в первую очередь в Москве и Санкт-Петербурге. Федеральная сеть центров ядерной медицины расширяется, охватывая различные регионы страны: уже построены ПЭТ-центры в Уфе, Хабаровске, Челябинске, Красноярске, Ханты-Мансийске, Казани, Екатеринбурге, Белгороде, Тольятти.
В связи с этим возникает ряд вопросов, которые интересны не только специалистам, но и широкой общественности. Например, какую информацию несут изображения, полученные с помощью диагностических методов ядерной медицины? В чем состоит их преимущество при онкологических заболеваниях? Какова лучевая нагрузка на пациента при обследованиях методами ПЭТ и ОЭКТ? Сколько стоит такое обследование, и кто будет за него платить?
От морфологии – к физиологии
К стандартным и широко известным методам диагностики сегодня можно отнести рентгеновскую компьютерную томографию (КТ) и магнитно-резонансную томографию (МРТ), каждый из этих методов имеет свою нишу приложения.
Метод МРТ основан на явлении ядерного магнитного резонанса. С его помощью получают изображение пространственного распределения протонов (ядер атомов водорода, входящих в состав молекулы H2O), которое наиболее контрастно для мягких тканей с различным содержанием воды. МРТ используют для исследования головного и спинного мозга, диагностики опухолей, заболеваний нервной системы.
Усилить чувствительность методов КТ и МРТ можно с помощью контрастных веществ. Большинство опухолей, особенно злокачественных, имеют лучшее кровоснабжение, чем здоровые ткани, и контрастное вещество будет накапливаться в них в большей концентрации. Однако эти отличия не всегда настолько значимы, чтобы на основе визуальных оценок можно было поставить диагноз.
Оба этих метода дают изображения, основанные преимущественно на морфологических различиях тканей. Принципиальное отличие диагностических методов ядерной медицины состоит в том, что они позволяют визуализировать метаболические процессы (химические реакции, необходимые для поддержания жизни), протекающие в организме на клеточном уровне.
Метим опухоль
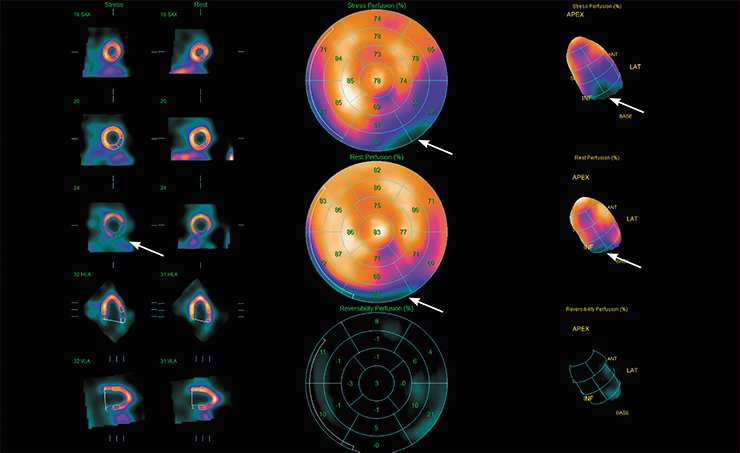
Например, в кардиологии для оценки кровоснабжения миокарда методом ОЭКТ широко применяется препарат Тс99m-МИБИ на основе метокси-изобутил-изонитрила, который захватывается здоровыми клетками миокарда. Метка накапливается в областях с ненарушенным кровоснабжением, и только в неповрежденных клетках, что позволяет диагностировать патологии кровоснабжения миокарда и выявлять области некротического повреждения.
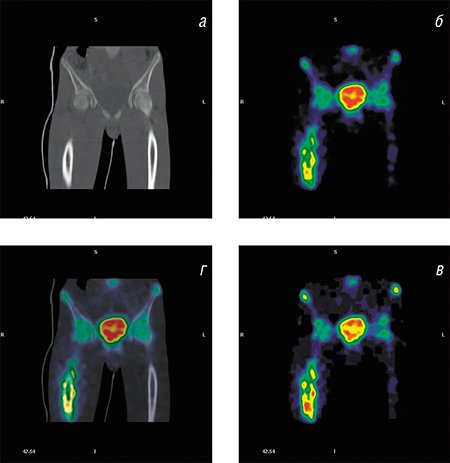
В онкологии метод ОЭКТ в последние годы уступает свои позиции ПЭТ. В этой области медицины практически все ПЭТ-обследования проводят с помощью препарата фтордезоксиглюкоза, по составу близкому к обыкновенной глюкозе и меченному изотопом фтора 18 F. Глюкоза – универсальный источник энергии, поэтому раковые клетки, отличающиеся усиленным метаболизмом, накапливают этот препарат в более высоких концентрациях, чем здоровые. И на ПЭТ-изображениях очаги поражения видны в виде ярких пятен.
В ОЭКТ и ПЭТ используются разные радионуклиды-метки. В первом случае это радиоактивные вещества, которые при распаде испускают гамма-кванты. Радионуклиды, использующиеся при ПЭТ-диагностике, испускают позитроны – античастицы электронов. В биологических тканях присутствует много свободных электронов, поэтому позитрон встречается с электроном, пройдя расстояние менее 1—2 мм. Частицы аннигилируют, выделяя энергию в виде двух гамма-квантов, вылетающих в противоположных направлениях, которые и регистрируются детекторами. Поток гамма-квантов при ПЭТ существенно выше, что и обеспечивает более высокое качество получаемых изображений.
В чем преимущества метода ПЭТ в сравнении с другими видами томографии для диагностики рака? Во-первых, он позволяет не только дифференцировать доброкачественные и злокачественные образования, но и обнаруживать опухоль на самой ранней стадии развития, когда шансов на успех излечивания существенно больше. Во-вторых, это единственный метод, с помощью которого можно просканировать все тело после обнаружения первичной опухоли, чтобы диагностировать наличие или отсутствие метастазов, что чрезвычайно важно для определения тактики лечения. Наконец, только ПЭТ дает самую раннюю оценку эффективности проводимого лечения, а также позволяет отличить рецидив от морфологических повреждений ткани после хирургических и лучевых процедур.
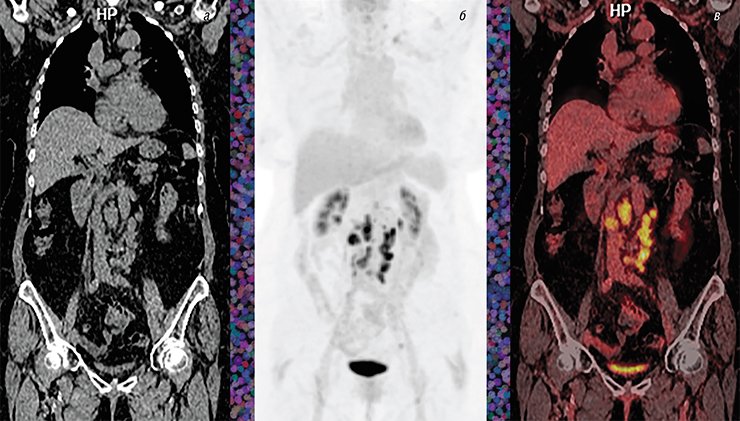
ПЭТ-исследования используют и для контроля опухолевого процесса уже после курса терапии. Например, при изначально гормонопозитивном раке молочной железы опухоль иногда прогрессирует после окончания стандартной 5-летней гормонотерапии. Но в рутинной клинической практике онкологи часто пренебрегают возможностью повторного установления диагноза, особенно при внутригрудной и внутрибрюшинной локализации метастазов. Это непросто сделать даже с помощью ПЭТ-диагностики из-за низкой метаболической активности очагов вследствие небольших размеров. Однако эти ограничения можно преодолеть за счет использования нового препарата – 18 F-фторэтилтирозина, который еще только входит в практику передовых клиник.
Решают кадры
В Европе, США, Японии и Китае быстрое развитие ядерной медицины в последние годы привело к росту числа исследований в этой области, увеличению численности и повышению уровня подготовки специалистов. Текущую ситуацию в России можно оценить как критическую. Чтобы решить проблему подготовки кадров для рутинной и исследовательской работы в области ядерной медицины, нужно вводить соответствующие курсы на действующих кафедрах медицинских вузов, а также готовить немедицинских специалистов: радиохимиков, медицинских физиков, математиков, биологов.
Назрела необходимость быстро решать вопрос образовательной подготовки специалистов для ядерной медицины, так как было бы стратегической ошибкой закупать дорогостоящее высокотехнологичное оборудование и при этом не иметь грамотных специалистов, которые могут на нем работать.
Будущее ядерной медицины определяется, прежде всего, мультидисциплинарными фундаментальными исследованиями, направленными на разработку более эффективных радиофармпрепаратов, обеспечение радиационной безопасности и создание новых аппаратных средств регистрации гамма-излучения, а также на совершенствование математических методов обработки полученной информации. Кстати сказать, в мире фундаментальные исследования в этой области ведутся сегодня настолько интенсивно и широко, что основной Европейский журнал по ядерной медицине и молекулярной визуализации (EJNMMI) даже разделился на несколько дисциплинарных журналов.
Ниже мы коснемся только одного из направлений, близкого автору по роду его научной деятельности, которое связано с применением математического моделирования и компьютерных имитаций в области диагностической ядерной медицины. Необходимость такого подхода диктуется невозможностью из-за лучевой нагрузки проводить исследования на людях, тогда как эксперименты на мелких животных не могут решить проблем, возникающих при диагностике человека.
Матмоделирование в помощь
Томографические исследования в новосибирском Институте теоретической и прикладной механики (ИТПМ) СО РАН были инициированы д. ф.–м. н. Н. Г. Преображенским еще в 1980-е гг. с целью использовать их для диагностики газа и плазмы. В начале 2000-х гг. специалисты института совместно с врачами НМИЦ им. академика Е. Н. Мешалкина (Новосибирск) начали применять математическое моделирование для компьютерной имитации процедуры обследования кардиологических больных методом ОЭКТ. Сейчас эти исследования продолжаются в сотрудничестве с Институтом вычислительной математики и математической геофизики СО РАН, а также Национальным медицинским исследовательским центром кардиологии (Москва), Венским медицинским университетом и отделением ядерной медицины Центральной клинической больницы Вены (Австрия) при поддержке РФФИ и Австрийского научного фонда.
В России подобная работа пока ведется только в ИТПМ СО РАН. Несколько лет тому назад совместно с отделением томографии НМИЦ им. ак. Е. Н. Мешалкина был разработан первый отечественный 3D-математический фантом для исследований в области диагностической ядерной кардиологии. Этот фантом описывает распределение препарата Тс99m-МИБИ в органах грудной клетки среднестатистического пациента мужского пола при исследовании перфузии (кровоснабжения) миокарда методом ОЭКТ. Рассчитанные для него проекционные данные хорошо согласуются с данными реальных клинических обследований. Фантом использовался в различных исследованиях, в том числе по снижению дозы радиофармпрепарата с целью уменьшения лучевой нагрузки на пациента.
Существует два подхода к развитию фантомов: на основе методов компьютерной графики и на основе простых фигур, описываемых уравнениями пространственной геометрии. С самого начала мы хотели построить фантомы, которые можно было бы легко трансформировать, меняя размеры и положение органов, чтобы исследовать влияние анатомического строения пациентов на качество изображений.
У Новосибирска имеется огромный научный потенциал в области диагностической, терапевтической и интервенционной ядерной медицины: перспективные разработки и хорошие заделы по разным направлениям наряду с большим опытом сотрудничества есть и в институтах СО РАН, и в медицинских учреждениях. Достаточно упомянуть лишь о методе бор-нейтронозахватной терапии рака, который успешно развивается в Институте ядерной физики СО РАН совместно с другими научными и медицинскими организациями. Создание в Новосибирске мультидисциплинарного исследовательского центра ядерной медицины даст крепкую основу для развития фундаментальных и прикладных исследований в этой области.
Беляев В. Н., Климанов В. А. Физика ядерной медицины. М.: НИЯУ МИФИ, 2012, Ч. 2, 248 с.
Климанов В. А. Физика ядерной медицины. М.: НИЯУ МИФИ, 2012, Ч. 1, 308 с.
Колядина И. В., Абдуллаев А. Г., Танишина Н. Б. и др. Мультимодальный подход к дифференциальной диагностике метастатического поражения при раке молочной железы: описание клинического случая // Злокачественные опухоли. 2017. Т. 7. № 3. С. 31—36.
Denisova N. V., Terekhov I. N. A study of myocardial perfusion SPECT imaging with reduced radiation dose using maximum likelihood and entropy-based maximum a posteriori approaches // Biomed. Phys. Eng. Express. 2016. V. 2. N. 5. P. 055015 (12).
Denisova N. V., Ansheles A. A. A study of false apical defects in myocardial perfusion imaging with SPECT/CT // Biomed. Phys. Eng. Express. 2018. V. 4. N. 6. P. 065018 (12).
Jones D. S., Podolsky S. H., Greene J. A. et al. The Burden of Disease and the Changing Task of Medicine // N Engl. J. Med. 2012. V. 366. P. 2333—2338.
Ядерная медицина: как найти рак на ранней стадии и обнаружить мозг серийного убийцы
16 марта 2017, 20:01 
657
15х4 — формат научно-популярных лекториев, где каждое мероприятие — четыре коротенькие лекции длительностью в 15 минут, за которые эксперт в той или иной области рассказывает вам о сложном простыми словами, иллюстрируя их схемами и (иногда!) таблицами с котиками. Раз в две недели по четвергам на ДГ будут появляться самые интересные лекции в сжатом формате — ничего лишнего, только по делу.
В лучевой диагностике есть пять способов определить причину страданий пациентов. Простая рентгенография, которая показывает многое, но далеко не всё — в частности, мы не можем увидеть головной мозг. Компьютерная томография лишена этого недостатка, мы можем увидеть внутреннюю анатомию органов на серии срезов. То же самое может делать магнитно-резонансная томография, которая не просто подробно, а детально показывает структуру тканей и органов. Ультразвуковая диагностика показывает то, как органы работают. Органы состоят из тканей, ткани состоят из клеток. То, как работают клетки в совокупности, показывает радионуклидная диагностика. И это то, о чём я сегодня расскажу подробнее.
Дело в том, что ядерная медицина — это крупная медицинская отрасль, которая занимается лечением и диагностикой различных заболеваний с помощью радионуклидов. Поскольку я занимаюсь рентгенологией, то расскажу вам о диагностической составляющей этого метода.
Радионуклид — это ядро атома, которое что-то излучает, то есть частицы или волны. Иначе говоря, оно радиоактивно. Мы вводим это радиоактивное вещество в организм пациента, оно накапливается в его клетках и излучает частицы и волны, которые попадают на специальное считывающее устройство, называемое гамма-камера. В результате получаем изображение.
Проблема в том, что сам по себе нуклид накапливается во всех клетках, а нам надо посмотреть, как работают клетки костей или клетки головного мозга. Для этого нам нужно поместить этот нуклид в специальную молекулу, которая его доставит до места назначения. Этот метод применяется в онкологии. Ежегодно от рака умирает около восьми миллионов человек, а новых случаев диагностируется 14 миллионов. Нормальные клетки, из которых мы состоим, рождаются, делятся, а потом организм даёт им команду — и они умирают. Но некоторые из клеток не подчиняются приказу, и продолжают размножаться и делиться, причём гораздо активнее и интенсивнее, чем это делали предыдущие собратья. Так и получаются раковые клетки. Отличие от нормальных клеток состоит в том, что они накапливают радиоактивные препарат гораздо активнее, чем обычные клетки. Поэтому из той области, где они находятся, излучение будет гораздо интенсивнее, и мы увидим их, как горячие очаги.
Радионуклидная диагностика позволяет определить узлы и раковые опухоли на 3-6 месяцев раньше, чем это может себе позволить компьютерная или магнитно-резонансная томография. Очень часто бывает такое, что раковые опухоли диагностируются на поздних стадиях, но их ведь можно диагностировать быстрее. Раковые клетки выделяют особые частицы, именуемые онкомаркеры — но их количество крайне ничтожно, и определение обычными методами невозможно. Если ввести онкомаркеры подопытному животному, то оно воспримет их, как чужеродные антигены, и выработает для них антитела. Представьте, что антиген, или молекула онкомаркера — это Мориарти. Антиген — это Шерлок. На каждого Мориарти есть Шерлок Холмс, на каждое действие — противодействие, на каждый антиген — своё антитело. Эти антитела будут связывать антигены, и таким образом их нейтрализовывать.
К нам приходит человек. Мы не знаем — болен он или нет. Мы берём у него кровь. Дальше возможны два варианта: либо онкомаркеры есть, либо их нет. Мы добавляем сюда антитела, и если онкомаркеры есть, то будут образовываться тяжёлые комплексы. Если их нет, то антиген будет лёгким. Мы берём специальный фильтр, и просто антиген через него проходит, а тяжёлый комплекс задержится. Когда мы возьмем фильтр и замерим активность, то будет фонить — это значит, что этот человек скорее всего болен раком.
Сердечно-сосудистые заболевания могут разлучить вас с близкими людьми. Сосуды питают сердце, и приносят туда белки, жиры и углеводы, кислород и питательные вещества. В сосудах могут образовываться бляшки — таким образом, просвет суживается, клетки начинают голодать и со временем погибают. На экране мы увидим холодные очаги, то есть участки ишемии, мёртвые клетки. Если мы знаем, что есть бляшка, мы можем или искусственно расширить этот просвет, или поставить стенд в обход этой бляшки, таким образом восстановив кровоток. Кроме того, часто бляшки образуются не только на сосудах сердца, но и на сосудах головного мозга — так возникают инсульты, обширные области мёртвой ткани в головном мозге.
Лекцию про 9 самарских писателей XIX века, произведения которых должен прочитать каждый, можно изучить здесь.
ПЭТ КТ
ПЭТ является одним из методов радионуклидной диагностики (одно из направлений лучевой ядерной медицины).
Ядерная (или радионуклидная) медицина в онкологии входит в раздел медицинской визуализации и подразумевает применение радиоактивных материалов в небольших количествах для выявления, определения степени тяжести и лечения различных заболеваний, включая
- многие виды злокачественных опухолей,
- нарушений со стороны сердца,
- желудочно-кишечного тракта,
- эндокринных органов,
- неврологических расстройств
- и других патологических состояний.
Ядерная медицина позволяет диагностировать заболевания на самых начальных стадиях, а также обеспечивает выявление непосредственного раннего ответа пациента на лечение, поскольку обладает способностью четко определять молекулярную активность клеток и тканей организма.
Методы радионуклидной диагностики являются неинвазивными (то есть исключают нарушение целостности тканей организма) и, за исключением внутривенных инъекций, безболезненными и помогают врачу поставить диагноз заболевания и оценить его тяжесть. Во время обследования используются специальные радиоактивные материалы под названием радиофармпрепараты (радиофармацевтические препараты) или радиоизотопные метки (радионуклиды, радиоактивные индикаторы).
В современных центрах и отделениях лучевой диагностики ПЭТ практически всегда совмещается с КТ и проводится с помощью специальных устройств (ПЭТ КТ сканеров). Комбинированное ПЭТ КТ (pet ct) исследование позволяет четко локализовать анатомическое положение очагов патологической метаболической активности клеток или тканей.
Доказано, что комбинированная методика обследования обладает большей чувствительностью, нежели каждое из исследований по отдельности. ПЭТ позволяет оценить важнейшие функции организма, такие как кровоток, использование клетками и тканями кислорода и метаболизм глюкозы, что помогает врачу центра лучевой диагностики проанализировать уровень функционирования тканей и органов. В ходе КТ применяется специальное рентгеновское оборудование и, в некоторых случаях, контрастные материалы, что позволяет получить большое количество изображений или снимков внутренних структур организма.
Полученные изображения радионуклидной диагностики с помощью ПЭТ КТ проецируются на экран компьютера и подробно изучаются врачами-радиологами, что предоставляет превосходную информацию об анатомическом строении тех или иных структур.
С развитием радионуклидной диагностики в 40-х годах 20-го века ядерная медицина шагнула на новый уровень в плане изобретения действенного инструментария для обследования организма. В отделении лучевой диагностики онкоцентра NeoLife мы работаем на новейшем оборудовании, которым только располагает ядерная медицина нашего времени. Мы следим за развитием средств ядерной медицины и поэтому наш центр может проводить наиболее точную лучевую, радионуклидную диагностику на уровне высоких мировых стандартов.
- Обнаружение злокачественных новообразований
- Обнаружение очагов метастазирования (распространения) рака
- Оценка эффективности составленного плана лечения, например, противоопухолевой терапии
- Диагностика рецидивов рака после проведенного лечения
- Определение параметров кровотока в сердечной мышце
- Определение объема поражения сердечной мышцы после сердечного приступа (инфаркта миокарда)
- Составление плана хирургических вмешательств на сердечной мышце, таких как ангиопластика или шунтирование коронарных артерий (в сочетании с миокардиосцинтиграфией)
- Оценка патологических состояний головного мозга, таких как опухоли, нарушения памяти, судороги и другие заболевания центральной нервной системы
- Оценка функции головного мозга и сердечной мышцы в норме
- Высокая детализация изображения и большая точность обследования. Одновременное использование двух методик (ПЭТ и КТ) без необходимости изменения положения тела пациента во время обследования сводит возможность ошибки к минимуму.
- Большое удобство для пациента: процедуры ПЭТ и КТ проводятся одновременно, без необходимости повторного посещения центра лучевой диагностики.
- Радионуклидная диагностика подразумевает введение крайне небольших доз радиоактивного вещества, что сопровождается относительно низким облучением организма. Следовательно, по сравнению с преимуществами, риски от использования радиоизотопов при ПЭТ КТ весьма малы.
- Лучевая диагностика применяется уже более 50 лет. При этом какие-либо долгосрочные нежелательные эффекты от ее использования отмечены не были.
- При выборе того или иного метода радионуклидной диагностики врач всегда проводит сравнение его возможных рисков и преимуществ. Перед проведением процедуры врач должен сообщить пациенту обо всех существенных рисках и предоставить возможность обсудить все интересующие его вопросы.
- В крайне редких случаях возможно развитие легких аллергических реакций на радионуклидные препараты. Как бы то ни было, очень важно заранее сообщить медицинскому персоналу о наличии аллергии или любых других осложнений, в том числе возникавших во время проведения радиоизотопных процедур ранее.
- Внутривенное введение радиофармпрепарата может быть немного болезненным и сопровождается быстро проходящим покраснением кожи.
- Женщинам обязательно следует сообщить лечащему врачу или радиологу о любой возможности беременности, а также о кормлении ребенка грудью на момент проведения исследования.
ПЭТ-сканер представляет собой массивное устройство с округлым отверстием в центре и похож на КТ- или МР-томограф. Внутри аппарата кольцевидным образом размещается большое количество датчиков, которые фиксируют излучение от радиоизотопных меток, находящихся в организме пациента.
Компьютерный томограф, как правило, представляет собой массивное прямоугольное устройство с отверстием (так называемым коротким туннелем) посередине. В течение всей процедуры пациент находится на узком диагностическом столе, который перемещается по туннелю. Рентгеновская трубка и электронные детекторы рентгеновского излучения, которые вращаются вокруг пациента, располагаются друг напротив друга внутри кольцевидной структуры под названием гентри.
В отдельном контрольном помещении монтируется компьютерная рабочая станция, где проводится обработка полученного изображения. Здесь же находится врач или техник-радиолог, который следит за работой томографа и ходом обследования и может непосредственно видеть и слышать пациента, а также общаться с ним с помощью микрофона. Оборудование для проведения ПЭТ-КТ сочетает в себе возможности обоих вышеописанных аппаратов и по внешнему виду почти не отличается от ПЭТ- и/или КТ-томографов. Изображения, полученные от сканера во время обследования, обрабатываются с помощью специальных компьютерных программ.
Женщинам всегда следует сообщать врачу или технику-радиологу о любой возможности беременности, а также о кормлении ребенка грудью на момент проведения обследования. Необходимо уведомить лечащего врача или техника-радиолога, который проводит обследование, обо всех лекарствах, принимаемых пациентом, в том числе витаминах и растительных пищевых добавках. Также врачу важно рассказать о наличии любых аллергических состояний или недавно перенесенных и любых хронических заболеваниях. Некоторые предварительные инструкции, которые дает лечащий врач, определяются типом процедуры ПЭТ.
Специальные правила подготовки к обследованию предназначены для пациентов с сахарным диабетом. Кормящим пациенткам перед обследованием необходимо дополнительно посоветоваться с лечащим врачом или радиологом о порядке своих действий. Например, можно заранее сцедить некоторый объем молока и использовать его для кормления ребенка в течение того периода времени после диагностики, пока радиоизотопная (радионуклидная) метка или контрастный материал выводятся из организма. Наличие металлических предметов, таких как ювелирные украшения, очки, съемные зубные протезы, слуховые устройства и заколки для волос, может повлиять на характеристики изображения, поэтому их лучше оставить дома или снять перед процедурой.
В целом, за несколько часов до проведения процедуры ПЭТ-КТ следует прекратить прием пищи, поскольку это может отрицательно повлиять на распределение радионуклидного вещества в тканях и, следовательно, внести искажение в результаты исследования. Соблюдение инструкций по подготовке к ПЭТ-КТ крайне важно: при неточности результатов на следующий день может потребоваться повторение процедуры. В течение нескольких часов до ПЭТ-КТ запрещается употребление содержащих сахар или высококалорийных жидкостей. Их следует заменить обычной водой. Пациентам, страдающим сахарным диабетом, необходимо соблюдать особые инструкции.
Очень важно сообщить врачу отделения лучевой диагностики обо всех препаратах, которые принимает пациент, а также о наличии аллергии любого типа, особенно на контрастные материалы, йодсодержащие вещества или морепродукты. Если врач посчитает риск возникновения аллергических реакций при внутривенном введении контраста высоким, то может потребоваться дополнительное обследование пациента.
При обычном рентгеновском исследовании изображение является результатом прохождения рентгеновских лучей, которые возникают во внешнем источнике, через организм пациента. В отличие от рентгенографии, ядерная медицина использует особые радиоактивные вещества под названием радиофармакологические препараты (радионуклиды) или радиоизотопные метки, которые вводятся в организм внутривенно. Радиоизотопные вещества задерживаются в обследуемом органе или участке тела и выделяют небольшое количество энергии в виде гамма-лучей. Исходящая энергия улавливается с помощью ПЭТ-сканера и далее, путем использования компьютерных программ, преобразуется в детальные изображения, которые помогают исследовать строение и функцию органов и тканей.
Процедуры с использованием методов радионуклидной диагностики проводятся амбулаторно, как правило в отделении ядерной диагностики. Перед обследованием пациент размещается в специальном кресле. Обычно радиоактивная метка вводится внутривенно, в жидком виде. Примерно в течение 45 минут введенный препарат перемещается по организму с током крови и накапливается в обследуемой ткани или органе. Все это время необходимо сохранять неподвижность, избегая каких-либо движений, и не разговаривать.
В некоторых случаях необходим дополнительный прием внутрь жидкого контрастного материала, который накапливается в кишечнике, что облегчает процесс интерпретации полученных результатов. Затем стол пациента перемещается внутрь ПЭТ-сканера, и начинается собственно обследование. Сначала проводится КТ, лишь после этого ПЭТ. Процедура ПЭТ КТ занимает от 15 до 20 минут. Таким образом, все обследование в клинике займет примерно один час.
Большинство процедур лучевой диагностики с использованием радионуклидных меток проходят безболезненно. Единственным исключением является момент постановки внутривенного катетера. ПЭТ-КТ крайне редко вызывает существенный дискомфорт или сопровождается выраженными побочными эффектами.
Внутривенное введение радиоизотопного материала через иглу, которая обычно устанавливается в вену локтевой ямки, сопровождается легким уколом. Инъекция радиоактивной метки может вызывать ощущение холода, которое распространяется по всей руке, однако другие нежелательные эффекты, как правило, не возникают.
Радиоактивные свойства введенного материала (радионуклида) со временем исчезают, что обусловлено естественными механизмами распада радиоизотопа. Кроме этого, после обследования радиофармпрепарат выводится с мочой и калом в течение нескольких часов или дней. Для ускорения процесса выведения радиоактивной метки из организма необходимо потреблять больше воды и других жидкостей, о чем пациента должен уведомить врач.
Отделение лучевой диагностики центра Neolife проводит точные и современные обследования на основе последних достижений ядерной медицины.
Читайте также:

