Взаимодействие оксида углерода с хлором
Задача 1. Взаимодействие оксида углерода (II) с хлором выражается уравнением:
Концентрация оксида углерода (II) равна 0,3 моль/л, а хлора - 0,2 моль/л. Как изменится скорость прямой реакции, если увеличить концентрацию оксида углерода (II) до 1,2 моль/л, а концентрацию хлора до 0,6 моль/л?
Решение. Скорость реакции взаимодействия оксида углерода (II) с хлором будет выражаться уравнением:
По условию задачи концентрация оксида углерода (II) была увеличена в 4 раза, а концентрация хлора - в 3 раза, поэтому для новых условий
Отсюда следует, что скорость данной реакции увеличится в 12 раз.
Задача 2. Скорость реакции А + 2В при [А] = 0,5 моль/л и [В] = 0,6 моль/л равна 0,018 моль/л · мин. Вычислить константу скорости реакции.
Решение. Скорость реакции будет выражаться уравнением
Из этого уравнения следует, что

k = 0,018 / 0,5 · 0,6 2 = 0,1 л 2 · моль -2 · мин -1
Задача 3. При какой температуре закончится некоторая реакция за 0,5 мин, если при 70°С она заканчивается за 40 мин? Температурный коэффициент реакции равен 2,3.
Решение. Из уравнения υ2/υ1 = γ (t 2 - t 1 ) / 10 находим t2:

Вопросы и задачи для самоконтроля
- Что такое скорость реакции? Что понимают под средней и истинной скоростью химической реакции? Как они могут быть определены?
- Сформулируйте правило Вант-Гоффа о влиянии температуры на скорость химической реакции. Что показывает температурный коэффициент скорости реакции? Как он выражается математически.
- Что такое катализ и какие вещества называются катализаторами? Покажите на конкретных примерах значение катализа в промышленности и жизни живых существ.
- Определите скорость реакции А + В = АВ при концентрациях [А] = 2 моль/л; [В] = 0,5 моль/л и константе скорости реакции 10 -3 моль -1 · л · с -1 .
- Как изменится скорость реакции
если молярную концентрацию оксида азота (II) увеличить в 2 раза, а молярную концентрацию кислорода - в 3 раза?
- Скорость некоторой реакции при нагревании на 20°С возросла в 9 раз. Определите температурный коэффициент скорости реакции.
- Реакция между веществами А и В выражается уравнением
Начальная скорость [А] равна 0,3 моль/л, [В] - 0,5 моль/л. Константа скорости реакции равна 0,4 л 2 · моль -2 · мин -1 . Чему будет равна скорость реакции в момент ее начала и по истечении некоторого времени, когда [А] уменьшится на 0,1 моль/л?
- Чему равен температурный коэффициент скорости реакции, если при увеличении температуры на 30° скорость реакции возрастает в 15,6 раза?
Урок посвящен изучению свойств и способов получения некоторых неорганических соединений углерода. В нем рассмотрены такие вещества, как оксид углерода (II) (или угарный газ), оксид углерода (IV) (или углекислый газ), угольная кислота, а также карбонаты и гидрокарбонаты.
I. Оксид углерода(II) – СО (угарный газ, окись углерода, монооксид углерода)
Физические свойства:
Бесцветный ядовитый газ без вкуса и запаха, горит голубоватым пламенем, легче воздуха, плохо растворим в воде. Концентрация угарного газа в воздухе 12,5—74 % взрывоопасна.
Строение молекулы:
Формальная степень окисления углерода +2 не отражает строение молекулы СО, в которой помимо двойной связи, образованной обобществлением электронов С и О, имеется дополнительная, образованная по донорно-акцепторному механизму за счет неподеленной пары электронов кислорода (изображена стрелкой):
Получение:
Основным антропогенным источником угарного газа CO в настоящее время служат выхлопные газы двигателей внутреннего сгорания. Угарный газ образуется при сгорании топлива в двигателях внутреннего сгорания при недостаточных температурах или плохой настройке системы подачи воздуха (подается недостаточное количество кислорода для окисления угарного газа CO в углекислый газ CO2). В естественных условиях, на поверхности Земли, угарный газ CO образуется при неполном анаэробном разложении органических соединений и при сгорании биомассы, в основном в ходе лесных и степных пожаров.
1) В промышленности (в газогенераторах):

CO2 + C = 2CO – 175 кДж
В газогенераторах иногда через раскалённый уголь продувают водяной пар:
смесь СО + Н2 – называется синтез – газом.
2) В лаборатории - термическим разложением муравьиной или щавелевой кислоты в присутствии H2SO4(конц.):
Химические свойства:
При обычных условиях CO инертен; при нагревании – восстановитель;
CO - несолеобразующий оксид.
1) Взаимодействие с кислородом: 2C +2 O + O2 t ˚ C → 2C +4 O2↑
2) Взаимодействие с оксидами металлов: CO + MexOy = CO2 + Me
C +2 O + CuO t ˚ C → Сu + C +4 O2↑
3) Взаимодействие с хлором (на свету)
CO + Cl2 свет → COCl2 (фосген – ядовитый газ)
4)* Взаимодействие с расплавами щелочей (под давлением)
CO + NaOH P → HCOONa (формиат натрия)
Влияние угарного газа на живые организмы:
Угарный газ опасен, потому что он лишает возможности кровь нести кислород к жизненно важным органам, таким как сердце и мозг. Угарный газ объединяется с гемоглобином, который переносит кислород к клеткам организма, в следствии чего тот становится непригодным для транспортировки кислорода. В зависимости от вдыхаемого количества, угарный газ ухудшает координацию, обостряет сердечно-сосудистые заболевания и вызывает усталость, головную боль, слабость, Влияние угарного газа на здоровье человека зависит от его концентрации и времени воздействия на организм. Концентрация угарного газа в воздухе более 0,1% приводит к смерти в течение одного часа, а концентрация более 1,2% в течении трех минут.
Применение оксида углерода:
Главным образом угарный газ применяют, как горючий газ в смеси с азотом, так называемый генераторный или воздушный газ, или же в смеси с водородом водяной газ. В металлургии для восстановления металлов из их руд. Для получения металлов высокой чистоты при разложении карбонилов.
II. Оксид углерода (IV) СO2 – углекислый газ
Учебный видео-фильм: “Углекислый газ”
Физические свойства:

Рис. 1. Сухой лед
Благодаря тому, что оксид углерода (IV) не поддерживает горения, им заполняют огнетушители.
Строение молекулы:
Все четыре связи ковалентые полярные.
Получение:
1. Термическим разложением солей угольной кислоты (карбонатов). Обжиг известняка – в промышленности:
2. Действием сильных кислот на карбонаты и гидрокарбонаты –
Способы собирания: вытеснением воздуха
3. Сгорание углеродсодержащих веществ:
4. При медленном окислении в биохимических процессах (дыхание, гниение, брожение)
Химические свойства:
1) С водой даёт непрочную угольную кислоту:
2)Рреагирует с основными оксидами и основаниями, образуя соли угольной кислоты:
3) При повышенной температуре может проявлять окислительные свойства – окисляет металлы: -СO2 + Me = MexOy + C
Качественная реакция на углекислый газ:
Помутнение известковой воды Ca(OH)2 за счёт образования белого осадка – нерастворимой соли CaCO3:

III. Угольная кислота и её соли
Химическая формула - H2CO3
Кислота слабая, существует только в водном растворе, очень непрочная, разлагается на углекислый газ и воду:
Химические свойства:
Для угольной кислоты характерны все свойства кислот.
1) Диссоциация – двухосновная кислота, диссоциирует слабо в две ступени, индикатор - лакмус краснеет в водном растворе:
2) с активными металлами
3) с основными оксидами
4) с основаниями
5) Очень непрочная кислота – разлагается
Соли угольной кислоты – карбонаты и гидрокарбонаты
Угольная кислота образует два ряда солей:
- Средние соли - карбонаты Na2СO3, (NH4)2CO3
- Кислые соли - бикарбонаты, гидрокарбонаты NaHCO3 , Ca(HCO3)2
В природе встречаются:
CaCO3



Мел Мрамор Известняк
NaHCO3 – питьевая сода


Na2CO3 – сода, кальцинированная сода
Na2CO3 x 10H2O – кристаллическая сода
Физические свойства:
Все карбонаты – твёрдые кристаллические вещества. Большинство из них в воде не растворяются. Гидрокарбонаты растворяются в воде.
Химические свойства солей угольной кислоты:
Общие свойства солей:
1) Вступают в реакции обмена с другими растворимыми солями
2) Разложение гидрокарбонатов при нагревании
3) Разложение нерастворимых карбонатов при нагревании
4) Карбонаты и гидрокарбонаты могут превращаться друг в друга:
Специфические свойства:
1) Качественная реакция на CO 3 2- карбонат – ион "вскипание" при действии сильной кислоты:
IV. Задания для закрепления
Задание №1. Закончите уравнения реакций, составьте электронный баланс для каждой из реакций, укажите процессы окисления и восстановления; окислитель и восстановитель:
Задание №2. Вычислите количество энергии, которое необходимо для получения 448 л угарного газа согласно термохимическому уравнению
CO2 + C = 2CO – 175 кДж
Задание №3. Закончите уравнения осуществимых химических реакций:
Реакции, взаимодействие углерода. Уравнения реакции углерода с веществами.










Углерод реагирует, взаимодействует с неметаллами, металлами, полуметаллами, оксидами, кислотами, солями, гидридами и пр. веществами.
Реакции, взаимодействие углерода с неметаллами. Уравнения реакции:
1. Реакция взаимодействия углерода и кислорода:
Реакция взаимодействия углерода и кислорода происходит с образованием оксида углерода (IV). Реакция представляет собой сжигание кокса на воздухе .
2C + O2 → 2CO (t > 1000 °C).
Реакция взаимодействия углерода и кислорода происходит с образованием оксида углерода (II).
2. Реакция взаимодействия бора и углерода:
4B + C → B4C (t > 2000 °C).
Реакция взаимодействия бора и углерода ( графит ) происходит с образованием карбида бора. Образуется также примесь B13C2.
3. Реакция взаимодействия углерода и серы:
C + 2S ⇄ CS2 (t = 750-1000 °C).
Реакция взаимодействия углерода и серы происходит с образованием сероуглерода.
4. Реакция взаимодействия углерода и водорода:
Реакция взаимодействия углерода и водорода происходит с образованием ацетилена .
Реакция взаимодействия углерода и водорода происходит с образованием метана . Реакция протекает самовольно при обычных условиях. В сторону образования метана равновесие сдвигается при наличии измельченного никелевого или платинового катализатора и высоких давлений.
5. Реакция взаимодействия аморфного углерода и фтора:
Реакция взаимодействия углерода и фтора происходит с образованием тетрафторида углерода .
6. Реакция взаимодействия углерода и кремния:
C + Si → SiC (t = 1200-1300 °C).
Реакция взаимодействия углерода и кремния происходит с образованием карбида кремния . Реакция протекает медленно.
Реакции, взаимодействие углерода с металлами и полуметаллами. Уравнения реакции:
1. Реакция взаимодействия углерода и бериллия:
2Be + C → Be2C (t = 1700-1900 °C).
Реакция взаимодействия бериллия и углерода ( графит ) происходит с образованием карбида бериллия. Реакция протекает в вакууме .
2. Реакция взаимодействия углерода (угля) и марганца:
3Mn + C → Mn3C (t = 1600 °C).
Реакция взаимодействия марганца и углерода ( угля ) происходит с образованием карбида марганца. Реакция протекает в вакууме.
3. Реакция взаимодействия углерода и железа:
Реакция взаимодействия железа и углерода происходит с образованием карбида железа.
4. Реакция взаимодействия углерода и гафния:
Hf + C → HfC (t = 1800-2000 °C).
Реакция взаимодействия гафния и углерода происходит с образованием карбида гафния .
5. Реакция взаимодействия углерода и циркония:
Zr + C → ZrC (t = 1800-2400 °C).
Реакция взаимодействия циркония и углерода происходит с образованием карбида циркония.
6. Реакция взаимодействия углерода и титана:
Ti + C → TiC (t = 1800-2400 °C).
Реакция взаимодействия титана и углерода происходит с образованием карбида титана .
7. Реакция взаимодействия углерода и вольфрама:
W + C → WC (t = 1430-1630 °C).
Реакция взаимодействия вольфрама и углерода происходит с образованием монокарбида вольфрама. Реакция протекает в атмосфере водорода.
8. Реакция взаимодействия углерода и алюминия:
Реакция взаимодействия алюминия и углерода происходит с образованием карбида алюминия .
9. Реакция взаимодействия углерода и натрия:
Реакция взаимодействия натрия и углерода происходит с образованием ацетиленида натрия.
Реакции, взаимодействие углерода с оксидами. Уравнения реакции:
1. Реакция взаимодействия углерода и оксида углерода (IV):
CO2 + C ⇄ 2CO (t = 700-1000 °C).
Реакция взаимодействия оксида углерода (IV) и углерода происходит с образованием оксида углерода (II). Реакция представляет собой взаимодействие углекислого газа с раскаленными углями.
2. Реакция взаимодействия углерода и оксида магния:
MgO + C → Mg + CO (t > 2000 °C).
Реакция взаимодействия оксида магния и углерода происходит с образованием магния и оксида углерода (II).
3. Реакция взаимодействия углерода и воды:
Реакция взаимодействия воды и углерода происходит с образованием оксида углерода (II) и водорода . Реакция представляет собой восстановление воды углеродом. Водяной пар при температуре свыше 1000°C взаимодействует с раскаленным коксом с образованием водяного газа (смеси водорода и оксида углерода (II)).
Реакция взаимодействия углерода и воды происходит с образованием оксида углерода (IV) и водорода.
4. Реакция взаимодействия углерода и оксида железа:
FeO + C → Fe + CO (t > 1000 °C).
Реакция взаимодействия оксида железа и углерода происходит с образованием железа и оксида углерода (II).
5. Реакция взаимодействия углерода и оксида меди:
C + CuO → Cu + CO (t = 1200 °C).
Реакция взаимодействия углерода и оксида меди происходит с образованием меди и оксида углерода (II).
6. Реакция взаимодействия углерода и оксида германия:
GeO2 + C → Ge + CO2 (t = 500-600 °C).
Реакция взаимодействия оксида германия и углерода происходит с образованием германия и оксида углерода (IV). Реакция протекает в атмосфере водорода.
7. Реакция взаимодействия углерода и оксида азота:
Реакция взаимодействия оксида азота (II) и углерода происходит с образованием азота и оксида углерода (IV).
8. Реакция взаимодействия углерода и оксида теллура:
TeO2 + C → Te + CO2 (t = 600-700 °C).
Реакция взаимодействия оксида теллура и углерода происходит с образованием теллура и оксида углерода (IV).
9. Реакция взаимодействия углерода и оксида цинка:
ZnO + C → Zn + CO (t = 1200-1300 °C).
Реакция взаимодействия оксида цинка и углерода происходит с образованием цинка и оксида углерода (II).
10. Реакция взаимодействия углерода и оксида серы:
Реакция взаимодействия оксида серы и углерода происходит с образованием серы и оксида углерода (IV).
11. Реакция взаимодействия углерода и оксида никеля:
NiO + C → Ni + CO (t = 300-400 °C).
Реакция взаимодействия оксида никеля и углерода происходит с образованием никеля и оксида углерода (II).
12. Реакция взаимодействия углерода и оксида марганца:
MnO2 + C → Mn + CO2 (t = 600-700 °C).
Реакция взаимодействия оксида марганца и углерода происходит с образованием марганца и оксида углерода (IV).
13. Реакция взаимодействия углерода и оксида свинца:
2PbO + C → 2Pb + CO2 (t = 600 °C).
Реакция взаимодействия оксида свинца и углерода происходит с образованием свинца и оксида углерода (IV).
14. Реакция взаимодействия углерода и оксида кремния (IV) :
SiO2 + C → SiO + CO (t = 1300 °C).
Реакция взаимодействия оксида кремния (IV) и углерода происходит с образованием оксида кремния (II) и оксида углерода (II). Реакция протекает в вакууме. Образуются примеси: кремний Si, карбид кремния SiC.
15. Реакция взаимодействия углерода, оксида магния и хлора:
MgO + Cl2 + C → MgCl2 + CO (t = 800-1000 °C).
Реакция взаимодействия оксида магния, хлора и углерода происходит с образованием хлорида магния и оксида углерода (II).
16. Реакция взаимодействия углерода, оксида кальция и хлора:
CaO + C + Cl2 → CaCl2 + CO (t = 1000 °C).
Реакция взаимодействия оксида кальция , углерода и хлора происходит с образованием хлорида кальция и оксида углерода (II).
17. Реакция взаимодействия углерода, оксида бериллия и хлора:
BeO + Cl2 + C → BeCl2 + CO (t = 700-900 °C).
Реакция взаимодействия оксида бериллия, хлора и углерода (графит) происходит с образованием хлорида бериллия и оксида углерода (II).
18. Реакция взаимодействия углерода, оксида титана и водорода:
Реакция взаимодействия оксида титана , углерода и водорода происходит с образованием карбида титана и воды.
19. Реакция взаимодействия углерода, оксида гафния и брома:
Реакция взаимодействия оксида гафния, углерода и брома происходит с образованием бромида гафния и оксида углерода (IV).
20. Реакция взаимодействия оксида углерода, циркония и брома:
Реакция взаимодействия оксида циркония, углерода и брома происходит с образованием бромида циркония и оксида углерода (IV).
Реакции, взаимодействие углерода с солями. Уравнения реакции:
1. Реакция взаимодействия углерода и карбоната лития:
Реакция взаимодействия карбоната лития и углерода происходит с образованием оксида лития и оксида углерода (II).
2. Реакция взаимодействия углерода (графита) и карбоната кальция:
CaCO3 + C → CaO + 2CO (t = 800-850 °C).
Реакция взаимодействия карбоната кальция и углерода (графита) происходит с образованием оксида кальция и оксида углерода (II).
3. Реакция взаимодействия углерода (кокса) и карбоната бария:
BaCO3 + C → BaO + 2CO (t > 1000 °C).
Реакция взаимодействия карбоната бария и углерода (кокс) происходит с образованием оксида бария и оксида углерода (II).
4. Реакция взаимодействия углерода и ортофосфата кальция:
Реакция взаимодействия ортофосфата кальция и углерода происходит с образованием фосфида кальция и оксида углерода (II).
5. Реакция взаимодействия углерода и сульфата магния:
2MgSO4 + C → 2MgO + 2SO2 + CO2 (t = 700-900 °C).
Реакция взаимодействия сульфата магния и углерода происходит с образованием оксида магния, оксида серы и оксида углерода (IV).
6. Реакция взаимодействия углерода (кокса) и сульфата кальция:
2CaSO4 + C → 2CaO + 2SO2 + CO2 (t = 1200-1400 °C).
Реакция взаимодействия сульфата кальция и углерода (кокса) происходит с образованием оксида кальция, оксида серы и оксида углерода (IV). Данная реакция представляет собой способ Мюллера-Кюна, применяемый для извлечения полезных соединений серы из агидрита и гипса. Реакцию проводят во вращающихся цилиндрических печах.
Реакции, взаимодействие углерода с кислотами. Уравнения реакции:
1. Реакция взаимодействия углерода и азотной кислоты:
Реакция взаимодействия углерода и азотной кислоты происходит с образованием оксида углерода (IV), оксида азота и воды. В ходе реакции используется концентрированный горячий раствор азотной кислоты.
Аналогичные реакции происходят и с другими кислотами.
Реакции, взаимодействие углерода с гидридами. Уравнения реакции:
1. Реакция взаимодействия углерода и гидрида лития:
Реакция взаимодействия гидрида лития и углерода происходит с образованием ацетиленида лития и ацетилена.
2. Реакция взаимодействия углерода и гидрида натрия:
Реакция взаимодействия гидрида натрия и углерода происходит с образованием ацетиленида натрия и ацетилена .
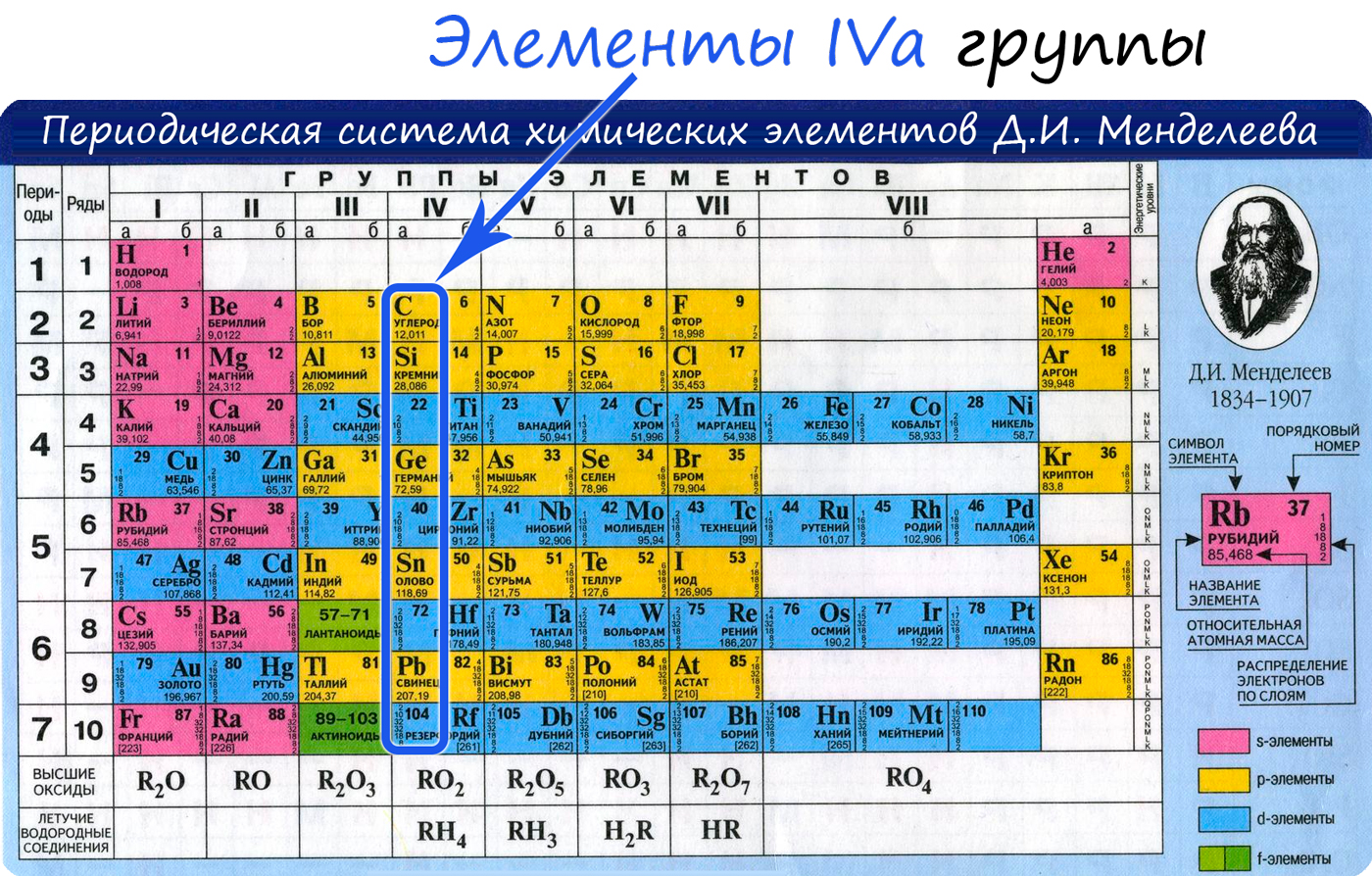
Углерод - неметаллический элемент IV группы периодической таблицы Д.И. Менделеева, является важнейшей частью всех органических веществ в природе.

От C к Pb (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Из элементов IVа группы углерод и кремний относятся к неметаллам, германий, олово и свинец - металлы.
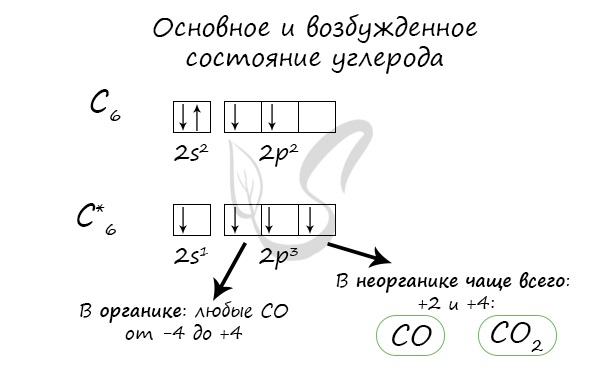
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2 np 2 :
- C - 2s 2 2p 2
- Si - 3s 2 3p 2
- Ge - 4s 2 4p 2
- Sn - 5s 2 5p 2
- Pb - 6s 2 6p 2
В природе углерод встречается в виде следующих соединений:
- Аллотропных модификаций - графит, алмаз, фуллерен
- MgCO3 - магнезит
- CaCO3 - кальцит (мел, мрамор)
- CaCO3*MgCO3 - доломит

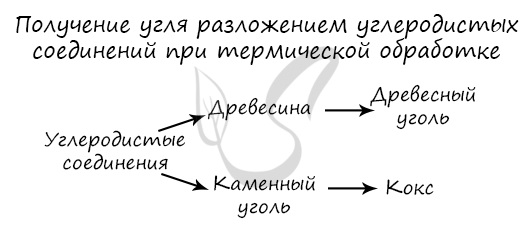
Углерод получают в ходе пиролиза углеводородов (пиролиз - нагревание без доступа кислорода). Также применяется получение углеродистых соединений: древесины и каменного угля.
- Реакции с неметаллами
При нагревании углерод реагирует со многими неметаллами: водородом, кислородом, фтором.
2С + O2 → (t) 2CO (угарный газ - продукт неполного окисления углерода, образуется при недостатке кислорода)
С + O2 → (t) CO2 (углекислый газ - продукт полного окисления углерода, образуется при достаточном количестве кислорода)
Реакции с металлами
При нагревании углерод реагирует с металлами, проявляя свои окислительные свойства. Напомню, что металлы могут принимать только положительные степени окисления.
Ca + C → CaC2 (карбид кальция, СО углерода = -1)
Al + C → Al4C3 (карбид алюминий, СО углерода -4)
Очевидно, что степень окисления углерода в соединении с различными металлами может отличаться.

Углерод - хороший восстановитель. С помощью него металлургическая промышленность справляется с задачей получения чистых металлов из их оксидов:
Углерод восстанавливает не только металлы из их оксидов, но и неметаллы подобным образом:
SiO2 + C → (t) Si + CO
Может восстановить и собственный оксид:

Известная реакция взаимодействия угля с водяным паром, называемая также газификацией угля, торфа, сланца - крайне важна в промышленности:
Реакции с кислотами
В реакциях с кислотами углерод проявляет себя как восстановитель:

Оксид углерода II - продукт неполного окисления углерода. Несолеобразующий оксид. Это чрезвычайно опасное вещество часто образуется при пожарах в замкнутых помещениях, при прогревании машины в гараже.
Растворяясь в крови угарный газ (имеющий в 300 раз большее сродство к гемоглобину, чем кислород) легко выигрывает конкуренцию у кислорода и занимает его место в эритроцитах. Отравление угарным газом нередко заканчивается летальным исходом.
В промышленности угарный газ получают восстановлением оксида углерода IV или газификацией угля (t = 1000 °С).
В лаборатории угарный газ получают при разложении муравьиной кислоты в присутствии серной:
Химические свойства
Полностью окисляется до углекислого газа в реакции с кислородом, восстанавливает оксиды металлов.
FeO + CO → Fe + CO2
Образование карбонилов - чрезвычайно токсичных веществ.

Продукт полного окисления углерода. Относится к кислотным оксидам, соответствует угольной кислоте H2CO3. Бесцветный газ, без запаха.
В промышленности углекислый газ получают при разложении известняка, в ходе производства алкоголя, при спиртовом брожении глюкозы.
В лабораторных условиях используют реакцию мела (мрамора) с соляной кислотой.
Углекислый газ образуется при горении органических веществ:

Химические свойства
-
Реакция с водой
В результате реакции с водой образуется нестойкая угольная кислота, которая сразу же распадается на воду и углекислый газ.
Реакции с основными оксидами и основаниями
В ходе реакций с основаниями и основными оксидами углекислый газ образует соли угольной кислоты: средние - карбонаты (при избытке основания), кислые - гидрокарбонаты (при избытке кислотного оксида).
2KOH + CO2 → K2CO3 + H2O (соотношение основание - кислотный оксид 2:1)
KOH + CO2 → KHCO3 (соотношение основание - кислотный оксид 1:1)
При нагревании способен окислять металлы до их оксидов.
Zn + CO2 → (t) ZnO + CO

Слабая двухосновная кислота, существующая только в растворах, разлагается на воду и углекислый газ.

Химические свойства
Определить наличие карбонат-иона можно с помощью кислоты: такая реакция сопровождается "закипанием" - появлением пузырьков бесцветного газа без запаха.
Я не раз встречал описание реакций, связанных с этой кислотой, которое заслуживает нашего внимания. В задании было сказано, что при добавлении к раствору гидроксида кальция углекислого газа осадок появлялся, при дальнейшем пропускании углекислого газа - помутнение исчезало.
Это можно легко объяснить, вспомнив про способность угольной кислоты образовывать кислые соли, которые растворимы.

Чтобы сделать из средней соли (карбоната) - кислую соль (гидрокарбонат) нужно добавить угольную кислоту. Однако написать ее формулу H2CO3 - ошибка. Ее следует записать в виде воды и углекислого газа.
Li2CO3 + CO2 + H2O → LiHCO3 (средняя соль + кислота = кислая соль)
Чтобы вернуть среднюю соль, следует добавить к кислой соли щелочь.
Нагревание солей угольной кислоты
При нагревании карбонаты распадаются на соответствующий оксид металла и углекислый газ, гидрокарбонаты - на карбонат металла, углекислый газ и воду.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Читайте также:

