Выживаемость при вторичном раке
Рак является одним из самых страшных заболеваний современности, и количество людей, страдающих от него, неуклонно растет. Вопросов о раке у обычных людей появляется много, и специалисты из Лондонского центра по исследованию и диагностике рака ответили на самые распространенные из них.
Сколько видов рака существует?
Всего известно около 200 разновидностей раковых заболеваний, некоторые из них встречаются реже, другие чаще. Не всегда боль является первым симптомом заболевания. Сами по себе раковые клетки не причиняют боль, но когда из-за них появляется опухоль, она может давить на органы человека, либо блокировать дыхательные пути. В таком случае появляется боль. Если болезнь развилась и распространилась на кости, то боль может быть симптомом.
Как рак убивает?
На ранних стадиях рак не убивает, смертельным он становится на последних. При определенных разновидностях рака выживают более 90 процентов пациентов.
Некоторые виды рака убивают посредством разрушения жизненно важных органов. Например, если он поражает легкое, то возникают проблемы с дыханием. Рак может заблокировать работу пищеварительной системы, и в таком случае организм не может всасывать питательные вещества. Если рак поражает кости или печень, то нарушается химический баланс организма.
Сколько стадий рака существует?
Специалисты выделяют четыре стадии рака:
первая стадия – локальный рак, то есть опасные клетки пока не распространяется за пределы очага заболевания.
вторая стадия означает, что опухоль, по сравнению с первой стадией, увеличилась. Может также означать, что раковые клетки распространились на соседние лимфатические узлы, могли проникнуть в кровь, повышая риск развития рака в любом органе.
третья стадия – опухоль большего размера, чем в первых двух стадиях. Раковые клетки распространились в соседние лимфатические узлы, и начинают проникать в расположенные рядом ткани и органы.
четвертая стадия, вторичный или метастатический рак. Раковые клетки распространились на другие органы тела. Люди живут и с четвертой стадией, но в этих случаях врачи чаще держат заболевание под контролем, а не вылечивают.
Можно ли определить, как давно начали развиваться раковые клетки?
Все пациенты задают этот вопрос. В случае с раком кожи можно удалить пораженный участок, и определить начало развития рака. С другими видами рака это сделать невозможно: он может развиваться годами до появления симптомов.
Если у пациента был уже рак, повышается ли риск развития рака другого типа?
Риск развития рака незначительно повышается из-за лечения на начальных стадиях. Если это была радиотерапия, особенно при раке груди, яичек и кожи, то она убивает раковые клетки, но, в то же время, повреждает здоровые клетки, которые могут мутировать в канцерогенные. Но этот риск незначительный.
Влияют ли раса и цвет кожи на риск развития рака?
В общем, нет, но некоторые виды рака чаще встречаются у "цветных" людей. Например, рак простаты чаще выявляют у жителей района Карибского моря, а рак крови – у чернокожих.
Какие виды рака наследственные?
Ученые обнаружили гены, ответственные за рак яичников, груди, матки и кишечника. Даже если у вас есть такие гены, это не означает, что рак у вас обязательно будет развиваться, но вы будете входить в группу повышенного риска его развития. Если вы захотите, вы можете пройти обследование и выяснить, передался ли вам этот ген. Рак простаты, яичек и поджелудочной железы также может наблюдаться у нескольких поколений, но их ген не обнаружен.
Какая разница между первичным и вторичным раком?
Рак называется первичным, если он локальный, то есть раковые клетки остаются в пределах очага заболевания. Вторичный рак наблюдается при отделении раковых клеток от первичной опухоли, их проникновении через кровеносную систему или лимфатические узлы в другой орган, и их развитии на новом месте.
Вторичный рак – это развитая форма рака, которую лечить сложнее. Когда раковые клетки попадают в кровь, опухоль может развиться на новом месте. В таких случаях доктора могут замедлить рост опухоли либо смягчить боль.
Почему нельзя лечить рак трансплантацией органов?
В случае, когда рак распространяется на другие органы, нет никакого смысла в трансплантации органа-очага заболевания, так как раковые клетки, уже проникшие в другие органы, будут развиваться на новом месте. К тому же, пациенту нужно будет пройти курс лечения против отторжения трансплантированного органа, что ослабит иммунную систему, которая борется с раком.
Можно ли заразиться раком от кого-то?
Нет, развитие раковых клеток – это внутренний процесс, и заразиться раковыми клетками невозможно.
Что происходит, когда семейный врач диагностирует рак?
Он должен направить пациента к специалисту. В большинстве случаев требуется хирургическое вмешательство, поэтому вначале пациент встретится с хирургом, затем специалист в области онкологических заболеваний решит, требуется ли терапия (химиотерапия, гормональная терапия) после операции. Если возникнет необходимость, пациента могут направить на радиотерапию к клиническому онкологу.
Могут ли диета и физические упражнения помочь в борьбе с раком?
Сбалансированная диета означает, что состояние здоровья пациента улучшиться перед началом лечения рака. Иммунная система сможет бороться с инфекцией, и выздоровление наступит раньше. Физические упражнения позволят чувствовать себя лучше, но нужно следовать предписаниям врача, и не переусердствовать с ними.
Влияет ли рак на способность иметь детей?
Это зависит от способа лечения рака: некоторые виды химио- и радиотерапии влияют на способность иметь детей. В случае с мужчинами это проще: они могут сдать сперму, а процедура замораживания яичниковой ткани женщин гораздо сложнее.
Почему нельзя оперировать при некоторых видах рака?
Если опухоль находится близко к основным органам, кровеносным сосудам, или у позвоночника, оперировать в таких случаях очень сложно. На последних стадиях, когда рак распространяется за пределы очага заболевания, оперирование неуместно.
Рак крови или костного мозга невозможно оперировать: в таких случаях применяют химиотерапию, радиотерапию, гормональное или биологическое лечение.
При каких видах рака выживаемость выше?
Выживаемость выше при раке яичек и простаты у мужчин, и у женщин с раком груди и матки, так как их можно раньше удалить.

Прогноз выживаемости при раке
Важен и такой показатель, как относительная выживаемость. При его подсчёте учитывают количество лиц, страдающих раком определённой локализации, которые умерли от сопутствующей патологии. Выживаемость при раке зависит от стадии заболеваемости, пола, возраста и, чувствительности к проводимому лечению и наличия фоновых заболеваний.
Согласно данным ВОЗ (Всемирной организации здравоохранения) смертность от онкологической патологии увеличилась за последнее время на 11%. Рост заболеваемости раком отмечают у детей и лиц среднего возраста. Так, в 2011 году распространённость злокачественными новообразованиями составила 15000 на 100000 жителей страны, в Украине – 1520, а в Беларуси – 1514.
Структура онкологических заболеваний выглядит таким образом:
рак лёгкого, бронхов и трахеи, - 13,8%;.
новообразования кожи - 11,0%, меланома - 12,4%;
опухоли желудка составили - 10,4%;
рак молочной железы установлен в 10,0%;
неопроцесс ободочной кишки - 5,9%, прямой кишки, прямокишечно-сигмовидного соединения и анальной области - 4,8%;
онкопатология лимфатической и кроветворной системы - 4,4%;
шейки матки - 2,7% ,рак тела матки - 3,4%, а яичников - 2,6 %,
опухоли почек - 3,1%;
злокачественные новообразования поджелудочной железы - 2,9 %;
рак мочевого пузыря - 2,6 %.
Выживаемость после лечения рака предполагает подсчёт количества пациентов, которые выжили в течение определённого периода после проведенного радикального или паллиативного лечения. Учитывается двухлетняя, пятилетняя, семилетняя и десятилетняя выживаемость.
Процент выживаемости при раке различной локализации
Рассмотрим показатели выживаемости при различной локализации злокачественных новообразований в зависимости от стадии заболевания. Для этого, прежде всего, определимся со стадиями рака. Наиболее приемлемой для определения прогноза выживаемости является классификация TNM, в которой T – размер опухоли, N – поражение лимфатических узлов, а M – наличие метастазов в отдалённых органах.
Прогноз выживаемости при раке кожи определяется, прежде всего, стадией заболевания. Он зависит и от гистологической структуры опухоли, а также степени дифференцировки раковых клеток.
Рак 1 степени. Прогноз таков: излечение наступает у 100% пациентов.
Рак 2 степени. Прогноз для выздоровления удовлетворительный у 86% пациентов.
Рак 3 степени. Прогноз выздоровления – 62%.
Рак 4 стадии. Прогноз пятилетней выживаемости 12%.
Меланома является чрезвычайно агрессивной опухолью, которая происходит из пигментных клеток. Прогноз выживаемости зависит от стадии болезни, локализации опухоли и степени дифференциации атипичных клеток.
При I стадии меланомы до пяти лет живут около 97% пациентов.
При II стадии пятилетняя выживаемость составляет 65%.
При III стадии рака процент выживаемости –37%.
При IV стадии заболевания до одного года доживает всего 15%пациентов.
Прогноз выживаемости при раке нижней губы находится в прямой зависимости от стадии заболевания, возраста пациента, степени дифференцировки опухоли и её чувствительности к лучевой терапии:
A. При I стадии до пяти лет живут 70% пациентов.
B. При II стадии пятилетняя выживаемость 59% .
C. Когда в III стадии определяют рак, процент выживаемости всего 35%.
D. При IV стадии рак губы до одного года доживает 21% болеющих людей.
Многим пациентам ставят диагноз рак ротовой полости. Процент выживаемости у них зависит не только от стадии заболевания, но и от формы роста опухоли, степени дифференцировки раковых клеток и возраста пациента. Прогноз выживаемости показан на таблице №1.
Таблица №1.Прогноз выживаемости при раке слизистой оболочке ротовой полости
Процент пятилетней выживаемости
Опухоль ротовой полости – это достаточно агрессивный рак. Процент выживаемости до одного года – всего лишь 16.
Динамику пятилетней выживаемости при раке щитовидной железы в зависимости от стадии заболевания можно увидеть на графике №1.
График №1. Динамика пятилетней выживаемости при разных стадиях рака щитовидной железы.

Трагическая судьба пациентов при выявлении неоперабельного рака лёгких: 90% из них погибает в течение первых двух лет после установления диагноза. При одном выполненном хирургическом вмешательстве в течение пяти лет выживает 30% пациентов, у которых в лёгких диагностирован рак. Процент выживаемости при радикальном комплексном лечении рака лёгких можно увидеть на таблице№2.
Таблица №2. Пятилетняя выживаемость пациентов, страдающих раком лёгких, в случае полноценного радикального лечения
Процент пятилетней выживаемости
Выживаемость после радикального оперативного лечения рака пищевода является чрезвычайно информативным показателем. Она представлена на таблице №3.
Таблица №3. Пятилетняя выживаемость после оперативных вмешательств по поводу рак пищевода
Конечно же, на показатель выживаемости пациентов, страдающих раком пищевода, влияет и стадия заболевания. При первой стадии онкологического процесса процент пятилетней выживаемости наиболее высокий: он составляет 57%. В течение пяти лет выживает 43% людей, у которых выявлен рак пищевода второй стадии. При третьей стадии заболевания в течение пяти лет живут 25% больных людей. К сожалению, только пациентов, у которых рак пищевода диагностирован на четвёртой стадии, выживают один год.


03 марта 2016, 14:23
Рак грудины – злокачественное новообразование, развивающееся в результате мутации костных клеток. В большинстве случаев он.

03 марта 2016, 14:17
Рак желудка до сих пор является одним из наиболее распространённых злокачественных новообразований органов пищеварения. В.

03 марта 2016, 14:09
Рак молочной железы относится к визуальным формам рака. Это значит, что опухоль на ранней стадии.
В онкологии шансы пациентов на выживаемость принято измерять пятилетним периодом.
Именно на его протяжении собирается необходимая статистика, на основании которой выводится т.н. коэффициент выживаемости, выраженный в проценте пациентов, которые остаются в живых спустя 5 лет после выявления злокачественной опухоли.
Этот показатель, как и любые другие статистические данные, в известной мере представляет из себя весьма приблизительную величину , поскольку имеет обобщенный характер, основан на устаревших данных, не учитывающих текущий уровень медицинской помощи, а главное – никак не отражает индивидуальных особенностей пациента: общего состояния здоровья, образа жизни, индивидуальных реакций на лечебное воздействие.
Другими словами, пятилетний коэффициент выживаемости не может предсказать, как будет проходить заболевание в данном конкретном случае. И только лечащий врач, знакомый со всеми деталями истории болезни, может объяснить пациенту, как интерпретировать статистические данные в отношении его ситуации.
И все же выживаемость очень четко коррелируется с видами онкологических заболеваний и их стадиями.
Мужчины чаще всего умирают от злокачественных опухолей легких, желудка, прямой кишки и предстательной железы, а для женщин особенно губителен рак молочных желез и рак шейки матки.
Прогнозы на выздоровление при раке легких
Прогнозы выживаемости при раке желудка
Начальные стадии рака желудка дают прогноз выживаемости на отрезке пяти лет от 80%. А вот с третьей и четвертой стадиями пациенты доживают до принятого в онкологии временного рубежа существенно реже – в 10-20% случаев.
Выживаемость при раке толстой кишки и кишечника
Выживаемость пациентов со злокачественными новообразованиями прямой кишки находится в прямой зависимости от глубины прорастания опухоли и наличия вторичных очагов патологии.
На ранних стадиях болезни пятилетний коэффициент выживаемости достигает 65-74% при условии проведения необходимой терапии. Последующие стадии при проведении операции дают показатель в диапазоне 5-30%.
Прогноз выживаемости при раке простаты
Чем раньше удастся диагностировать опухоль простаты – тем лучше. Ранняя стадия обнаружения болезни, которая на первых порах протекает, к сожалению, бессимптомно, обеспечивает выживаемость на уровне 75-85%. А вот на поздних стадиях патологии больные живут в среднем один-два года.
Процент выживаемости при раке молочной железы
Среди всех видов онкологической смертности среди женщин рак грудной железы безоговорочно лидирует. При этом почти 50% пациенток с таким диагнозом успешно минуют первое пятилетие, а 35% живут и до 10 лет.
Вероятность выживаемости при раке шейки матки
До пяти лет после в зависимости от стадии заболевания доживают 5-85% женщин с диагнозом злокачественная опухоль шейки матки. Причем на самых ранних стадиях дается прогноз с 85-90% пятилетней выживаемости. Прямо противоположная картина на поздних этапах: здесь показатель не превышает 7%.
Выживаемость при раке печени
Больные раком печени преодолевают пятилетний срок только в 10% случаев. Но не стоит пугаться этой цифры, поскольку печальной статистике потворствует не сам рак, а наличие у пациента не менее смертельных заболеваний – того же цирроза печени. В случае отсутствия сопутствующих обременений и при правильной терапии выживаемость достигает 50-70%.
Рак яичников: прогноз выживаемости
Первая стадия рака яичников характеризуется выживаемостью до 75% на пятилетнем горизонте, вторая стадия снижает показатель до 55-60%, третья стадия дает лишь 15-20% положительных исходов, четвертая – не более 5%.
Выживаемость при раке кожи
Долгие годы наблюдений за пациентами с раковыми поражениями кожи вселяют оптимизм: если в послевоенные годы выживаемость составляла 49%, то в 2010 г. она была уже 92%.
Более того, больные с этим диагнозом не только стали жить дольше, многие из них успешно излечиваются от недуга.
При этом на конкретные цифры влияет возраст больных: чем они старше, тем хуже прогноз.
Шансы на выздоровление при раке головного мозга

Учитывая накопившийся в онкологии опыт, происходят и изменения в тактике лечения рака. В 1980-х годах, врачи начинали работу над уничтожением опухоли как бы с тонкой настройки, которая помогла бы уберечь пациентов от развития вторичного рака и других, связанных с лечением побочных эффектов. Эти усилия включали назначение меньшего количества циклов химиотерапии или более низкие дозы некоторых лекарств.
Другие изменения включают назначение меньших доз радиации, направленной на более целенаправленные области тела или с использованием различных источников излучения, которые могут внести меньшие риски возникновения вторичного рака. Многие исследователи в настоящее время кроме непосредственно самого лечения рака, тщательно оценивают генетику и повседневные привычки человека, чтобы создать идеальную преграду для развития вторичного рака. Фридман в настоящее время анализирует данные из исследования, в котором она изучала гены пациентов, получавших радиотерапию перед трансплантацией стволовых клеток.
Она пытается выяснить, являются ли определенные пациенты генетически более чувствительны к радиации, и какова роль употребления табака и загорания на солнце как до, так и после лечения, то есть изучает факторы, которые могут приводить к развитию вторичного рака.
Также знание поведения человека в разном возрасте может позволить докторам настроить лечение некоторых пациентов так, чтобы передвинуть возможность развития вторичного рака на более поздний возраст. Например, генетические различия могут привести к медленному метаболизму после химиотерапии, что приведет к длительному присутствию токсичных химических веществ в организме. “Мы могли бы назначать таким пациентам индивидуальные дозы химиотерапии, уменьшая риск возникновения вторичного рака”, говорит Фридман.
Аналогично, организация по исследованию детского рака Children’s Oncology Group, ищет, как гены детского организма могут увеличить риск развития вторичного рака после проведенного лечения. Результаты исследования 2001 года, опубликованные в журнале Journal of Clinical Oncology показывают, что у одного из 10 оставшихся в живых после лечения детского рака, развивается вторичный рак, хотя этот риск зависит от исходного типа рака.
Что может сделать лично каждый
Возможно, будет трудно пациенту сосредоточиться на разговоре о профилактике рака в разгар лечения. “Вы говорите им о риске вторичного рака в начале терапии и, что у большинства пациентов такое возможно. Ага, ну да”, говорит Фридман. “Они борются за свои жизни в тот момент, и их ум в другом месте”.
Тем не менее, обсуждение необходимо при постановке диагноза исходя из онкологической истории семьи пациента и возможных генетических онкологических рисков, а также определение потенциала для некоторых процедур, чтобы увеличить вероятность развития вторичного рака в более позднем возрасте. Это должно последовать со вторым разговором после лечения, когда пациент находится в состоянии ума “Что теперь?”.

Оставшиеся в живых после лечения рака должны говорить со своими врачами о рисках развития у них вторичного рака и попросить индивидуальный план выживаемости, который детализирует, как уменьшить этот риск, считают эксперты. Многие лечебные центры в США уже начала подобные разговоры. Например, в онкологическом институте Дана-Фарбера в Бостоне, все выжившие после лечения рассказывают о своих индивидуальных рисках развития вторичного рака, говорит онколог Энн Партридж, которая руководит программой выживаемости для взрослых. Выжившие также консультируются о здоровом образе жизни, который сможет снизить риски и о методах контроля возможного развития вторичного рака, которые они должны использовать.
Оставшиеся в живых после лечения детского рака, как показали исследования, которые могут быть особенно восприимчивы к воздействию лечения рака, должны следовать руководящим принципам диагностики рака, разработанным специально для них, говорит Трэвис. Возьмите женщин, получавших облучение груди для лимфомы Ходжкина в молодом возрасте. Поскольку они сейчас имеют повышенный риск развития рака молочной железы, их врачи должны определить, нуждаются ли они в ежегодной маммографии и МРТ груди, начиная с возраста 25 лет, или от пяти до 10 лет после воздействия радиации. Рекомендации по диагностике для оставшихся в живых после лечения рака опубликованы в Journal of Clinical Oncology в октябре 2012 года.
Через 16 лет после того как Дейл Смит лечился от рака яичек с метастазами в легких, на очередном тестировании с помощью компьютерной томографии в 2010 году у него была обнаружена опухоль в почке. Вторичный рак не имеет ничего общего с первым, сказали Смиту врачи, и его бы не нашли, если бы он не продолжал периодически обследоваться по поводу рака яичек.
“Пять лет я утверждал: вылечено! Однако я продолжал видеться с моим онкологом каждые три года для прохождения томографии. И я доволен, что это делал”, говорит Смит, 66-летний пенсионер. Впоследствии у него удалили часть почки с опухолью.
Оставшиеся в живых должны также воспользоваться онкологическими диагностическими процедурами, рекомендованными для их возраста, указывает Партридж. Это означает, что, например, 50-летняя женщина, выжившая после лечения рака молочной железы, по-прежнему нуждается в контроле ее толстой кишки, на основе руководящих принципов американского общества рака. “У меня было несколько больных раком молочной железы, у которых со временем развился рак толстой кишки”, говорит Партридж. “Частично это может быть просто потому, что это не редкий рак, и люди становясь старше, получают их оба”.

Трэвис говорит, что взрослые люди, пережившие первый рак, должны сосредоточиться на развитии здорового образа жизни. Не курить, не пить слишком много алкоголя, поддерживать нормальную массу тела и все это на регулярной основе.
Возвращаясь к истории Авиды Рамезанифар, следует сказать, что сейчас рак занимает в ее жизни лишь несколько дней в году, когда она подвергается последующей процедуре МРТ головного мозга и сканированию всего тела. “Мои врачи говорят, что я склонна к тому, что у меня может развиться вторичный рак, когда я стану старше, так как я имела лечение от рака в таком молодом возрасте”, говорит она. “Но теперь я буду готова к этому”.
Новому росту опухоли, как правило, предшествует период ремиссии. Ее длительность зависит от того, как долго организм будет восстанавливаться. Рецидив злокачественной опухоли может быть ранним (образование раковой опухоли происходит через 2-4 месяца после окончания основного курса лечения) и поздним (вторичное онкологическое поражение диагностируется спустя 2-4 года).
- Очень важно, чтобы операция по удалению опухоли была выполнена профессионально, - говорит онколог Алексей Дикарев. - Рецидив рака может быть связан с проведением неполноценного или некачественного лечения, что провоцирует вторичные проявления заболевания.

Сложнее всего онкологам лечить пациентов с так называемыми запущенными формами рака, где опухоль начала прорастать.

- На разных этапах онкологического заболевания требуется оценить эффективность лечения, степень распространенности процесса. Поэтому очень важно, чтобы пациент своевременно проходил обследования – современная медицина располагает высокотехнологичными инструментами диагностики.
Мультидисциплинарный подход к лечению больных обеспечивает не только качественную диагностику и правильно подобранный курс процедур, но и постклиническую реабилитацию, социальную адаптацию и помощь профессионального психотерапевта. Задача наших специалистов – победить болезнь и бороться за качество жизни российских онкологических больных.
У пожилых людей, замечено, рецидивы рака случаются чаще.
Медики отмечают, что очень важно, чтобы первый этап лечения был выполнен профессионально.


После того, как человек побеждает рак, велика вероятность впадения в крайности. В еде это отражается на кардинальной смене рациона. На столах появляется много высококалорийной пищи, ввиду необходимости набора веса. Во втором варианте рацион изобилует теми продуктами, которые якобы борются с раком. Вся эта пища потребляется бесконтрольно и в ущерб всему остальному.
Однако онкопациенту нужно придерживаться принципов правильного питания, что и остальным людям. Упор на овощи и фрукты, больше продуктов, содержащих клетчатку, меньше мяса и больше рыбы, ограничить животные жиры, мясную кулинарию, выпечку, свести до минимума потребление соли.
Также нужно держать свой вес. Особенно надо избегать полноты и лишнего веса. Кроме того, не стоит зацикливаться в поисках специфических продуктов с якобы противоопухолевой активностью. Эффект их, как правило, сомнителен, а вот неумеренное потребление может оказаться проблематичным.


Регулярные и умеренные физические нагрузки способствуют укреплению иммунитета и помогают избежать рецидива онкологии.
- Многочисленные исследования доказывают — даже самому ослабленному пациенту (не обязательно онкологическому), даже прикованному к кровати посильные регулярные физические нагрузки улучшают прогноз и качество жизни! Пока есть силы шевелиться, надо это делать! - советует доктор Александр Мясников. - Что же касается подавляющего числа людей, перенесших онкологическое лечение, к ним относится общий постулат всех докторов: каждый должен посвятить какому-то виду физической нагрузки минимум полчаса в день пять раз в неделю!
Средняя продолжительность жизни при карциноматозе брюшины без лечения – от 1,5 до 6 месяцев. Лечить же таких больных еще совсем недавно было нечем. Ни хирургия, ни химиотерапия не справлялись. Пациентов признавали инкурабельными (неизлечимыми). Показатель 5-летней выживаемости в начале 90-х был практически равен 0.
Но последние 20 лет активно развивается методика лечения перитонеального канцероматоза с применением HIPEC (англ. hyperthermic intraperitoneal chemotherapy) – гипертермической интраперитонеальной (внутрибрюшинной) химиотерапии. Методика дает отличные результаты: увеличивает 5-летнюю выживаемость до 40-50%, а иногда дает полное излечение.
Самое плохое – даже многие врачи не знают, что при канцероматозе существует способ продлить жизнь. Поэтому сегодня мы расскажем про HIPEC подробно: кому это поможет, какие дает результаты и сколько стоит.
Цель – уничтожить максимум опухолевых клеток, которые неизбежно останутся даже после самого тщательного хирургического удаления очагов и спровоцируют рецидив.
Свойства, которые делают HIPEC действительно уникальной методикой, мы разъясним чуть ниже, а сначала определимся, при каких диагнозах она может помочь и почему она иногда оказывается единственным способом продлить жизнь человеку на последних стадиях рака.
При каких опухолях образуется канцероматоз брюшины, и почему он так опасен
В брюшную полость распространяются многие из часто встречающихся видов рака.
- рак яичников – в 60-70% случаев приводит к канцероматозу;
- рак желудка – канцероматоз в 40-50% случаев;
- рак поджелудочной железы – в 30-40% случаев;
- рак толстой и прямой кишки (колоректальный рак) – в 10-15% случаев;
- рак печени;
- рак шейки матки;
- рак червеобразного отростка (аппендикса);
- редкие первичные опухоли брюшины (мезотелиома и псевдомиксома).
Все эти злокачественные новообразования распространяют раковые клетки либо когда первичная опухоль физически прорастает в брюшную полость, либо вместе с током крови и лимфы – иногда это происходит во время хирургических операций по поводу первичных опухолей.
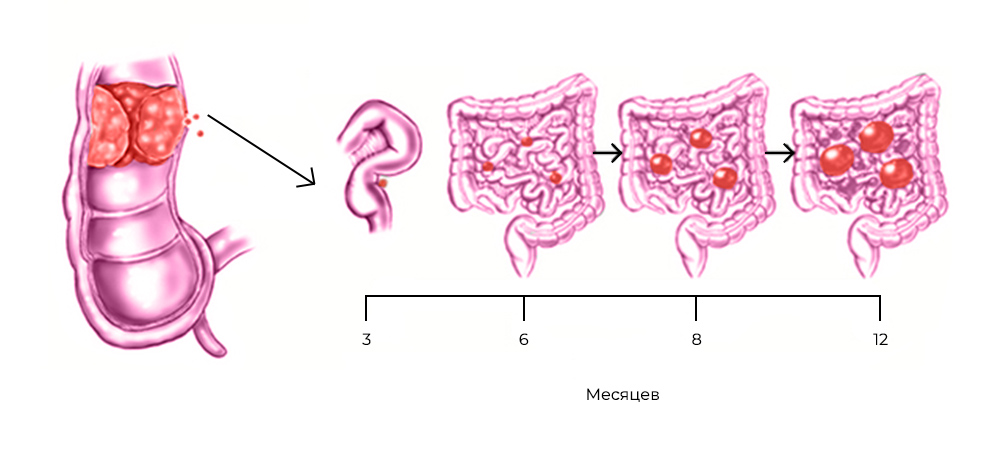
Развитие канцероматоза при колоректальном раке: из прямой кишки в брюшную полость
Стоит раковым клеткам попасть в полость, ограниченную брюшиной – они, скорее всего, дадут начало вторичным опухолям, метастазам. Перитонеальная ткань – богатый источник факторов роста и комфортная среда для их развития. Микроскопические метастазы распространяются по поверхности брюшины, поражают внутренние органы.
Метастазы нарушают кровоток и лимфоток, лишают внутренние органы питания и пространства, зачастую становятся причиной непроходимостей (например, кишечной, или сдавливают мочеточники). Кроме того, это провоцирует асцит – выпот и скопление жидкости в брюшной полости – наиболее распространенный симптом при канцероматозе.
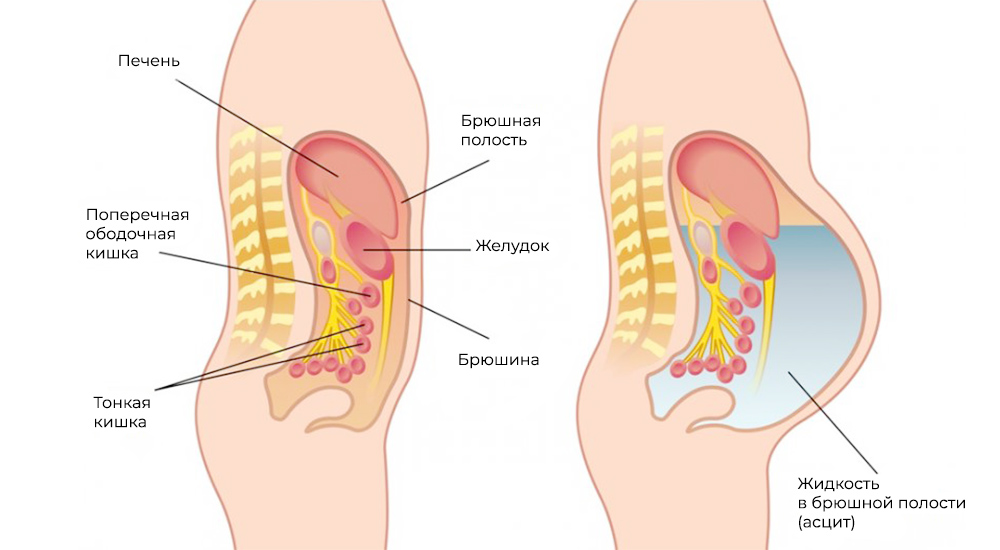
Асцит – скопление жидкости в брюшной полости
Застой крови и лимфы, интоксикация, сдавление внутренних органов метастазами и/или скопившейся жидкостью при асците – это причины, почему пациенты с канцероматозом без лечения не проживают и года.
На протяжении почти всей истории онкологии считалось, что перитонеальный карциноматоз и опухоли брюшины не поддаются никакому из существующих видов лечения.
Лучевая терапия в лечении канцероматоза не применяется, поскольку высокие дозы облучения такой обширной области живота опасны для пациента еще более серьезными осложнениями.
Хирургическое лечение малоэффективно, т.к. метастазы на поверхности брюшины могут быть микроскопического размера, либо расположены в недоступных местах, и врач не видит их во время операции. А для быстрого рецидива канцероматоза достаточно и единичных раковых клеток, оставшихся в полости брюшины.
Системная химиотерапия почти не дает чувствительного воздействия на опухоли брюшины –опухолевые очаги размером до 3 мм (таких при канцероматозе большинство) практически не развивают систему собственных кровеносных сосудов – и поэтому слабо доступны для системной внутривенной химиотерапии.
Вводить химиотерапию в более высоких дозах, чтобы повысить концентрацию препаратов в перитонеальной области – невозможно, т.к. это может необратимо навредить остальным органам и тканям, до которых доберется перенасыщенный химиопрепаратом кровоток.
Во второй половине 20 века появились первые работы, рассказывающие о возможностях применения внутрибрюшинной химиотерапии. Последние 20 лет это направление активно развивается, а создал его еще в 80-х годах XX века американский хирург-онколог Пол Шугабейкер – он первым придумал совместить циторедуктивную операцию с горячей химиотерапией, вводимой непосредственно в брюшную полость. И это дало результат
Гипертермия – это повышение температуры.
- Высокая температура сама по себе способна вызывать повреждение и гибель опухолевых клеток. К тому же, делает их более уязвимыми для действия химиопрепаратов: усиливает проницаемость клеточных мембран.
- Причем чувствительность увеличивается избирательно – опухолевые клетки начинают гибнуть при температуре 40 °C, а здоровые – сохраняются до 44°C. В условиях гипертермии особенности опухолевых тканей (иное кровоснабжение, степень оксигенации, особенности репарации ДНК) становятся для них не преимуществом, а слабым местом.
- Кроме того, повышение температуры обычно вызывает иммунную реакцию: растет количество лимфоцитов – клеток иммунитета, способных уничтожать опухолевые клетки. В плазме крове увеличивается уровень интерлейкинов, интерферонов, факторов некроза опухоли и т.д. Все они имеют собственную противоопухолевую активность, и дополнительно способны усиливать эффект некоторых химиопрепаратов.
- Еще один важный плюс гипертермии – она способствует более активному проникновению препарата в ткани – на глубину до 3 мм – этого хватит, чтобы охватить большинство микро-метастазов, которые останутся после хирургической операции.
Внутри брюшины – химиотерапия работает лучше. Для HIPEC используются стандартные химиопрепараты, но их локальное применение при перитонеальном карциноматозе – куда эффективнее.
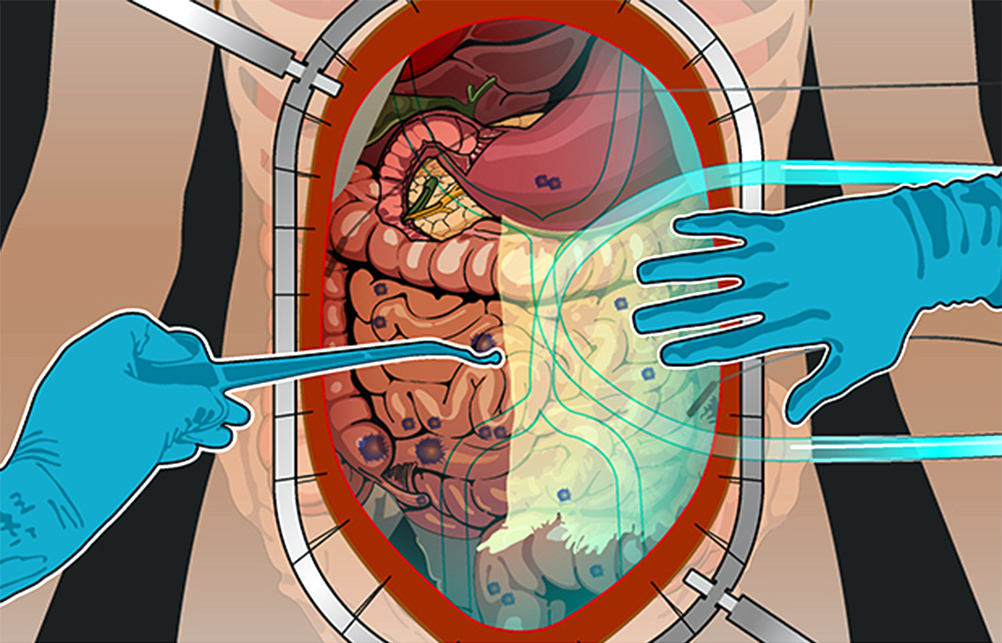
Процедура HIPEC – это, строго говоря, вторая половина целого комплекса мероприятий. Без циторедуктивной хирургической операции HIPEC может проводиться в считанном количестве случаев по особым показаниям. Обычно процедура – продолжение хирургической операции, которое дает серьезное улучшение прогноза выживаемости.
Вместе с удалением опухолевых очагов, все вмешательство занимает от 6 до 18 часов. Процесс можно разделить на 4 этапа.
1) Ревизия брюшной полости. Проводится она для того, чтобы понять, показано ли лечение с помощью HIPEC для этого пациента, принесет ли оно увеличение продолжительности жизни и улучшение ее качества. Во время ревизии хирург внимательно осматривает брюшную полость и определяет перитонеальный индекс рака (peritoneal cancer index – PCI).
Чтобы его рассчитать, брюшную полость и тонкую кишку условно делят на 13 областей-квадрантов, в каждом из них оценивают самый крупный опухолевый очаг по шкале от 0 до 3:
- очагов не обнаружено — 0 баллов;
- очаги размером менее 0,5 см — 1 балл;
- очаги размером менее 0,5–5 см — 2 балла;
- очаг более 5 см или несколько узлов меньшего размера— 3 балла.
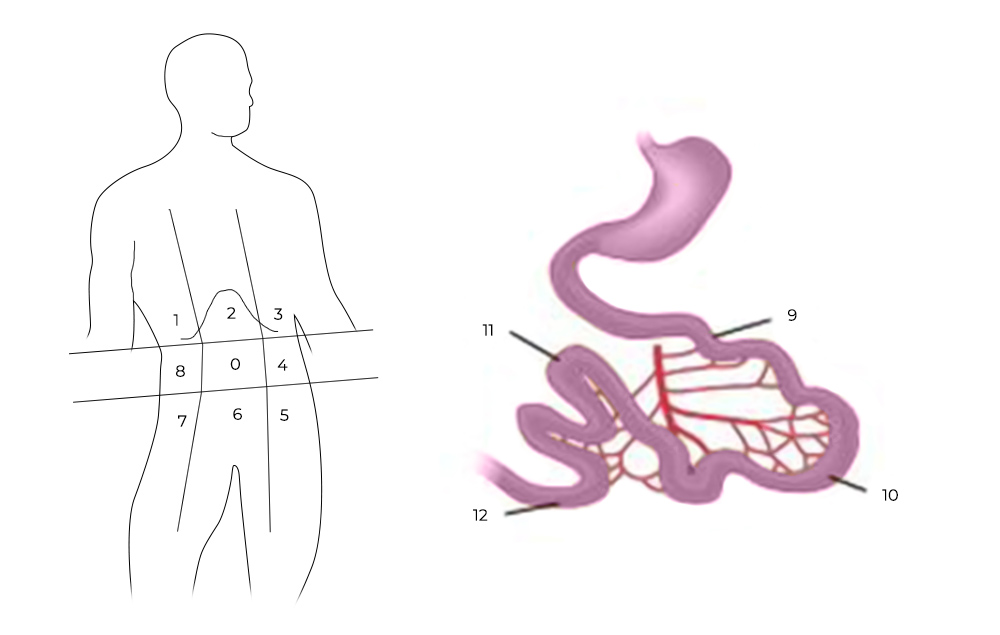
Разделение брюшной полости на участки для определения PCI
Баллы суммируются по всем квадрантам – это и есть значение PCI. Чем больше баллов – тем хуже прогноз. Если PCI выше критического (принимая во внимание тип опухоли и состояние пациента) – то и операцию, и процедуру HIPEC могут признать нецелесообразными.
Проводят ревизию интраоперационно – т.е. непосредственно перед проведением основной операции. В некоторых случаях ее можно провести в виде отдельной диагностической лапароскопической операции – малотравматичной, через небольшие проколы в стенке живота.
2) Циторедуктивная операция. Если по результатам ревизии PCI оценен как удовлетворительный, то хирург приступает к удалению всех видимых и пальпируемых (те, что чувствуются наощупь) опухолевых узлов.
Удаляют отдельные участки брюшины, орган, в котором находится первичная опухоль, соседние внутренние органы или их части, если они тоже поражены метастазами. Часто это участки кишечника, селезенка, желчный пузырь.
3) Гипертермическая интраперитонеальная химиотерапия. Собственно, HIPEC. В брюшную полость вводят катетеры и температурные датчики, соединенные со специальным аппаратом и емкостью с раствором химиопрепарата. Эта перфузионная система (под контролем врачей, конечно) поддерживает заданную температуру и давление циркулирующей жидкости. Раствор химиопрепарата в течение 60–90 минут циркулирует в брюшной полости пациента.
После процедуры препарат удаляют из брюшной полости, промывают ее физраствором, удаляют датчики и катетеры.
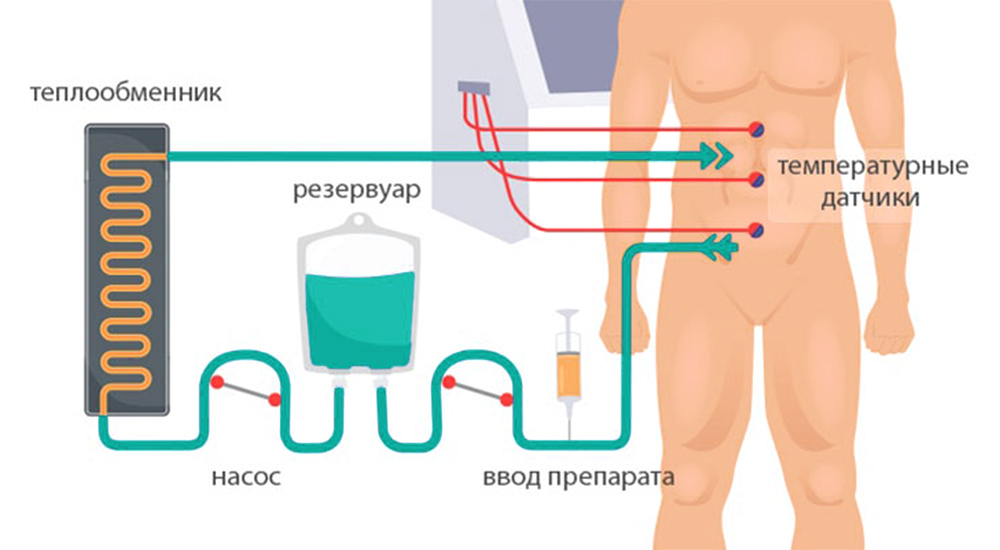
Схема проведения HIPEC
4) Реконструктивная операция. Если удалены части кишечника, хирург восстанавливает непрерывность кишки – формирует анастомоз, выводит верхний конец толстой/тонкой/слепой кишки на поверхность живота для отхождения каловых масс.
В среднем, в клинике пациент проводит 2-4 недели. Через 2-3 недели после операции проводится контрольное обследование. Его необходимо повторять через 3 месяца, и постепенно частоту проверок снижают до 1 раза в год.
В этом видео наши коллеги проводят процедуру HIPEC пациентке с раком яичников.
Как любое лечение, HIPEC имеет риски и противопоказания
Послеоперационный период стоит отдельным этапом, но он не менее важен. Мы всегда понимаем, насколько сложным для наших пациентов (а многие попадают к нам в крайне тяжелом состоянии) может быть период восстановления после такого длительного и достаточно агрессивного вмешательства, как циторедуктивная операция + HIPEC. Поэтому сразу после операции мы переводим пациента в отделение интенсивной терапии, под круглосуточное наблюдение.
Осложнения могут быть те же, что и после любого хирургического вмешательства на брюшной полости, поэтому за пациентом внимательно следят на случай появления признаков кровотечения или воспаления послеоперационной раны – и готовы в любую минуту оказать помощь.
Побочные действия от химиотерапевтического препарата при внутрибрюшной гипертермической химиотерапии даже менее выражены, чем при внутривенном введении – при том, что дозировки, а значит, и противоопухолевое действие, при HIPEC в десятки раз выше.
К сожалению, при всем нашем желании и мастерстве наших хирургов, есть пациенты, для которых полезный эффект вмешательства не оправдает сложностей послеоперационного восстановления.
Чтобы циторедуктивная операция с последующей процедурой HIPEC была эффективной, нужно соблюдение нескольких условий:
- Пациент должен быть в состоянии перенести и хирургическую операцию, и химиотерапию одновременно. Возраст или показатели здоровья не должны этому препятствовать – например, не должно быть почечной или печеночной недостаточности. Перед процедурой мы обязательно всесторонне обследуем пациента.
- Процесс распространения метастазов должен быть ограничен только брюшной полостью. Если есть метастазы в других органах, которые нельзя удалить – они будут распространяться дальше, и сведут эффект HIPEC на нет.
- Метастазы размером более 2,5 мм не должны покрывать всю поверхность брюшины – удалить их все будет невозможно.
Мы провели ей циторедуктивную операцию и процедуру HIPEC, и после этого она уже 10 месяцев живет без прогрессирования заболевания.
В некоторых случаях HIPEC приводит к устойчивому излечению. Например, коллеги из США сообщали о женщине с мезотелиомой брюшины. С помощью HIPEC она преодолела болезнь, уже 3 года живет без признаков рака и смогла родить ребенка.

Jessica Blackford-Cleeton, которой HIPEC позволила выжить и стать мамой.
К сожалению, HIPEC пока применяется в считанном количестве клиник. Причин этому несколько, и они характерны для всех новых технологичных способов лечения.
- Методика все еще считается инновационной, не все врачи имеют нужный опыт работы. К тому же, для проведения процедуры нужен не 1 и не 2, а целая бригада медиков самой высокой квалификации – это длительная, сложная и напряженная операция.
- Оборудование дорогое, не все страны и не все клиники могут потратиться на перфузионную систему и расходные материалы.
- Врачи бывают довольно консервативны. Кто-то считает, что процедура требует более подробного изучения. А кто-то из них не любит участвовать в проведении гипертермической химиотерапией, потому что опасается за собственное здоровье – испарения химиопрепаратов во время HIPEC могут быть вредными для медиков, которые при этом присутствуют. Хотя, в целом, испарения из закрытого контура минимальны, негативные последствия, даже если есть – не являются необратимыми, врачу нужно лишь более внимательно следить за состоянием почек и печени.
Однако более 70 ведущих хирургов-онкологов из 55 онкоцентров в 14 странах мира, включая США (где и родилась эта процедура), Канаду, Францию и Великобританию, пришли к выводу о том, что HIPEC может существенно повысить ожидаемую продолжительность жизни у пациентов, страдающих канцероматозом, особенно при колоректальном раке.
Клинические исследования из разных стран показывали результаты, когда пациенты после лечения канцероматоза брюшины с применением HIPEC жили 7 лет при опухолях аппендикса, более 5 лет при мезотелиоме брюшины, 5 лет при колоректальном раке, 2 года при раке яичников – тогда как при стандартном лечении их выживаемость колебалась от 2 до 14 месяцев.
Мы в свою очередь убедились в эффективности HIPEC на собственном обширном клиническом опыте. Мы надеемся, что через несколько лет HIPEC будет внедряться в стандарты лечения по ОМС и станет доступна по всей стране. А пока – мы даем пациентам возможность не искать подобную помощь за рубежом, а получить ее в Москве.
Читайте также:

