Высокодифференцированный плоскоклеточный рак полового члена
С. Х. Аль-Шукри 1 , И. А. Корнеев 1 , Т. Г. Гиоргобиани 1 , М. Н. Агеев 2 , Д. Б. Батмаев 1
1 Кафедра урологии Санкт-Петербургского государственного медицинского университета имени акад. И. П. Павлова;
2 Городская поликлиника №56 Фрунзенского района г. Санкт-Петербурга
Рак полового члена — редко встречающееся новообразование с агрессивным злокачественным потенциалом. Возможность применения органосохраняющего лечения при начальных стадиях болезни диктует необходимость раннего выявления и обследования с целью стадирования опухолевого процесса. В статье представлен обзор литературы, посвященной новообразованиям полового члена, на клиническом примере из собственной практики обсуждены современные подходы к диагностике и лечению больных.
Ключевые слова: рак полового члена; оперативное лечение.
Согласно современным представлениям рак полового члена (РПЧ) — это сравнительно редко встречающееся заболевание, которое в индустриально развитых странах наблюдается с частотой менее 1,0 на 100 000 населения и составляет от 0,3 % до 1 % злокачественных новообразований у мужчин. В странах с жарким и влажным климатом оно распространено в значительно большей степени.
Чаще всего злокачественное поражение полового члена диагностируют у мужчин старше 50‑летнего возраста, в подавляющем большинстве случаев оно представляет собой плоскоклеточную карциному. Описаны также базально-клеточные карциномы, меланомы, мезенхимальные опухоли, включая фибросаркому и саркому Капоши. Основными факторами риска, предрасполагающими к развитию рака полового члена, считают несоблюдение правил личной гигиены, застой смегмы в препуциальном мешке и фимоз. РПЧ крайне редко выявляют в странах, где мужчинам вскоре после рождения выполняют обрезание крайней плоти. Доказано, что РПЧ чаще наблюдается у курящих мужчин. К предраковым заболеваниям относят кожный рог, лейкоплакию, ксерозный облитерирующий баланит, а также неопластические процессы, обусловленные вирусом папилломы человека: остроконечные кондиломы и опухоль Бушке-Левинштейна. Нередко развитию плоскоклеточной карциномы полового члена предшествует рак in situ, который описан как болезнь Боуэна и эритроплазия Кейра [1].
В типичном случае плоскоклеточная карцинома полового члена представляет собой папиллярное или изъязвленное образование, располагающееся на головке полового члена или коже крайней плоти. Чаще всего больные сами обращают внимание на его появление, однако весьма часты поздние обращения за квалифицированной медицинской помощью после продолжительных безуспешных попыток самолечения. Нередко у пациентов имеется фимоз, степень выраженности которого во многом определяет их жалобы, клинические проявления и возможность визуальной оценки новообразования. Сужение крайней плоти часто сопровождается баланопоститом и появлением дискомфорта, зуда и выделений из препуциального мешка. Метастазы при раке полового члена в первую очередь поражают паховые лимфатические узлы, увеличение которых при пальпации отмечают у 40–80 % больных. Нередко, однако, лимфаденопатия является лишь следствием воспаления в результате инфицирования. Отдаленные метастазы РПЧ обнаруживают у 1–10 % больных при первичной диагностике опухоли. Чаще всего поражаются легкие, печень, кости и головной мозг. В целом РПЧ относят к агрессивным и быстро прогрессирующим новообразованиям, а пациенты, не получающие лечения, как правило, умирают в течение двух лет [2].
На ранних этапах РПЧ требуется дифференциальная диагностика с предраковыми заболеваниями, сифилисом, язвенным баланитом и баланопоститом. Морфологическую верификацию злокачественного характера опухолевого процесса можно получить при цитологическом исследовании мазков‑отпечатков и материала, полученного при биопсии новообразования. Обнаружение увеличенных лимфатических узлов при подтверждении злокачественного характера опухолевого процесса является показанием к лимфаденэктомии.
В связи с низкой частотой встречаемости рака полового члена и сравнительно небольшим числом посвященных этой проблеме работ российских авторов приводим собственное наблюдение.
Больной Р., 87 лет, поступил в клинику урологии СПБГМУ им акад. И. П. Павлова в плановом порядке по направлению уролога поликлиники с жалобами на боли и уплотнение в головке полового члена, сужение крайней плоти. При сборе анамнеза удалось узнать, что сужение крайней плоти больной наблюдал с детства, оно заметно прогрессировало в течение последних трех лет после развития сахарного диабета и на фоне периодических обострений хронического баланопостита. За несколько месяцев до госпитализации пациент обнаружил язву на головке полового члена, частично прикрытую рубцово‑деформированной крайней плотью. Пытался лечиться самостоятельно, используя тампоны с растворами антисептиков, однако лечение не было эффективным. Последующее появление уплотнения в области поражения головки полового члена стало поводом для обращения к специалисту.
При обследовании наружных половых органов из-за сужения крайней плоти раскрыть препуциальную область и осмотреть головку полового члена не представлялось возможным. У основания головки пальпировали участок выраженного уплотнения около двух сантиметров в диаметре. В паховых областях слева и справа пальпировали одиночные не спаянные с окружающими тканями увеличенные до 1,5–2,0 см лимфатические узлы.
Результаты лабораторных анализов в пределах границ нормальных значений. Больной осмотрен терапевтом, диагностированы компенсированные сопутствующие заболевания: артериальная гипертензия, сахарный диабет 2‑го типа, ожирение 1-й ст. Противопоказаний к хирургическому лечению не выявлено.
В предоперационном периоде выполнено цитологическое исследование мазка-отпечатка из препуциальной области, которое показало наличие воспаления, признаков гипер, диси паракератоза, а также единичных скоплений патологически измененных клеток плоского эпителия, соответствующих интраэпителиальной неоплазии III степени.

Рис. 1. Рассечение препуциального мешка
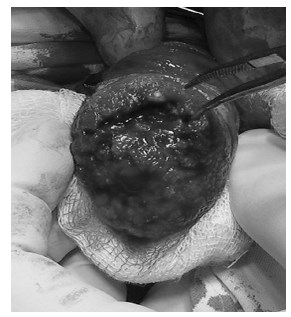
Рис. 2. Головка полового члена, пораженная новообразованием с участками некроза
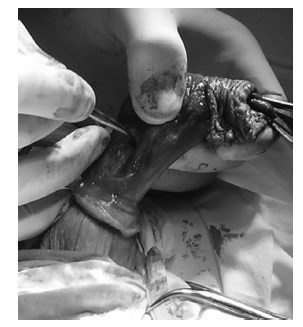
Рис. 3. Пересечение кавернозных тел полового члена. Мобилизация уретры
Предварительный диагноз: рак полового члена Т2 Nх Mх.
При планировании тактики оперативного лечения было решено провести диагностическую циркумцизию и при обнаружении новообразования выполнить резекцию полового члена, пораженного опухолью, в пределах здоровых тканей.
В ходе операции после рассечения препуциального мешка (рис. 1) определялась пораженная новообразованием с участками некроза головка полового члена (рис. 2). Отступив 2 см от края пальпируемой опухоли, были пересечены кожа, фасции полового члена и кавернозные тела (рис. 3).
Уретра мобилизована на 1,5 см дистально и отсечена. Белочные оболочки кавернозных тел ушиты (рис. 4), над ними наложены швы на фасции и кожу, сформировано наружное отверстие мочеиспускательного канала. Операция завершена дренированием мочевого пузыря 2‑ходовым катетером Фолея (рис. 5) и наложением асептической повязки.
Гистологическое исследование удаленной ткани показало наличие высокодифференцированного ороговевающего плоскоклеточного рака с инвазией в толщу собственной дермы и лимфоидной инфильтрацией по периферии и в толще опухоли. Постхирургический гистопатологический диагноз: pТ2 Nх Mх.
Течение послеоперационного периода было осложнено некрозом дистального отдела уретры, протяженностью около 1 см и заживлением этого участка послеоперационной раны вторичным натяжением (рис. 6). Больной был выписан в удовлетворительном состоянии под наблюдение уролога и онкоуролога по месту жительства с рекомендацией завершения заживления операционной раны и повторной госпитализации в онкологическое отделение для выполнения паховой лимфаденэктомии и решения вопроса о необходимости адьювантного лечения.
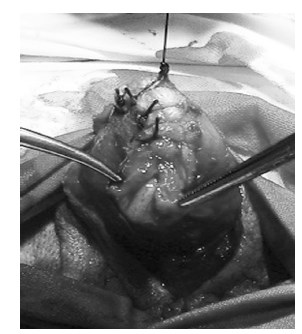
Рис. 4. Сшивание белочных оболочек кавернозных тел
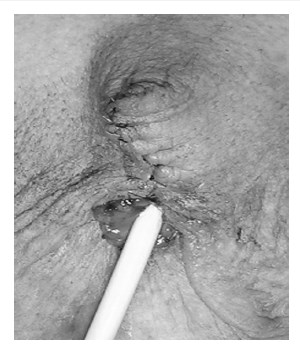
Рис. 5. Операция завершена. Мочевой пузырь дренирован 2-ходовым катетером Фолея
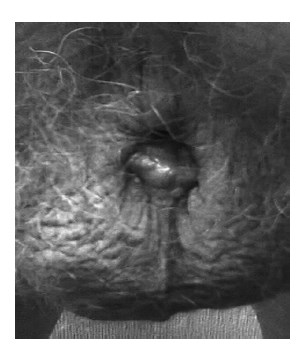
Рис. 6. Послеоперационная рана зажила вторичным натяжением
Представленный случай из практики подтверждает представление о более высокой предрасположенности к развитию рака полового члена мужчин с рубцовыми сужениями крайней плоти и хроническим воспалением в препуциальной области. Согласно опубликованным данным эти факторы риска наблюдают у 25–60 % пациентов [3, 4]. Считается, что фимоз и накопление смегмы поддерживают хронический воспалительный процесс крайней плоти и головки полового члена, который при длительном течении в может привести к метаплазии, анаплазии и в несколько раз повышает риск развития злокачественной опухоли [5, 6, 7]. У оперированного нами пациента при цитологическом исследовании были описаны предраковые изменения эпителия, непосредственно прилежащие к малигнизированному участку ткани. Не исключено, что длительному течению хронического воспаления препуциальной области у него также способствовали нарушения углеводного обмена и наличие сахарного диабета 2‑го типа [2, 4].
Согласно рекомендациям Европейской ассоциации урологов окончательное представление о глубине инвазии рака полового члена может быть получено только по результатам гистологического исследования удаленной в пределах здоровых тканей опухоли. При необходимости уточнению степени местного распространения помогает ультразвуковое исследование, которое может предоставить более точное представление о границах опухоли по сравнению с компьютерной томографией [8]. Точность диагностики глубины поражения мягких тканей полового члена возрастает при использовании МРТ (в том числе и с эндоректальной катушкой) в сочетании с фармакологически индуцированной эрекцией [9].
Наличие пальпируемых лимфоузлов в паховой области у больных раком полового члена является показанием для лимфаденэктомии. Для визуализации оценки распространенности лимфогенного метастазирования можно использовать УЗИ в комбинации с цветной допплерографией и МРТ [10].
При стадиях рака полового члена Tis, Та, и Т1а применяют органосохраняющие методики. Особый интерес представляет микрографическая хирургия Моха, при которой получают тонкие срезы тканей полового члена, производят их срочную гистопатологическую верификацию для определения чистоты хирургического края резекции [11].
При лечении опухоли с глубиной инвазии T1b-T2, как и в рассмотренном нами случае, обычно используются методики удаления новообразования в пределах здоровых тканей, позволяющие сохранить акт мочеиспускания и сексуальную функцию.
При небольших злокачественных опухолях головки полового члена возможно комбинированное лечение лазерным облучением и неоадъювантной химиотерапией винбластином, блеомицином и метотрексатом [12]. 5‑летняя выживаемость при применении дистанционной лучевой терапии составляет 88 %, однако такой подход по сравнению с хирургическим лечением приводит к большей частоте развития рецидивов [13, 14] и нередко сопровождается развитием рубцовых осложнений [15].
Распространенные опухоли стадии T3 и T4 в настоящее время встречаются редко. Основным подходом к лечению таких пациентов является удаление полового члена с выведением наружного отверстия уретры на промежность, паллиативно может быть использована лучевая терапия [16].
Паховая лимфодиссекция является стандартным хирургическим вмешательством как у пациентов с доказанным метастатическим поражением лимфоузлов, так и у пациентов с РПЧ высокого метастатического риска [17, 18]. В последние годы стали применять эндоскопическую паховую лимфодиссекцию с визуализацией операционного поля на видеомониторе. Такой подход эффективен, менее травматичен, сопровождается меньшим количеством осложнений и требует более короткого периода госпитализации [15, 19].
Таким образом, в настоящее время применение современных методов диагностики и лечения больных раком полового члена позволяет оказывать им высокоэффективную медицинскую помощь с минимальным риском развития осложнений. В то же время принципиально важным прогностически значимым фактором является ранняя диагностика, которая напрямую зависит от клинических проявлений этого редко встречающегося заболевания и их интерпретации пациентом.
Список литературы
- Аль-Шукри С. Х., Ткачук В. Н. Опухоли мочеполовых органов. — СПб: Питер. 2000. — 320 с.
- Pow'Sang M. R., Ferreira U., Pow'Sang J. M., Nardi A. C., Destefano V. Epidemiology and natural history of penile cancer // J. Urol. — 2010. — Vol. 76(2, supplement 1). — P. 26.
- Bleeker M. C., Heideman D. A., Snijders P. J., Horenblas S., Dillner J., Meijer C. J. Penile cancer: epidemiology, pathogenesis and prevention. prevention // World J. Urol. — 2009. — Vol. 27, N 2. — P. 141–150.
- Maden C., Sherman K. J., Beckmann A. M. et al. History of circumcision, medical conditions, and sexual activity and risk of penile cancer // J. Nat. Canc. Inst. — 1993. — Vol. 85, N 1. — P. 19–24.
- Bleeker M. C., Heideman D. A., Snijders P. J., Horenblas S., Dillner J., Meijer C. J. Penile cancer: epidemiology, pathogenesis and prevention // World J. Urol. — 2009. — Vol. 27, N 2. — P.141–150.
- Dillner J., Von Krogh G., Horenblas S., Meijer C. J. Etiology of squamous cell carcinoma of the penis // Scand. J. Urol. Nephrol. — 2000. Suppl. 205. — P. 189–193.
- Hellberg D., Valentin J., Eklund T., Nilsson S. Penile cancer: is there an epidemiological role for smoking and sexual behavior? // Br. Med. J. (Clin. Res. Ed.). — 1987. — Vol. 259. — P. 1306–1308.
- Stewart S. B., Leder R. A., Inman B. A. Imaging tumors of the penis and urethra // Urol. Clin. North Am. — 2010. — Vol. 37, N 3. — P. 353–367.
- Petralia G., Villa G., Scardino E. et al. Local staging of penile cancer using magnetic resonance imaging with pharmacologically induced penile erection // Radiol. Med. — 2008. — Vol. 113, N 4. — P. 517–528.
- Crawshaw J. W., Hadway P., Hoffland D. et al. Sentinel lymph node biopsy using dynamic lymphoscintigraphy combined with ultrasound — guided fine needle aspiration in penile carcinoma // Brit. J. Radiol. — 2009. — Vol. 82. — P. 41–48.
- Shindel A. W., Mann M. W., Lev R. Y. et al. Mohs micrographic surgery for penile cancer: management and long — term followup // Journal Urol. — 2007. — Vol. 178. — P. 1980–1985.
- Windahl T., Andersson S. O. Combined laser treatment for penile carcinoma: results after long'term followup // J. Urol. — 2003. — Vol. 169. — P. 2118–2121.
- A., Wylie J. P., Livsey J. E. External'beam radiotherapy in T1'2 N0 penile carcinoma // Clin. Oncol. — 2006. — Vol. 18, N 4. — P. 320–325.
- Crook J. M., Jezioranski J., Grimard L., Esche B., Pond G. Penile brachytherapy: results for 49 patients // Int. J. Radiat. Oncol. Biol. Phys. — 2005. — Vol. 62, N 2. — P. 460–467.
- Rossari J. R., Vora T., Gil T. Advances in penile cancer management // Curr. Opin. Oncol. — 2010. — Vol.22, N 3. — P. 226–235.
- Pizzocaro G., Algaba F., Horenblas S. et al. EAU penile cancer guidelines 2009 // Eur. Urol. — 2010. — Vol. 57. — P. 1002–1012.
- Spiess P. E., Hernandez M. S., Pettaway C. A. Contemporary inguinal lymph node dissection: minimizing complications // World Journal Urol. — 2009. — Vol. 2, N 2. — P. 205–212.
- Bonner J. A., Harari P. M., Giralt J. et al. Radiotherapy plus cetuximab for squamous'cell carcinoma of the head and neck // New Eng. J. Med. — 2006. — Vol. 354, N 6. — P. 567–578.
- Heyns C. F., Fleshner N., Sangar V., Schlenker B., Yuvaraja T. B., Van Poppel H. Management of the lymph nodes in penile cancer // Urology. — 2010. — Vol. 76, N 2, suppl.1. P. 43–57.
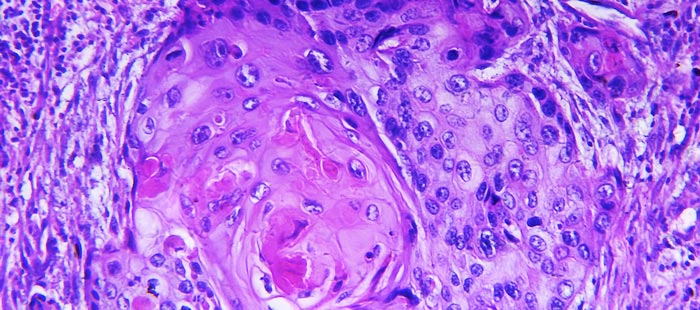
Плоскоклеточный рак, или плоскоклеточная карцинома – это гистологический тип злокачественных опухолей, такой диагноз устанавливают по результатам биопсии после исследования образца опухолевой ткани под микроскопом. Новообразование формируется из плоских клеток эпидермиса, которые выглядят как чешуйки. Оно может возникать на коже, в полости рта, в гортани, трахее, бронхах, пищеводе, на половых органах, в прямой кишке.
В Европейской онкологической клинике диагностикой и лечением плоскоклеточного рака занимаются врачи экспертного уровня, за плечами которых обширный опыт работы в ведущих онкологических центрах Москвы. С пациентом работает команда, в которую входят онкологи, дерматоонкологи, хирурги, химиотерапевты, радиотерапевты и другие специалисты. Мы применяем инновационные методы лечения, препараты последних поколений, проводим противоопухолевую терапию в соответствии с ведущими международными рекомендациями. Европейская онкологическая клиника – первый российский частный онкологический центр, в котором можно получить эффективное паллиативное лечение на поздних стадиях, даже в случаях, когда от пациента отказались в других клиниках.
- Причины возникновения плоскоклеточного рака
- Какие бывают виды плоскоклеточного рака?
- Виды диагностики заболевания
- Лечение плоскоклеточного рака
- Прогноз выживаемости при плоскоклеточном раке
- Профилактика
Причины возникновения плоскоклеточного рака
Основные факторы риска плоскоклеточного рака:
- На коже такие опухоли часто возникают из-за действия ультрафиолетовых лучей. Наиболее уязвимы открытые участки тела.
- Плоскоклеточный рак половых органов, головы и шеи вызывают некоторые типы вируса папилломы человека.
- Риск развития плоскоклеточного рака повышен у курильщиков и людей, которые употребляют много алкоголя.
- Вероятность развития онкологического заболевания повышается с возрастом, так как в клетках тела накапливаются мутации.
- Шрамы, ожоги, хронический воспалительный процесс.
- Воздействие некоторых канцерогенных веществ, например, если человек работает на производстве и контактирует с химикатами.
- Снижение иммунитета.
Ни один из этих факторов не приводит гарантированно к заболеванию – каждый из них лишь в определенной степени повышает вероятность.
Какие бывают виды плоскоклеточного рака?
Злокачественные новообразования данного гистологического типа встречаются на разных частях тела. В зависимости от локализации, могут несколько различаться их свойства, подходы к диагностике и лечению, прогноз для пациента.
Злокачественные опухоли кожи представлены плоскоклеточным раком примерно в 20% случаев. Намного чаще пациенты страдают базальноклеточным раком, который происходит из клеток, находящихся в нижнем слое эпидермиса.
Плоскоклеточный рак более агрессивен по сравнению с базальноклеточным. Он с большей вероятностью прорастет в глубокие слои кожи, будет распространяться в организме с образованием отдаленных метастазов. Тем не менее, это происходит довольно редко. Чаще всего опухоль удается обнаружить и удалить на ранней стадии.
Как правило, плоскоклеточный рак возникает на коже лица, ушей, шеи, тыльной стороне рук, реже – в области половых органов. Нередко новообразование развивается там, где находятся шрамы и хронические повреждения.
Злокачественные опухоли губ составляют не более 1–3% от всех онкологических заболеваний. В большинстве случаев (95%) они представлены плоскоклеточным раком, который бывает двух типов:
- Плоскоклеточный ороговевающий рак ведет себя не так агрессивно, медленно растет, редко образует отдаленные метастазы.
- Плоскоклеточный неороговевающий рак растет быстро, раньше приводит к изъязвлению и чаще метастазирует.
Исследования показывают, что у мужчин этот тип рака встречается в 3–13 раз чаще, чем у женщин. Вероятно, это связано с тем, что представители мужского пола чаще подвергаются воздействию солнечных лучей на рабочем месте, среди них более распространено курение, употребление алкоголя.
Раком ротовой полости называют злокачественные опухоли, которые возникают на слизистой оболочке губ, щек, десен, передних двух третей языка, неба, дна ротовой полости (находится под языком). В 90% случаев они представлены плоскоклеточным раком, из них 5% – плоскоклеточный ороговевающий рак, который менее агрессивен, реже прорастает в окружающие ткани, распространяется в лимфатические узлы и метастазирует.
Слизистая оболочка пищевода выстлана многослойным плоским эпителием, и из него может развиваться плоскоклеточный рак. Чаще всего такие опухоли находятся в шейном отделе пищевода и верхних двух третях грудного отдела. В нижней трети органа чаще встречаются аденокарциномы – злокачественные опухоли из железистых клеток.

Плоскоклеточный рак – наиболее распространенный тип злокачественных опухолей в трахее. Обычно он возникает в нижней части трахеи, довольно быстро растет, прорастает ее стенку, приводит к изъязвлениям и кровотечению. Это редкий тип рака, его основной причиной является курение.
Наиболее распространенным раком легкого является немелкоклеточный рак – он встречается в 80% случаев и в 30% случаев представлен плоскоклеточной карциномой. Нередко эти опухоли находятся в бронхах.
Шейка матки состоит из двух частей. Экзоцервикс находится снаружи, во влагалище, это то, что видит гинеколог во время осмотра. Эндоцервикс – канал шейки матки, он соединяет матку с влагалищем. В норме экзоцервикс выстлан плоским эпителием, а эндоцервикс – железистым. Место, где они встречаются, называется зоной трансформации.
Плоскоклеточным раком представлены 90% злокачественных опухолей шейки матки. Чаще всего новообразование возникает в области зоны трансформации. Раки, которые развиваются из железистых клеток эндоцервикса, называются аденокарциномами.
В редких случаях в шейке матки встречается железисто-плоскоклеточный рак.
Вульвой называют наружные женские половые органы: преддверие влагалища, большие и малые половые губы, клитор. Большинство типов рака, которые развиваются в этой области, представлены плоскоклеточным раком (70–90%). Они делятся на две группы:
- Большая группа – опухоли, происхождение которых неизвестно. Чаще всего их диагностируют у женщин старшего возраста.
- Меньшая группа – злокачественные опухоли, вызванные вирусом папилломы человека.
В большинстве случаев злокачественные опухоли прямой кишки представлены аденокарциномами – железистым раком. Плоскоклеточный рак в этом органе встречается очень редко и составляет от 10 до 25 случаев на каждые 100 тысяч случаев колоректального рака.
Плоскоклеточный рак составляет 90% от всех злокачественных новообразований анального канала – узкого прохода, который соединяет прямую кишку с анусом.
У человека есть четыре вида миндалин: небные (при их воспалении развивается тонзиллит), трубные (находятся в глотке возле отверстий слуховых труб), язычная (позади языка) и глоточная (у детей из-за нее бывают аденоиды). Чаще всего злокачественные опухоли развиваются в небных миндалинах. В большинстве случаев это плоскоклеточный рак. Его сложно диагностировать, поэтому зачастую он выявляется на поздних стадиях.
Виды диагностики заболевания
Врач-онколог назначает пациенту те или иные виды диагностики, в зависимости от того, в каком органе находится злокачественная опухоль:
Место локализации рака
Методы диагностики
Во всех случаях, когда обнаружено патологическое образование, проводят биопсию – исследование, во время которого получают фрагмент подозрительной ткани и отправляют в лабораторию для гистологического и цитологического исследования. Биопсия – самый точный метод диагностики рака. Она помогает не только достоверно установить диагноз, но и определить гистологический тип новообразования.Для того чтобы проверить степень распространения рака в организме и уточнить стадию, врач может назначить дополнительные исследования:
- компьютерную томографию, МРТ;
- рентгенографию грудной клетки, костей;
- ПЭТ-сканирование;
- УЗИ и эндоскопические исследования органов, в которые мог прорасти рак.
Лечение плоскоклеточного рака
Лечение зависит от локализации, стадии рака, общего состояния пациента, наличия у него сопутствующих заболеваний и других факторов.
Ионизирующее излучение повреждает опухолевые и другие быстро размножающиеся клетки. Этот вид лечения плоскоклеточного рака может быть назначен до или после операции, либо на поздних стадиях в паллиативных целях.
Радикальные операции возможны, если нет метастазов, и не произошло сильное прорастание рака в окружающие ткани. В одних случаях таким пациентам показано только хирургическое лечение, в других его дополняют противоопухолевыми препаратами, лучевой терапией – это помогает снизить риск рецидива.
При запущенном плоскоклеточном раке может быть выполнено паллиативное хирургическое вмешательство, направленное на ликвидацию симптомов, восстановление проходимости и функции пораженного органа.
Химиотерапия при плоскоклеточном раке может быть адъювантной (после операции), неоадъювантной (до хирургического вмешательства) или применяется в качестве самостоятельного метода лечения на поздних стадиях.
Если опухоль обладает определенными молекулярно-генетическими характеристиками, назначают таргетную терапию. Таргетные препараты прицельно воздействуют на молекулы, которые помогают раку расти и поддерживать свою жизнедеятельность.
Лечение при плоскоклеточном раке и любых других злокачественных новообразованиях должно быть направлено не только на борьбу с самой опухолью, но и на купирование симптомов, улучшение состояния пациента. В Европейской онкологической клинике пациент может получить все виды симптоматической терапии при раке:
- Купирование болевого синдрома в соответствии с трехступенчатой схемой ВОЗ.
- Восстановление проходимости пищевода, кишечника, дыхательных путей.
- Устранение кровотечений, при необходимости – переливание крови.
- Купирование тошноты.
- Устранение сдавления опухолью внутренних органов, нервов, сосудов.
- Лечение экстренных состояний в условиях палаты интенсивной терапии, оснащенной современной аппаратурой.
- Контроль и коррекция нутритивного статуса.
- Поддерживающая терапия помогает комфортно перенести курс химиотерапии, предотвратить и купировать побочные эффекты.

Прогноз выживаемости при плоскоклеточном раке
Прогноз зависит от того, в каком месте начался рост рака, на какой стадии установлен диагноз и начато лечение. Например, зачастую выживаемость при раке кожи и красной каймы губ стремится к 100%, потому что такие опухоли, как правило, удается обнаружить достаточно рано, и они не очень агрессивны. Если появились отдаленные метастазы, шансы на ремиссию становятся крайне низкими. Но таким пациентам все еще можно помочь: затормозить прогрессирование плоскоклеточного рака, продлить жизнь, улучшить общее состояние, купировать мучительные симптомы.
Профилактика
Основные меры профилактики плоскоклеточного рака:
- Отказ от курения и употребления алкоголя.
- Защита от воздействия на кожу ультрафиолетовых лучей – важнейшая мера профилактики рака кожи. Не стоит посещать солярии, ходить на пляж с 10.00 до 16.00 часов, когда наиболее высока солнечная активность. Защититься помогает одежда с длинными рукавами и штанинами, шляпа с широкими полями, солнцезащитные очки.
- Предотвращение заражения ВПЧ, приводящими к развитию рака: нужно избегать беспорядочных половых связей, использовать презервативы. В настоящее время существует вакцина против папилломавирусной инфекции. Прививать рекомендуется всех подростков до начала половой жизни.
Плоскоклеточный рак языка в 10 раз чаще встречается у мужчин, возникает на фоне хронических воспалительных заболеваний (красного плоского лишая, гуммы), рубцов, лейкоплакии, цветущего орального папиломатоза. Чаще поражаются латеральные края, чем основание и кончик языка. Опухолевый процесс вначале представлен плотными узлами или очагами уплотнения, позже — изъязвлением, распространяющимся на различную глубину. Язва может быть довольно болезненной.
Прогноз рака языка плохой. Характерной особенностью рака языка, как и рака полости рта в целом, является раннее и почти исключительно лимфогенное метастазирование. При этом его частота увеличивается по мере распространенности первичной опухоли. Ранние лимфо-генные метастазы обычно плотные, безболезненные, медленно увеличивающиеся в размере.
Дифференциальный диагноз рака языка проводится с гуммой, а также с другими доброкачественными или злокачественными опухолями языка.
Основной метод лечения рака языка — лучевая терапия. Обычно она используется как самостоятельный и единственный метод, реже — как компонент комбинированного метода в сочетании с оперативным вмешательством или как составная часть комплексной терапии в сочетании с хирургическим лечением и химиотерапией.
Большинство злокачественных новообразований полового члена состоят из эпителиальных клеток и в 85,5-95% случаев представлены плоскоклеточным раком полового члена (ПРПЧ), доля которого в обшей структуре онкологической летальности оценивается в 1-2%. Хотя возраст развития ПРПЧ варьируется в широких пределах (от 30 до 70 лет), пик его частоты отмечается на 5-м десятилетии жизни. Он может встречаться удетей.
Вирусная этиология ПРПЧ подтверждена обнаружением ДНК-последовательностей ВПЧ в тканях ПРПЧ. В многоступенчатом процессе канцерогенеза наряду с ВПЧ участвует и множество других коканцерогенных агентов различной природы. Это, в первую очередь, химические вещества. Установлено, например что клетки эпителия половых путей, трансформированные ВПЧ-16, реагируют на генотоксичес-кое действие полициклических углеводородов, алкилирующих агентов или конденсата сигаретного дыма, но не претерпевают при этом злокачественных изменений; злокачественная же их трансформация происходит под влиянием онкогена Ras и вируса простого герпеса-2. Риск развития ПРПЧ возрастает также под воздействием УФИ, ПУВА-терапии, а также при иммуносупрессии, особенно связанной с пересадкой органов и ВИЧ-инфекцией.
Среди местных факторов, предрасполагающих к развитию ПРПЧ, следует отметить врожденную узость крайней плоти и приобретенный фимоз, выявленный почти у 50% больных. В то же время улиц с иссеченной крайней плотью заболевание встречается крайне редко. Определенную роль в возникновении ПРПЧ играет и отсутствие достаточных гигиенических навыков. Профилактический эффект обрезания связывают именно с предотвращением задержки смегмы — частой причины присоединения вторичной инфекции и фимоза. Смегма формируется в первые дни жизни и образуется из опущенных эпителиальных клеток препуциального мешка, ее стероиды под влиянием Micobacterium smegmatis превращаются в канцерогенные составляющие. Экспериментальный перенос человеческой смегмы во влагалище мышей показал возможность индуцирования у них рака шейки матки. Половой путь передачи ПРПЧ подтвержден высокой частотой обнаружения рака шейки матки у жен пациентов с ПРПЧ. Патогенетическая основа для ПРПЧ, кроме смегмы, создается хроническим рецидивирующим воспалением и предраком кожи. В настоящее время в качестве важных факторов развития ПРПЧ рассматриваются также гигантская кондилома Бушке—Левенштейна, рак in situ и ряд дерматозов, таких, как склероатрофический лишай, хронический рецидивирующий баланит лей коплакия, кожный рог, нередко встречающиеся у лиц с наличием крайней плоти.
В то же время многие особенности развития ПРПЧ еще не нашли своего объяснения. Так неясно почему:
— частота выявления ВПЧ при ПРПЧ ниже, чем при раке шейки матки;
— у мужчин, половых партнеров женщин с интраэпителиальной цервикальной неоплазией и раком шейки матки, частота злокачественных или предраковых ВПЧ-индуцированных поражений полового члена составила только 32,8%;
— не отмечается повышения частоты ПРПЧ у мужчин — половых партнеров женщин, страдавших раком шейки матки;
— отсутствует зависимость частоты ПРПЧ от сроков начала половой жизни, сексуальной активности, числа и типа половых партнеров;
— ПРПЧ чаще возникает de novo (92,4%), а не на фоне предраковых поражений, как плоскоклеточный рак кожи другихлокализаций.
Все это не только свидетельствует о различиях в течении ВПЧ-инфекции у мужчин и женщин, но послужило поводом к выдвижению гипотезы о наличии двух различных по этиологии типов ПРПЧ: у мужчин молодого возраста — опухолей, связанных с вирусом, передающимся половым путем, у пожилых мужчин — обусловленных пока неизвестным агентом, не ассоциирующимся с раком шейки матки.
ПРПЧ локализуется в области головки по лового члена в 48%, крайней плоти — в 9%, венечной борозды — в 6%, ствола — менее, чем в 2% случаев.
Хотя паховая лимфаденопатия при ПРПЧ выявляется в 58% случаев, в 55% она носит воспалительный, а не специфический характер, однако почти 20% непальпируемых лимфатических узлов содержат метастазы. Отдаленные метастазы (как результат сосудистой диссеминации) редки.
Морфологическая структура ПРПЧ может иметь различные характеристики. ПРПЧ с ороговением относится к более дифференцированным формам, чем ПРПЧ без ороговения. В зависимости от выраженности атипии принято вьщелять следующие формы ПРПЧ.
Низкодифференцированные очаги ПРПЧ (III, IV) отличаются незначительной кератинизацией опухолевых клеток или не имеют ее вовсе, для них характерны высокий ядерный плеоморфизм и гиперхромазия, большая глубина инвазиии в сочетании с участками некроза и гнойного воспаления.
У 80-85% больных ПРПЧ является высоко-дифференцированным плоскоклеточным раком полового члена.
Кроме того, описано 2 редких варианта ПРПЧ — веретенообразный и псевдожелезистый. Веретенообразный рак полового члена, также известный как псевдосаркоматозный рак, по гистологическим признакам напоминает саркому, опухолевые клетки имеют веретенообразную форму. Опухоль отличается высокой степенью злокачественности, однако клиническое течение скорее аналогично ПРПЧ, чем саркоме. Псевдожелезистый, или акантолитичес-кий, плоскоклеточный рак характеризуется наличием железистоподобных структур, образовавшихся вследствие дискератоза и акантоли-за опухолевых клеток.
Выявление стадии ПРПЧ имеет важное значение при выборе лечебной тактики рака полового члена и определении прогноза заболевания. С этой целью используются классификации Jackson и TNM.
Классификация рака полового члена Jackson:
I стадия рака полового члена — опухоль ограничена головкой полового члена или крайней плотью;
II стадия рака полового члена — инвазия в ствол или кавернозные тела без регионарных иди отдаленных метастазов;
III стадия рака полового члена — опухоль, ограниченная половым членом с операбельными метастазами в паховые лимфатические узлы;
IV стадия рака полового члена — опухоль поражает соседние структуры; неоперабельные метастазы в регионарные и(или) отдаленные лимфатические узлы.
Прогноз рака полового члена плохой. Обилие кровеносных и лимфатических сосудов в органе — причина высокой частоты метастазирования, сравнимой с гшоскоклеточным раком языка. Ранние метастазы встречаются почти в 50% случаев. Они обнаруживаются в лимфатических узлах (паховых и парааортальных). Гематогенное мета-стазирование встречается довольно редко.
При лечении больных ПРПЧ используют хирургический или лучевой метод и их комбинацию. При этом хирургическое вмешательство в одних случаях может быть функционально щадящим, т.е. ограничивающимся удалением опухоли в пределах подозрительных участков, в других же случаях требуется частичная ампутация полового члена с удалением или без удаления лимфатических узлов. Реже применяется химиотерапия (метотрексат, винкри-стин, винбластин) и лазеротерапия, главным образом, углекислотным лазером.
Особенность профилактики ПРПЧ заключается в предотвращении инфицирования ВПЧ и его персистирования, т.е. в ограничении количества случайных половых связей и использовании барьерных методов контрацепции.
Читайте также:

