Водород с хлором взрыв

Хлор является сильнодействующим ядовитым веществом удушающего характера. Что делать, если на предприятии или близлежащем химическом заводе произошла утечка хлора?
Хлор – это газ с резким специфическим запахом. Он тяжелее воздуха, при испарении похож на туман.
Как эффективный бактерицид хлор начал использоваться почти два столетия назад. С одной стороны, хлор спас сотни тысяч жизней благодаря своей способности разрушать вредные бактерии и вирусы, но в то же время он оказывает отравляющее воздействие и на человека.
Кроме этого, хлор является одним из важнейших продуктов химической промышленности по объёму производства и области применения.
При нормальных условиях хлор представляет собой газ зеленовато-жёлтого цвета с резким раздражающим запахом, в сжиженном же состоянии хлор может находиться только при избыточном давлении или при температуре ниже минус 34 °С.
При утечке хлор дымит, при температуре -34 °С сжижается, при температуре -101 °С затвердевает. Хлор малорастворим в воде – в одном объёме воды растворяется около двух его объёмов. Жидкий хлор в 1,5 раза тяжелее воды, газообразный хлор в 2,5 раза тяжелее воздуха.
Один килограмм жидкого хлора при испарении дает 315 литров газообразного хлора, при испарении на воздухе в значительных количествах даёт с водяными парами белый туман. В смеси с водородом (более 50 % водорода) хлор взрывоопасен, а при нагревании ёмкости с хлором взрываются.
Хранится и транспортируется жидкий хлор в сосудах, выдерживающих избыточное давление. Один баллон с жидким хлором при разгерметизации становится бомбой с радиусом поражения от 150 метров до 1 километра, с действием в зоне поражения более суток.
Наибольшую опасность представляет хлор в сжиженном состоянии. При выбросах жидкого хлора смертельно опасную зону составляет площадь в радиусе примерно 400 м от места выброса.
Опасность хлора заключается во взаимодействии хлоргаза со слизистыми оболочками человека – образуется соляная кислота, вызывающая отёк лёгких, поражение глаз и носа, кожные раздражения. При вдыхании высоких концентраций хлора возможен смертельный исход – попадая в лёгкие, он обжигает лёгочную ткань и вызывает удушье.
Учёные предполагают, что хлор, как и продукты его взаимодействия с другими веществами, увеличивает риск сердечно-сосудистых заболеваний, аллергических реакций и выкидышей у беременных женщин.
При вдыхании хлор вызывает судорожный, мучительный кашель, в тяжёлых случаях происходит спазм голосовых связок и отёк лёгких. Хлор раздражающе действует на влажную кожу, вызывая её покраснение, могут иметь место химические ожоги и обморожение. Также хлор оказывает сковывающее воздействие на центральную нервную систему.
Первыми явными признаками отравления хлором являются:
резкая боль в груди,
резь в глазах (слезотечение),
нарушение координации движений.
При получении информации об аварии нужно:
Защитить органы дыхания и поверхность тела. Лицо, нос и рот можно защитить с помощью противогазов всех типов, марлевой повязки, смоченной водой или 20 % раствором соды (1 чайная ложка на стакан воды). Средством защиты кожи может послужить любая накидка.
Покинуть район аварии в направлении, указанном в сообщении. Вне помещения выходить из зоны химического заражения следует в сторону, перпендикулярную направлению ветра. Избегайте перехода через туннели, овраги и лощины, так как в низких местах концентрация хлора будет выше.
Если из опасной зоны выйти невозможно, нужно остаться в помещении и произвести его герметизацию: плотно закройте окна, двери, вентиляционные отверстия, дымоходы, уплотните щели в окнах и на стыках рам. Входные двери зашторьте, используя одеяла и любые плотные ткани. При возможности поднимитесь на верхние этажи здания. Нельзя укрываться на первых этажах многоэтажных зданий, в подвальных и полуподвальных помещениях.
Оказавшись вне опасной зоны, нужно снять верхнюю одежду и оставить её на улице.
Как можно быстрее принять душ, промыть глаза и носоглотку.
Наблюдать за своим самочувствием, при первом появлении признаков отравления обратиться к врачу. В ожидании помощи пострадавшему необходим покой и тёплое питьё.
Пострадавшего от отравления хлором нужно как можно быстрее вынести из опасной зоны. При транспортировке пострадавший должен быть в горизонтальном положении.
Вне опасной зоны снимите с пострадавшего всю одежду, стесняющую дыхание, и уложите в горизонтальное положение. Необходимо обеспечить покой, тепло, приток свежего воздуха.
В ожидании медицинской помощи рекомендуется:
обильное тёплое питьё – 2 % раствор соды, боржоми, молоко с содой, чай, кофе;
при кашле или першении в горле необходимы тёпло-влажные ингаляции 2 % раствором соды, противокашлевые препараты;
при слезотечении, жжении в глазах – промывание глаз водой или 2 % раствором соды. Этим же раствором нужно промыть нос. В глаза можно закапать 30 % раствор альбуцида;
при затруднении дыхания, осиплости голоса – вводится подкожно 1 мл 0,1 %-ного раствора атропина;
при обмороке – нужно дать понюхать нашатырный спирт. При отсутствии дыхания немедленно приступить к его восстановлению.
Рекомендуется затемнить помещение. При первой возможности пострадавшие должны быть доставлены в медицинское учреждение для обследования и дальнейшего лечения.
Химические свойства водорода
Атом водорода имеет электронную формулу внешнего (и единственного) электронного уровня 1s 1 . С одной стороны, по наличию одного электрона на внешнем электронном уровне атом водорода похож на атомы щелочных металлов. Однако, ему, так же как и галогенам не хватает до заполнения внешнего электронного уровня всего одного электрона, поскольку на первом электронном уровне может располагаться не более 2-х электронов. Выходит, что водород можно поместить одновременно как в первую, так и в предпоследнюю (седьмую) группу таблицы Менделеева, что иногда и делается в различных вариантах периодической системы:
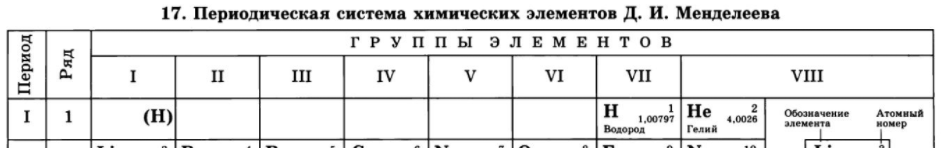
С точки зрения свойств водорода как простого вещества, он, все-таки, имеет больше общего с галогенами. Водород, также как и галогены, является неметаллом и образует аналогично им двухатомные молекулы (H2).
В обычных условиях водород представляет собой газообразное, малоактивное вещество. Невысокая активность водорода объясняется высокой прочностью связи между атомами водорода в молекуле, для разрыва которой требуется либо сильное нагревание, либо применение катализаторов, либо и то и другое одновременно.
Из металлов водород реагирует только с щелочными и щелочноземельными! К щелочным металлам относятся металлы главной подгруппы I-й группы (Li, Na, K, Rb, Cs, Fr), а к щелочно-земельным — металлы главной подгруппы II-й группы, кроме бериллия и магния (Ca, Sr, Ba, Ra)
При взаимодействии с активными металлами водород проявляет окислительные свойства, т.е. понижает свою степень окисления. При этом образуются гидриды щелочных и щелочноземельных металлов, которые имеют ионное строение. Реакция протекает при нагревании:
Следует отметить, что взаимодействие с активными металлами является единственным случаем, когда молекулярный водород Н2 является окислителем.
Из неметаллов водород реагирует только c углеродом, азотом, кислородом, серой, селеном и галогенами!
Под углеродом следует понимать графит или аморфный углерод, поскольку алмаз — крайне инертная аллотропная модификация углерода.
При взаимодействии с неметаллами водород может выполнять только функцию восстановителя, то есть только повышать свою степень окисления:
Водород не реагирует с оксидами металлов, находящихся в ряду активности металлов до алюминия (включительно), однако, способен восстанавливать многие оксиды металлов правее алюминия при нагревании:
Из оксидов неметаллов водород реагирует при нагревании с оксидами азота, галогенов и углерода. Из всех взаимодействий водорода с оксидами неметаллов особенно следует отметить его реакцию с угарным газом CO.
С неорганическими кислотами водород не реагирует!
Из органических кислот водород реагирует только с непредельными, а также с кислотами, содержащими функциональные группы способные к восстановлению водородом, в частности альдегидные, кето- или нитрогруппы.
В случае водных растворов солей их взаимодействие с водородом не протекает. Однако при пропускании водорода над твердыми солями некоторых металлов средней и низкой активности возможно их частичное или полное восстановление, например:
Химические свойства галогенов
Галогенами называют химические элементы VIIA группы (F, Cl, Br, I, At), а также образуемые ими простые вещества. Здесь и далее по тексту, если не сказано иное, под галогенами будут пониматься именно простые вещества.
Все галогены имеют молекулярное строение, что обусловливает низкие температуры плавления и кипения данных веществ. Молекулы галогенов двухатомны, т.е. их формулу можно записать в общем виде как Hal2.
Следует отметить такое специфическое физическое свойство йода, как его способность к сублимации или, иначе говоря, возгонке. Возгонкой, называют явление, при котором вещество, находящееся в твердом состоянии, при нагревании не плавится, а, минуя жидкую фазу, сразу же переходит в газообразное состояние.
Электронное строение внешнего энергетического уровня атома любого галогена имеет вид ns 2 np 5 , где n – номер периода таблицы Менделеева, в котором расположен галоген. Как можно заметить, до восьмиэлектронной внешней оболочки атомам галогенов не хватает всего одного электрона. Из этого логично предположить преимущественно окисляющие свойства свободных галогенов, что подтверждается и на практике. Как известно, электроотрицательность неметаллов при движении вниз по подгруппе снижается, в связи с чем активность галогенов уменьшается в ряду:
Все галогены являются высокоактивными веществами и реагируют с большинством простых веществ. Однако, следует отметить, что фтор из-за своей чрезвычайно высокой реакционной способности может реагировать даже с теми простыми веществами, с которыми не могут реагировать остальные галогены. К таким простым веществам относятся кислород, углерод (алмаз), азот, платина, золото и некоторые благородные газы (ксенон и криптон). Т.е. фактически, фтор не реагирует лишь с некоторыми благородными газами.
Остальные галогены, т.е. хлор, бром и йод, также являются активными веществами, однако менее активными, чем фтор. Они реагируют практически со всеми простыми веществами, кроме кислорода, азота, углерода в виде алмаза, платины, золота и благородных газов.
При взаимодействии всех галогенов с водородом образуются галогеноводороды с общей формулой HHal. При этом, реакция фтора с водородом начинается самопроизвольно даже в темноте и протекает со взрывом в соответствии с уравнением:
Реакция хлора с водородом может быть инициирована интенсивным ультрафиолетовым облучением или нагреванием. Также протекает со взрывом:
Бром и йод реагируют с водородом только при нагревании и при этом, реакция с йодом является обратимой:
Взаимодействие фтора с фосфором приводит к окислению фосфора до высшей степени окисления (+5). При этом происходит образование пентафторида фосфора:
При взаимодействии хлора и брома с фосфором возможно получение галогенидов фосфора как в степени окисления + 3, так и в степени окисления +5, что зависит от пропорций реагирующих веществ:
При этом в случае белого фосфора в атмосфере фтора, хлора или жидком броме реакция начинается самопроизвольно.
Взаимодействие же фосфора с йодом может привести к образованию только триодида фосфора из-за существенно меньшей, чем у остальных галогенов окисляющей способности:
Фтор окисляет серу до высшей степени окисления +6, образуя гексафторид серы:
Хлор и бром реагируют с серой, образуя соединения, содержащие серу в крайне не свойственных ей степенях окисления +1 и +2. Данные взаимодействия являются весьма специфичными, и для сдачи ЕГЭ по химии умение записывать уравнения этих взаимодействий не обязательно. Поэтому три нижеследующих уравнения даны скорее для ознакомления:
Как уже было сказано выше, фтор способен реагировать со всеми металлами, даже такими малоактивными как платина и золото:
Остальные галогены реагируют со всеми металлами кроме платины и золота:
Более активные галогены, т.е. химические элементы которых расположены выше в таблице Менделеева, способны вытеснять менее активные галогены из образуемых ими галогеноводородных кислот и галогенидов металлов:
Аналогичным образом, бром вытесняет серу из растворов сульфидов и сероводорода:
Хлор является более сильным окислителем и окисляет сероводород в его водном растворе не до серы, а до серной кислоты:
Вода горит во фторе синим пламенем в соответствии с уравнением реакции:
Бром и хлор реагируют с водой иначе, чем фтор. Если фтор выступал в роли окислителя, то хлор и бром диспропорционируют в воде, образуя смесь кислот. При этом реакции обратимы:
Взаимодействие йода с водой протекает в настолько ничтожно малой степени, что им можно пренебречь и считать, что реакция не протекает вовсе.
Фтор при взаимодействии с водным раствором щелочи опять же выступает в роли окислителя:
Умение записывать данное уравнение не требуется для сдачи ЕГЭ. Достаточно знать факт о возможности такого взаимодействия и окислительной роли фтора в этой реакции.
а при нагревании:
Йод реагирует с щелочами исключительно по второму варианту, т.е. с образованием йодата, т.к. гипоиодит не устойчив не только при нагревании, но также при обычной температуре и даже на холоду:
Атом водорода имеет всего один электрон, поэтому при образовании химических соединений может легко отдавать его, либо образовывать одну общую электронную пару, либо присоединять еще один электрон, образуя двухэлектронную внешнюю оболочку, как у благородного газа гелия.
Из-за малого заряда ядра атом водорода сравнительно слабо притягивает электроны и может присоединять их только в том случае, когда другой элемент легко их отдает. Такими элементами являются щелочные и щелочноземельные металлы, которые при нагревавши в атмосфере водорода образуют солеобразные соединения - гидриды:
2 К+ Н2 = 2 КН (гидрид калия)
Са + Н2 = СаН2 (гидрид кальция)
Для водорода более характерны соединения, в которых он проявляет положительную степень окисления. Он взаимодействует со многими неметаллами. В зависимости от активности неметаллов реакция может протекать с различной скоростью. Так, со фтором водород взаимодействует всегда со взрывом:
Хлор взаимодействует с водородом значительно спокойнее: в темноте и без нагревания реакция протекает довольно медленно, на свету - значительно быстрее, а при наличии инициатора (искра, нагревание) - моментально и со взрывом. Поэтому смесь хлора и водорода является гремучей и требует чрезвычайной осторожности в обращении. Водород хорошо горит в атмосфере хлора. Во всех случаях реакция водорода с хлором протекает по уравнению
Н2 + Сl2 = 2 НСl (хлороводород)
С бромом и иодом водород реагирует очень медленно.
С другими неметаллами водород реагирует либо при высокой температуре, либо при высоких. температуре и давлении. Например, с серой водород реагирует только при нагревании, а с азотом - при нагревании и высоком давлении:
Водород может отнимать кислород или галогены от многих металлов и неметаллов. В этом случае он выступает как восстановитель:
Эти реакции используются в металлургии для получения свободных металлов. Они, как правило, протекают при высоких температурах. Чем активнее металл, тем более высокая температура требуется для его восстановления.
Водород не поддерживает горение обычных горючих веществ (являющихся соединениями углерода). Так, зажжённая свеча гаснет в нём. Однако, например, кислород горит в атмосфере водорода. Отсюда видна относительность понятия "поддерживает" или "не поддерживает" горения. Обычно его относят именно к горению соединений углерода.
Сам водород горит и в чистом кислороде, и на воздухе, причём продуктом сгорания является вода. При поджигании смеси обоих газов ("гремучего газа") взаимодействие протекает со взрывом. Если вместо поджигания привести эту смесь в соприкосновение с очень малым количеством мелко раздробленной платины (играющей роль катализатора), то реакция протекает быстро, но спокойно.
Реакция образования воды из водорода и кислорода сильно экзотермична:
Помимо прямого соединения с кислородом водород способен отнимать его от оксидов многих элементов: Cu, Pb, Hg и др. В результате из оксида получается свободный элемент, например:
СuO + H2 = H2O + Cu + 130 кДж.
Однако эти реакции, в которых водород выступает как восстановитель, протекают лишь при нагревании. При высоких давлениях водород вытесняет некоторые металлы также из растворов их солей.
Опыт показывает, что химическая активность водорода иногда сильно повышается. Это наблюдается тогда, когда реагирующие с ним вещества находятся в непосредственном контакте с выделяющимся водородом. Повышенную активность такого водорода "в момент выделения" ("in statu nascendi") объясняется тем, что реагируют не молекулы Н2, а атомы. Действительно, при реакциях получения водорода (например, действием цинка на кислоту) первоначально выделяются именно отдельные атомы. Если же у места их выделения имеется вещество, способное с ними реагировать, то такая реакция может происходить без предварительного образования молекул Н2.
Это представление было косвенно подтверждено, когда удалось получить атомарный водород в газообразном состоянии и изучить его реакционную способность. Оказалось, что он значительно активнее молекулярного. Так, атомарный водород уже при обычных условиях соединяется с серой, фосфором, мышьяком и т. д., восстанавливает оксиды многих металлов, вытесняет некоторые металлы (Cu, Pb, Ag и др.) из их солей и вступает в другие химические реакции, на которые при тех же условиях не способен обычный молекулярный водород.
При химических взаимодействиях с участием обычного водорода молекула его должна распадаться на атомы. Но сама реакция такого распада (диссоциация на атомы) сильно эндотермична:
Н2 + 435 кДж = Н + Н.
Очевидно, что затрачиваемая на эту реакцию энергия (энергия диссоциации) должна быть восполнена энергией, выделяющуюся при взаимодействии атомов водорода с введённым в реакцию веществом. Следовательно, можно ожидать, что реакция водорода, при которых выделяется менее 435 кДж/моль, не будет протекать самопроизвольно. В случае взаимодействия веществ с атомарным водородом такой затраты энергии на диссоциацию уже не требуется. Поэтому здесь и возможен значительно более широкий круг реакций.
Атомарный водород удобно получать действием на обычный водород тихого электрического разряда. При этом часть молекул распадается на атомы, которые под уменьшенным давлением соединяются в молекулы не моментально, благодаря чему и могут быть изучены химические свойства атомарного водорода.
Аналогично водороду может быть получен в атомарном состоянии и кислород. Его химическая активность при переходе в атомарное состояние тоже резко возрастает.
Большое количество энергии, выделяющейся при образовании молекулы водорода, объясняет её устойчивость при обычных условиях. Вместе с тем оно же наводит на мысль о возможности термической диссоциации (разложения при нагревании) молекулы Н2, если сообщить ей достаточное количество тепла. Опыт показывает, что заметная термическая диссоциация водорода начинается примерно с 2000 °С и происходит тем в большей степени, чем выше температура. Наоборот, при понижении температуры отдельные атомы вновь соединяются в молекулы.
Термическая диссоциация водорода (под обычным давлением) характеризуется следующими данными:
Переход водорода в атомарное состояние может вызываться также излучением с длинами волн менее 85 нм. Этим и обусловлено резкое преобладание атомарного водорода над молекулярным в космическом пространстве.
Соединение атомов водорода в молекулы протекает значительно быстрее на поверхности металлов, чем в самом газе. При этом металл воспринимает ту энергию, которая выделяется при образовании молекул и нагревании до очень высоких температур. Последнее создаёт возможность технического использования атомарного водорода для атомно-водородной сварки металлов: между двумя вольфрамовыми стержнями создаётся электрическая дуга, сквозь которую по облегающим стержни трубкам пропускается ток водорода. При этом часть молекул Н2 распадается на атомы, которые затем вновь соединяются на металлической поверхности, помещенной недалеко от дуги. Таким путём металл может быть нагрет выше 3500 °С. В этих условиях происходит быстрая и прочная сварка отдельных его кусков. Большим достоинством атомно-водородной сварки является равномерность нагрева, позволяющая сваривать даже тонкие металлические детали.
Соединение атомов водорода осуществляется гораздо легче на твёрдой поверхности. При реакции по схеме Н + Н = Н2 молекула водорода заключает в себе и кинетическую энергию обоих соединяющихся атомов, и энергию их взаимодействия. В сумме это даёт запас энергии, с избытком превышающий энергию диссоциации молекулы Н2 на атомы. Такая диссоциация не происходит только в том случае, если молекула быстро освобождается от избытка энергии, передавая его какой-либо другой частице. В самом газе это может осуществляться лишь путём тройного столкновения по схеме Н + Н + Х = Н2 + Х, где Х - частица, принимающая избыток энергии. Но вероятность тройного столкновения несравненно меньше вероятности двойного, и поэтому в газе рекомбинация (обратное соединение) атомов Н идёт сравнительно медленно. Напротив, у твёрдой поверхности к образованию молекулы может вести каждое двойное столкновение атомов Н, так как воспринимающая избыток энергии частица (в виде атома или молекулы вещества самой поверхности) всегда имеется.
Химические свойства молекулярного водорода
Исключительная прочность молекул водорода (например, прочнее молекул фтора в 2,7 раза) обуславливает высокие энергии активации химических реакции с участием молекулярного водорода. При обычных условиях в газообразном водороде активных молекул немного и молекулярный водород малоактивен. Он способен непосредственно соединяться лишь с наиболее активными из неметаллов – с фтором и на свету с хлором. С фтором водород взрывается уже при температуре жидкого воздуха. Для инициирования реакций молекулярного водорода с другими веществами требуется нагрев или другие способы активации. При нагревании же молекулярный водород вступает в химическое взаимодействие со многими металлами, неметаллами и сложными веществами.
| Реагент | Условия реакции | Продукт |
| S | 600 °C | H2S |
| F2, Cl2 | свет | HHal |
| Br2, J2 | нагрев | HHal |
| N2 | Катализатор, 450-550 °C | NH3 |
| O2 | 700 °C | H2O |
| C | акт. уголь, 500-1000 °C | CH4 |
| Металлы | нагрев | Солеподобные (s-элементы, элементы IA группы, Ca, Sr, Ba); Металлоподобные (d- и f-элементы); Полимерные (Be, Mg, p-элементы IIIA группы) вещества. |
Смеси водорода с хлором взрываются не только при нагревании, но и при освещении.
Водород горит несветящимся пламенем, образуя воду. При поджигании смеси двух объемов водорода с одним объемом кислорода соединение газов происходит почти мгновенно во всем объеме смеси и сопровождается сильным взрывом. Поэтому такую смесь называют гремучим газом. Смеси водорода с воздухом или кислородом взрываются при поджигании в интервале составов от 5 до 95% по объему. При горении водорода выделяется большое количество теплоты. Температура водородного пламени может достигать 2800 °C. Водородно-кислородным пламенем пользуются для сварки и резки металлов, для плавления тугоплавких металлов.
При низких температурах водород с кислородом практически не взаимодействуют. Если смешать оба газа и оставить смесь, то и через несколько лет в ней нельзя обнаружить даже признаков воды. Если же смесь водорода с кислородом поместить в запаянный сосуд и держать в нем при 300 °C, то уже через несколько дней образуется немного воды. При 500 °C, водород полностью соединиться с кислородом за несколько часов, а при 700 °C происходит взрыв смеси.
Благодаря высокой энергии (прочности) связей H-O и H-Cl при высокой температуре водород может отнимать кислород и хлор от многих соединений, в т.ч. от большинства оксидов и галогенидов металлов:
На этом основано применение водорода в качестве восстановителя для получения ряда простых веществ из оксидов и галогенидов.
Водород при нагревании восстанавливает металлы из их оксидов, галогенидов, нитратов, неметаллы – из их высших степеней окисления в низшие. По восстановительной активности водород уступает таким широко распространенным в технике восстановителям, как уголь, алюминий, кальций и др., щелочные металлы, гидриды, щелочно-земельные металлы.
Химические свойства атомарного водорода
Уже при комнатной температуре атомарный водород восстанавливает многие оксиды металлов, непосредственно соединяется с серой, азотом, фосфором, мышьяком, кислородом и др.
С кислородом образуется пероксид водорода:
Реакционная способность водорода сильно возрастает и в момент его выделения из соединений:
Реакция водорода

Реакция водорода с хлором идёт или при нагревании, или при освещении синим или ультрафиолетовым светом. И если нагревание или освещение будут слишком сильными, то смесь взорвётся (а вот смесь водорода с парами йода никогда не взрывается).
Тот же Боденштейн в 1913 году обнаружил поразительный факт: на один квант света, поглощённый хлором (водород свет не поглощает), может образоваться до миллиона молекул продукта — хлороводорода!
Для объяснения этого необычного факта был предложен (а затем доказан) цепной механизм реакции.
Н + С12 = НС1 + С1. Так возникает цепочка следующих друг за другом химических превращений.
В результате цепь обрывается.
Это легко происходит при низких давлениях, когда частицы в газе пролетают значительное расстояние, не встречаясь с другими частицами.
Но если ввести в реакцию даже самые малые количества веществ, способных реагировать с этими атомами так, чтобы новые активные частицы не возникали, то цепи начнут обрываться и реакция остановится. Таким веществом может служить кислород: реагируя с атомами водорода, он образует воду, а с атомами хлора даёт оксид хлора, не участвующий далее в реакции.
Такие вещества, тормозящие или вовсе останавливающие реакцию, называются ингибиторами (отлат.
Цепные реакции идут со взрывной скоростью во многих газовых смесях горючего вещества с кислородом или с воздухом. Взрыв происходит, например, при поджигании смеси природного газа с воздухом.
По цепному механизму идут реакции синтеза многих полимеров, растворителей (в том числе ацетона), реагентов для получения моющих средств.
Именно поэтому так много усилий было направлено на изучение механизма цепных реакций. А вот ещё один очень важный пример сложного механизма реакции.
Поэтому для того, чтобы связать атмосферный азот, превратить его в аммиак NH3, строят огромные колонны, в которых молекулы N2 и Н2 превращаются в молекулы NH3 при давлении 300 атмосфер и температуре 500 °С. Аммиак же нужен для производства удобрений, лекарств, полимеров и многих других веществ, содержащих азот. В то же время давно известно, что в природе в огромных количествах происходит биологическая азотфиксация — связывание атмосферного азота в аммиак (вернее, в ион аммония NH4). Протекает этот процесс в микроорганизмах, которые называются азотфиксирующими; они обитают в почве, в особых клубеньках на корнях, а иногда и на стеблях бобовых растений.
И эти организмы прекрасно справляются со своей работой при комнатной температуре и атмосферном давлении! Как же они это делают?
Главную роль в азотфиксации играет биологический катализатор — фермент, который называется нитрогеназой.
И как для исполнения симфонии требуется большой оркестр, каждый участник которого исполняет свою партию и при этом внимательно слушает других, так же и для расщепления молекулы азота необходима слаженная работа множества сложно устроенных биохимических механизмов. Прежде всего, оказалось, что нитрогеназа состоит из двух белков, содержащих атомы железа и молибдена, и имеет молекулярную массу около 300 тысяч!
Но и это не всё. Для работы этого фермента требуется непрерывный приток энергии и электронов, которые поставляются другими молекулами.
В свою очередь, этот приток обеспечивается процессами дыхания и брожения в микроорганизмах, а иногда — и за счёт солнечного света. То есть здесь работает целый биохимический завод!
Если бы химики смогли воспроизвести в своих колбах этот процесс, а также множество других реакций, управляемых ферментами, мир изменился бы до неузнаваемости!
- Политика (1191)
- Аксессуары (1191)
- Поиск (214)
- Лирика (210)
- Полезный материал (19)
- Печатная продукция. Оформление (17)
- Кошельки и сумки (12)
- Полезное для детей (12)
- Психология (10)
- Детский сад (9)
- Занятия (5)
- Зарядка (2)
- Для родителей (2)
- Drops (9)
- В работу (8)
- Хлебопечка (7)
- Ткачество (6)
- Легкий крой (3)
- Йога (3)
- Фото (3)
- Библиотека по шитью (3)
- Для Женщины (2)
- История (2)
- Магазины (2)
- Огород (1)
- Самое интересное (1)
- Театр (1)
- Сам себе парикмахер (1)
- Малахов (1)
- Умные мысли (1)
- Туризм (1)
- Свое дело (1)
- Аптека (144)
- Астрология (2)
- Библиотека вязания (210)
- Библиотека рукоделия (38)
- Бижутерия (22)
- Бисероплетение (4)
- Видео (12)
- Видеорецепты (3)
- Виртуальные экскурсии (5)
- Витражи. Роспись. (8)
- Все для принцесс (53)
- Все о пряже (10)
- вышивание (97)
- Вязание для детей (452)
- Вязание крючком (347)
- Вязание крючком и спицами (77)
- Вязание крючком, узоры (142)
- Вязание на вилке (9)
- Вязание на машине (282)
- Вязание на тенерифе (1)
- Вязание спицами (1799)
- Вязание спицами, узоры (155)
- Декор интерьера (79)
- Декупаж (13)
- Для ножек (94)
- Заготовки на зиму (4)
- Здоровье малышей (5)
- Игрушки (50)
- Идеи (55)
- Интересные сайты (17)
- К праздникам (47)
- Кино (53)
- Комнатные цветы (12)
- Красивости (8)
- Крючок и спицы для дома (159)
- Кулинария (249)
- Мастер-классы по вязанию (92)
- Мастер-классы по шитью (22)
- Мастер-классы, ассорти (29)
- Мебель (10)
- Мода (75)
- Музыка (10)
- Мыловарение (44)
- Новая жизнь старых вещей (22)
- Объявления (0)
- Оформление дневника (23)
- Парикмахерская (4)
- Переводы (31)
- Полезное (104)
- Помощь (70)
- Праздничные рецепты (4)
- Программы по рукоделию (10)
- Пэчворк (30)
- Развлечения (14)
- Раздумья (180)
- Рукоделие (151)
- Сайты по вязанию (15)
- Салон красоты (151)
- Тенерифе (1)
- Техника энтерлак (1)
- Ткань+вязание, комбинированные модели (17)
- Тунисское вязание (1)
- Хозяйство (32)
- ХОЧУ. (246)
- Читальный зал (3)
- Шитье (265)
- Школа по вязанию (79)
- Юмор (15)
- Все (4)
ЭТО НЕОБХОДИМО ЗНАТЬ КАЖДОМУ . - Предупреждён - вооружен. Действия при аварии с выбросом хлора
1.
Предупреждён - вооружен. Действия при аварии с выбросом хлора
Хлор - газ с резким специфическим запахом, тяжелее воздуха, при испарении стелется над землей в виде тумана, может проникать в нижние этажи и подвалы зданий, при выходе в атмосферу дымит. Пары сильно раздражают органы дыхания, глаза, кожу. При вдыхании высоких концентраций возможен смертельный исход.
При получении информации об аварии с АХОВ наденьте средства защиты органов дыхания, средства защиты кожи (плащ, накидка) , покиньте район аварии в направлении, указанном в сообщении по радио (телевидению) .
Выходить из зоны химического заражения следует в сторону, перпендикулярную направлению ветра. При этом избегайте перехода через туннели, овраги и лощины - в низких местах концентрация хлора выше.
Если из опасной зоны выйти невозможно, останьтесь в помещении и произведите его экстренную герметизацию: плотно закройте окна, двери, вентиляционные отверстия, дымоходы, уплотните щели в окнах и на стыках рам и поднимитесь на верхние этажи здания.
Выйдя из опасной зоны, снимите верхнюю одежду, оставьте ее на улице, примите душ, промойте глаза и носоглотку.
При появлении признаков отравления: покой, теплое питье, обратитесь к врачу.
Признаки отравления хлором: резкая боль в груди, сухой кашель, рвота, резь в глазах, слезотечение, нарушение координации движений.
Средства индивидуальной защиты: противогазы всех типов.
ВЫБРОС ХЛОРА: СИМПТОМЫ ОТРАВЛЕНИЯ И ПЕРВАЯ ПОМОЩЬ
Поделиться…
Выброс хлора: симптомы отравления и первая помощьХлор является сильнодействующим ядовитым веществом удушающего характера. Что делать, если на предприятии или близлежащем химическом заводе произошла утечка хлора?
Хлор – это газ с резким специфическим запахом. Он тяжелее воздуха, при испарении похож на туман.
Как эффективный бактерицид хлор начал использоваться почти два столетия назад. С одной стороны, хлор спас сотни тысяч жизней благодаря своей способности разрушать вредные бактерии и вирусы, но в то же время он оказывает отравляющее воздействие и на человека.
Кроме этого, хлор является одним из важнейших продуктов химической промышленности по объёму производства и области применения.
При нормальных условиях хлор представляет собой газ зеленовато-жёлтого цвета с резким раздражающим запахом, в сжиженном же состоянии хлор может находиться только при избыточном давлении или при температуре ниже минус 34 °С.
При утечке хлор дымит, при температуре -34 °С сжижается, при температуре -101 °С затвердевает. Хлор малорастворим в воде – в одном объёме воды растворяется около двух его объёмов. Жидкий хлор в 1,5 раза тяжелее воды, газообразный хлор в 2,5 раза тяжелее воздуха.
Один килограмм жидкого хлора при испарении дает 315 литров газообразного хлора, при испарении на воздухе в значительных количествах даёт с водяными парами белый туман. В смеси с водородом (более 50 % водорода) хлор взрывоопасен, а при нагревании ёмкости с хлором взрываются.
Хранится и транспортируется жидкий хлор в сосудах, выдерживающих избыточное давление. Один баллон с жидким хлором при разгерметизации становится бомбой с радиусом поражения от 150 метров до 1 километра, с действием в зоне поражения более суток.
Чем опасен хлор?
Наибольшую опасность представляет хлор в сжиженном состоянии. При выбросах жидкого хлора смертельно опасную зону составляет площадь в радиусе примерно 400 м от места выброса.
Опасность хлора заключается во взаимодействии хлоргаза со слизистыми оболочками человека – образуется соляная кислота, вызывающая отёк лёгких, поражение глаз и носа, кожные раздражения. При вдыхании высоких концентраций хлора возможен смертельный исход – попадая в лёгкие, он обжигает лёгочную ткань и вызывает удушье.
Учёные предполагают, что хлор, как и продукты его взаимодействия с другими веществами, увеличивает риск сердечно-сосудистых заболеваний, аллергических реакций и выкидышей у беременных женщин.
Признаки отравления хлором
При вдыхании хлор вызывает судорожный, мучительный кашель, в тяжёлых случаях происходит спазм голосовых связок и отёк лёгких. Хлор раздражающе действует на влажную кожу, вызывая её покраснение, могут иметь место химические ожоги и обморожение. Также хлор оказывает сковывающее воздействие на центральную нервную систему.
Первыми явными признаками отравления хлором являются:
резкая боль в груди,
сухой кашель,
рвота,
резь в глазах (слезотечение),
нарушение координации движений.
Действия при аварии с выбросом хлора
При получении информации об аварии нужно:
Защитить органы дыхания и поверхность тела. Лицо, нос и рот можно защитить с помощью противогазов всех типов, марлевой повязки, смоченной водой или 20 % раствором соды (1 чайная ложка на стакан воды). Средством защиты кожи может послужить любая накидка.
Покинуть район аварии в направлении, указанном в сообщении. Вне помещения выходить из зоны химического заражения следует в сторону, перпендикулярную направлению ветра. Избегайте перехода через туннели, овраги и лощины, так как в низких местах концентрация хлора будет выше.
Если из опасной зоны выйти невозможно, нужно остаться в помещении и произвести его герметизацию: плотно закройте окна, двери, вентиляционные отверстия, дымоходы, уплотните щели в окнах и на стыках рам. Входные двери зашторьте, используя одеяла и любые плотные ткани. При возможности поднимитесь на верхние этажи здания. Нельзя укрываться на первых этажах многоэтажных зданий, в подвальных и полуподвальных помещениях.
Оказавшись вне опасной зоны, нужно снять верхнюю одежду и оставить её на улице.
Как можно быстрее принять душ, промыть глаза и носоглотку.
Наблюдать за своим самочувствием, при первом появлении признаков отравления обратиться к врачу. В ожидании помощи пострадавшему необходим покой и тёплое питьё.
Как помочь пострадавшему?
Пострадавшего от отравления хлором нужно как можно быстрее вынести из опасной зоны. При транспортировке пострадавший должен быть в горизонтальном положении.
Вне опасной зоны снимите с пострадавшего всю одежду, стесняющую дыхание, и уложите в горизонтальное положение. Необходимо обеспечить покой, тепло, приток свежего воздуха.
В ожидании медицинской помощи рекомендуется:
обильное тёплое питьё – 2 % раствор соды, боржоми, молоко с содой, чай, кофе;
при кашле или першении в горле необходимы тёпло-влажные ингаляции 2 % раствором соды, противокашлевые препараты;
при слезотечении, жжении в глазах – промывание глаз водой или 2 % раствором соды. Этим же раствором нужно промыть нос. В глаза можно закапать 30 % раствор альбуцида;
при затруднении дыхания, осиплости голоса – вводится подкожно 1 мл 0,1 %-ного раствора атропина;
при обмороке – нужно дать понюхать нашатырный спирт. При отсутствии дыхания немедленно приступить к его восстановлению.
Рекомендуется затемнить помещение. При первой возможности пострадавшие должны быть доставлены в медицинское учреждение для обследования и дальнейшего лечения.
Читайте также:

