Визуализация рака поджелудочной железы
Авторы: Christoph F. Dietrich, Christian Jenssen
Введение: чем меньше поражение, тем лучше прогноз
Симптоматическая аденокарцинома протоков поджелудочной железы (АППЖ), которая является наиболее часто диагностируемой солидной злокачественной опухолью поджелудочной железы, обычно диагностируется на поздних стадиях с метастазами или без них.
Большинство международно признанных руководств рекомендуют радикальные операции при всех небольших солидных образованиях поджелудочной железы (СОПЖ), если нет подозрений на этиологию другого образования или отсутствуют противопоказания.
Ранняя диагностика этой опухоли в бессимптомных стадиях имеет решающее значение для улучшения ее прогноза. Данные из японского реестра рака поджелудочной железы показывают, что чем меньше поражение во время диагностики, тем дольше ожидаемая 5-летняя выживаемость.
Точность традиционных методов визуализации, включая ультразвуковое исследование (УЗИ), компьютерную томографию (КТ) и магнитно-резонансную томографию (МРТ), в дифференциальной диагностике образований поджелудочной железы оказалась не утешительной.
КТ была рекомендованным методом диагностики для постановки стадии рака ПЖ, но показала неудовлетворительные результаты для выявления небольших солидных образований (
Эндоскопическая ультрасонография (ЭУЗИ) считается методом визуализации, исключающим АППЖ. На основании 22 исследований, включающих 1170 случаев, суммарная чувствительность ЭУЗИ для выявления солидных образований составила 94%, что заметно выше, чем сообщаемые результаты для мультидетекторной КТ, МРТ и трансабдоминальной УЗИ. Кроме того, ЭУЗИ предоставляет возможность обнаружить бессимптомные варианты АППЖ.
Методы визуализации с контрастом позволяют улучшить видимость характеристик опухоли перед радикальной операцией, а биопсия тонкой иглой успешно позволяет проводить предоперационную дифференциальную диагностику во многих случаях.
CEUS или C-EUS
Применение контрастной ЭУЗД (C-EUS) улучшило производительность эндоскопической визуализации. Многоцентровое исследование поджелудочной железы в США с участием более 1000 пациентов и другие исследования, использующие УЗИ с контрастным усилением (CEUS) и C-EUS, показали улучшенную диагностическую точность для характеристики очаговых образований поджелудочной железы.
Только 146 из 394 небольших солидных новообразований (37%) были окончательно диагностированы как АППЖ. В подгруппе солидных образований размером 15 мм (n = 83) 51 поражение оказалось АППЖ (62%).
Наиболее важным дифференциальным диагнозом АППЖ является нейроэндокринные опухоли. Третьей по частоте этиологии были метастазы в поджелудочной железе (n = 28,7%). Другие дифференциальные диагнозы включали нередко гиперваскулярную серозную микроцистную цистаденому, солидную псевдопапиллярную опухоль, неходжкинскую лимфому, очаговый панкреатит, внутрипанкреатическую добавочную селезенку и гамартому.
Можно сделать вывод, что чем меньше солидное новообразование, тем менее вероятен диагноз АППЖ и тем чаще диагностируется нейроэндокринные опухоли.
CEUS и/или C-EUS были выполнены у 219 из 394 пациентов с использованием внутривенной инъекции SonoVue 2,4 мл (CEUS) или 4,8 мл (C-EUS) в соответствии с рекомендациями Европейской федерации ультразвука в медицине и биологии.
Изо-, гипер- или гипо-усиление по сравнению с окружающей паренхимой поджелудочной железы были задокументированы: у 57 из 62 пациентов (92%) АППЖ демонстрировала гипоусиление, в то время как у пациентов без АППЖ наблюдалось изо- или гиперусиление по сравнению с окружающей паренхимой. Кроме того, 91 из 102 нейроэндокринных опухолей (89%) имели гипер- или изоусиление, что привело к правильной дифференциальной диагностике.
Результаты с использованием CEUS были достовернее по сравнению с КТ; КТ не очертила очаговое поражение поджелудочной железы у 14 из 38 пациентов (средний диаметр 8 мм [диапазон от 4 до 12 мм) ])
В соответствии с опубликованной литературой, CEUS и C-EUS позволяют проводить дифференциальную диагностику солидных опухолей поджелудочной железы примерно в 90% случаев.
ЭУЗИ против УЗИ
УЗИ проводилась до ЭУЗИ у 45 пациентов (средний возраст: 59 лет; диапазон от 18 до 81 года; 20 мужчин и 25 женщин) с 25 (56%) злокачественными и 20 (44%) доброкачественными солидными образованиями.
У 5 из 45 пациентов (11%) солидные опухоли не были обнаружены во время УЗИ. У 6 из 45 пациентов (13%) выявление поражения при УЗИ и CEUS было возможно только при знании результатов ЭУЗИ. У 34 из 45 пациентов (76%) солидные опухоли были обнаружены во время УЗИ до обследования ЭУЗИ.
Мы пришли к выводу, что большинство солидных образований может быть обнаружено с помощью УЗИ, а оценка CEUS возможна для дальнейшей характеристики (рис. 1, 2).

Рисунок 1 : Нейроэндокринная неоплазия.
A, B. Показаны очаговые поражения поджелудочной железы, которые были гиперцентричными при использовании методов визуализации с контрастным усилением (7 × 6 мм, между маркерами) с использованием эндоскопической ультрасонографии (A) и чрескожной контрастной ультрасонографии (B). C. Также показано мягкое эластографическое изображение, указывающее на доброкачественное поражение.
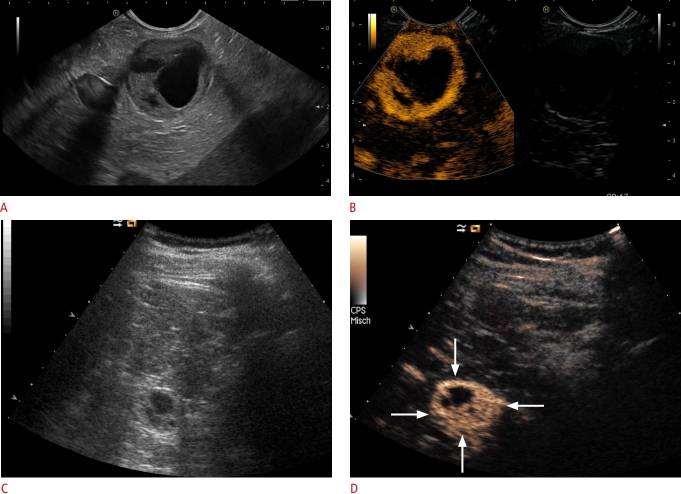
Рисунок 2 : Нейроэндокринная смешанная солидно-кистозная неоплазия.
Показаны солидно-кистозные очаговые поражения поджелудочной железы (отмечены стрелками) с использованием B-режима (A), которые были гиперцентричными при эндоскопической ультрасонографии с контрастом (B) и B-режиме (C) и ультрасонографии с контрастом (D). Нейроэндокринная неоплазия была диагностирована с помощью биопсии и гистопатологической оценки.
Ультразвуковая эластография
Ультразвуковая эластография позволяет оценить жесткость ткани путем виртуальной пальпации. Для оценки небольших очаговых поражений поджелудочной железы была разработана ультразвуковая тензометрическая эластография с использованием ЭУЗИ.
Мягкие небольшие солидные образования обычно доброкачественные, тогда как более жесткие (более твердые) в паренхиме поджелудочной железы – злокачественные.
Можно сказать, что, особенно у пациентов с небольшими поражениями поджелудочной железы, ЭУЗИ-эластография может исключать злокачественные новообразования с высокой степенью достоверности, если поражение отображается как мягкое. В более крупных (> 30 мм) результаты менее убедительны, главным образом, из-за гетерогенности поражений, но также из-за сопутствующих изменений окружающей паренхимы поджелудочной железы.
Эластография не способна окончательно дифференцировать очаговый панкреатит от АППЖ, поскольку хронический очаговый панкреатит также может быть более жестким, чем в остальном здоровая паренхима поджелудочной железы. Туберкулез поджелудочной железы также жестче, чем окружающая паренхима, но применение и правильная интерпретация эластографии при хроническом панкреатите являются более сложными.
Вывод
У пациентов с солидными опухолями этиологическая дифференциация необходима для принятия обоснованных решений о дальнейшем лечении:
- радикальное хирургическое вмешательство у пациентов с резектабельным АППЖ
- онкологическое лечение у пациентов с неоперабельным злокачественным новообразованием
- стратегии сохранения панкреатической паренхимы или наблюдение при доброкачественной нейроэндокринной неоплазии
- последующее наблюдение при небольших доброкачественных поражениях (рис. 3).

Рисунок 3 : Алгоритм диагностики.
На основании паттерна улучшения результатов CEUS и эластографии возможна дальнейшая характеристика солидных новообразований. Гиповаскулярность наблюдается примерно в 90% случаев АППЖ. Мягкие солидные опухоли являются доброкачественными, за очень немногими исключениями.
Таким образом, у пациентов с гиперваскулярными и/или мягкими образованиями, биопсия ткани рекомендуется до принятия решения о лечении, поскольку радикальная операция может быть нецелесообразной.
ПРАВИЛЬНО ЛИ ВЫ УХАЖИВАЕТЕ ЗА УЗ-АППАРАТОМ?
Скачайте руководство по уходу прямо сейчас

Пациентам с серозной цистаденомой, мезенхимальными поражениями, и нефункциональными нейроэндокринными опухолями 10 мм с индексом Ki67> 3% часто требуют наблюдения из-за их злокачественного потенциала.
Авторы: Christoph F. Dietrich, Christian Jenssen
Введение: чем меньше поражение, тем лучше прогноз
Симптоматическая аденокарцинома протоков поджелудочной железы (АППЖ), которая является наиболее часто диагностируемой солидной злокачественной опухолью поджелудочной железы, обычно диагностируется на поздних стадиях с метастазами или без них.
Большинство международно признанных руководств рекомендуют радикальные операции при всех небольших солидных образованиях поджелудочной железы (СОПЖ), если нет подозрений на этиологию другого образования или отсутствуют противопоказания.
Ранняя диагностика этой опухоли в бессимптомных стадиях имеет решающее значение для улучшения ее прогноза. Данные из японского реестра рака поджелудочной железы показывают, что чем меньше поражение во время диагностики, тем дольше ожидаемая 5-летняя выживаемость.
Точность традиционных методов визуализации, включая ультразвуковое исследование (УЗИ), компьютерную томографию (КТ) и магнитно-резонансную томографию (МРТ), в дифференциальной диагностике образований поджелудочной железы оказалась не утешительной.
КТ была рекомендованным методом диагностики для постановки стадии рака ПЖ, но показала неудовлетворительные результаты для выявления небольших солидных образований (
Эндоскопическая ультрасонография (ЭУЗИ) считается методом визуализации, исключающим АППЖ. На основании 22 исследований, включающих 1170 случаев, суммарная чувствительность ЭУЗИ для выявления солидных образований составила 94%, что заметно выше, чем сообщаемые результаты для мультидетекторной КТ, МРТ и трансабдоминальной УЗИ. Кроме того, ЭУЗИ предоставляет возможность обнаружить бессимптомные варианты АППЖ.
Методы визуализации с контрастом позволяют улучшить видимость характеристик опухоли перед радикальной операцией, а биопсия тонкой иглой успешно позволяет проводить предоперационную дифференциальную диагностику во многих случаях.
CEUS или C-EUS
Применение контрастной ЭУЗД (C-EUS) улучшило производительность эндоскопической визуализации. Многоцентровое исследование поджелудочной железы в США с участием более 1000 пациентов и другие исследования, использующие УЗИ с контрастным усилением (CEUS) и C-EUS, показали улучшенную диагностическую точность для характеристики очаговых образований поджелудочной железы.
Только 146 из 394 небольших солидных новообразований (37%) были окончательно диагностированы как АППЖ. В подгруппе солидных образований размером 15 мм (n = 83) 51 поражение оказалось АППЖ (62%).
Наиболее важным дифференциальным диагнозом АППЖ является нейроэндокринные опухоли. Третьей по частоте этиологии были метастазы в поджелудочной железе (n = 28,7%). Другие дифференциальные диагнозы включали нередко гиперваскулярную серозную микроцистную цистаденому, солидную псевдопапиллярную опухоль, неходжкинскую лимфому, очаговый панкреатит, внутрипанкреатическую добавочную селезенку и гамартому.
Можно сделать вывод, что чем меньше солидное новообразование, тем менее вероятен диагноз АППЖ и тем чаще диагностируется нейроэндокринные опухоли.
CEUS и/или C-EUS были выполнены у 219 из 394 пациентов с использованием внутривенной инъекции SonoVue 2,4 мл (CEUS) или 4,8 мл (C-EUS) в соответствии с рекомендациями Европейской федерации ультразвука в медицине и биологии.
Изо-, гипер- или гипо-усиление по сравнению с окружающей паренхимой поджелудочной железы были задокументированы: у 57 из 62 пациентов (92%) АППЖ демонстрировала гипоусиление, в то время как у пациентов без АППЖ наблюдалось изо- или гиперусиление по сравнению с окружающей паренхимой. Кроме того, 91 из 102 нейроэндокринных опухолей (89%) имели гипер- или изоусиление, что привело к правильной дифференциальной диагностике.
Результаты с использованием CEUS были достовернее по сравнению с КТ; КТ не очертила очаговое поражение поджелудочной железы у 14 из 38 пациентов (средний диаметр 8 мм [диапазон от 4 до 12 мм) ])
В соответствии с опубликованной литературой, CEUS и C-EUS позволяют проводить дифференциальную диагностику солидных опухолей поджелудочной железы примерно в 90% случаев.
ЭУЗИ против УЗИ
УЗИ проводилась до ЭУЗИ у 45 пациентов (средний возраст: 59 лет; диапазон от 18 до 81 года; 20 мужчин и 25 женщин) с 25 (56%) злокачественными и 20 (44%) доброкачественными солидными образованиями.
У 5 из 45 пациентов (11%) солидные опухоли не были обнаружены во время УЗИ. У 6 из 45 пациентов (13%) выявление поражения при УЗИ и CEUS было возможно только при знании результатов ЭУЗИ. У 34 из 45 пациентов (76%) солидные опухоли были обнаружены во время УЗИ до обследования ЭУЗИ.
Мы пришли к выводу, что большинство солидных образований может быть обнаружено с помощью УЗИ, а оценка CEUS возможна для дальнейшей характеристики (рис. 1, 2).

Рисунок 1 : Нейроэндокринная неоплазия.
A, B. Показаны очаговые поражения поджелудочной железы, которые были гиперцентричными при использовании методов визуализации с контрастным усилением (7 × 6 мм, между маркерами) с использованием эндоскопической ультрасонографии (A) и чрескожной контрастной ультрасонографии (B). C. Также показано мягкое эластографическое изображение, указывающее на доброкачественное поражение.

Рисунок 2 : Нейроэндокринная смешанная солидно-кистозная неоплазия.
Показаны солидно-кистозные очаговые поражения поджелудочной железы (отмечены стрелками) с использованием B-режима (A), которые были гиперцентричными при эндоскопической ультрасонографии с контрастом (B) и B-режиме (C) и ультрасонографии с контрастом (D). Нейроэндокринная неоплазия была диагностирована с помощью биопсии и гистопатологической оценки.
Ультразвуковая эластография
Ультразвуковая эластография позволяет оценить жесткость ткани путем виртуальной пальпации. Для оценки небольших очаговых поражений поджелудочной железы была разработана ультразвуковая тензометрическая эластография с использованием ЭУЗИ.
Мягкие небольшие солидные образования обычно доброкачественные, тогда как более жесткие (более твердые) в паренхиме поджелудочной железы – злокачественные.
Можно сказать, что, особенно у пациентов с небольшими поражениями поджелудочной железы, ЭУЗИ-эластография может исключать злокачественные новообразования с высокой степенью достоверности, если поражение отображается как мягкое. В более крупных (> 30 мм) результаты менее убедительны, главным образом, из-за гетерогенности поражений, но также из-за сопутствующих изменений окружающей паренхимы поджелудочной железы.
Эластография не способна окончательно дифференцировать очаговый панкреатит от АППЖ, поскольку хронический очаговый панкреатит также может быть более жестким, чем в остальном здоровая паренхима поджелудочной железы. Туберкулез поджелудочной железы также жестче, чем окружающая паренхима, но применение и правильная интерпретация эластографии при хроническом панкреатите являются более сложными.
Вывод
У пациентов с солидными опухолями этиологическая дифференциация необходима для принятия обоснованных решений о дальнейшем лечении:
- радикальное хирургическое вмешательство у пациентов с резектабельным АППЖ
- онкологическое лечение у пациентов с неоперабельным злокачественным новообразованием
- стратегии сохранения панкреатической паренхимы или наблюдение при доброкачественной нейроэндокринной неоплазии
- последующее наблюдение при небольших доброкачественных поражениях (рис. 3).

Рисунок 3 : Алгоритм диагностики.
На основании паттерна улучшения результатов CEUS и эластографии возможна дальнейшая характеристика солидных новообразований. Гиповаскулярность наблюдается примерно в 90% случаев АППЖ. Мягкие солидные опухоли являются доброкачественными, за очень немногими исключениями.
Таким образом, у пациентов с гиперваскулярными и/или мягкими образованиями, биопсия ткани рекомендуется до принятия решения о лечении, поскольку радикальная операция может быть нецелесообразной.
ПРАВИЛЬНО ЛИ ВЫ УХАЖИВАЕТЕ ЗА УЗ-АППАРАТОМ?
Загрузите руководство по уходу прямо сейчас
Пациентам с серозной цистаденомой, мезенхимальными поражениями, и нефункциональными нейроэндокринными опухолями 10 мм с индексом Ki67> 3% часто требуют наблюдения из-за их злокачественного потенциала.
Вы открыли или планируете открыть медицинский центр?
Загрузите маркетинговый план развития медицинского центра бесплатно!
Скачать PDF 
Получите доступ к материалам где мы разбираем ТОП-5 главных критериев при выборе УЗ апарата

Ультразвуковое исследование является традиционным методом диагностики различных опухолей в брюшной полости. Рак поджелудочной железы на УЗИ определяется в виде неоднородного образования в ткани органа. Заболевание отличается высокой злокачественностью. Пятилетняя выживаемость после операции составляет до 20%. Раннее выявление продлевает жизнь на несколько лет. Лечат онкологию поджелудочной железы оперативным методом, дополняя лучевой, гормональной и иммунной терапией.
Строение и функционал органа
Поджелудочная железа – орган пищеварительного тракта, расположенный в верхней части живота. Состоит из хвоста, головки и тела. Мелкие протоки поджелудочной, объединяясь с общим желчным ходом, открываются в двенадцатиперстную кишку.
Функционально железа состоит из двух частей: внешнесекреторной (основная масса клеток) и эндокринной. В экзокринной части синтезируются ферменты – амилаза, липазы, а также протеазы.
Эндокринная ткань сосредоточена в хвостовой части органа. Ее клетки синтезируют инсулин, глюкагон и другие биологически активные вещества.
Как работает ультразвуковое исследование
Ультразвуковой сканер позволяет визуализировать патологические новообразования. Датчик, находящийся в контакте с поверхностью тела, проводит звуковые волны через брюшную стенку. Далее сигнал пронизывает органы. Разные ткани отличаются по сопротивляемости к звуку. Феномен называется акустическим сопротивлением. В месте препятствий часть волн отражается. Рак поджелудочной железы по УЗИ определяется как эхогенное препятствие ходу сигнала. Во время исследования сонолог оценивает характер кровоснабжения образования, определяя степень его злокачественности.
В каких случаях нужна УЗИ-диагностика
Назначают УЗИ, если у пациента есть признаки, характерные для поражения органа. Триадой симптомов рака поджелудочной железы являются:
- желтуха,
- боль в эпигастрии,
- резкое похудение.
Симптомы свидетельствуют о прогрессировании опухоли, сопровождающимся раковой интоксикацией.

Также показаниями для проведения исследования являются:
- травма в проекции органа,
- расстройство стула, метеоризм,
- сахарный диабет,
- дискомфорт в животе, связанный с приемом пищи,
- изменение лабораторных показателей в крови и моче,
- подозрение на злокачественных процесс в поджелудочной железе,
- метастазы в брюшине от опухолей другой локализации,
- ведение хронического панкреатита.
Разновидностью УЗИ является допплерография. Во время исследования с помощью специального датчика сонолог оценивает характер кровотока органа. Извилистые сосуды говорят о злокачественном процессе.
Подготовка к исследованию
Подготовку к процедуре начинают за 2-3 суток. Для точной диагностики РПЖ (рака поджелудочной железы) необходимо исключить продукты, способствующие усиленному газообразованию:
- бобовые,
- сдобная выпечка,
- фрукты и овощи с высоким содержанием клетчатки,
- цельное молоко,
- алкоголь.
Накануне проведения исследования пропускают ужин. Последний прием пищи должен состояться как минимум за 6-7 часов до процедуры.
Проведение диагностики
Исследование проводят утром. Диагностику выполняет врач-сонолог. Процедура абсолютно безболезненна. Проведение обследования практически не требует приложения усилий со стороны пациента.
Брюшную стенку перед началом процедуры оголяют. Для лучшей визуализации исследуемого просят надуть живот и на несколько секунд задержать дыхание. Для хорошего проведения сигнала на датчик наносят изоэлектрический гель.
Результаты исследования
Результаты зависят от локализации и размера опухоли. При единичном новообразовании заметен один очаг, при прогрессии – визуализируется плотный опухолевый конгломерат.
УЗИ покажет онкологию при размере опухоли больше 2 мм. Современные датчики визуализируют образования меньшего диаметра, но доступны только в научно-исследовательских центрах.
Опухоль видна на мониторе УЗИ-аппарата в виде объемного образования неправильной формы с неровными краями. Измененные ткани низкой эхогенности. Структура образования неоднородная.
Часто тяжело дифференцировать рак от псевдотуморозной формы панкреатита. При данной патологии Вирсунгов проток значительно расширен, а при раке наблюдается неравномерное изменение его просвета.
Во время исследования оценивают возможность проведения операции. Расположение опухоли между ножками крупных артериальных сосудов является противопоказанием к хирургическому вмешательству.
Метастазы ищут в печени, почках, регионарных лимфоузлах. Они визуализируются в виде слабо эхогенных очагов.
Наиболее чувствительным методом является метод эндосонографии. В отличие от классического датчика УЗИ, используют гибкий видеоэндоскоп с ультразвуковым элементом. Вводится аппарат в кишечник и подводится непосредственно к образованию. Метод позволяет выявить раннюю стадию опухоли. На мониторе видно рак со всеми его особенностями. Состояние сосудов оценивают с помощью допплеровского датчика. При злокачественном новообразовании кровоток приобретёт патологический характер. Сосуды становятся хрупкими, отмечается также контактная кровоточивость.
УЗИ-заключение не является диагнозом. Для подтверждения проводят компьютерную томографию и берут образец ткани. Только гистологическое исследование подтверждает онкологическое заболевание.
Как правило, во время УЗИ брюшной полости оценивают состояние печени и желчного пузыря, почек, селезенки. Ультразвуковая диагностика позволяет выявить нефролитиаз (камни в почках), который тоже дает болевой синдром. Холестаз (застой желчи), связанный с закупоркой желчных путей, вызывает желтушность кожных покровов. Также расширение желчных протоков служит причиной нарушения функции поджелудочной железы.
Диффузное увеличение органа говорит об остром воспалительном процессе. Наличие кист свидетельствует о хронической патологии поджелудочной. Часто кисты ошибочно принимают за раковую опухоль.
Насколько часто можно делать скрининги

Ультразвуковое исследование – абсолютно безобидная процедура. Она не требует специальной подготовки. На основании данных УЗИ и других методик предполагают диагнозы: рак поджелудочной железы, панкреатит, кисты. Заболевания поджелудочной железы быстро прогрессируют, вызывая необратимые последствия. Пациентам группы риска (отягощенный анамнез, курение, работа с вредными факторами производства) необходимо проходить исследование 1 раз в 6 месяцев.
Другие методы диагностики
Для лабораторной диагностики рака поджелудочной железы используют дополнительные методы исследования:
- В общем анализе крови выявляют увеличение количества лейкоцитов, СОЭ, тромбоцитов.
- При передавливании опухолью общего желчного протока в биохимическом анализе крови повышается концентрация печеночных ферментов (АЛТ, АСТ), билирубина, щелочной фосфатазы.
- В копрограмме (исследование кала) выявляют стеаторею (непереваренный жир).
- Специфическим методом является определение онкомаркера CA 19-9.
- Информативным является цитологическое исследование.
- Смыв дуоденального содержимого сканируют на наличие злокачественных клеток.
Из инструментальных методов применяются компьютерная томография (КТ) и магнитно-резонансное сканирование. Мультиспиральная компьютерная томография (МСКТ) и эндоУЗИ используются для выявления метастазов опухолей поджелудочной.
Лапароскопия – это метод хирургической диагностики, позволяющий обнаружить метастазы в брюшной полости. Во время процедуры проводят биопсию опухоли для дальнейшего гистологического исследования.
В последнее время злокачественные новообразования (опухоли) в панкреатодуоденальной зоне, включающей в себя поджелудочную железу, двенадцатиперстную кишку и внепеченочные желчные протоки, имеют значительный рост. Особую тревогу у медиков вызывает рак поджелудочной железы, диагностика и лечение которого, несмотря на определенные успехи в этой области, всё же характеризуются неудовлетворительными показателями.
Как правило, в связи с отсутствием специфической симптоматики ранняя диагностика поджелудочной железы практически не определяется. Большинство наблюдений – это стадия экстраорганного распространения раковых клеток в поджелудочной железе, что является причиной высокой частоты диагностических лапаротомий или паллиативных, то есть защитных действий от тягостных проявлений онкологического заболевания.
- Общие сведения
- УЗИ рака поджелудочной железы
- КТ рака поджелудочной железы
- МРТ поджелудочной железы
- Хирургические методы исследования
- Лапароскопия
- Биопсия рака поджелудочной железы
- Заключение
Общие сведения
Первые клинические симптомы онкологического заболевания проявляются достаточно поздно, когда опухолевый процесс уже имеет значительное прогрессирование. Постановка диагноза рака поджелудочной железы без ультразвукового исследования, компьютерной томографии, магнитно-резонансной томографии и ангиографии невозможна.
Анатомическая топография поджелудочной железы подразделяется на головку, тело и хвост.
Стойким симптоматическим признаком локализации злокачественного образования в поджелудочной железе является механическая желтуха, причины которой – это распространение опухоли на желчные протоки.
По медицинской статистике Всемирной организации здравоохранения, наиболее поражаемым органом, приблизительно в 50-60% случаев, является головка поджелудочной железы, реже – тело и хвост жизненно важного органа пищеварительной системы.
Тотальное поражение крупной железы злокачественным новообразованием отмечается примерно у 25% пациентов онкологических и гастроэнтерологических клиник.

УЗИ рака поджелудочной железы
Ультразвуковая диагностика рака поджелудочной железы выявляет в больней степени злокачественные новообразования превышающие размер свыше 40 мм, определяемые как участок гипоэхогенной структуры с неправильными контурами, что в целом недостаточно в выявлении опухолей небольших размеров, не превышающих 2 см.

Традиционные методы ультразвукового сканирования не позволяют с высокой точностью провести диф. диагностику рака поджелудочной железы и уверенно разделить злокачественные опухоли от доброкачественных новообразований.
В первую очередь это объясняется техническими особенностями УЗИ – низкой чувствительностью и некачественной эхографической картинкой.
В 75 % случаев диагностика рака поджелудочной железы при одном лишь ультразвуковом сканировании даёт ложноположительное заключение.
КТ рака поджелудочной железы
Более информативным диагностическим методом визуализации считается компьютерная томография – КТ при раке поджелудочной железы, которая позволяет с высокой степенью точности определить распространённость опухолевого процесса, и тем самым более достоверно устанавливать вовлеченность в онкологию лимфатических узлов, сосудов и прочих периферийных структур органа пищеварительной системы, что оказывает существенное значение при выборе хирургического лечения.
Компьютерная томография выполняется в комплексе предоперационного обследования для оценки степени распространенности злокачественной опухоли на прилежащие органы жизнедеятельности.
Точность дифференциальной диагностики рака поджелудочной железы при помощи компьютерной томографии достигает 85%.
КТ поджелудочной железы позволяет хорошо визуализировать забрюшинную жировую клетчатку, окружающую орган пищеварения, даже при расширении кишечных петель и большой отёчности. В этом и заключается основное преимущество диагностической эффективности компьютерной томографии над УЗИ.
МРТ поджелудочной железы
Магнитно-резонансная диагностика рака поджелудочной железы на ранней стадии также не эффективна, и не имеет значительных преимуществ перед компьютерной томографией. Однако она целесообразна в случае визуализации желчных и панкреатических протоков без введения контраста.

Основное предназначение МРТ-исследования рака поджелудочной железы, заключается в разграничении опухолевого поражения и псевдотуморозного процесса и для уточнения характера обструкции желчных протоков.
Существуют определенные ограничения на проведение МРТ поджелудочной железы:
- присутствие в организме инородного тела,
- клаустрофобия у пациента,
- асцит брюшной полости,
- отсутствие визуализации дистального отдела холедоха – желчного протока, отводящего желчь из желчного пузыря и общего печеночного протока.
При анализе результатов МРТ-исследования опытный специалист может определить не только распространённость злокачественного образования и связи его с магистральными сосудами, но и установить гистологическую структуру опухоли.
Хирургические методы исследования
Малоинвазивная оперативная диагностика рака поджелудочной железы, симптомы которого, выражаются механической желтухой, болью в левом подреберье, опоясывающим болевым синдромом, тошнотой и рвотным рефлексом, заключается в нарушении целостности эпителия кожного покрова и слизистой оболочки воспаленной поджелудочной железы.
Подобные методы исследования позволяют с высокой точностью определить диагностическую клинику рака поджелудочной железы и установить правильное лечение.
Эндоскопическая хирургия – радикальный метод оперативного вмешательства без рассечения кожного покрова. Одной из эффективных разновидностей хирургического малоинвазивного вмешательства в брюшную полость считается лапароскопия, при помощи которой удаётся выявить все узловые злокачественные образования и/или метастазы в поджелудочной железе.
Преимуществом малоинвазивной эндоскопической технологии является отсутствие операционной травмы, значительное снижение кровопотери, уменьшение риска инфицирования брюшной полости, отсутствие послеоперационных осложнений и быстрый срок восстановительной послеоперационной реабилитации.
В случае подозрения на онкологию проводится дополнительное гистологическое исследование, входящее в комплекс диагностических мероприятий.
Для подтверждения диагноза при подозрении на наличие онкологического заболевания, проводится лабораторное исследование клеток и биоптата (тканей) исследуемого органа. Проще говоря, проводится тонкоигольная аспирационная биопсия поджелудочной железы под эндоскопическим контролем.
Пункция трепан-биопсия выполняемая через брюшную полость, с целью гистологической дооперационной верификации рака поджелудочной железы является наиболее чувствительным и безопасным методом диагностического исследования.
Чувствительность к положительному результату трепан-биопсии под эндоскопическим контролем составляет 93-95%.
Заключение
Совместное и своевременное проведение ультразвуковой и компьютерной диагностики позволит выявить раковую опухоль поджелудочной железы на ранней стадии формирования, а дальнейшее малоинвазивное хирургическое вмешательство позволит, правильно установив диагноз, принять адекватное решение по лечению рака поджелудочной железы.
Как выявить рак поджелудочной железы, расскажет следующее видео:
Читайте также:

