Трижды негативный рак при вич
ВИЧ-инфекция — один из факторов, который во много раз повышает вероятность развития рака. Выяснили, какие именно онкозаболевания чаще всего могут возникать при положительном ВИЧ-статусе, как их вовремя обнаружить, и на какие факторы риска еще нужно обратить внимание людям, живущим с ВИЧ.
Главная мишень вируса — CD4-Т-лимфоциты. Они передают сигнал другим клеткам, которые защищают организм от рака. В результате вмешательства вируса количество CD4-T-лимфоцитов постепенно уменьшается. Критически низкий уровень этих клеток - одна из причин отсутствия согласованной работы между звеньями иммунитета и главный механизм, приводящий к развитию СПИДа.
Иммунитет человека с ВИЧ-инфекцией перестает контролировать процессы избыточного клеточного деления и злокачественной трансформации клеток. Вместе с уменьшением количества CD4-T-лимфоцитов происходит накопление раковых клеток. В результате у человека развиваются несколько видов опухолей, которые называют СПИД-индикаторными: появление такого вида рака с очень большой вероятностью означает наличие у человека СПИДа.
Однако повышается риск появления не только СПИД-индикаторных опухолей, но и тех видов рака, которые развиваются из-за потери иммунного контроля над несколькими онкогенными инфекциями: вирусом герпеса человека 8 типа (ВГЧ-8), вирусом папилломы человека (ВПЧ), вирусами гепатита В и С (ВГВ, ВГС), вирусом Эпштейна-Барр (ВЭБ) и другими.
Все эти состояния развиваются у людей с ВИЧ-инфекцией преимущественно на фоне снижения количества CD4-T-лимфоцитов до уровня менее 200 клеток/мкл (при разбросе в норме от 500 до 1100 клеток), но также могут возникать при нормальном или близком к нормальному уровню CD4-T-лимфоцитов.
Саркома Капоши (СК) — СПИД-индикаторная опухоль, при которой происходит злокачественная трансформация клеток лимфатических и кровеносных сосудов. Риск развития СК у пациентов с ВИЧ-инфекцией увеличивается в несколько сотен раз. Различные белки ВИЧ-1 способны усиливать воспаление и нарушать регуляцию в эндотелиальных клетках. Это приводит к тому, что саркома Капоши может развиться до того, как уровень CD4-T-лимфоцитов упадет ниже 200 клеток/мкл. Еще одно обязательное условие для возникновения СК — наличие в организме вируса герпеса человека 8 типа.
Саркома Капоши развивается в виде папулы, пятна, узелка, бляшки коричневого, розового, красного или темно-красного цвета от нескольких миллиметров до нескольких сантиметров в диаметре. Обычно высыпания концентрируются на ногах, голове, шее, на слизистой оболочке — в области неба, десен, конъюнктивы.
До эры внедрения лекарств от ВИЧ — антиретровирусной терапии (АРТ) 5-летняя выживаемость (с момента диагностики опухоли) пациентов с саркомой Капоши составляла менее 10%. Применение АРТ значительно улучшило ситуацию — сейчас речь идет о 74%, — а также позволило снизить риск развития СК.
Более половины случаев СК (56%) диагностируются сейчас в локальной форме — до того, как опухоль распространится на лимфатические узлы, слизистую ЖКТ, печень, селезенку и другие органы. Прием антиретровирусной терапии помогает значительно замедлить прогрессию болезни и предотвратить распространение СК по всему организму.
К сожалению, обнаружить саркому Капоши до появления симптомов не получится
Однако, человеку с ВИЧ и его амбулаторному врачу-инфекционисту необходимо учитывать несколько факторов риска развития этой опухоли:
- Этническая принадлежность: люди еврейского или средиземноморского происхождения, а также экваториальные африканцы;
- Мужской пол;
- Иммунодефицит: Люди с уровнем CD4-клеток менее 200 кл/мкл, те, кто перенес трансплантацию органов или костного мозга или постоянно принимает глюкокортикостероиды;
- Сексуальная ориентация: мужчины, имеющие секс с мужчинами(МСМ), подвержены более высокому риску развития СК.
К онкологическим заболеваниям, ассоциированным с вирусом папилломы человека, относятся инвазивный рак шейки матки (ИРШМ), сквамозный (чешуйчатый) рак головы/шеи, рак анального канала, вульвы и влагалища. СПИД-индикаторной из них является только ИРШМ.
Распространенность генитальной онкогенной инфекции ВПЧ среди женщин, живущих с ВИЧ, в целом выше, чем у остального населения.
Вирус папилломы человека способен к самопроизвольной элиминации — исчезновению из организма. У ВИЧ-положительных женщин этот процесс занимает больше времени, что увеличивает вероятность появления патологических изменений в шейке матки.
Продолжительный прием АРТ приводит к более низкой распространенности ВПЧ высокого риска и поражений шейки матки и даже предотвращает новые случаи ИРШМ.
Раннее начало антиретровирусной терапии, приверженность лечению обеспечивают снижение вирусной нагрузки — количества вируса в крови. Эти меры очень эффективны в отношении местного иммунитета слизистой оболочки и профилактики ИРШМ.
Скрининг ИРШМ заключается в проведении ПАП-теста и ВПЧ-теста (ПЦР). Женщины с ВИЧ-инфекцией в возрасте от 21 до 29 лет должны пройти ПАП-тест во время первичной диагностики ВИЧ, затем — через 12 месяцев, если анализ не показал патологии. Некоторые эксперты рекомендуют делать следующий ПАП-тест через 6 месяцев после первого. Если результаты трех последовательных мазков без отклонений, повторные тесты следует проводить каждые 3 года. ВПЧ-тест не рекомендуется подключать к ПАП-тесту до 30 лет — высока вероятность положительного результата, при этом оснований для активных действий нет. Лечения ВПЧ не существует, а для развития РШМ требуется, как правило, от 10 лет.
После 30 лет ПАП-тест и ВПЧ-тест проводятся совместно
У пациентов с ВИЧ-инфекцией повышается риск развития:
- гепатоцеллюлярной карциномы (ГЦК), связанной с вирусами гепатита С и В (ВГВ и ВГС) — в три раза;
- рака желудка, ассоциированного с инфекцией H.pylori;
- лимфомы Ходжкина — 8-13 раз. Риск связан с сопутствующей Эпштейн-Барр-инфекцией. Важно, что повсеместное внедрение АРТ не повлияло на показатели заболеваемости лимфомой Ходжкина в популяции людей с ВИЧ.
К факторам риска развития ГЦК у пациентов с ВИЧ относятся: цирроз печени, ожирение, диабет, возраст старше 60 лет, мужской пол.
Скрининг ГЦК проводится с помощью анализа крови на альфа-фетопротеин (АФП), который может продуцироваться раковыми клетками, или инструментальных методик диагностики — УЗИ, КТ, МРТ.
В последние годы всё чаще используется фиброскан для оценки стадии фиброза и близости к циррозу, независимому фактору риска ГЦК.
Предотвратить появление гепатоцеллюлярной карциномы можно с помощью своевременной вакцинации и ревакцинации от вирусного гепатита В и контроля вирусной нагрузки.
Несмотря на появление АРТ, НХЛ остаются актуальной проблемой для людей, длительное время живущих с ВИЧ. Хотя в большом количестве случаев неходжкинские лимфомы являются СПИД-индикаторными, они способны развиваться при нормальном уровне CD4-клеток и являются одной из наиболее частых причин смерти среди ВИЧ-положительных.
Общая выживаемость у пациентов с этим диагнозом низкая: более половины умирают в течение пяти лет от момента постановки диагноза
Отсюда возникают факторы риска развития НХЛ при ВИЧ-инфекции:
- наличие ко-инфекции вирусными гепатитами В, C, H.pylori;
- наличие вирусной нагрузки вируса Эпштейна-Барр или цитомегаловируса;
- наличие аутоиммунных заболеваний до постановки диагноза ВИЧ-инфекция;
- наличие специфических изменений в протеинограмме до или во время ВИЧ-инфекции;
- наличие минимальной вирусной нагрузки ВИЧ, несмотря на АРТ;
- снижение CD4-Т-лимфоцитов.
К скринингу неходжкинских лимфом относятся мониторинг вирусной нагрузки ВЭБ, ВГС, ВГВ и проведение инструментальной диагностики (КТ, МРТ, УЗИ, ФГДС).
С помощью контроля факторов риска и своевременного скрининга можно не только найти опухоль на ранней стадии, но и предотвратить заболевание.
Если рак все же обнаружили, ни в коем случае нельзя прерывать антиретровирусную терапию — она проводится по жизненным показаниям, что означает высокую вероятность неблагоприятного исхода противоопухолевой терапии без сопутствующего противовирусного лечения.
Агрессивный и рано метастазирующий подтип. Трижды негативный рак молочной железы относится к худшему варианту опухолевого роста: чаще возникает у молодых женщин, нет мишеней для лечения, прогноз неблагоприятный.

Трудно лечить при плохом прогнозе для выживания
Трижды негативный рак молочной железы
Все иммуногистохимические реакции отрицательны. Трижды негативный рак молочной железы (ТНРМЖ) выявляется у 20-24% пациенток. Этот подтип опухоли характеризуется:
- Отсутствием в железистой ткани груди рецепторов к женским гормонам (эстрогенам и гестагенам);
- Негатив HER2;
- Высокая пролиферативная активность.
Кроме этих стандартных показателей, для тройного негативного РМЖ характерны другие отрицательные параметры, формирующие крайне неблагоприятный вариант опухолевого роста. Лечить можно и нужно, но важно понимать – отсутствие мишеней для прицельной терапии снижает эффективность стандартных методов лечения.
Особенности опухолевого роста
Биологический подтип карциномы с неблагоприятным прогнозом. Трижды негативный рак молочной железы имеет следующие особенности:
- Чаще обнаруживается у молодых женщин в возрасте от 35 до 59 лет (в среднем 40-55 лет);
- Наличие в прошлом беременностей, родов и длительной лактации никак не влияет на снижение риска рака груди;
- Большой размер первичного злокачественного очага;
- Преобладание инвазивных протоковых гистологических типов карцином;
- У большей части пациенток обнаруживается 3 степень злокачественности (около 70%);
- Отсутствие некротических процессов внутри опухоли;
- Высокая частота выявления мутации генов BRCA (наследственные варианты опухоли);
- Повышенная агрессивность карциномы, выявляемая при определении индекса пролиферации Ki-67;
- Высокая вероятность возникновения синхронного и метахронного рака в молочных железах (сразу в обеих железах или последовательное возникновение злокачественных узлов);
- Ранее начало метастазирования;
- Реальный риск рецидива опухоли;
- Низкая выживаемость пациенток.
Кажется, что негатив во всем – от молекулярных характеристик до прогноза. И так оно и есть, но при этом у части пациенток возникает хороший ответ на химиотерапевтические и таргетные препараты.
Лечение ТНРМЖ
Порой с 3-4 стадией карциномы в груди пациентка успешно излечивается и живет долгие годы без рецидива, но бывают ситуации, когда уже при 1-2 стадии болезнь развивается столь стремительно, что в течение года все заканчивается. Трижды негативный рак молочной железы – это именно тот фактор, который во многом определяет дальнейшее неблагоприятное развитие событий.
Пока трижды негативный рак молочной железы относится к неблагоприятным подвидам злокачественной опухоли в груди, что связано с быстрым ростом опухоли, ранним формированием метастазов и отсутствием эффекта к стандартным схемам химиотерапии. Но – молекулярные и иммуногистохимические исследования ведутся, поиск комбинаций лекарств продолжается, новые препараты апробируются и внедряются в клиническую практику.
Лечение трижды негативного рака молочной железы
Трижды негативный рак молочной железы не содержит рецепторов эстрогенов и прогестерона, а также амплифицированного гена Her2. Это означает, что он имеет очень малое количество точек воздействия для его лечения. Долгое время он считался практически неизлечимым, сегодня имеются методы дающие пациенткам надежду.
По материалам беседы с профессором Мерц, заведующим отделения ультразвуковой гинекологической клинической диагностики.
Как часто врачи диагностируют трижды негативный рак молочной железы? Существуют ли определенные группы женщин, у которых этот вид рака наблюдается чаще?
Трижды негативный рак молочной железы встречается у 10-15 процентов заболевших пациенток. Чаще эта форма рака поражает молодых женщин. Тесная взаимосвязь имеется между трижды негативным раком и мутацией гена BRCA1. У пациенток с мутацией гена BRCA1 в большинстве случаев диагностируется трижды негативный рак молочной железы.
Какая терапия назначается на ранних стадиях заболевания?
В основном пациентки с трижды негативным раком молочной железы получают так называемую неоадъювантную химиотерапию, т.е. терапию, которая проводится перед операцией. Это дает возможность точного контроля реакции заболевания на лечение. Примерно у трети пациенток к началу операции опухолевые клетки в молочной железе
после химиотерапии не определяются. Это называют полной ремиссией патологического процесса. В таком случае рецидивы заболевания маловероятны.
Как Вы оцениваете применение Карбоплатина при трижды негативном раке молочной железы?
Значение Карбоплатина при трижды негативном раке молочной железы сегодня, как и вчера, подтверждено недостаточно. Но стоит отметить, что проводимые онкологические исследования доказывают, что применение химиотерапии с карбоплатином перед операцией увеличивает положительную реакцию на терапию и процент выживаемости пациенток при трижды негативном раке молочной железы. И это касается не только, как считалось ранее, пациенток с мутацией гена BRCA1. Поэтому платино-содержащую химиотерапию следует чаще назначать пациенткам с ТНРМЖ, учитывая естественно возможные побочные действия.
Имеются ли другие терапевтические возможности на ранних стадиях заболевания?
В настоящее время тестирование проходят несколько новых медикаментов для лечения трижды негативного рака молочной железы. Некоторые (как например, ингибиторы PARP( поли(АДФ-рибоза)-полимеразы) уже доступны в рамках клинических исследований.
Каково положение при метастазированной стадии заболевания?
Проводятся ли в настоящее время исследования в области трижды негативного рака молочной железы?
Да, особенно в направлении использования ингибиторов контрольных пунктов, а также ингибиторов PARP( поли(АДФ-рибоза)-полимеразы). На Конгрессе по поводу прогрессивного рака молочной железы в Лиссабоне были представлены данные о том, что шесть процентов трижды негативных опухолей обнаруживают рецепторы андрогенов. Ингибиторы андрогенов успешно применяются при лечении рака простаты. И как показывают исследования пациентки, у которых обнаруживаются рецепторы андрогенов, также могли бы получать эффект от использования этих препаратов.
Каково Ваше мнение? Являются ли ингибиторы андрогенов, учитывая их низкие побочные эффекты, одним из возможных видов лечения?
Данные по антиандрогенам действительно являются многообещающими, немаловажным является и то, что медикаменты уже допущены к применению, хотя и не использовались для лечения рака груди. С одной стороны в отношении терапии антиандрогенами имеется много открытых вопросов: мы не знаем, например, при каком количестве адрогеновых рецепторов в клетке, следует назначать терапию. С другой стороны есть пациентки с прогрессивной и устойчивой к химиотерапии стадией заболевания, при лечении которых следует принимать во внимание наличие подобной терапии.
Тем не менее, в последние десятилетия адекватная противовирусная терапия позволила не только улучшить результаты противоракового воздействия, но и в разы уменьшить вероятность развития злокачественного процесса у ответственного пациента.
Когда при ВИЧ появляются злокачественные опухоли
Рак и другие злокачественные опухоли развиваются при переходе ВИЧ-инфекции в позднюю стадию болезни, когда концентрация иммунных клеток устремляется к минимальной, позволяя активно и почти беспрепятственно размножаться разнообразной микрофлоре — от простейший и грибов до бактерий и вирусов.
Всё, что происходило в организме инфицированного пациента ранее, было обычной ВИЧ-инфекцией, появление рака или других опухолей, а также тяжёлых распространённых инфекций — это уже СПИД.
Благодаря лечению период от заражения вирусом иммунодефицита до последней стадии болезни растянулся почти на три десятилетия, тогда как в конце 1980-х годов занимал несколько лет.
Какие раки развиваются при ВИЧ-инфекции
В конце ХХ века выявление определённых, практически не встречающихся при нормальном иммунитете заболеваний и злокачественных процессов, позволяло ставить диагноз ВИЧ/СПИД без сложных лабораторных исследований. Такие процессы обозначили как ассоциированные с вирусом иммунодефицита или, по-современному, СПИД-индикаторные. В этот список наряду с необычными инфекциями включены инвазивный рак шейки матки, саркома Капоши и злокачественные лимфомы, вероятность которых у инфицированного пациента возрастает в сотни раз.
Значительно чаще, но не в сотни раз, при ВИЧ-инфекции вероятно развитие плоскоклеточного рака анального канала и рака вульвы, карциномы лёгкого и злокачественных опухолей яичка, плоскоклеточного рака головы и шеи, меланомы и рака кожи.
Для большинства злокачественных процессов доказана основополагающая патогенетическая роль вирусов, в первую очередь, папилломы человека (ВПЧ) и гепатита В, С и D. Способствует раннему развитию злокачественных новообразований носительство вирусов герпеса, особенно 4 типа — вируса Эпштейна-Барр. Традиционно значимы у ВИЧ-инфицированных факторы риска злокачественного перерождения клеток бронхолегочной системы — курение и наследственная предрасположенность.
Как ВИЧ-инфекция влияет на течение рака
Однозначно — очень неблагоприятно, усугубляя скорость прогрессирования и увеличивая массив опухолевого поражения. И хотя рак у ВИЧ-инфицированного пациента возникает много раньше, чем в общей популяции, практически в молодом возрасте, пациенты не могут похвастать исходным хорошим здоровьем.

Как ВИЧ сказывается на переносимости химиотерапии
В большинстве случаев злокачественный процесс на фоне ВИЧ-инфекции течёт агрессивнее, поэтому на первом этапе требует системного лечения с использованием противоопухолевых препаратов, гарантирующих разнообразный спектр токсических реакций. При этом ни в коем случае нельзя отказываться от специфической противовирусной терапии, также изобилующей неблагоприятными проявлениями.
В итоге переносимость противоракового лечения, проводимого на фоне ВААРТ, ухудшается, а продолжительность жизни пациентов не в пример короче, чем это могло быть в отсутствии ВИЧ. При активной противоопухолевой и противовирусной терапии больше года после выявления опухоли живёт только каждый четвёртый, пятилетку — всего 19%.
Существует ещё одна серьёзная проблема — клинического изучения эффективности противоопухолевой терапии у ВИЧ-инфицированных не проводится из-за малочисленности групп пациентов и, следовательно, сомнительной достоверности результатов. Поэтому очень важно в этот тяжёлый период найти клинику и специалистов одинаково высоко компетентных в вопросах лечения ВИЧ и противораковой химиотерапии.
Как лечат рак у ВИЧ-инфицированных
В большинстве случаев терапия рака не должна отличаться от таковой у пациентов с нормальными показателями иммунитета.
При технической возможности хирургической операции ВИЧ-пациенту от неё нельзя отказываться, поскольку излечение возможно только при удалении всех очагов рака. Если для злокачественной опухоли лимфатической системы признана необходимость высокодозной химиотерапии с трансплантацией стволовых клеток, то и инфицированный вирусом пациент должен получить программное лечение. При раке шейки матки практически невозможно обойтись без лучевой терапии.
ВИЧ-компрометированному пациенту потребуется ВААРТ и гораздо более серьёзное сопроводительное лечение. Чтобы провести химиотерапию без сокращения доз и интервалов необходима индивидуальная программа реабилитационного воздействия. Кроме того, пациент должен получать множество препаратов для лечения грибковых поражений и сдерживания вирусов герпеса, разнообразные антибактериальные средства, каждое из которых имеет собственную токсичность.

Такое комплексное воздействие способна осуществить только команда врачей разных специальностей, блестяще ориентированная как в потребностях онкологического пациента, так и в возможностях организма инфицированного.
- Recent Entries
- Archive
- Friends
- Profile
- Memories
Книга про трижды негативный РМЖ: продолжение истории
Первая линия химиотерапии: антрациклины (адриамицин/доксорубицин + цитоксан/циклофосфамид + таксаны (паклитаксел). Таксаны показывают лучшие результаты при еженедельном введении. При задетых л/у добавляют препараты платины (карбоплатин или цисплатин). По результатам некоторых исследований, цисплатин более эффективен при ТНРМЖ с мутацией BRCA1.
Автор ссылается на 21 исследование (36 тыс. женщин) с ранними стадиями РМЖ. Результаты были опубликованы в 2009 году. Оценивалось воздействие таксанов. Выводы: таксаны однозначно улучшают результаты химиотерапии. Проценты улучшений разные: женщины до 50 лет добавление таксанов снижает риск рецидива на 37%; от 50 до 69 – на 20%.
Если после первой лечении возникает рецидив, то к делу должны подключаться другие химиопрепараты: варианты платины, антиметаболиты (Кселода) и ингибиторы микротрубочек (Икземпра – Ixempra). Икземпра и Кселода по отдельности показывали хорошие результаты при ТНРМЖ. А комбинация Икземпра + Кселода вообще удваивала выживаемость без прогрессирования при ТНРМЖ.
Авастин (Бевацизумаб). Это лекарство нового поколения, которое блокирует рост кровеносных сосудов в опухоли и она погибает. Авастин применяют вместе с химией при метастатическом РМЖ. По результатам исследований, он более эффективен именно при триппле, чем при гормональном РМЖ. Но вообще мнения о нем в отношении РМЖ разделяются: в США считают, что не так он и хорош, а в Европе назначают вместе с таксолом. В 2009 году опубликовали результаты исследования: авастин + таксол удваивали выживаемость без прогрессирования в сравнении с таксолом моно, и в большей степени выигрывали женщины с ТНРМЖ.
Нексавар (Сорафениб). Принцип действия – подавляет рецепторы Her1 на поверхности опухолевых клеток, не дает им размножаться. Используется при лечении других форм рака, но идут испытания в отношении ТНРМЖ (по идее, должен при нем работать). Было исследование, в котором пациенткам с ТНРМЖ давали Сорафениб + цисплатин, а затем паклитаксел – ответ был хороший.
Тарцева (Эрлотиниб), Эрбитукс (Цетуксимаб), Вектибикс (Панитумумаб). Эти лекарства одобрены для лечения других видов рака, но участвуют в испытаниях по РМЖ. По ним надеются получить хорошие результаты конкретно для ТНРМЖ.
А ЧТО ВПЕРЕДИ?
Инипариб
По результатам одного исследования, препарат достоверно увеличил общую выживаемость у женщин с метастатическим ТНРМЖ в сочетании с гемцитабином и платиной. В другой фазе исследования такого сильного положительного эффекта не отметили, исследования продолжаются.
Эрибулин (Халавен).
Ингибитор микротрубочек, активно испытывается. Особенно хорошо работал там, где ранее не справились таксаны, и в случаях с ТНРМЖ.
Вакцина
Компания Vaxon Biotech испытывает препарат Vx-001 – вакцину, которая, возможно, будет эффективной против ТНРМЖ с возможностью внедрения в практику к 2020 году.
Препараты на основе инсулина
Во многих случаях в клетках ТНРМЖ встречается повышенная экспрессия инсулиноподобного рецептора IGF-1R. Некоторые исследователи видят в этом путь к новому лекарству от ТНРМЖ.

ВИЧ-инфекция негативно влияет на риски возникновения онкологических заболеваний у человека, данные риски значительно увеличиваются при возникновении выраженного иммунодефицита – СПИД. Впрочем, и при достаточно высоком уровне функционирования иммунной системы при ВИЧ-инфекции риски все же выше – это очень важно знать, однако, не менее и даже более важно понимать, что практически всеми данными рисками можно и нужно управлять, снижая риски онкологии.
Онкологические заболевания при ВИЧ-инфекции исторически разделяют на СПИД-ассоциированные (САР) и не-СПИД-ассоциированные (не-САР) формы рака. Данное разделение именно историческое, так как многие формы рака нашли свое подтверждение связи с ВИЧ-инфекцией, однако, продолжают рассматриваться как не-САР. Онкозаболевания, риски которых возрастают именно у ВИЧ-инфицированных, обычно связаны с потенциально онкогенными вирусами: Вирус Эпштейна–Барр (ВЭБ), герпесвирус человека 8 типа (ГССК/KSHV), вирус папилломы человека (ВПЧ), вирусные гепатиты B и С… Кроме того, среди людей с ВИЧ-инфекцией более распространено курение, а также больше людей, злоупотребляющих алкоголем, что также является мощными факторами риска.
| Событие | Люди с ВИЧ | Не инфицированные ВИЧ |
| Саркома Капоши | 130,4 | 0,2 |
| Неходжкинская лимфома | 153,5 | 12,6 |
| Рак легких | 129,3 | 45,4 |
| Анальный рак | 60,1 | 1,2 |
| Колоректальный рак | 36,4 | 27,7 |
| Рак печени | 46,3 | 10,9 |
| Ходжкинская лимфома | 33,5 | 1,9 |
| Меланома | 16,4 | 14,5 |
| Рак ротовой полости/глотки | 34,3 | 18,4 |
Показатели заболеваемости и смертности от некоторых онкозаболеваний в зависимости от ВИЧ-статуса. Данные NA-ACCORD, 1996 –2009. Частота случаев на 100 000 лет наблюдений.
С наступлением эпохи антиретровирусной терапии стремительно снижается распространенность тех форм рака, которые часто наблюдается именно при возникновении СПИД. АРВ-терапия сохраняет иммунную систему, позволяя организму бороться с рисками онкологии. Оборотной стороной медали стало то, что продолжительность жизни людей с ВИЧ практически сравнялась с продолжительностью жизни без ВИЧ-инфекции, и стало очевидно, что старение с ВИЧ также сопряжено с ростом рисков возникновения онкозаболеваний. Важно понимать, что основные факторы риска рака при ВИЧ-инфекции являются управляемыми, их можно и нужно серьезно снизить или практически устранить.
Раннее начало терапии позволяет очень значительно снизить риски развития многих форм рака и увеличить общую выживаемость. В особенности это относится к рискам тех видов рака, которые обусловлены воздействием онкогенных вирусов, например, саркома Капоши и неходжкинская лимфома.
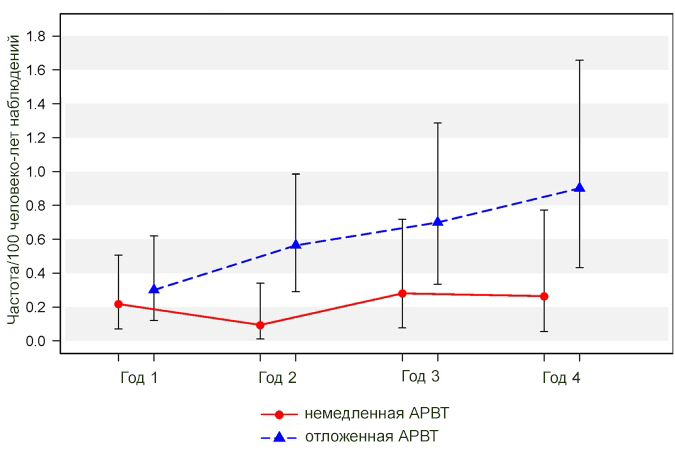
Темпы прироста заболеваемости всеми типами рака по частоте (на 100 человеко-лет наблюдений) и в зависимости от начала АРВ-терапии. Данные исследования START.
Отказ от курения очень значительно снижает не только риски рака легких, глотки или ротовой полости, но почти в два раза снижает все риски смерти, не связанные со СПИД при ВИЧ-инфекции.
Устранить вирусный гепатит С и подавить гепатит B. Риски онкозаболеваний печени при ко-инфекции практически в два раза выше. Современные безинтерфероновые режимы позволяют почти во всех случаях устранить гепатит С за непродолжительное время и с очень хорошей переносимостью лечения. Правильный подбор АРВ-терапии позволяет и подавить вирус гепатита В.
Профилактика ВПЧ и регулярный скрининг изменений эпителия шейки матки и прямой кишки, который включает тест Папаниколау и тест ДНК ВПЧ, позволяет своевременно принять меры, которые способны практически полностью устранить риски рака шейки матки, а также анального рака. Центр по контролю и профилактике заболеваний (CDC, США) рекомендует вакцинацию против вируса папилломы человека (ВПЧ) для женщин и мужчин с ВИЧ-инфекцией в возрасте до 26 лет, а в октябре 2018 года регулятор в США одобрил вакцину Gardasil-9 для людей в возрасте до 45 лет.
Герпесвирус 8 типа (ГССК/KSHV) выделяется со слюной, не следует использовать слюну в качестве лубриканта при сексуальных контактах. Использование лубрикантов, вместо слюны, позволяет снизить вероятность заражения ГССК и тем самым уменьшить риски саркомы Капоши.
Антиретровирусная терапия, устранение или минимизация управляемых факторов риска, в сочетании с формированием и выполнением рационального индивидуального плана обследований – позволяют сегодня достичь радикального снижения рисков возникновения онкологических заболеваний у людей с ВИЧ-инфекцией, а если таковые риски и реализуются, то своевременная диагностика дает крайне высокие шансы на излечение.
Трижды негативный рак молочной железы – заболевание, которое в онкологии считается одним из самых злокачественных и агрессивных. В медицинской практике, к счастью, эта патология встречается довольно редко. Полноценная диагностика болезни стала возможна недавно, когда начали применять иммунологические методики. В чем особенности болезни и почему она так опасна?
Трижды негативный рак молочной железы – патология, которая диагностируется в 10-15% всех эпизодов онкозаболеваний грудных желез. Почему болезнь получила такое название? Объясняется это тем, что патологические клетки или не выделяют вовсе или выделяют в наименьшем количестве в окружающие ткани три важных белка, к которым относят:
- Рецепторы эстрогена;
- Прогестероновые рецепторы;
- Рецепторы фактора роста эпидермального типа.
Основной особенностью заболевания является то, что для него очень сложно подобрать лечение, избавляющее от опухоли. Сегодня в терапии рака молочной железы активно используются гормональные средства, а если клетки опухоли не имеют рецепторов гормонов, то и воздействие на них становится невозможным. Еще одна особенность заболевания, которую нельзя упускать из виду, – скорость развития. Трижды негативный рак молочной железы прогрессирует с огромной скоростью. Из-за этого в промежутках между скрининговыми исследованиями опухоль может развиваться до невероятных размеров. В результате скрининг, как метод профилактики, становится малоэффективным.
Несмотря на сложность лечения данного заболевания, специалисты Юсуповской больницы могут помочь и таким пациенткам. Для этого в больнице при составлении протоколов химиотерапии используются достижения персонализированной медицины. Кроме того, здесь разрабатываются и внедряются новые методы лечения тройного негативного рака груди.

Причины развития заболевания
Онкологическое поражение груди – следствие широкого спектра процессов, происходящих в организме женщины. Тройной негативный рак молочной железы чаще всего формируется из-за:
- Сильных гормональных изменений, происходящих в теле в период климакса, беременности;
- Нарушений менструального цикла, возникающих в течение жизни;
- Избыточного продуцирования половых гормонов, которые способствуют росту опухолей, зависимых от гормонов;
- Абортов, которые также выступают в качестве гормонального потрясения для организма.
Помимо гормональных изменений выделяют ряд процессов, которые способствуют развитию болезни:
- Если женщина никогда не беременела и не рожала;
- Поздние роды (женщина старше 35 лет);
- Предрасположенность по наследству;
- Генные мутации (BRCA). Гены BRCA1 и BRCA2 предотвращают возникновение раковых клеток. Если у женщины они мутируют, то есть высокая вероятность заболеть раком, в том числе и раком груди;
- Использование контрацептивов перорального типа в течение длительного времени;
- Использование препаратов с гормонами.
- Беременность больше трех раз в 2 раза повышает развитие данного вида рака;
- Беременность у женщин моложе 26 лет;
- Рождение трех детей без грудного вскармливания
Мировыми учеными уточняются и разрабатываются новые классификации трижды негативного рака молочной железы. В настоящее время врачами-онкологами используется классификация по гистологическому строению:
- медуллярный трижды негативный рак молочной железы представлен в виде широких полос. Данный тип рака на начальных этапах протекает бессимптомно;
- метапластический рак имеет неблагоприятный прогноз, так как диагностируется в большинстве случаев на поздних стадиях;
- аденокистозный рак является редкой разновидностью;
- низкодифференцированный рак поражает эпителиальную ткань протоков и прорастает в окружающие ткани.
Данные типы трижды негативного рака молочной железы выделяются специалистами условно, они используются для составления схемы терапии. Применение современных технологий лечения трижды негативного рака груди позволяет не только улучшить качество жизни, но и повысить шансы пациента на благоприятный исход.
Симптоматика и первые признаки
Симптомы заболевания, несмотря на его агрессивность, не отличаются от других новообразований груди. Из-за этого трижды негативный рак молочной железы легко спутать, например, с карциномой, если не изучить его гистологическое строение. Важно то, что первые признаки болезни стерты, это значительно затрудняет своевременную диагностику. Первоначально жалобы будут типичны:
- Появление специфического уплотнения, которое вначале небольшого размера и безболезненное. При прогрессировании заболевания, уплотнение увеличивается и начинает болеть;
- Деформации самой железы и соска;
- Появление патологических выделений.
Иногда возможно местное развитие воспаления, из-за чего болезнь первоначально можно принять за абсцесс.
Методы диагностики
При трижды негативном раке молочной железы важна своевременная диагностика болезни, чтобы подобрать необходимое лечение и улучшить прогноз для пациентки.
- Маммографию в качестве скринингового метода и метода постановки диагноза, в сомнительных случаях дополняется УЗИ-исследованием;
- Биопсию подозрительного новообразования, благодаря чему удается установить, какова природа опухоли, насколько она злокачественная;
- Дуктографию, которая исключает наличие папиллом внутрипротокового типа;
- Анализы крови на маркеры CA15-3, Cyfra 21-1, CEA.
При выявлении рака груди для подтверждения диагноза трижды негативного рака молочной железы используют лабораторное исследование, которое показывает, есть ли у новообразования ответ на применение прогестерона, эстрогена и эпидермального фактора роста (Her2). Если опухоль негативна к этим рецепторам, то трижды негативный рак молочной железы подтверждается.
Методы лечения
Лечение заболевания представляет значительные сложности в связи с невозможностью использовать гормональную терапию, которая является основополагающей в избавлении от рака молочной железы.
1. Основа терапии – хирургическое лечение. Вмешательство может проводиться двумя основными способами.
- В первом случае молочная железа, пораженная опухолью, удаляется полностью (мастэктомия) или частично;
- Во втором случае проводят только удаление опухоли в пределах здоровых тканей (лампэктомия). Это щадящая операция, которая сохраняет орган и проводится при небольших образованиях на 1 и 2 стадиях. После операции проводится лучевая терапия.
Выбор метода хирургического лечения остается за врачом.
Химиотерапия позволяет не только местно воздействовать на новообразование, но и на метастазы, благодаря чему ее широко применяют при трижды негативной патологии. Без химиотерапии лечение трижды негативного рака молочной железы не обходится, ее назначают даже после хирургического вмешательства.
Существуют разные схемы лечения данного типа онкологии – например, часто применяемые, схема АС (цитостатические лекарства плюс таксаны), схема FAC — добавляется ещё один препарат (противоопухолевый) 5-фторурацил.
В Юсуповской больнице схема подбирается врачом индивидуально, в зависимости от диагностических мероприятий, стадии и вовлеченности злокачественного процесса.
Длительность химиотерапии зависит от применяемых препаратов, их переносимости женщиной, проводится курсами с учетом показателей крови.
Меры профилактики
Специфической профилактики, которая помогла бы предотвратить болезнь, нет. Разработать комплекс профилактических мер нельзя, так как патогенез болезни изучен не до конца.
В основе всех профилактических мероприятий лежит своевременная диагностика, которая базируется на регулярном самостоятельном обследовании, а также на прохождении скрининговых исследований.
Уменьшить вероятность развития заболевания можно, если помнить о базовых правилах здорового образа жизни, не злоупотреблять контрацептивами гормонального типа. Рекомендуется также правильно выбирать нижнее белье, чтобы травматизация груди сводилась к минимуму.
Прогноз
Для трижды негативного рака груди характерно быстрое развитие и ранее начало метастазирования. Женщины, которые смогли победить трижды негативный рак молочной железы, отмечают, что обратились в медицинское учреждение на начальной стадии. Женщинам, имеющим наследственную предрасположенность к развитию данной онкологии, следует регулярно проводить самообследования и обращаться к врачам-маммологам для диагностики. Шансы на выздоровление зависят от того:
- Удалось ли выявить опухоль на ранней стадии;
- Сдать анализы на предмет наличия рецепторов ЭР, ПР, HER2;
- Насколько быстро женщине удалили опухоль хирургическим путем;
- Возраста пациентки и жизненных ресурсов ее организма;
- Насколько эффективны препараты, которые были назначены врачом во время формирования курса лечения.
Для того чтобы прогноз на полное излечение был как можно более благоприятным, лечение трижды негативного рака молочной железы должно проходить так же быстро и агрессивно, каким является и само заболевание.
Такой подтип рака груди чаще всего встречается у женщин, которые перешагнули тридцатилетний рубеж. Прогноз внушает некоторый оптимизм: в 1/3 случаев пациентки сумели победить болезнь. Речь идет о тех женщинах, у которых новообразование выявили на ранней стадии.
Выживаемость
Трижды негативный рак молочной железы, прогноз при котором благоприятен при ранней диагностике, наиболее часто метастазирует в мозг и легкие. Невысокая выживаемость больных при данном заболевании объясняется высокой вероятностью развития рецидивов и стремительным распространением раковых клеток по организму.
Статистические данные указывают, что трехлетняя выживаемость пациенток с данным диагнозом достигает 68%. Шансы на выживаемость увеличиваются при проведении оперативного удаления молочной железы. Кроме этого, если во время лечения опухоль уменьшается в размерах, ее проявления становятся менее агрессивными, то вероятность благоприятного исхода высока.
Онкологи Юсуповской больницы имеют огромный опыт в лечении рака молочной железы, они ежедневно спасают жизни большому количеству пациентов. Звоните по телефону и записывайтесь на прием. Врач-координатор ответит на все интересующие вас вопросы.
Читайте также:

