Траумель при кистах в головном мозге
Киста головного мозга представляет собой полую структуру не онкологической природы, дислоцированную во внутренних тканях ЦНС или в её оболочках и заполненную цереброспинальной или иной жидкой средой. Это образование диагностируются как у взрослых так и у детей, имеет изменяющиеся симптомы и разные схемы лечения.

Что это за образование и чем опасно
Подобная киста в голове имеет код по МКБ 10 G93 (другие поражения головного мозга).
Иногда новообразования выглядят как опухоли, поэтому требуется тщательная дифференциальная диагностика. Для уточнения назначается специальное региональное МРТ.
Более чем в половине всех случаев киста ЦНС обнаруживается случайно при общем МРТ головного мозга.
Размеры кист сильно изменчивы:
Такая патология представляет опасность, но потенциальную.
Все зависит от двух факторов:
- диаметр;
- дислокация, расположение.
Примерно в 70% из всех случаев новообразование имеет бессимптомное или субклиническое течение (отсюда и высокий процент случайных обнаружений при медосмотре).
Механизм развития патологической манифестации базируется также на двух моментах:
- киста сдавливает окружающие ткани ЦНС — пережимаются сосуды, нарушается кровоснабжение, изменяются нейронные связи;
- новообразование само по себе занимает определенный объём, на месте которого в норме должна быть нервная ткань.
Обычно симптоматика не сильно выражена и не представляет опасности для жизни.
Но иногда, при крупной кисте, может произойти:
- отек головного мозга;
- внутримозговое кровоизлияние;
- деструкция жизненно важных зон в результате недостаточности кровоснабжения (ишемия).
Кто в группе риска
Киста головного мозга у ребенка в настоящее время диагностируется примерно у 30% новорожденных. Малышам с каждым пятилетием последние лет 30 подобный диагноз ставят всё чаще.
Специалисты связывают это:
- с ухудшением условий экологии;
- с распространением вирусных инфекций;
- рост потребления населением продуктов фармацевтической промышленности.
У взрослого человека данное новообразование обнаруживается реже, чем у младенца (примерно 10%).
Киста у плода во время беременности, в рамках наступления подобного случая, происходит в результате:
- тератогенного воздействия, например, антибиотиков (тетрациклины, сульфаниламиды);
- при внутриутробном заражении (например, вирусом Эпштейна-Барр, цитомегаловирусом).
То есть в группе риска находятся женщины с хроническими инфекциями, включая ЗППП.
Классификация
По основной классификации все кисты делятся на:
- врожденные;
- приобретенные.
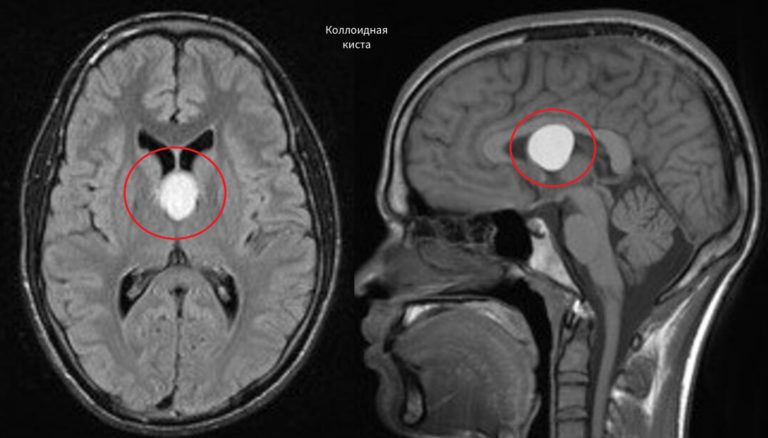
Врождённые кистозные структуры в головном мозгу формируются в антенатальный период (от момента образования зиготы до завершения беременности).
Врождённая церебральная киста симптоматически проявляет себя чаще в возрасте 30-55 лет, реже в юношеско-подростковом возрасте и практически никогда в детском возрасте.
Существующие врожденные варианты:
По локализации такие новообразования делятся на две большие группы:
- арахноидальная киста;
- внутримозговая киста.
Первая располагается в оболочках мозга, вторая — во внутренних тканях мозга.
- Арахноидальная форма дислоцируется в мозговых оболочках (паутинных оболочках).
— Формируется за счет накопления цереброспинальной жидкости в очагах воспаления оболочек.
— Часто её обнаруживают в височной области.
— Арахноидальное образование бывает приобретённое и врождённое. - Внутримозговая (ретроцелебеллярная) форма образуется на месте некроза участка внутренней структуры мозга.
— В качестве примера подходит перивентрикулярная киста ЦНС.
— Бывает и арахноидальная ретроцелебеллярная киста, когда образование регистрируется в межоболочковом пространстве.
Основная классификация приобретенных кист включает 6 разновидностей:
- посттравматическая;
- эхинококковая (паразитарная);
- постинсультная;
- постишемическая;
- постинфекционная;
- возрастная.
Иногда выделяют постгеморрагическое кистозное поражение, но это не слишком корректно, поскольку кровоизлияние в мозг может быть и при инсульте, и при механической травме.
- Посттравматическая форма.
— Возникает вследствие механического повреждения, черепно-мозговой травмы.
— Появляется в результате образования регионального отека мозговой ткани. - Эхинококковая кистозная форма.
— Возникает в результате заражения человека одним из видов ленточных червей эхинококком.
— Попав в ЖКТ, личинки эхинококка проходят через стенки кишечника и через систему воротной вены попадают в кровоток, а оттуда разносятся по организму.
— Чаще всего они формируют кистозные очаги в печени, но могут попадать и в мозг.
— В головном мозгу личинка поражает эпифиз (шишковидная железа).
— Также киста пинеальной железы может возникать при закупорке канала, выводящего вырабатываемый эпифизом мелатонин. - Постишемическая и постинсультная кисты часто взаимосвязаны.
— Они возникают на фоне регионального нарушения кровообращения.
— Недостаточность кровоснабжения приводит к хроническому кислородному голоданию.
— Нейроны начинают отмирать, возникают очаги микронекроза.
— Если ишемическое поражение оказалось обширным, то отмечаются кистозно глиозные изменения головного мозга.
— Когда формируется не одно образование, а несколько структур, напоминающих виноградную гроздь.
— Ишемической природы является субэпендимальная форма, когда зона желудочков испытывает недостаток в кровоснабжении. - Постинфекционная кистозная форма.
— Может развиться в результате инфекционного отека тканей головного мозга, а также из-за повреждения нейронных структур инфекцией.
— Таким возбудителем могут стать менингококки, вирус клещевого энцефалита, клещевой боррелиоз (болезнь Лайма). - Среди патологий, возникающих вследствие возрастных патологий, например, атеросклероза, наиболее известна лакунарная киста.
— Дислоцируемая в зоне варолиева моста или подкорковых узлов (очень редко – мозжечок).
- Посттравматическая форма.
Локализации новообразований головного мозга сильно различаются:
По содержимому эти патологические структуры делятся на:
- Ликворные кисты.
— Содержит внутри цереброспинальную жидкость, которая постоянно обращается в желудочках головного мозга, выполняя функции поддержки внутричерепного давления, электролитного тканевого баланса, трофики и метаболизма. - Слизисто-гнойные.
— Типичным примером будет киста клиновидной пазухи носа (основной пазухи головного мозга). - Коллоидальная форма.
— Содержит белковую желеобразную массу, наполненную нейроэпителиальными и эндодермальными клетками.
— Возникает внутриутробно, предположительно, по причине генетических аномалий, определяется в третьем желудочке. - Эхинококковая киста.
— Наполнена, в основном, продуктами жизнедеятельности паразита. - Тератома.
— Наполнена кусочками эпителиальной и прочих тканей, и даже зачатками органов, так как является рудиментом паразитического близнеца.
Основные причины
Врожденная киста головного мозга начинает формироваться не ранее 4-ой недели. Другой пик уязвимости наступает в середине второго триместра.
- тератогенное воздействие фармацевтических препаратов — это антибиотики, некоторые антидепрессанты (соли лития, Диазепам), противоэпилептические (Фенобарбитал, Этосуксимид), гипотензивные (Хлоротиазид);
- заражение плода инфекцией от матери через гематоплацентарный барьер (хронические вирусные инфекции, типа различных видов вируса герпеса);
- неблагоприятные экологические факторы (химическое и радиационное загрязнение региона проживания);
- вредные факторы в образе жизни матери (курение, злоупотребление алкоголем);
- внутриутробная или родовая асфиксия ребёнка;
- нарушение кровообращения через гематоплацентарный барьер и как следствие – ишемия тканей плода;
- генетические дефекты;
- определённое значение имеет и психосоматика матери – регулярные стрессы не идут на пользу и будущему младенцу.
Приобретённые (вторичные) кисты возникают в результате иных факторов воздействия:
При этом признаки кистозного образования в мозге могут быть совершенно одинаковыми как для врождённой, так и для приобретённой кисты.
Симптомы заболевания

Симптомы кисты головного мозга проявляются далеко не всегда. Выраженность симптоматики зависит от двух пунктов: размер и место.
- головные боли, не купирующиеся обезболивающими средствами;
- онемения конечностей, судороги и парезы;
- спонтанные головокружения и дезориентация в пространстве;
- приступы тошноты и рвоты, которая не улучшают состояние;
- нарушения сна;
- психоэмоциональные нарушения (неврозы, тревожные состояния, эмоциональная нестабильность);
- ощущение давления и пульсации внутри головы;
- ухудшение памяти.
Ни один из перечисленных симптомом не является однозначным указателем на наличие образования. Необходимо стойкое присутствие хотя бы 3-4 симптомов, чтобы дать предварительный диагноз.
Особенности диагностики
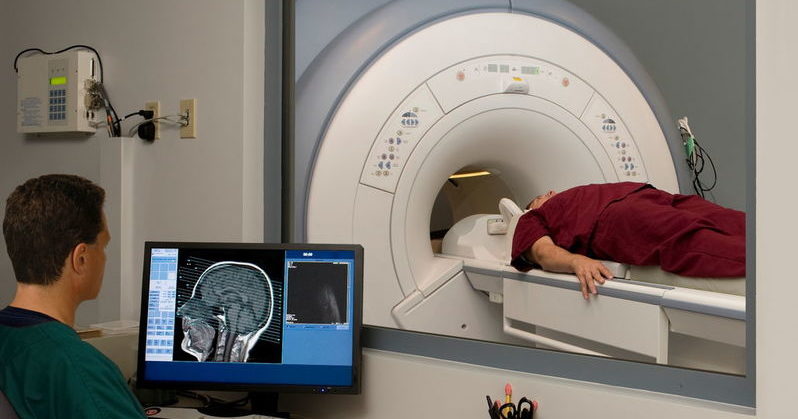
Стандартные методы (анализ крови и пр.) и даже функционально-диагностические методы (аудиометрия, визиометрия, периметрия, офтальмоскопия) здесь не являются достоверными.
- УЗИ может показать изменённую эхогенность, но этого недостаточно.
- Также к УЗИ прибегают для выявления некоторых видов кист в пренатальный период.
- Энцефалография способна зарегистрировать повышенное давление.
Но только МРТ головного мозга и КТ являются окончательно достоверными нейровизуализирующими диагностическими методами.
На МРТ кистозное образование можно визуально локализовать с высокой точностью, а также определить тип кисты. Однако исследование в рамках дифференциальной диагностики лучше проводить с контрастированием. Т.к. только опухоли склонны к накоплению контрастного вещества.
Дополнительно могут провести доплерографию для оценки состояния сосудов ЦНС. Новорожденным младенцам кисту выявляют с помощью нейросонографии.
Способы лечения
Лечение кисты в голове далеко не всегда необходимо. При диагностировании подобной структуры в мозгу выбирается выжидающая тактика с регулярным наблюдением, включая самонаблюдения пациента.
По данным статистике 70%-75% всех образований в головном мозге:
Медицинская помощь требуется только в особых случаях:
- нетипичный вариант, например, тератома головного мозга;
- новообразование уже в момент диагностирования крупное;
- активно прогрессирует в размерах;
- произошёл разрыв;
- киста угрожает работе каких-то центров головного мозга;
- пациента длительное время мучает тяжёлая симптоматика, включая развитие гидроцефалии.
Поскольку речь идёт о медицинском вмешательстве в область ЦНС, то в определённых случаях приходится пользоваться услугами зарубежной медицины. Например, лечение в Германии и Израиле.

Без операции избавиться от кистозного образования довольно сложно. Киста может самопроизвольно рассосаться, но ни один врач не скажет с уверенностью, является ли это результатом медикаментозной терапии, или новообразование исчезло бы и так.
В данном случае прибегают к препаратам:
- для нормализации АД (Каптоприл, Тенокс, Профлосин, Конкор, АД-баланс);
- для снижения сосудистых спазмов (блокатор кальциевых каналов Циннаризин);
- снижение холестерина низкой плотности (Симгал, Нолипрел, Розукард);
- против тромбов (Берлиприл, Престариум, Лизиноприл);
- БАДы для мозга (типа Гинкго Билоба), но их эффективность не доказана.
Лечение кисты головного мозга народными средствами, вообще говоря, не рекомендовано. Ведь даже фармацевтические средства будут бесполезны в большинстве случаев. Травяные компрессы на лоб, отвары травяных сборов, втирания – всё это поможет ослабить неприятную симптоматику, но на саму причину вряд ли повлияет.
Народная медицина может быть рекомендована как вспомогательная мера в послеоперационный период.
Так, внутричерепное давление хорошо снижают водные настои спаржи, полевого хвоща, чёрной бузины, фиалки.

Удаление данного новообразования – прерогатива нейрохирурга. Здесь очень много решающих факторов:
- размеры кисты;
- её дислокация;
- её этиология;
- динамика развития.
Всё это влияет на выбор методики хирургического вмешательства:
- Если новообразование создаёт критически высокий уровень внутричерепного давления, то потребуется срочное наружное вентрикулярное дренирование.
- Если произошёл разрыв патологической структуры, необходимо радикальное иссечение кисты, для чего проводится трепанация.
— Также трепанация является обязательным выбором, если киста оказалась паразитарной или тератомой с множеством жёстких включений. - Эндоскопия в данном случае это основной способ хирургического вмешательства, когда операция по удалению кисты головного мозга плановая.
— Такой вариант операции имеет самую низкую степень травматичности – аспирация происходит через небольшое фрезевое отверстие в черепе.
— Эндоскопический прокол кистозной структуры может быть противопоказан пациентам имеющим проблемы со зрением.
— Дополнительно могут установить соединения с естественными ликворными полостями мозга, что предупредить рецидив. - Для этого же производят шунтирование, которое бывает необходимо при высоком риске повторного заполнения кистозной полости.
— Здесь устанавливают отвод (дренаж) путём кистоперитонеального шунтирования, когда жидкость патологии уходит в брюшную полость по шунту. - В современной медицине прибегают к использованию гамма-ножа (лазер).
— Метод хорош тем, что не предполагает классической хирургической инвазии.
— Лазер действует угнетающе на прогрессирующие новообразования.
Необходимо повторить, что хирургическое вмешательство всегда рассматривается как вынужденная мера. Сам по себе диагноз в рамках G93 не предполагает какого-то целенаправленного лечения.
Основная уязвимость в послеоперационный период обусловлена риском инфекционного заражения. Это надо учитывать.
Восстановительная программа подразумевает следующие мероприятия:
- рефлексотерапия;
- посещение нейропсихотерапевта;
- ЛФК (лечебная физкультура);
- лечебный массаж;
- приём препаратов, снимающих отёк и способствующих рассасыванию гематом.
Время восстановительного периода индивидуальна для каждого больного.
Берут ли в армию с кистой
При таком диагнозе возможен полный медотвод, либо отсрочка от армии.
- стойкое повышение внутричерепного давления;
- неврологические нарушения;
- патологии вегетососудистой системы;
- хронические головные боли и периодические проблемы со сном.
Дадут ли инвалидность
Такой диагноз не является поводом для инвалидности. Инвалидность устанавливается только в случае стойких нарушений, когда пациент частично или полностью становится нетрудоспособен.
Противопоказания
Противопоказания при кисте головного мозга являются спорными, так как у всех данное заболевание может проявляться по-разному.
Основные врачебные предостережения таковы:
- спорт при кисте не противопоказан, но необходимо избегать чрезмерных нагрузок (только лёгкие, умеренные) и тех видов спорта, где высок риск серьёзных ЧМТ: бокс и большинство прочих единоборств (исключая, пожалуй, только ударные стили с запретом на удары в голову), альпинизм и скалолазание, экстремальные виды спорта;
- необходимо избегать перегревов (например, в летнюю жару);
- надо отказаться от курения, а потребление алкоголя свести к минимуму;
- минимизация стрессов и достаточный сон.
Соблюдение противопоказаний является частью профилактических мер.
Заключение
Совершенствование методов хирургического лечения больных с одонтогенными кистами челюстей, профилактики их воспалительных осложнений после хирургического вмешательства является одной из актуальных проблем в челюстно-лицевой хирургии. Среди операций, выполняемых хирургами-стоматологами в условиях амбулаторной клиники, операции по поводу удаления одонтогенных кист челюстей занимают второе место после обычного удаления зуба (Соловьев М. М. с соавт., 2004; Аснина С. А., 2012).
Стандартным методом оперативного лечения одонтогенных образований является цистэктомия с одномоментной резекцией верхушки корня причинного зуба. Микрофлора, локализующаяся в замкнутых полостях, часто является причиной возникновения воспалительной реакции (Ботбаев Б. Д., 1990; Ефимов Ю. В., 1993), поэтому в ходе поэтапного хирургического лечения устранение бактериальной инфекции в ране осуществляется различными антисептиками (Губайдуллина Ж. Я., 2007). Однако к данным препаратам имеются претензии, обоснованные на способности эндодонтической микрофлоры приобретать к ним резистентность (Ханенко О. Н. и соавт., 2006).
Имеются рекомендации о необходимости применения антибиотиков при хронических воспалительных инфильтратах, развившихся вследствие периапикальных абсцессов. Между тем практически отсутствуют данные, постулирующие о необходимости повального назначения антибиотиков в стоматологической практике (Камаев К. С., 2009).
В то же время широкое признание гомеопатии как одного из методов практической медицины обусловило увеличение в последние годы производства одно- и многокомпонентных гомеопатических лекарственных средств. Правильно подобранное гомеопатическое средство способно прервать обострение заболевания на любой стадии его развития, предотвратить или облегчить последующие обострения, обеспечить стойкую ремиссию. (Бадья Л. Н., Бадья Е. А., 2008). Все вышеприведенные рекомендации о назначении и применении гомеопатических средств требуют достоверной оценки их преимущества по сравнению с аллопатической терапией, которая включает назначение антибиотиков, противовоспалительных препаратов и др.
Для сокращения сроков реабилитации пациентов и возникновения рецидивов заболевания в послеоперационном периоде разработать алгоритм хирургического лечения одонтогенных кист с применением антигомотоксической терапии.
Критерий включения: пациенты обоего пола, любого возраста с кистогранулемами и радикулярными кистами челюстей. Критерий невключения: пациенты с истинными кистами, резидуальными кистами, кератокистами, одонтогенными опухолями доброкачественного и злокачественного генеза, патологическими дефектами костной ткани челюстей. Критерий исключения: пациенты с соматической патологии в период обострения заболевания, развитие пульпита, периодонтита, гингивита и пародонтита в различной стадии воспаления, нежелание пациента участвовать в исследовании.
Все пациенты с одонтогенными кистами челюстей были распределены на группы методом случайной выборки и имели одинаковую возможность получить хирургическое лечение с использованием антигомотоксической или традиционной терапии. Первая группа (основная) была представлена 32 пациентами (10 мужчин и 22 женщины) в возрасте от 23 до 65 лет (mean 45,9±2,26 года), которым проводилась цистэктомия в комплексе с антигомотоксической терапией.
Во вторую группу (группа сравнения) вошел 41 пациент (18 мужчин и 23 женщины) в возрасте от 24 до 74 лет (mean 42,9±2,47 года). Этим пациентам проводилась традиционная цистэктомия с применением стандартной антибиотикотерапии. Контрольная группа была представлена 6 мужчинами и 4 женщинами в возрасте от 40 до 50 лет, которые выступали в качестве контроля состояния тканей периапикальной области.
За несколько часов до хирургического лечения по методу Partch I и Partch I при необходимости пациентам проводилось эндодонтическое лечение корней зубов, расположенных в области кисты
Субъективную и объективную оценку состояния пациентов оценивали до и после операции и заносили в специальную таблицу. Протокол клинического обследования пациентов включал следующие критерии: сбор анамнеза, осмотр, перкуссия и пальпация зубов и тканей полости рта, выполнение цифровой ортопантомографии и/или внутриротовой контактной рентгенографии для оценки очага деструкции костной ткани и регенерации костного дефекта через 3, 6 и 12 месяцев. Оценку болевого синдрома проводили с учетом субъективных ощущений пациента до хирургического вмешательства и на 1, 3 и 7-й дни после операции по аналогово-визуальной шкале (Visual Analog Scale, VAS).
Степень выраженности коллатерального отека слизистой оболочки у пациентов оценивали визуально до операции, на 1, 3 и 7-й дни в области операционной раны. Отмечали сглаженность переходной складки, флюктуацию, а также наличие выделяемого экссудата. Операционную рану, ушитую швами, у пациентов осматривали на 1, 3 и 7-е сутки после операции. Визуально по предложенной нами оттеночной шкале отмечали наличие или отсутствие признаков воспаления переходной складки по интенсивности окраски слизистой оболочки в зоне оперативного вмешательства. Оценку состояния периапикальных тканей зуба проводили по индексу PAI (по S. Huumonen и D. Qrstavik, 2002).
За несколько часов перед хирургическим лечением при необходимости пациентам проводилось эндодонтическое лечение корней зубов, расположенных в области кисты. Операции выполнялись по методу Partch I (для больших кист, проросших в гайморову пазуху и при значительном истончении костной стенки) и Partch II (для одонтогенных образований небольших размеров).
Пациентам 1-й группы (n = 32) с кистогранулемами и радикулярными кистами челюстей проводилась медикаментозная подготовка по предложенной нами схеме:
Пациентам 2-й группы (n = 41) с кистогранулемами и радикулярными кистами челюстей операции выполнялись с использованием стандартных антибактериальных и противовоспалительных препаратов.
Для оценки заживления раневого дефекта в качестве критерия была использована десневая жидкость (ДЖ). Образцы ДЖ с помощью полосок из хроматографической бумаги в течение 5 минут отбирались из десневой борозды зубов здоровых волонтеров, не имеющих одонтогенных челюстных полостей и воспалительных изменений в пародонте, и у пациентов с одонтогенными кистами до операции, через 3 и 7 дней и 1 месяц после операции.
Все полученные в процессе обследования цифровые данные были подвергнуты статистической обработке методами вариационной статистики с использованием программы Microsoft Excel и пакета прикладных программ Statistica 6.0.
В настоящей работе наше клиническое обследование пациентов от 23 до 73 лет на дооперационном этапе выявило, что на болевые ощущения предъявляли жалобы 56,2 % пациентов с кистозными образованиями. При осмотре у 13,7 % пациентов имелись деформации в челюстно-лицевой области, а у 19,2 % пациентов выявлено наличие свищевых ходов на поверхности слизистой оболочки альвеолярного отростка. У 58,9 % пациентов кистозные образования возникли в ранее леченных зубах, а у 41,1 % пациентов явились последствиями осложненного кариеса.
Одонтогенные кисты челюстей выявлены в 72 зубах верхней челюсти и в 41 зубе нижней челюсти, и их диаметр колебался от 0,5 до 12 см. В центральных и боковых резцах верхней челюсти выявлено наибольшее число одонтогенных кист — 22 зуба. Альвеолярный сегмент только у 1 зуба охватывали 68 % одонтогенных образований, у 2 зубов — 20 %, у 3 зубов — 9 %, у 4 зубов и более — всего 3 %. У женщин в патологический очаг верхней и нижней челюстей было вовлечено в 2 раза больше зубов, чем у мужчин.
Самые большие одонтогенные кисты челюстей наблюдались у пациентов среднего (от 31 до 40 лет) и старшего возраста (от 51 до 60 лет), а небольшие кисты и кистогранулемы были характерны для пациентов от 41 до 50 лет. Размеры кистозных образований не зависели от пола, возраста, соматического статуса пациентов и локализации на челюсти.
Результаты рентгенологического исследования до операции по периапикальному индексу PAI показали, что в основной группе (I, n = 32) у 14 (43,7 %) пациентов он был равен 3 баллам, у 11 (34,4 %) пациентов — 4 баллам, а у 7 (21,9 %) — 5 баллам. В группе сравнения (n = 41) индекс PAI у 32 (78,1 %) человек был равен 3 баллам, у 6 (14,6 %) человек — 4 баллам, а у 3 (7,3 %) — 5 баллам.
Самые большие одонтогенные кисты челюстей наблюдались у пациентов среднего (от 31 до 40 лет) и старшего возраста (от 51 до 60 лет), а небольшие кисты и кистогранулемы — у пациентов от 41 до 50 лет. При этом размеры не зависели от пола, возраста, соматического статуса пациентов и локализации на челюсти
На фоне комплексного лечения после хирургического вмешательства в основной группе пациентов имело место более быстрое исчезновение болевого синдрома, гиперемии СОПР и локального отека в области операционной раны. Согласно данным об интенсивности болевого синдрома в основной группе на 3-и сутки 71,9 % пациентов ощущали слабовыраженную боль, у 18,7 % пациентов боль была выражена умеренно, у 9,4 % пациентов болезненные ощущения были выражены сильнее. Ни один из пациентов этой группы не отмечал очень сильно выраженную болевую реакцию. На 7-е сутки уже 78,1 % пациентов не ощущали болезненности в области операционной раны, 18,8 % отмечали слабовыраженную боль и оценивали ее от 2 до 4 баллов и только 3,1 % пациентов жаловались на умеренно выраженную болезненность.
У пациентов группы сравнения на 3-и сутки после оперативного вмешательства на слабовыраженную боль указали 58,6 % пациентов, умеренно выраженную боль — 9 человек, что составило 21,9 %, 6 человек (14,6 %) жаловались на сильно выраженную боль и 2 человека (4,9 %) — на очень сильную боль. То есть в этой группе пациентов, которым была назначена аллопатическая лекарственная терапия 19,5 % из числа обследованных на 3-и сутки после операции испытывали выраженную и очень сильно выраженную боль. На 7-е сутки 12,2 % пациентов группы сравнения, несмотря на прием противовоспалительных и антибактериальных препаратов, продолжали жаловаться на сильные болевые ощущения, тогда как на умеренную болевую реакцию указали 7,3 % человек. На отсутствие боли указали 36,6 % человек, что было в два раза меньше, нежели в основной группе.
Оценка продолжительности болевого синдрома показала, что в группе сравнения этот показатель составил 2,6±0,44 суток (в среднем 4,43±0,31 балла на 3-и сутки и 2,65±0,35 балла на 7-е сутки), что немного больше, чем в основной, где он равен 2,1±0,13 суток (в среднем 4,03±0,29 балла на 3-и сутки и 1,06±0,25 балла на 7-е сутки) (р>0,05).
Определенные различия между группами пациентов выявлялись не только в продолжительности развившейся гиперемии слизистой оболочки ротовой полости, но и в степени интенсивности.
Детальное изучение показало, что у пациентов основной группы интенсивность гиперемии к 7-м суткам заживления раны уменьшилась от 1 до 4 баллов. Однако у 5 пациентов, у которых на 3-и сутки показатели интенсивности гиперемии сохранялись на высоком уровне, к 7-м суткам эти значения приобрели не столь выраженную форму. У 71,9 % пациентов слизистая оболочка имела розовый цвет без признаков гиперемии. То есть на фоне проводимой антигомотоксической терапии к 7-м суткам у 71,9 % пациентов отсутствовали признаки воспаления, а у 28,1 % они были слабовыраженны.
На фоне проводимой антигомотоксической терапии к 7-м суткам у 71,9 % пациентов отсутствовали признаки воспаления, а у 28,1 % они были слабовыраженны
В группе сравнения на фоне проводимой стандартной терапии в послеоперационном периоде слизистая оболочка приобрела розовый цвет только у 48,9 % пациентов, у 26,8 % обследованных и 9,7 %, соответственно, степень гиперемии была очень слабо и слабовыраженна. Однако у 12,2 % пациентов гиперемия слизистой оболочки в области операционной раны была умеренно выражена и у 1 пациента сильно выражена. То есть интенсивность воспалительной реакции сохранялась у 14,6 % пациентов через 1 неделю после операции.
Длительность гиперемии слизистой оболочки полости рта у пациентов группы сравнения в среднем составила 5,57±0,39 суток (в среднем 3,80±0,21 балла на 3-и сутки и 1,92±0,18 балла на 7-е сутки), а в основной группе этот показатель достигал 4,38±0,13 суток (в среднем 3,15±0,21 балла на 3-и сутки и 1,53±0,17 балла на 7-е сутки) (р>0,05).
Об уменьшении выраженности воспаления в обеих группах, но с разной скоростью свидетельствовал показатель уменьшения локального отека, который мы также выразили в баллах. На 3-и сутки после операции локальный отек в области операционной раны отсутствовал только у 5 пациентов основной группы, слабовыражен он был у 56,3 % лиц основной группы против 24,3 % обследованных пациентов группы сравнения. На 7-е сутки явления коллатерального отека исчезли у 71,9 % оперированных пациентов основной группы и у 58,6 % пациентов группы сравнения. В основной группе пациентов определялся преимущественно слабовыраженный (9,4 %) и умеренно выраженный (18,7 %) коллатеральный отек.
В группе сравнения у большего числа лиц на 3-и сутки имелась умеренно выраженная и сильно выраженная отечность (48,9 % и 26,8 % соответственно). На 7-е сутки заживления раны у 21,9 % пациентов группы сравнения имелись признаки слабо выраженного отека и у 19,5 % — умеренно выраженного отека. Средний срок купирования локального отека у пациентов группы сравнения составил 7,4±0,54 суток (в среднем 2,02±0,11 балла на 3-и сутки и 0,60±0,12 балла на 7-е сутки), а в основной группе 6,3±0,24 суток (в среднем 1,22±0,15 балла на 3-и сутки и 0,46±0,14 балла на 7-е сутки) (р>0,05).
Данные рентгенологического исследования через шесть месяцев после операции показывали значительное уменьшение размеров костного дефекта, но без полного восстановления структуры костной ткани
Через 1 месяц визуальное обследование в обеих группах не выявило признаков гиперемии и локального отека СОПР. На переходной складке слизистой оболочки в области наложения швов имелись малозаметные рубцы. Пальпация безболезненная, в области оперированного участка челюсти определяется неуплотненная мягкая кортикальная пластинка. Клиническое обследование во всех группах, проведенное через 3 месяца после операции, выявило положительный результат. Пациенты не предъявляли жалоб, область операционной раны при пальпации была безболезненна. В сравниваемой и основной группах при пальпации оперированного участка челюсти по поводу малых и средних кист определялась плотная костная ткань.
У 100 % пациентов основной группы, которым назначалась антигомотоксическая терапия, через 6 месяцев после операции на рентгенограммах наблюдалось уменьшение размеров костного дефекта на 1/2 и 1/3 за счет незрелого костного регенерата. Через 12 месяцев после операции на рентгенограммах определялся дефект костной ткани с нечеткими контурами, по краям которого располагались костные балочки, что свидетельствовало о незавершенной регенерации кости. Процессы резорбции и синтеза кости распространялись от периферии костной полости к центру.
Полное восстановление структуры костной ткани через 6 месяцев наблюдалось в случае удаления одонтогенных образований до 1,5 см в диаметре. Через 12 месяцев у пациентов с исходными размерами костных дефектов от 0,5 до 1,5 см через 6 месяцев отмечалось полное восстановление костной ткани. У пациентов, у которых изначально имелась величина костного дефекта от 2 до 3 см с сохраненными стенками, выявлялось полное замещение дефекта собственной костью только через 12 месяцев.
В группе сравнения, согласно рентгенологическому исследованию, после операции с ведением раны по традиционной методике (кровяный сгусток) восстановление костной ткани в области дефекта происходило иначе. Данные рентгенологического исследования через 6 месяцев после операции показывали значительное уменьшение размеров костного дефекта, но без полного восстановления структуры костной ткани.
Через 12 месяцев после операции на рентгенограммах определялся дефект костной ткани. Контуры дефекта были нечеткие, по краям дефекта видны костные балочки, свидетельствующие о медленно протекающем процессе регенерации костной ткани. У пациентов с исходными размерами одонтогенных кист от 1,0 до 1,5 см наблюдалось заполнение дефекта молодой костной тканью. В остальных случаях, когда размеры кисты превышали 1,5 см, происходило уменьшение очага деструкции на 3/4 от исходного размера.
Через 6 месяцев после операции отмечено значительное уменьшение размеров костного дефекта, но без полного восстановления структуры костной ткани
У пациентов основной группы через 3 месяца обследования в 81,3 % случаев выявлялось сокращение индекса PAI: до 1 балла в 56,3 % случаев, до 2 баллов в 25 % случаев. Через 6 месяцев у 71,9 % пациентов индекс PAI был в норме, а через 12 месяцев эта цифра достигала 81,3 %. В группе сравнения через 3 месяца у 63,4 % пациентов индекс PAI был равен 1 баллу и у 26,8 % пациентов — 2 баллам. Через полгода после операции у 85,4 % данный индекс соответствовал норме, к 12-му месяцу репарации тканей эти значения еще больше снизились и достигали 95,2 %.
Замедленная регенерация тканей выявлена у 3,1 % пациентов, лечившихся комплексной гомеопатической терапией, и в 2,4 % случаев у пациентов, лечившихся традиционным методом. Это зависело от того, что в основной группе было 5 пациентов с радикулярными кистами, захватывающими 3 и более альвеолярных сегментов, тогда как в группе сравнения было всего 2 человека с большим диаметром кист.
Состояние операционного поля также оценивали по выделению тканевой жидкости через десневой желобок в области причинного зуба. Полученные данные были сопоставлены как в различные сроки обследования, так и с результатами лиц контрольной группы, не имеющих воспалительного процесса в пародонте.
Примечание: различия достоверны при ** р 0,05) возрастало, а содержание лактоферрина существенно не менялось (р>0,5). Полученные данные отражают наличие воспалительной реакции в обеих группах как до операции, так и на 7-е сутки после проведенной цистэктомии независимо от вида назначаемой лекарственной терапии.
Через 3 месяца у пациентов основной группы с одонтогенными образованиями до 1 см количество ИЛ-1β в элюате ДЖ приблизилось к значениям контрольной группы (р>0,5) и не определялся лактоферрин, что соответствовало показателям здорового периодонта. У оперированных пациентов, которым проводили цистэктомию одонтогенных образований диаметром до 3 см и более, в элюате ДЖ сохранялось повышенное содержание ИЛ-1β и лактоферрина (р>0,05 и р 0,5), но присутствовали следы лактоферрина.
Исследование количества ИЛ-1β и лактоферрина в элюате ДЖ пациентов группы сравнения в отдаленные сроки (табл. № 2) также выявило положительную динамику в сторону нормализации исследованных показателей.
Таблица № 2. Показатели элюата десневой жидкости пациентов группы сравнения с одонтогенными кистами челюстей в динамике заживления раневого дефекта.
Читайте также:

