Т клетки при лимфоме и лейкозе
Хронический лимфоцитарный лейкоз (ХЛЛ) является одной из разновидностей рака крови. Его также называют хронической лимфоидной лейкемией или лимфомой малых лимфоцитов.
Что такое хронический лимфоцитарный лейкоз?
ХЛЛ развивается из-за аномалий в образовании и развитии одной из разновидностей кровяных телец – лимфоцитов.
Большинство случаев ХЛЛ (около 95%) начинается с повреждения B-лимфоцитов (B-клеток). Основные признаки:
Из-за этого лейкоциты не могут нормально выполнять некоторые свои функции по борьбе с инфекциями;
Постепенно они накапливаются в костном мозге и крови, вытесняя из кровотока здоровые лимфоциты;
Низкий уровень здоровых лимфоцитов может привести к заражению вторичными инфекциями, анемии и кровотечениям;
Поврежденные клетки разносятся кровотоком по всему телу и мешают нормальному функционированию органов;
В редких случаях хроническая форма лейкоза переходит в агрессивную.
Другие разновидности хронических лимфом
Помимо ХЛЛ существуют и другие разновидности лейкозов.
Пролимфоцитарная лейкома (ПЛЛ). Она более агрессивна, чем большинство типов ХЛЛ. Поражает как B-лимфоциты, так и T-лимфоциты. Обычно развивается стремительнее ХЛЛ, но все-таки не так быстро, как острый лимфобластный лейкоз.
Крупнозернистая лимфоцитарная лейкемия (КЛЛ). Имеет тенденцию к медленному росту, однако, в некоторых случаях быстро переходит в агрессивную стадию. Характеризуется увеличенными лимфоцитами с видимыми гранулами, поражает T-лимфоциты или естественные киллеры (NK-клетки).
Волосатоклеточный лейкоз (ВКЛ). Медленно растущая разновидность рака B-клеток, при этом довольно редкая. Название происходит от внешнего вида лимфоцитов – точечных проекций на поверхности клеток, которые делают их волосатыми на вид.
Малая лимфоцитарная лимфома (МЛЛ). Это заболевание тесно связано с хронической формой лимфомы, однако, при МЛЛ раковые клетки обнаруживаются в лимфоузлах и селезенке, а не в костном мозге и крови.
Органы кроветворения и ХЛЛ
Для начала полезно разобраться, как вообще устроено кроветворение в организме и какую роль в этом играет костный мозг.
Стволовыми клетками называют особый тип клеток в организме, которые могут трансформироваться практически в любую иную форму: клетки печени, кожи, мозга или крови. Они формируются в костном мозге. Те стволовые клетки, которые участвуют в кроветворении, называются гемопоэтическими (стволовыми клетками крови).
Кровяные тельца непрерывно стареют, повреждаются и погибают. На них место должны непрерывно поступать новые, причем в достаточном количестве. Так, например, в норме у здорового взрослого человека должно содержаться от 500 до 1500 лимфоцитов на 1 мкл (примерно 25-40% от общего объема крови).
Стволовые клетки продуцируются в основном в мягкой губчатой ткани костей, но некоторое их число также можно встретить в циркулирующей крови.
Гемопоэтические клетки активно трансформируются в лимфоидные и миелоидные стволовые клетки:
-
Лимфоидные вырабатывают лимфобласты, которые в свою очередь преобразуются в несколько типов лейкоцитов, включая лимфоциты и NK-клетки;
Миелоидные, соответственно, продуцируют миелобласты. А те превращаются в другие типы лейкоцитов: гранулоциты, эритроциты и тромбоциты.
У каждого типа клеток крови своя специализация и предназначение.
Лейкоциты активно противостоят инфекциям и внешним раздражителям.
Красные кровяные тельца (эритроциты) отвечают за перенос кислорода из легких к тканям и доставку углекислого газа обратно в легкие для удаления.
Тромбоциты образуют сгустки, чтобы замедлить или прекратить кровотечение.
На ранних стадиях ХЛЛ обычно не беспокоит пациента. Для развития выраженных симптомов могут уйти годы, но как только они появляются – это уже повод говорить о хронической стадии заболевания.
Симптомы ХЛЛ часто путают с гриппом и прочими распространенными заболеваниями. При этом падает уровень содержания всех типов клеток крови. Симптомы низких лейкоцитов в крови:
жар, потливость, боли в различных частях тела;
Также может наблюдаться снижение уровня эритроцитов:
усталость, слабость, недостаток энергии и сонливость.
Симптомы низких тромбоцитов:
красные пятна нёбе или лодыжках;
частое или сильное носовое кровотечение;
синяки по всему телу и плохая свертываемость крови при порезах.
Общие симптомы хронического лимфоцитарного лейкоза:
необъяснимая потеря веса;
боли в костях или суставах;
опухание лимфатических узлов в шее, подмышках, желудке или паху.
Диагностика хронического лимфоцитарного лейкоза
Вышеперечисленные симптомы уже могут навести вашего врача на подозрения, однако, чтобы поставить окончательный диагноз, ему потребуется изучить историю болезни и провести полное медицинское обследование.
Для точной диагностики ХЛЛ потребуется несколько тестов. Некоторые из них могут не понадобиться, но будут нужны, чтобы уточнить диагноз и разработать более эффективную стратегию лечения.
Тест на типы и количество клеток крови, наличие аномальных лимфоцитов или уже сформировавшихся раковых клеток. Врачу здесь необходимо определить тип дефектных клеток, признаки замедления или наоборот прогрессирования рака. Применяется два вида специальных анализов крови: имунофенотипирование и проточная цитометрия. Иногда ХЛЛ можно заподозрить и при помощи общего анализа.
Отбор тканей из костей таза при помощи иглы (аспирация и биопсия костного мозга) и их проверка на наличие раковых клеток.
Клетки крови или костного мозга проверяют на наличие хромосомных аномалий: недостающих частей, дополнительных копий, дублировании хромосом. Также могут быть проверены изменения в белках иммунной системы, которые могут предсказать степень агрессивности ХЛЛ. В целом, выделяют три вида генетических тестов: цитогенетический анализ, флуоресцентную гибридизацию in situ (FISH)и полимеразную цепную реакцию (ПЦР-тест).
Сюда входят рентген грудной клетки, компьютерная и магнитно-резонансная томографии, а также ультразвуковое исследование лимфоузлов.
Стадии хронического лимфоцитарного лейкоза по Rai
Чтобы определить, как далеко зашла болезнь, и спланировать лечение, врачи пользуются системой Rai. Она была специально разработана для ХЛЛ:
Стадии заболевания зависят от количества лимфоцитов, эритроцитов и тромбоцитов в костном мозге и кровотоке, а также от того, были ли поражены селезенка, печень и лимфоузлы;
Стадии варьируются от 0 до IV, где 0 – наименее, а IV – наиболее тяжелая.
Ваш этап Rai даст онкологу информацию о вероятности прогрессирования болезни и необходимости лечения. Этап 0 характеризуется низким уровнем риска, этапы I–II – умеренным, этапы III–IV – высоким.
Ваш врач должен тщательно изучить и другие факторы, чтобы спрогнозировать перспективы и подобрать наиболее оптимальную стратегию лечения. В их числе:
Генетические отклонения и мутации в лейкоцитах (к примеру, отсутствие части хромосомы или наличие дополнительной хромосомы);
Наличие мутационного статуса IGHV-гена (наличие тяжелых цепей иммуноглобулина с переменной областью);
Проявляются ли симптомы ХЛЛ;
Возраст, наличие сопутствующих заболеваний, образ жизни;
Количество онкогенных (прелейкемических) клеток;
Скорость деления лейкемических клеток;
Как болезнь реагирует на первичное лечение и как долго длится ответная реакция.
Онкологу потребуется провести дополнительные тесты, анализы крови и костного мозга после анализа лечения.
Ремиссия будет означать, что болезнь реагирует на терапию. Полная ремиссия означает отсутствие каких-либо симптомов и клинических признаков рака. Частичная ремиссия означает уменьшение всех симптомов на 50%;
Рецидив означает, что ХЛЛ возвращается после пребывания в ремиссии более шести месяцев;
Резистентность – заболевание прогрессирует в течение шести месяцев после лечения.
Насколько распространен хронический лимфоцитарный лейкоз?
В США ежегодно диагностируется порядка 20 тысяч случаев ХЛЛ. По статистике это наиболее распространенная разновидность лейкемии среди взрослых – на нее приходится почти 40% случаев.
Причины хронического лейкоза
Медицине не известно, что является причиной ХЛЛ. Известно, что болезни подвержены люди среднего и старшего возраста. Средний возраст пациентов на момент постановки диагноза составляет 72 года. ХЛЛ чаще встречается среди мужчин, чем среди женщин.
В целом, это заболевание более распространено в Северной Америке и Европе, чем в Азии. Однако это зависит не от места проживания, а скорее от генетической предрасположенности отдельных рас. Азиаты, живущие в США, Канаде или европейских странах, подвергаются примерно одинаковому риску ХЛЛ со своими соплеменниками из азиатских стран.
В настоящий момент выявлено всего два фактора риска по ХЛЛ:
случаи ХЛЛ или иных типов лейкозов среди близких родственников.
Нужно иметь в виду, что у многих людей с ХЛЛ вообще не было факторов риска в анамнезе.
Лимфобластный лейкоз/лимфома
Основную часть лимфобластных лимфом (ЛЛ) - около 80% - составляют Т-клеточные опухоли в пре- и интратимической стадии Т-клеточной дифференцировки; в 20% случаев лимфобластных лимфом представлены предшественниками В-клеток.
ЛЛ чаще встречаются в детском и юношеском возрасте. Т-ЛЛ отличается высокой склонностью к развитию массивных опухолей в средостении, лейкемической трансформацией костного мозга и поражению ЦНС.
Если клетки лимфобластных лимфом в миелограмме составляют более 20%, заболевание классифицируется как острый лимфобластный лейкоз (ОЛЛ).
В основе диагностики лежат иммунофенотипические характеристики клеток лимфомы, находящихся в опухоли и костном мозге.
Неблагоприятные прогностические факторы идентичны таковым при ОЛЛ (см. острый лимфобластный лейкоз).
В момент установления диагноза у большинства больных определяется III-IV стадия болезни, поэтому обязательным компонентом обследования является люмбальная пункция.
Терапия данного варианта лимфомы проводится по протоколам лечения Т-ОЛЛ с выполнением всех этапов терапии, включая профилактику поражения ЦНС и облучение лимфоузлов средостения в суммарной очаговой дозе (СОД) 20 Гр. Поддерживающая терапия проводится в течение трех лет и идентична таковой при Т-клеточном ОЛЛ.
Анапластическая крупноклеточная (CD30+) лимфома
Анапластическая крупноклеточная лимфома (АККЛ) составляет 2-8% всех неходжкинских лимфом (НХЛ). Ранее АККЛ трактовалась как злокачественный гистиоцитоз (болезнь Абт-Леттерер-Зиве). Заболевание чаще диагностируется в детском возрасте, преимущественно болеют мужчины.
Анапластическая крупноклеточная лимфома начинается с появления экстранодальных поражений, хотя иногда в начале заболевания выявляется лимфоаденопатия. Интоксикационный синдром часто имеет место в дебюте заболевания. Для АККЛ характерен цитогенетический маркер - t (2; 5), который очень редко встречается при других формах неходжкинских лимфом.
В результате транслокации образуется сливной ген NPM-ALK, молекулярный продукт которого обладает трансформирующим действием на лимфоциты. Анапластическая крупноклеточная лимфома характеризуются пролиферацией плеоморфных больших лимфоидных клеток, которые положительны по CD30 антигену и размножаются в синусах лимфоузлов. Некоторые АККЛ имеют фенотип CD8+, но часть АККЛ не экспрессирует никаких маркеров (нулевой фенотип).
Лечение проводится по протоколам терапии высокоагрессивных крупноклеточных лимфом с проведением профилактики нейролейкемии.
Периферические Т-клеточные лимфомы
Периферические Т-клеточные лимфомы являются гетерогенной по клиническим проявлениям и гистологическим признакам группой опухолей. Наиболее часто проявления болезни сходны с В-клеточными лимфомами (нодальная и экстранодальная локализация). При локализации опухоли в области лица, синусов, носа часто отмечаются некрозы.
Морфологически периферические Т-клеточные НХЛ подразделяюся на подварианты в зависимости от преобладания крупных клеток (в 40-60%), малых лимфоцитов (15-17%), или сочетания малых лимфоцитов и трансформированных больших лимфоцитов (до 40%). Основой диагностики является иммунофенотипирование.
Опухолевые клетки имеют фенотип CD4+, CD8+, реже CD3+ в сочетании или в отсутствии CD4 и CD8. Наиболее часто при цитогенетическом исследовании отмечена структурная перестройка Хр6 (q23), что является фактором неблагоприятного прогноза (ФНП). Кроме того, отмечаются аномалии Хр11 и Хр14: t (8; 14) (q24; 11), t (11; 14) (q13; 11), inv (14) (q11; 32), t (11; 14) (p15; q11).
Полихимиотерапия (ПХТ) проводится с учетом ФНП, поскольку их наличие предполагает возможность интенсификации ПХТ на всех этапах прогрессирования болезни. При наличии опухолевых клеток в костном мозге более 20% заболевание расценивается как НХЛ с лейкемизацией процесса; соответственно, терапия в таких случаях проводится как при Т-клеточном ОЛЛ.
Ангиоиммунобластная лимфома
Ангиоиммунобластная лимфома является редким вариантом клональной Т-клеточной пролиферации. Ранее она рассматривалась как гипериммунная реакция организма на неуточненный этиологический фактор с высоким риском прогрессии в злокачественную лимфому.
Заболевание встречается у взрослых, течение острое. В момент установления диагноза у 50% больных выявляется IV стадия. Отмечается значительное повышение уровня лактатдегидрогеназы (ЛДГ) у 87%, интоксикационный синдром у 60%, поражение костного мозга у 30%, поражение кожи у 13% больных.
Клинически отмечается генерализованная лимфаденопатия, поражение и зуд кожи, артралгии, интоксикационный синдром (высокая лихорадка, профузная ночная потливость, резкое снижение массы тела), гепатоспленомегалия. Лимфома имеет тенденцию к ранней диссеминации.
В анализах крови определяется приобретенная гемолитическая анемия с положительной пробой Кумбса, поликлональная гипергаммаглобулинемия. При гистологическом исследовании лимфоузла отмечается потеря реактивных зародышевых центров, повышенная васкуляризация, наличие смешанноклеточных инфильтратов, состоящих из иммунобластов, эозинофилов, крупных дендритических клеток, эпителиоидных гистиоцитов.
Иммунофенотипически лимфоциты опухоли положительны по CD4 и CD8. Специфических цитогенетических нарушений не выявлено.
Применение стероидов и алкилирующих агентов для терапии возможно в начальной стадии заболевания. Однако вскоре наступает прогрессирование, появляется тенденция к поражению различных экстранодальных зон.
Поэтому заболевание требует применения схем ПХТ, применяемых при НХЛ высокой степени злокачественности. Высокоэффективным является протокол COP-BLAM/IMVP-16 с последующей аллогенной трансплантации костного мозга (алло-ТКМ) или аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК).
Дизайн протокола (протокол повторяется через 21 день) приводится ниже:
• циклофосфамид 400 мг/м2 в/венно в 1-й день
• винкристин 1 мг/м2 в/венно в 1-й день
• адрибластин 40 мг/м2 в/венно в 1-й день
• преднизолон 40 мг/м2 внутрь 1-10 дни
• натулан 100 мг/м2 внутрь 1-10 дни
• блеомицин 10 мг/м2 в/венно в 14 день
• митоксантрон 10 мг/м2 в 1-й день
• ифосфамид 1500 мг/м2 1-3 дни
• этопозид 150 мг/м2 13 дни
Т-клеточный крупногранулярный лимфоцитарный лейкоз встречается в 30-50 раз реже В-клеточного ХЛЛ и развивается в возрасте 50-55 лет, чаще у женщин. Основной морфологический признак заболевания — наличие больших гранулярных (содержащих азурофильные гранулы) лимфоцитов в периферической крови и костном мозге. Критерий диагностики — обнаружение больше 2 • 109/л больших гранулярных лимфоцитов в периферической крови. Наиболее частый иммунофенотип: CD3+, CD8+, CD4-, TCRab+.
Лейкемические клетки экспрессируют маркеры апоптоза (Fas или CD95 и Fas-лиганд), но резистентны к Fas-индуцируемому апоптозу.
Спленомегалия выявляется у 20% пациентов, лимфаденопатия и гепа-томегалия встречаются еще реже. В связи с выраженной нейтропенией нередко возникают рецидивирующие инфекции. У 30% больных наблюдается ассоциация с аутоиммунными заболеваниями (аутоиммунная гемолитическая анемия, ревматоидный артрит и др.).
Течение заболевания вариабельно, стандартное лечение не разработано.
Т-клеточная лейкемия/лимфома взрослых — редкое лимфопролиферативное заболевание, встречающееся преимущественно в странах бассейна Карибского моря и Японии. Доказанным этиологическим фактором является ретровирус HTLV-1. В эндемичных районах инфицировано 5% населения; в течение жизни заболевает один человек из 50-100 инфицированных (в Японии при наличии около 1 миллиона вирусоносителей в год регистрируется около 500 случаев заболевания). Спорадические случаи Т-клеточной лейкемии/лимфомы взрослых отмечены в Европе и Северной Америке.
Опухолевые клетки полиморфны, с полисегментированными, похожими на лепестки цветка, ядрами. Иммунофенотип клеток: CD7-, CD2+, CD3+, CD4+, CD5+, CD25+. Наиболее частые цитогенетические находки — трисомия 12, del 6q.
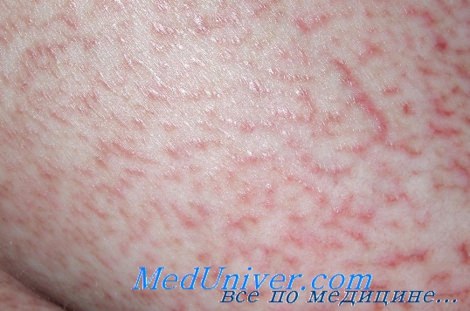
Грибовидный микоз
Т-клеточные лимфомы кожи — гетерогенная группа лимфопролиферативных заболеваний с первичным поражением кожи. В последние десятилетия заболеваемость Т-клеточными лимфомами кожи достоверно увеличилась. В большинстве случаев встречаются грибовидный микоз и синдром Сезари. Реже наблюдаются первичные СD30-позитивные Т-клеточные лимфопролиферативные заболевания: первичная кожная анапластическая крупноклеточная лимфома (КМ+) и лимфоматоидный папулез.
Грибовидный микоз многие годы протекает с изолированным поражением кожи (эритема, папулы, бляшки, эритродермия), однако в дальнейшем в большинстве случаев развивается агрессивная Т-клеточная лимфома с поражением лимфатических узлов, селезенки, печени и других органов и неблагоприятным исходом. При этом в крови и костном мозге часто обнаруживаются клетки Сезари (перекрестный синдром).
Синдром Сезари — генерализованная Т-клеточная лимфома, характеризующаяся поражением кожи, лимфоаденопатией и наличием в периферической крови неопластически трансформированных Т-лимфоцитов — клеток Сезари (атипичные лимфоциты с большим ядром неправильной формы и скудной базофильной цитоплазмой).
Синдром Сезари характеризуется сходным с грибовидным микозом поражением кожи, однако заболевание сопровождается ранней генерализацией и неблагоприятным течением (лишь 20% больных живут более 5 лет).
Диагноз лимфом кожи доказывается при морфологическом исследовании и результатами иммунофенотипирования (особенно важно это при CD30-позитивных лимфомах). При грибовидном микозе и синдроме Сезари нередко выявляются различные нарушения кариотипа (прежде всего при прогрессировании заболевания). При молекулярно-генетическом исследовании у большинства больных Т-клеточными лимфомами кожи обнаруживается клональная реаранжировка генов Т-клеточных рецепторов.
При локализованных формах Т-клеточных лимфом кожи применяется местное лечение: PUVA-терапия (ультрафиолетовое облучение с фотосенсибилизатором), локальное облучение и введение цитостатиков в опухолевые очаги. При синдроме Сезари используются монохимиотерапия и полихимиотерапия, однако частота ремиссий невелика и они обычно непродолжительны.
13 марта 2020 г. 9:07
Пациенты с раком имеют подавленную иммунную систему и более восприимчивы к инфекциям.
12 марта 2020 г. 8:26
Исследователи представили структуру и механизм белков, которые экспрессируются при различных формах рака и связаны с плохим прогнозом пациента.
9 марта 2020 г. 12:07
В низких дозах тетродотоксин заменяет опиоиды для облегчения боли, связанной с раком.
5 марта 2020 г. 14:24
Новый метод картирования сил, которые кластеры клеток оказывают на микроокружение, может помочь в изучении развития тканей и метастазирования рака.
Лейкемия означает рак белых клеток крови (лейкоцитов). Большинство типов этого заболевания вызывают синтез аномальных лейкоцитов в костном мозге. Они могут попасть в кровоток и распространиться по всему телу. Поскольку эти клетки не работают полноценно, то не способны защитить организм от инфекций и бактерий.
Лейкоз разделяют на две основные группы – острый (очень быстро развивается болезнь) и хронический (отмечаются медленные темпы, на протяжении нескольких месяцев или лет, в основном бессимптомно).
Острый лимфобластный лейкоз (лимфоцитарный, лимфолейоз, ОЛЛ) поражает незрелые лимфоидные клетки, быстро прогрессирует. При отсутствии необходимой терапии завершается летальным исходом.
Симптомы острого лимфобластного лейкоза
Основная задача лейкоцитов – бороться с инфекций. Поскольку аномальные клетки не способны полноценно работать, возрастает риск инфекции, которая тяжело поддается лечению.
Избыточное количество лимфоцитов переполняет костный мозг, не хватает места для других типов клеток крови. Возникает недостаток эритроцитов и тромбоцитов. Дефицит эритроцитов провоцирует анемию, тромбоцитов - проблемы со свертываемостью крови.
Из-за увеличивающегося количества лейкоциты начинают накапливаться в селезенке, костном мозге, лимфоузлах, вызывая отек. Иногда это происходит в печени, спинном или головном мозге, у мужчин – в яичках.
Разница между острым лимфобластным лейкозом и лимфомой
Острый лимфолейкоз развивается в костном мозге, а потом проникает в другие части тела; лимфома – в лимфоузлах и иных органах, а затем может поразить костный мозг.
Если аномальные лимфоциты есть и в костном мозге, и в лимфатической системе, иногда трудно сказать, лейкоз это или лимфома.
Многие симптомы острого лимфобластного лейкоза у взрослых являются расплывчатыми. Состояние напоминает грипп. Возможные признаки:
- Общая слабость.
- Усталость.
- Высокая температура.
- Потеря веса.
- Частные инфекции.
- Легко возникающие ушибы, без какой-либо очевидной причины.
- Кровотечение из десен и носа.
- Кровь в моче и стуле.
- Боли в костях и суставах.
- Одышка.
- Увеличение лимфатических узлов.
- Ощущение переполненности и дискомфорта в области живота из-за опухшей печени или селезенки.
Эти симптомы возникают вследствие избытка аномальных лейкоцитов и недостатка здоровых лейкоцитов, эритроцитов и тромбоцитов.
Отмечаются трудности у организма человека с ОЛЛ, справиться с инфекцией, поскольку нет достаточного количества белых клеток крови для борьбы с бактериями или вирусами.
Скопление лейкозных клеток происходит в лимфоузлах, суставах и костях, провоцируя боль и отек.
Дефицит тромбоцитов приводит к проблемам со свертываемостью крови, недостаток эритроцитов – к анемии.
Симптомы Т-клеточного лейкоза
Данный тип лейкемии может вызывать опухание лимфоузлов в центре грудной клетки и вилочковой железы. Они оказывают давление на трахею, провоцируя одышку и кашель. Помимо этого, возможно давление на вены, по которым проходит кровь от головы. Это становится причиной давления в кровеносных сосудах; лицо, шея и руки опухают и приобретают красный цвет. Такое состояние носит название обструкция верхней полой вены.
Причины острого лимфобластного лейкоза (ОЛЛ)
Данное заболевание реже возникает у взрослых, однако, это наиболее распространенный тип лейкемии у детей. Чаще болезнь диагностируют у мужчин, чем у женщин.
Исследования обозначают следующие факторы риска:
- Радиационное облучение. Давно известно, что высокие дозы радиации увеличивают риск острого лимфоцитарного лейкоза. Существует ряд доказательств, что проведение рентгена во время беременности повышает вероятность лейкемии у ребенка в детском возрасте.
- Воздействие бензола. Взаимодействие с этим химическим веществом возможно в таких отраслях промышленности, как химическая, фармацевтическая, полиграфическая; по производству резины, обуви, бензина. Чем выше уровень воздействия в течение многих лет, тем больше риск. Бензол также содержится в сигаретном дыме.
- Курение и потребление кофе. Обзор исследований (мета-анализ) в 2009 году показал, что курение родителей в доме повышает риск ОЛЛ у детей. Это включает курение отца до зачатия ребенка. Данные французского исследования (ESCALE) 2013 года показали, что потребление более 2 чашек кофе в день во время беременности незначительно увеличивает вероятность возникновения ОЛЛ у ребенка в детском возрасте. Однако требуются дополнительные исследования.
- Генетика. Некоторые редкие наследственные заболевания повышают риск острого лимфобластного лейкоза: синдром Дауна, анемия Фанкони, атаксия телеангиоэктазия. Также в качестве возможной причины лимфоцитарного лейкоза называют химиотерапию. Лечение такими химиопрепаратами, как этопозид, митоксантрон, амсакрин и идарубицин – увеличивает вероятность ОЛЛ спустя много лет.
- Вирусы. Т-лимфотропный вирус человека повышает риск редкого типа лейкоза Т-клеток.
- Электромагнитные поля. Некоторые исследования говорят, что воздействие очень высоких уровней электропередач увеличивает вероятность лейкемии у детей, однако их результаты недостаточно ясны.
- Избыточный вес. Некоторые исследования отмечают, что у людей с ожирением наблюдается повышенный риск лейкемии.
- Воздействие краски в качестве возможного фактора риска отметило одно из исследований. Однако требуется дальнейшее изучение данного вопроса.
- Ослабленный иммунитет. Увеличение вероятности развития лимфоцитарного лейкоза вдвое или втрое отмечается у людей с ВИЧ (СПИД) и у тех, кто перенес трансплантацию органов.
Факторы, снижающие риск лейкемии:
- Грудное вскармливание.
- Воздействие инфекций в детстве. Сниженная вероятность ОЛЛ отмечается у детей, которые ходили в ясли или с раннего возраста были под присмотром няни.
Врачи подразделяют острый лейкоз на миелоидный и лимфобластный. Но миелоидный и лимфобластный разделяют также на более мелкие группы (подтипы). Идентификация лейкоза помогает врачу правильно спланировать лечение в Ассуте.
Израильские врачи используют систему классификации ВОЗ. Она основана на типе лимфоцита, который стал злокачественным. Выделяют три подтипа:
- Пре-В-клеточный – наиболее распространённый тип лейкоза у взрослых.
- Зрелый В-клеточный – идентифицируется в связи с конкретными генетическими нарушениями. Также его называют тип Беркитта, поскольку он похож на другой вид рака – лимфому Беркитта.
- Пре-Т-клеточный – чаще всего развивается у молодых взрослых, в большинстве случаев – у мужчин.
Более редко применяется французско-американо-британская классификация, которая подразделяют ОЛЛ на три типа:
- L1 – лимфоциты выглядят как зрелые.
- L3 – лимфоциты являются незрелыми и выглядят аномальными.
- L2 – средний показатель между L1 и L3, наиболее распространенный тип у взрослых.
Лейкозные клетки изучают под микроскопом, чтобы идентифицировать и соотнести с каким-либо подтипом. Кроме того, проводится исследование белков (маркеры антител) в аномальных клетках, изменения в хромосомах злокачественных клетках (цитогенетика).
Смешанный тип лейкемии
Иногда лейкоз оказывается сочетанием ОЛЛ и острой миелоидной лейкемии (ОМЛ). Аномальные клетки обладают белками (маркерами) от обоих типов. Это острая бифенотипическая лейкемия. Бифенотипический означает оба типа.
Диагностика острого лимфобластного лейкоза у взрослых в клинике Ассута
С пациентом работает гематолог, возможно проведение нижеперечисленных видов тестов.
Могут быть выполнены:
- полный анализ крови (FBC), в процессе которого исследуются различные типы клеток;
- анализы крови, чтобы выяснить, насколько хорошо работает печень или почки;
- если присутствует инфекция, выполняются тесты для ее определения и назначения типа антибиотика.
Исследование костного мозга
Костный мозг синтезирует клетки крови. Врач может взять образец органа, чтобы проверить на наличие признаков лейкоза и других заболеваний. Есть два типа диагностики острого лимфобластного лейкоза – аспирация костного мозга и биопсия или трепанобиопсия.
При аспирации врач берет пробу жидкости костного мозга из кости бедра. Больному предварительно делают инъекцию локального анестетика.
В процессе биопсии врач используют иглу большего размера, чтобы удалить небольшое количество кости и костного мозга. Обычно эти две процедуры проводят одновременно.
В дополнении гематолог может проверить, есть ли изменения в хромосомах лейкозных клеток. Такие тесты называются цитогенетическими. Проводится анализ на наличие конкретных белков, которые производят определенные типы лейкозных клеток. Этот тест называют иммунофенотипированием.
В ряде случаев заболевания у людей с острым лимфолейкозом в лейкозных клетках есть мутация под названием филадельфийская хромосома. Она образуется, когда ген ABL на 9 хромосоме отрывается и присоединяется к гену BCR на 22 хромосоме, что приводит к созданию нового гена - BCR-ABL. Это провоцирует синтез избыточного количества белка – тирозинкиназы, стимулирующей рост и деление лейкозных клеток.
Этот тест помогает выявить мутации в генах клеток и правильно подобрать лечение.
Пункция необходима, чтобы выяснить, есть ли аномальные клетки в ликворе (жидкости вокруг мозга и позвоночника). С помощью иглы, введенной в позвоночник, врач собирает небольшое количество ликвора.
Рентген грудной клетки
Данный тест проводится, чтобы проверить общее состояние здоровья. При остром лимфолейкозе иногда возникают опухоли из лейкозных клеток в центре грудной клетки, в области вокруг сердца (зона средостения).
КТ выполняют, чтобы выявить конкретные признаки лимфоцитарного лейкоза или изучить общее состояние здоровья.
На протяжении всего курса лечения в Израиле и последующего наблюдения будет проводиться диагностика костного мозга. Это может помочь:
- В первую очередь, определить правильный тип лейкоза.
- Узнать, как лейкемия реагирует на лечение.
- Проверить лейкозные клетки после окончания терапии. Оценить минимальную остаточную болезнь.
Могут быть выполнены следующие виды обследований:
- КТ проводится с целью визуализировать увеличенные лимфатические узлы или иные аномалии в органах тела.
- МРТ отображает подробную картину тела, более четко, чем КТ, визуализирует мягкие ткани.
- УЗИ выполняется, чтобы проверить, есть ли острый лимфолейкоз в селезенке или в яичках (у мужчин).
- Тканевое типирование проводится, если врач рассматривает пересадку стволовых клеток в качестве подходящего лечения. Это специальный анализ крови, который покажет, насколько ткань костного мозга возможного донора совпадает с тканью пациента. Лейкоциты на своей поверхности имеют белки - HLA маркеры. Если клетки костного мозга пациента и донора имеют очень похожие HLA маркеры, больше шансов, что иммунная система пациента не отвергнет донорский орган.
Обнаружение лейкозных клеток после лечения
Часто после химиотерапии кажется, что пациент излечился. В крови и образцах костного мозга не находят аномальных клеток, такое состояние означает ремиссию. Но лейкозные клетки могут сохраниться. Тест на минимальную остаточную болезнь поможет убедиться, присутствует ли болезнь.
Есть два способа. Один – полимеразная цепная реакция (ПЦР) – ищет генетические изменения в клетках. С его помощью можно найти одну лейкозную клетку среди миллионов здоровых. Другой тест – иммунофенотипирование – проверяет белки, созданные аномальными клетками. Таким образом, эти тесты определят эффективность химиотерапии и вероятность рецидива.
Выживаемость при остром лимфобластном лейкозе
Лечащий врач может дать самую полную информацию о прогнозе для конкретного пациента. Приведенная здесь статистика предоставлена для общего ознакомления. Термины 5-летняя и 10-летняя выживаемость при остром лимфобластном лейкозе означает число людей, участвовавших в испытаниях, которые были живы спустя 5 или 10 лет после диагностики и проведенной терапии.
Успешность лечения рака обусловлена рядом факторов:
- Типом лейкемии.
- Развитием болезни.
- Ответом на лечение цитостатическими препаратами.
Более 8 из 10 человек достигают ремиссии. Если наблюдаются рецидивы, иногда возможно достижение второй ремиссии с помощью цитостатического лечения.
Перспективы при остром лимфобластном лейкозе
Возраст очень влияет на исход. Отчасти это связано с тем, что люди молодого возраста лучше справляются с очень интенсивной терапией.
В среднем для всех возрастных групп для 70% человек отмечают выживаемость 5 лет и более после постановки диагноза. Далее выживаемость 5 лет и более обозначают:
- Для 90% пациентов в возрасте 14 лет и младше.
- Для 66% человек в возрасте 15-24 года.
- Для 40 % - в возрасте 25-64 года.
- Для 15% - в возрасте 65 лет и старше.
- Возраст.
- Пол (у женщин прогноз лучше, чем у мужчин).
- Количество лейкоцитов (если высокое, прогноз хуже).
- Конкретный тип лейкоцитов.
- Генетические мутации в хромосомах.
Прогноз при остром лимфолейкозе хуже, если аномальные клетки находят в мозгу или цереброспинальной жидкости при постановке диагноза. Некоторые конкретные генетические мутации в лейкозных клетках затрудняют успешное лечение онкологии. Если патологические клетки остаются после индукционной химиотерапии, лейкемия может с трудом поддаваться терапии.
Лечение лейкоза в Израиле
Лечение лейкоза в Израиле дает положительный эффект в 98% случаев. Созвонитесь с экспертами клиники Ассута, чтобы договориться об обслуживании.
ЗАЯВКА НА ЛЕЧЕНИЕ
Отправляя форму Вы соглашаетесь с политикой конфиденциальности
Читайте также:

