Стволовая клетка мезенхимальная опухоль

Мезенхимальные опухоли происходят из производных мезенхимы - зародышевой соединительной ткани большинства многоклеточных животных и человека:
соединительной (фиброзной), жировой, мышечной, сосудистой, костной, хрящевой тканей, синовиальных и серозных оболочек.
- Встречаются намного реже эпителиальных.
- Чрезвычайно гетерогенны, что объясняется гетерогенностью мезенхимальных тканей.
- Не обладают органной специфичностью (могут встречаться в любом органе).
- Доброкачественные варианты крайне редко подвергаются малигнизации.
- При некоторых разновидностях мезенхимальных опухолей трудно определить разницу между паренхимой опухоли и стромой.
Доброкачественные опухоли
- Врожденное образование. Чаще локализуется в коже, обнаруживается в печени (наиболее часто встречающаяся первичная опухоль печени).
- Увеличивается с ростом организма.
- Спонтанно не исчезает.
- Может сопровождаться тромбозом, изъязвлением, инфицированием.
- Макроскопическая картина: на коже имеет вид темно-красных пятен или узла красно-синюшного цвета с четкими границами.
- Микроскопическая картина: множество тонкостенных сосудистых полостей, выстланных эндотелиальными клетками без признаков клеточного атипизма. Полости различной формы и величины (тканевой атипизм), заполнены кровью и тромботическими массам
Злокачественные опухоли
Саркома Капоши – множественная злокачественная опухоль из мало-дифференцированной сосудистой ткани.
Существуют 4 клинические разновидности:
- Спорадическая форма (классический вариант) – возникает у мужчин в возрасте старше 60 лет (преимущественно евреев и жителей Средиземноморья).
- Эндемическая форма - распространена в некоторых районах Центральной Африки (10% всех опухолей).
- Эпидемическая форма (ВИЧ-ассоциированная) – возникает при ВИЧ-инфекции на стадии выраженного иммунодефицита и относится к ВИЧ-ассоциированным заболеваниям.
- Саркома Капоши, развивающаяся при применении иммунодепрессантов.
Морфология саркомы Капоши.
- Макроскопическая картина: красновато-голубоватые или фиолетовые пятна и бляшки на коже, часто с изъязвлением.
- Микроскопическая картина (не зависит от клинической формы): сосудистые полости, выстланные эндотелиальными клетками и заполненными эритроцитами. Пучки вытянутых фибробластоподобных клеток. Характерны кровоизлияния, гемосидероз.
Редкая злокачественная опухоль из гладкомышечной ткани. Встречается забрюшинно, в матке. Чаще возникает de novo и не связана с озлокачествлением лейомиомы.
Прогноз крайне плохой: более половины больных умирают в течение 2 лет.
В подавляющем большинстве случаев меланома локализуется в коже, реже в оболочках глаз, еще реже в мягких мозговых оболочках и пр. Чаще возникает у женщин 30 – 50 лет на коже нижних конечностей, головы, шеи. Прослеживается связь меланом кожи с инсоляцией (УФО). Большинство меланом возникает de novo, крайне редко на фоне предсуществующих пигментных образований.
Основные варианты меланомы. Клинико-морфологическая классификация меланомы:
- Злокачественная лентиго-меланома.
- Нодулярная меланома.
- Акральная лентигинозная меланома.
- Поверхностно-распространяющаяся меланома - наиболее частый вариант. Типичная локализация – конечности и туловище. Преобладает радиальная форма роста (до 10 лет).
- Макроскопическая картина: пятно или бляшка без четких границ, окрашенные в различные цвета – от розово-бурого до темно- коричневого.
- Микроскопическая картина: мономорфные атипичные меланоциты, образующие гнезда из педжетоидных клеток – крупные клетки с вакуолизированной светлой цитоплазмой (горизонтальный рост). Очаги инвазии в дерму, часто окруженные клеточным инфильтратом и фиброзной тканью (вертикальный рост). Прогноз - очень хороший, после появления препарата Кейтруда, можно сказать о возможности полного излечения вбольшинстве случаев.
Общая характеристика: большинство этих опухолей – опухоли головного мозга. Опухоли ЦНС значительно чаще встречаются у детей, чем у взрослых. Первичные злокачественные опухоли ЦНС метастазируют редко, в основном в пределах ЦНС по току ликвора.
Доброкачественные интракраниальные опухоли могут привести к смерти благодаря сдавлению жизненно важных отделов мозга (т.е. клинически быть злокачественными).
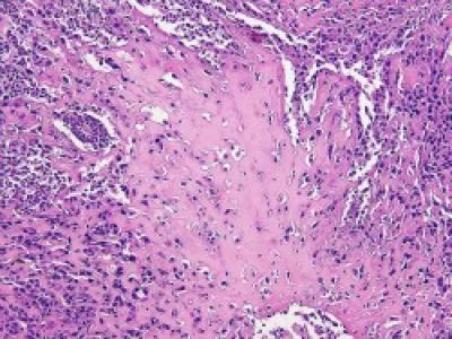
Рак яичников, выращенный в присутствии карцинома-ассоциированных мезенхимальных стволовых клеток (CA-MSCs). (Фото: University of Michigan Health System)
Раковые стволовые клетки – небольшое количество клеток опухоли, играющих ключевую роль в ее росте и распространении. Традиционные методы лечения рака не убивают эти клетки, что и является причиной частых неудач противораковой терапии.
В исследовании, опубликованном в журнале The Journal of Clinical Investigation , ученые изучали мехенхимальные стволовые клетки ткани яичников - нормальные клетки, обнаруживаемые по всему организму. Мехенхимальные стволовые клетки могут дифференцироваться в различные специализированные клетки, такие как жировые, костные или хрящевые.
Мезенхимальные стволовые клетки могут дифференцироваться в клетки костной (остеобласты), жировой (адипоциты) и хрящевой (хондроциты) ткани. (Рис. sigmaaldrich.com)
Известно, что мезенхимальные стволовые клетки вовлечены в процесс заживления ран, что заставляет многих ученых предполагать, что они могут помочь и в борьбе с раком. Мезенхимальные стволовые клетки опухолевой ткани яичников отличаются от мезенхимальных стволовых клеток здоровых яичников и фактически стимулируют рост опухоли.
Для изучения того, что происходит с мезенхимальными стволовыми клетками, ученые использовали мышиные модели и образцы человеческой ткани как здоровых, так и пораженных раком яичников. Они установили, что ассоциированные с раком мезенхимальные стволовые клетки увеличивают размер опухоли в первую очередь за счет увеличения количества раковых стволовых клеток.
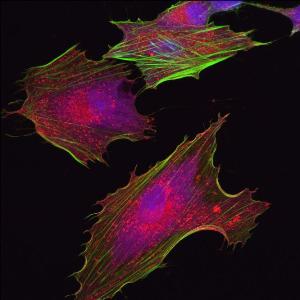
Мезенхимальные стволовые клетки. (Фото: cellmedicine.com)
В мезенхимальных стволовых клетках опухолевой ткани более активно экспрессировался один из белков BMP – BMP2 . BMP2 относится к регуляторным белкам, и при нормальной функции клеток его собственная экспрессия тщательно контролируется. Ученые установили, что количество BMP2 в мезенхимальных стволовых клетках раковой опухоли больше чем в три раза превышает его уровень в нормальных мезенхимальных стволовых клетках. При добавлении BMP к раковым клеткам количество раковых стволовых клеток увеличивалось.
При этом известный ингибитор BMP – белок ноггин (Noggin) - блокирует стимуляцию мезенхимальными стволовыми клетками роста раковых стволовых клеток.
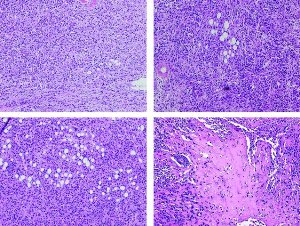
Окрашенные гематоксилином и эозином образцы опухолевой ткани, выращенные с мезенхимальными стволовыми клетками или карцинома-ассоциированными мезенхимальными стволовыми клетками, показывающие опухолевые адипоциты (жировые клетки) (вверху справа и внизу слева). Опухоли с CA-MSC демонстрируют области раннего формирования кости (снизу справа). (Фото: jci.org)
Прежде чем могут быть начаты клинические испытания на пациентах, исследование должно быть продолжено в лаборатории. Тем временем в течение следующего года Центр всестороннего изучения рака ожидает начала двух новых клинических испытаний, в которых будут протестированы другие препараты, направленные на раковые стволовые клетки яичников.
По данным Американского общества рака (American Cancer Society), в этом году в США будет диагностировано 21880 случаев рака яичников и 13850 пациентов умрут от этого заболевания.
Karen McLean, Yusong Gong, Yunjung Choi, Ning Deng, Kun Yang, Shoumei Bai, Lourdes Cabrera, Evan Keller, Laurie McCauley, Kathleen R. Cho, and Ronald J. Buckanovich. Human ovarian carcinoma–associated mesenchymal stem cells regulate cancer stem cells and tumorigenesis via altered BMP production
Накапливающиеся свидетельства показывают, что мезенхимальные стволовые клетки (MSCs) рекрутируются опухолевым микроокружением; однако вопрос об их роли в солидных опухолях является спорным. В этом исследовании мы определили и подтвердили присутствие карцинома-ассоциированных мезенхимальных стволовых клеток (CA-MSCs) в большинстве из проанализированных тканевых образцов человеческого рака яичников. Эти CA-MSCs имеют нормальную морфологию, нормальный кариотип и нетуморогенны. Карцинома-ассоциированные мезенхимальные стволовые клетки мультипотентны и обладают способностью дифференцироваться в жир, кость и хрящ. В сочетании с опухолевыми клетками in vivo CA-MSCs стимулируют опухолевый рост более эффективно, чем контрольные MSCs. Исследования in vivo и in vitro показали, что CA-MSCs способствуют опухолевому росту за счет увеличения количества раковых стволовых клеток. Хотя CA-MSCs экспрессируют обычные маркеры MSCs, профиль их экспрессии отличается от такового MSCs здоровых людей, включая усиленную экспрессию BMP2, BMP4 и BMP6. Важно отметить, что применение BMP2 in vitro имитирует действие CA-MSCs на раковые стволовые клетки, в то время как ингибирование сигналинга BMP in vitro и in vivo частично отменяет стимулируемый MSC опухолевый рост. Взятые вместе, наши данные свидетельствуют о том, что мезенхимальные стволовые клетки в микроокружении опухоли яичников имеют профиль экспрессии, способствующий туморогенезу, и что ингибирование BMP может стать эффективным терапевтическим подходом к лечению рака яичников.
Еще о раковых стволовых клетках
Стромальные опухоли желудка
Вначале термин желудочно-кишечные стромальные опухоли (ЖКСО) ввели как нейтральный для новообразований, не относящихся ни к гладкомышечным опухолям, ни к неврилеммоме. Термины лейомиома, лейомиосаркома зарезервированы для опухолей с гладкомышечной дифференцировкой, выявляемой гистологически или иммуноморфологически (сильная диффузная реакция на актин и десмин). ЖКСО (8936/0-3) составляют 2.2% злокачественных опухолей желудка. Здесь нет преобладания пола, в отличие от рака, более частого у мужчин (2:1). Поражение диагностируют у взрослых в шестом-восьмом десятилетии жизни. ЖКСО могут локализоваться в любом органе ЖКТ, но преимущественно в желудке (до 70%), в тонкой кишке (20-30%), толстой, прямой кишке и пищеводе (вместе 5 на 50 полей зрения при большом увеличении микроскопа обычно доброкачественные; опухоли 10 митозов на 10 полей зрения, считают высоко злокачественными стромальными опухолями. Большие опухоли, особенно >10см, даже без митозов, нередко дают рецидивы и отдаленные метастазы и вместе с анеуплоидностью, высоким пролиферативным индексом (>10% при учете Ki67 или его аналогов типа MIB1) отражают высокую степень злокачественности ЖКСО. Гистологические признаки злокачественности те же, что и в саркомах мягких тканей (см. том 5 серии): выраженная плотность расположения клеток (высокая клеточность); выраженная атипия и полиморфизм ядер и клеток; прорастание слизистой оболочки; наличие опухолевых эмболов в просвете сосудов; очаги некроза; наличие метастазов.
Цитологической диагностики ЖКСО редки. При рутинном исследовании мазка их невозможно отличить от гладкомышечных опухолей (четкие рыхлые фрагменты в виде пластов.или пучков клеток веретенообразной формы с однотипными удлиненными ядрами или с более крупными полиморфными ядрами, содержащими крупные ядрышки). Однако, при использовании материала АПТИ и иммуноцитохимической реакции на KIT (CD117, CD34) в мазке появляется возможность цитологической идентификации опухоли; реакция на десмин, миоглобин, белок S 100 в ЖКСО отрицательная. В отличие от этого, при лейомиоме отрицательная реакция на CD117, CD34 и белок S 100, а при солитарной фиброзной опухоли — на CD117 и белок S-100, но положительная на CD34.При цитогенетическом анализе и сравнительной геномной гибридизации в доброкачественных и злокачественных ЖКСО, как правило, выявляют потери по хромосомам 14 и 22, достаточно часто — делеции в коротком плече хромосомы 1 и по хромосоме 15. Высокий уровень амплификации отмечен в злокачественных ЖКСО по длинным плечам хромосом 3,5,8, а также по короткому плечу Х-хромосомы. Наиболее распространены мутации в регуляторном домене (экзон 11) c-kit гена, являющегося примембранным белком. У больных ЖКСО выявлено семейное наследование KIT мутаций.
Гладкомышечные опухоли
Лейомиома (8890/0) и лейомиосаркома (8890/3) ЖКТ наиболее часто локализованы в желудке. Лейомиома обычно одиночная асимптоматическая опухоль (изредка множественные), четко отграниченная, расположена в подслизистом слое, может выбухать под серозную оболочку и в просвет желудка, нередко приводя к изъязвлению слизистой оболочки; тогда опухоль диагностируют при исследовании эксфолиативного материала. Чаще исследуют материал АПТИ, полученный при эндоскопии. Изредка у молодых женщин встречают триаду Carney’s (многоопухолевый синдром): лейомиобластома+хондромы легкого+функционирующая вненадпочечниковая параганглиома.
Дифференциально-диагностический ряд: лейомиома.
Для лейомиомы характерны небольшие размеры ( 7.5см), клеточность; появляется атипия клеток, более грубый хроматин, некроз и метастазы. Хотя нет корреляций между числом митозов и клиническим течением, подсчет митозов может стать ключевым признаком правильного диагноза. Если в гладко-мышечной опухоли обнаруживают >5 митозов на 10 полей зрения, то она считается злокачественной. Наличие даже одного (!) митоза в мазке должно вызвать предположение о лейомиосаркоме.
Небольшие комплексы округлых эпителиоидных клеток напоминают рак, зернистость цитоплазмы — зернисто-клеточную опухоль, веретенообразная форма клеток— фибробластическую опухоль. Поиск более дифференцированных участков помогает установить правильный диагноз. При дифференциальной диагностике полиморфноклеточного варианта опухоли следует помнить о других типах полиморфнокле-точной саркомы, метастазах в мягкие ткани анапластического рака и саркомоподобной меланомы.
Гломусная опухоль (8711/0). Мезенхимальная опухоль из клеток, сходных с модифицированными глад-комышечными клетками нормального гломусного тельца (специальный артерио-венозный шунт, контролирующий кровоток и регулирующий температуру). При ЭМ гломусная клетка имеет признаки мышечной клетки и перицита. В желудке локализована преимущественно в антральном отделе в виде небольшого (1-4см) внутристеночного образования. Чаще наблюдают в шестом десятилетии, независимо от пола. Треть опухолей проявляется в виде язвы, треть кровотечением, треть протекает асимптоматически.
Гистологическая картина: характерен солидный органоидный рост из гнезд однотипных мелких гло-мусных клеток, округлой формы, окружающих сосуды капиллярного типа или образующих манжетки вокруг небольших сосудов. Нередко видны очаги эпителиоидных клеток. Ядра однотипные, округлой формы, иногда более крупные, гиперхромные; четкие контуры цитоплазмы; клетки окружены базальной мембраной, различимой при ШИК-реакции, окрашивании толуи-диновым синим, иммуноморфологическом выявлении характерных белков базальной мембраны (ламинин, коллаген IV типа). Митозы отсутствуют. Строма гиали-низирована или миксоидная.
Цитологическая картина: в желудке опухоль редко является предметом цитологического исследования, но знание о ней может понадобиться цитопато-логу во время экспресс-диагностики. Мазок содержит вариабельное число клеток опухоли, преимущественно изолированных, редко в скоплениях. Гломус-ные клетки мелкие и среднего размера, однотипные, округлой формы, с центрально расположенным ядром, округлой или овоидной формы, едва заметными ядрышками и слабо базофильной цитоплазмой с нечеткими контурами. Иногда ядра более крупные, гиперхромные. Можно обнаружить тучные клетки, единичные гладкомышечные клетки, очень редко фрагменты мелких сосудов, вариабельное количество миксоидного фибриллярного вещества.
Клетки экспрессируют гладкомышечный актин, кальдесмон и обильный перицеллюлярный коллаген IV типа. Отсутствует экспрессия CD31, CD34 (отличие от сосудистых опухолей), цитокератина и белка S 100 (отличие от эпителиальных опухолей). Гломусные клетки не содержат десмина и гликогена (отличие от гладкомышечных клеток). При ЭМ выявляют выраженную наружную мембрану, короткие переплетающиеся отростки цитоплазмы, пучки тонких филаментов, напоминающих филаменты из актина, с плотными тельцами и изредка присоединенными к цитоплазмати-ческой мембране бляшками.
Другие неэпителиальные опухоли
Нейрогенные опухоли: неврилеммома (9560/0), нейрофиброма (9540/0), нейросаркома (9540/3). Не-врилеммому (шванному) редко встречают в ЖКТ, обычно в желудке у пожилых больных. Чаще покрыта интактной слизистой оболочкой, вовлекая мышечную пластинку слизистой оболочки. Размеры 0.5-7 см, имеет сферическую или овоидную форму.
Сосудистые опухоли: гемангиома (9120/0), лим-фангиома (9170/0), саркома Капоши (9140/3). Последняя локализуется в слизистой оболочке или реже в стенке желудка, особенно у ВИЧ-инфицированных больных.
Жировые опухоли: липома (8850/0); типично выступает в просвет желудка.
Зернисто-клеточную опухоль (9580/0) чаще наблюдают в среднем возрасте. В желудке имеет вид небольшого подслизистого узла, реже расположена внутристеночно или субсерозно. Гистологическая и цитологическая картина зернисто-клеточной, а также сосудистых, жировых опухолей см. в гл. IV.
При мезенхимальных опухолях желудка распространены мутации c-kit гена. Амплификацию с-егЬВ-2, тирозинкиназного рецептора онкогенов находят
в 10% опухолей желудка, суперэкспрессия сочетается с плохим прогнозом заболевания.
Герминогенные опухоли
В желудке очень редко наблюдают хориокарци-ному— 9100/3 (два типа причудливых клеток: одноядерные цитотрофобласты и многоядерные синти-циотрофобласты, атипические митозы, экспрессия цитокератинов и человеческого хорионического β-гонадотропина); опухоль эндодермального синуса (9071/3); тератому — 9080/1-3 (гистологическая и цитологическая картина аналогична таковой в опухолях этого типа другой локализации).
Вторичные опухоли желудка
Метастазы или прорастание в желудок злокачественных опухолей других органов наблюдают редко (1.2-1.7 % при аутопсии больных, умерших от злокачественных опухолей). Половина больных отмечает кровотечение, боли в брюшной полости. В желудок часто метастазируют рак молочной железы, мелано-ма, рак легкого, реже рак яичника, печени, толстой кишки. При раке молочной железы гематогенные метастазы в желудке или кишке появляются в среднем через б лет после обнаружения первичной опухоли. Указывают, что при раке молочной железы половины больных имеют метастазы в желудке; иногда метастаз в желудке диагностируют раньше, чем первичную опухоль. Рак поджелудочной железы, желчного пузыря, пищевода непосредственно распространяется на желудок, АК яичника — через брюшину и лимфатические каналы, лишь иногда гематогенно.
При диагностике метастазов используют эндоскопию. Обнаруживают изъязвление или полип. При метастазах долькового рака молочной железы картина напоминает linitis plastica. Во время эндоскопии обращают внимание на глубину инфильтрации стенки желудка опухолью. Подслизистая инфильтрация и метастазы нередко более интенсивные, чем предполагают при эндоскопии и рентгенологическом исследовании.
Гистологическая картина сходна с таковой первичной опухоли. Современные методы помогают отличить перстневидноклеточный рак от рака молочной железы. Наличие метастазов указывает на позднюю диссе-минированную стадию поражения; часто выявляют гематогенные метастазы с неблагоприятным прогнозом.
Цитологическая картина аналогична таковой первичных опухолей. Иногда в смыве желудка макрофаги напоминают эпителиальные клетки, по которым ошибочно можно диагностировать рак молочной железы, пищевода, гортани, легкого. Материал из желудка может содержать также проглоченные клетки рака полости рта, гортани, пищевода, бронхов, что изредка приводит к необоснованной лапаротомии и даже резекции желудка, или обнаруживают клетки рака поперечно-ободочной кишки и поджелудочной железы при их прорастании в желудок.
Мезенхимома – это редка и необычная опухоль, которая состоит сразу из нескольких производных мезенхимы. Ее симптомы могут долгое время отсутствовать, поэтому необходимо быть особенно внимательным, чтобы вовремя обнаружить опасную патологию.
Мезенхимома (мкб 8990/3) – это опухоль мезенхимального происхождения, которая включает в себя фиброзную ткань и еще несколько компонентов других тканей (это могут быть жировые клетки липомы или липосаркомы, сосудистые клетки ангиомы, хрящевые компоненты хондросаркомы и т.д.). Кроме того, в мезенхимоме могут присутствовать недифференцированные участки с полиморфными клетками.
Данная опухоль зачастую локализуется в тканях верхних и нижних конечностей, но также могут поражаться забрюшинное пространство, область шеи и средостение.
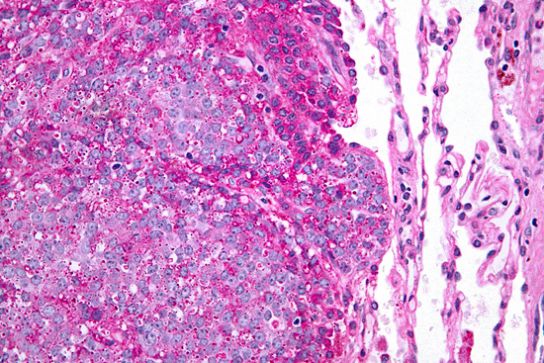
Встречается доброкачественная мезенхимома и злокачественная. Первая растет в капсуле, поэтому она хорошо отграничена от окружающих тканей. Доброкачественные новообразования развиваются в течение длительного времени и никак себя не проявляют, но в определенный момент (даже спустя десятки лет) они могут стать злокачественными. Поэтому к таким патологиям нужно относиться серьезно и постоянно контролировать их, хотя никто не исключает возможности того, что опухоль не малигнизирует всю жизнь.
Злокачественная мезенхимома растет быстро, инфильтрируя ткани, а затем – образовывая метастазы во внутренних органах. По этой причине и наступает смерть.
Новообразование может достигать огромных размеров. На разрезе часто видны кисты, участки ослизнения, окостенения, хрящи.
Классификация мезенхимомы по стадиям
Мезенхимому классифицируют по системе TNM, принятой для опухолей мягких тканей.
- 1 стадия – это низкозлокачественная опухоль небольшого размера (Т1, G1, N0, М0).
- К мезенхимоме 2 стадии относятся большие новообразования низкой степени злокачественности (Т2, G1, N0, М0).
- 3 стадия мезенхимомы характеризуется высокой степенью злокачественности и наличием метастазов в лимфатических узлах. Размер опухоли может быть любой (Т любое, G2, N1, М0).
- Мезенхимома 4 стадии – это завершающий этап, на котором происходит развитие метастазов в отдаленных органах.
Расшифровка показателей:
| ПОКАЗАТЕЛИ | ОБОЗНАЧЕНИЕ | |
| Т (первичная опухоль) | Т1 – не более 5 см в наибольшем измерении | Т2 – более 5 см в наибольшем измерении |
| N (метастазы в лимфатических узлах) | N0 – метастазов нет | N1 – обнаружены метастазы в лимфоузлах |
| М (отдаленные метастазы) | М0 – нет отдаленных метастазов | М1 – есть метастазы в отдаленных органах |
| G (степень злокачественности) | G1 – низкая | G2 – высокая |
От чего возникает злокачественная мезенхимома?
Причины возникновения мезенхимомы точно не известны.
Ученые выделяют следующие факторы риска, которые способствуют развитию болезни:
- ионизирующая радиация (в том числе лучевая терапия и радиоизотопное сканирование);
- химические канцерогены;
- травмы и металлические инородные тела;
- онкология в семье;
- генетические патологии.
Как было сказано ранее, причины возникновения мезенхимомы злокачественной формы может стать доброкачественная опухоль. В зоне риска находятся люди в возрасте от 40 лет и старше, так как именно в этот период чаще диагностируют образования мягких тканей.
Симптомы и признаки мезенхимомы
Основной признак болезни на начальных стадиях – это пальпируемое образование. Как правило, оно бугристое, имеет мягкую консистенцию. При опухолях больших размеров можно наблюдать видимые изменения на коже: она растягивается, просвечивается венозный рисунок. При надавливании может ощущаться болезненность.
К общим симптомам мезенхимомы относятся лихорадка и потеря массы тела. Опухолевая интоксикация организма вызывает ухудшение общего состояния, человек чувствует слабость, усталость.Также часто онкобольных мучают боли, локализация которых зависит от расположения патологии. Если это опухоль ноги, то возникают нарушения двигательной функции и боль при ходьбе.
Остальные симптомы мезенхимомы являются местными и зависят от воздействия опухоли на тот или иной орган.
Больной может жаловаться на:
- диспептические расстройства (связаны с влиянием на ЖКТ). Человека мучают тошнота и рвота, понос, тяжесть в животе, изжога и отрыжка;
- дизурические расстройства (при поражении мочевого пузыря). К ним относятся, задержка мочи или недержание, боль при мочеиспускании;
- одышку (при сдавливании легких);
- нарушение сердечного ритма и боль в сердце (при опухолях средостения, которые распространились на перикард);
- сильную боль и переломы костей (при распространении на кость).
Также особые симптомы проявляются при сдавливании крупных венозных стволов. Например, при компрессии нижней полой вены отекают ноги и расширяются вены. Могут проявляться гематомы под кожей, а также трофические язвы. При сдавливании сосудов шеи наблюдаются головокружения, потемнение в глазах, отек лица, цианоз.
Диагностика заболевания
Диагностика мезенхимомы начинается с внешнего осмотра пациента. Врач может заметить уплотнение, опухлость в мягких тканях. На ощупь он определит ее консистенцию, степень подвижности и болезненности. Также при внешнем осмотре могут быть выявлены увеличение лимфатических узлов или внутренних органов, нарушение подвижности кости и сустава, отек, набухание вен, изменение цвета кожных покровов и другие важные признаки.
Далее для подтверждения диагноза нужно пройти ряд исследований:
- УЗИ в области локализации новообразования, а также региональных лимфатических узлов и органов брюшной полости.
- Рентгенографию костей.
- КТ пораженного участка и органов грудной клетки.
Они дадут сведения о том, есть ли у больного опухоль мягких тканей, где она расположена, какой у нее размер, есть ли метастазы в лимфатических узлах, костях и органах, повреждены ли сосуды и нервы. Если у врача есть какие-то сомнения, то он может назначить уточняющие диагностические методики, например, магнитно-резонансную или позитронно-эмиссионную томографию.
Кроме того, понадобится сдать следующие анализы:
- Общий анализ крови (определяют такие параметры, как уровень эритроцитов, лейкоцитов, гемоглобин, СОЭ).
- Биохимический анализ крови (определяют кретинин, мочевину, общий белок, билирубин, глюкозу, холестерин и т.д.).
- Общий анализ мочи (обращают внимание на наличие белка или крови в моче).
- Определение группы крови и резус-фактора.
- Исследование на ВИЧ.
Рентгенологическое и ультразвуковое исследование не может дать точный ответ о типе опухоли и ее злокачественности. Чтобы узнать эти важные данные прибегают к биопсии – это взятие клеток новообразования для последующего микроскопического исследования. Кусочек тканей берут через специальный шприц с иглой или напрямую через хирургический разрез в коже.
Далее образец подвергают цитологическому и гистологическому обследованию и ставят окончательный диагноз.
К дополнительным методам исследования, которые могут понадобиться для диагностики мезенхимомы, относятся:
- колоноскопия (для обследования кишечника);
- ЭКГ (для оценки работы сердца);
- лапаротомия (для обследования брюшной полости);
- торакотомия (при поражении средостения и грудной полости);
- сцинтиграфия скелета;
- ангиография (для определения прорастания новообразования в сосуды).
Перед проведением операции может потребоваться консультация специалистов: хирурга, уролога, гинеколога, терапевта, кардиолога.
Лечение мезенхимомы
Основным методом лечения опухолей мягких тканей считается хирургическое их удаление. Во время операции важно вырезать всю опухоль и поврежденные нею структуры. Как правило, операцию дополняют противоопухолевой терапией (химией или облучением).
В большинстве случаев хирургическое лечение мезенхимомы предполагает удаление опухоли в мышечно-фасциальном футляре. Также во время операции вырезают пораженный участок кожи, кости, лимфатические узлы, сосуды (при необходимости). Такой подход используют для того, чтобы полностью убрать все частички новообразования из организма и избежать прогрессирования болезни.
При мелких, отграниченных узелках могут обойтись отсечением опухоли с отступом от ее краев 5-6 см. Если же процесс сильно распространенный и есть угроза осложнений, то проводят ампутацию или вычленение конечностей.
При расположении мезенхимомы в забрюшинном пространстве или средостении провести операцию сложнее, чем на конечности. Часто приходится удалять селезенку, кишку, почку, легкое, ребра, диафрагму, что требует последующих тяжелых реконструктивных этапов. Также такие вмешательства чреваты различными осложнениями: абсцессом, кровотечением, нагноением раны и т.д. Обязанность врача – учесть все положительные стороны и риск, чтобы выбрать оптимальный вариант лечения мезенхимомы.
Добиться наилучших показателей выживаемости позволяет лишь радикальное удаление опухоли, но оно не всегда является возможным. Тогда врачи вырезают максимально возможный объем образования и назначают химиотерапию и облучение. Паллиативная операция при мезенхимоме позволяет снизить вероятность осложнений, улучшает качество жизни пациента и создает благоприятные условия для последующей терапии.
Цитостатическая терапия может применяться до операции, по усмотрению врача. Ее цель – уменьшить размер опухоли и сделать последующее хирургическую резекцию более легкой. Химиотерапия при мезенхимоме, назначаемая после операции в обязательном порядке, нужна для борьбы с микрометастазами, которые в последствие могут стать причиной рецидива.
Далее представлены примеры полихимиотерапии несколькими препаратами для опухолей мягких тканей:
- Схема CyADIC: 1 день курса – 50 мг/м2 внутривенно Доксорубицин; 2 день курса – Циклофосфамид 500 мг/м2 в/в; с 1 по 5 день – Дакарбазин 250 мг/м2 в/в.
- Схема САРО: 1 день – Цисплатин 100 мг/м2 в/в; 2, 3 и 4 дни – Доксорубицин 30 мг/м2 в/в; 5 день – Винкристин 30 мг/м2 в/в; 6 день – Циклофосфан 300 мг/м2.
Циклы повторяются от 3 до 10 раз. Между ними делают перерывы по 2-3 недели. Во время химиотерапии больной находится под наблюдением специалистов, так как от химиопрепаратов возникают побочные эффекты. Если наблюдаются серьезные осложнения, то схему меняют на другую. Курс лечения устанавливает лечащий врач.
Лучевая терапия, как правило, проводится после нерадикальных операций. Дозу облучения направляют на остаточную опухоль, чем вызывают гибель ее клеток. Суммарная доза может варьироваться от 50 до 70 Гр. Ее разделяют на 5-10 сеансов, которые проводят по определенному графику.
Некоторым неоперабельным больным удается с помощью химио-лучевой терапии добиться уменьшения опухоли и превращения ее в резектабельную. Тогда проводят операцию, и у человека появляется шанс на выживание.Так как на данный момент нет единого рандомизированного исследования по лечению мезенхимомы, то врачам приходится использовать индивидуальный подход, ориентируясь на конкретного пациента. Возможно применение новых методик, которые ранее не применялись.
Метастазирование и рецидив
Рецидив мезенхимомы происходит у половины пациентов. Их заново подвергают хирургическому лечению. При прогрессировании болезни могут пострадать органы и структуры, которые до этого были здоровыми, поэтому приходится проводить расширенные операции и иногда по несколько раз. Химия и облучения не показывают хороших результатов.
Метастазы при мезенхимоме распространяются по кровеносным сосудам. Таким образом, опухоль может распространиться на любой орган, но чаще всего страдают легкие. По возможности метастазы удаляют вместе с первичным образованием. Хорошие результаты в лечении метастазов показывает усиленная полихимиотерапия.
Прогноз при злокачественной мезенхимоме
Прогноз при мезенхимоме в целом неблагоприятный, так как она долго не дает о себе знать и ее диагностируют, когда уже образовываются метастазы. Прогноз будет лучше у пациентов с начальной стадией мезенхимомы, расположенной на руке или ноге, после полного удаления опухоли и хорошего ответа на химиотерапию. При таких условиях почти все больные переживают 5-летний рубеж.
При локализации опухоли в забрюшинном пространстве или средостении показатели будут хуже: до 5 лет не доживают и половина больных и это после радикальной операции. Если же тотальная резекция невозможна, то после паллиативной помощи у больного есть шанс прожить 1-2 года.
Рецидивы мезенхимомы снижают показатели выживаемости и могут привести к смерти пациента. Чтобы их предотвратить рекомендуется максимально радикальное лечение.
Не последнюю роль в успешном выздоровлении играет внимательность больного к своему здоровью и опытность врача.
Читайте также:

